UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
|
|
|
- Gerhard Ursler
- vor 6 Jahren
- Abrufe
Transkript
1 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 1
2 Reminder: MO-Diagramm von O 2 2- MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 2
3 Reminder: MO-Diagramm von CO MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 3
4 Elektronenanregung mal ganz schematisch MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 4
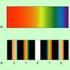
5 Komplementärfarben Absorbiert eine Probe gelbes Licht (~570 nm) erscheint sie unserem Auge als blau, da blaues Licht durchgelassen wird MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 5
6 Messung von UV/vis-Spektren Strahlungsquelle: Monochromator: Probenzelle: Halogenlampe Prisma Quarzküvette Vorteil: Nur extrem niedrige Konzentrationen notwendig (10-5 M) MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 6
7 Wie sieht so ein UV/Vis-Spektrum nun aus? Lichtabsorbierende Gruppe: Chromophor O Lambert-Beer sches Gesetz MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 7
8 Ein weiteres Beispielspektrum MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 8
9 Mögliche Übergänge Grobe Einordnung im Spektrum: * < 180 nm * n * n * > 200 nm > nm ~ nm MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 9
10 Konjugierte -Systeme Konjugation führt zur Verringerung der HOMO-LUMO-Energiedifferenz Verschiebung von max zu höheren Wellenlängen (Rotverschiebung) MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 10
11 So viele mögliche Übergänge und welche sehen wir davon? Die Intensität einer UV/Vis-Bande hängt entscheidend von der Differenz der Ladungsverteilungen von Grundzustand und angeregtem Zustand (dem Übergangdipolmoment) ab. Quantenmechanisch: Dipolstärke D bzw. Oszillatorstärke f MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 11
12 Qualitative Bestimmung des Übergangsdipolmoments (edtm) 1) Beteiligte MOs identifizieren 2) Multiplizieren der MOs und bestimmen des Produktorbitals 3) Vorzeichen invertieren um Elektronendichte in Ladungen zu konvertieren 4) Haben die Produktorbitale dipolaren Charakter? * der C=O Gruppe O Großes edtm für * Übergang, d.h. starke Bande µ ij MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 12
13 Weitere Beispiele n * der C=O Gruppe Quadrupol, aber kein Dipol, d.h. verbotener Übergang n * der C=O Gruppe Produkt-MO nicht gleichmäßig um Sauerstoff und senkrecht zu C-O Aufteilung in schwachen Quadrupol und mittleren Dipol Erlaubter Übergang (mittlere Intensität) MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 13
14 Quantenmechanische Auswahlregeln Symmetrie-Auswahlregel (Symmetrie-Verbot) bezieht sich auf Symmetriebeziehung der am Übergang beteiligten MO * n * MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 14
15 Quantenmechanische Auswahlregeln Symmetrie-Auswahlregel (Symmetrie-Verbot) bezieht sich auf Symmetriebeziehung der am Übergang beteiligten MO Spin-Auswahlregel (Spin-Verbot) Damit ein Übergang erlaubt ist, darf sich der Gesamtspin bzw. die Multiplizität des Systems nicht ändern ( S = 0, M = 0) MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 15
16 Quantenmechanische Auswahlregeln n (HOMO) * (LUMO) Singulett- Grundzustand S 0 angeregter Singulettzustand S 1 angeregter Tripletttzustand T 1 zweiter angeregter Singulettzustand S 2 MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 16
17 Franck-Condon-Prinzip Elektronische Anregung resultiert oft in Änderung der Geometrie (Bindungslänge, -winkel) Potentialenergie eines zweiatomigen Moleküls im Grundzustand und im ersten angeregten Zustand: S 0 Grundzustand S 1 angeregter Zustand Frank-Condon-Prinzip: Übergangswahrscheinlichkeit am größten für den Übergang, bei dem alle geometrischen Parameter unverändert bleiben. MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 18
18 Franck-Condon-Prinzip Lage der Potentialkurven zueinander bestimmt die Form der Absorptionsbande MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 19
19 UV/vis Spektrum von Benzol Manchmal können Schwingungsfeinstrukturen in den Spektren organischer Verbindungen sogar aufgelöst werden und damit Informationen über den elektronisch angeregten Zustand gewonnen werden. MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 20
20 Relaxationsprozesse: Jablonski-Schema Auswahlregeln sagen, dass S 0 S 1 spinerlaubt sei, S 0 T 1 aber nicht. Spinverboten heißt aber nur, dass ein Übergang mit wesentlich geringerer Wahrscheinlichkeit stattfindet MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 21
21 Relaxationsprozesse: Jablonski-Schema S 0 T 1 findet meist nicht direkt statt, sondern durch intersystem crossing ausgehend von S 1 MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 22
22 Lage von Absorptionbanden Problem: Von Struktur kann man selten auf die genaue Lage von Übergangen schließen bzw. von der Lage eines Übergangs alleine lässt sich nicht auf die Struktur schließen Lösungen : (1) Empirisch entwickelte Inkrementsysteme (2) Chromophore = 214 nm + 5 für jeden Alkysubstituenten + 30 je weitere konjugierte Doppelbindung + - absorbieren oft in typischen Wellenlängenbereichen Beispiele: -NO 2, -N=N-, Metallionen (d-d-übergänge), Peptid-Bindungen, MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 23
23 UV/vis Spektrum eines Metallkomplexes C. Merten et al. Inorg. Chem. 43 (2014) Schwingungsfeinstruktur H 2 N NH 2 NH 2 Ni 2+ NH 2 H 2 N NH 2 d-d-übergang Achtung: d-d-übergänge sind nach weiteren quantenmechanisch begründeten Verboten (Paritätsverbot, Laporte-Verbot) nicht erlaubt. Durch Schwingungen der Liganden gegen das Metallzentrum werden die Auswahlregeln kurzzeitig aufgehoben. ( Anorganik-Vorlesung) MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 24
24 Terminologie zur Beschreibung von Veränderungen im Spektrum MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 25
25 Lösungsmittelabhängigkeit: 4-Methyl-3-penten-2-on Methanol Heptan polar unpolar Übergang polar unpolar Anhebung von n- und *-Orbital n-orbital wird stärker angehoben Abstand -> * wird größer Blauverschiebung Abstand n -> * wird kleiner Rotverschiebung MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 26
26 Zusammenfassung Elektronische Übergänge allein nicht ausreichend um Struktur zu charakterisieren Anwendungen von UV/vis-Spektroskopie Quantitative Analyse, Titrationen Reinheitsprüfung Spurenanalytik Detektoren in Chromatographie Reaktionskinetiken Photochemie Biochemie: Strukturveränderungen in Peptiden MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 27
27 Anwendung: Verfolgen von Schaltprozessen 1.0 absorption Azobenzol-Derivate können durch Licht der Wellenlänge 365 nm von trans (schwarz) nach cis (rot) geschaltet werden. Durch Licht höherer Wellenlänge, Temperatur oder schlicht über die Zeit schalten sie zurück in die trans- Konformation wavelength / nm MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 28
28 Übung Welches Spektrum gehört zu den Substanzen und warum? Cycloheptatrien (C 7 H 8 ) 1-Methyl-Cyclohexen (C 7 H 12 ) MdS-1 UV/Vis-Spektroskopie Dr. C. Merten WS 2017/18 29
UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie
 Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
Teil 5 UV/Vis-Spektroskopie oder auch: Elektronenanregungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2018/19 www.ruhr-uni-bochum.de/chirality 1 Komplementärfarben Absorbiert eine Probe gelbes
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
Teil 1 Schwingungsspektroskopie (Raman-Spektroskopie) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: Die Essentials der letzten Vorlesung Funktionelle Gruppen
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick Chemische Verschiebung Chemische Umgebung Funktionelle Gruppen Signalintensitäten
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Methoden der Strukturaufklärung
 Methoden der Strukturaufklärung LVN: 180542 Ort: HNC 30 Zeit: Mo 9-11 Uhr Mi 15-17 Uhr Kontaktinfos: Büro: NC 4/173 Email: christian.merten@rub.de www: www.rub.de/chirality Dr. Christian Merten, Ruhr-Uni
Methoden der Strukturaufklärung LVN: 180542 Ort: HNC 30 Zeit: Mo 9-11 Uhr Mi 15-17 Uhr Kontaktinfos: Büro: NC 4/173 Email: christian.merten@rub.de www: www.rub.de/chirality Dr. Christian Merten, Ruhr-Uni
Methoden der Strukturanalyse I
 Methoden der Strukturanalyse I LVN: 180542 Ort: HNC 30 Zeit: Mo 9-11 Uhr Mi 15-17 Uhr Kontaktinfos: Büro: NC 4/173 Email: christian.merten@rub.de www: www.rub.de/chirality Dr. Christian Merten, Ruhr-Uni
Methoden der Strukturanalyse I LVN: 180542 Ort: HNC 30 Zeit: Mo 9-11 Uhr Mi 15-17 Uhr Kontaktinfos: Büro: NC 4/173 Email: christian.merten@rub.de www: www.rub.de/chirality Dr. Christian Merten, Ruhr-Uni
Kapitel 7: Elektronische Spektroskopie
 Kapitel 7: Elektronische Spektroskopie Übersicht: 7.1 Drehimpuls-Kopplungshierarchien in Molekülen: Hundsche Fälle 7.2 Auswahlregeln für rovibronische Übergänge 7.3 Das Franck-Condon-Prinzip 7.4 Zerfall
Kapitel 7: Elektronische Spektroskopie Übersicht: 7.1 Drehimpuls-Kopplungshierarchien in Molekülen: Hundsche Fälle 7.2 Auswahlregeln für rovibronische Übergänge 7.3 Das Franck-Condon-Prinzip 7.4 Zerfall
4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration
 g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
g 4.2.2.Das Wasserstoff-Molekül H 2 Vergleich der Wellenfunktionen für antiparallele Spinkonfiguration a () ϕ ( 2) ϕ ( 2) ϕ ( 1) ψ = ϕ + 1 b a b Heitler-London ( ) ϕ ( 2) + ϕ ( 2) ϕ ( 1) + [ ϕ ( 1) ϕ (
Übungen zur Vorlesung Physikalische Chemie 2 (B. Sc.) Lösungsvorschlag zu Blatt 12
 Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Übungen zur Vorlesung Physikalische Chemie B. Sc. ösungsvorschlag zu Blatt 1 Prof. Dr. Norbert Hampp Jens Träger Wintersemester 7/8. 1. 8 Aufgabe 1 Welche Schwingungsübergänge in einem elektronischen Spektrum
Theoretical Biophysics - Quantum Theory and Molecular Dynamics. 13. Vorlesung. Pawel Romanczuk WS 2016/17
 Theoretical Biophysics - Quantum Theory and Molecular Dynamics 13. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Variationsrechnung LCAO-Verfahren am Beispiel
Theoretical Biophysics - Quantum Theory and Molecular Dynamics 13. Vorlesung Pawel Romanczuk WS 2016/17 http://lab.romanczuk.de/teaching Zusammenfassung letzte VL Variationsrechnung LCAO-Verfahren am Beispiel
Chemistry Department Cologne University. Photochemie 1 PC 2 SS Chemistry Department Cologne University. Photochemie
 Photochemie 1 PC 2 2016 Photochemie 2 PC 2 2016 1 Wichtige photophysikalische Prozesse 3 PC 2 2016 Der Grundzustand Boltzmann Verteilung: Alle Moleküle sind im elektronischen Grundzustand (0) chwingungsgrundzustand
Photochemie 1 PC 2 2016 Photochemie 2 PC 2 2016 1 Wichtige photophysikalische Prozesse 3 PC 2 2016 Der Grundzustand Boltzmann Verteilung: Alle Moleküle sind im elektronischen Grundzustand (0) chwingungsgrundzustand
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm.
 Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
Physik IV Einführung in die Atomistik und die Struktur der Materie
 Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 20 29.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 20 Prof. Thorsten Kröll 29.06.2011 1 Anmeldung
Physik IV Einführung in die Atomistik und die Struktur der Materie Sommersemester 2011 Vorlesung 20 29.06.2011 Physik IV - Einführung in die Atomistik Vorlesung 20 Prof. Thorsten Kröll 29.06.2011 1 Anmeldung
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Elektronenspektroskopie
 Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Teil 3 2D-NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 3 2D-NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Protonen-Protonen-Korrelation durch J-Kopplung Pulssequenz für ein klassisches 1D- 1 H-NMR
Teil 2 NMR-Spektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Teil 2 NMR-Spektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality 1 Rückblick: Kopplungskonstanten Kopplungskonstante ist abhängig von der Entfernung der Kopplungspartner:
Einführung in die Schwingungsspektroskopie
 Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Einführung in die Schwingungsspektroskopie Quelle: Frederik Uibel und Andreas Maurer, Uni Tübingen 2004 Molekülbewegungen Translation: Rotation: Die Bewegung des gesamten Moleküls ls in die drei Raumrichtungen.
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Ausbreitung von elektromagnetischer Strahlung
 Ausbreitung von elektromagnetischer Strahlung E! B Der elektrische Feldvektor und der magnetische Feldvektor stehen senkrecht aufeinander Die elektromagentische Welle ist beschrieben durch x x E = E 0
Ausbreitung von elektromagnetischer Strahlung E! B Der elektrische Feldvektor und der magnetische Feldvektor stehen senkrecht aufeinander Die elektromagentische Welle ist beschrieben durch x x E = E 0
Fluoreszenz und Excimerenbildung
 Fluoreszenz und Excimerenbildung Fragen und Stichworte zur Vorbereitung: Aufbau und Funktion eines Fluoreszenzspektrometers Spektrale und natürliche Bandbreite Signal-Rausch-Verhältnis Jablonski-Diagramm:
Fluoreszenz und Excimerenbildung Fragen und Stichworte zur Vorbereitung: Aufbau und Funktion eines Fluoreszenzspektrometers Spektrale und natürliche Bandbreite Signal-Rausch-Verhältnis Jablonski-Diagramm:
Klausur zur Vorlesung Symmetrie in Chemie und Spektroskopie
 Klausur zur Vorlesung Symmetrie in Chemie und Spektroskopie Zulässige Hilfsmittel: Charakterentafeln, Schema Hierarchie der Punktgruppen SS 6 Prof. Dr. B. Dick Aufgabe 1 (15P): Finden Sie die Punktgruppe
Klausur zur Vorlesung Symmetrie in Chemie und Spektroskopie Zulässige Hilfsmittel: Charakterentafeln, Schema Hierarchie der Punktgruppen SS 6 Prof. Dr. B. Dick Aufgabe 1 (15P): Finden Sie die Punktgruppe
Die Erwartungswerte von Operatoren sind gegeben durch. (x, t)a (x, t) =h A i
 Die Wahrscheinlichkeit, das System zu einem bestimmten Zeitpunkt in einem bestimmten Zustand anzutreffen, ist durch das Betragsquadrat der Wellenfunktion (x, t) 2 gegeben Die Erwartungswerte von Operatoren
Die Wahrscheinlichkeit, das System zu einem bestimmten Zeitpunkt in einem bestimmten Zustand anzutreffen, ist durch das Betragsquadrat der Wellenfunktion (x, t) 2 gegeben Die Erwartungswerte von Operatoren
A. Mezzetti Fragenkatalog X
 Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Anorganische Chemie I Elektronenespektren A. Mezzetti ragenkatalog X 1. K n [V 6 ] (n muss bestimmt werden) (B) hat µ eff = 2.66 BM. Sein UV-VIS-Spektrum enthält eine sehr schwache Bande (10'000 cm 1 )
Protokoll zum Versuch 50: Photometrie vom Thema: Photometrische Fe 2+ -Konzentrationsbestimmung mit Phenanthrolin
 Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Protokoll zum Versuch 50: Photometrie vom 06.11.00 Thema: Photometrische Fe + -Konzentrationsbestimmung mit Phenanthrolin für das Protokoll: Datum: 5.11.00 1 1 Materialien 1.1 Chemikalien NH Fe SO H O
Versuch Fluoreszenz-Quenching
 Versuch Fluoreszenz-Quenching Zielstellung: 1.) Aufnahme des UV-Vis-Spektrums eines Fluoreszenzfarbstoffes 2.) Aufnahme der Kennlinie des verwendeten Photon-Counting-Moduls (PCM) im Bereich von 1,9 2,9
Versuch Fluoreszenz-Quenching Zielstellung: 1.) Aufnahme des UV-Vis-Spektrums eines Fluoreszenzfarbstoffes 2.) Aufnahme der Kennlinie des verwendeten Photon-Counting-Moduls (PCM) im Bereich von 1,9 2,9
Spektroskopische Methoden
 Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
2 Grundlagen der Photochemie
 folie191 2 Grundlagen der Photochemie 2.1 UV-Vis-Absorptionsspektren in organischen Verbindungen; Jablonski-Diagramm, Franck-Condon-Prinzip, Emissionsspektren (Fluoreszens, Phosphoreszens, Stokes-Verschiebung)
folie191 2 Grundlagen der Photochemie 2.1 UV-Vis-Absorptionsspektren in organischen Verbindungen; Jablonski-Diagramm, Franck-Condon-Prinzip, Emissionsspektren (Fluoreszens, Phosphoreszens, Stokes-Verschiebung)
Auswahlregeln UV/VIS-Spektroskopie
 Auswahlregeln UV/VIS-Spektroskopie H H H H Ethen: π-π*übergang erlaubt? π LUMO π HOMO hν zunächst Punktgruppe bestimmen Symmetrieoperationen σ xz σ yz C 2 (x) C 2 (z) σ xy i C 2 (y) 3 Spiegelebenen i,
Auswahlregeln UV/VIS-Spektroskopie H H H H Ethen: π-π*übergang erlaubt? π LUMO π HOMO hν zunächst Punktgruppe bestimmen Symmetrieoperationen σ xz σ yz C 2 (x) C 2 (z) σ xy i C 2 (y) 3 Spiegelebenen i,
z n z m e 2 WW-Kern-Kern H = H k + H e + H ek
 2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
2 Molekülphysik Moleküle sind Systeme aus mehreren Atomen, die durch Coulomb-Wechselwirkungen Elektronen und Atomkerne ( chemische Bindung ) zusammengehalten werden. 2.1 Born-Oppenheimer Näherung Der nichtrelativistische
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
Infrarot-Spektroskopie
 SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
Strukturaufklärung (BSc-Chemie): Einführung
 Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
Strukturaufklärung (BSc-Chemie): Einführung Prof. S. Grimme OC [TC] 13.10.2009 Prof. S. Grimme (OC [TC]) Strukturaufklärung (BSc-Chemie): Einführung 13.10.2009 1 / 25 Teil I Einführung Prof. S. Grimme
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC
 IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
IR-Spektroskopie Seminar Analytische Chemie I (BC3.4, MCB B1; WS2016/17) Dr. Peter Bellstedt NMR Plattform IAAC & IOMC Peter.Bellstedt@uni-jena.de Terminübersicht (14 täg.) Gruppe 1 Gruppe 2 1. Seminar
4.Teil Kovalente Bindung
 4.Teil Kovalente Bindung Lewis-Konzept, Valenstrichformel, Oktettregel Polare Elektronenpaarbindung und Elektronegativität Gebrochene Bindungsordnung und Mesomerie Valenzschalen-Elektronenpaar-Abstoßungsmodell
4.Teil Kovalente Bindung Lewis-Konzept, Valenstrichformel, Oktettregel Polare Elektronenpaarbindung und Elektronegativität Gebrochene Bindungsordnung und Mesomerie Valenzschalen-Elektronenpaar-Abstoßungsmodell
Absorptionsspektren von Farbstoffen
 Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 50 Absorptionsspektren von Farbstoffen Aufgabe Es sind die Absorptionsspektren verschiedener Cyanin-Farbstoffe im Wellenlängenbereich
Versuchsanleitungen zum Praktikum Physikalische Chemie für Anfänger 1 A 50 Absorptionsspektren von Farbstoffen Aufgabe Es sind die Absorptionsspektren verschiedener Cyanin-Farbstoffe im Wellenlängenbereich
Blitzlichtphotolyse 1
 Blitzlichtphotolyse 1 Reaktionskinetik einer Spiropyranbildung WICHTIG: 1. Sie sollten einen USB-Speicherstick o.ä. mitbringen! 2. Lesen Sie sich diese Anleitung VOR dem Tag des Praktikums gut durch. 3.
Blitzlichtphotolyse 1 Reaktionskinetik einer Spiropyranbildung WICHTIG: 1. Sie sollten einen USB-Speicherstick o.ä. mitbringen! 2. Lesen Sie sich diese Anleitung VOR dem Tag des Praktikums gut durch. 3.
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 4 NMR-Spektroskopie 5.1 1 H-NMR-Spektroskopie Wasserstoffatome ( 1 H, natürliche Häufigkeit 99,985 %) mit
Betrag des Drehimpulses
 Voresung Spektroskopie Sommersemester 001 Prof. Dr. W. Knoche 5. Rotations- und Schwingungsspektren 5.1. Rotationsspektren Freie Rotation eines starren Moeküs um drei Achsen: x y J = J + J + J z J J =
Voresung Spektroskopie Sommersemester 001 Prof. Dr. W. Knoche 5. Rotations- und Schwingungsspektren 5.1. Rotationsspektren Freie Rotation eines starren Moeküs um drei Achsen: x y J = J + J + J z J J =
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
Einführung in die Spektroskopie für Studenten der Biologie
 Einführung in die Spektroskopie für Studenten der Biologie Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Literatur Banwell, C. N., Elaine M. McCash, Molekülspektroskopie. Ein
Einführung in die Spektroskopie für Studenten der Biologie Jörg H. Kleinschmidt http://www.biologie.uni-konstanz.de/folding/home.html Literatur Banwell, C. N., Elaine M. McCash, Molekülspektroskopie. Ein
Die 18 Valenzelektronen-Regel
 Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Die 18 Valenzelektronen-Regel 18 VE-Regel basiert auf VB-Betrachtung lokalisierter Bindungen und besagt: Stabile ÜM-Komplexe liegen vor wenn die Summe der Metall-d-Elektronen und der Elektronen, die von
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Molekulare Kerndynamik. Grundlagen
 Grundlagen Bei der Bestimmung der elektronischen Struktur von Molekülen haben wir bis jetzt den Fall betrachtet, daß die Kerne fest sind. Lösung der elektronischen Schrödingergleichung in einem festen
Grundlagen Bei der Bestimmung der elektronischen Struktur von Molekülen haben wir bis jetzt den Fall betrachtet, daß die Kerne fest sind. Lösung der elektronischen Schrödingergleichung in einem festen
2. Klausur zur Vorlesung Physikalische Chemie II - Wintersemester 02/ Februar 2003, Uhr
 2. Klausur zur Vorlesung Physikalische Chemie II - Wintersemester 02/03 07. Februar 2003, 10 15 -- 13 00 Uhr Name, Vorname:... Geburtsdatum, -ort:... Matrikelnummer:... Studienfach, Fachsemester:... Hinweise
2. Klausur zur Vorlesung Physikalische Chemie II - Wintersemester 02/03 07. Februar 2003, 10 15 -- 13 00 Uhr Name, Vorname:... Geburtsdatum, -ort:... Matrikelnummer:... Studienfach, Fachsemester:... Hinweise
UV-Vis Spektroskopie
 UV-Vis Spektroskopie Instrumentelle Analytik SoSe 2019 Dr. Oliver Thorn-Seshold C1.059 (Fr 12-13) / oliver.thorn-seshold@cup.lmu.de Ziele Recap: UVVis Elektronanregung, genauer angeschaut Chromophoren
UV-Vis Spektroskopie Instrumentelle Analytik SoSe 2019 Dr. Oliver Thorn-Seshold C1.059 (Fr 12-13) / oliver.thorn-seshold@cup.lmu.de Ziele Recap: UVVis Elektronanregung, genauer angeschaut Chromophoren
Stark konz., Fluoreszierend
 hemie-protokoll 28.10.02, Seite 1 von 5 Lukman Iwan, 30.10.02 Stundenprotokoll vom Montag, 28. Oktober 2002 Es fehlen: keine VB: Lösungsmittel Extraktfarbe VD: Ethanol (Brennspiritus) Blaugrün, Stark konz.,
hemie-protokoll 28.10.02, Seite 1 von 5 Lukman Iwan, 30.10.02 Stundenprotokoll vom Montag, 28. Oktober 2002 Es fehlen: keine VB: Lösungsmittel Extraktfarbe VD: Ethanol (Brennspiritus) Blaugrün, Stark konz.,
Fluoreszenzspektroskopie
 A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
5 Elektronengas-Modell und Polyene
 5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
5.1 Übersicht und Lernziele Übersicht Im vorherigen Kapitel haben Sie gelernt, das Elektronengas-Modell am Beispiel der Cyanin-Farbstoffe anzuwenden. Sie konnten überprüfen, dass die Berechnungen für die
Short Summary of the Essentials of the PC V Lecture. To be covered by the first excercise of this class
 Short Summary of the Essentials of the PC V Lecture To be covered by the first excercise of this class Das elektromagnetische Spektrum und Spektralbereiche Lineare Polarisation Elektromagnetische Wellen
Short Summary of the Essentials of the PC V Lecture To be covered by the first excercise of this class Das elektromagnetische Spektrum und Spektralbereiche Lineare Polarisation Elektromagnetische Wellen
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
2.2 Intermolekulare Wechselwirkungen
 2.2 Intermolekulare Wechselwirkungen -15-2.2 Intermolekulare Wechselwirkungen Die Bildung der hier vorgestellten molekularen Aggregate beruht auf schwachen Wechselwirkungen zwischen Atomen oder Molekülen.
2.2 Intermolekulare Wechselwirkungen -15-2.2 Intermolekulare Wechselwirkungen Die Bildung der hier vorgestellten molekularen Aggregate beruht auf schwachen Wechselwirkungen zwischen Atomen oder Molekülen.
Aufgabe 2: Quantenmechanisches Modell für pseudolineare Polyene
 Lösungsvorschlag Übung 10 Aufgabe 1: Ein Teilchen im eindimensionalen Kasten a Die Energiedifferenz zwischen zwei aufeinanderfolgenden Energie-Eigenwerten ist E n,n+1 = E n+1 E n ml n + 1 n 1.1 n + 1.
Lösungsvorschlag Übung 10 Aufgabe 1: Ein Teilchen im eindimensionalen Kasten a Die Energiedifferenz zwischen zwei aufeinanderfolgenden Energie-Eigenwerten ist E n,n+1 = E n+1 E n ml n + 1 n 1.1 n + 1.
9. Moleküle. 9.1 Wasserstoff-Molekül Ion H Wasserstoff-Molekül H Schwerere Moleküle 9.4 Angeregte Moleküle. Physik IV SS
 9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
9.1 Wasserstoff-Molekül Ion H + 9. Wasserstoff-Molekül H 9.3 Schwerere Moleküle 9.4 Angeregte Moleküle 9.1 9.1 Wasserstoff-Molekül Ion H + Einfachstes Molekül: H + = p + e p + Coulomb-Potenzial: Schrödinger-Gleichung:
3 Elektronengas-Modell und Polyene
 3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
3.1 Lernziele 1. Sie können die Anregungsenergie ΔE für den Ügang vom höchsten besetzten (HOMO) zum niedrigsten unbesetzten (LUMO) Niveau von Polyenen mit dem Elektronengas-Modell echnen. 2. Sie sind in
12.8 Eigenschaften von elektronischen Übergängen. Übergangsfrequenz
 phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
phys4.024 Page 1 12.8 Eigenschaften von elektronischen Übergängen Übergangsfrequenz betrachte die allgemeine Lösung ψ n der zeitabhängigen Schrödinger-Gleichung zum Energieeigenwert E n Erwartungswert
Photom etrieren Photometrie Fraunhofer sche Linien
 17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
17 Photometrieren Die Spektroskopie, auch Spektralphotometrie, Spektrophotometrie oder einfach nur Photometrie genannt, umfasst eine Anzahl experimenteller Messverfahren, die generell die Wechselwirkung
Das Spektrum elektromagnetischer Strahlung
 Druckversion: Virtuelles Labor: UV-Vis-Spektroskopie 1 Versuchsziel ufnahme eines Spektrums von Sulfanilamid (SN) und Sulfathiazol (ST) zur Ermittlung der maximalen Wellenlänge max und der entsprechenden
Druckversion: Virtuelles Labor: UV-Vis-Spektroskopie 1 Versuchsziel ufnahme eines Spektrums von Sulfanilamid (SN) und Sulfathiazol (ST) zur Ermittlung der maximalen Wellenlänge max und der entsprechenden
Dynamik von Molekülen. Rotationen und Schwingungen von Molekülen
 Rotationen und Schwingungen von Molekülen Schwingungen und Rotationen Bis jetzt haben wir immer den Fall betrachtet, daß die Kerne fest sind Was geschieht nun, wenn sich die Kerne bewegen können? Zwei
Rotationen und Schwingungen von Molekülen Schwingungen und Rotationen Bis jetzt haben wir immer den Fall betrachtet, daß die Kerne fest sind Was geschieht nun, wenn sich die Kerne bewegen können? Zwei
Teil 1 Schwingungsspektroskopie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Teil 1 Schwingungsspektroskopie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Themenüberblick Schwingungsspektroskopie Physikalische Grundlagen: Mechanisches Bild
Spektroskopie. im IR- und UV/VIS-Bereich. Proben, Probengefässe, Probenvorbereitung.
 Spektroskopie im IR- und UV/VIS-Bereich Proben, Probengefässe, Probenvorbereitung Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers d
Spektroskopie im IR- und UV/VIS-Bereich Proben, Probengefässe, Probenvorbereitung Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Allgemeiner Aufbau eines Spektrometers d
Gruppentheorie ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD. Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE
 ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
ERNST MORITZ ARNDT UNIVERSITÄT GREIFSWALD Mathematisch-Naturwissenschaftliche Fakultät INSTITUT FÜR BIOCHEMIE Arbeitskreis Physikalische Chemie Prof. Dr. Walter Langel Gruppentheorie Molekülschwingungen
Valenz-Bindungstheorie H 2 : s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie
 Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
Valenz-Bindungstheorie Beschreibung von Molekülen mit Hilfe von Orbitalen H H H 2 : H 2 s Ueberlappung von Atomorbitalen s-bindung: 2 Elektronen in einem Orbital zylindrischer Symmetrie um die interatomare
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
Teil 4 Massenspektrometrie. Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
Teil 4 Massenspektrometrie Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality 1 Rückblick auf die letzte Vorlesung Grundprinzip der MS: Trennung nach Ladung und Masse
5 Elektronenübergänge im Festkörper
 5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
5 Elektronenübergänge im Festkörper 5.1 Übersicht und Lernziele Übersicht Die Bindung in einem Molekül erfolgt durch gemeinsame Elektronenpaare, die jeweils zwei Atomen angehören (Atombindung, Elektronenpaarbindung).
Atom-, Molekül- und Festkörperphysik
 Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 6. Vorlesung, 16. 5. 2013 Molekülspektren, Normalkoordinaten, Franck-Condonprinzip,
Atom-, Molekül- und Festkörperphysik für LAK, SS 2013 Peter Puschnig basierend auf Unterlagen von Prof. Ulrich Hohenester 6. Vorlesung, 16. 5. 2013 Molekülspektren, Normalkoordinaten, Franck-Condonprinzip,
5.1 Der elektronische Grundzustand in der MP2-Naherung 31 Parameter HF MP2 exp. R OH 0.95 A 0.97 A 0.95 A R NO A 1.41 A 1.41 A R NO2;
 Kapitel 5 Ergebnisse der quantenchemischen Rechnungen In diesem Kapitel werden die Ergebnisse der quantenchemischen ab-initio-rechnungen vorgestellt. Zur Berechnung der Potentialachen im Rahmen des in
Kapitel 5 Ergebnisse der quantenchemischen Rechnungen In diesem Kapitel werden die Ergebnisse der quantenchemischen ab-initio-rechnungen vorgestellt. Zur Berechnung der Potentialachen im Rahmen des in
Spektroskopische Methoden in der Organischen Chemie (OC IV)
 H 3 C 10 O G F D E 8 5 I H GF E D CB A 10 8 5 3 2 1 125 MHz 13 C NMR Spektrum 500 MHz 1 H NMR Spektrum NMR -_1 32 1 H 3 C 10 8 5 10 O G F D E 8 5 Dieder-Winkel: H 10 -H : 5, H -H : 80 H H 8 : 2, H -H :
H 3 C 10 O G F D E 8 5 I H GF E D CB A 10 8 5 3 2 1 125 MHz 13 C NMR Spektrum 500 MHz 1 H NMR Spektrum NMR -_1 32 1 H 3 C 10 8 5 10 O G F D E 8 5 Dieder-Winkel: H 10 -H : 5, H -H : 80 H H 8 : 2, H -H :
3.1 Zur Photochemie von HNO 3 11 Abbildung 3.1: Das UV-Absorptionsspektrum von HNO 3 nach [71] Abbildung 3.2: Das UV-Absorptionsspektrum von HNO 3 nac
![3.1 Zur Photochemie von HNO 3 11 Abbildung 3.1: Das UV-Absorptionsspektrum von HNO 3 nach [71] Abbildung 3.2: Das UV-Absorptionsspektrum von HNO 3 nac 3.1 Zur Photochemie von HNO 3 11 Abbildung 3.1: Das UV-Absorptionsspektrum von HNO 3 nach [71] Abbildung 3.2: Das UV-Absorptionsspektrum von HNO 3 nac](/thumbs/53/31354364.jpg) Kapitel 3 Grundlagen der Photochemie von HNO 3 und Modellentwicklung 3.1 Zur Photochemie von HNO 3 Salpetersaure ist ein wichtiges Nebenprodukt des photochemischen Smogs [67], und es ist ein relevanter
Kapitel 3 Grundlagen der Photochemie von HNO 3 und Modellentwicklung 3.1 Zur Photochemie von HNO 3 Salpetersaure ist ein wichtiges Nebenprodukt des photochemischen Smogs [67], und es ist ein relevanter
1. Zusammenfassung. Zusammenfassung High-spin Verbindungen
 Zusammenfassung 1 1. Zusammenfassung 1.1 High-spin Verbindungen 3-Nitrenodiphenylmethylen (1) und 3,3 -Dinitrenodiphenylmethylen (2) sind gemischte high-spin Verbindungen, die jeweils ein Carbenzentrum
Zusammenfassung 1 1. Zusammenfassung 1.1 High-spin Verbindungen 3-Nitrenodiphenylmethylen (1) und 3,3 -Dinitrenodiphenylmethylen (2) sind gemischte high-spin Verbindungen, die jeweils ein Carbenzentrum
Kinetik zusammengesetzter Reaktionen
 Kinetik zusammengesetzter Reaktionen Kap. 23 1 PC 2 SS 2016 Kinetik zusammengesetzter Reaktionen Kettenreaktionen Explosionen Polymerisationen Schrittweise Polymerisation Kettenpolymerisation Homogene
Kinetik zusammengesetzter Reaktionen Kap. 23 1 PC 2 SS 2016 Kinetik zusammengesetzter Reaktionen Kettenreaktionen Explosionen Polymerisationen Schrittweise Polymerisation Kettenpolymerisation Homogene
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Übungen Atom- und Molekülphysik für Physiklehrer (Teil 2)
 Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen Atom- und Molekülphysik für Physiklehrer (Teil ) Aufgabe 38) Welche J-Werte sind bei den Termen S, P, 4 P und 5 D möglich? Aufgabe 39) Welche Werte kann der Gesamtdrehimpuls eines f-elektrons im
Übungen zur Vorlesung Physikalische Chemie II Lösungsvorschlag zu Blatt 5
 Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Wintersemester 006 / 007 04.1.006 1. Aufgabe Die Wellenfunktionen unterscheiden sich gar nicht. Während der Lösung der elektronischen Schrödingergleichung werden die Kerne als ruhend betrachtet. Es kommt
Anorganische Chemie III
 Seminar zur Vorlesung Anorganische Chemie III Wintersemester 2015/16 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah # Darstellungen für
Seminar zur Vorlesung Anorganische Chemie III Wintersemester 2015/16 Christoph Wölper Institut für Anorganische Chemie der Universität Duisburg-Essen Wiederholung Was bisher geschah # Darstellungen für
VL 24 VL Homonukleare Moleküle VL Heteronukleare Moleküle VL Molekülschwingungen
 VL 24 VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle VL 24 24.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 17.07.2012 1 Zum Mitnehmen Moleküle: Rotation und
VL 24 VL 22 22.1. Homonukleare Moleküle VL 23 23.1. Heteronukleare Moleküle VL 24 24.1. Molekülschwingungen Wim de Boer, Karlsruhe Atome und Moleküle, 17.07.2012 1 Zum Mitnehmen Moleküle: Rotation und
Ψ = Dexp( k II a) mit k II = [ 2m e (V 0 E)/ 2] 1/2
![Ψ = Dexp( k II a) mit k II = [ 2m e (V 0 E)/ 2] 1/2 Ψ = Dexp( k II a) mit k II = [ 2m e (V 0 E)/ 2] 1/2](/thumbs/97/132117650.jpg) Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 015/016 Prof. Dr. Eckhard Bartsch / Marcel Werner M.Sc. Aufgabenblatt 11 vom 9.01.16 Aufgabe 11 1 L
Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 015/016 Prof. Dr. Eckhard Bartsch / Marcel Werner M.Sc. Aufgabenblatt 11 vom 9.01.16 Aufgabe 11 1 L
FLUORESZENZSPEKTROSKOPIE. Biophysik Vorlesung Gábor Talián
 FLUORESZENZSPEKTROSKOPIE Biophysik Vorlesung 05.02.2015. Gábor Talián ENTWURF Lumineszenz Fluoreszenzvorgang Fluorimeter Charakterisierung der Fluoreszenz Fluorophore, Biolumineszenz Lumineszenz Elektronenanregung
FLUORESZENZSPEKTROSKOPIE Biophysik Vorlesung 05.02.2015. Gábor Talián ENTWURF Lumineszenz Fluoreszenzvorgang Fluorimeter Charakterisierung der Fluoreszenz Fluorophore, Biolumineszenz Lumineszenz Elektronenanregung
 Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Vorlesung 20: Roter Faden: Auswahlregeln. Folien auf dem Web:
 Vorlesung 20: Roter Faden: Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/ Wim de Boer, Karlsruhe Atome
Vorlesung 20: Roter Faden: Auswahlregeln Folien auf dem Web: http://www-ekp.physik.uni-karlsruhe.de/~deboer/ Siehe auch: http://www.uni-stuttgart.de/ipf/lehre/online-skript/ Wim de Boer, Karlsruhe Atome
Abiturprüfung Physik, Grundkurs
 Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Homoaromatizität. Charlotte Over Lara Schultes
 Homoaromatizität Charlotte Over Lara Schultes 02.12.2010 Übersicht 1. Einführung 2. Aromatizität 3. Homoaromatizität 4. Beispiele 4.1 Kationische Homoaromaten 4.2 Neutrale Homoaromaten 4.3 Anionische Homoaromaten
Homoaromatizität Charlotte Over Lara Schultes 02.12.2010 Übersicht 1. Einführung 2. Aromatizität 3. Homoaromatizität 4. Beispiele 4.1 Kationische Homoaromaten 4.2 Neutrale Homoaromaten 4.3 Anionische Homoaromaten
Einführung in die Biophysik - Übungsblatt 8
 Einführung in die Biophysik - Übungsblatt 8 July 2, 2015 Allgemeine Informationen: Die Übung ndet immer montags in Raum H030, Schellingstr. 4, direkt im Anschluss an die Vorlesung statt. Falls Sie Fragen
Einführung in die Biophysik - Übungsblatt 8 July 2, 2015 Allgemeine Informationen: Die Übung ndet immer montags in Raum H030, Schellingstr. 4, direkt im Anschluss an die Vorlesung statt. Falls Sie Fragen
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
