Biochemie I. Fachschaft Zahnmedizin Münster
|
|
|
- Kerstin Melsbach
- vor 6 Jahren
- Abrufe
Transkript
1 Biochemie I Fachschaft Zahnmedizin Münster
2 1te Auflage II
3 Zusammenfassung: Biochemie I Inhaltsverzeichnis EINFÜHRUNG:... 1 Grundlagen... 1 Physikalischer/Physiologischer Brennwert... 1 Respiratorischer Quotient... 1 Essentielle Nahrungsfaktoren... 2 Hungerstoffwechsel... 2 Zellkompartimente und ihre diagnostische Bedeutung... 3 Plasmamembran... 3 Lysosomen... 4 Mitochondrien... 4 Peroxisomen... 5 Stoffklassen der Biochemie... 6 Aminosäuren, Peptide und Proteine... 6 Proteine... 6 Aufbau einer Aminosäure... 6 Funktion von Proteinen... 7 Kohlenhydrate... 7 Funktion:... 8 Lipide und Fettsäuren... 8 CoA = Coenzym A... 8 Funktion:... Fehler! Textmarke nicht definiert. Weitere Stoffklassen... Fehler! Textmarke nicht definiert. Theorie chemischer Reaktionen... Fehler! Textmarke nicht definiert. Gleichgewichtslage und Geschwindigkeit unkatalysierter Raktionen... Fehler! Textmarke nicht definiert. Massenwirkungsgesetz... Fehler! Textmarke nicht definiert. Freie Enthalpie / Freie Energie... Fehler! Textmarke nicht definiert. Entropie und Enthalpie... Fehler! Textmarke nicht definiert. Fließgleichgewicht... Fehler! Textmarke nicht definiert. Reaktionskinetik... Fehler! Textmarke nicht definiert. AMINOSÄUREN... Fehler! Textmarke nicht definiert. III
4 Die proteinogenen Aminosäuren... Fehler! Textmarke nicht definiert. Ungeladene (neutrale) Aminosäruen... Fehler! Textmarke nicht definiert. Geladene Aminosäuren... Fehler! Textmarke nicht definiert. Nichtessentielle und essentielle proteinogene AS... Fehler! Textmarke nicht definiert. Selenocystein... Fehler! Textmarke nicht definiert. Nichtproteinogene Aminosäuren... Fehler! Textmarke nicht definiert. Post-Translationale Modifikation... Fehler! Textmarke nicht definiert. Glykosylierungen... Fehler! Textmarke nicht definiert. Desaminierung... Fehler! Textmarke nicht definiert. Transaminierung... Fehler! Textmarke nicht definiert. Decarboxylierung... Fehler! Textmarke nicht definiert. Die wichtigsten posttranslationalen Modifikationen... Fehler! Textmarke nicht definiert. Grundzüge des Aminosäurestoffwechsels... Fehler! Textmarke nicht definiert. Harnstoffzyklus... Fehler! Textmarke nicht definiert. Glutamin- und Ammoniakausscheidung... Fehler! Textmarke nicht definiert. Biogene Amine... Fehler! Textmarke nicht definiert. Ausgewählte Aminosäuren... Fehler! Textmarke nicht definiert. Tyrosin... Fehler! Textmarke nicht definiert. Tryptophan... Fehler! Textmarke nicht definiert. PROTEINE... Fehler! Textmarke nicht definiert. Funktionen... Fehler! Textmarke nicht definiert. Peptidbindung... Fehler! Textmarke nicht definiert. Bindungstypen... Fehler! Textmarke nicht definiert. Wasserstoffbrückenbindungen... Fehler! Textmarke nicht definiert. Hydrophobe Bindungen / Wechselwirkungen... Fehler! Textmarke nicht definiert. Van der Waals-Kräfte... Fehler! Textmarke nicht definiert. Disulfidbindungen... Fehler! Textmarke nicht definiert. Ionenbeziehung / Ionenbindung... Fehler! Textmarke nicht definiert. Proteinstrukturen... Fehler! Textmarke nicht definiert. Primärstruktur... Fehler! Textmarke nicht definiert. Sekundärstruktur... Fehler! Textmarke nicht definiert. Tertiär- und Quartärstruktur... Fehler! Textmarke nicht definiert. Abbau von Proteinen... Fehler! Textmarke nicht definiert. Abbau der Nahrungsproteine... Fehler! Textmarke nicht definiert. Resorption der Abbauprodukte... Fehler! Textmarke nicht definiert. IV
5 Aminosäurestoffwechsel... Fehler! Textmarke nicht definiert. Medizinisch relevante Proteinanalytik... Fehler! Textmarke nicht definiert. Isoelektrische Fokussierung (IEF)... Fehler! Textmarke nicht definiert. Plasma-Elektrophorese... Fehler! Textmarke nicht definiert. SDS-PAGE... Fehler! Textmarke nicht definiert. Anwendungen:... Fehler! Textmarke nicht definiert. Immunoblotting... Fehler! Textmarke nicht definiert. Gelpermeations-Chromatographie... Fehler! Textmarke nicht definiert. Ionenaustausch- Chromatographie... Fehler! Textmarke nicht definiert. Reverse Phase Chromatographie (Hochdruckverfahren)... Fehler! Textmarke nicht definiert. ENZYME... Fehler! Textmarke nicht definiert. Funktion der Enzyme... Fehler! Textmarke nicht definiert. Aktives Zentrum... Fehler! Textmarke nicht definiert. Spezifität... Fehler! Textmarke nicht definiert. Katalytische Zentren... Fehler! Textmarke nicht definiert. Enzymklassen... Fehler! Textmarke nicht definiert. Oxidoreduktasen... Fehler! Textmarke nicht definiert. Transferasen... Fehler! Textmarke nicht definiert. Hydrolasen... Fehler! Textmarke nicht definiert. Lyasen... Fehler! Textmarke nicht definiert. Isomerasen... Fehler! Textmarke nicht definiert. Ligasen... Fehler! Textmarke nicht definiert. Enzymkinetik... Fehler! Textmarke nicht definiert. Maximale Reaktionsgeschwindigkeit... Fehler! Textmarke nicht definiert. Michaelis-Menten-Konstante K m... Fehler! Textmarke nicht definiert. Die Michaelis Menten-Gleichung... Fehler! Textmarke nicht definiert. Das Lineweaver-Burk-Diagramm... Fehler! Textmarke nicht definiert. Enzymhemmung... Fehler! Textmarke nicht definiert. Kompetitive / isosterische Hemmung... Fehler! Textmarke nicht definiert. Nicht-kompetitive Hemmung... Fehler! Textmarke nicht definiert. Allosterische Effekte und Kooperativität... Fehler! Textmarke nicht definiert. Physiologische Reagulation von Enzymaktivitäten... Fehler! Textmarke nicht definiert. Interkonversion:... Fehler! Textmarke nicht definiert. Cofaktor... Fehler! Textmarke nicht definiert. Coenzyme... Fehler! Textmarke nicht definiert. V
6 Prosthetische Gruppen... Fehler! Textmarke nicht definiert. Enzymdiagnostik... Fehler! Textmarke nicht definiert. KOHLENHYDRATE... Fehler! Textmarke nicht definiert. Monosaccharide... Fehler! Textmarke nicht definiert. Struktur und Eigenschaften... Fehler! Textmarke nicht definiert. Pentosen... Fehler! Textmarke nicht definiert. Hexosen... Fehler! Textmarke nicht definiert. Ringschluss bei Glucose und Fructose... Fehler! Textmarke nicht definiert. Oligo- und Polysaccharide... Fehler! Textmarke nicht definiert. Saccharose (α-glc-(1-2)β-fru)... Fehler! Textmarke nicht definiert. Lactose (β-gal(1-4)glc)... Fehler! Textmarke nicht definiert. Maltose (α-glc(1-4)glc)... Fehler! Textmarke nicht definiert. Homoglykane... Fehler! Textmarke nicht definiert. Heteroglykane... Fehler! Textmarke nicht definiert. Reduzierende Zucker... Fehler! Textmarke nicht definiert. Glykosidische Bindung... Fehler! Textmarke nicht definiert. O-glykosidische Bindung... Fehler! Textmarke nicht definiert. N-glykosidische Bindung:... Fehler! Textmarke nicht definiert. Funktionen der Kohlenhydrate im energiestoffwechsel... Fehler! Textmarke nicht definiert. STOFFWECHSELVORGÄNGE... Fehler! Textmarke nicht definiert. Verdauung der Kohlenhydrate... Fehler! Textmarke nicht definiert. 1) Nahrungsaufnahme... Fehler! Textmarke nicht definiert. 2) Verdauung der Disaccharide... Fehler! Textmarke nicht definiert. 3) Resorption der Glucose... Fehler! Textmarke nicht definiert. 4) Glucosetransporter... Fehler! Textmarke nicht definiert. Glykolyse... Fehler! Textmarke nicht definiert. Abschnitt 1... Fehler! Textmarke nicht definiert. Abschnitt 2... Fehler! Textmarke nicht definiert. Reversible und irreversible Schritte... Fehler! Textmarke nicht definiert. Aerobe und Anerobe Glykolyse... Fehler! Textmarke nicht definiert. Substratkettenphosphorilierung... Fehler! Textmarke nicht definiert. Regulation der Glykolyse... Fehler! Textmarke nicht definiert. HARNSTOFFZYKLUS... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. Regulation des Harnstoffzyklus... Fehler! Textmarke nicht definiert. VI
7 Gluconeogenese... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. Ausgangsstoffe der Gluconeogenese... Fehler! Textmarke nicht definiert. Regulation der Gluconeogenese... Fehler! Textmarke nicht definiert. Glykogenstoffwechsel... Fehler! Textmarke nicht definiert. Glykogensynthese... Fehler! Textmarke nicht definiert. Glukogenabbau (Glykogenolyse)... Fehler! Textmarke nicht definiert. Regulation des Glykogenstoffwechsels... Fehler! Textmarke nicht definiert. Pentosephosphatweg... Fehler! Textmarke nicht definiert. Oxidativer Abschnitt... Fehler! Textmarke nicht definiert. Regenerativer Abschnitt /Nichtoxidativer Teil... Fehler! Textmarke nicht definiert. Regulation... Fehler! Textmarke nicht definiert. Pentosephosphatweg in Erythrozyten... Fehler! Textmarke nicht definiert. Stoffwechsel der Galaktose... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. Klinik... Fehler! Textmarke nicht definiert. Stoffwechsel der Fructose... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. Klinik: Fructoseintoleranz... Fehler! Textmarke nicht definiert. LIPIDE, FETTSÄUREN, KETONKÖRPER... Fehler! Textmarke nicht definiert. Chemie der Fettsäuren und Lipide... Fehler! Textmarke nicht definiert. Nicht verseifbare Lipide... Fehler! Textmarke nicht definiert. Verseifbare Lipide... Fehler! Textmarke nicht definiert. Funktionen der Lipide... Fehler! Textmarke nicht definiert. Energiespeicher... Fehler! Textmarke nicht definiert. Strukturelemente... Fehler! Textmarke nicht definiert. Bausteine des Nervengewebes... Fehler! Textmarke nicht definiert. Bausteine biologischer Membranen... Fehler! Textmarke nicht definiert. Bausteine von Signalmolekülen und Vitaminen... Fehler! Textmarke nicht definiert. Aufnahme der Lipide aus der Nahrung... Fehler! Textmarke nicht definiert. Verdauung der lipide... Fehler! Textmarke nicht definiert. Resorption der Lipid-Hydrolyseprodukte... Fehler! Textmarke nicht definiert. Fettsäuresynthese... Fehler! Textmarke nicht definiert. Mechanismus der Fettsäuresynthese... Fehler! Textmarke nicht definiert. Regulation der Fettsäuresynthese... Fehler! Textmarke nicht definiert. VII
8 NADPH für die Fettsäuresynthese Fettsäureabbau und Abbau von TAGs... Fehler! Textmarke nicht definiert. Lipolyse im Fettgewebe... Fehler! Textmarke nicht definiert. β-oxidation... Fehler! Textmarke nicht definiert. Vergleich von Fettsäuresynthese und Fettsäureabbau... Fehler! Textmarke nicht definiert. Synthese von Triacylglycerinen... Fehler! Textmarke nicht definiert. Ketonkörpersynthese... Fehler! Textmarke nicht definiert. Abbau von Ketonkörpern... Fehler! Textmarke nicht definiert. Lipoproteine... Fehler! Textmarke nicht definiert. Chylomikronen... Fehler! Textmarke nicht definiert. VLDL (Very low density lipoproteins)... Fehler! Textmarke nicht definiert. LDL (Low density liporpoteins)... Fehler! Textmarke nicht definiert. HDl (high density lipoproteins)... Fehler! Textmarke nicht definiert. KLINIK: Ateriosklerose... Fehler! Textmarke nicht definiert. Cholesterin... Fehler! Textmarke nicht definiert. Allgemeines... Fehler! Textmarke nicht definiert. Cholesterinbiosynthese... Fehler! Textmarke nicht definiert. OXIDATIVER ENDABBAU... Fehler! Textmarke nicht definiert. PYRUVAT-DEHYDROGENASE... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. Regulation... Fehler! Textmarke nicht definiert. CITRATZYKLUS... Fehler! Textmarke nicht definiert. Funktionen des Citratzyklus... Fehler! Textmarke nicht definiert. Dehydrogenasem... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. Regulation des Citratzyklus... Fehler! Textmarke nicht definiert. Anaplerotosche Reaktionen... Fehler! Textmarke nicht definiert. ATMUNGSKETTE... Fehler! Textmarke nicht definiert. Aufbau der Atmungskette... Fehler! Textmarke nicht definiert. Regulation der Atmungskette und ATP Synthase... Fehler! Textmarke nicht definiert. Beeinflussung der Atmungskette... Fehler! Textmarke nicht definiert. Die ATP Synthase... Fehler! Textmarke nicht definiert. 4 Komponenten... Fehler! Textmarke nicht definiert. Mechanismus... Fehler! Textmarke nicht definiert. MEDIATOREN... Fehler! Textmarke nicht definiert. VIII
9 Eikosanoide... Fehler! Textmarke nicht definiert. Biosynthese... Fehler! Textmarke nicht definiert. Wirkungen... Fehler! Textmarke nicht definiert. Medizinische Nutzung:... Fehler! Textmarke nicht definiert. VITAMINE... Fehler! Textmarke nicht definiert. Fettlösliche Vitamine... Fehler! Textmarke nicht definiert. SPURENELEMENTE... Fehler! Textmarke nicht definiert. Eisen... Fehler! Textmarke nicht definiert. Aufgaben:... Fehler! Textmarke nicht definiert. Eisenstoffwechsel... Fehler! Textmarke nicht definiert. BLUT... Fehler! Textmarke nicht definiert. Erythrozyten... Fehler! Textmarke nicht definiert. Erythrozytenstoffwechsel... Fehler! Textmarke nicht definiert. Hämoglobin... Fehler! Textmarke nicht definiert. Erythropoese... Fehler! Textmarke nicht definiert. Myoglobin... Fehler! Textmarke nicht definiert. IX
10 X
11 EINFÜHRUNG: Grundlagen Der Körper muss Nahrung zu sich nehmen um seinen täglichen Energiebedarf zu decken und essentielle Nahrungsbestandteile (= die er nicht selbst synthetisieren kann) aufzunehmen Energiebedarf wird durch 3 Nährstoffklassen gedeckt: o Kohlenhydrate o Fette o Proteine (=Eiweiße) Ausgewogene Ernährung: 60% Kohlenhydrate, 25% Fette, 15% Proteine Der Organismus baut die verschiedenen Nährstoffe unabhängig von ihrer Klasse zu ATP, Kohlendioxid, Wasser und Wärme ab. Beim Abbau der Proteine/Aminosäuren entsteht als zusätzliches Abbauprodukt Ammoniak, der im Harnstoffzyklus weiter zu Harnstoff abgebaut/entgiftet werden muss Physikalischer/Physiologischer Brennwert Physikalischer Brennwert: die gesamte frei werdende Energie bei der Reaktion eines Nährstoffs mit Suaerstoff im Kalorimeter Physiologischer Brennwert: frei werdender Energiebetrag eines Nährstoffs, der dem Organismus auch wirklich zur Verfügung steht Die Werte für den physiologischen und physikalischen Brennwert sind für Fette und Kohlenhydrate annähernd identisch. Für den Abbau von Proteinen unterscheiden sie sich jedoch, da das Endprodukt des Proteinstoffwechsels (=Harnstoff) selbst noch Energie enthält, die der Organismus jedoch nicht weiter nutzen kann. Daher ist der physikalische Brennwert der Proteine höher als ihr physiologischer Nährstoffklasse Physikalischer Brennwert Physiologischer Brennwert Kohlehydrate 17 kj/g 17 kj/g Fette 37 kj/g 37 kj/g Proteine 23 kj/g 17 kj/g Respiratorischer Quotient Der respiratorische Quotient (=RQ) gibt das Verhältnis von abgegeben CO 2 zu aufgenommenen O 2 (=CO 2/ O 2) wieder Für die Verstoffwechselung der einzelnen Nährstoffklassen erhält man die folgenden Werte: o Kohlenhydrate: 1,0 o Fette: 0,7 o Proteine: 0,85 Die Differenz der Werte von Fetten und Eiweißen gegenüber Kohlenhydraten lässt sich dadurch erklären, dass deren Bestandteile (=Fettsäuren, Aminosäuren) weniger Sauerstoff als die Kohlenhydrate enthalten und folglich zu ihrer Oxidation mehr O 2 aufgenommen werden muss 1
12 Anhand des respiratorischen Quotienten lässt sich die Stoffwechsellage eines Menschen bestimmen: Ist der RQ hoch (=1,0) metabolisert der Organismus vor allem Kohlenhydrate. Sinkt der RQ ab, ist die ein Hinweis auf gestiegene Fettsäure- und Proteinmetabolisierung = Energiemangelzustand Essentielle Nahrungsfaktoren =Stoffe, die für den Ablauf eines normalen Stoffwechsels notwendig sind, aber nicht vom Organismus slsbt synthetisiert werden können Essentielle Aminosäuren o Tryptophan o Lysin o Treonin o Menthionin o Phenylalanin o Leuzin o Isoleuzin o Valin Essentielle Fettsäuren: o Der menschliche Organismus kann nur ungesättigte Fettsäuren mit einer Doppelbindung zwischen der Carboxylgruppe und dem 9. C-Atom einbauen (z.b. Ölsäure) o Fettsäuren mit weiter entfernten Doppelbindungen sind essentiell o Mehrfach ungesättigte Fettsäure Linolsäure (2 Doppelbindungen, C9 und C12) o Linolensäure (drei Doppelbindungen, C9, C12, C15) Weitere essentielle Nahrungsfakroen sind Vitamine, Elektrolyte und Spurenelemente (z.b. Jod, Selen) o Vitamin D ist das einzige nicht essentielle Vitamin, da es vom Menschlichen Organismus aus Cholesterin synthetisiert werden kann Hungerstoffwechsel Bei totaler Nahrungskarenz kommt es im Organismus zu charakteristischen Veränderungen, die folgenden Zielen dienen. o Versorgung peripherer Gewebe mit Energieträgern o Konstanthaltung des Blutzuckerspiegels (Glucosehomöostase) zur Versorgung der oblugaten Glucoseverwerter (=Erythrozyten, Zellen des Nebennierenmarks, Nervenzellen, wobei Nervenzellen be9 längerfristiger Nahrungskarenz einen Teil ihres Energiebedarfs durch die Verwertung von Ketonkörpern decken können) Hungerphasen 1) Glykogenolyse: Beginn der Hungerphase: Glykogenolyse der Leber, die Glykogenvorräte reichen für ca. 24 Stunden; respiratorischer Quotient beträgt zu diesem Zeitpunkt ca. 1 2) Frühphase: Proteinumsatz, Ketogenese o Andauernde Hungerphase: Gluconeogenese deckt minimalen Glucosebedarf der peripheren Gewebe (=Skelettmuskel, Herzmuskel, innere Organe) mit energiereichen 2
13 Substraten. Stoffwechsel stellt sich um und metabolisiert vermehrt Proteine und Fettsäuren, was zu einem Abfall des respiratorischen Quotienten führt (<0,8) o Proteinkatabole Stoffwechsellage: Zunächst werden dabei die Proteine der Peripherie (v.a. Muskleprotein) abgebaut, deren glucoplastische Aminosäuren der Leber als Substrate für die Gluconeogenese dienen 3) Spätphase: Proteinumsatz, Ketogenese o Parallel steigt die Lipolyse im Fettgewebe, um einen exzessiven Abbau der wertvollen Körperproteine zu verhindern. o Die Fettsäuren werden mit Hilfe von Albumin zur Leber transportiert und dort im Rahmen der β-oxidation zu Acteyl-CoA abgebaut. Diese Acetyl-CoA Einheiten verwendet die Leber sowohl als Energielieferanten für ihre aufwendige Gluconeogense (über Einschleusung in den Citratzyklus und die Atmungskette), als auch zur Herstellung von Ketonkörpern, die den peripheren Geweben lebenswichtige Energie liefern. o Unter den Bedingungen eine langfristigen Nahrungskarenz (hohe Ketonkörperkonzentration im Blut) kann auch das ZNS anstelle von Glucose Ketonkörper zur Energiegewinnung verwenden und so zusätzlich Glucose einsparen o Der erhöhte Spiegel von Acetyl-CoA i der Leber kurbelt die Gluconeogenese an Im Hungerstoffwechsel werden die Fettsäuren auch vermehrt von der Skelettmuskulatur selbst oxidiert = abgebaut Zellkompartimente und ihre diagnostische Bedeutung Plasmamembran Aufbau: o Phospholipiddoppelchicht (v.a. Phosphatidylchloin, teils Glyko- und Sphingolipide) o Außen polar, innen unpolar o Je höher der Anteil ungesättigter Fettsäuren ist, desto beweglicher (fluider) ist die Membran o Cholesterin stabilisiert Membranen o Membranproteine können in einer Hälfte der Membran verankert sein, oder sie ganz durchziehen. Membrandurchlässigkeit: o Die Membran ist durchlässig für kurze polare Moleküle wie Wasser, Ammoniak, Ethanol, sowie für Gase o Unpolare Moleküle wie Triacyglycerine und Choelsterinester passieren die membran nicht o Ionen passieren die Membran über Kanäle, größere polare Moleküle über Carrier 3
14 Lysosomen Membranumhüllte intrazelluläre Vesikel zum Abbau von durch Endozytose aufgenommenen Makromolekülen Dabei verschmelzen die sauen, enzymhaltigen primären Lysosomen mit den Endozytosevesikeln zu sekundären Lysosomen Der niedrige ph-wert im Inneren der lysosomen wird durch ATP-abhängige Pumpen aufrechterhalten Typische Lysosomale Enzyme: Glykosidasen, Proteinasen, saure Phosphatase Mitochondrien Von zwei Membranen umschlossene intrazelluläre Strukturen, die vor allem den Energiegewinn dienen Mitochondrien verfügen über eigene, ringförmige DNA mit eigene Code Enzymausstattung: Ciratzyklus, Amungskette, β-oxidation Ketogenese, Glutamatdehydrogenase, GOT Die Enzyme der Atmungskette sitzen in der inneren Mitochondrienmembran, alle anderen schwimmen im gelartigen Plasma =Matrix Die äußere Membran ist mit feinen Poren versehen, die innere Membran verfügt über eine Reihe von Transportsystemen: o ATP/ADP und Phosphat Atmungskette o Acyl-carnitin zweckse EInschleudung von aktivierten Fettsäuren in der β- Oxidation o Citrat/Malat Ausschleudung von Acteyl-CoA zwecks Fettsäure-de-novo Synthese o Malat Ocalacetatausschleusung zwecks Gluconeogenese Stoffwechselwege Im Mitochondrium laufen folgende Stoffwechselwege ab: Β-Oxidation der Fettsäuren Ketonkörperbildung Harnstoffzyklus (teilweise) Porphyrinsynthese Citratszyklus Atmungskette KEINE Glykolyse und KEIN Pentosephosphatweg! Zytosol 4
15 Transportsysteme Mitochondiren sind von zwei Membranen umgeben. Die äußere Membran ist sehr durchlässig. Die innere Membran ist für viele Stoffe jedoch NICHT durchlässig Spezifische Transportsysteme in der inneren Memebran für o ATP, Phosphat, Pyruvat, Malat, α-ketoglutarat, Aspartat, Citrat Substrat ohne spezifisches Transportsystem Wasserstoffatome Acetyl-CoA Acyl-CoA Oxalacetat KEIN spezifisches Transportsystem für NADH +H + Zuständiger Transporter Malat-Shuttle. Glycerophosphat-Shuttle Citrat-Shuttle Carnitin-Shuttle Malat-Shuttle Peroxisomen Mambranumhüllte Vesikel mit hohem Gehalt an H 2O 2 und Sauerstoffradikalen Dienen u.a. zur Fettsäureoxodation. Bei Makrophagen und leukozyten zerstören die Sauerstoffradikalen die membranen phgozytierter Bakterien 5
16 Stoffklassen der Biochemie Aminosäuren, Peptide und Proteine Proteine Proteine (=Eiweiße) sind lange unverzweigte Ketten aus Aminosäuren. Alle Proteine sind aus nur 20 verschiedenen Aminosäuren aufgebaut. Diese Aminosäuren (AS) werden als proteinogen bezeichnet. Die AS Selencystein ist die seltene, aber beachtenswerte 21. Aminosäure, die in ca. 25 Proteinen des Menschen enthalten ist Die Zusammenstellung der AS eines Proteins wird durch die zugehörigen Gene vorgegeben PROTEINE: lange unverzweigte Ketten aus Aminosäuren Aufbau einer Aminosäure Alle AS bestehen aus einem zentralen α-c-atom und seinen vier Bindungspartnern, von denen drei stets identisch sind: o Ein Wasserstoffatom -H o Eine Aminogruppe -NH 2 o Eine Carboxylgruppe -COOH o Der vierte Partner bestimmt die chemischen Eigenschaften der AS Aminosäuren unterscheiden sich also lediglich in der 4. Position am α-c-atom 1 PEPTIDE: Peptide sind kurze Ketten aus Aminosäuren; Die grenze zwischen Peptid und Protein liegt unscharf zwischen 30 und 50 Aminosäuren 6
17 Funktion von Proteinen Viele Proteine sind in erster Linie Baustoffe. o Proteine sind wesentlich an der Bildung zellulärer und extrazellulärer Strukturen beteiligt Komponenten des Zytoskeletts (Aktin, Mikrotubuli, intermediäre Filamente) Kernlamina, die die Membranen der Zellkerne an deren Innenseite stabilisiert Keratine = wesentlicher Bestandteil der haare und der Keratinozyten der äußeren Hautschicht Kollagen (extrazellulär), wichtiger Strukturgeber des Binde- und Stützgewebes Viele Proteine wirken zusätzlich oder ausschließlich als Katalysatoren bestimmter biochemischer Reaktionen = ENZYME ENZYME: Proteine mit katalytischer Funktion. Sie beschleunigen als biologische Katalysatoren spezifisch bestimmte biochemische Reaktionen Kohlenhydrate KOHLENHYDRATE (Saccaride): Bestehen aus einer Kette von mindestens 3 C-Atomen Das Molekül enthält eine Carbonylgruppe (C=O), sodass sich eine Aldehyd- oder eine Ketogruppe ergibt Alle übrigen Kohlenstoffatome sind mit einer OH-Gruppe sowie mit einem Wasserstoffatom verbunden, sodass sich eine H-C-OH Gruppe ergibt. Monosaccaride: Kohlenhydrate, die durch Hydrolyse in Gegenwart von Säzren NICHT in kleinere Moleküle gespalten werden können Oligosaccharid: Mehrere Monosaccharide können durch Bildung kovalenter Bindungen zu Oligosacchariden verknüpft werden Polysaccharide: Polysaccharide sind aus sehr vielen Monosaccharideinheiten aufgebaut. Die Abgrenzung zwischen Oligo- und Polysacchariden ist nicht genau definiert 2 7
18 Funktion: Monosaccharid: Glucose o Glucose (Traubenzucker) ist das berühmteste Kohlenhydrat. Es enthält sechs C- Atome und zählt damit zu den Hexosen. Polymere Formen der Glucose sind z.b. Stärke (Speicherform der Glucose in pflanzlichen Zellen), Glykogen (Speicherform in tierischen Zellen), und Cellulose (wichtigste Bestandteil des Holzes) o Im Verdauungstrakt werden viele verschiedene Kohlenhydrate der Nahrung (z.b. Stärke und Glykogen) zu Glucose abgebaut oder in Glucose umgewandelt o Die Glucose wird in das Blut abgegeben und dient als einer der wichtigsten Energieträger des gesamten Stoffwechsels Oligo-/ Polysaccharide o Dienen als Energiespeicher (Glykogen) in Leber und Muskulatur o Sind mitunter kovalent mit Proteinen bzw. Membranlipiden verbunden (Glykolisierung) Lipide und Fettsäuren LIPIDE Als Lipide werden alle Inhaltsstoffe von Organismen bezeichnet, die in Wasser nur schlecht oder gar nicht löslich sind, die sich aber leicht in organischen Lösungsmitteln wie Chloroform oder Methanol lösen lassen Die verschiedensten Lipide werden von allen Organismen stets ausgehend von Acetyl-CoA synthetisiert FETTSÄUREN Fettsäuren sind unterschiedlich lange Ketten aus Kohlenwasserstoffmolekülen, an deren ende sich eine Carboxylgruppe (-COOH) befindet. Die Kohlenwasserstoffkette ist typischerweise linear und besteht aus CH2- Gruppen. Bei kurzer Wasserstoffkette ist die Fettsäure hydrophil (= wasserlöslich), bei langer Kette schlecht wasserlöslich. Wie die Lipide werden Fettsäuren ausgehend von Acetyl-CoA synthetisiert CoA = Coenzym A Coenzym A hat im Stoffwechsel die Funktion, Acetyl-Gruppen zu übertragen. Alle Lipide und Fettsäuren entstehen, indem mehrere Acetyl-CoA Moleküle ihre Acetylgruppen abgeben und diese durch kovalente Bindungen miteinander verknüpft werden. 3 8
19 9
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
Inhaltsverzeichnis. Organische Chemie und Biochemie 1. Proteine und Peptide 23. Enzyme 47. Coenzyme 71
 Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Inhaltsverzeichnis Organische Chemie und Biochemie 1 1. Die chemische Bindung 1 2. Das Wasser 2 3. Der Kohlenwasserstoff als Grandkörper 4 4. Die funktionellen Gruppen 6 5. Biochemisch wichtige Reaktionen
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, TG, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese, MalonylCoA,
Seminar Biochemie. Lipide und Lipidstoffwechsel. Dr. Christian Hübbers
 Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
Seminar Biochemie Lipide und Lipidstoffwechsel Dr. Christian Hübbers Lernziele Lipidklassen: Fettsäuren, Triglyceride, Phospholipide, Cholesterin, Sphingolipide, Glykolipide. ß-Oxidation, FS-Biosynthese,
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Stoffwechsel - Energiebereitstellung - Biomoleküle
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Biochemie. Kurzes Lehrbuch der. für Mediziner und Naturwissenschaftler. Von Peter Karlson. 12., völlig neubearbeitete Auflage
 Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Aminosäuren 1. Aufbau der Aminosäuren
 Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Aminosäuren 1 Aufbau der Aminosäuren Aminosäuren bestehen aus einer Carbonsäuregruppe und einer Aminogruppe. Die einfachste Aminosäure ist das Glycin mit 2 Kohlenstoffatomen. Das Kohlenstoffatom nach der
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Funktion von Proteinen:
 Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Funktion von Proteinen: Transport und Speicherung Beispiel Myoglobin / Hämoglobin Myoglobin Hämoglobin Globin-Faltung ist konserviert Häm-Gruppe Cofaktoren, Coenzyme & Prosthetische Gruppen Cofaktor wird
Kohlenhydrate Aminosäuren Peptide
 Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Kohlenhydrate Aminosäuren Peptide Kohlenhydrate Kohlenhydrate = Saccharide Sie stellen zusammen mit Fetten und Proteinen den quantitativ größten verwertbaren (z.b. Stärke) und nicht-verwertbaren (Ballaststoffe)
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Stoffwechsel der essentiellen Aminosäuren
 Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Stoffwechsel der essentiellen Aminosäuren Andrea Schulte aus: Löffler/Petrides, Biochemie und Pathobiochemie, 7. Aufl., Kap. 15.3 Gliederung Einleitung: essentielle Aminosäuren, Biosynthese Abbau, Stoffwechselbedeutung
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Hast du dich schon mal gefragt, wie aus dem Essen in deinem Mund eigentlich Energie wird und wie du das am effizientesten für dich nutzen kannst?
 Hast du dich schon mal gefragt, wie aus dem Essen in deinem Mund eigentlich Energie wird und wie du das am effizientesten für dich nutzen kannst? Dann ist diese Grundlagenreihe zum Stoffwechsel und Energiegewinnung
Hast du dich schon mal gefragt, wie aus dem Essen in deinem Mund eigentlich Energie wird und wie du das am effizientesten für dich nutzen kannst? Dann ist diese Grundlagenreihe zum Stoffwechsel und Energiegewinnung
Basiswissen Ernährungslehre
 Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne
 Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Entstehung der Erde und Lebewesen Entwicklung der Zellforschung Kennzeichen des Lebens Grundbaupläne Kennzeichen einer lebenden Zelle Zellen entstehen aus Zellen jede Zelle hat einen kompletten Satz Erbanlagen
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine
 4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
4. Naturstoffe 4.1 Kohlenhydrate 4.2 Lipide 4.3 Aminosäuren, Peptide und Proteine 1 4.1 Kohlenhydrate Einteilung der Kohlenhydrate in drei Gruppen: Monosaccharide (einfache Zucker) Beispiele: Glucose,
Grundlagen Der 50 Die Biochemie und
 Inhalt Einleitung 13 Der 44 2.6.1 Der 45 1.1 Wozu Biochemie? 13 46 1.2 Der Intermediärstoffwechsel 13 2.6.3 Glykogenstoff- 1.3 Die Grundlagen der 13 46 1.4 Die Molekularbiologie 14 Der 48 1.5 Die Hormone
Inhalt Einleitung 13 Der 44 2.6.1 Der 45 1.1 Wozu Biochemie? 13 46 1.2 Der Intermediärstoffwechsel 13 2.6.3 Glykogenstoff- 1.3 Die Grundlagen der 13 46 1.4 Die Molekularbiologie 14 Der 48 1.5 Die Hormone
Organische Chemie der biologischen Stoffwechselwege
 Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
Organische Chemie der biologischen Stoffwechselwege John McMurry / Tadhg Begley aus dem Amerikanischen übersetzt von Karin Beifuss ELSEVIER SPEKTRUM AKADEMISCHER VERLAG Spektrum k_/l AKADEMISCHER VERLAG
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
1. Biochemie-Klausur Zahnmediziner, WS 03/04
 1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
1. Biochemie-Klausur Zahnmediziner, WS 03/04 1. Welche Aussage zur ß-Oxidation von Fettsäuren in Peroxisomen ist falsch? A) Die Aufnahme langkettiger Fettsäuren in die Peroxisomen erfolgt Carnitin-unabhängig!
Proteinogene Aminosäuren. Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren
 Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Proteinogene Aminosäuren Unpolare, aliphatische Seitenketten Monoaminomonocarbonsäuren Proteinogene Aminosäuren Unpolare, heterozyklische Seitenkette Monoaminomonocarbonsäuren Proteinogene Aminosäuren
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Weitere Übungsfragen
 1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
1 Strategie bei multiple choice Fragen Wie unterscheidet sich Glucose von Fructose? (2 Punkte) Glucose hat 6 C Atome, Fructose hat nur 5 C Atome. In der Ringform gibt es bei Glucose α und β Anomere, bei
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
4. Makronährstoffe: Das Wichtigste in Kürze
 4. Makronährstoffe: Das Wichtigste in Kürze Nahrungsbestandteile, die Energie liefern oder liefern können, werden als Makronährstoffe bezeichnet. Nur diese wollen wir im vorliegenden Ratgeber berücksichtigen.
4. Makronährstoffe: Das Wichtigste in Kürze Nahrungsbestandteile, die Energie liefern oder liefern können, werden als Makronährstoffe bezeichnet. Nur diese wollen wir im vorliegenden Ratgeber berücksichtigen.
Energie aus Aminosäuren - Wundermittel Protein?
 Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Jeder von uns kennt die Versprechen der Eiweißshakes: Mehr Proteine machen dich schlank, jung und wunderschön. Aber was haben Proteine an sich, das diese Versprechen rechtfertigt? Dies ist der vierte Teil
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
Proteinstoffwechsel. Bildung der Aminosäuren. Protein-Abbau der Körperproteine. Protein-Abbau der Nahrungsproteine. Verwertung der Aminosäuren
 Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Bildung der Aminosäuren Körperproteine 10000 g Nahrungsproteine Proteinstoffwechsel Proteolyse (300 400 g/d) AminosäurePool Verdauung (50 100 g/d) 100 g Vortragender: Dr. W. Helliger Neusynthese aus z.b.
Die Biochemie der Fette und deren Bedarfsempfehlungen für den Menschen
 Autor: Dr. Ulrike Jambor de Sousa Klinik, Institut: Titel: Die Biochemie der Fette und deren Bedarfsempfehlungen für den Menschen Inhaltsverzeichnis Einleitung Triglyceride Fett-Verdauung Lipoproteine
Autor: Dr. Ulrike Jambor de Sousa Klinik, Institut: Titel: Die Biochemie der Fette und deren Bedarfsempfehlungen für den Menschen Inhaltsverzeichnis Einleitung Triglyceride Fett-Verdauung Lipoproteine
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Kohlenhydrate. Prof. Dr. Albert Duschl
 Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
Kohlenhydrate Prof. Dr. Albert Duschl Kohlenhydrate in der Nahrung Kohlenhydrate sind in zwei Formen in unserer Nahrung vorhanden: Als komplexe Zucker, wie Stärke in Getreideprodukten, und als einfache
DIGITAL & ANALOG
 DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG WORT & BILD ~,
DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG DIGITAL & ANALOG WORT & BILD ~,
Auswahlverfahren Medizin Prüfungsgebiet Chemie. 6.Termin Organische Chemie Naturstoffe
 Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Auswahlverfahren Medizin Prüfungsgebiet Chemie 6.Termin Organische Chemie Naturstoffe Kursleiter Mag. Wolfgang Mittergradnegger IFS Kurs 2009 Organische Chemie Naturstoffe Fette Kohlenhydrate Proteine
Membranen (3a) Membrane
 Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Membranen (3a) Biochemie Membrane Funktionen Abgrenzung der Zelle nach außen hin schaffen geeignete Voraussetzungen für einzelne enzymatische Reaktionen Signalübertragung tragen Signalstrukturen für die
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Aminosäuren und Proteine
 Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Aminosäuren und Proteine Von Mohammed Jaber Aminosäuren und Proteine Kleinigkeit: 23 proteinogene AS 250 nicht-proteinogene AS (Anzahl synthetisch erzeugten erheblich größer) Aminosäuren und Proteine Kleinigkeit:
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Mehr Proteine für mehr Gesundheit und weniger Übergewicht?
 Medizin Sven-David Müller Mehr Proteine für mehr Gesundheit und weniger Übergewicht? Alles über Eiweiß, Eiweiße, Protein und Proteine Wissenschaftlicher Aufsatz Mehr Proteine für mehr Gesundheit und weniger
Medizin Sven-David Müller Mehr Proteine für mehr Gesundheit und weniger Übergewicht? Alles über Eiweiß, Eiweiße, Protein und Proteine Wissenschaftlicher Aufsatz Mehr Proteine für mehr Gesundheit und weniger
Glykogen. 1,6-glykosidisch verbunden sind. Die Verzweigungen dienen dazu das Molekül an vielen Stellen gleichzeitig ab- oder aufzubauen.
 Glykogen Glykogen stellt die Speicherform der Glucose dar. Der menschliche Körper kann Glucose nicht speichern (Osmose). Es können ca. 400g Glucose als Glykogen aufbewahrt werden. Chemischer Aufbau: Glykogen
Glykogen Glykogen stellt die Speicherform der Glucose dar. Der menschliche Körper kann Glucose nicht speichern (Osmose). Es können ca. 400g Glucose als Glykogen aufbewahrt werden. Chemischer Aufbau: Glykogen
Taschenatlas Biochemie des Menschen
 Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Taschenatlas Biochemie des Menschen Bearbeitet von Jan Koolman, Klaus-Heinrich Röhm 4., vollständig überarbeitete und erweiterte Auflage 2009. Buch. XII, 529 S. Kartoniert ISBN 978 3 13 759404 8 Format
Biologie für Mediziner
 Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Biologie für Mediziner - Zellbiologie 1 - Prof. Dr. Reiner Peters Institut für Medizinische Physik und Biophysik/ CeNTech Robert-Koch-Strasse 31 Tel. 0251-835 6933, petersr@uni-muenster.de Dr. Martin Kahms
Lipide. Dr. med. Tamás Pándics. Biochemie I. SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie
 Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Lipide Biochemie I Dr. med. Tamás Pándics SEMMELWEIS UNIVERSITÄT Institut für Medizinische Biochemie Lipide Definition: hydrophobe Biomoleküle Heterogene Gruppe mit abwechslungsreichen Funktionen: Bestandteile
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Fettsäurebiosynthese
 Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Fettsäurebiosynthese Inhalt Fettsäuren Triacylglyceride FS-Biosynthese und einzelne Schritte Fettsäuren Lange CH-Ketten mit einer endständigen Carboxylgruppe 3 Gruppen: -> gesättigte FS -> einfach ungesättigte
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau. (Biomoleküle allgemein)
 Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
0.1 Eiweißstoffe (Proteine)
 1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
1 22.06.2006 0.1 Eiweißstoffe (Proteine) 0.1.1 Die Aminosäuren Bausteine der Proteine Proteine sind aus einer Vielzahl (bis Tausende) von Baueinheiten zusammengesetzte Makromoleküle. Die einzelnen Bausteine,
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur ( )
 Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Mohammed Jaber KOHLENHYDRATE
 Mohammed Jaber KOHLENHYDRATE Wichtige Disaccharide: Maltose alpha-glc(1-4)glc entsteht als Zwischenprodukt beim Stärkeund Glykogenabbau Saccharose a-glc(1-6)ß-fru kann bei parenteraler Zufuhr nicht gespalten
Mohammed Jaber KOHLENHYDRATE Wichtige Disaccharide: Maltose alpha-glc(1-4)glc entsteht als Zwischenprodukt beim Stärkeund Glykogenabbau Saccharose a-glc(1-6)ß-fru kann bei parenteraler Zufuhr nicht gespalten
Stoffklasse: LIPIDE Funktionen in der Zelle
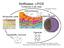 Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Stoffklasse: LIPIDE Funktionen in der Zelle Zellmembranen Industrielle Nutzung Strukturelle Lipide Speicherstoffe Signalstoffe, Hormone Pigmente 2 1 R 1 R 2 3 5 7 2 4 A 6 B 8 R 3 1 21 22 9 N N H 17 1 20
Examensklausur Ernährungsphysiologie und angewandte Biochemie
 Examensklausur Ernährungsphysiologie und angewandte Biochemie Prüfungsnummer Bevor Sie beginnen + Teilen Sie sich Ihre Zeit gut ein! Die Arbeit umfasst 8 Aufgaben und sie haben 4 Stunden Zeit. Achten Sie
Examensklausur Ernährungsphysiologie und angewandte Biochemie Prüfungsnummer Bevor Sie beginnen + Teilen Sie sich Ihre Zeit gut ein! Die Arbeit umfasst 8 Aufgaben und sie haben 4 Stunden Zeit. Achten Sie
Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte)
 Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Scheinbedingungen für die Lehrveranstaltung Praktikum der Biochemie/ Molekularbiologie
 Scheinbedingungen für die Lehrveranstaltung Praktikum der Biochemie/ Molekularbiologie gültig ab: Wintersemester 2011/12 verantwortlicher Fachvertreter: Prof. K.-D. Fischer, Institut für Biochemie und
Scheinbedingungen für die Lehrveranstaltung Praktikum der Biochemie/ Molekularbiologie gültig ab: Wintersemester 2011/12 verantwortlicher Fachvertreter: Prof. K.-D. Fischer, Institut für Biochemie und
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lehrerhandreichungen zu: "Zellatmung" Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Zellatmung" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter ADP; Atmungskette; ATP;
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Zellatmung" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter ADP; Atmungskette; ATP;
10 BIOGENE-AMINE 4 NICHT-PROTEINOGENE- AS. 20 PROTEINOGENE AS glucoplastisch/ketoplastisch 8 ESSENTIELLE AS
 Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
Für uns! - es gibt 20 AS Diese sind wiederum aufgeteilt in: Neutrale AS Saure AS Basische AS Schwefelhaltige AS Aromatische AS Heterocyklische AS - es gibt 20 AS - davon sind 8 essentiell d.h.: der Körper
1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog.
 FRAGENKATALOG 1 1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog. 3) Bei der schriftlichen Prüfung kommt je eine Frage aus 10 der 11 Kapitel (10 Hauptfragen), plus eine Zusatzaufgabe.
FRAGENKATALOG 1 1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog. 3) Bei der schriftlichen Prüfung kommt je eine Frage aus 10 der 11 Kapitel (10 Hauptfragen), plus eine Zusatzaufgabe.
Was ist denn NAD / NADP??
 Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Exkurs Oxidative Desaminierung: Was ist denn NAD / NADP?? Exkurs Oxidative Desaminierung: NAD / NADP gehört zum Vitamin B2- Komplex Nikotinsäureamid = Nikotinamid= Vit B3 Exkurs Oxidative Desaminierung:
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Kraftwerk Körper Energiegewinnung in unseren Zellen
 Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Was passiert eigentlich, wenn wir etwas essen und dann loslaufen müssen? Wie können unsere Zellen die Stoffen aus der Nahrung zur Energiegewinnung nutzen? Die Antwort auf diese Fragen gibt s in diesem
Beispiele für Prüfungsfragen zu den Einheiten. 2, 3, 5, 9-12, 15, 16, und 21 (Hartig)
 Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Beispiele für Prüfungsfragen zu den Einheiten 2, 3, 5, 9-12, 15, 16, und 21 (Hartig) Untenstehendes Molekül ist ein Peptidhormon. Wieviele Peptidbindungen besitzt dieses Molekül (zeichnen Sie diese ein)?
Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher)
 Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher) Wieviele Elektronen, Protonen und Neutronen besitzt ein Kohlenstoffatom? Wie unterscheiden sich die Kohlenstoffisotope
Fragen zur Vorlesung Grundlagen der Biologie (I) Teil 1: Biomoleküle (B. Moerschbacher) Wieviele Elektronen, Protonen und Neutronen besitzt ein Kohlenstoffatom? Wie unterscheiden sich die Kohlenstoffisotope
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Inhaltsverzeichnis. Vorwort. Stoffe in Zellen 1 Wasser
 V Vorwort XI Stoffe in Zellen 1 Wasser 2 Bau- und Inhaltsstoffe der Zelle 3 Ribose und Desoxyribose 4 UV-Absorption von Tyrosin 5 Anthocyan-Blütenfarbstoffe 6 Rotkraut - Blaukraut 7 Warum ist die Kornblume
V Vorwort XI Stoffe in Zellen 1 Wasser 2 Bau- und Inhaltsstoffe der Zelle 3 Ribose und Desoxyribose 4 UV-Absorption von Tyrosin 5 Anthocyan-Blütenfarbstoffe 6 Rotkraut - Blaukraut 7 Warum ist die Kornblume
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
«Ausdauertraining» Naturwissenschaftliche Aspekte
 EHSM / Trainerbildung Jost Hegner Was verstehen wir unter «Leistung» im pädagogischen Sinne? unter «Leistung» im physikalischen Sinne: Power (in Joule/s; Watt)? unter «Leistung» im physiologischen Sinne:
EHSM / Trainerbildung Jost Hegner Was verstehen wir unter «Leistung» im pädagogischen Sinne? unter «Leistung» im physikalischen Sinne: Power (in Joule/s; Watt)? unter «Leistung» im physiologischen Sinne:
Der Stoffwechsel: Konzepte und Grundmuster
 Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Der Stoffwechsel: Konzepte und Grundmuster 1 Lebende Organismen Was unterscheidet lebende Organismen von toter Materie? Lebende Organismen haben einen hohen Gehalt an chemischer Komplexität und Organisation
Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur
 Naturwissenschaft Sarah Fuhrken Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur Zusammenfassung Stoffwechselphysiologie Lernzettel Biologie, 1. Semester Brown sche Molekularbewegung:
Naturwissenschaft Sarah Fuhrken Stoffwechselphysiologie. Zusammenfassung für das mündliche Abitur Zusammenfassung Stoffwechselphysiologie Lernzettel Biologie, 1. Semester Brown sche Molekularbewegung:
Hemmung der Enzym-Aktivität
 Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Hemmung der Enzym-Aktivität Substrat Kompetitiver Inhibitor Enzym Enzym Substrat Nichtkompetitiver Inhibitor Irreversibler Inhibitor Enzym Enzym Enzym - Kinetik Michaelis Menten Gleichung Lineweaver -
Zellulärer Abbau von Proteinen in Aminosäuren:! Proteine werden in Zellen durch Proteasom-Komplexe in! einzelne Aminosäuren abgebaut.!
 Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Zellulärer Abbau von Proteinen in Aminosäuren: Proteine werden in Zellen durch Proteasom-Komplexe in einzelne Aminosäuren abgebaut. Abbau von Aminosäuren: Uebersicht über den Aminosäureabbau Als erster
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion. Mag. Gerald Trutschl
 Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Enzyme (Teil 1) Aminosäuren, Aufbau, Eigenschaften & Funktion Mag. Gerald Trutschl 1 Inhalt 1. Einführung 2. Aufbau: - Aminosäuren - Peptidbindung - Primärstruktur - Sekundärstruktur - Tertiär- und Quatärstrukturen
Leseprobe. Biologie, Physik, Chemie und Mathematik für angehende Mediziner. Thomas Knauss
 Leseprobe Biologie, Physik, Chemie und Mathematik für angehende Mediziner Thomas Knauss Skriptum zur Vorbereitung auf den Medizinaufnahmetest MED-AT -H/-Z an den österreichischen Universitäten in Wien,
Leseprobe Biologie, Physik, Chemie und Mathematik für angehende Mediziner Thomas Knauss Skriptum zur Vorbereitung auf den Medizinaufnahmetest MED-AT -H/-Z an den österreichischen Universitäten in Wien,
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
