Station 2: Wieviel Zucker enthält der Honig?
|
|
|
- Dirk Schäfer
- vor 6 Jahren
- Abrufe
Transkript
1 Station 2: Wieviel Zucker enthält der Honig? Quantitative Gesamtzuckerbestimmung [1] Geräte und Chemikalien: Erlenmeyerkolben (300 ml), Messkolben mit Schraubdeckel (250 ml), Glastrichter, Faltenfilter, Messzylinder (100 ml), Stativ (2 x), Stativklemme (3 x), Erlenmeyerkolben mit Schliff (300 ml), Heizplatte/Magnetrührer (2 x), Laborhebebühne, Schliffklammer NS 29, Rückflusskühler, Wasserschlauch (2x), Schlauchschellen (3x), Siedesteinchen, Stoppuhr, Plastikschüssel, Waage, Spatel, Becherglas (50 ml), Bürette (25 ml), Vollpipetten (2 x 25 ml, 2 x 5 ml), Messpipette (5 ml), Glastrichter (klein), Rührfisch, Einmalpipette, Taschenrechner zur Auswertung Eingesetzte Stoffe Gefahrensymbole H- und P-Sätze destilliertes Wasser - - Honig - - Carrez-Lösung I - H: 412 P: 273 EUH: 032 Carrez-Lösung II H: P: Luff sche Lösung H: P: Kaliumiodid H: P: %ige Schwefelsäure H: P: Stärke-Lösung - - Natriumthiosulfat-Lösung (c = 0,1 mol ) l Eis
2 Probenvorbereitung: Da bestimmte Bestandteile im Honig die Ausfällung von Kupfer(I)-oxid beeinflussen können, müssen diese zunächst abgetrennt werden. Hierfür werden exakt 5 g Honig in einem Becherglas in 150 ml destilliertem Wasser gelöst und in einen 250ml-Messkolben überführt. Die Lösung wird mit 5 ml der Carrez-Lösung I versetzt und kräftig geschüttelt. Nach Zugabe von 5 ml der Carrez-Lösung II wird erneut geschüttelt, der Messkolben bis zur 250 ml-marke mit destilliertem Wasser aufgefüllt und für ca. eine Minute stehen gelassen. Die Lösung wird anschließend über einen Faltenfilter filtriert. Durchführung: (Wiederholung des Ablaufs im Blindversuch mit Wasser ohne Honig) a) Oxidation der reduzierenden Zucker mit Kupfer(II)-Ionen: Zunächst werden 2,5 ml der Carrez-geklärten Honig-Lösung mit destilliertem Wasser auf 25 ml aufgefüllt und in einen Erlenmeyerkolben mit Schliff überführt. Anschließend werden 25 ml Luff sche Lösung zugefügt. (Achtung! Im Abzug arbeiten und Schutzhandschuhe tragen!) Nach Zugabe von fünf Siedesteinchen wird die Lösung auf einer vorgeheizten(!) Heizplatte unter Rückfluss in zwei Minuten bis zum Sieden erhitzt (vgl. Abb. 1). Nach einer Siedezeit von exakt zehn Minuten wird das Gemisch in einem Eiswasserbad gekühlt. b) Iodometrische Titration des Kupfer(II)-Überschusses: Ist die Probenlösung erkaltet, so werden 3 g Kaliumiodid sowie 25 ml 25%ige Schwefelsäure unter vorsichtigem Umschwenken zugegeben. Nach der Zugabe von circa 3 ml Stärke- Lösung wird mit einer 0,1-molaren Natriumthiosulfat-Maßlösung bis zum Verschwinden der Blaufärbung titriert (vgl. Abb. 1). Abb. 1: Versuchsaufbau zum Erhitzen unter Rückfluss (links) und zu Titration (rechts)
3 Beobachtung: a) Durch Zusammenführen der Carrez-geklärten Honig-Lösung und dem Luff schen Reagenz entsteht eine blaue Lösung. Aus dieser fällt beim Erhitzen ein rotbrauner Niederschlag aus. b) Nach der Zugabe von Kaliumiodid und verdünnter Schwefelsäure ist ein Farbumschlag nach orange-braun zu erkennen. Durch Zugabe der Stärke-Lösung entsteht eine blau-schwarze Färbung. Bei der Titration mit Natriumthiosulfat-Lösung verschwindet die blau-schwarze Färbung und die Lösung wird milchig grau. Der Verbrauch an Natriumthiosulfat-Lösung beträgt ca. 8,7 ml, bei der Blindprobe liegt der Verbrauch bei ca. 23,6 ml. Deutung: a) Die Blaufärbung ist auf das Vorhandensein von Kupfersulfat zurückzuführen. Bei dem rot-braunen Niederschlag handelt sich um Kupfer(I)-oxid (vgl. Station 1). b) Die Iodid- und die Kupfer(II)-Ionen reagieren in einer Redoxreaktion zu Iod und Kupfer(I)-iodid. Nach Zugabe der Stärke-Lösung bildet sich eine tiefblaue Einschlussverbindung (vgl. Station 3). Durch Titration mit der Natriumthiosulfat- Lösung wird das Iod wieder zu Iodid reduziert, wodurch die Einschlussverbindung abgebaut wird. Die relevanten Reaktionsgleichungen dieser Methode nach Luff-Schoorl [1] sind in Abb. 2 dargestellt. Oxdation der Kupfer(II)-Ionen : 2 Cu 2+ reduzierende Zucker Cu 2 O Iodbildung: 2 Cu I - 2 CuI 2 2 CuI + I 2 Titration: I S 2 O I - + S 4 O 6 2- Abb. 2: Reaktionsgleichungen der Methode nach Luff- Schoorl [1] Auswertung: Der korrigierte Verbrauch an Natriumthiosulfat-Lösung V(Na2S2O3) in ml wird berechnet, indem man den Verbrauch im Versuch vom Verbrauch bei der Blindprobe abzieht: V(Na 2 S 2 O 3 ) = V(Na 2 S 2 O 3 ) Blindprobe - V(Na 2 S 2 O 3 ) Hauptversuch Der Zuckergehalt kann anschließend für den so berechneten Verbrauch aus Tabelle 1 abgelesen werden. In der titrierten Probe liegen damit ca. 38,5 mg Invertzucker vor. Bei der Carrez-Klärung wurden 5 g Honig in insgesamt 250 ml destilliertem Wasser gelöst. Da exakt 2,5 ml dieser Honig-Lösung im Versuch eingesetzt wurden, liegen in der titrierten Probe 50 mg Honig vor. Somit enthalten 50 mg Honig ca. 38,5 mg Glucose und Fructose, dies entspricht etwa 77 %.
4 Tab. 1: Ermittlung des Gehalts an reduzierendem Zucker [1] V(Na 2S 2O 3) in [ml] Invertzucker (Glucose und Fructose in gleichem Anteil) in [mg] Lactose, wasserfrei in [mg] Maltose, wasserfrei in [mg] 1 2,4 3,6 3,9 2 4,8 7,3 7,8 3 7,2 11,0 11,7 4 9,7 14,7 15,6 5 12,2 18,4 19,6 6 14,7 22,1 23,5 7 17,2 25,8 27,5 8 19,8 29,5 31,5 9 22,4 33,2 35, ,0 37,0 39, ,6 40,8 43, ,3 44,6 47, ,0 48,4 51, ,7 52,2 55, ,5 56,0 59, ,3 59,9 63, ,2 63,8 68, ,1 67,7 72, ,0 71,7 75, ,0 75,7 80, ,0 79,8 85, ,1 83,9 90, ,2 88,0 94,6 Entsorgung: Zur Probelösung wird im Eisbad vorsichtig so viel Natronlauge zugegeben bis der ph-wert im schwach alkalischen Bereich liegt. Vorsicht! Die Lösung kann dabei sehr heiß werden! Die Entsorgung erfolgt nach Abkühlen als anorganische, schwermetallhaltige Abfälle.
5 Zusatzmaterial zur Station 2 Die Bestimmung des Zuckeranteils im Honig erfolgt unter der Annahme, dass die Menge des experimentell bestimmten Invertzuckers in guter Näherung dem Gesamtzuckergehalt des Honigs entspricht (vgl. Station 1). Die gewonnenen Ergebnisse können abschließend mit Angaben auf den Etiketten kommerziell erhältlicher Honige (z.b. Abb. 3) verglichen und entsprechende Schlussfolgerungen werden. Abb. 3: Typisches Honigetikett mit angegebenem Zuckeranteil zum Vergleich mit den experimentellen Ergebnissen Die verwendete Methode nach Luff-Schoorl ist ein Verfahren zur quantitativen Bestimmung reduzierender Zucker, welches auf dem Prinzip der Fehling-Probe basiert. Da die Reaktionen bei der Fehling-Probe nicht quantitativ ablaufen, wird bei diesem Verfahren unter exakt festgelegten Bedingungen gearbeitet und die Aus-wertung wird anhand einer darauf abgestimmten Tabelle vorgenommen. Für die Lernenden erweist sich das Verständnis der Methode wegen der teilweise komplexen Reaktionsabfolge und der Zugabe von Lösungen im Überschuss vielfach als schwierig. Zur Veranschaulichung der Stoffumsätze kann deshalb das in Abb. 4 dargestellte, vereinfachte Schema herangezogen werden. Zu Beginn liegt eine Probe-lösung vor, in der sich eine bestimmte, unbekannte Menge an reduzierenden Zuckern befindet. Diese wird mit einer definierten Menge an Kupfer(II)-Ionen versetzt, wobei diese im Überschuss zugegeben wird. Hierdurch entsteht eine von der Menge
6 an reduzierenden Zuckern abhängige Menge Kupfer(I)-oxid. Durch die quantitative Bestimmung des Überschusses an Kupfer(II)-Ionen kann auf die Kupfer(I)-oxid- Konzentration und somit auf die Menge an reduzierenden Zuckern geschlossen werden. Zu diesem Zweck wird die Lösung mit einer definierten Menge an Iodid-Ionen wiederum im Überschuss versetzt. Hierdurch entsteht in Abhängigkeit von der vorliegenden Kupfer(II)-Ionen-Konzentration unter anderem eine bestimmte Menge an Iod. Die Iod-Menge kann durch Titration mit Natriumthiosulfat-Lösung ermittelt werden. Literatur: [1] Matissek, R.; Steiner, G.; Fischer, M.: Lebensmittelanalytik 4. vollständig überarbeitete Auflage, Springer-Verlag, Berlin, 2010.
7 Abb. 4: Vereinfachte, schematische Darstellung der Methode nach Luff-Schoorl
8 Versuchsbezogene Betriebsanweisungen Versuchsbezogene Betriebsanweisung nach 20 GefStoffV Schülerlabor Chemie des Bienenhonigs Bestimmung des Gehalts an reduzierendem Zucker mittels der Methode nach Luff-Schoorl Reaktionsgleichungen: reduzierende Zucker 2 Cu 2+ Cu 2 O 2 CuSO KI 2 CuI + I K 2 SO 4 eingesetzte Stoffe I Na 2 S 2 O 3 2 NaI + Na 2 S 4 O 6 Gefahrensymbole Nummern der H und P Sätze Destilliertes Wasser - - Honig - - Carrez-Lösung I Carrez-Lösung II Luff sche Lösung Kaliumiodid 25%ige Schwefelsäure - H: 412 P: 273 EUH: 032 H: P: H: P: H: P: H: P: Stärke-Lösung - - Natriumthiosulfat-Lösung (c = 0,1 mol ) - - l Eis - -
9 H290 Kann gegenüber Metallen korrosiv sein. H302 Gesundheitsschädlich bei Verschlucken. H314 Verursacht schwere Verätzungen der Haut und Augenschäden. H318 Verursacht schwere Augenschäden. Wortlaut der oben genannten H und P Sätze H410 Sehr giftig für Wasserorganismen mit langfristiger Wirkung. H411 Giftig für Wasserorganismen, mit langfristiger Wirkung. H412 Schädlich für Wasserorganismen, mit langfristiger Wirkung. P280 Schutzhandschuhe / Schutzkleidung / Augenschutz / Gesichtsschutz tragen. P Bei Verschlucken: Mund ausspülen. Kein Erbrechen herbeiführen. P Bei Kontakt mit den Augen: Einige Minuten lang behutsam mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. P Bei Exposition oder Unwohlsein: Sofort GIFTINFORMATIONSZENTRUM oder Arzt anrufen. P501 Inhalt / Behälter zuführen. EUH032 Entwickelt bei Berührung mit Säure sehr giftige Gase. Gefahren für Mensch und Umwelt, die von den Edukten oder Produkten ausgehen, soweit sie nicht durch die Angaben auf der Vorderseite abgedeckt sind: Kaliumiodid: Reizt die Augen und Atmungsorgane. Resorption größerer Mengen führt zu Blutdruckabfall, Lähmungen und Erbrechen. Nicht mit Alkalimetallen, Ammoniak, Halogen- Halogenverbindungen, Fluor oder Wasserstoffperoxid in Berührung bringen. Schwefelsäure: heftige Reaktion mit Basen und vielen organischen Stoffen möglich. Die meisten Metalle werden korrodiert. Beim Verdünnen mit Wasser erfolgt exotherme Reaktion. Verursacht schwere Verätzungen. Reizt die Atmungsorgane. Starke Mineralsäuren bewirken allgemein auf Haut-oder Schleimhautgewebe in Abhängigkeit von Konzentration und Einwirkungsdauer zunehmend Entzündungen und Nekrosen. Besonders gefährdet sind die Augen durch Hornhautverätzungen oder Perforation. Hustenreiz, Entzündung der oberen Atemwege bis zu Ödemen. Erstickungsgefahr! Beim Verschlucken konzentrierter Säuren Lebensgefahr!
10 Verhalten im Gefahrfall, Erste-Hilfe-Maßnahmen: Kaliumiodid, Schwefelsäure, Luff sche Lösung, Carrez-Lösungen: Nach Hautkontakt: Mit reichlich Wasser abwaschen. Nach Augenkontakt: Mit reichlich Wasser bei geöffnetem Lidspalt mindestens 15 Minuten ausspülen. Sofort Augenarzt hinzuziehen. Nach Einatmen: Frischluft. Nach Kleidungskontakt: Kontaminierte Kleidung sofort entfernen. Entsorgung: Kaliumiodid: gelöst in Wasser in den Abguss. Schwefelsäure: nach vorsichtiger Neutralisation im Eisbad mit viel Wasser in den Abguss Probenlösung: im Eisbad vorsichtig so viel Natronlauge zugegeben bis der ph-wert im schwach Alkalischen liegt. Nach Abkühlen als anorganische, schwermetallhaltige Lösung entsorgen Gefährdungsbeurteilung Versuch: Bestimmung des Gehalts an reduzierendem Zucker mittels der Methode nach Luff-Schoorl Ausgangsstoffe: destilliertes Wasser: kein Gefahrstoff Honig: kein Gefahrstoff Stärke-Lösung: kein Gefahrstoff Natriumthiosulfat-Lösung: kein Gefahrstoff Citronensäure: mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. Natriumcarbonat
11 mit Wasser spülen. Eventuell vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. Kupfersulfat H302 Gesundheitsschädlich bei Verschlucken. H410 Sehr giftig für Wasserorganismen mit langfristiger Wirkung. mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. P501 Inhalt/ Behälter einer anerkannten Abfallentsorgungsanlage zuführen. Kaliumhexacyanoferrat(II) H412 Schädlich für Wasserorganismen, mit langfristiger Wirkung. EUH032 Entwickelt bei Berührung mit Säure sehr giftige Gase. Zinkacetat-Dihydrat H302 Gesundheitsschädlich bei Verschlucken. H410 Sehr giftig für Wasserorganismen mit langfristiger Wirkung mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. P501 Inhalt/ Behälter einer anerkannten Abfallentsorgungsanlage zuführen. Kaliumiodid: H302 Gesundheitsschädlich bei Verschlucken. mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen 25%ige Schwefelsäure: Signalwort: Gefahr! H290 Kann gegenüber Metallen korrosiv sein. H314 Verursacht schwere Verätzungen der Haut und schwere Augenschäden. P280 Schutzhandschuhe / Schutzkleidung / Augenschutz / Gesichtsschutz tragen. P Bei Verschlucken: Mund ausspülen. Kein Erbrechen herbeiführen.
12 P Bei Kontakt mit den Augen: Einige Minuten lang behutsam mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. P Bei Exposition oder Unwohlsein: Sofort Giftinformationszentrum oder Arzt anrufen. Produkte: Kupfer(I)oxid: H302 Gesundheitsschädlich bei Verschlucken. H410 Sehr giftig für Wasserorganismen mit langfristiger Wirkung. P501 Inhalt/ Behälter einer anerkannten Abfallentsorgungsanlage zuführen. Gluconsäure: H319 Verursacht schwere Augenreizung Kupfer(I)iodid: H302 Gesundheitsschädlich bei Verschlucken. H335 Kann die Atemwege reizen. H410 Sehr giftig für Wasserorganismen mit langfristiger Wirkung P261 Einatmen von Staub vermeiden. mit Wasser spülen. Eventuell vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. P501 Inhalt/ Behälter einer anerkannten Abfallentsorgungsanlage zuführen. Iod: Signalwort: Gefahr! H312 + H332 Gesundheitsschädlich bei Hautkontakt oder Einatmen H335 Kann die Atemwege reizen. H372 Schädigt die Organe bei längerer oder wiederholter Exposition durch Verschlucken. H400: Sehr giftig für Wasserorganismen. P302 + P352 Bei Berührung mit der Haut: Mit viel Wasser und Seife waschen. mit Wasser spülen. Eventuell vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen.
13 P314 Bei Unwohlsein ärztlichen Rat einholen/ ärztliche Hilfe hinzuziehen. Kaliumtetrathionat: H335 Kann die Atemwege reizen. P261 Einatmen von Staub/ Rauch/ Gas/ Nebel/ Dampf/ Aerosol vermeiden. mit Wasser spülen. Vorhandene Kontaktlinsen nach Möglichkeit entfernen. Weiter spülen. Dikaliumtrizinkhexacyanoferrat: unbekannter Gefahrstoff Ersatzstoffprüfung: Substitution der Ausgangsstoffe wurde geprüft und ist als nicht möglich einzustufen, da es sich um eine genormte Methode handelt, die auf die speziell vorliegenden Bedingungen und Chemikalien abgestimmt ist. Gefahren: Einatmen / Hautkontakt: Brandgefahr: Explosionsgefahr: Sonstige Gefahren: Ergebnis: Als Schülerversuch möglich nur Lehrerversuch Weitere Maßnahmen: Die konzentrierte Schwefelsäure darf nur von Betreuern zugegeben werden.
Präparat 7: 7,7 Dichlorbicyclo[4.1.0]heptan (Carbenaddition an Olefine)
![Präparat 7: 7,7 Dichlorbicyclo[4.1.0]heptan (Carbenaddition an Olefine) Präparat 7: 7,7 Dichlorbicyclo[4.1.0]heptan (Carbenaddition an Olefine)](/thumbs/97/132036332.jpg) Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2018/19 Präparat 7: 7,7 Dichlorbicyclo[4.1.0]heptan (Carbenaddition an Olefine) Allgemeine Arbeitsvorschrift zur Addition von Dichlorcarbenen
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2018/19 Präparat 7: 7,7 Dichlorbicyclo[4.1.0]heptan (Carbenaddition an Olefine) Allgemeine Arbeitsvorschrift zur Addition von Dichlorcarbenen
Präparat 9: 1 Morpholinocyclopent 1 en (Enamindarstellung)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 9: 1 ocyclopent 1 en (Enamindarstellung) Literatur: H. G. O. Becker et al., Organikum, Wiley-VCH, Weinheim, 23.
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 9: 1 ocyclopent 1 en (Enamindarstellung) Literatur: H. G. O. Becker et al., Organikum, Wiley-VCH, Weinheim, 23.
Anionen-Nachweis durch Fällungsreaktionen
 Lehrer-/Dozentenblatt Anionen-Nachweis durch Fällungsreaktionen (Artikelnr.: P7511300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung
Lehrer-/Dozentenblatt Anionen-Nachweis durch Fällungsreaktionen (Artikelnr.: P7511300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Allgemeine Chemie- Einführung
Zuckernachweis mit Tollens-Reagenz
 Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Präparat 5: D,L Dibrombernsteinsäure (Bromaddition an Olefine)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 5: D,L Dibrombernsteinsäure (addition an Olefine) Darstellung von Literatur: Th. Eicher, L. F. Tietze, Organisch-chemisches
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 5: D,L Dibrombernsteinsäure (addition an Olefine) Darstellung von Literatur: Th. Eicher, L. F. Tietze, Organisch-chemisches
Präparat 2: 3 Dimethylaminomethylindol (Gramin) (Mannich Reaktion)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 2: 3 Dimethylaminomethylindol (Gramin) (Mannich Reaktion) Darstellung von Gramin Literatur: H. G. O. Becker et
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 2: 3 Dimethylaminomethylindol (Gramin) (Mannich Reaktion) Darstellung von Gramin Literatur: H. G. O. Becker et
Präparat 10: Essigsäureisopentylester (Veresterung)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 10: (Veresterung) Literatur: D. R. Palleros, Experimental Organic Chemistry, John Wiley & Sons, Weinheim 2000,
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 10: (Veresterung) Literatur: D. R. Palleros, Experimental Organic Chemistry, John Wiley & Sons, Weinheim 2000,
Präparat 3: Chlorcyclohexan (Radikalische Chlorierung)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 3: (Radikalische Chlorierung) Allgemeine Arbeitsvorschrift für die Chlorierung von Kohlenwasserstoffen mit Sulfurylchlorid
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 3: (Radikalische Chlorierung) Allgemeine Arbeitsvorschrift für die Chlorierung von Kohlenwasserstoffen mit Sulfurylchlorid
Fehlingreaktion verschiedener Zucker. Gefährdungsbeurteilung. Lehrerexperiment. Schülerexperiment
 Fehlingreaktion verschiedener Zucker * Fehling I (Kupfer(II)-sulfat-Lösung) R-Sätze: 22-36/38-50/53 Fehling II (Kaliumnatriumtartrat-Lösung) S-Sätze: 26-36/37/39-45 Kupfer(I)-oxid R-Sätze: 22-50/53 Man
Fehlingreaktion verschiedener Zucker * Fehling I (Kupfer(II)-sulfat-Lösung) R-Sätze: 22-36/38-50/53 Fehling II (Kaliumnatriumtartrat-Lösung) S-Sätze: 26-36/37/39-45 Kupfer(I)-oxid R-Sätze: 22-50/53 Man
Präparat 11: Dibenzylidenaceton (Aldolkondensation)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2016/17 Präparat 11: (Aldolkondensation) Darstellung von Literatur: H. G. O. Becker et al., Organikum, Wiley-VCH, Weinheim, 23.
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2016/17 Präparat 11: (Aldolkondensation) Darstellung von Literatur: H. G. O. Becker et al., Organikum, Wiley-VCH, Weinheim, 23.
Präparat 4: n Butylethylether (Williamsonsche Ethersynthese)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 4: n Butylethylether (Williamsonsche Ethersynthese) Allgemeine Arbeitsvorschrift Arbeitsvorschrift zur Veretherung
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 4: n Butylethylether (Williamsonsche Ethersynthese) Allgemeine Arbeitsvorschrift Arbeitsvorschrift zur Veretherung
Elektrolyse einer Zinkiodidlösung Lehrerversuch, Versuchsvariante Thomas Seilnacht Geräte 2 Kohlelektroden im Stopfen 2 Krokoklemmen
 1 Elektrolyse einer Zinkiodidlösung Lehrerversuch, Versuchsvariante Thomas Seilnacht Geräte 2 Kohlelektroden im Stopfen 2 Krokoklemmen 2 Kabel Stromquelle U-Rohr mit Seitenrohren Stoffe Zinkiodid-Lösung
1 Elektrolyse einer Zinkiodidlösung Lehrerversuch, Versuchsvariante Thomas Seilnacht Geräte 2 Kohlelektroden im Stopfen 2 Krokoklemmen 2 Kabel Stromquelle U-Rohr mit Seitenrohren Stoffe Zinkiodid-Lösung
6.1. Kunststoffmodifizierungen (1) - Herstellung eines Phenolharzschaums. Aufgabe. Wie lassen sich Polymere weiterverarbeiten? (1)
 Naturwissenschaften - Chemie - Polymerchemie - 6 Kunststoffmodifizierungen (P78800) 6.. Kunststoffmodifizierungen () - Herstellung eines Phenolharzschaums Experiment von: Seb Gedruckt: 02.04.204 4:8:0
Naturwissenschaften - Chemie - Polymerchemie - 6 Kunststoffmodifizierungen (P78800) 6.. Kunststoffmodifizierungen () - Herstellung eines Phenolharzschaums Experiment von: Seb Gedruckt: 02.04.204 4:8:0
Präparat 12: Diphenylmethanol (Grignard Reaktion)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2016/17 Präparat 12: (Grignard Reaktion) Allgemeine Arbeitsvorschrift zur Darstellung von Alkoholen über Grignard-Verbindungen
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2016/17 Präparat 12: (Grignard Reaktion) Allgemeine Arbeitsvorschrift zur Darstellung von Alkoholen über Grignard-Verbindungen
Chromatographie von Acetylsalicylsäure. Gefährdungsbeurteilung. Schülerexperiment. Lehrerexperiment
 Chromatographie von Acetylsalicylsäure Brandgefahr! Cyclohexan R-Sätze: 11-38-65-67-50/53 S-Sätze: 9-16-25-33-60-61-62 Acetylsalicylsäure R-Sätze: 22 S-Sätze: 26-37/39-45 Aceton R-Sätze: 11-36-66-67 S-Sätze:
Chromatographie von Acetylsalicylsäure Brandgefahr! Cyclohexan R-Sätze: 11-38-65-67-50/53 S-Sätze: 9-16-25-33-60-61-62 Acetylsalicylsäure R-Sätze: 22 S-Sätze: 26-37/39-45 Aceton R-Sätze: 11-36-66-67 S-Sätze:
Warum werden Alkane "gesättigte" Kohlenwasserstoffe genannt?
 Naturwissenschaften - Chemie - Organische Chemie - 2 Kohlenwasserstoffe (P770900) 2.3 Reaktivität der Alkane Experiment von: Anouch Gedruckt: 20.02.204 08:59:6 intertess (Version 3.2 B24, Export 2000)
Naturwissenschaften - Chemie - Organische Chemie - 2 Kohlenwasserstoffe (P770900) 2.3 Reaktivität der Alkane Experiment von: Anouch Gedruckt: 20.02.204 08:59:6 intertess (Version 3.2 B24, Export 2000)
Risiken der verwendeten Gefahrstoffe und Sicherheitsvorkehrungen. H319 Verursacht schwere Augenreizung. H225 Flüssigkeit und Dampf leicht entzündbar
 Stand 4.04.2012 Krebserzeugende Substanzen Karz. 1A und 1B und erbgutverändernde Substanzen (Mutag. 1A und 1B) werden im Praktikum nicht eingesetzt. Abkürzungen: Mutag.= Mutagen; Karz.=Karzinogen Gesetzliche
Stand 4.04.2012 Krebserzeugende Substanzen Karz. 1A und 1B und erbgutverändernde Substanzen (Mutag. 1A und 1B) werden im Praktikum nicht eingesetzt. Abkürzungen: Mutag.= Mutagen; Karz.=Karzinogen Gesetzliche
Präparat 13: Bis(2 cyanoethyl)malonsäurediethylester (Michael Addition)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 13: Bis(2 cyanoethyl)malonsäurediethylester (Michael Addition) Allgemeine Vorschrift für die Michael-Addition
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2017/18 Präparat 13: Bis(2 cyanoethyl)malonsäurediethylester (Michael Addition) Allgemeine Vorschrift für die Michael-Addition
Dokumentierte Gefährdungsbeurteilung Achtung: Die Beurteilung muss den jeweiligen Bedingungen angepasst werden!
 Dokumentierte Gefährdungsbeurteilung Achtung: Die Beurteilung muss den jeweiligen Bedingungen angepasst werden! 1. Allgemeine Angaben und Vorprüfungen 1 Beurteilung Nr.: Schule: Fach (unterstreichen),
Dokumentierte Gefährdungsbeurteilung Achtung: Die Beurteilung muss den jeweiligen Bedingungen angepasst werden! 1. Allgemeine Angaben und Vorprüfungen 1 Beurteilung Nr.: Schule: Fach (unterstreichen),
S 36/37/39 Bei der Arbeit geeignete Schutzhandschuhe, Schutzkleidung und Schutzbrille/Gesichtsschutz
 Blue-Bottle-Experiment keine! Natriumhydroxid (Ätznatron) R-Sätze: 35 S-Sätze: 26-36/37/39-45 Methylenblau R-Sätze: 22 S-Sätze: keine 0,2 Gramm Methylenblau werden in 100 Milliliter Wasser gelöst. In einem
Blue-Bottle-Experiment keine! Natriumhydroxid (Ätznatron) R-Sätze: 35 S-Sätze: 26-36/37/39-45 Methylenblau R-Sätze: 22 S-Sätze: keine 0,2 Gramm Methylenblau werden in 100 Milliliter Wasser gelöst. In einem
Ergänzende Hinweise Hautkontakt vermeiden! Indikator: Ninhydrinlösung (0,5 Gramm in 100 Milliliter Aceton)
 Aminosäure-Reaktion mit Ninhydrin Brandgefahr! Propan-2-ol R-Sätze: 11-36-67 S-Sätze: 7-16-24/25-26 Butan-1-ol R-Sätze: 10-22-37/38-41-67 S-Sätze: 7/9-13-26-37/39-46 Essigsäure R-Sätze: 10-35 S-Sätze:
Aminosäure-Reaktion mit Ninhydrin Brandgefahr! Propan-2-ol R-Sätze: 11-36-67 S-Sätze: 7-16-24/25-26 Butan-1-ol R-Sätze: 10-22-37/38-41-67 S-Sätze: 7/9-13-26-37/39-46 Essigsäure R-Sätze: 10-35 S-Sätze:
5.3 Glucosenachweis mit Fehlingscher Lösung. Aufgabe. Wie kann Traubenzucker nachgewiesen werden?
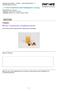 Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P786800) 5.3 Glucosenachweis mit Fehlingscher Lösung Experiment von: Anouch Gedruckt: 28.02.204 :0:4 intertess (Version 3.2 B24, Export
Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P786800) 5.3 Glucosenachweis mit Fehlingscher Lösung Experiment von: Anouch Gedruckt: 28.02.204 :0:4 intertess (Version 3.2 B24, Export
3.2 Salzbildung durch Reaktion von Säuren mit Metalloxiden. Aufgabe. Wie regieren Säuren mit Metalloxiden?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759500) 3.2 Salzbildung durch Reaktion von Säuren mit Metalloxiden Experiment von: Phywe Gedruckt: 5.0.203 2:8:53 intertess (Version 3.06
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759500) 3.2 Salzbildung durch Reaktion von Säuren mit Metalloxiden Experiment von: Phywe Gedruckt: 5.0.203 2:8:53 intertess (Version 3.06
Ligandenaustausch am Chrom(III)-ion. Gefährdungsbeurteilung. Lehrerexperiment. Schülerexperiment
 Ligandenaustausch am Chrom(III)-ion keine! Chrom(III)-chlorid-Lösung (0,1 mol/l) R-Sätze: 22 S-Sätze: 24-25 Ammoniak-Lösung (20%ig) Eine Chrom(III)-chloridlösung wird im Reagenzglas tropfenweise bis zur
Ligandenaustausch am Chrom(III)-ion keine! Chrom(III)-chlorid-Lösung (0,1 mol/l) R-Sätze: 22 S-Sätze: 24-25 Ammoniak-Lösung (20%ig) Eine Chrom(III)-chloridlösung wird im Reagenzglas tropfenweise bis zur
GHS-Einstufung und Kennzeichnung der verwendeten Gefahrstoffe
 Lernen durch Lehren im Fachgebiet Chemie GHS-Einstufung und Kennzeichnung der verwendeten Gefahrstoffe (Quellen: http://gestis.itrust.de/nxt/gateway.dll/gestis_de/000000.xml?f=templates$fn=default.htm$3.0,
Lernen durch Lehren im Fachgebiet Chemie GHS-Einstufung und Kennzeichnung der verwendeten Gefahrstoffe (Quellen: http://gestis.itrust.de/nxt/gateway.dll/gestis_de/000000.xml?f=templates$fn=default.htm$3.0,
Untersuche einige Reaktionen von konzentrierter Schwefelsäure auf ihre Gefährlichkeit.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75700).2 Gefährlichkeiten von konzentrierter Schwefelsäure Experiment von: Phywe Gedruckt: 5.0.203 :8:09 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75700).2 Gefährlichkeiten von konzentrierter Schwefelsäure Experiment von: Phywe Gedruckt: 5.0.203 :8:09 intertess (Version 3.06 B200, Export
Säurestärke (Artikelnr.: P )
 Lehrer-/Dozentenblatt Säurestärke (Artikelnr.: P7157600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren und Basen, Protonenübergänge
Lehrer-/Dozentenblatt Säurestärke (Artikelnr.: P7157600) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren und Basen, Protonenübergänge
1.7 Säurestärke. Aufgabe. Gibt es verschieden starke Säuren? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157600) 1.7 Säurestärke Experiment von: Phywe Gedruckt: 15.10.2013 11:41:12 intertess (Version 13.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157600) 1.7 Säurestärke Experiment von: Phywe Gedruckt: 15.10.2013 11:41:12 intertess (Version 13.06 B200, Export 2000) Aufgabe Aufgabe
Präparat 8: Caprolactam (Beckmann Umlagerung)
 Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2016/17 Präparat 8: Caprolactam (Beckmann Umlagerung) Darstellung von -Caprolactam Literatur: H. G. O. Becker et al., Organikum,
Institut für Organische Chemie Grundpraktikum Organische Chemie (OC1P) WS 2016/17 Präparat 8: Caprolactam (Beckmann Umlagerung) Darstellung von -Caprolactam Literatur: H. G. O. Becker et al., Organikum,
3.7 Osmose - Chemischer Garten. Aufgabe. Wie lösen sich Salze in Wasserglas? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P760000) 3.7 Osmose - Chemischer Garten Experiment von: Phywe Gedruckt: 5.0.203 2:25:55 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P760000) 3.7 Osmose - Chemischer Garten Experiment von: Phywe Gedruckt: 5.0.203 2:25:55 intertess (Version 3.06 B200, Export 2000) Aufgabe
Dichlormethan, CH2Cl2
 Betriebsanweisung über den Umgang mit Gefahrstoffen in Verbindung mit der Laborordnung des Instituts für Chemie und Biochemie Freie Universität Berlin Arbeitsplatz: U209-214, F201/203, U 412 FB BioChemPharm,
Betriebsanweisung über den Umgang mit Gefahrstoffen in Verbindung mit der Laborordnung des Instituts für Chemie und Biochemie Freie Universität Berlin Arbeitsplatz: U209-214, F201/203, U 412 FB BioChemPharm,
Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P )
 Lehrer-/Dozentenblatt Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P757000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Allgemeine Vorsichtsmaßnahmen beim Umgang mit Säuren (Artikelnr.: P757000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie
5.4. Polykondensation (2) - Nylonherstellung. Aufgabe. Wie wird Nylon hergestellt?
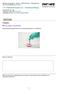 Naturwissenschaften - Chemie - Polymerchemie - 5 Mechanismus der Kunststoffbildung (P78300) 5.4. Polykondensation (2) - Nylonherstellung Experiment von: Seb Gedruckt: 02.04.204 3:37:22 intertess (Version
Naturwissenschaften - Chemie - Polymerchemie - 5 Mechanismus der Kunststoffbildung (P78300) 5.4. Polykondensation (2) - Nylonherstellung Experiment von: Seb Gedruckt: 02.04.204 3:37:22 intertess (Version
Liste der H-Statements (H = Hazard)
 Liste der H-Statements (H = Hazard) H-Statements sind weltweit gültig, EUH-Statements sind nur in der EU vorgeschrieben H200 Instabil, explosiv. H201 Explosiv, Gefahr der Massenexplosion. H202 Explosiv;
Liste der H-Statements (H = Hazard) H-Statements sind weltweit gültig, EUH-Statements sind nur in der EU vorgeschrieben H200 Instabil, explosiv. H201 Explosiv, Gefahr der Massenexplosion. H202 Explosiv;
2.1 Abbau natürlich vorkommender Polymere (2) - Stärkeabbau. Aufgaben. Aus welchen Bestandteilen setzt sich Stärke zusammen?
 Naturwissenschaften - Chemie - Polymerchemie - 2 Natürliche Polymere (P780200) 2. Abbau natürlich vorkommender Polymere (2) - Stärkeabbau Experiment von: Seb Gedruckt: 24.03.204 3:43:24 intertess (Version
Naturwissenschaften - Chemie - Polymerchemie - 2 Natürliche Polymere (P780200) 2. Abbau natürlich vorkommender Polymere (2) - Stärkeabbau Experiment von: Seb Gedruckt: 24.03.204 3:43:24 intertess (Version
Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt-Reaktion) (Artikelnr.: P )
 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt-Reaktion) (Artikelnr.: P1149300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische
Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration (Landolt-Reaktion) (Artikelnr.: P1149300) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Physikalische
5.2 Schiffsche und Fehlingsche Probe. Aufgabe. Wie lassen sich Alkanale von Alkanolen unterscheiden?
 Naturwissenschaften - Chemie - Organische Chemie - 5 Carbonylverbindungen (P772400) 5.2 Schiffsche und Fehlingsche Probe Experiment von: Anouch Gedruckt: 25.02.204 4:00:42 intertess (Version 3.2 B24, Export
Naturwissenschaften - Chemie - Organische Chemie - 5 Carbonylverbindungen (P772400) 5.2 Schiffsche und Fehlingsche Probe Experiment von: Anouch Gedruckt: 25.02.204 4:00:42 intertess (Version 3.2 B24, Export
Salzbildung durch Reaktion von Säuren mit Laugen
 Lehrer-/Dozentenblatt Salzbildung durch Reaktion von Säuren mit Laugen (Artikelnr.: P7159400) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie
Lehrer-/Dozentenblatt Salzbildung durch Reaktion von Säuren mit Laugen (Artikelnr.: P7159400) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie
Kennzeichnung von Gefahrstoffen nach Chemikalienrecht (Stand: Januar 2005)
 Kennzeichnung von Gefahrstoffen nach Chemikalienrecht (Stand: Januar 2005) 1. Gefahrensymbole und bezeichnungen für gefährliche Stoffe und Zubereitungen (Richtlinie 67/548/EWG Anhang II) 2. Hinweise auf
Kennzeichnung von Gefahrstoffen nach Chemikalienrecht (Stand: Januar 2005) 1. Gefahrensymbole und bezeichnungen für gefährliche Stoffe und Zubereitungen (Richtlinie 67/548/EWG Anhang II) 2. Hinweise auf
Schulversuchspraktikum. Dennis Roggenkämper. Sommersemester Klassenstufen 11 & 12. Kohlenhydrate. Kurzprotokoll
 Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 11 & 12 Kohlenhydrate Kurzprotokoll Auf einen Blick: Das Kurzprotokoll umfasst vier Lehrer- und zwei Schülerexperimente, die
Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 11 & 12 Kohlenhydrate Kurzprotokoll Auf einen Blick: Das Kurzprotokoll umfasst vier Lehrer- und zwei Schülerexperimente, die
Modul 3 Schülergerechtes Experimentieren
 Modul 3 Schülergerechtes Experimentieren Unterrichtseckentwurf - Gefährdungsbeurteilung Fachdidaktik Chemie WS 2016/17 Studiengang: Bachelor of Education Apl. Prof. Dr. G. Hornung, A. Molitor-Schworm,
Modul 3 Schülergerechtes Experimentieren Unterrichtseckentwurf - Gefährdungsbeurteilung Fachdidaktik Chemie WS 2016/17 Studiengang: Bachelor of Education Apl. Prof. Dr. G. Hornung, A. Molitor-Schworm,
Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P7510200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Lehrer-/Dozentenblatt Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren (Artikelnr.: P7510200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema:
Weise nach, dass Stärke durch das im Speichel enthaltene Verdauungsenzym Ptyalin zu Malzzucker abgebaut wird.
 Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P787700) 5.2 Stärkespaltung bei der Verdauung Experiment von: Anouch Gedruckt: 28.02.204 :2:07 intertess (Version 3.2 B24, Export 2000)
Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P787700) 5.2 Stärkespaltung bei der Verdauung Experiment von: Anouch Gedruckt: 28.02.204 :2:07 intertess (Version 3.2 B24, Export 2000)
Versuchsbezogene Betriebsanweisung nach 14 GefStoffV & Versuchsauswertung
 Versuchsbezogene Betriebsanweisung nach 14 GefStoffV & Versuchsauswertung für chemische Laboratorien der Universität Heidelberg - Organisches Praktikum (Modul OC_B2) - Name: Mustermann Vorname: Max Datum:
Versuchsbezogene Betriebsanweisung nach 14 GefStoffV & Versuchsauswertung für chemische Laboratorien der Universität Heidelberg - Organisches Praktikum (Modul OC_B2) - Name: Mustermann Vorname: Max Datum:
Ergänzende Hinweise Feste Reaktionsprodukte nicht in den Ausguß schütten! Vorsicht; es entsteht Knallgas!
 Dehydrierung von ** Wassergefährdend! Kupferoxid R-Sätze: 22-50/53 S-Sätze: 22-61 Wasserstoff R-Sätze: 12 S-Sätze: 9-16-33 wird in einem Rundkolben erhitzt. Die Dämpfe werden über erhitzte Kupferspäne
Dehydrierung von ** Wassergefährdend! Kupferoxid R-Sätze: 22-50/53 S-Sätze: 22-61 Wasserstoff R-Sätze: 12 S-Sätze: 9-16-33 wird in einem Rundkolben erhitzt. Die Dämpfe werden über erhitzte Kupferspäne
(±)-4-Methyl-3- heptanon
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
3.5 Hydrolyse von Salzen. Aufgabe. Reagieren wässrige Salzlösungen neutral? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Die Reduktion von Kupfer(II)-oxid Entwicklung und Bearbeitung Thomas Seilnacht
 1 Die Reduktion von Kupfer(II)-oxid Entwicklung und Bearbeitung Thomas Seilnacht Geräte: Reagenzglas mit Seitenrohr, RG-Gestell mit 6 RG s, RG-Halter, Stativ, Brenner, Stopfen, Stopfen mit Bohrung, Tiegelzange,
1 Die Reduktion von Kupfer(II)-oxid Entwicklung und Bearbeitung Thomas Seilnacht Geräte: Reagenzglas mit Seitenrohr, RG-Gestell mit 6 RG s, RG-Halter, Stativ, Brenner, Stopfen, Stopfen mit Bohrung, Tiegelzange,
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung
 V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
V 2 Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration und der Temperatur bei der Reaktion von Kaliumpermanganat mit Oxalsäure in Lösung Bei diesem Versuch geht es darum, die Geschwindigkeit
Hochentzündliche und leichtentzündliche Gefahrstoffe
 Gruppe A Hochentzündliche und leichtentzündliche Gefahrstoffe F+/F hochentzündlich leichtentzündlich Die Gefahrstoffe der Gruppe A enthalten organische Lösemittel, die mit Luft explosionsfähige Gemische
Gruppe A Hochentzündliche und leichtentzündliche Gefahrstoffe F+/F hochentzündlich leichtentzündlich Die Gefahrstoffe der Gruppe A enthalten organische Lösemittel, die mit Luft explosionsfähige Gemische
Wirkung von Säuren auf Metalle (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wirkung von Säuren auf Metalle (Artikelnr.: P7157500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren
Lehrer-/Dozentenblatt Wirkung von Säuren auf Metalle (Artikelnr.: P7157500) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-10 Lehrplanthema: Anorganische Chemie Unterthema: Säuren
Untersuche die Wirkung verschiedener Säuren und Laugen auf natürliche und industriell hergestellte Indikatoren.
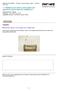 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157400) 1.5 Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:37:56
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157400) 1.5 Wirkung von Säuren und Laugen auf natürliche und technische Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:37:56
Sicherheitshinweise (P)
 Sicherheitshinweise (P) P101 P102 P103 P201 P202 P210 P211 P220 P221 P222 P223 P230 P231 P232 P233 P234 P235 P240 P241 P242 Ist ärztlicher Rat erforderlich, Verpackung oder Kennzeichnungsetikett bereithalten.
Sicherheitshinweise (P) P101 P102 P103 P201 P202 P210 P211 P220 P221 P222 P223 P230 P231 P232 P233 P234 P235 P240 P241 P242 Ist ärztlicher Rat erforderlich, Verpackung oder Kennzeichnungsetikett bereithalten.
Schulversuchspraktikum. Jans Manjali. Sommersemester Klassenstufen 9 & 10. Titration. Kurzprotokoll
 Schulversuchspraktikum Jans Manjali Sommersemester 2015 Klassenstufen 9 & 10 Titration Kurzprotokoll Auf einen Blick: Die hier vorgestellte Argentometrie ist eine Fällungstitration, bei der Silberionen
Schulversuchspraktikum Jans Manjali Sommersemester 2015 Klassenstufen 9 & 10 Titration Kurzprotokoll Auf einen Blick: Die hier vorgestellte Argentometrie ist eine Fällungstitration, bei der Silberionen
7.1 Ester der Essigsäure. Aufgabe. Wie reagieren Alkansäuren mit Alkoholen? Naturwissenschaften - Chemie - Organische Chemie - 7 Ester
 Naturwissenschaften - Chemie - Organische Chemie - 7 Ester (P773000) 7. Ester der Essigsäure Experiment von: Anouch Gedruckt: 25.02.204 4:20:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 7 Ester (P773000) 7. Ester der Essigsäure Experiment von: Anouch Gedruckt: 25.02.204 4:20:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Kohlenhydrat-Analytik
 Kohlenhydrat-Analytik Kohlenhydrate sind in ihrem strukturellen Aufbau sehr ähnlich. Eine spezifische Bestimmung wird dadurch erschwert. Ein gruppenweises Unterscheiden mit verschiedenen einfachen Nachweisreaktionen
Kohlenhydrat-Analytik Kohlenhydrate sind in ihrem strukturellen Aufbau sehr ähnlich. Eine spezifische Bestimmung wird dadurch erschwert. Ein gruppenweises Unterscheiden mit verschiedenen einfachen Nachweisreaktionen
8.1 Ammonium in Lakritz. Aufgabe. Warum schmecken Lakritze scharf? Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P )
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788200) 8. Ammonium in Lakritz Experiment von: Anouch Gedruckt: 28.02.204 :5:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788200) 8. Ammonium in Lakritz Experiment von: Anouch Gedruckt: 28.02.204 :5:33 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Ch 15/02 K_Online-Ergänzung
 Ch 15/02 K_Online-Ergänzung S. I S. I + II S. II CHEMIE MARTIN HOLFELD Online-Ergänzung 1 Gefährdungsbeurteilung Rot-Grün-Gelb-Ampel aufgerufen: 07.11.2015 Vorgang: Oszillierende Redoxreaktion mit Indigocarmin
Ch 15/02 K_Online-Ergänzung S. I S. I + II S. II CHEMIE MARTIN HOLFELD Online-Ergänzung 1 Gefährdungsbeurteilung Rot-Grün-Gelb-Ampel aufgerufen: 07.11.2015 Vorgang: Oszillierende Redoxreaktion mit Indigocarmin
Gefahren (R-Sätze) - Sicherheitsratschläge (S-Sätze)
 Gefahren (R-Sätze) - Sicherheitsratschläge (S-Sätze) R-Satz Hinweise auf besondere Gefahren R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R 19 R 20 R 21 R 22 R 23 R 24 R 25
Gefahren (R-Sätze) - Sicherheitsratschläge (S-Sätze) R-Satz Hinweise auf besondere Gefahren R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R 19 R 20 R 21 R 22 R 23 R 24 R 25
Stelle Salzlösungen her und überprüfe die Vorgänge beim Mischen der Lösungen.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P7159700) 3.4 Salzbildung durch Fällungsreaktion Experiment von: Phywe Gedruckt: 15.10.2013 12:20:35 intertess (Version 13.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P7159700) 3.4 Salzbildung durch Fällungsreaktion Experiment von: Phywe Gedruckt: 15.10.2013 12:20:35 intertess (Version 13.06 B200, Export
LISTE DER SICHERHEITSHINWEISE
 Verordnung (EG) Nr. 1272/2008 über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen (CLP-Verordnung) ANHANG IV LISTE DER SICHERHEITSHINWEISE P-Sätze (Precautionary statements) Sicherheitshinweise
Verordnung (EG) Nr. 1272/2008 über die Einstufung, Kennzeichnung und Verpackung von Stoffen und Gemischen (CLP-Verordnung) ANHANG IV LISTE DER SICHERHEITSHINWEISE P-Sätze (Precautionary statements) Sicherheitshinweise
Ergänzende Hinweise Nicht zu lange und intensiv spülen! Nur Glasgefäße zum Färben verwenden! Hautkontakt vermeiden!
 Beizenfärbung mit Alizarin * Eisen(III)-chlorid R-Sätze: 22-38-41 S-Sätze: 26-39 Kaliumchrom(III)-sulfat) Natronlauge (verdünnt) R-Sätze: 36/38 S-Sätze: 26-36/37/39-45 Eine Spatelspitze Eisen(III)-chlorid,
Beizenfärbung mit Alizarin * Eisen(III)-chlorid R-Sätze: 22-38-41 S-Sätze: 26-39 Kaliumchrom(III)-sulfat) Natronlauge (verdünnt) R-Sätze: 36/38 S-Sätze: 26-36/37/39-45 Eine Spatelspitze Eisen(III)-chlorid,
Quelle: Verordnung vom 18. Mai 2005 über den Schutz vor gefährlichen Stoffen und Zubereitungen (Chemikalienverordnung, ChemV, SR 813.
 Quelle: Verordnung vom 18. Mai 2005 über den Schutz vor gefährlichen Stoffen und Zubereitungen (Chemikalienverordnung, ChemV, SR 813.11) Anhang 1 1 (Art. 39 Abs. 1, 40, 46, 47 Abs. 2, 100 Abs. 2 Bst. c)
Quelle: Verordnung vom 18. Mai 2005 über den Schutz vor gefährlichen Stoffen und Zubereitungen (Chemikalienverordnung, ChemV, SR 813.11) Anhang 1 1 (Art. 39 Abs. 1, 40, 46, 47 Abs. 2, 100 Abs. 2 Bst. c)
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
R- und S-Sa tze in deutscher Sprache
 R- und S-Sa tze in deutscher Sprache R-Sätze R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R 19 R 20 R 21 R 22 R 23 R 24 R 25 R 26 R 27 R 28 In trockenem Zustand explosionsgefährlich.
R- und S-Sa tze in deutscher Sprache R-Sätze R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R 19 R 20 R 21 R 22 R 23 R 24 R 25 R 26 R 27 R 28 In trockenem Zustand explosionsgefährlich.
Bezeichnungen der besonderen Gefahren bei gefährlichen Stoffen und Zubereitungen (R-Sätze) Jeden Tag mit ins Labor bringen!
 Bezeichnungen der besonderen Gefahren bei gefährlichen Stoffen und Zubereitungen (R-Sätze) Jeden Tag mit ins Labor bringen! R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R
Bezeichnungen der besonderen Gefahren bei gefährlichen Stoffen und Zubereitungen (R-Sätze) Jeden Tag mit ins Labor bringen! R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R
A.6 Auflistung der R- und S-Sätze
 A.6 Auflistung der R- und S-Sätze Auflistung der R- und S-Sätze nach der EG-Richtlinie 67/548/EWG, Anhang III bzw. IV, zuletzt geändert durch die 28. Anpassungsrichtlinie 2001/59/EG. R-Sätze R 1: In trockenem
A.6 Auflistung der R- und S-Sätze Auflistung der R- und S-Sätze nach der EG-Richtlinie 67/548/EWG, Anhang III bzw. IV, zuletzt geändert durch die 28. Anpassungsrichtlinie 2001/59/EG. R-Sätze R 1: In trockenem
Sicherheitshinweise P-Sätze (früher S-Sätze)
 Sicherheitshinweise P-Sätze (früher S-Sätze) Kodierung der S-Sätze: 1. Sicherheitshinweise Allgemein P101: Ist ärztlicher Rat erforderlich, Verpackung oder Kennzeichnungsetikett bereithalten. P102: Darf
Sicherheitshinweise P-Sätze (früher S-Sätze) Kodierung der S-Sätze: 1. Sicherheitshinweise Allgemein P101: Ist ärztlicher Rat erforderlich, Verpackung oder Kennzeichnungsetikett bereithalten. P102: Darf
Welche Vorsichtsmaßnahmen sind beim Umgang mit Laugen zu beachten?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7158600) 2.1 Vorsichtsmaßnahmen beim Umgang mit Laugen Experiment von: Phywe Gedruckt: 15.10.2013 11:54:37 intertess (Version 13.06 B200,
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7158600) 2.1 Vorsichtsmaßnahmen beim Umgang mit Laugen Experiment von: Phywe Gedruckt: 15.10.2013 11:54:37 intertess (Version 13.06 B200,
Liste der R- und S-Sätze
 Liste der R- und S-Sätze R-Sätze: Liste der Hinweise auf die besonderen Gefahren (R-Sätze): R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R 19 R 20 R 21 R 22 R 23 R 24 R 25
Liste der R- und S-Sätze R-Sätze: Liste der Hinweise auf die besonderen Gefahren (R-Sätze): R 1 R 2 R 3 R 4 R 5 R 6 R 7 R 8 R 9 R 10 R 11 R 12 R 14 R 15 R 16 R 17 R 18 R 19 R 20 R 21 R 22 R 23 R 24 R 25
Untersuche die Wirkung von verschiedenen Säuren auf Gemüse- und Blütenfarbstoffe.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157300) 1.4 Die Wirkung von Säuren auf Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:36:51 intertess (Version 13.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 1 Säuren (P7157300) 1.4 Die Wirkung von Säuren auf Indikatoren Experiment von: Phywe Gedruckt: 15.10.2013 11:36:51 intertess (Version 13.06 B200, Export
Explosiv; Gefahr durch Feuer, Luftdruck oder Splitter, Spreng- und Wurfstücke.
 http://www.msds-europe.com H200 Instabil, explosiv. H201 Explosiv, Gefahr der Massenexplosion. H202 Explosiv; große Gefahr durch Splitter, Spreng- und Wurfstücke. H203 Explosiv; Gefahr durch Feuer, Luftdruck
http://www.msds-europe.com H200 Instabil, explosiv. H201 Explosiv, Gefahr der Massenexplosion. H202 Explosiv; große Gefahr durch Splitter, Spreng- und Wurfstücke. H203 Explosiv; Gefahr durch Feuer, Luftdruck
Bringe Natronlauge mit Salzsäure zur Reaktion und untersuche das Reaktionsprodukt.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759400) 3. Salzbildung durch Reaktion von Säuren mit Laugen Experiment von: Phywe Gedruckt: 5.0.203 2:8:03 intertess (Version 3.06 B200,
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759400) 3. Salzbildung durch Reaktion von Säuren mit Laugen Experiment von: Phywe Gedruckt: 5.0.203 2:8:03 intertess (Version 3.06 B200,
5.6 Milchzucker. Aufgabe. Wie kann Milchzucker gewonnen werden? Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P )
 Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P78700) 5.6 Milchzucker Experiment von: Anouch Gedruckt: 28.02.204 :04:46 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie
Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P78700) 5.6 Milchzucker Experiment von: Anouch Gedruckt: 28.02.204 :04:46 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie
Nachweis von Methanol (Artikelnr.: P )
 Lehrer-/Dozentenblatt Nachweis von Methanol (Artikelnr.: P7186200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Organische Chemie Unterthema: Lebensmittelchemie:
Lehrer-/Dozentenblatt Nachweis von Methanol (Artikelnr.: P7186200) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 10-13 Lehrplanthema: Organische Chemie Unterthema: Lebensmittelchemie:
Wie lassen sich die Eigenschaften des Kohlenstoffdioxids nutzen?
 Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P754000) 2.8 Modell eines Feuerlöschers Experiment von: Seb Gedruckt: 24.03.204 :0:45 intertess (Version 3.2 B24, Export 2000)
Naturwissenschaften - Chemie - Anorganische Chemie - 2 Luft und andere Gase (P754000) 2.8 Modell eines Feuerlöschers Experiment von: Seb Gedruckt: 24.03.204 :0:45 intertess (Version 3.2 B24, Export 2000)
Welche Elemente außer Kohlenstoff und Wasserstoff können in Polymeren enthalten sein?
 Naturwissenschaften - Chemie - Polymerchemie - Der Polymerbegriff (P78000).2 Polymerbestandteile (2) - Nachweis von Polymerbestandteilen - Beilsteinprobe Experiment von: Seb Gedruckt: 24.03.204 3:09:20
Naturwissenschaften - Chemie - Polymerchemie - Der Polymerbegriff (P78000).2 Polymerbestandteile (2) - Nachweis von Polymerbestandteilen - Beilsteinprobe Experiment von: Seb Gedruckt: 24.03.204 3:09:20
1.14 Darstellung und Eigenschaften von Kohlensäure. Aufgabe. Welche Eigenschaften besitzt Kohlensäure?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758300).4 Darstellung und Eigenschaften von Kohlensäure Experiment von: Phywe Gedruckt: 5.0.203 :5:22 intertess (Version 3.06 B200, Export
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758300).4 Darstellung und Eigenschaften von Kohlensäure Experiment von: Phywe Gedruckt: 5.0.203 :5:22 intertess (Version 3.06 B200, Export
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Ergänzende Hinweise Im Abzug arbeiten! Mit einem angefeuchteten Indikatorpapier überprüfen.
 Reaktion von Brom mit Alkanen ** Brom R-Sätze: 26-35-50 S-Sätze: 7/9-26-45-61 Heptan Pentan R-Sätze: 12-51/53-65-66-67 S-Sätze: 9-16-29-33-61-62 Mehrere Milliliter Bromlösung (wenige Tropfen Brom in Heptan
Reaktion von Brom mit Alkanen ** Brom R-Sätze: 26-35-50 S-Sätze: 7/9-26-45-61 Heptan Pentan R-Sätze: 12-51/53-65-66-67 S-Sätze: 9-16-29-33-61-62 Mehrere Milliliter Bromlösung (wenige Tropfen Brom in Heptan
MODUL 3A SCHÜLERGERECHTES EXPERIMENTIEREN
 MODUL 3A SCHÜLERGERECHTES EXPERIMENTIEREN Fachdidaktik Chemie WS 14/15 Fachbereich Chemie Studiengang: Bachelor of Education TU Kaiserslautern Dozententeam: apl. Prof. Dr. G. Hornung, A. Molitor -Schworm
MODUL 3A SCHÜLERGERECHTES EXPERIMENTIEREN Fachdidaktik Chemie WS 14/15 Fachbereich Chemie Studiengang: Bachelor of Education TU Kaiserslautern Dozententeam: apl. Prof. Dr. G. Hornung, A. Molitor -Schworm
Alte Gefahren neue Zeichen
 Alte Gefahren neue Zeichen Partieführerschulung 2011 1 GHS System GHS Globally Harmonized System Angleichung von Einstufungskriterien Global einheitliches System zur Gefahrenkennzeichnung Partieführerschulung
Alte Gefahren neue Zeichen Partieführerschulung 2011 1 GHS System GHS Globally Harmonized System Angleichung von Einstufungskriterien Global einheitliches System zur Gefahrenkennzeichnung Partieführerschulung
Herstellung und Eigenschaften von Natronlauge
 Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Natronlauge (Artikelnr.: P759000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie Unterthema:
Lehrer-/Dozentenblatt Herstellung und Eigenschaften von Natronlauge (Artikelnr.: P759000) Curriculare Themenzuordnung Fachgebiet: Chemie Bildungsstufe: Klasse 7-0 Lehrplanthema: Anorganische Chemie Unterthema:
Gefahrensymbole und Gefahrgüter
 eqiooki.de Gefahrensymbole Seite 1 von 6 Gefahrensymbole und Gefahrgüter Gefahrensymbole alt Nur noch bis 31.05.2015 zulässig. C ätzend E explosiv F oder F+ leicht-/hochentzündlich N umweltgefährdend T
eqiooki.de Gefahrensymbole Seite 1 von 6 Gefahrensymbole und Gefahrgüter Gefahrensymbole alt Nur noch bis 31.05.2015 zulässig. C ätzend E explosiv F oder F+ leicht-/hochentzündlich N umweltgefährdend T
How To Determine The
 ZÜRCHER HCHSCHULE FÜR ANGEWANDTE WISSENSCHAFTEN DEPARTEMENT LIFE SCIENCES UND FACILITY MANAGEMENT INSTITUT FÜR CHEMIE UND BILGISCHE CHEMIE (ICBC) WÄDENSWIL Aufschluss von Legierungen Messing von Remo Badertscher
ZÜRCHER HCHSCHULE FÜR ANGEWANDTE WISSENSCHAFTEN DEPARTEMENT LIFE SCIENCES UND FACILITY MANAGEMENT INSTITUT FÜR CHEMIE UND BILGISCHE CHEMIE (ICBC) WÄDENSWIL Aufschluss von Legierungen Messing von Remo Badertscher
Gefährdungsbeurteilung
 Lotuseffekt - hydrophobe CD-Oberfläche durch Aceton Ausgangssituation für den Versuch 11180 Schülerversuch hrgangsstufe: Kein hrgangsbezug Versuchsbeschreibung Die Lernausgangslage wurde berücksichtigt:
Lotuseffekt - hydrophobe CD-Oberfläche durch Aceton Ausgangssituation für den Versuch 11180 Schülerversuch hrgangsstufe: Kein hrgangsbezug Versuchsbeschreibung Die Lernausgangslage wurde berücksichtigt:
Vergleich der Kennzeichnungen: RL 67/548/EWG VO EG/1272/2008 geordnet nach R-Sätzen
 Vergleich der Kennzeichnungen: RL 67/548/EWG VO EG/1272/2008 geordnet nach R-Sätzen brauner Text: blauer Text: grauer Text: violetter Text: H-Satz: EUnnn: RL 67/548/EWG VO EG/1272/2008 noch nicht in VO
Vergleich der Kennzeichnungen: RL 67/548/EWG VO EG/1272/2008 geordnet nach R-Sätzen brauner Text: blauer Text: grauer Text: violetter Text: H-Satz: EUnnn: RL 67/548/EWG VO EG/1272/2008 noch nicht in VO
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
5.5 Fructose. Aufgabe. Wie unterscheiden sich Fructose und Glucose? Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P )
 Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P787000) 5.5 Fructose Experiment von: Anouch Gedruckt: 28.02.204 :04:06 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie
Naturwissenschaften - Chemie - Lebensmittelchemie - 5 Kohlenhydrate (P787000) 5.5 Fructose Experiment von: Anouch Gedruckt: 28.02.204 :04:06 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe Wie
