Archiv der Pharmazie
|
|
|
- Rainer Walter
- vor 6 Jahren
- Abrufe
Transkript
1 Sonderdruck aus Archiv der Pharmazie 314. Band, Heft 6, Seite Verlag Chemie GmbH, Weinheim (Bergstr.) Ortho-Effekte in l-(o-aminomethylaryl)-buten(l)-3-onen und ihren Hydrierungsprodukten, 1. Mitt. o-aminomethyl-naphthalacetone Klaus K. Mayer, Theodor Poettinger und Wolf gang Wiegrebe* ) ** )
2
3 Archiv der Pharmazie 314. Band Juni 1981 Heft 6 Arch. Pharm. (Weinheim) 314, (1981) Ortho-Effekte in l-(o-aminomethylaryl)-buten(l)-3-onen und ihren Hydrierungsprodukten, 1. Mitt. o-aminomethyl-naphthalacetone Klaus K. Mayer, Theodor Poettinger und Wolfgang Wiegrebe*)**) Falkultät für Chemie und Pharmazie der Universität Regensburg, Postfach Regensburg Eingegangen am 21. August 1980 Die Herstellung der Verbindungen 3 bis 21 wird beschrieben. Ortho Effects in l-[(o-aminomethyi)aryl]-l-buten-3-ones and their Hydrogenation Products, I: o-(aminomethyl)naphthalacetones Synthetic procedures leading to compounds 3 to 21 are described. Bei ms-untersuchungen des von Faber l) aus Cynanchum vincetoxicum isolierten Vincetens (la) beobachtete Budzikiewicz 2) einen Verlust von^ogjhs (m/z 308; 99 % r.i.) und beim Dihydro-Vinceten (lb) die Abspaltung der gesamten Seitenkette (C 4 H 9 0 ; m/z 282; 55 % r.i.). Wir untersuchten daraufhin das Fragmentierungsverhalten von Naphthalinen mit C 4 -Seitenketten und stellten fest, daß diese Naphthalin-Derivate aus den Molekülionen C 4 -Bruchstücke abspalten, es sei denn, die Seitenkette ist ungesättigt mit Konjugation zum Ring 3). Durch Untersuchung komplizierter aufgebauter Modellsubstanzen mit basischer o-ständiger Seitenkette und D-Markierungen in der basischen und der Butyl-Seitenkette sollte der Mechanismus dieser ms-reaktionen geklärt werden. Im folgenden werden die Synthesen der Verbindungen 3 bis 21 beschrieben (Abb. 1). 2,3-Dimethoxy-6-methyl-naphthalin (2) 3) wurde nach Friedel-Crafts zu 3 umgesetzt. Das ^H-NMR-Spektrum beweist das Substitutionsmuster (4 aromat. Protonen als Singuletts). Vilsmeier-Formylierung von 2 führte nicht zu 4, sondern lt. GC zum 2 : **) Herrn Prof. Dr. Ing. H. Hartmann, Braunschweig, zum 85. Geburtstag in Dankbarkeit gewidmet /81/ $ 02.50/0 Verlag Chemie GmbH, Weinheim 1981
4 1-Gemisch aus zwei monoformylierten Verbindungen, das nicht weiter untersucht wurde, da 4 in größerer Menge für die Weiterverarbeitung gebraucht worden wäre. - Zum Aufbau der Butylseitenkette wurde 3 mit n-butyl-li und Acetaldehyd umgesetzt. Das Reaktionsgemisch enthielt u. a. folgende Produkte: durch nucleophilen Angriff des Butylanions entsteht der tert. Alkohol 5; als 1 : 1-Additionsprodukt bildet sich der gewünschte sek. Alkohol 6, durch 1+2-Reaktion das Additionsprodukt 7. C H 3 rt C H 3 0 ^ ^AR" J R' R" R' R" 12: CH2Br C0-0CH3 2: CH3 H 13: C0-CH3 3*. C0-CH3 14: CH2N(Et)2 C0-0CH3 (4:» CH=0) 15: CH20H 5:» C(OH)CH3-nC4Hg 16: CH=0 6: C0-CH2-CH(0H)-CH3 (17: - CH 2-0- CO-) 7: C0-CH[CH(0H)-CH3]2 18: CH2N(Et) CH(OH)-CH2-CO-CH3 8: CO-CH2-CH(0-Ac)-CH3 19: CH=CH-C0-CH3 9: COOH 20: CH = CH-CH(OH)-CH3 10: C0-0CH3 20a: ' CH=CH-CD(OH)-CH3 11: C0-0C2H5 21: CH3 CH2-CH2-CH(OH)-CH3 Abgesehen von (M + -C 3 H 6 0; 35 % r.i.) entstehen alle Fragmente bei 5, 6 und 7 durch einfachen Bindungsbruch und sind im Einklang mit den angegebenen Strukturen (s. Exp. Teil). Die erwähnte Aceton-Abspaltung kann durch eine vorgelagerte Redox-Reaktion zur l-hydroxy-butanon(3)-partialstruktur erklärt werden. - 6 läßt sich zu 8 acetylieren, das sich allerdings mit NBS nicht an der aromat. Methylgruppe bromieren läßt. Auch die Borhydrid-Reduktion mit anschließender Wasserabspaltung zum Allylalkohol gelingt nicht im präparativen Maßstab: in beiden Fällen entstehen komplexe Gemische. Durch Hypobromit-Spaltung 4) von 3 entsteht die als Abbauprodukt des Podophyllins 5) bekannte Carbonsäure 9, die zum Methyl-(10) bzw. Ethyl-Ester (11) umgesetzt wurde. Das komplizierte MS von 11 wurde durch DADI 6) geklärt: M + ' = m/z 274 -» m/z [259 (-' CH 3 ); 246 (-C 2 H 4 ); 245 (-' C 2 H 5 ) 229 (-C 2 H 5 0'); 228 (-C 2 H 5 OH; o-effekt der Methylgruppe); 201 (-"COOEt)]. m/z 229 -> m/z [214 (-*CH 3 ); 201 (-CO); 183; 157] m/z 228 m/z [213 (- - CH 3 ); 200 (-CO); 181; 171] Aus 10 entsteht mit NBS die Brommethylverbindung 12. Die entspr. Umsetzung von 3 liefert zwar 13, das aber im Gegensatz zu 12 (-» 14) nur unzulänglich mit Diethylamin
5 reagiert. - Versuche, die Carbonsäure 9 durch Photobromierung oder mit NBS umzusetzen, gaben nur Spuren der erwarteten o-brommethylverbindung ließ sich problemlos zum Alkohol 15 reduzieren, während dessen Oxidation zu 16 schwierig war: Chromylchlorid 7)8) als Beispiel einer Chrom-Ester-Oxidation führte lt. DC zu vielen Dragendorff-negätiven Produkten; vergleichsweise günstig war Mn0 2 in CC1 4, obwohl auch hier abhängig von der Reaktionszeit (dc-kontrolle) N-freie Verbindungen auftreten. Die Mn0 2 -Oxidation liefert auf ungeklärtem Weg 2,3-Dimethoxy-naphthalin, die Carbonsäure 9 - sie ist lt. MS mit einer Verbindung verunreinigt, die 2 H weniger besitzt und möglicherweise das Lakton 17 ist - und den gewünschten Aminoaldehyd 16, der mit Aceton zum Aldoladditionsprodukt 18 und zum a, ß-ungesättigten Keton 19 reagiert. 18 ist durch das Multiple«bei ppm für 0-CH(OH)-CH 2 -CO-charakterisiert. - Im MS verliert Mt = m/z 359 (8 % r.i.) Wasser zu m/z 341. Der weitere Zerfall entspricht Im MS von 19 ist die * CO-CH3-Abspaltung interessant, die wir als Folge einer Ringschlußreaktion (Abb. 3) erklären. Abb. 3 Borhydrid-Reduktion von 19 führt zum Aminoalkohol 20, Bordeuterid zu 20a. 20 und 20a sind Modellverbindungen für la: ihre spektroskopischen Daten werden in einer nachfolgenden Publikation besprochen. - Versuche, aus 20 durch Hydrierung (Pd/C) das entspr. Dihydroderivat als lb-modell herzustellen, führten unter gleichzeitiger reduktiver Desamininierung zu 21. Die Abspaltung von C 3 H 6 0 im MS dieser Verbindung durch McLafferty-Umlagerung wird ebenfalls später diskutiert. Experimenteller Teil Schmp.: Apparatur nach Dr. Tottoli, (unkorr.). IR: Beckman Acculab III. Falls nichts anderes 1 angegeben, als KBr-Preßling, bei Ölen als Film (NaCl-Platten). H-NMR: Varian EM 360 A (60 MHz) in CDCI3, ca. 5proz., bei 35, TMS inn. Stand., falls nichts anderes angegeben. Bruker WH 90 (90 MHz), entspr. MS: Varian MAT CH 5, Anregungsenergie 70 ev, falls nichts anderes angegeben. Hochauflösende Messungen und Analyse metastabiler Übergänge (DADI; E/B und E/B 2 Linked Scan Methode): Gerät 311A, Varian MAT. UV: Shimadzu 210, Beckman DB-GT, in Methanol (Uvasol Merck), 10 mm Schichtdicke. Elementaranalysen: Mikroanalytisches Labor der Universität Regensburg (Leiter G. Wandinger). 2,3-Dimethoxy-6-acetyl-7-methyl-naphthalin (3) 72 g AICI3 wurden in 450 ml absol. Dichlorethan suspendiert und unter Kühlung im Eis/NaCl-Bad mit 38.5 g Acetylchlorid versetzt. Dazu wurde bei 0 eine Lösung von 90 g 2 in 1400 ml absol. Dichlorethan getropft. Nach einigen h Rühren im Eisbad und über Nacht bei Raumtemp. wurde auf 1000 ml Eis/2N-HCl gegossen. Die organ. Phase wurde abgetrennt und wie üblich aufgearbeitet. Aus dem beim Einengen zurückbleibenden schwarzbraunen öligen Rückstand kristallisierte das Produkt
6 beim Versetzen mit wenig Ether in der Tiefkühltruhe. Die gelbweißen Kristalle wurden aus EtOH umkristallisiert. Aus der Mutterlauge konnte durch Feststoff destination eine zusätzliche Produktfraktion gewonnen werden. Ausb g (46 %), Schmp C 1 5 H 1 6 (244.1) Ber. C 73.8 H 6.55 Gef. C 73.9 H IR (KBr): 1690 cm" 1 (CO). MS (70 ev): m/e 244 (63 % M + ), 229 (100 %), 201 (33 %). *H-NMR (CDC1 3 ): 6 (ppm) = 2.70 (s; 6H, 0-CH 3 und 0-CO-CH 3 ), 4.05 (s; 6H, 2 0-OCH 3 ), 7.02 (s; 1H, 0-H-l), 7.15 (s; 1H, 0-H-4), 7.48 (s; 1H, 0-H-8), 8.13 (s; 1H, 0-H-5). UV (Methanol): X max (log e) = 217 (4.30), 252 (4.60), 258 (4.59), 308 nm (4.07). Umsetzung von 3 mit Butyllithium und Acetaldehyd 4.88 g 3 wurden in 100 ml absol. THF gelöst und im Trockeneis/Aceton-B ad auf -78 gekühlt. Dazu wurden unter N ml einer 15proz. Lösung von BuLi in Hexan zugegeben. Während der folgenden 4 h wurden 0,88 g Acetaldehyd in 100 ml absol. THF durch einen auf -20 gekühlten Tropftrichter zugegeben. Anschließend wurde noch 1 h bei -78 gerührt, dann langsam auf Raumtemp.erwärmt, mit 5 ml Wasser versetzt, eine geringe Menge Niederschlag abfiltriert, das Filtrat eingeengt und der Rückstand in CH 2 aufgenommen. Die organ. Phase wurde mit Wasser gewaschen und über Na 2 getrocknet. Beim Einengen blieb ein gelbgrünes Öl. Die DC an Si0 2 /EtOAc zeigte, daß es aus 4 Substanzen bestand, von denen die zwei mit den höchsten RF-Werten positiv mit 2,4-Dinitrophenylhydrazin reagierten. Das Reaktionsgemisch wurde über eine SiO r Säule (50 cm/0 4 cm, -20 ) mit EtOAc getrennt (Fraktionen zu 15 ml). Die Fraktionen 8-10 enthielten wenige mg einer Substanz mit RF 0,79, die ms als 2,3-Dimethoxy-6-(l-hydroxy-l-methyl-pentyl)-7-methyl-naphthalin (5) identifiziert wurde. Die Fraktionen bestanden aus 3. Die Fraktionen mit RF 0.64 enthielten das gewünschte 2,3-Dimethoxy-6-(3-hydroxy-l-oxo-butyl)-7-methyl-naphthalin (6), Schmp Aus den Fraktionen mit RF 0.47 wurde 2,3-Dimethoxy-7-methyl-6-[3-hydroxy-2-(a-hydroxyethyl)]-butyronaphthon (7) als Öl isoliert. 5: MS (70 ev): C 1 9 H 2 6 m/e 302 (32 % M + ), 284 (18 %), 245 (100 %), 203 (79 %), 202 (37 %), 198 (40 %). MS (Hochauflösung): Ber Gef (Am 1.4; 4.6 ppm) X H-NMR (CDC1 3 ): 6 (ppm) = (m; 9H, -C 4 H 9 ), 1.65 (s; 3H, CR 2 (OH)-CH 3 ), 2.62 (s; 3H, 0-CH 3 ), 3.91 (s; 6H, 2 0-OCH 3 ), 6.90, 7.00, 7.48, 7.74 (s; 4H, 0-H). 6: IR (KBr): 1674 cm" 1 (CO). MS (12 ev): C 1 7 H 2 0 O 4 m/e 288 (100 % M + ), 270 (22 %), 255 (22 %), 245 (12 %), 244 (69 %), 230 (35 %), 229 (83 %). *H-NMR (CDC1 3 ): 6 (ppm) = 0.80 (d; J = 6 Hz, 3H, -CH(OH)-CH3), 2.10 (s; 3H, 0-CH 3 ), 2.67 (d; J = 6 Hz, 2H, -CH2-CH(OH)-), 3.50 (s; 1H, -OH), (m; 1H, -CH(OH)-), 3.93 (s; 6H, 2 0-OCH 3 ), 6.58, 6.76, 6.92, 7.71 (s; 4H, 0-H). 7: MS (70 ev): C 1 9 H m/e 332 (4 % M + ), 291 (1 %), 288 (3 %), 270 (9 %), 255 (29 %), 229 (100 %), 201 (25 %). *H-NMR (CDC1 3 ): 6 (ppm) = 1.00 (m; 1H, -CO-CH<), 1.26 (d; J = 6 Hz, 6H, 2x -CH(OH)-CH3), 2.63 (s; 3H, 0-CH 3 ), (m; 2H, 2 x -CH(OH)-), 4.05 (s; 6H, 2 x 0-OCH 3 ), 4.40 (s breit; 2H, 2 x OH), 7.05, 7.17, 7.51, 8.10 (s; 4H, 0-H). 2,3-Dimethoxy-6-(l-oxo-3-acetoxy~butyl)-7-methyl-naphthalin (8) 1,2 g 6 wurden in 80 ml frisch dest. Acetanhydrid mit 1,0 ml Pyridin versetzt und unter Feuchtigkeitsausschluß 18 h bei Raumtemp. gerührt. Unter Eiskühlung wurde mit 200 ml Wasser hydrolysiert, mit konz. Ammoniak annähernd neutralisiert und 3mal mit 100 ml Ether ausgeschüttelt. Die Etherphase wurde mit Wasser gewaschen, über Na 2 getrocknet und eingeengt. Der leicht gelbliche, ölige Rückstand war de einheitlich (Si0 2 /EtOAc). Ausb g (96 %). IR (Film): 1735,
7 1673 cm" 1 (CO). MS (70 ev): C 1 9 H m/e 330 (58 % M + ), 288 (2 %), 270 (24 %, *220.91), 255 (55 %, *240.83),229 (100 %,*158,91,*194,22), 201 (24 %, *176.42). *H-NMR (CDC1 3 ): ö(ppm) = 1.38 (d; J = 6Hz, 3H, -CH(OAc)-CH3), 2.00 (s; 3H -COCH 3 ) 2.57 (s,3h, 0-CH 3 ), 3.05,3.50 (ABX; J = 16/7 Hz, 2H,-CO-CH 2 -),3.95(s;6H,20-OCH 3 ),5.49(tvomq;J=6/7Hz, lh,-ch(oac)-),6.97,7.10,7.43,8.05 (s; 4H, 0-H). UV (Methanol: X max (log E) = 215 (4.41), 244 (4.46, sh), 252 (4.59), 258 (4.58), 304 nm (4.10). 2,3-Dimethoxy-7-methyl-naphthalin-6-carbonsäure (9) 2,3 g 3 wurden analog 2,3-Dimethoxy-6-acetonaphthon 4) mit 38 g NaOH in 200 ml Wasser und 45 g Brom umgesetzt. Umkristallisation aus EtOH. Ausb. 18 g (78 %), Schmp , Lit. 5) : IR (KBr): 3250 (OH), 1708 cm" 1 (CO). X H-NMR (F 3 CCOOD): ö (ppm) = 2.21 (s; 3H, 0-CH 3 ), 3.54 (s; 6H, 2 0-OCH 3 ), 6.54, 6.66, 6.96, 7.90 (s; 4H, 0-H), (s; 1H, -COOH). UV (Methanol): X max (log e) = 229 (4.68), 270 (3.61, sh), 326 nm (3.47). 2,3-Dimethoxy'7-methyl-6-naphthalincarbonsäure-methylester (10) 5) ' 9), 2,3-Dimethoxy-7-methyl-6-naphthalincarbonsäure-ethylester (11) Veresterung mit Diazomethan: 3,42 g 9 wurden in 200 ml MeOH/H 2 010/1 gelöst und mit etherischer Diazomethanlösung versetzt, bis eine leichte Gelbfärbung bestehen blieb. Die Lösung wurde nach 1 h bei Raumtemp. eingeengt, der Rückstand in Ether aufgenommen, mit verd. NaOH und Wasser gewaschen, über Mg getrocknet und abdestilliert. Umkristallisation aus MeOH ergab 3,5 g 10 (96 %). Veresterung mit MeOH/H 2 : 17,5 g 9 wurden in 500 ml MeOH absol. mit 30 ml konz.h 2 5 h unter Rückfluß erhitzt. Übliche Aufarbeitung; 14.8 g 10 (79 %). Veresterung mit EtOH/H 2 : Darstellung des Ethylesters 11 analog, Schmp (EtOH). 10: IR (KBr): 1715 cm 4 (CO). MS (70 ev): C 1 5 H m/e 260 (100 % M + ), 229 (32 %), 228 (21 %, *199.94), 200 (48 %, *175.44). X H-NMR (CDC1 3 ): ö (ppm) = 2.70 (s; 3H, 0-CH 3 ), 3.90 (s; 3H, -COOCH 3 ),4.OO(s;6H,^0-OCH 3 ),7.OO,7.12,7.49,8.34(s;4H,0-H).UV(Methanol):Xmax(loge) = 208 (4.06, sh), 220 (4.19, sh), 247 (4.71), 296 nm (4.00). 11: IR (KBr): 1705 cm" 1 (CO). MS (70 ev): C 1 6 H m/e 274 (100 % M + ), 259 (4 %), 246 (8 %), 245 (19 %), 229 (39 %), 228 (34 %), 201 (48 %), 200 (37 %, *145.44). X H-NMR (CDC1 3 ): ö (ppm) = 1.42 (t, J = 7 Hz, 3H, -CH 2 -CH3), 2.68 (s; 3H, 0-CH 3 ), 3.98 (s; 6H, 2 0-OCH 3 ), 4.42 (q; J = 7 Hz, 2H, -COOCH 2 -), 7.00,7.13,7.50, 8.33 (s; 4H, 0-H). UV (Methanol): X max (log e) = 208 (4.07, sh), 220 (4.17, sh), 248 (4.67), 253 (4.64, sh), 296 nm (4.01). 2J-Dimethoxy-6-brommethyl-7-naphthalincarbonsäure-methylester (12) 13 g (50 mmol) 10 wurden in 200 ml absol. CC1 4 gelöst und mit 8,2 g (50 mmol) N-Bromsuccinimid sowie 100 mg Azo-bisisobutyronitril versetzt. Die Lösung wurde unter Rückfluß bis zum Anspringen der Reaktion erwärmt und ca. 2 h im leichten Sieden gehalten. Dann wurde vom Succinimid abgesaugt, mit CC1 4 gewaschen und das Filtrat eingeengt. Es blieben 12 g eines hellbraunen, amorphen Rückstands. Schmp Umkristallisation aus Benzol/Petrolether 1: 2 ergab 11,5 g (68 %) des kristallinen Produktes. Schmp IR (KBr): 1710 cm" 1 (CO). MS (70 ev): C 1 5 H 1 5 Br0 4 m/e 338/340 (4 % M + ), 259 (100 %), 258 (49 %), 229 (35 %, *202.47), 201 (32 %, *176.72), 200 (27 %). X H-NMR (CDC1 3 ): ö (ppm) = 3.96 (s; 9H, 2 0-OCH 3 und -COOCH 3 ), 5.09 (s; 2H, 0-CH 2 Br), 7.02,7.10, 7.67, 8.34 (s; 4H, 0-H). UV (Methanol): X max (log e) = 205 (4.29), 245 (sh), 260 (4.80), 285 nm (4.12, sh).
8 2,3-Dimethoxy-6-brommethyl-acetonaphthon (13) 21 g (86 mmol) 3 wurden in 600 ml absol. CC1 4 zum Sieden erhitzt. Dazu wurden 14,3 g (89 mmol) Brom in 200 ml absol. CC1 4 getropft, während die Reaktionsmischung mit einer 500 Watt-Lampe bestrahlt wurde. Nach 1 h war die Reaktion beendet. Das Lösungsmittel wurde zu 2/3 abdestilliert, das Produkt durch Zugabe von 11 Petrolether gefällt. Umkristallisation aus Benzol/Petrolether ergab 13,4g 13 (48 %), Schmp C 1 5 H 1 5 Br (323.0) Ber. C55.7 H 4.64 Br 24.8 Gef. C 55.7 H4.70 Br24.5. MS (70eV): m/e322/324 (9 % M + ), 244 (62 %), 229 (100 %), 201 (29 %). X H-NMR (CDC1 3 ): ö (ppm) = 2.58 (s; 3H, -COCH 3 ), 3.96 (s; 6H, 2 0-OCH 3 ), 4.47 (s; 2H, 0-CH 2 Br), 7.00, 7.11,7.57, 8.15 (s; 4H, 0-H). 2,3-Dimethoxy-6- (N, N-diethyl-aminomethyl) - 7-naphthalincarbonsäure-methylester (14) Zu 5,3 g 12 in 200 ml absol. Benzol wurden bei Raumtemp. 3,4 g frisch dest. Diethylamin in 50 ml absol. Benzol getropft. Dann wurde 2 d bei 40 gerührt. Dabei schied sich ein feiner kristalliner Niederschlag ab. Die Benzollösung wurde mit verd. NaHC -Lsg. und Wasser gewaschen, über Na 2 getrocknet und eingeengt. Der ölige Rückstand ließ sich nicht im Kugelrohr destillieren. IR (Film): 1710cm" 1 X (CO). H-NMR (CDC1 3 ): 6 (ppm) = 1.77 (t; J = 7 Hz, 6H, 2N-C^-CH*), 2.29 (q; J = 7 Hz, 4H, 2N-CH2-), 3.59 (s; 3H, -COOCH 3 ), 3.62 (s; 2H, 0-CH 2 -N<), 3.67 (s; 6H, 2 0-OCH 3 ), 6.79 (s; 2H, 0-H), 7.47, 7.83 (s; 2H, 0-H). 2,3-Dimethoxy-6- (N, N-diethyl-aminomethyl) - 7-hydroxymethyl-naphthalin (15) Zu 1 g LiAlH 4 in 50 ml absol. THF wurden 2,5 g des rohen Aminoesters 14 in 100 ml absol. THF unter Eiskühlung getropft. Danach wurde 2 h unter Rückfluß erhitzt, die Reaktionsmischung im Eisbad gekühlt und überschüssiges LiAlH 4 mit möglichst wenig Wasser hydrolysiert. Vom Niederschlag wurde abfiltriert, der Rückstand mehrmals mit Ether gewaschen, die organ. Phase über Na 2 getrocknet und i. Vak. abdestilliert: 2,1 g bräunliches Öl, das im Kugelrohr destilliert wurde (Sdp. 0.o Luftbadtemp.). Das leicht gelblich gefärbte Öl wurde im Kühlschrank kristallin. Schmp C 1 8 H 2 5 N (303.2) Ber. C71.3 H 8.25 N4.6; Gef. C70.8 H 8.19 N4.8. MS (70eV): m/e 303 (10 %, M + ), 272 (3 %), 230 (100 %), 229 (23 %, *228.00), 201 (12 %). X H-NMR (CDC1 3 ): 6 (ppm) = 1.03 (t; J = 7 Hz, 6H, 2 N-C^-CHj), 2.50 (q; J = 7 Hz, 4H, 2 N-CHr), 3.67 (s; 2H, 0-CH 2 -N<), 3.90 (s; 6H, 2 0-OCH 3 ), 4.56 (s; 2H, 0-CHrOH), 5.69 (s breit; 1H, austauschbar mit D 2 0, -OH), 6.99 (s; 2H, 0-H), 7.42, 7.53 (s; 2H, 0-H). 2,3-Dimethoxy-6-(N,N-diethyl-aminomethyl)-7-naphthaldehyd (16) 1,5 g 15 wurden in 300 ml absol. CC1 4 gelöst und mit 12 g Mn0 2 aktiv (Merck) bei Raumtemp. kräftig gerührt. Die Reaktion wurde dabei de verfolgt (A1 2 /CH 2 ; Detektion mit Dragendorff s Reagens und Dinitrophenylhydrazin). 20 h wurden als optimale Reaktionszeit ermittelt. Die Lösung wurde durch ein gehärtetes Filter filtriert oder zentrifugiert und abgedampft, der ölige, hellbraune Rückstand in wenig CH 2 aufgenommen und über eine 30 cm Säule (cm,al 2 ) mit CH 2 chromatographiert. Damit konnten N 2 -freie Reaktionsprodukte (Dragendorff-negative Reaktion) abgetrennt werden. Der Aldehyd enthielt nur eine geringe Beimengung von Ausgangsmaterial und war für die weitere Verwendung rein genug. Für analytische Zwecke wurde 16 durch PSC an A1 2 /CH 2 gereinigt. Laufstrecke 18 cm, zweimalige Entwicklung. Eines der N-freien Produkte (oberste Zone) konnte durch PSC isoliert (RF 0.66) und durch MS und Vergleich mit authentischem Material (DC, IR, NMR) als 2,3-Dimethoxy-naphthalin identifiziert
9 werden. Die zweitoberste Zone enthielt 9 und 17 (?). Drittoberste Zone: 15, Unterste Zone: : IR (Film): 1685 cm" 1 (CO). MS (70 ev): C 1 8 H 2 3 N m/e 301 (1 % M + ), 272 (7 %), 230 (100 %), 229 (27 %), 215 (6 %), 201 (16 %), 187 (16 %). X H-NMR (CDC1 3 ): ö (ppm) = 1.00 (t; J = 7 Hz, 6H, 2 N-CH 2 -CH 3 ), 2.57 (q; J = 7 Hz, 4H, 2 N-CHr), 4.03 (s; 8H, 2 0-OCH 3 und 0-CH2-N<), 7.07,7.17 (s; 2H, 0-H, H-l und H-4), 7.66 (s; 1H, 0-H, H-5), 8.18 (s; 1H, 0-H, H-8), (s; 1H, 0-CHO). 2,3-Dimethoxy-6-(N,N-diethyl-aminomethyl)-7-(buten(l)-on(3)yl)-naphthalin (19) und 2,3-Dimethoxy-6-(N,N-diethyl-aminomethyl)-7-{l-hydroxy-3-oxo-butyl)-naphthalin (18) Zu 1 g 16 in 150 ml absol. MeOH und 10 ml absol. Aceton wurden unter N 2 bei Raumtemp. 50 ml 2N-NaOH langsam zugetropft. Nach 5 h wurde die Lösung auf 70 ml eingeengt, mit 100 ml Wasser verdünnt und 5mal mit 50 ml Ether ausgeschüttelt. Die Etherlösung wurde über Na 2 getrocknet und i. Vak. eingeengt, der hellgelbe, ölige Rückstand de untersucht (A1 2 /CH 2 ): zwei mit Dinitrophenylhydrazin anfärbbare Substanzen mit RF 0.58 und 0.42, daneben noch 4 sehr kleine Substanzflecke mit RF unter 0.25, die sich mit Dinitrophenylhydrazin nicht anfärben ließen. Der gesamte Reaktionsrückstand wurde daraufhin sc an A1 2 mit CH 2 getrennt (Säulenlänge 60 cm, cm, Fraktionen zu 15 ml): Die Fraktionen 1-25 enthielten sehr geringe Substanzmengen, die sich zwar mit Dinitrophenylhydrazin anfärben ließen, jedoch mit Dragendorff's und Mayer's Reagens keine Reaktion gaben. In den Fraktionen war das gewünschte 19, das mit Dragendorff's Reagens, Dinitrophenylhydrazin und Mayer's Reagens positiv reagierte. Ausb. ca. 400 mg, Schmp Die Fraktionen >85 enthielten 19 im Gemisch mit wenig 18 (MS) und wurden durch PSC an A1 2 /CH 2 getrennt. Dabei wurden 70 mg 19 und ca. 10 mg 18 erhalten. 19: IR (KBr): 1671 cm" 1 (CO). MS (70 ev): C 2 1 H 2 7 N m/e 341 (62 % M + ), 326 (15 %, *311.65), 312 (22 %, *285.46), 298 (39 %, *260.42), 283 (6 %, *234.86), 270 (42 %, *213.78), 268 (24 %), 255(26 %), 227 (100 %, *190.85), 212 (55 %, *197.99). X H-NMR (CDC1 3 ): 6 (ppm) = 1.09 (t; J = 7 Hz, 6H, 2 N-CHj-Cty, 2.50 (s; 3H, -COCH 3 ), 2.61 (q; J = 7Hz, 4H, 2 N-CHr), 3.79 (s; 2H, 0-CH 2 -N<), 4.04 (s; 6H, 2 0-OCH 3 ), 6.62,8.34 (AB; J = 17 Hz, 2H, -CH=CH-), 7.08,7.13 (s; 2H, 0-H, H-l und H-4), 7.61, 7.99 (s; 2H, 0-H, H-5 und H-8). 2,3-Dimethoxy-6- (N, N-diethyl-aminomethyl)-7- (3-hydroxy-buten(l)yl) -naphthalin (20) Zu 100 mg 19 in 20 ml absol. MeOH und 20 ml absol. THF wurden unter N mg NaBH 4 bei Raumtemp. in kleinen Anteilen gegeben. Die anfangs gelb gefärbte Lösung wurde binnen 5 min farblos. Die Reaktion wurde de verfolgt. Nach 15 min war 19 nicht mehr nachweisbar (A1 2 /CH 2 ). Die Lösung wurde i. Vak. bei Raumtemp. zur Trockne gebracht, der weiße Rückstand in 50 ml Wasser suspendiert und die wäßrige Lösung 3mal mit 50 ml Ether extrahiert. Die org. Phase wurde i. Vak. eingeengt und der weiße Rückstand aus wenig MeOH umkristallisiert. Ausb. 70 mg (70 %). Schmp MS (70 ev): C 2 1 H 2 9 N m/e 343 (35 % M + ), 342 (23 %), 328 (9%), 314 (5%), 298 (15%), 285 (4%), 272 (12%), 270 (40%), 255 (24%), 239 (13%), 227 (100%), 212 (36 %). MS (12 ev): 343 (100 % M + ), 328 (5 %), 298 (10 %), 272 (11 %), 270 (23 %). ^-NMR (CDC1 3 ): ö (ppm) = 1.05 (t; J = 7 Hz, 6H, 2 N-C^-CILj), 1.48 (d; J = 6 Hz, 3H, -CH(OH)-CH3), 2.60 (q; 7 = Hz, 4H, 2 N-CH 2 -), 3.05 (s breit; 1H, -OH), 3.68 (s; 2H, 0-CH 2 -N<), 3.97 (s; 6H, 2 0-OCH 3 ), (m; 1H, -CH(OH)-), 6.20, 7.18 (ABX; J = 16/4 Hz, 2H, -CH=CH-, A-Teil aufgespalten zum d), 7.10 (s; 2H, 0-H, H-l und H-4), 7.56,7.78 (s; 2H, 0-H, H-5 und H-8). UV (Methanol): X max (log e) = 215 (4.28), 252 (4.70), 290 nm (3.92).
10 2,3-Dimethoxy-6-(N, N-diethyl-aminomethyl)-7-(3-deutero-3-hydroxy-buten(l)yl)-naphthalin (20a) 50 mg 19 in 10 ml absol. MeOH und 10 ml absol. THF wurden unter N 2 mit 100 mg NaBD 4 versetzt und 15 min bei Raumtemp. gerührt. Aufarbeitung wie 20. Der beim Eindampfen der getrockneten (Na 2 ) Etherlösung verbliebene Rückstand wurde 2mal in MeOH gelöst und wieder eingeengt, um das D an der OD-Gruppe auszutauschen. Ausb. ca. 45 mg (90 %), Schmp MS (70 ev): C 2 1 H 2 8 DN m/e 344 (36 % M + ), 343 (26 %), 329 (9 %), 315 (5 %), 298 (20 %), 285 (4 %), 273 (10 %), 272 (6 %), 271 (10 %), 270 (25 %), 255 (11 %), 242 (7 %), 240 (7 %), 227 (100 %), 212 (26 %). MS (12eV): 314 (100% M + ),329(15%),326(10%),298(15%),273(15%),272(7%),271 (15 %), 270 (22 %). 1 H-NMR (CDC1 3 ): 6 (ppm) = 1.06 (t; J = 7 Hz, 6H, 2 N-CHrCH*), 1.42 (s; 3H, CD(OH)-CH3), 2.42 (s breit; 1H, -OH), 2.55 (q; J = 7 Hz, 4H, 2 N-CH 2 -), 3.67 (s; 2H, 0-CH 2 -N<) (s; 6H, 2 0-OCH 3 ), 6.18,7.20 (AB; J = 16 Hz, 2H, -CH=CH-), 7.08 (s; 2H, 0-H, H-l und H-4), 7.56,7.78 (s; 2H, 0-H, H-5 und H-8). UV (Methanol): X max (log s) = 215 (4.29), 252 (4.72), 290 nm (3.94). 2,3-Dimethoxy-6-(3-hydroxy-butyl)-7-methyl-naphthalin (21) 20 mg 20 wurden an 50 mg Pd/C (10 %) in 20 ml MeOH bei Raumtemp. und Normaldruck hydriert. Der ölige Rückstand wurde ms als 21 identifiziert. MS (70 ev): C 1 7 H 2 2 m/e 274 (48 % M + ), 229 (11 %), 216 (100 %, *170.28), 215 (50 %), 201 (23 %, *187.04). Literatur 1 Dissertation L. Faber, Braunschweig H. Budzikiewicz, L. Faber, E.-G. Herrmann, F. F. Perrollaz, U. P. Schlunegger und W. Wiegrebe, Justus Liebigs Ann. Chem. 7979, W. Wiegrebe, U. P. Schlunegger, F. F. Perrollaz und P. Riedl, Arch. Pharm. (Weinheim) 311,328 (1978). 4 vergl. N.Buu-Hoi und D. Lavit, J. Org. Chem. 21, 21 (1956). 5 W. Borsche und J. Niemann, Justus Liebigs Ann. Chem. 499, 59 (1932). 6 U. P. Schlunegger, Angew. Chem. 87, 731 (1975). 7 Anorganikum, 7. Aufl., S. 1193, VEB Verlag der Wissenschaften, Berlin R. Stewart, Oxidation Mechanisms, S. 55, W. A. Benjamin, Inc., New York R. Adams, T. A. Geissman, B. R. Baker und H. M. Teeter, J. Am. Chem. Soc. 63, 528 (1941). [Ph 305]
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
Archiv der Pharmazie
 J Sonderdruck aus Archiv der Pharmazie 311. Band, Heft 4, Seite 328-340 Verlag Chemie, GmbH, Weinheim/Bergstr. Wolfgang Wiegrebe, Urs P. Schlunegger, Franjois F. Perrollaz und Peter Riedl Fragmentierungsreaktionen
J Sonderdruck aus Archiv der Pharmazie 311. Band, Heft 4, Seite 328-340 Verlag Chemie, GmbH, Weinheim/Bergstr. Wolfgang Wiegrebe, Urs P. Schlunegger, Franjois F. Perrollaz und Peter Riedl Fragmentierungsreaktionen
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 317. Band, Heft 5, Seite 43 47 Verlag Chemie GmbH, Weinheim (Bergstr.) Synthese der Pyrrolizidine (± )-Tussilagin und (± )-Isotussilagin Erhard Röder*, Helmut Wiedenfeld
Sonderdruck aus Archiv der Pharmazie 317. Band, Heft 5, Seite 43 47 Verlag Chemie GmbH, Weinheim (Bergstr.) Synthese der Pyrrolizidine (± )-Tussilagin und (± )-Isotussilagin Erhard Röder*, Helmut Wiedenfeld
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
5 Chemisch-experimenteller Teil
 5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 312. Band, Heft 5, Seite 385-389 Verlag Chemie, GmbH, Weinheim (Bergstr.) Stereoselektive Synthese des R-(+)-3-Phenyl-isochromans Erwin v. Angerer und Wolfgang Wiegrebe
Sonderdruck aus Archiv der Pharmazie 312. Band, Heft 5, Seite 385-389 Verlag Chemie, GmbH, Weinheim (Bergstr.) Stereoselektive Synthese des R-(+)-3-Phenyl-isochromans Erwin v. Angerer und Wolfgang Wiegrebe
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 316. Band, Heft 9, Seite 801 812 Verlag Chemie GmbH, Weinheim (Bergstr.) Elektronenstoßinduzierter Verlust der Substituenten an C-5 und C-8 bei 1,2,3,4-Tetrahydroisochinolinen,
Sonderdruck aus Archiv der Pharmazie 316. Band, Heft 9, Seite 801 812 Verlag Chemie GmbH, Weinheim (Bergstr.) Elektronenstoßinduzierter Verlust der Substituenten an C-5 und C-8 bei 1,2,3,4-Tetrahydroisochinolinen,
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 303. Band, Heft 2, Seite 145 148 Verlag Chemie, GmbH, Weinheim / Bergstr. W. Wiegrebe und W. D. Sasse Synthese und Hofmann-Abbau des l-hydroxymethyl-2,2 dimethyl-l,2,3,4-tetrahydroisochinolinium-ions
Sonderdruck aus Archiv der Pharmazie 303. Band, Heft 2, Seite 145 148 Verlag Chemie, GmbH, Weinheim / Bergstr. W. Wiegrebe und W. D. Sasse Synthese und Hofmann-Abbau des l-hydroxymethyl-2,2 dimethyl-l,2,3,4-tetrahydroisochinolinium-ions
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b
 3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
Experimenteller Teil
 II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
II 137 1. Allgemeine Anmerkungen Alle beschriebenen Versuche wurden, wenn nicht anders vermerkt, unter Stickstoff- Schutzgas-Atmosphäre durchgeführt. Zur Bestimmung der Schmelzpunkte wurde das Heiztischmikroskop
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon
 Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Präparat Nr. 2: Darstellung von Methyl-1-naphtylketon 3 3 l 1,2-Dichlorethan Naphthalin Acetylchlorid Methyl-1-naphtylketon ( 10 8 ) ( 2 3 l) ( 12 10 ) M=128.18 M=78.50 M=133.34 M=170.21 1. Ansatz: Es
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 314. Band, Heft 3, Seite 240 250 Verlag Chemie, GmbH, Weinheim (Bergstr.) Synthese von (±)-14-Hydroxy-2,3,6-trimethoxy-9,ll,12,13,13a, 14-hexahydro-dibenzo[f,h]pyrrolo[l,2-b]isochinolin**)***)
Sonderdruck aus Archiv der Pharmazie 314. Band, Heft 3, Seite 240 250 Verlag Chemie, GmbH, Weinheim (Bergstr.) Synthese von (±)-14-Hydroxy-2,3,6-trimethoxy-9,ll,12,13,13a, 14-hexahydro-dibenzo[f,h]pyrrolo[l,2-b]isochinolin**)***)
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren Brombutanen
 1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1.2.2 Williamson sche Ethersynthese: Isomere Butyl-phenylether (2a c) aus Natriumphenolat und den isomeren ombutanen Na R R + Adogen 464 + Na 4 9 (137.) 6 5 Na (116.1) 2a-c 1 14 (15.2) a: 2 1-ombutan b:
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
5001 Nitrierung von Phenol zu 2-Nitrophenol und 4-Nitrophenol
 00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid
 NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
NP 1006 Bromierung von 4-Ethoxyacetanilid (Phenacetin) zu 3-Brom-4-ethoxyacetanilid KBr 3, HBr Essigsäure Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Literatur P.F. Schatz, J. chem.
4010 Synthese von p-methoxyacetophenon aus Anisol
 4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
3 Experimenteller Teil
 77 3 Experimenteller Teil 3.1 Allgemeine Untersuchungsverfahren Chromatographie *Dünnschichtchromatographie Sorbentien: [a] DC-Alufolien, Kieselgel 60 F 254, Schichtdicke 0.2 mm (Merck) [b] Glasplatten,
77 3 Experimenteller Teil 3.1 Allgemeine Untersuchungsverfahren Chromatographie *Dünnschichtchromatographie Sorbentien: [a] DC-Alufolien, Kieselgel 60 F 254, Schichtdicke 0.2 mm (Merck) [b] Glasplatten,
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Synthese von DOC (2,5-Dimethoxy-4-chloramphetamin)
 T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
T + K (2000) 68 (2): 62 Synthese von D (2,5-Dimethoxy-4-chloramphetamin) Dorothea Ehlers und Johanna Schäning Technische Fachhochschule Berlin, FB V, Kurfürstenstrasse 141, D-1210 Berlin, e-mail: ehlers@tfh-berlin.de
4 Experimenteller Teil
 4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
4 EXPERIMENTELLER TEIL 62 4 Experimenteller Teil 4.1 Allgemeine Angaben Lösungsmittel und Reagenzien wurden vor Gebrauch gereinigt und falls angegeben entsprechend den Literaturangaben absolutiert 129.
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid
 1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
Chloro(triphenylphosphin)gold(I)
 raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
6011 Hippursäure aus Glycin und Benzoylchlorid
 P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
Zum Mechanismus der Umsetzung von l-(2 -a-hydroxyalkyl-benzyl)- N-methyl-tetrahydroisochinolinen zu phenylsubstituierten Isochromanen*
 Institut für Pharmazeutische Technologie der Technischen Universität Braunschweig und Pharmazeutisches Institut der Universität Bern Zum Mechanismus der Umsetzung von l-(2 -a-hydroxyalkyl-benzyl)- N-methyl-tetrahydroisochinolinen
Institut für Pharmazeutische Technologie der Technischen Universität Braunschweig und Pharmazeutisches Institut der Universität Bern Zum Mechanismus der Umsetzung von l-(2 -a-hydroxyalkyl-benzyl)- N-methyl-tetrahydroisochinolinen
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on)
 6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
5009 Synthese von Kupferphthalocyanin
 P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
2023 Reduktion von D-(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b).
 23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
Gruppenpräparat: Versuch Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon
 P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch 7.4.1.1 Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan
P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch 7.4.1.1 Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol
 1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)-
 Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Christina Sauermann 1 Präparat 5: Darstellung von Triphenylmethanol -Reaktion der Carbonylfunktion mit Kohlenstoff-Nukleophilen (Grignard-Verbindungen)- C + Et 2 C H C 13 H 10 (M=182,22 g/mol) C 6 H 5
Endersch, Jonas Praktikum Allgemeine Chemie 2, Saal G1, Platz 53
 Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
Endersch, Jonas 30.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.5a: Herstellung von Cholesterylbenzoat Reaktionsgleichung: Einleitung und Theorie: In diesem Versuch
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol
 3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
3001 Hydroborierung/Oxidation von 1-Octen zu 1-Octanol 1. NaBH, I CH H 3 C C. H O /NaOH H 3 OH C 8 H 16 NaBH H O I NaOH C 8 H 18 O (11.) (37.8) (3.0) (53.8) (0.0) (130.) Literatur A.S. Bhanu Prasad, J.V.
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
Arch. Pharm. (Weinheim) 318, (1985)
 648 Eiden, Winkler, Wanner und Markhauser Arch. Pharm. Arch. Pharm. (Weinheim) 318, 648-655 (1985) Zentralwirksame 4-Phenylpyrane: Hydrierte Phenylchromene, Phenylaza- und Phenyloxachromene sowie Phenyl-oxa-
648 Eiden, Winkler, Wanner und Markhauser Arch. Pharm. Arch. Pharm. (Weinheim) 318, 648-655 (1985) Zentralwirksame 4-Phenylpyrane: Hydrierte Phenylchromene, Phenylaza- und Phenyloxachromene sowie Phenyl-oxa-
SKRIPT ZUM INTEGRIERTEN SYNTHESEPRAKTIKUM
 Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Integriertes Synthesepraktikum 2016 rganische Chemie SKRIPT ZUM ITEGRIERTE SYTHESEPRAKTIKUM Woche 1 und 2 (rganische Chemie) 1. Herstellung eines Alkens über die lefinierung eines Aldehyds nach Wittig
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid
 1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
Mittlere Ringe aus Alprenolol und Oxprenolol
 Institut für Pharmazeutische Chemie der Technischen Universität Braunschweig, Germany Mittlere Ringe aus Alprenolol und Oxprenolol K. Görlitzer, A. Lorenz Herrn Prof. Dr. Dr. h.c. G. Zinner mit den besten
Institut für Pharmazeutische Chemie der Technischen Universität Braunschweig, Germany Mittlere Ringe aus Alprenolol und Oxprenolol K. Görlitzer, A. Lorenz Herrn Prof. Dr. Dr. h.c. G. Zinner mit den besten
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Benzol-d. Illumina-Chemie.de - Artikel
 Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2
![Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2](/thumbs/95/126253543.jpg) Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Janine Schneider 05.05.00 Darstellung von 4-Acetylcumol (1-Acetyl-4-isopropylbenzol) [1] Präparat 2 1. Reaktionstyp: Friedel-rafts-Acylierung 2. Reaktionsgleichung: + Al 3 9 12 2 3 Al 3 11 14 M=120.2 g/mol
Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff -
 hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
hristina Sauermann 1 - A- Praktikum Präparat 3: Isolierung und Verseifung von Trimyristin aus Muskatnuss - Naturstoff - Teil I: Isolierung von Trimyristin aus Muskatnuss 1. Prinzip Gepulverte Muskatnüsse
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
Tris(acetylacetonato)cobalt(III)
 Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Betrachtungen zur Herstellung von Methadon-nitril und Isomethadon-nitril sowie verwandten Verbindungen
 Scientia Pharmazeutica (Sei. Pharm.) 68, 229-234 (2000) Österreich ische Apotheker-Verlagsgesellschaft m. b. H, Wien, Printed in Austria 229 Betrachtungen zur Herstellung von Methadon-nitril und Isomethadon-nitril
Scientia Pharmazeutica (Sei. Pharm.) 68, 229-234 (2000) Österreich ische Apotheker-Verlagsgesellschaft m. b. H, Wien, Printed in Austria 229 Betrachtungen zur Herstellung von Methadon-nitril und Isomethadon-nitril
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid
 4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
Dibenzoylmethan
 9.1.2. Dibenzoylmethan Dibenzoylmethan ist eine Stufe eines Zweistufenprärates: Benzoylchlorid (8.1.11) Benzoesäureethylester (8.1.3) Dibenzoylmethan Reaktion: Ansatz: 1,75 g Natrium, 16,0 g Acetophenon,
9.1.2. Dibenzoylmethan Dibenzoylmethan ist eine Stufe eines Zweistufenprärates: Benzoylchlorid (8.1.11) Benzoesäureethylester (8.1.3) Dibenzoylmethan Reaktion: Ansatz: 1,75 g Natrium, 16,0 g Acetophenon,
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv)
 Cp2(H) Seite 1 Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv) [Cp 2 (H)] H (SCHWARTZ Reagens) Cp2(H) Seite 2 1. Synthese [1,2,3] 1.1 Methode Dicyclopentadien wird in einer Retro-DIELS-ALDER-Reaktion
Cp2(H) Seite 1 Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv) [Cp 2 (H)] H (SCHWARTZ Reagens) Cp2(H) Seite 2 1. Synthese [1,2,3] 1.1 Methode Dicyclopentadien wird in einer Retro-DIELS-ALDER-Reaktion
Darstellung von Malachitgrün Präparat 5
 Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Janine Schneider 22.05.00 Darstellung von Malachitgrün Präparat 5 1. Reaktionstyp: säurekatalysierte Kondensation (elektrophile Substitution) 2. Reaktionsgleichung: O + 2 ( + ) Benzaldehyd N,N- Dimethylanilin
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
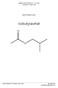 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
sz) Archiv der Pharmazie Sonderdruck aus 313. Band, Heft 9, Seite Verlag Chemie, GmbH, Weinheim (Bergstr.)
 sz) Sonderdruck aus Archiv der Pharmazie 313. Band, Heft 9, Seite 800 803 Verlag Chemie, GmbH, Weinheim (Bergstr.) Tritium- und 14 C-markiertes Dithranol-l,8,9-triacetat Hans-Peter Faro** 0, Angelika Retzow***
sz) Sonderdruck aus Archiv der Pharmazie 313. Band, Heft 9, Seite 800 803 Verlag Chemie, GmbH, Weinheim (Bergstr.) Tritium- und 14 C-markiertes Dithranol-l,8,9-triacetat Hans-Peter Faro** 0, Angelika Retzow***
Archiv der Pharmazie
 Sonderdruck aus Archiv der Pharmazie 301. Band, Heft 1, Seite 33 38 Verlag Chemie, GmbH, Weinheim/ Bergstr. W. Wiegrebe, D. Sasse und E. Roesel Uberführung von 1-Benzylisochinolinen in Berbinium-Salze
Sonderdruck aus Archiv der Pharmazie 301. Band, Heft 1, Seite 33 38 Verlag Chemie, GmbH, Weinheim/ Bergstr. W. Wiegrebe, D. Sasse und E. Roesel Uberführung von 1-Benzylisochinolinen in Berbinium-Salze
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid
 2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
2013 Umsetzung von Zimtsäure mit Thionylchlorid zu Zimtsäurechlorid H + SCl 2 Cl + HCl + S 2 C 9 H 8 2 (148.2) (119.0) C 9 H 7 Cl (166.6) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
Europäisches Patentamt. European Patent Veröffentlichungsnummer: Office europeen des brevets ^ PATENTANMELDUNG EUROPAISCHE
 i» Europäisches Patentamt European Patent Office @ Veröffentlichungsnummer: 0 1 3 0 3 2 7 Office europeen des brevets ^ A1 1 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 84105508.0 @ Int. Cl.*: C07H 13/12,
i» Europäisches Patentamt European Patent Office @ Veröffentlichungsnummer: 0 1 3 0 3 2 7 Office europeen des brevets ^ A1 1 EUROPAISCHE PATENTANMELDUNG Anmeldenummer: 84105508.0 @ Int. Cl.*: C07H 13/12,
Titration von Metallorganylen und Darstellung der dazu benötigten
 Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:
Kapitel 1 Titration von tallorganylen und Darstellung der dazu benötigten Indikatoren -(2-Tolyl)pivalinsäureamid, ein Indikator zur Konzentrationsbestimmung von -rganylen [1] Reaktionstyp: Syntheseleistung:

 7
7