Nutzenbewertung. von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V. Wirkstoff: Tegafur, Gimeracil, Oteracil
|
|
|
- Heiko Zimmermann
- vor 6 Jahren
- Abrufe
Transkript
1 Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Tegafur, Gimeracil, Oteracil Datum der Veröffentlichung: 1. Oktober 2012
2 Tegafur, Gimeracil, Oteracil Zugelassenes Anwendungsgebiet Teysuno ist für die Behandlung von fortgeschrittenem Magenkrebs bei Erwachsenen indiziert bei Gabe in Kombination mit. 1. Zusatznutzen des Arzneimittels im Verhältnis zur zweckmäßigen Vergleichstherapie Der Zusatznutzen im Verhältnis zur zweckmäßigen Vergleichstherapie gilt als nicht belegt. Der pharmazeutische Unternehmer hat die erforderlichen Nachweise für die Nutzenbewertung nach 35a SGB V dem G-BA trotz Aufforderung nicht vollständig vorgelegt. Die in 35a Abs.1 Satz 5 SGB V angeordnete Rechtsfolge ist, dass ein Zusatznutzen als nicht belegt gilt. Zweckmäßige Vergleichstherapie: Die zweckmäßige Vergleichstherapie ist die Zweifachkombination von mit 5-Fluorouracil oder Capecitabin. 2. Anzahl der Patienten bzw. Abgrenzung der für die Behandlung in Frage kommenden Patientengruppen Beschreibung der Erkrankung und Charakterisierung der Zielpopulation Die Zielpopulation ergibt sich aus dem Anwendungsgebiet von Teysuno : Teysuno ist für die Behandlung von fortgeschrittenem Magenkrebs bei Erwachsenen indiziert bei Gabe in Kombination mit. In der Klassifikation nach ICD-10 entspricht dies den bösartigen Neubildungen des Magens (Klassifikation C16). Die Einteilung erfolgt in Stadien zwischen 0 und IV, wobei die Stadien II bis IV weitestgehend der Definition des fortgeschrittenen Magenkarzinoms entsprechen. 1 Prävalenz und Inzidenz der Erkrankung in Deutschland Es ist davon auszugehen, dass die relevante Anzahl der Patienten für die Behandlung mit der Wirkstoffkombination Tegafur/Gimeracil/Oteracil (Teysuno ) am ehesten der Anzahl der am fortgeschrittenen Magenkarzinom neuerkrankten Patienten, also der Inzidenz dieser Erkrankung entspricht. Die Angaben der Prävalenz (z.b. 5-Jahres-Prävalenz) werden im Folgenden nicht dargestellt, da sie insbesondere auch solche Patienten beinhalten, die nicht mehr für die Behandlung mit der Wirkstoffkombination Tegafur/Gimeracil/Oteracil (Teysuno ) in Frage kommen (z.b. Best-Supportive-Care). 2
3 Es wurde zunächst eine Handrecherche in öffentlich verfügbaren Datenbanken, Fachportalen oder Institutionen (wie z.b. Gesundheitsberichterstattung des Bundes, Robert Koch- Institut, etc.) sowie eine systematische Literaturrecherche durchgeführt. Die Recherche ergab insgesamt 33 Treffer, die auf Themenrelevanz überprüft wurden. Insgesamt werden die aktuellen Statistiken der Gesellschaft der epidemiologischen Krebsregister in Deutschland e.v. (GEKID) 2, die Daten des Zentrum für Krebsregisterdaten (ZfKD) im Robert Koch-Institut 3 sowie die gemeinsame Veröffentlichung des Robert Koch- Instituts (RKI) und der GEKID als die bestverfügbaren Quellen zur Inzidenz in Deutschland eingeschätzt. 4 Im Instant Atlas der GEKID werden folgende Zahlen zur Inzidenz eines Magenkarzinoms (alle Stadien) für Jahre 2006 bis 2009 mit dem Datenstand vom Dezember 2011 angegeben. 5 Jahr Geschlecht Männer Frauen Männer Frauen Männer Frauen Männer Frauen Region Fallzahl Fallzahl Fallzahl Fallzahl Fallzahl Fallzahl Fallzahl Fallzahl Baden-Württemberg Bayern Berlin Brandenburg Bremen Hamburg Hessen Mecklenburg- Vorpommern Niedersachsen NRW (nur RB Münster) Rheinland-Pfalz Saarland Sachsen Sachsen-Anhalt Schleswig-Holstein Thüringen Deutschland (Hochrechnung) Etwas niedrigere Inzidenz-Zahlen für Jahre 2006 bis 2009 liefert die Publikation des RKI und der GEKID Krebs in Deutschland 2007/ sowie die Daten des Zentrums für Krebsregisterdaten (ZfKD). 3 Jahr Geschlecht Männer Frauen Männer Frauen Männer Frauen Fallzahl Zu berücksichtigten ist ein leicht abnehmender Trend der letzten Jahre bei Frauen, so dass für das Jahr 2012 bzw. die darauf folgenden Jahre von einer geringfügig niedrigeren Anzahl an Neuerkrankungen ausgegangen werden kann. Dies bestätigt sich auch in der Prognose 3
4 für das Jahr 2012 durch GEKID und RKI mit 9100 Neuerkrankungen für Männer und 6200 Fällen für Frauen.2 Insgesamt kann somit von einer geschätzten Spannweite von etwa bis Neuerkrankungsfällen im Jahr 2012 bei einer leicht abnehmenden Tendenz in folgenden Jahren ausgegangen werden. Zur Ableitung der für die Behandlung mit der Wirkstoffkombination Tegafur/Gimeracil/Oteracil (Teysuno ) relevanten Tumor-Stadien kann die Statistik des Robert Koch-Instituts (RKI) und der GEKID zur Verteilung der Tumor-Stadien bei Erstdiagnose herangezogen werden.6 Der Anteil der Stadien T2 bis T4 liegt hierbei bei etwa 80 bis 85%. Diese Angaben entstammen der Statistik ohne fehlende Angaben und Death Certificate Only (DCO)-Fälle. Da für einen erheblichen Anteil von Fällen jedoch keine Angaben zum Tumorstadium vorliegen (etwa 25% der Fälle), ist die Annahme zur Verteilung der Stadien von limitierter Validität. Unter Berücksichtigung eines Anteils von 82,5% der Tumor-Stadien T2 bis T4 ergibt sich eine geschätzte Spannweite von ca bis der am fortgeschrittenen Magenkarzinom neuerkrankten Patienten im Jahr Anzahl der GKV-Patienten in der Zielpopulation ca bis Patienten Ausgehend von der geschätzten Spannweite wird für die Berechnung ein Anteil von 85% der in der GKV versicherten Bevölkerung zugrunde gelegt.7 Es wird von der etwa gleichen Inzidenz für Versicherte der GKV und der PKV ausgegangen. Referenzliste 1 Tumorzentrum Ludwig Heilmeyer - Comprehensive Cancer Center Freiburg (CCCF). Klinisches Krebsregister Kodierhilfe - Magenkrebs (1). Stand: Februar Zugriff am Gesellschaft der epidemiologischen Krebsregister in Deutschland e.v.(gekid). GEKID-Atlas: Inzidenz und Mortalität von Krebserkrankungen in den Bundesländern, Datenstand: 12/ Zugriff am Zentrum für Krebsregisterdaten im Robert Koch-Insitut. Neuerkrankungen: ICD-10 C16 (Magen). Stand: (Excel Tabelle). Datenbankabfrage/c16_magen.html, Zugriff am Robert Koch-Institut (Hrsg.), Gesellschaft der epidemiologischen Krebsregistern in Deutschland e.v.(hrsg.). Krebs in Deutschland 2007/ Ausgabe. Robert Koch-Institut: Berlin, Gesellschaft der epidemiologischen Krebsregister in Deutschland e.v.(gekid). Tabellen zum GEKID-Atlas: Krebsneuerkrankungen (Inzidenz), altersstandardisierte Rate [Europastandard](je Einwohner): C16 Magen. Datenstand: Dezember (Online Tabelle). Zugriff am Robert Koch-Institut (Hrsg.), Gesellschaft der epidemiologischen Krebsregistern in Deutschland e.v.(hrsg.). Krebs in Deutschland 2007/ Ausgabe. Robert Koch-Institut: Berlin, Robert Koch-Institut (Hrsg.), Statistisches Bundesamt (Hrsg.). Mitglieder und mitversicherte Familienangehörige der gesetzlichen Krankenversicherung am 1.7. eines Jahres (Anzahl). (Primärquelle: KM 6-Statistik (gesetzliche Krankenversicherung: Versicherte), Bundesministerium für Gesundheit). (Online Abfrage). In: (Thematische Recherche: Rahmenbedingungen- Gesetzliche Krankenversicherung- GKV, Mitglieder/Versicherte) Zugriff am
5 3. Anforderungen an eine qualitätsgesicherte Anwendung Die Vorgaben der Fachinformation werden als Anforderungen an eine qualitätsgesicherte Anwendung benannt. Die europäische Zulassungsbehörde European Medicines Agency (EMA) stellt die Inhalte der Fachinformation zu Teysuno (Wirkstoff: Tegafur/Gimeracil/Oteracil) unter folgendem Link frei zugänglich zur Verfügung (letzter Zugriff: ): _Product_Information/human/001242/WC pdf 5
6 4. kosten Behandlungsdauer: Bezeichnung der Behandlungsmodus Anzahl Zyklen Patient Jahr Behandlungstage je Zyklus Behandlungstage Patient Jahr zu bewertendes Arzneimittel; Tegafur/Gimeracil/Oteracil in Kombination mit Tegafur/Gimeracil/ Oteracil in Zyklen; 1 Zyklus = 28 Tage Tag 1-21: 2x tägl. in Zyklen; 1 Zyklus = 28 Tage 1x Zyklus zweckmäßige Vergleichstherapie; 5-Fluorouracil in Kombination mit 5-Fluorouracil in Zyklen: 1 Zyklus= 28 Tage Tag 1-5: 1x tägl. in Zyklen; 1 Zyklus = 28 Tage 1x Zyklus zweckmäßige Vergleichstherapie; Capecitabin in Kombination mit Capecitabin in Zyklen; 1 Zyklus = 21 Tage Tag 1-14: 2x tägl. in Zyklen; 1 Zyklus = 21 Tage 1x Zyklus rechnerisch auf ein Jahr standardisiert Die Angaben zur Kombination Tegafur/Gimeracil/Oteracil mit wurden der Fachinformation entnommen (Fachinformation Teysuno, Stand Februar 2012). Die Fachinformation zu 5-Fluorouracil enthält nur einen allgemeinen Richtwert für die Polychemotherapie des fortgeschrittenen Magenkarzinoms und es wird auf Behandlungstokolle verwiesen, die sich in der als wirksam erweisen haben (Fachinformation 5-FU medac 50mg/ml, Stand Dezember 2010). Für 5-Fluorouracil in Kombination mit wurde daher der Behandlungsmodus im Vergleichsarm der Zulassungsstudie (5-Fluorouracil plus ) des zu bewertenden Arzneimittels zugrunde gelegt (A Safety and Efficacy Study in Patients With Gastric Cancer, clinical trials gov NCT ; Zugriff am ). 6
7 Die Angaben zu Capecitabin in Kombination mit sind der Fachinformation zu Capecitabin entnommen (Fachinformation Xeloda, Stand Juni 2011). Ist in der jeweiligen Fachinformation keine maximale dauer angegeben, wurde als Behandlungsdauer rechnerisch ein Jahr angenommen, auch wenn die tatsächliche dauer patientenindividuell unterschiedlich ist. Obwohl die Fachinformation zu Tegafur/Gimeracil/Oteracil ausführt, dass nach 6 Zyklen abgesetzt werden soll, die Fachinformationen zu den anderen regimen jedoch keine Angaben zur Behandlungsdauer enthalten, wurde aus Gründen der Vergleichbarkeit für alle regime die Behandlungsdauer für als reine Rechengröße auf ein Jahr standardisiert. Verbrauch: Bezeichnung der Wirkstärken der jeweiligen Darreichungs form [mg] Dosierung Dosis Patient Behandlungstag Verbrauch nach Wirkstärke Behandlungstag Behandlungsta ge Patient Jahr Jahresdurchschnittsverbrauch nach Wirkstärke zu bewertendes Arzneimittel; Tegafur/Gimeracil/Oteracil in Kombination mit Tegafur/Gimeracil/ Oteracil x 45 mg 6 x Kapseln mit 15 mg mg 1 x 50 1 x Durchstechflaschen mit 50 mg 13 Durchstechflaschen mit 100 mg zweckmäßige Vergleichstherapie; 5-Fluorouracil in Kombination mit 5-Fluorouracil mg 2 x Injektionsflaschen mit 1000 mg 189 mg 2 x Durchstechflaschen mit 100 mg zweckmäßige Vergleichstherapie; Capecitabin in Kombination mit Capecitabin x 1800 mg 4 x x Tabletten mit 150 mg 1428 Tabletten mit 500 mg 7
8 Bezeichnung der Wirkstärken der jeweiligen Darreichungs form [mg] Dosierung Dosis Patient Behandlungstag Verbrauch nach Wirkstärke Behandlungstag Behandlungsta ge Patient Jahr Jahresdurchschnittsverbrauch nach Wirkstärke mg 1 x 10 1 x 50 1 x Durchstechflaschen mit 10 mg 17 Durchstechflaschen mit 50 mg 17 Durchstechflaschen mit 100 mg Der Berechnung der Dosis Patient wurde eine Körperoberfläche (KOF) von 1,89 m² zugrunde gelegt. Die KOF wurde mittels der Du Bois-Formel unter Verwendung eines durchschnittlichen Köpergewichts von 75,6 Kg und einer durchschnittlichen Körpergröße von 1,72 m laut Mikrozensus 2009 errechnet. Unterschiede zwischen Frauen und Männern waren aufgrund des Anwendungsgebietes nicht zu berücksichtigen. Für Tegafur/Gimeracil/Oteracil sowie für Capecitabin wurde die in der jeweiligen Fachinformation angegebene Standarddosis für eine KOF von 1,89 m² übernommen. Für den Fall, dass sich eine Dosis aus verschieden Wirkstärken zusammensetzt, so wurde dies bei der Berechnung des Verbrauchs berücksichtigt. Kosten: Kosten der Arzneimittel: Bezeichnung der Kosten (Apothekenabgabepreis nach Arzneimittel, Wirkstärke, Darreichungsform und Packungsgröße ) Kosten nach Abzug gesetzlich vorgeschriebener Rabatte zu bewertendes Arzneimittel; Tegafur/Gimeracil/Oteracil in Kombination mit Tegafur/Gimeracil/ Oteracil 195,41 TEYSUNO 15 mg Hartkapseln; 42 St. 46,91 Konzentrat; 50 ml 83,32 Konzentrat; 100 ml 169,96 [2,05 2 ; 23,40 3 ] 43,13 [2,05 2 ; 1,73 3 ] 77,80 [2,05 2 ; 3,47 3 ] 8
9 Bezeichnung der Kosten (Apothekenabgabepreis nach Arzneimittel, Wirkstärke, Darreichungsform und Packungsgröße ) Kosten nach Abzug gesetzlich vorgeschriebener Rabatte zweckmäßige Vergleichstherapie; 5-Fluorouracil in Kombination mit 5-Fluorouracil 15, mg 83,32 Konzentrat; 100 ml 13,38 [2,05 2 ; 0, 42 3 ] 77,80 [2,05 2 ; 3,47 3 ] zweckmäßige Vergleichstherapie; Capecitabin in Kombination mit Capecitabin 77,03 XELODA 150 mg Filmtabletten; 60 St. 451,97 XELODA 500 mg Filmtabletten; 120 St. 17,46 Konzentrat; 10 ml 46,91 Konzentrat; 50 ml 83,32 Konzentrat; 100 ml 71,82 [2,05 2 ; 3,16 3 ] 428,97 [2,05 2 ; 20,95 3 ] 15,08 [2,05 2 ; 0,33 3 ] 43,13 [2,05 2 ; 1,73 3 ] 77,80 [2,05 2 ; 3,47 3 ] 1 Festbetrag 2 Rabatt nach 130 SGB V 3 Rabatt nach 130a SGB V Stand Lauer-Taxe: Kosten für zusätzlich notwendige GKV-Leistungen: Es wurden nur direkt mit der Anwendung des Arzneimittels unmittelbar in Zusammenhang stehende Kosten berücksichtigt, sofern bei der Anwendung des zu bewertenden Arzneimittels und der zweckmäßigen Vergleichstherapie entsprechend der Fach- oder Gebrauchsinformation regelhaft Unterschiede bei der notwendigen Inanspruchnahme ärztlicher Behandlung oder bei der Verordnung sonstiger Leistungen bestehen. Regelhafte Laborleistungen, wie z.b. Blutbildbestimmungen, oder ärztliche Honorarleistungen, die nicht über den Rahmen der üblichen Aufwendungen im Verlauf einer onkologischen Behandlung hinausgehen, wurden nicht berücksichtigt. 9
10 Jahrestherapiekosten: Bezeichnung der Jahrestherapiekosten Patient zu bewertendes Arzneimittel; Tegafur/Gimeracil/Oteracil in Kombination mit Tegafur/Gimeracil/Oteracil 6628, ,09 zweckmäßige Vergleichstherapie; 5-Fluorouracil in Kombination mit 5-Fluorouracil 1739,4 2022,8 zweckmäßige Vergleichstherapie; Capecitabin in Kombination mit Capecitabin 6296, ,17 Für die Berechnung der Arzneimittelkosten wurde zunächst anhand des Verbrauchs die benötigte Anzahl an Packungen nach Wirkstärke ermittelt. Mit der aufgerundeten Anzahl der benötigten Packungen wurden dann die Arzneimittelkosten auf Basis der Kosten Packung, nach Abzug der gesetzlich vorgeschriebenen Rabatte, berechnet. Die Arzneimittelkosten wurden zur besseren Vergleichbarkeit näherungsweise sowohl auf der Basis der Apothekenverkaufspreisebene als auch abzüglich der gesetzlich vorgeschriebenen Rabatte nach 130a SGB V (Abs. 1, 1a, 3a) und nach 130 Abs. 1 SGB V, erhoben. Sonstige GKV-Leistungen Die Hilfstaxe (Vertrag über die Preisbildung für Stoffe und Zubereitungen aus Stoffen) wird zur Berechnung der Kosten nicht vollumfänglich herangezogen, da sie (1) dynamisch verhandelt wird, (2) aufgrund der Vielzahl in der GKV-Versorgung bestehender, größtenteils in nicht öffentlichen Verträgen geregelten Abrechnungsmodalitäten für Zytostatika- Zubereitungen, die nicht an die Hilfstaxe gebunden sind, für die Versorgung nicht repräsentativ ist, (3) ggf. zu einem bestimmten Zeitpunkt nicht alle relevanten Wirkstoffe umfasst und aus diesen Gründen insgesamt für eine standardisierte Kostenerhebung nicht geeignet ist. Demgegenüber ist der in der Lauer-Taxe öffentlich zugängliche Apothekenverkaufspreis eine für eine standardisierte Berechnung geeignete Grundlage. Bei zytostatikahaltigen parenteralen Zubereitungen fallen nach der Hilfstaxe (Stand: 2. Ergänzungsvereinbarung zum Vertrag über die Preisbildung für Stoffe und Zubereitungen aus Stoffen vom ) Zuschläge für die Herstellung von maximal 79,- applikationsfertiger Zubereitung an. Dieser Betrag kann in Verträgen unterschritten werden. Diese zusätzlichen sonstigen Kosten fallen nicht additiv zur Höhe des Apothekenverkaufspreises an, sondern folgen den Regularien zur Berechnung in der Hilfstaxe. Die Kostendarstellung erfolgt aufgrund des AVP und des maximalen Zuschlages und stellt nur eine näherungsweise Abbildung der kosten dar. 10
11 Bezeichnung der Art der Leistung Kosten Einheit Anzahl Zyklus Anzahl Patient Jahr Kosten Patient Jahr zu bewertendes Arzneimittel; Tegafur/Gimeracil/Oteracil in Kombination mit Tegafur/Gimeracil/ Oteracil keine Zuschlag für die Herstellung einer Zytostatika-haltigen parenteralen Zubereitung zweckmäßige Vergleichstherapie; 5-Fluorouracil in Kombination mit 5-Fluorouracil Zuschlag für die Herstellung einer Zytostatika-haltigen parenteralen Zubereitung. Zuschlag für die Herstellung einer Zytostatika-haltigen parenteralen Zubereitung zweckmäßige Vergleichstherapie; Capecitabin in Kombination mit Capecitabin keine Zuschlag für die Herstellung einer Zytostatika-haltigen parenteralen Zubereitung
BAnz AT B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT 23.04.2015 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT 12.10.2015 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT 11.11.2014 B1. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
2. Anzahl der Patienten bzw. Abgrenzung der für die Behandlung infrage kommenden Patientengruppen
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT 20.11.2014 B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Nutzenbewertung. von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V. Wirkstoff: Nepafenac. nach 2 Abs. 2 VerfO des G-BA
 Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Nepafenac nach 2 Abs. 2 VerfO des G-BA Datum der Veröffentlichung: 1. Oktober 2013 1 Nepafenac Zugelassenes Anwendungsgebiet
Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Nepafenac nach 2 Abs. 2 VerfO des G-BA Datum der Veröffentlichung: 1. Oktober 2013 1 Nepafenac Zugelassenes Anwendungsgebiet
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Bundesministerium für Gesundheit. Bekanntmachung
 Seite 1 von 5 Bundesministerium für Gesundheit eines Beschlusses des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII Beschlüsse über die Nutzenbewertung
Seite 1 von 5 Bundesministerium für Gesundheit eines Beschlusses des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII Beschlüsse über die Nutzenbewertung
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Vortioxetin wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT 25.04.2014 B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Secukinumab wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Carfilzomib Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung
 IQWiG-Berichte Nr. 367 Carfilzomib Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung Auftrag: G15-16 Version: 1.0 Stand: 25.02.2016 Impressum Herausgeber: Institut für Qualität und Wirtschaftlichkeit
IQWiG-Berichte Nr. 367 Carfilzomib Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung Auftrag: G15-16 Version: 1.0 Stand: 25.02.2016 Impressum Herausgeber: Institut für Qualität und Wirtschaftlichkeit
1. Zusatznutzen des Arzneimittels im Verhältnis zur zweckmäßigen Vergleichstherapie
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Prospektive Erfassung neu erkrankter Patienten mit einem Malignen Melanom der Haut in Niedersachsen
 197 Wegener Folien-04/07/08_MM/E Mittwoch 07.07.2004 17:29:09 Epidemiologische Daten zur Zwischenauswertung Dezember 2003 des Projektes Prospektive Erfassung neu erkrankter Patienten mit einem Malignen
197 Wegener Folien-04/07/08_MM/E Mittwoch 07.07.2004 17:29:09 Epidemiologische Daten zur Zwischenauswertung Dezember 2003 des Projektes Prospektive Erfassung neu erkrankter Patienten mit einem Malignen
Institut für Krebsepidemiologie e.v. An der Universität zu Lübeck
 Institut für Krebsepidemiologie e.v. An der Universität zu Lübeck Registerstelle des Krebsregisters Schleswig-Holstein Vorsitzender: Dr. med. M. Hamschmidt * Direktor: Prof. Dr. med. A. Katalinic Ratzeburger
Institut für Krebsepidemiologie e.v. An der Universität zu Lübeck Registerstelle des Krebsregisters Schleswig-Holstein Vorsitzender: Dr. med. M. Hamschmidt * Direktor: Prof. Dr. med. A. Katalinic Ratzeburger
BAnz AT 06.08.2014 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
B3)
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Bevölkerungsentwicklung im Freistaat Sachsen 1990 bis 2025
 Bevölkerungsentwicklung im Freistaat Sachsen 1990 bis 2025 Bevölkerung insgesamt in Tausend 5.000 4.800 4.600 4.400 4.200 4.000 3.800 3.600 3.400 3.200 Bevölkerungsfortschreibung - Ist-Zahlen Variante
Bevölkerungsentwicklung im Freistaat Sachsen 1990 bis 2025 Bevölkerung insgesamt in Tausend 5.000 4.800 4.600 4.400 4.200 4.000 3.800 3.600 3.400 3.200 Bevölkerungsfortschreibung - Ist-Zahlen Variante
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Apixaban wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BAnz AT B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Auswertung. Fachabteilung Entwicklung 1991 bis 2003 Kinderheilkunde -14,09% Kinderchirurgie -29,29% Kinder- und Jugendpsychiatrie 5,35% Gesamt -13,00%
 Bundesrepublik gesamt Anzahl der Kinderabteilungen Kinderheilkunde -14,09% Kinderchirurgie -29,29% Kinder- und Jugendpsychiatrie 5,35% Gesamt -13,00% Anzahl der Kinderbetten Kinderheilkunde -32,43% - davon
Bundesrepublik gesamt Anzahl der Kinderabteilungen Kinderheilkunde -14,09% Kinderchirurgie -29,29% Kinder- und Jugendpsychiatrie 5,35% Gesamt -13,00% Anzahl der Kinderbetten Kinderheilkunde -32,43% - davon
Nutzenbewertung. von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V (nach 5. Kapitel 1 Abs. 2 Nr. 2 i.v.m. 2 Abs.
 Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V (nach 5. Kapitel 1 Abs. 2 Nr. 2 i.v.m. 2 Abs. 2 VerfO des G-BA) Wirkstoff: Insulin degludec Datum der Veröffentlichung: 15. September
Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V (nach 5. Kapitel 1 Abs. 2 Nr. 2 i.v.m. 2 Abs. 2 VerfO des G-BA) Wirkstoff: Insulin degludec Datum der Veröffentlichung: 15. September
BAnz AT 04.04.2014 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Regionales Klinisches Krebsregister Dresden
 Regionales Klinisches Krebsregister Dresden Bösartige Neubildungen der Bronchien und der Lunge Region des Regionalen Klinischen Krebsregisters Dresden 1996-2015 Gesamt Inhaltsverzeichnis Daten des Gemeinsamen
Regionales Klinisches Krebsregister Dresden Bösartige Neubildungen der Bronchien und der Lunge Region des Regionalen Klinischen Krebsregisters Dresden 1996-2015 Gesamt Inhaltsverzeichnis Daten des Gemeinsamen
BAnz AT 07.07.2016 B4. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Die Evangelische Kirche in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern
 Die Evangelische in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern NORDRHEIN- WESTFALEN BREMEN SCHLESWIG- HOLSTEIN BADEN- WÜRTTEMBERG HESSEN HAMBURG NIEDERSACHSEN SACHSEN- ANHALT THÜ RINGEN
Die Evangelische in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern NORDRHEIN- WESTFALEN BREMEN SCHLESWIG- HOLSTEIN BADEN- WÜRTTEMBERG HESSEN HAMBURG NIEDERSACHSEN SACHSEN- ANHALT THÜ RINGEN
Spielhallenkonzessionen Spielhallenstandorte Geldspielgeräte in Spielhallen
 Alte Bundesländer 1.377 von 1.385 Kommunen Stand: 01.01.2012 13.442 Spielhallenkonzessionen 8.205 Spielhallenstandorte 139.351 Geldspielgeräte in Spielhallen Einwohner pro Spielhallenstandort 2012 Schleswig-
Alte Bundesländer 1.377 von 1.385 Kommunen Stand: 01.01.2012 13.442 Spielhallenkonzessionen 8.205 Spielhallenstandorte 139.351 Geldspielgeräte in Spielhallen Einwohner pro Spielhallenstandort 2012 Schleswig-
Epidemiologische Krebsregistrierung in Deutschland
 Epidemiologische Krebsregistrierung in Deutschland Methoden, Stand und Ergebnisse Alexander Katalinic 1, Joachim Bertz 2, Christa Stegmaier 3 1 Institut für Krebsepidemiologie e.v., Universität zu Lübeck,
Epidemiologische Krebsregistrierung in Deutschland Methoden, Stand und Ergebnisse Alexander Katalinic 1, Joachim Bertz 2, Christa Stegmaier 3 1 Institut für Krebsepidemiologie e.v., Universität zu Lübeck,
KHG-Investitionsförderung - Auswertung der AOLG-Zahlen für das Jahr
 KHG-Investitionsförderung - Auswertung der AOLG-Zahlen für das Jahr 2010 - Datengrundlage Die folgenden Darstellungen basieren auf den Ergebnissen einer Umfrage, die das niedersächsische Gesundheitsministerium
KHG-Investitionsförderung - Auswertung der AOLG-Zahlen für das Jahr 2010 - Datengrundlage Die folgenden Darstellungen basieren auf den Ergebnissen einer Umfrage, die das niedersächsische Gesundheitsministerium
1.4.1 Sterblichkeit in Ost- und Westdeutschland
 1.4.1 in Ost- und Westdeutschland Die ist im Osten noch stärker gesunken als im Westen. Die Gesamtsterblichkeit ist in Deutschland zwischen 1990 und 2004 bei Frauen und Männern deutlich zurückgegangen
1.4.1 in Ost- und Westdeutschland Die ist im Osten noch stärker gesunken als im Westen. Die Gesamtsterblichkeit ist in Deutschland zwischen 1990 und 2004 bei Frauen und Männern deutlich zurückgegangen
Deutschlandweite Prognose der bevölkerungsbezogenen Morbiditätserwartung für häufige Krebserkrankungen - Auswirkungen auf die Versorgung
 Deutschlandweite Prognose der bevölkerungsbezogenen Morbiditätserwartung für häufige Krebserkrankungen - Auswirkungen auf die Versorgung Studie im Auftrag der DGHO Jeanette Bahr, Ulrike Stentzel, Franziska
Deutschlandweite Prognose der bevölkerungsbezogenen Morbiditätserwartung für häufige Krebserkrankungen - Auswirkungen auf die Versorgung Studie im Auftrag der DGHO Jeanette Bahr, Ulrike Stentzel, Franziska
Die Evangelische Kirche in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern
 Die Evangelische in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern NORDRHEIN- WESTFALEN BREMEN SCHLESWIG- HOLSTEIN HESSEN HAMBURG NIEDERSACHSEN THÜ RINGEN SACHSEN- ANHALT MECKLENBURG-
Die Evangelische in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern NORDRHEIN- WESTFALEN BREMEN SCHLESWIG- HOLSTEIN HESSEN HAMBURG NIEDERSACHSEN THÜ RINGEN SACHSEN- ANHALT MECKLENBURG-
Klinisch-epidemiologische Daten zum Harnblasenkarzinom
 197 Wegener Folien-3/1_Y Freitag 24.1.23 22:15:52 Klinisch-epidemiologische Daten zum Harnblasenkarzinom G. Wegener Medizinische Hochschule Hannover, Tumorzentrum Amtliche Todesursachenstatistik Gestorbene
197 Wegener Folien-3/1_Y Freitag 24.1.23 22:15:52 Klinisch-epidemiologische Daten zum Harnblasenkarzinom G. Wegener Medizinische Hochschule Hannover, Tumorzentrum Amtliche Todesursachenstatistik Gestorbene
Armutsgefährdungsquoten nach Bundesländern (Teil 1)
 Armutsgefährdungsquoten nach Bundesländern (Teil 1) * um das mittlere Einkommen zu berechnen, wird der Median (Zentralwert) verwendet. Dabei werden hier alle Personen ihrem gewichteten Einkommen nach aufsteigend
Armutsgefährdungsquoten nach Bundesländern (Teil 1) * um das mittlere Einkommen zu berechnen, wird der Median (Zentralwert) verwendet. Dabei werden hier alle Personen ihrem gewichteten Einkommen nach aufsteigend
BAnz AT B3. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
3 Ergebnisse nach ICD-10
 Krebs in 19 3 Ergebnisse nach ICD-10 3.1 Krebs gesamt Tabelle 3.1.1 Übersicht über die wichtigsten epidemiologischen Maßzahlen 2007 2008 Prognose für 2012 Neuerkrankungen 243.900 215. 246.700 223. 258.000
Krebs in 19 3 Ergebnisse nach ICD-10 3.1 Krebs gesamt Tabelle 3.1.1 Übersicht über die wichtigsten epidemiologischen Maßzahlen 2007 2008 Prognose für 2012 Neuerkrankungen 243.900 215. 246.700 223. 258.000
Der Arzneimittelmarkt in Deutschland
 GAmSi GKV Arzneimittel Schnellinformation Der Arzneimittelmarkt in Deutschland Januar bis Dezember 2006 (Stand: 29. März 2007) Projektträger der GKV-Arzneimittel-Schnellinformation: AOK-Bundesverband BKK
GAmSi GKV Arzneimittel Schnellinformation Der Arzneimittelmarkt in Deutschland Januar bis Dezember 2006 (Stand: 29. März 2007) Projektträger der GKV-Arzneimittel-Schnellinformation: AOK-Bundesverband BKK
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um den Wirkstoff Daclatasvir wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Nutzenbewertung. von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V. Wirkstoff: Lomitapid. nach 2 Abs. 2 VerfO des G-BA
 Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Lomitapid nach 2 Abs. 2 VerfO des G-BA Datum der Veröffentlichung: 17. März 2014 Stand 12.03.2014 1 Lomitapid Zugelassenes
Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB V Wirkstoff: Lomitapid nach 2 Abs. 2 VerfO des G-BA Datum der Veröffentlichung: 17. März 2014 Stand 12.03.2014 1 Lomitapid Zugelassenes
Angst vor Krankheiten
 Angst vor Krankheiten Datenbasis: 3.019 Befragte *) Erhebungszeitraum: 22. Oktober bis 9. November 2012 statistische Fehlertoleranz: +/- 2,5 Prozentpunkte Auftraggeber: DAK-Gesundheit Eine übergroße Mehrheit
Angst vor Krankheiten Datenbasis: 3.019 Befragte *) Erhebungszeitraum: 22. Oktober bis 9. November 2012 statistische Fehlertoleranz: +/- 2,5 Prozentpunkte Auftraggeber: DAK-Gesundheit Eine übergroße Mehrheit
BAnz AT 06.04.2016 B7. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
0-14. Mortalitätsrate. und mehr 137,2 124,2 111,8. bis unter. bis unter 124,2 100,0 88,9. bis unter. bis unter 111,8 78,4 68,6
 EPIDEMIOLOGISCHE KREBSREGISTRIERUNG // EINZELNE KREBSARTEN ÖSOPHAGUS (C15) SITUATION IN DEUTSCHLAND INZIDENZ UND MORTALITÄT MÄNNER FRAUEN Altersstandardisierte Rate (/1.) Europastandard Inzidenz Saarland
EPIDEMIOLOGISCHE KREBSREGISTRIERUNG // EINZELNE KREBSARTEN ÖSOPHAGUS (C15) SITUATION IN DEUTSCHLAND INZIDENZ UND MORTALITÄT MÄNNER FRAUEN Altersstandardisierte Rate (/1.) Europastandard Inzidenz Saarland
Tragende Gründe. Vom 2. Februar 2017
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
Angst vor Krankheiten
 Angst vor Krankheiten Datenbasis: 3.086 Befragte *) Erhebungszeitraum: 31. Oktober bis 19. November 2013 statistische Fehlertoleranz: +/- 2,5 Prozentpunkte Auftraggeber: DAK-Gesundheit Die meisten Befragten
Angst vor Krankheiten Datenbasis: 3.086 Befragte *) Erhebungszeitraum: 31. Oktober bis 19. November 2013 statistische Fehlertoleranz: +/- 2,5 Prozentpunkte Auftraggeber: DAK-Gesundheit Die meisten Befragten
Der Arzneimittelmarkt in Deutschland
 GAmSi GKV Arzneimittel Schnellinformation Der Arzneimittelmarkt in Deutschland Januar bis Dezember 2007 (Stand: 24. April 2008) Projektträger der GKV-Arzneimittel-Schnellinformation: AOK-Bundesverband
GAmSi GKV Arzneimittel Schnellinformation Der Arzneimittelmarkt in Deutschland Januar bis Dezember 2007 (Stand: 24. April 2008) Projektträger der GKV-Arzneimittel-Schnellinformation: AOK-Bundesverband
2. Kurzbericht: Pflegestatistik 1999
 Statistisches Bundesamt Zweigstelle Bonn 2. Kurzbericht: Pflegestatistik 1999 - Pflege im Rahmen der Pflegeversicherung - Ländervergleich: Pflegebedürftige Bonn, im Oktober 2001 2. Kurzbericht: Pflegestatistik
Statistisches Bundesamt Zweigstelle Bonn 2. Kurzbericht: Pflegestatistik 1999 - Pflege im Rahmen der Pflegeversicherung - Ländervergleich: Pflegebedürftige Bonn, im Oktober 2001 2. Kurzbericht: Pflegestatistik
B E S C H L U S S. des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 362. Sitzung am 22. September 2015
 B E S C H L U S S des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 362. Sitzung am 22. September 2015 zu Empfehlungen zur Vereinbarung des Umfangs des nicht vorhersehbaren Anstiegs des morbiditätsbedingten
B E S C H L U S S des Bewertungsausschusses nach 87 Abs. 1 Satz 1 SGB V in seiner 362. Sitzung am 22. September 2015 zu Empfehlungen zur Vereinbarung des Umfangs des nicht vorhersehbaren Anstiegs des morbiditätsbedingten
Die Evangelische Kirche in Deutschland Die Gliedkirchen und ihre Lage in den Bundesländern
 Die Gliedkirchen und ihre Lage in den Bundesländern SCHLESWIG- HOLSTEIN MECKLENBURG- VORPOMMERN NORDRHEIN- WESTFALEN BREMEN BADEN- WÜRTTEMBERG Ku rhesse n- HAMBURG NIEDERSACHSEN SACHSEN- ANHALT THÜRINGEN
Die Gliedkirchen und ihre Lage in den Bundesländern SCHLESWIG- HOLSTEIN MECKLENBURG- VORPOMMERN NORDRHEIN- WESTFALEN BREMEN BADEN- WÜRTTEMBERG Ku rhesse n- HAMBURG NIEDERSACHSEN SACHSEN- ANHALT THÜRINGEN
Beschluss. I. Anlage XII wird wie folgt geändert:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Celgene GmbH Joseph-Wild-Straße München. Telefon: (089) PRESSEMITTEILUNG
 Celgene GmbH Joseph-Wild-Straße 20 81829 München Telefon: (089) 451519-010 info@celgene.de www.celgene.de PRESSEMITTEILUNG Zweiter AMNOG-Prozess für Orphan Drug IMNOVID (Pomalidomid) innerhalb der gesetzlichen
Celgene GmbH Joseph-Wild-Straße 20 81829 München Telefon: (089) 451519-010 info@celgene.de www.celgene.de PRESSEMITTEILUNG Zweiter AMNOG-Prozess für Orphan Drug IMNOVID (Pomalidomid) innerhalb der gesetzlichen
Innovative Arzneimittelversorgung im Spannungsfeld zwischen Nutzenbewertung und Sicherstellung des medizinischen Fortschritts
 Innovative Arzneimittelversorgung im Spannungsfeld zwischen Nutzenbewertung und Sicherstellung des medizinischen Fortschritts Roger Jaeckel, Leiter Gesundheitspolitik, GlaxoSmithKline Gemeinsame Fachtagung
Innovative Arzneimittelversorgung im Spannungsfeld zwischen Nutzenbewertung und Sicherstellung des medizinischen Fortschritts Roger Jaeckel, Leiter Gesundheitspolitik, GlaxoSmithKline Gemeinsame Fachtagung
 Tabelle 1: Verständnis der Bezeichnung "alkoholfreies Bier" Manche Lebensmittel werben mit dem Hinweis, dass ein Stoff nicht in dem Produkt enthalten ist (zum Beispiel "frei von..." oder "ohne..."). Bitte
Tabelle 1: Verständnis der Bezeichnung "alkoholfreies Bier" Manche Lebensmittel werben mit dem Hinweis, dass ein Stoff nicht in dem Produkt enthalten ist (zum Beispiel "frei von..." oder "ohne..."). Bitte
Ivacaftor (neues Anwendungsgebiet)
 IQWiG-Berichte Nr. 371 Ivacaftor (neues Anwendungsgebiet) Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung Auftrag: G15-13 Version: 1.0 Stand: 01.03.2016 Impressum Herausgeber: Institut für Qualität
IQWiG-Berichte Nr. 371 Ivacaftor (neues Anwendungsgebiet) Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung Auftrag: G15-13 Version: 1.0 Stand: 01.03.2016 Impressum Herausgeber: Institut für Qualität
Kinderarmut. Factsheet. Sachsen-Anhalt. Kinder im SGB-II-Bezug
 Factsheet Sachsen-Anhalt Kinderarmut Kinder im SGB-II-Bezug ABBILDUNG 1 Anteil der Kinder unter 18 Jahren in Familien im SGB-II-Bezug in den Jahren 2011 und 2015 im Vergleich 2011 2015 Saarland Rheinland-
Factsheet Sachsen-Anhalt Kinderarmut Kinder im SGB-II-Bezug ABBILDUNG 1 Anteil der Kinder unter 18 Jahren in Familien im SGB-II-Bezug in den Jahren 2011 und 2015 im Vergleich 2011 2015 Saarland Rheinland-
Aktuelle Statistiken aus der DCS Pflege
 Datenbestand Transparenzberichte in der DatenClearingStelle, Stand 04.07.2011 Gesamtübersicht Bezeichnung Aktuelle Statistiken aus der DCS Pflege Anzahl Anzahl Pflegeberichte 26108 Anzahl Registrierung
Datenbestand Transparenzberichte in der DatenClearingStelle, Stand 04.07.2011 Gesamtübersicht Bezeichnung Aktuelle Statistiken aus der DCS Pflege Anzahl Anzahl Pflegeberichte 26108 Anzahl Registrierung
Kurarztverträge - Kurärztliche Behandlung
 GB Abrechnung - Plausibilitätsprüfung Spitzenverband Bund der Krankenkassen Kassenärztliche Bundesvereinigung Seite: 2 1 Die (KÄV) Die (KÄV) betreute im Jahr 2008 bundesweit 1.100 Kurärzte * 373 Kurorte
GB Abrechnung - Plausibilitätsprüfung Spitzenverband Bund der Krankenkassen Kassenärztliche Bundesvereinigung Seite: 2 1 Die (KÄV) Die (KÄV) betreute im Jahr 2008 bundesweit 1.100 Kurärzte * 373 Kurorte
Dossierbewertung A16-10 Version 1.0 Ramucirumab (Kolorektalkarzinom)
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Ramucirumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Dossierbewertung A15-28 Version 1.0 Netupitant/Palonosetron Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Netupitant/Palonosetron gemäß 35a SGB V beauftragt. Die Bewertung erfolgte
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Netupitant/Palonosetron gemäß 35a SGB V beauftragt. Die Bewertung erfolgte
Unterversorgung psychisch kranker Kinder und Jugendlicher. Bestandsaufnahme/Handlungsbedarf
 Unterversorgung psychisch kranker Kinder und Jugendlicher Bestandsaufnahme/Handlungsbedarf Psychische Krankheiten bei Kindern und Jugendlichen Etwa jedes/r zwanzigste Kind und Jugendlicher in Deutschland
Unterversorgung psychisch kranker Kinder und Jugendlicher Bestandsaufnahme/Handlungsbedarf Psychische Krankheiten bei Kindern und Jugendlichen Etwa jedes/r zwanzigste Kind und Jugendlicher in Deutschland
Systematische Arzneimittelbewertung nach AMNOG
 Systematische Arzneimittelbewertung nach AMNOG Vereinbarung eines Erstattungsbetrages und das Schiedsstellenverfahren G-BA - Informationsveranstaltung 2. März 2011, Berlin Wolfgang Kaesbach Abteilung Arznei-
Systematische Arzneimittelbewertung nach AMNOG Vereinbarung eines Erstattungsbetrages und das Schiedsstellenverfahren G-BA - Informationsveranstaltung 2. März 2011, Berlin Wolfgang Kaesbach Abteilung Arznei-
BAnz AT B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die utzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Änderungstarifvertrag Nr. 1 zum Tarifvertrag über die Arbeitsbedingungen der Personenkraftwagenfahrer der Länder (Pkw-Fahrer-TV-L) vom 1.
 Änderungstarifvertrag Nr. 1 zum Tarifvertrag über die Arbeitsbedingungen der Personenkraftwagenfahrer der Länder (Pkw-Fahrer-TV-L) vom 1. März 2009 Zwischen der Tarifgemeinschaft deutscher Länder, vertreten
Änderungstarifvertrag Nr. 1 zum Tarifvertrag über die Arbeitsbedingungen der Personenkraftwagenfahrer der Länder (Pkw-Fahrer-TV-L) vom 1. März 2009 Zwischen der Tarifgemeinschaft deutscher Länder, vertreten
Beschluss. Vom 17. Juli 2014
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
BARMER GEK Arztreport 2016
 BARMER GEK Arztreport 2016 Infografiken Infografik 1 Chronische Schmerzen in Brandenburg und Berlin am häufigsten Infografik 2 Rücken: Schmerzproblem Nr. 1 Infografik 3 Hausarzt versorgt die meisten Patienten
BARMER GEK Arztreport 2016 Infografiken Infografik 1 Chronische Schmerzen in Brandenburg und Berlin am häufigsten Infografik 2 Rücken: Schmerzproblem Nr. 1 Infografik 3 Hausarzt versorgt die meisten Patienten
Gesetzliche Rahmenbedingungen der Telemedizin in Deutschland
 Gesetzliche Rahmenbedingungen der Telemedizin in Deutschland B. Schütze Klinikum der Johannes Gutenberg-Universität Mainz Klinik und Poliklinik für Radiologie Nationale und Europäische Gesetze, die bei
Gesetzliche Rahmenbedingungen der Telemedizin in Deutschland B. Schütze Klinikum der Johannes Gutenberg-Universität Mainz Klinik und Poliklinik für Radiologie Nationale und Europäische Gesetze, die bei
Altersarmuts-Atlas 2015 Zentrale Ergebnisse und Methodik.
 Altersarmuts-Atlas 2015 Zentrale Ergebnisse und Methodik. 19. August 2015 / 1 Inhaltsübersicht. 1. Management Summary 2. Altersarmuts-Index 3. Exklusiv-Befragung im Auftrag der Stuttgarter 4. Pressekontakt
Altersarmuts-Atlas 2015 Zentrale Ergebnisse und Methodik. 19. August 2015 / 1 Inhaltsübersicht. 1. Management Summary 2. Altersarmuts-Index 3. Exklusiv-Befragung im Auftrag der Stuttgarter 4. Pressekontakt
Die ärztliche Versorgung im ländlichen Raum: Herausforderungen und Zukunftskonzepte
 Die ärztliche Versorgung im ländlichen Raum: Herausforderungen und Zukunftskonzepte Oppurger Gespräch am 04.April 2011 Matthias Zenker Kassenärztliche Vereinigung Thüringen Folie 1 Eröffnung einer Praxis
Die ärztliche Versorgung im ländlichen Raum: Herausforderungen und Zukunftskonzepte Oppurger Gespräch am 04.April 2011 Matthias Zenker Kassenärztliche Vereinigung Thüringen Folie 1 Eröffnung einer Praxis
Meinungen zur Kernenergie
 Meinungen zur Kernenergie Datenbasis: 1.002 Befragte Erhebungszeitraum: 27. bis 29. August 2013 statistische Fehlertoleranz: +/- 3 Prozentpunkte Auftraggeber: DAtF e.v. 1. Einfluss der Energiepolitik auf
Meinungen zur Kernenergie Datenbasis: 1.002 Befragte Erhebungszeitraum: 27. bis 29. August 2013 statistische Fehlertoleranz: +/- 3 Prozentpunkte Auftraggeber: DAtF e.v. 1. Einfluss der Energiepolitik auf
Block 1: Block 2: Block 3: Block 1:
 Elternchance II - Kurse in 2016 Egestorf bei Hamburg Block 1: 26.05.2016 29.05.2016 Block 2: 14.07.2016 17.07.2016 Block 3: 28.09.2016 02.10.2016 Laubach bei Gießen (Hessen) Block 1: 16.06.2016 19.06.2016
Elternchance II - Kurse in 2016 Egestorf bei Hamburg Block 1: 26.05.2016 29.05.2016 Block 2: 14.07.2016 17.07.2016 Block 3: 28.09.2016 02.10.2016 Laubach bei Gießen (Hessen) Block 1: 16.06.2016 19.06.2016
Länderfinanzausgleich und Bundesergänzungszuweisungen (Teil 1)
 und (Teil 1) In absoluten Zahlen*, und Geberländer Empfängerländer -3.797-1.295 Bayern -2.765-1.433 Baden- Württemberg * Ausgleichszuweisungen des s: negativer Wert = Geberland, positiver Wert = Empfängerland;
und (Teil 1) In absoluten Zahlen*, und Geberländer Empfängerländer -3.797-1.295 Bayern -2.765-1.433 Baden- Württemberg * Ausgleichszuweisungen des s: negativer Wert = Geberland, positiver Wert = Empfängerland;
Pro-Kopf-Ausgaben für Kindertagesbetreuung: 2006 2014
 Pro-Kopf-Ausgaben für Kindertagesbetreuung: 2006 2014 Martin R. Textor Das Statistische Bundesamt stellt eine Unmenge an Daten zur Kindertagesbetreuung in der Bundesrepublik Deutschland zur Verfügung.
Pro-Kopf-Ausgaben für Kindertagesbetreuung: 2006 2014 Martin R. Textor Das Statistische Bundesamt stellt eine Unmenge an Daten zur Kindertagesbetreuung in der Bundesrepublik Deutschland zur Verfügung.
Bedarf an seniorengerechten Wohnungen in Deutschland
 Bedarf an seniorengerechten Wohnungen in Deutschland Entwicklung der Einwohnerzahl Deutschlands bis 2060 84 Mio. Personen 82 80 78 76 74 72 70 68 66 Variante1-W1 Variante 2 - W2 64 62 60 2010 2015 2020
Bedarf an seniorengerechten Wohnungen in Deutschland Entwicklung der Einwohnerzahl Deutschlands bis 2060 84 Mio. Personen 82 80 78 76 74 72 70 68 66 Variante1-W1 Variante 2 - W2 64 62 60 2010 2015 2020
Dossierbewertung A15-20 Version 1.0 Secukinumab Nutzenbewertung gemäß 35a SGB V
 2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Secukinumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
2 Nutzenbewertung 2.1 Kurzfassung der Nutzenbewertung Hintergrund Der G-BA hat das IQWiG mit der Nutzenbewertung des Wirkstoffs Secukinumab gemäß 35a SGB V beauftragt. Die Bewertung erfolgte auf Basis
Factsheet. Kinderarmut. Kinder im SGB-II-Bezug 14,3 14,7. Deutschland 19,3 17,0. Berlin. Brandenburg 20,1 16,9 12,4 13,2. Sachsen.
 Factsheet Baden-Württemberg Kinderarmut Kinder im SGB-II-Bezug ABBILDUNG 1 Anteil der Kinder unter 18 Jahren in Familien im 2011 2015 Nordrhein-Westfalen 15,0 17,6 Saarland 28,8 31,6 Bremen 10,7 11,5 Rheinland-
Factsheet Baden-Württemberg Kinderarmut Kinder im SGB-II-Bezug ABBILDUNG 1 Anteil der Kinder unter 18 Jahren in Familien im 2011 2015 Nordrhein-Westfalen 15,0 17,6 Saarland 28,8 31,6 Bremen 10,7 11,5 Rheinland-
Ermittlung der Bezugsgröße zur Berechnung der Arbeitslosenquoten
 Ermittlung der Bezugsgröße zur Berechnung der Arbeitslosenquoten Dokumentation für das Jahr 2006 Stand: 25.05.2007 Bundesagentur für Arbeit Datenzentrum Statistik Regensburger Straße 104 90478 Nürnberg
Ermittlung der Bezugsgröße zur Berechnung der Arbeitslosenquoten Dokumentation für das Jahr 2006 Stand: 25.05.2007 Bundesagentur für Arbeit Datenzentrum Statistik Regensburger Straße 104 90478 Nürnberg
13. Bericht über Struktur und Leistungszahlen der Herzkatheterlabors in der Bundesrepublik Deutschland
 13. Bericht über Struktur und Leistungszahlen der Herzkatheterlabors in der Bundesrepublik Deutschland herausgegeben vom Vorstand der Deutschen Gesellschaft für Kardiologie Herz- und Kreislaufforschung
13. Bericht über Struktur und Leistungszahlen der Herzkatheterlabors in der Bundesrepublik Deutschland herausgegeben vom Vorstand der Deutschen Gesellschaft für Kardiologie Herz- und Kreislaufforschung
Tabelle 1: Anzahl der Ärzte und Psychotherapeuten mit hälftiger Zulassung nach Kassenärztlichen
 Anlage Kassenärztliche Bundesvereinigung Tabelle 1: Anzahl der Ärzte und Psychotherapeuten mit hälftiger Zulassung nach Kassenärztlichen Vereinigungen Kassenärztliche Vereinigung Gesamt mit halber Vertragsärzte
Anlage Kassenärztliche Bundesvereinigung Tabelle 1: Anzahl der Ärzte und Psychotherapeuten mit hälftiger Zulassung nach Kassenärztlichen Vereinigungen Kassenärztliche Vereinigung Gesamt mit halber Vertragsärzte
Bildgebende Diagnostik in der Onkologie 20. Februar Epidemiologie und Prognose maligner Tumore
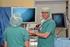 Bildgebende Diagnostik in der Onkologie 20. Februar 2010 Epidemiologie und Prognose maligner Tumore Prof. Dr. med. Hans-Werner Hense Institut für Epidemiologie Leiter Bereich Klinische Epidemiologie Universität
Bildgebende Diagnostik in der Onkologie 20. Februar 2010 Epidemiologie und Prognose maligner Tumore Prof. Dr. med. Hans-Werner Hense Institut für Epidemiologie Leiter Bereich Klinische Epidemiologie Universität
Beschluss. I. Die Anlage XII wird in alphabetischer Reihenfolge um die Wirkstoffkombination Ledipasvir/Sofosbuvir wie folgt ergänzt:
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
(BIAJ) An Interessierte Knochenhauerstraße 20-25
 Bremer Institut für Arbeit smarktforschung und Jugend berufshilfe e.v. () An Interessierte Knochenhauerstraße 20-25 Von Paul M. Schröder (Verfasser) email: institut-arbeit-jugend@t-online.de Seiten 6 Datum
Bremer Institut für Arbeit smarktforschung und Jugend berufshilfe e.v. () An Interessierte Knochenhauerstraße 20-25 Von Paul M. Schröder (Verfasser) email: institut-arbeit-jugend@t-online.de Seiten 6 Datum
Satzungsleistungen (soweit nicht anders vermerkt: Eheerfordernis & Altersgrenzen w25/40, m25/50)
 Kasse (Stand: 1.9.2016) AOKenn AOK Baden-Württemberg AOK Bayern AOK Bremen/ Bremerhaven AOK Hessen AOK NordOst Satzungsleistungen (soweit nicht anders vermerkt: Eheerfordernis & Altersgrenzen w25/40, m25/50)
Kasse (Stand: 1.9.2016) AOKenn AOK Baden-Württemberg AOK Bayern AOK Bremen/ Bremerhaven AOK Hessen AOK NordOst Satzungsleistungen (soweit nicht anders vermerkt: Eheerfordernis & Altersgrenzen w25/40, m25/50)
Listeriose-Infektionen Aktuelle Trends
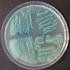 Listeriose-Infektionen Aktuelle Trends 2001-2006 Judith Koch Abteilung für Infektionsepidemiologie Lebensmittelbedingte Infektionskrankheiten, Zoonosen und Tropische Erkrankungen Übersicht Krankheitsbilder
Listeriose-Infektionen Aktuelle Trends 2001-2006 Judith Koch Abteilung für Infektionsepidemiologie Lebensmittelbedingte Infektionskrankheiten, Zoonosen und Tropische Erkrankungen Übersicht Krankheitsbilder
Tag der Marktforschung- Umfrage 2012
 Tag der Marktforschung- Umfrage 2012 Vergleich der bundesweiten und der regionalen Ergebnisse der Umfrage Wohlfühlfaktoren des Wohnorts Das wurde gefragt: Frage 1: Manche Menschen fühlen sich an ihrem
Tag der Marktforschung- Umfrage 2012 Vergleich der bundesweiten und der regionalen Ergebnisse der Umfrage Wohlfühlfaktoren des Wohnorts Das wurde gefragt: Frage 1: Manche Menschen fühlen sich an ihrem
Tragende Gründe. Vom 4. Februar 2016
 Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
Tragende Gründe zum Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen
HEK - Qualitätssicherungsmaßnahmen für Diabetes mellitus Typ-2 für 2015
 HEK - Qualitätssicherungsmaßnahmen für Diabetes mellitus Typ-2 für 2015 Bericht über die kassenseitig durchgeführten Qualitätssicherungsmaßnahmen im Rahmen des strukturierten Behandlungsprogramms (DMP)
HEK - Qualitätssicherungsmaßnahmen für Diabetes mellitus Typ-2 für 2015 Bericht über die kassenseitig durchgeführten Qualitätssicherungsmaßnahmen im Rahmen des strukturierten Behandlungsprogramms (DMP)
Führerschein mit 17 / Begleitetes Fahren Ergebnisse einer repräsentativen Befragung von Deutschen zwischen 14 und 64 Jahren
 Führerschein mit 17 / Begleitetes Fahren Ergebnisse einer repräsentativen Befragung von Deutschen zwischen 14 und 64 Jahren Inhalt 1 : Methode 2 : Sind Sie für den Führerschein ab 17 / Begleitetes Fahren?
Führerschein mit 17 / Begleitetes Fahren Ergebnisse einer repräsentativen Befragung von Deutschen zwischen 14 und 64 Jahren Inhalt 1 : Methode 2 : Sind Sie für den Führerschein ab 17 / Begleitetes Fahren?
Fragebogen zur Beschreibung einer Erkrankung und derer Behandlung für Patienten und Patientinnen bzw. Patientenorganisationen
 Beteiligung an der frühen Nutzenbewertung des IQWiG Fragebogen zur Beschreibung einer Erkrankung und derer Behandlung für Patienten und Patientinnen bzw. Patientenorganisationen (Stand: 01/2013) Fragebogen
Beteiligung an der frühen Nutzenbewertung des IQWiG Fragebogen zur Beschreibung einer Erkrankung und derer Behandlung für Patienten und Patientinnen bzw. Patientenorganisationen (Stand: 01/2013) Fragebogen
Kinderarmut. Factsheet. Nordrhein-Westfalen. Kinder im SGB-II-Bezug
 Factsheet Nordrhein-Westfalen Kinderarmut Kinder im SGB-II-Bezug ABBILDUNG 1 Anteil der Kinder unter 18 Jahren in Familien im SGB-II-Bezug in den Jahren 2011 und 2015 im Vergleich 2011 2015 Saarland Rheinland-
Factsheet Nordrhein-Westfalen Kinderarmut Kinder im SGB-II-Bezug ABBILDUNG 1 Anteil der Kinder unter 18 Jahren in Familien im SGB-II-Bezug in den Jahren 2011 und 2015 im Vergleich 2011 2015 Saarland Rheinland-
Papier verarbeitende Industrie
 Papier verarbeitende Industrie In den ausgewerteten Tarifbereichen arbeiten rund 74.400 Beschäftigte. 3 von 91 Vergütungsgruppen liegen zwischen 8 und 8,50. Alle anderen Gruppen liegen darüber, 78 Gruppen
Papier verarbeitende Industrie In den ausgewerteten Tarifbereichen arbeiten rund 74.400 Beschäftigte. 3 von 91 Vergütungsgruppen liegen zwischen 8 und 8,50. Alle anderen Gruppen liegen darüber, 78 Gruppen
Gesundheit in Deutschland, 2006
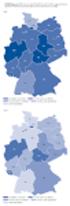 1.2.6 Krebs Zusammenfassung Krebsleiden sind nach den Herz-Kreislauf-Krankheiten die zweithäufigste Todesursache bei Frauen und Männern in Deutschland. Durch bösartige Tumoren gehen viele potenzielle Lebensjahre
1.2.6 Krebs Zusammenfassung Krebsleiden sind nach den Herz-Kreislauf-Krankheiten die zweithäufigste Todesursache bei Frauen und Männern in Deutschland. Durch bösartige Tumoren gehen viele potenzielle Lebensjahre
Bauen und Wohnen. Statistisches Bundesamt. Baugenehmigungen / Baufertigstellungen Lange Reihen z. T. ab 1949
 Statistisches Bundesamt Bauen und Wohnen Baugenehmigungen / Baufertigstellungen Lange Reihen z. T. ab 1949 2015 Erscheinungsfolge: jährlich Erschienen am 25.08.2016 Artikelnummer: 5311101157004 Ihr Kontakt
Statistisches Bundesamt Bauen und Wohnen Baugenehmigungen / Baufertigstellungen Lange Reihen z. T. ab 1949 2015 Erscheinungsfolge: jährlich Erschienen am 25.08.2016 Artikelnummer: 5311101157004 Ihr Kontakt
Ivacaftor (neues Anwendungsgebiet)
 IQWiG-Berichte Nr. 258 Ivacaftor (neues Anwendungsgebiet) Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung Auftrag: G14-09 Version: 1.0 Stand: 26.11.2014 Impressum Herausgeber: Institut für Qualität
IQWiG-Berichte Nr. 258 Ivacaftor (neues Anwendungsgebiet) Bewertung gemäß 35a Abs. 1 Satz 10 SGB V Dossierbewertung Auftrag: G14-09 Version: 1.0 Stand: 26.11.2014 Impressum Herausgeber: Institut für Qualität
