Zur Erinnerung. Spezifische Wärmekapazität. Spezifische Molwärme idealer Gase: C p und C V
|
|
|
- Chantal Rosenberg
- vor 6 Jahren
- Abrufe
Transkript
1 Zur Erinnerung Stichworte aus der 18. orlesung: Spezifische Wärmekapazität Spezifische Molwärme idealer Gase: C p und C C ½ f R C P C + R Spezifische Molwärme von Festkörpern (Dulong-Petit sches Gesetz) C mol 3 R Experimentalphysik I SS
2 Wärmekapazität von Festkörpern Wärmekapazität C: ΔQ C Δ ν C mol Δ mit ν m / M m / (N A A eilchen ) Q mc N A A mol eilchen Masse m für alle Proben gleich, emperaturerhöhung Δ gleich, C mol fast gleich, aber A Al < A Cu < A Pb (im erhältnis 27 : 63,5 : 207), so dass ΔQ Al > ΔQ Cu > ΔQ Pb. Experimentalphysik I SS
3 Energieumsatz bei Phasenübergängen Wenn E vib > E Bindung schmelzen, verdampfen ΔQ Aufbrechen von Bindungen Kondensation: Bildung von Bindungen E Bindung für Bindung A-B auf C übertragen Experimentalphysik I SS
4 Schmelzen, erdampfen Zufuhr von Energie ΔQ steigt. Wenn <E vib > E Bindung iele Bindungen brechen auf. Wenn Schmelzvorgang begonnen hat: const. im Körper (durch Wärmeleitung) bis Material vollständig geschmolzen. Experimentalphysik I SS
5 Schmelzen, erdampfen Energieverteilung N (E) festgelegt durch. Bindung wird gelöst für eilchen mit E > E B, deren Anzahl * N N ( E) de E B Wenn Energiezufuhr gestoppt: Schmelzen/erdampfen endet erst wenn E B N 1 ( E) de << 0 N 0 ( E) de Experimentalphysik I SS
6 Schmelzen, erdampfen Spezifische Schmelzwärme λ S : Spezifische erdampfungswärme λ : Energie, die zum Schmelzen von 1 kg eines Stoffes nötig ist: Q schmelz [J] λ S [J/kg] m [kg] Energie, die zum erdampfen von 1 kg eines Stoffes nötig ist: Q verdampf [J] λ [J/kg] m [kg] Experimentalphysik I SS
7 Wärmetransport Jeder sich selbst überlassene Körper mit der emperatur K tauscht mit seiner Umgebung so lange Energie aus, bis er die gleiche emperatur U wie seine Umgebung hat thermisches Gleichgewicht Konvektion: Wärmeleitung: durch ransport makroskopischer olumina: (Gase und Flüssigkeiten) durch ransport einzelner eilchen Wärmeleitung in Gasen durch Kopplung von Schwingungen und Energietransport im FK (bei Metallen i.w. durch Elektronen) Wäremstrahlung: durch Strahlung (einziger Mechanismus im akuum) Experimentalphysik I SS
8 Wärmetransport durch Konvektion Erwärmung von unten (a) >(b) da dρ/d<0 ρ(a)<ρ(b) Auftrieb untere Schichten steigen auf Durchmischung durch Konvektion Experimentalphysik I SS
9 Wärmetransport durch Konvektion Seewind: iefdruckgebiet: Experimentalphysik I SS
10 Wärmeleitung nur Energietransport, kein Massentransport, 1 und 2 < 1 durch Kontakt mit Wärmereservoirs fixiert. Wärmeleitzahl: angenommen: Wärmestrom nur in x-richtung, nach einiger Zeit stationärer Fall: dq dt dq dt const. λ q x 1 1 [ λ] W m K Experimentalphysik I SS
11 Wärmeleitung in Metallen Metall: freie Elektronen hohe elektrische Leitfähigkeit Elektronen: geringe Masse, starke Wechselwirkung mit Atomrümpfen dominanter Beitrag der Elektronen zur Wärmeleitung (Metall) Gute Wärmeleiter sind auch gute elektrische Leiter. Wiedemann-Franz- Gesetz: Zusammenhang von Wärmeleitzahl λ und elektrischer Leitfähigkeit σ: experimentell λ a σ heorie: 2 k a π 3 e 2 2 Experimentalphysik I SS
12 Wärmeleitung in Metallen Cu: Stahl: gute Wärmeleitung A steigt an, ΔQ fließt schnell nach E E steigt bald nach Beginn der Zufuhr an schlechte Wärmeleitung, ΔQ fließt nur langsam nach E A steigt stark an, erluste auf maßgeblicher Zeitskala, durch Ableitung in Umgebung: E steigt kaum an Wärmemenge: Q1 ( t) t 0 dq dt dt Gleichgewicht (ΔQ 1 ΔQ 2 ) wird für Stahl, wg. schlechterer Wärmeleitung i. vgl. zu Kupfer, erst bei höherer erreicht Experimentalphysik I SS
13 Wärmeleitung in Metallen Experimentalphysik I SS
14 Wärmeleitung in Flüssigkeiten Experimentalphysik I SS
15 Wärmeleitung in Gasen Ohne Diffusion: dw dt κ 1 ) κ ( 2 Wärmeübergangszahl Mit Diffusion: dw dt d λ λ dx Wärmeleitfähigkeit 1 λ 12 f k σ v ransport von Energie: kleine Masse großes <v> Draht glüht im oberen Bereich weniger stark, da dort höhere Dichte von H 2, daher bessere Wärmeleitung Experimentalphysik I SS
16 Wärmestrahlung Strahlungsgesetze: hier nur: elementare Zusammenhänge entwickelt von Max-Planck um 1900: war ein Schlüssel für die Entwicklung der Quantenmechanik Aussagen über: ariation von Intensität und Spektrum der Abstrahlung von einer Oberfläche mit der emperatur sowie Abhängigkeit von Oberflächen-Beschaffenheit Experimentalphysik I SS
17 Wärmestrahlung Wärmetransport durch Strahlung: Körper K, Wandung U Hochvakuum: kein -Ausgleich durch Wärmetransport über Atome/Moleküle Energietransport durch elektromagnetische Strahlung dadurch Ausgleich: K m und U m im thermischen Gleichgewicht muss ebensoviel Leistung (Strahlung) absorbiert wie emittiert werden. Experimentalphysik I SS
18 Wärmestrahlung Abhängigkeit von der Oberflächenbeschaffenheit: abgestrahlte Leistung I() dw()/dt Beobachtung: I dunkel/rauh () > I hell/blank () I( 2 ) > I( 1 ) für 2 > 1 Experimentalphysik I SS
19 Wärmestrahlung von Fläche df in Raumwinkel dω [pro m 2 >> 1 Sterad] abgestrahlte Leistung dw/dt: Emissionsvermögen E*(): dw dt J E *( ) df dω, [ E *( )] 2 S m Sr Absorptionsvermögen A(): W A W absorbiert auftreffend A ist dimensionslos! es gilt (Beobachtung): E *( ) A( ) K( ) erhältnis ist nur von abhängig! Schwarzer Körper: A() 1 für alle Frequenzen (Wellenlängen) Experimentalphysik I SS
20 Wärmestrahlung Realisierung eines schwarzen Körpers: Realisierung einer Fläche mit den Eigenschaften schwarzer Körper im Sinne der Strahlungsgesetze: kleines Loch in der Wandung eines Hohlraumes schwarzer Körper Fläches des Loches Das spektrale Emissionsvermögen E* eines schwarzen Körpers ist identisch mit der spektralen Strahlungsdichte S* der Hohlraumstrahlung. Experimentalphysik I SS
21 Wärmestrahlung Strahlungsformel von Max Planck: Max Planck um 1900: spektrale Energiedichte der Startpunkt zur Entwicklung der Quantenmechanik Aussagen über: emperatur-ariation von Intensität und Spektrum der Abstrahlung einer Oberfläche sowie Abhängigkeit der Strahlung von der Oberflächen- Beschaffenheit Experimentalphysik I SS
22 Wärmestrahlung Strahlungsformel von Max Planck: 2 8πν ρ( ν ) 3 c hν e hν k 1 1 Statistisches Gewicht 8π hc ρ( λ) 5 λ e Energie pro Quant hν 1 hc kλ 1 Besetzungswahrscheinlichkeit W(ν,Τ) ρ(λ) bzw. ρ(ν): spektrale Energiedichte ρ(λ)dλ bzw. ρ(ν)dν: Energiedichte im Spektral- Interval dλ bzw. dν Zunahme des Integrals über K(λ) geregelt durch: Stefan-Boltzmann-Gesetz erschiebung des Maximums geregelt durch: Wien sches erschiebungsgesetz Experimentalphysik I SS
23 Wärmestrahlung Stefan-Boltzman: dw dt 4 σ S S strahlende Fläche, 2 σ W/(m 2 K 4 ) dw 2 ( A 1 m, 300 K ) 470 W dt 4 4 dw2 dw1 2 1, , 10 dt dt z. B. 300 K (27 C), 533 K (260 C) 1 Wien sches erschiebungsgesetz: λ max b di( λ) 0 für λ λ dλ λ (300 K) 10 µm max max, b 2, m K Experimentalphysik I SS
24 Konsequenzen der Wärmestrahlung Lichtmühle: Übertrag von Photonen-Impulsen?? Experimentalphysik I SS
25 Konsequenzen der Wärmestrahlung Lichtmühle: Übertrag von eilchen-impulsen Experimentalphysik I SS
26 Konsequenzen der Wärmestrahlung Photonenimpuls: E p Z ph ph ph p F t F h ν " m " m dn F ph h ν " c c 2 c photon dt blank F ph F " c blank schwarz 2 Z h λ pro Zeiteinheit auftreffende Photonen 2Z ph h, λ h λ ph Photonenenergie Photonenimpuls F schwarz Z ph h λ Drehung schwarze Seite voran Experimentalphysik I SS
27 Konsequenzen der Wärmestrahlung eilchenimpuls: eilchen aus dem Gasvolumen landen auf der Fläche der Drehflügel mit Impuls <p> p m v( gas ) Kraftübertrag beim Landen identisch für beide Seiten: landen d planden F Z ph m v( gas ) dt Kraftübertrag beim Starten : Start mit F start F ph start schwarz v( Oberfläche F start blank ) : Oberfläche Z m v( ) > schwarz > blank gas Drehung schwarze Seite rückwärts Experimentalphysik I SS
28 Wärme-Isolierung Strahlungsabschirmung und erwendung von Materialien mit geringer Wärmeleitung Experimentalphysik I SS
29 Die Hauptsätze der Wärmelehre hermodynamisches Gleichgewicht: die erteilungsfunktionen F (X) (X Energien, Impulse, etc. ) sind durch festgelegt Zustandsgrößen: {Z} (p,, ) beschreiben im thermodynamischen Gleichgewicht den Zustand des Systems (eindeutig) Zustand ist stationär, wenn für die Zustandsgrößen Z gilt dz/dt 0 Hauptsätze: Beschreibung der Änderung der Zustandsgrößen p, und bei Aufnahme/Abgabe von Energie zunächst betrachtet: ideales Gas Experimentalphysik I SS
30 Die Hauptsätze der Wärmelehre 1. Hauptsatz: (alternative Formulierungen) 2. Hauptsatz: (alternative Formulierungen) 3. Hauptsatz: Die Gesamtenergie (inklusive Wärmeenergie) bleibt bei einem Prozess erhalten. Es gibt keine Maschine, die mehr Energie erzeugt als eingesetzt wird (es gibt kein perpetuum mobile 1. Art). Diese Aussage ist nicht beweisbar, reine Erfahrungssache! Der Wirkungsgrad η (η nutzbare Arbeit/eingesetzte Energie) einer Wärmekraftmaschine ist η < 1 Es gibt keine periodisch arbeitende Maschine, deren Wirkungsgrad höher ist als derjenige der Carnot Maschine Es gibt keine periodisch arbeitende Maschine,welche ohne Energiezufuhr ein Wärmereservoir abkühlt und die dabei entzogene Energie vollständig in mechanische Energie umwandelt (kein perpetuum mobile 2. Art) Es ist prinzipiell unmöglich, den absoluten Nullpunkt der emperatur zu erreichen. Experimentalphysik I SS
31 Grundlagen, Definitionen und Bezeichnungen Zustandsgleichung: Innere Energie: Arbeit: p ν R 1 U ν f R, 2 dw p d C U Kompression: d < 0 dw > 0 dem System zugeführte Energie (Arbeit) wird positiv gerechnet Expansion: d > 0 dw < 0 vom System geleistete Arbeit wird negativ gerechnet Zustandsänderungen: Bezeichnung von Zustandsänderungen: const. isotherm p const. isobar const. isochor p(ν,,) Experimentalphysik I SS
32 Erster Hauptsatz der hermodynamik (Erhaltung der Energie) 1. Hauptsatz: ΔU ΔQ + ΔW Die Erhöhung der inneren Energie ist gegeben durch die zugeführte Wärmemenge ΔQ und die durch mechanische Arbeit ΔW zugeführte Energie Expansion: ΔW < 0, Kompression: ΔW > 0 1. Hauptsatz für ideales Gas in differentieller Form: in differentiellen Größen geschrieben: du dq - p d (1.Hauptsatz, ideales Gas) gilt nicht allgemein für reales Gas, da z.b. Δp durch ΔN (Kondensation, erdampfung) nicht berücksichtigt Experimentalphysik I SS
33 Erster Hauptsatz: Konsequenzen Isochorer Prozess: du dq p d Isobarer Prozess: isochorer Prozess: d 0 du dq zugeführte Wärmeenergie geht vollständig in die Änderung der inneren Energie U dq du C d, C dp 0 dq du + p d dq C d Enthalpie H: Def.: H U + p d, Bezogen auf ein Mol: H C U p + p H U + R + R C p + R dh dq du dh + p d + dp (für dp 0) C p H H Maß für die Energie eines therodynamischen Systems p Experimentalphysik I SS
34 Erster Hauptsatz: Konsequenzen du Isothermer Prozess: 0 dq p d Wärmeleitung o enger Kontakt mit Wärmereservoir im Kolben und im Reservoir gleich p o, o, o Q p o + p, o +, o o Kompressionsarbeit W p d Wärmemenge Q W wird über Wärmeleitung an Reservoir abgeführt bis Kolben o Experimentalphysik I SS
35 Experimentalphysik I SS Erster Hauptsatz: Konsequenzen Isothermer Prozess: d p dq du ln R d R d p W R p R p dw dq mit ln R W
36 Experimentalphysik I SS Erster Hauptsatz: Konsequenzen Adiabatischer Prozess: ( ) ( )... ln. ln ln. ln ln 0 const const const const const R C d R d C d R d C R p d C d p du d p du dq p p C C C C C C C R C R C const p f f R f R R f C C const p + + κ κ κ da R p Poisson sche Gleichungen/Adiabaten- Gleichungen:
37 Erster Hauptsatz: Konsequenzen Adiabatischer Prozess: In der hermodynamik bedeutet: adiabatisch meist schneller Prozess, damit ΔQ (erlust durch Wärmeleitung) klein. Später (in Quantenmechanik) bedeutet adiabatisch oft langsamer Prozess (kein Energieverlust durch Übergang in anderen Energiezustand) (immer: ΔQ 0!) Experimentalphysik I SS
38 Isothermer und adiabatischer Prozess pp(): Isothermen und Adiabaten in einem p--diagramm isotherme Änderung: adiabatische Änderung: p R 0 pisotherm ( ) R κ κ κ p0 0 p const. ( p0 0 ) padiabatisch ( ) κ p() Druck ändert sich mit bei adiabtischem Prozess (dq 0) schneller als bei isothermem Prozess (du 0), da: d < 0: Kompressionsarbeit, steigt p steigt d > 0: Expansionsarbeit, sinkt p sinkt 0 Experimentalphysik I SS
39 Isothermer und adiabatischer Prozess Isothermer Prozess: organg (Δ) langsam : ΔW: Kompressions-/Expansionsarbeit ΔQ: Erwärmung/Abkühlung vollständiger Ausgleich durch Wärmebad adiabatischer Prozess: organg (Δ) schnell : ΔW: Kompressions-/Expansionsarbeit ΔQ: Erwärmung/Abkühlung 1 z. B.: kein Ausgleich durch Wärme-Abfuhr/-Zufuhr κ , κ 1 0 0,4 κ ( N 0 2 ) 1 2, ,4 0 1 κ K K Experimentalphysik I SS
40 Kreisprozesse p 1, 1, 1 p 1 p 2 p 2, 2, 1 p 4 p 3 p 3, 3, 2 Ein thermodynamisches System durchläuft verschiedene Zustände mit unterschiedlichen Zustandsgrößen und kehrt in den Ausgangszustand (identische Zustandsgrößen) zurück. Es gibt reversible und irreversible Kreisprozessse Experimentalphysik I SS
Zur Erinnerung V M. Stichworte aus der 17. Vorlesung: Viskosität. laminare Strömung, Gesetz von Hagen- Poiseuille. Gleichungen der Strömungslehre
 Zur Erinnerung Stichworte aus der 17. Vorlesung: Viskosität laminare Strömung, Gesetz von Hagen- Poiseuille F R = η u dv V M ρ = t π p = ρ R 8η z 4 Gleichungen der Strömungslehre Temperatur, Temperaturskalen,
Zur Erinnerung Stichworte aus der 17. Vorlesung: Viskosität laminare Strömung, Gesetz von Hagen- Poiseuille F R = η u dv V M ρ = t π p = ρ R 8η z 4 Gleichungen der Strömungslehre Temperatur, Temperaturskalen,
Zur Erinnerung. Wärmetransport durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung. Planck sches Strahlungsgesetz. Stefan-Boltzman-Gesetz
 Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Zur Erinnerung Stichworte aus der 9. orlesung: Wärmetransort durch: -Wärmekonvektion -Wärmestrahlung -Wärmeleitung Planck sches Strahlungsgesetz Stefan-Boltzman-Gesetz Wiensches erschiebungsgesetz Hautsätze
Energieumsatz bei Phasenübergang
 Energieumsatz bei Phasenübergang wenn E Vib > E Bindung schmelzen verdampfen Q Aufbrechen von Bindungen Kondensation: Bildung von Bindungen E Bindung Q E Transl. E Bindung für System A B durch Stöße auf
Energieumsatz bei Phasenübergang wenn E Vib > E Bindung schmelzen verdampfen Q Aufbrechen von Bindungen Kondensation: Bildung von Bindungen E Bindung Q E Transl. E Bindung für System A B durch Stöße auf
Zusammenfassung: Zustandsänderungen (jeweils für 1 mol)
 Zusammenfassung: Zustandsänderungen (jeweils für mol) dq du p d isochor ( = const) isochor : dq du d 0 C d keine mechanische rbeit isobar (p = const) isotherm ( = const) adiabatisch (Q = const) isobar
Zusammenfassung: Zustandsänderungen (jeweils für mol) dq du p d isochor ( = const) isochor : dq du d 0 C d keine mechanische rbeit isobar (p = const) isotherm ( = const) adiabatisch (Q = const) isobar
Der 1. Hauptsatz. Energieerhaltung:
 Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
Wärmelehre Wärme als Energie-Form
 Wärmelehre Wärme als Energie-Form Joule's Vorrichtung zur Messung des mechanischen Wärme-Äquivalents alte Einheit: 1 cal = 4.184 J 1 kcal Wärme erwärmt 1 kg H 2 O um 1 K Wird einem Körper mit der Masse
Wärmelehre Wärme als Energie-Form Joule's Vorrichtung zur Messung des mechanischen Wärme-Äquivalents alte Einheit: 1 cal = 4.184 J 1 kcal Wärme erwärmt 1 kg H 2 O um 1 K Wird einem Körper mit der Masse
10. Thermodynamik Der erste Hauptsatz Der zweite Hauptsatz Thermodynamischer Wirkungsgrad Der Carnotsche Kreisprozess
 Inhalt 10.10 Der zweite Hauptsatz 10.10.1 Thermodynamischer Wirkungsgrad 10.10.2 Der Carnotsche Kreisprozess Für kinetische Energie der ungeordneten Bewegung gilt: Frage: Frage: Wie kann man mit U Arbeit
Inhalt 10.10 Der zweite Hauptsatz 10.10.1 Thermodynamischer Wirkungsgrad 10.10.2 Der Carnotsche Kreisprozess Für kinetische Energie der ungeordneten Bewegung gilt: Frage: Frage: Wie kann man mit U Arbeit
II. Wärmelehre. II.2. Die Hauptsätze der Wärmelehre. Physik für Mediziner 1
 II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
Kapitel IV Wärmelehre und Thermodynamik
 Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas - makroskopisch e) Das reale Gas / Phasenübergänge f) Das ideale Gas mikroskopisch g)
Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas - makroskopisch e) Das reale Gas / Phasenübergänge f) Das ideale Gas mikroskopisch g)
Versuch: Sieden durch Abkühlen
 ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
Zur Erinnerung. p R 8
 Zur Erinnerung Stichworte aus der 17. Vorlesung: Viskosität laminare Strömung, Gesetz von Hagen- Poiseuille F R V M t u dv R 8 z 4 Gleichungen der Strömungslehre Temeratur, Temeraturskalen, thermische
Zur Erinnerung Stichworte aus der 17. Vorlesung: Viskosität laminare Strömung, Gesetz von Hagen- Poiseuille F R V M t u dv R 8 z 4 Gleichungen der Strömungslehre Temeratur, Temeraturskalen, thermische
Hauptsatz der Thermodynamik
 0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
Ferienkurs Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen
 Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
Temperatur. Temperaturmessung. Grundgleichung der Kalorik. 2 ² 3 2 T - absolute Temperatur / ºC T / K
 Temperatur Temperatur ist ein Maß für die mittlere kinetische Energie der Teilchen 2 ² 3 2 T - absolute Temperatur [ T ] = 1 K = 1 Kelvin k- Boltzmann-Konst. k = 1,38 10-23 J/K Kelvin- und Celsiusskala
Temperatur Temperatur ist ein Maß für die mittlere kinetische Energie der Teilchen 2 ² 3 2 T - absolute Temperatur [ T ] = 1 K = 1 Kelvin k- Boltzmann-Konst. k = 1,38 10-23 J/K Kelvin- und Celsiusskala
13.Wärmekapazität. EP Vorlesung 14. II) Wärmelehre
 13.Wärmekapazität EP Vorlesung 14 II) Wärmelehre 10. Temperatur und Stoffmenge 11. Ideale Gasgleichung 12. Gaskinetik 13. Wärmekapazität 14. Hauptsätze der Wärmelehre Versuche: Mechanisches Wärmeäquivalent
13.Wärmekapazität EP Vorlesung 14 II) Wärmelehre 10. Temperatur und Stoffmenge 11. Ideale Gasgleichung 12. Gaskinetik 13. Wärmekapazität 14. Hauptsätze der Wärmelehre Versuche: Mechanisches Wärmeäquivalent
Beispiel für ein thermodynamisches System: ideales Gas (Edelgas)
 10. Hauptsätze tze der Wärmelehre Thermodynamik: zunächst: Klassische Mechanik punktförmiger Teilchen, starrer und deformierbarer Körper aber: Bewegungsgleichungen für N=10 23 Teilchen mit 6N ariablen
10. Hauptsätze tze der Wärmelehre Thermodynamik: zunächst: Klassische Mechanik punktförmiger Teilchen, starrer und deformierbarer Körper aber: Bewegungsgleichungen für N=10 23 Teilchen mit 6N ariablen
Ferienkurs Experimentalphysik II Elektro- und Thermodynamik. Thermodynamik Teil II. 12. September 2011 Michael Mittermair
 Ferienkurs Experimentalphysik II Elektro- und Thermodynamik Thermodynamik Teil II 12. September 2011 Michael Mittermair Inhaltsverzeichnis 1 Allgemeines 3 1.1 Kategorisierung von Systemen..................
Ferienkurs Experimentalphysik II Elektro- und Thermodynamik Thermodynamik Teil II 12. September 2011 Michael Mittermair Inhaltsverzeichnis 1 Allgemeines 3 1.1 Kategorisierung von Systemen..................
4 Hauptsätze der Thermodynamik
 I Wärmelehre -21-4 Hauptsätze der hermodynamik 4.1 Energieformen und Energieumwandlung Innere Energie U Die innere Energie U eines Körpers oder eines Systems ist die gesamte Energie die darin steckt. Es
I Wärmelehre -21-4 Hauptsätze der hermodynamik 4.1 Energieformen und Energieumwandlung Innere Energie U Die innere Energie U eines Körpers oder eines Systems ist die gesamte Energie die darin steckt. Es
Wärmelehre Zustandsänderungen ideales Gases
 Wärmelehre Zustandsänderungen ideales Gases p Gas-Gleichung 1.Hauptsatz p V = N k B T U Q W p 1 400 1 isobar 300 200 isochor isotherm 100 p 2 0 2 adiabatisch 0 1 2 3 4 5 V V 2 1 V Bemerkung: Mischung verschiedener
Wärmelehre Zustandsänderungen ideales Gases p Gas-Gleichung 1.Hauptsatz p V = N k B T U Q W p 1 400 1 isobar 300 200 isochor isotherm 100 p 2 0 2 adiabatisch 0 1 2 3 4 5 V V 2 1 V Bemerkung: Mischung verschiedener
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Der Zustand eines Systems ist durch Zustandsgrößen charakterisiert.
 Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Isotherme 3. 4 Adiabate 2 T 1. Adiabate Isotherme T 2. Arbeit nach außen = eingeschlossene Kurve
 Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
22. Entropie; Zweiter Hauptsatz der Wärmelehre
 22. Entropie; Zweiter Hauptsatz der Wärmelehre Nicht alle Prozesse, die dem Energiesatz genügen, finden auch wirklich statt Beispiel: Um alle Energieprobleme zu lösen, brauchte man keine Energie aus dem
22. Entropie; Zweiter Hauptsatz der Wärmelehre Nicht alle Prozesse, die dem Energiesatz genügen, finden auch wirklich statt Beispiel: Um alle Energieprobleme zu lösen, brauchte man keine Energie aus dem
Wärme als Energieform
 Wärme als Energieform Wärme bedeutet ungeordnete thermische Bewegung der Atome bzw. Moleküle Gase und Flüssigkeiten Festkörper Translation, Rotation und innere Schwingung von Molekülen Schwingung aller
Wärme als Energieform Wärme bedeutet ungeordnete thermische Bewegung der Atome bzw. Moleküle Gase und Flüssigkeiten Festkörper Translation, Rotation und innere Schwingung von Molekülen Schwingung aller
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
3 Diskussion und Beispiele
 Woche 2 3 Diskussion und Beispiele 31 Abhängigkeit zwischen kalorischer und thermischer Zustandsgleichung Die kalorische und die thermische Zustandsgleichungen sind nicht unabhängig Aus den Integrabilitätsbedingungen
Woche 2 3 Diskussion und Beispiele 31 Abhängigkeit zwischen kalorischer und thermischer Zustandsgleichung Die kalorische und die thermische Zustandsgleichungen sind nicht unabhängig Aus den Integrabilitätsbedingungen
Formelsammlung. Experimentalphysik II. Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester Pascal Del Haye 27.
 Formelsammlung Experimentalphysik II Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester 2003 Pascal Del Haye www.delhaye.de 27. Juli 2003 Inhaltsverzeichnis Thermodynamik 3. Ideale Gasgleichung........................
Formelsammlung Experimentalphysik II Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester 2003 Pascal Del Haye www.delhaye.de 27. Juli 2003 Inhaltsverzeichnis Thermodynamik 3. Ideale Gasgleichung........................
Thermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden.
 Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Übungen zu Experimentalphysik 2 für MSE
 Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
8.3 Hauptsätze der Thermodynamik Der erste Hauptsatz (Energieerhaltung)
 Experimentalphysik I ortmund S0/ Shaukat Khan @ - ortmund. de Kapitel 8 8. Hauptsätze der hermodynamik 8.. er erste Hauptsatz (Energieerhaltung) Zunahme an innerer Energie = zugeführte ärmemenge + zugeführte
Experimentalphysik I ortmund S0/ Shaukat Khan @ - ortmund. de Kapitel 8 8. Hauptsätze der hermodynamik 8.. er erste Hauptsatz (Energieerhaltung) Zunahme an innerer Energie = zugeführte ärmemenge + zugeführte
Carnotscher Kreisprozess
 Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
10. Thermodynamik Wärmetransport Wämeleitung Konvektion Wärmestrahlung Der Treibhauseffekt. 10.
 10.5 Wärmetransport Inhalt 10.5 Wärmetransport 10.5.1 Wämeleitung 10.5.2 Konvektion 10.5.3 Wärmestrahlung 10.5.4 Der Treibhauseffekt 10.5.1 Wärmeleitung 10.5 Wärmetransport an unterscheidet: Wärmeleitung
10.5 Wärmetransport Inhalt 10.5 Wärmetransport 10.5.1 Wämeleitung 10.5.2 Konvektion 10.5.3 Wärmestrahlung 10.5.4 Der Treibhauseffekt 10.5.1 Wärmeleitung 10.5 Wärmetransport an unterscheidet: Wärmeleitung
Kapitel 9 Wä l rme h e re 1
 Kapitel 9 Wärmelehre 1 zur Erinnerung : Kinetische Gastheorie aus mikroskopischer heorie folgte : 3 1 E k m v E kin d.h. emperatur ist definiert über (mittlere) eilchenbewegung Definition eines absoluten
Kapitel 9 Wärmelehre 1 zur Erinnerung : Kinetische Gastheorie aus mikroskopischer heorie folgte : 3 1 E k m v E kin d.h. emperatur ist definiert über (mittlere) eilchenbewegung Definition eines absoluten
13.Wärmekapazität. EP Vorlesung 15. II) Wärmelehre
 13.Wärmekapazität EP Vorlesung 15 II) Wärmelehre 10. Temperatur und Stoffmenge 11. Ideale Gasgleichung 12. Gaskinetik 13. Wärmekapazität 14. Hauptsätze der Wärmelehre Versuche: Wärmekapazität von Festkörpern
13.Wärmekapazität EP Vorlesung 15 II) Wärmelehre 10. Temperatur und Stoffmenge 11. Ideale Gasgleichung 12. Gaskinetik 13. Wärmekapazität 14. Hauptsätze der Wärmelehre Versuche: Wärmekapazität von Festkörpern
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Thermodynamik. Thermodynamics. Markus Arndt. Quantenoptik, Quantennanophysik und Quanteninformation Universität Wien January 2008
 Thermodynamik Thermodynamics Markus Arndt Quantenoptik, Quantennanophysik und Quanteninformation Universität Wien January 2008 Die Hauptsätze der Thermodynamik & Anwendungen in Wärmekraft und Kältemaschinen
Thermodynamik Thermodynamics Markus Arndt Quantenoptik, Quantennanophysik und Quanteninformation Universität Wien January 2008 Die Hauptsätze der Thermodynamik & Anwendungen in Wärmekraft und Kältemaschinen
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #16 am 0.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #16 am 0.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Kapitel 9 Wä l rme h e re 1
 Kapitel 9 Wärmelehre 1 zur Erinnerung : Kinetische Gastheorie aus mikroskopischer heorie folgte : 3 1 E k m v E kin d.h. emperatur ist definiert über (mittlere) eilchenbewegung Definition eines absoluten
Kapitel 9 Wärmelehre 1 zur Erinnerung : Kinetische Gastheorie aus mikroskopischer heorie folgte : 3 1 E k m v E kin d.h. emperatur ist definiert über (mittlere) eilchenbewegung Definition eines absoluten
13.5 Photonen und Phononen
 Woche 11 13.5 Photonen und Phononen Teilchen mit linearem Dispersionsgesetz: E = c p, c - Ausbreitungsgeschwindigkeit (Licht- oder Schallgeschwindigkeit). 13.5.1 Photonen Quantisierung der Eigenschwingungen
Woche 11 13.5 Photonen und Phononen Teilchen mit linearem Dispersionsgesetz: E = c p, c - Ausbreitungsgeschwindigkeit (Licht- oder Schallgeschwindigkeit). 13.5.1 Photonen Quantisierung der Eigenschwingungen
Physik I TU Dortmund WS2017/18 Gudrun Hiller Shaukat Khan Kapitel 6
 Physik I U Dortmund WS7/8 Gudrun Hiller Shaukat Khan Kapitel Carnotscher Kreisprozess Modell eines Kreisprozesses (Gedankenexperiment). Nicht nur von historischem Interesse (Carnot 84), sondern auch Prozess
Physik I U Dortmund WS7/8 Gudrun Hiller Shaukat Khan Kapitel Carnotscher Kreisprozess Modell eines Kreisprozesses (Gedankenexperiment). Nicht nur von historischem Interesse (Carnot 84), sondern auch Prozess
9. Wärmelehre. 9.5 Wärmetransport Wärmeleitung Konvektion Der Treibhauseffekt. 9. Wärmelehre Physik für Informatiker
 9. Wärmelehre 9.5 Wärmetransport 9.5.1 Wärmeleitung 9.5.2 Konvektion 953 9.5.3 Wärmestrahlung 9.5.4 Der Treibhauseffekt 9.5 Wärmetransport Man unterscheidet: Wärmeleitung Energietransport durch Wechselwirkung
9. Wärmelehre 9.5 Wärmetransport 9.5.1 Wärmeleitung 9.5.2 Konvektion 953 9.5.3 Wärmestrahlung 9.5.4 Der Treibhauseffekt 9.5 Wärmetransport Man unterscheidet: Wärmeleitung Energietransport durch Wechselwirkung
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik -. Hauptsatz der Thermodynamik - Prof. Dr. Ulrich Hahn WS 2008/09 Energieerhaltung Erweiterung des Energieerhaltungssatzes der Mechanik Erfahrung: verschiedene
Physik III im Studiengang Elektrotechnik -. Hauptsatz der Thermodynamik - Prof. Dr. Ulrich Hahn WS 2008/09 Energieerhaltung Erweiterung des Energieerhaltungssatzes der Mechanik Erfahrung: verschiedene
8.1. Kinetische Theorie der Wärme
 8.1. Kinetische Theorie der Wärme Deinition: Ein ideales Gas ist ein System von harten Massenpunkten, die untereinander und mit den Wänden elastische Stöße durchühren und keiner anderen Wechselwirkung
8.1. Kinetische Theorie der Wärme Deinition: Ein ideales Gas ist ein System von harten Massenpunkten, die untereinander und mit den Wänden elastische Stöße durchühren und keiner anderen Wechselwirkung
3 Der 1. Hauptsatz der Thermodynamik
 3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
Der Zweite Hauptsatz der TD- Lernziele
 Der Zweite Hauptsatz der D- Lernziele o Einleitung o Entropie (Definition, Entropie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hauptzatz der D o Die Entropieänderungen bei speziellen
Der Zweite Hauptsatz der D- Lernziele o Einleitung o Entropie (Definition, Entropie als Zustandsfunktion, die Clausius sche Ungleichung) o Der Zweite Hauptzatz der D o Die Entropieänderungen bei speziellen
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 8 Lösungsvorschlag
 T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik III (heorie F Statistische Mechanik) SS 17 Prof. Dr. Alexander Mirlin Blatt 2 PD Dr. Igor Gornyi,
Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik III (heorie F Statistische Mechanik) SS 17 Prof. Dr. Alexander Mirlin Blatt 2 PD Dr. Igor Gornyi,
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 ladimir Dyakonov #0 am 4.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E43, Tel. 888-5875,
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 ladimir Dyakonov #0 am 4.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E43, Tel. 888-5875,
Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt
 1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
Q i + j. dτ = i. - keine pot. und kin. Energien: depot. - adiabate ZÄ: Q i = 0 - keine technische Arbeit: Ẇ t,j = 0
 Institut für hermodynamik hermodynamik - Formelsammlung. Hauptsätze der hermodynamik (a. Hauptsatz der hermodynamik i. Offenes System de = de pot + de kin + du = i Q i + j Ẇ t,j + ein ṁ ein h tot,ein aus
Institut für hermodynamik hermodynamik - Formelsammlung. Hauptsätze der hermodynamik (a. Hauptsatz der hermodynamik i. Offenes System de = de pot + de kin + du = i Q i + j Ẇ t,j + ein ṁ ein h tot,ein aus
Grundlagen der Physik 2 Schwingungen und Wärmelehre
 Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik 04. 06. 2007 Othmar Marti (Universität Ulm) Schwingungen und Wärmelehre 04. 06.
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik 04. 06. 2007 Othmar Marti (Universität Ulm) Schwingungen und Wärmelehre 04. 06.
d) Das ideale Gas makroskopisch
 d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
Winter-Semester 2017/18. Moderne Theoretische Physik IIIa. Statistische Physik
 Winter-Semester 2017/18 Moderne Theoretische Physik IIIa Statistische Physik Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie Do 11:30-13:00, Lehmann Raum 022, Geb 30.22 http://www.tkm.kit.edu/lehre/
Winter-Semester 2017/18 Moderne Theoretische Physik IIIa Statistische Physik Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie Do 11:30-13:00, Lehmann Raum 022, Geb 30.22 http://www.tkm.kit.edu/lehre/
Statistische Zustandsgröße Entropie Energieentwertung bei Wärmeübertragungen II. Hauptsatz der Thermodynamik
 Statistische Zustandsgröße Entropie Energieentwertung bei Wärmeübertragungen II. Hauptsatz der hermodynamik Die nachfolgenden Ausführungen stellen den Versuch dar, die zugegeben etwas schwierige Problematik
Statistische Zustandsgröße Entropie Energieentwertung bei Wärmeübertragungen II. Hauptsatz der hermodynamik Die nachfolgenden Ausführungen stellen den Versuch dar, die zugegeben etwas schwierige Problematik
9. Thermodynamik. 9.5 Wärmetransport Wärmeleitung Konvektion Der Treibhauseffekt. 9. Thermodynamik Physik für E-Techniker
 9. Thermodynamik 9.5 Wärmetransport 9.5.1 Wärmeleitung 9.5.2 Konvektion 953 9.5.3 Wärmestrahlung 9.5.4 Der Treibhauseffekt 9.5 Wärmetransport Man unterscheidet: Wärmeleitung Energietransport durch Wechselwirkung
9. Thermodynamik 9.5 Wärmetransport 9.5.1 Wärmeleitung 9.5.2 Konvektion 953 9.5.3 Wärmestrahlung 9.5.4 Der Treibhauseffekt 9.5 Wärmetransport Man unterscheidet: Wärmeleitung Energietransport durch Wechselwirkung
C Metallkristalle. Allgemeine Chemie 60. Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4. Tabelle 7: weiter Strukturtypen. kubisch innenzentriert KZ = 8
 Allgemeine Chemie 60 Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4 Tabelle 7: weiter Strukturtypen C Metallkristalle kubisch primitiv KZ = 6 kubisch innenzentriert KZ = 8 kubisch flächenzentriert, kubisch dichteste
Allgemeine Chemie 60 Fluorit CaF 2 KZ(Ca) = 8, KZ(F) = 4 Tabelle 7: weiter Strukturtypen C Metallkristalle kubisch primitiv KZ = 6 kubisch innenzentriert KZ = 8 kubisch flächenzentriert, kubisch dichteste
Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie
 Sommer-Semester 2011 Moderne Theoretische Physik III Statistische Physik Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie Di 09:45-11:15, Lehmann HS 022, Geb 30.22 Do 09:45-11:15,
Sommer-Semester 2011 Moderne Theoretische Physik III Statistische Physik Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie Di 09:45-11:15, Lehmann HS 022, Geb 30.22 Do 09:45-11:15,
Thermodynamik (Wärmelehre) IV Kreisprozesse und Entropie
 Physik A VL7 (..0) hermodynamik (Wärmelehre) IV Kreisprozesse und Entropie Kreisprozesse Carnot scher Kreisprozess Reale Wärmemaschinen (tirling-motor, Dampfmaschine, Otto- und Dieselmotor) Entropie Der.
Physik A VL7 (..0) hermodynamik (Wärmelehre) IV Kreisprozesse und Entropie Kreisprozesse Carnot scher Kreisprozess Reale Wärmemaschinen (tirling-motor, Dampfmaschine, Otto- und Dieselmotor) Entropie Der.
Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler
 TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
9. Thermodynamik. 9.5 Wärmetransport Wärmeleitung Konvektion Der Treibhauseffekt. 9. Thermodynamik Physik für E-Techniker
 9. Thermodynamik 9.5 Wärmetransport 9.5.1 Wärmeleitung 9.5.2 Konvektion 953 9.5.3 Wärmestrahlung 9.5.4 Der Treibhauseffekt 9.5 Wärmetransport Man unterscheidet: Wärmeleitung Konvektion Strahlung Energietransport
9. Thermodynamik 9.5 Wärmetransport 9.5.1 Wärmeleitung 9.5.2 Konvektion 953 9.5.3 Wärmestrahlung 9.5.4 Der Treibhauseffekt 9.5 Wärmetransport Man unterscheidet: Wärmeleitung Konvektion Strahlung Energietransport
Die Carnot-Maschine SCHRITT III. Isotherme Kompression bei einer Temperatur T 2 T 2. Wärmesenke T 2 = konstant. Nicolas Thomas
 Die Carnot-Maschine SCHRITT III Isotherme Kompression bei einer Temperatur T 2 T 2 Wärmesenke T 2 = konstant Die Carnot-Maschine SCHRITT IV Man isoliert das Gas wieder thermisch und drückt den Kolben noch
Die Carnot-Maschine SCHRITT III Isotherme Kompression bei einer Temperatur T 2 T 2 Wärmesenke T 2 = konstant Die Carnot-Maschine SCHRITT IV Man isoliert das Gas wieder thermisch und drückt den Kolben noch
EP Vorlesung 15. II) Wärmelehre
 EP Vorlesung 15 II) Wärmelehre 14.Hauptsätze der Wärmelehre 15.Wärmetransprot und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion Versuche: Mechanisches Wärmeäquivalent Lufttisch
EP Vorlesung 15 II) Wärmelehre 14.Hauptsätze der Wärmelehre 15.Wärmetransprot und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion Versuche: Mechanisches Wärmeäquivalent Lufttisch
Kapitel IV Wärmelehre und Thermodynamik ctd.
 Kapitel IV Wärmelehre und Thermodynamik ctd. a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas mikroskopisch e) Das idealegas - makroskopisch f) Das reale Gas / Phasenübergänge
Kapitel IV Wärmelehre und Thermodynamik ctd. a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas mikroskopisch e) Das idealegas - makroskopisch f) Das reale Gas / Phasenübergänge
Konvektion. Prinzip: Bei Konvektion ist Wärmetransport an Materialtransport. Beispiel: See- und Landwind
 Konvektion Fluides Medium dehnt sich durch Erwärmung lokal aus erwärmte Stoffmenge hat kleinere Dichte steigt auf und wird durch kälteren Stoff ersetzt Konvektionskreislauf Prinzip: Warme Flüssigkeit steigt
Konvektion Fluides Medium dehnt sich durch Erwärmung lokal aus erwärmte Stoffmenge hat kleinere Dichte steigt auf und wird durch kälteren Stoff ersetzt Konvektionskreislauf Prinzip: Warme Flüssigkeit steigt
Thermodynamik. Kapitel 4. Nicolas Thomas
 Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Wärmestrahlung. Einfallende Strahlung = absorbierte Strahlung + reflektierte Strahlung
 Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Wärmestrahlung Gleichheit von Absorptions- und Emissionsgrad Zwei Flächen auf gleicher Temperatur T 1 stehen sich gegenüber. dunkelgrau hellgrau Der Wärmefluss durch Strahlung muss in beiden Richtungen
Zur Erinnerung. p isotherm. Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: Kreisprozesse:
 Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
Zur Erinnerung Stichworte aus der 20. Vorlesung: Poisson sche leichungen/adiabaten- Gleichungen: T V V 1 const. const. adiabatisch ( V ) 0 V V 0 R T0 isotherm ( V ) V Kreisrozesse: Ein thermodynamisches
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Mitschrift Thermodynamik
 Mitschrift hermodynamik Herleitung für den Gasdruck Berechnung des oberen Kreisradius d cosϕ dϕ dψ d N eilchen im Gesamtvolumen dn d N Aufschlagswahrscheinlichkeit eines eilchens Fläche df df sinϕ Gesamte
Mitschrift hermodynamik Herleitung für den Gasdruck Berechnung des oberen Kreisradius d cosϕ dϕ dψ d N eilchen im Gesamtvolumen dn d N Aufschlagswahrscheinlichkeit eines eilchens Fläche df df sinϕ Gesamte
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 2. Prof. Dr. Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3Bilanzgleichungen 3.3.1Massenbilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 2 Prof. Dr. Ing. Heinz Pitsch Kapitel 3, Teil 2: Übersicht 3 Energiebilanz 3.3Bilanzgleichungen 3.3.1Massenbilanz 3.3.2 Energiebilanz und 1. Hauptsatz
Wissenschaft öffentlich machen
 Wissenschaft öffentlich machen Allgemeinverständliche öffentliche Vorträge zur Astronomie und Astrophysik Heinrich-Plett-Str. 40, Kassel, Oberzwehren Gebäude AVZ, Hörsaal 298, Uni Kassel Samstag, 14.11.2015,
Wissenschaft öffentlich machen Allgemeinverständliche öffentliche Vorträge zur Astronomie und Astrophysik Heinrich-Plett-Str. 40, Kassel, Oberzwehren Gebäude AVZ, Hörsaal 298, Uni Kassel Samstag, 14.11.2015,
Physik I Mechanik der Kontinua und Wärmelehre Thomas Schörner-Sadenius
 Physik I Mechanik der Kontinua und Wärmelehre Thomas Universität Hamburg Wintersemester 2014/15 ORGANISATORISCHES Thomas : Wissenschaftler (Teilchenphysik) am Deutschen Elektronen-Synchrotron (DESY) Kontakt:
Physik I Mechanik der Kontinua und Wärmelehre Thomas Universität Hamburg Wintersemester 2014/15 ORGANISATORISCHES Thomas : Wissenschaftler (Teilchenphysik) am Deutschen Elektronen-Synchrotron (DESY) Kontakt:
ST Der Stirling-Motor als Wärmekraftmaschine
 ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
Die absolute Temperaturskala und der 3. Hauptsatz der Thermodynamik
 Kapitel 1 Die absolute emperaturskala und der 3. Hauptsatz der hermodynamik 1.1 Die allgemeine Definition der absoluten emperatur Bisher haben wir die emperatur über die thermische Zustandsgleichung pv
Kapitel 1 Die absolute emperaturskala und der 3. Hauptsatz der hermodynamik 1.1 Die allgemeine Definition der absoluten emperatur Bisher haben wir die emperatur über die thermische Zustandsgleichung pv
Physikdepartment. Ferienkurs zur Experimentalphysik 4. Daniel Jost 10/09/15
 Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Max Planck: Das plancksche Wirkungsquantum
 Max Planck: Das plancksche Wirkungsquantum Überblick Person Max Planck Prinzip schwarzer Strahler Klassische Strahlungsgesetze Planck sches Strahlungsgesetz Beispiele kosmische Hintergrundstrahlung Sternspektren
Max Planck: Das plancksche Wirkungsquantum Überblick Person Max Planck Prinzip schwarzer Strahler Klassische Strahlungsgesetze Planck sches Strahlungsgesetz Beispiele kosmische Hintergrundstrahlung Sternspektren
Das plancksche Strahlungsgesetz Das plancksche Strahlungsgesetz
 Das plancksche Strahlungsgesetz 1 Historisch 164-177: Newton beschreibt Licht als Strom von Teilchen 1800 1900: Licht als Welle um 1900: Rätsel um die "Hohlraumstrahlung" Historisch um 1900: Rätsel um
Das plancksche Strahlungsgesetz 1 Historisch 164-177: Newton beschreibt Licht als Strom von Teilchen 1800 1900: Licht als Welle um 1900: Rätsel um die "Hohlraumstrahlung" Historisch um 1900: Rätsel um
4.6 Hauptsätze der Thermodynamik
 Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Aufgaben zur Experimentalphysik II: Thermodynamik
 Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #15 am 01.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #15 am 01.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Thermodynamik Hauptsatz
 Thermodynamik. Hauptsatz Inhalt Wärmekraftmaschinen / Kälteprozesse. Hauptsatz der Thermodynamik Reversibilität Carnot Prozess Thermodynamische Temperatur Entropie Entropiebilanzen Anergie und Exergie
Thermodynamik. Hauptsatz Inhalt Wärmekraftmaschinen / Kälteprozesse. Hauptsatz der Thermodynamik Reversibilität Carnot Prozess Thermodynamische Temperatur Entropie Entropiebilanzen Anergie und Exergie
2. Thermodynamik Grundbegriffe Hauptsätze Thermodynamische Potentiale response -Funktionen
 2. Thermodynamik 1 2.1 Grundbegriffe 2 2.2 Hauptsätze 3 2.3 Thermodynamische Potentiale 4 2.4 response -Funktionen G. Kahl & F. Libisch (E136) Statistische Physik I Kapitel 2 5. April 2016 1 / 25 2.1 Grundbegriffe
2. Thermodynamik 1 2.1 Grundbegriffe 2 2.2 Hauptsätze 3 2.3 Thermodynamische Potentiale 4 2.4 response -Funktionen G. Kahl & F. Libisch (E136) Statistische Physik I Kapitel 2 5. April 2016 1 / 25 2.1 Grundbegriffe
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Prof. Dr. U. Schollwöck Sommersemester 2013
 Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Repetitorium. Thermodynamik. 3., überarbeitete und ergänzte Auflage. von. Wilhelm Schneider. unter Mitarbeit von. Stefan Haas und Karl Ponweiser
 Repetitorium Thermodynamik 3., überarbeitete und ergänzte Auflage von Wilhelm Schneider unter Mitarbeit von Stefan Haas und Karl Ponweiser Oldenbourg Verlag München Inhaltsverzeichnis 1 Grundbegriffe 1
Repetitorium Thermodynamik 3., überarbeitete und ergänzte Auflage von Wilhelm Schneider unter Mitarbeit von Stefan Haas und Karl Ponweiser Oldenbourg Verlag München Inhaltsverzeichnis 1 Grundbegriffe 1
Wellen und Dipolstrahlung
 Wellen und Dipolstrahlung Florian Hrubesch 25. März 2010 Inhaltsverzeichnis 1 Photoeffekt 1 2 Comptoneffekt 3 3 Bragg Streuung 4 4 Strahlungsgesetze 5 1 Photoeffekt Der Photoeffekt wurde erstmals 1839
Wellen und Dipolstrahlung Florian Hrubesch 25. März 2010 Inhaltsverzeichnis 1 Photoeffekt 1 2 Comptoneffekt 3 3 Bragg Streuung 4 4 Strahlungsgesetze 5 1 Photoeffekt Der Photoeffekt wurde erstmals 1839
Fermi-Dirac-Verteilung
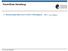 Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k B T + 6.7.23 Michael Buballa Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k
Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k B T + 6.7.23 Michael Buballa Fermi-Dirac-Verteilung Besetzungsfunktion pro innerem Freiheitsgrad: n(ε) = e (ε µ)/k
Thermodynamik I PVK - Tag 2. Nicolas Lanzetti
 Thermodynamik I PVK - Tag 2 Nicolas Lanzetti Nicolas Lanzetti 05.01.2016 1 Heutige Themen Carnot; Wirkungsgrad/Leistungsziffer; Entropie; Erzeugte Entropie; Isentroper Wirkungsgrad; Isentrope Prozesse
Thermodynamik I PVK - Tag 2 Nicolas Lanzetti Nicolas Lanzetti 05.01.2016 1 Heutige Themen Carnot; Wirkungsgrad/Leistungsziffer; Entropie; Erzeugte Entropie; Isentroper Wirkungsgrad; Isentrope Prozesse
Vorlesung Physik für Pharmazeuten PPh - 08
 Vorlesung Physik für Pharmazeuten PPh - 08 Wärmelehre 18.12. 2006 Der erste Hauptsatz der Thermodynamik Verallgemeinerung der Energieerhaltung von makroskopischen Systemen auf mikroskopische Der erste
Vorlesung Physik für Pharmazeuten PPh - 08 Wärmelehre 18.12. 2006 Der erste Hauptsatz der Thermodynamik Verallgemeinerung der Energieerhaltung von makroskopischen Systemen auf mikroskopische Der erste
Ferienkurs - Experimentalphysik 2
 Technische Universität München Department of Physics Ferienkurs - Experimentalphysik 2 Wärmelehre Qi Li 22/08/2012 Inhaltsverzeichnis Inhaltsverzeichnis 1 Wärmelehre 1 2 Das ideale Gas 1 3 Nullter Hauptsatz
Technische Universität München Department of Physics Ferienkurs - Experimentalphysik 2 Wärmelehre Qi Li 22/08/2012 Inhaltsverzeichnis Inhaltsverzeichnis 1 Wärmelehre 1 2 Das ideale Gas 1 3 Nullter Hauptsatz
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
Moderne Theoretische Physik IIIa WS 18/19
 Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik IIIa WS 18/19 Prof. Dr. Alexander Mirlin Lösungen zu Blatt 2 Dr. Stefan Rex Besprechung: 06.11.2018
Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik IIIa WS 18/19 Prof. Dr. Alexander Mirlin Lösungen zu Blatt 2 Dr. Stefan Rex Besprechung: 06.11.2018
Übungen zur Theoretischen Physik F SS Ideales Boltzmann-Gas: ( =25 Punkte, schriftlich)
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zur Theoretischen Physik F SS 2016 Prof. Dr. A. Shnirman Blatt 2 Dr. B. Narozhny, Dipl.-Phys. P. Schad Lösungsvorschlag
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zur Theoretischen Physik F SS 2016 Prof. Dr. A. Shnirman Blatt 2 Dr. B. Narozhny, Dipl.-Phys. P. Schad Lösungsvorschlag
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #4 am 3.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E43, Tel. 888-5875,
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 007 Vladimir Dyakonov #4 am 3.0.007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E43, Tel. 888-5875,
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung
 Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
Vorlesung 15 II Wärmelehre 15. Wärmetransport und Stoffmischung a) Wärmestrahlung b) Wärmeleitung c) Wärmeströmung d) Diffusion 16. Phasenübergänge (Verdampfen, Schmelzen, Sublimieren) Versuche: Wärmeleitung
