H δ+ H H H H. Addition von HBr an Ethen. Zufällig kommt ein HBr-Molekül in die Nähe der elektronenreichen Doppelbindung. Schritt 1
|
|
|
- Falko Böhm
- vor 5 Jahren
- Abrufe
Transkript
1 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 1/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen δ- δ+ Ulrich elmich 2015
2 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 δ- 2/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen ---? δ+ Ulrich elmich 2015
3 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 δ- δ+ 3/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen ist stark polarisiert; das -Atom stellt den positiven Pol dar, das -Atom den negativen. Ulrich elmich 2015
4 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 δ- δ+ 4/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen ist stark polarisiert; das -Atom stellt den positiven Pol dar, das -Atom den negativen. ---? Ulrich elmich 2015
5 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 1 5/ Zufällig kommt ein -Molekül in die Nähe der elektronenreichen δ- δ+ ist stark polarisiert; das -Atom stellt den positiven Pol dar, das -Atom den negativen. Das -Atom wird von der hohen Elektronendichte der Doppelbindung angezogen. Ulrich elmich 2015
6 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 2 ---? 6/ - + Ulrich elmich 2015
7 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 2 - Das -Molekül wird heterolytisch gespalten, das Proton nähert sich der elektronenreichen 7/ + Ulrich elmich 2015
8 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 2 - Das -Molekül wird heterolytisch gespalten, das Proton nähert sich der elektronenreichen 8/ ---? + Ulrich elmich 2015
9 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 2 - Das -Molekül wird heterolytisch gespalten, das Proton nähert sich der elektronenreichen 9/ Das Proton setzt sich an eines der beiden -Atome des Ethens. + Ulrich elmich 2015
10 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 2-10/ Das -Molekül wird heterolytisch gespalten, das Proton nähert sich der elektronenreichen Das Proton setzt sich an eines der beiden -Atome des Ethens. ---? + Ulrich elmich 2015
11 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 2-11/ Das -Molekül wird heterolytisch gespalten, das Proton nähert sich der elektronenreichen Das Proton setzt sich an eines der beiden -Atome des Ethens. + Das andere -Atom übernimmt die positive Ladung und wird zu einem arbenium-ion. Ulrich elmich 2015
12 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 3 ---? 12/ - + Ulrich elmich 2015
13 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 3 Ein omid-ion wird von dem arbenium-ion angezogen. 13/ - + Ulrich elmich 2015
14 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 3 Ein omid-ion wird von dem arbenium-ion angezogen. 14/ ---? Ulrich elmich 2015
15 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen Schritt 3 Ein omid-ion wird von dem arbenium-ion angezogen. 15/ Das omid-ion setzt sich an das arbenium-ion, es entsteht om-ethan, das Endprodukt. Ulrich elmich 2015
16 hemie Q1 / 4. Reaktionswege der Organik / 4.2 Alkene und elektrophile Addition Addition von an Ethen, Zusammenfassung / Ulrich elmich 2015
Bromierung von Cycloalkenen
 hemie Q1 / 4. Reaktionswege der organischen hemie / 4.2 Alkene und elektrophile Addition 1/ omierung von ycloalkenen Zufällig kommt ein 2-Molekül in die Nähe der elektronenreichen Doppelbindung. Ulrich
hemie Q1 / 4. Reaktionswege der organischen hemie / 4.2 Alkene und elektrophile Addition 1/ omierung von ycloalkenen Zufällig kommt ein 2-Molekül in die Nähe der elektronenreichen Doppelbindung. Ulrich
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser Reaktion: Chemikalien:
CHE 172.1: Organische Chemie für die Life Sciences
 1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
1 E 172.1: Organische hemie für die Life Sciences Prof Dr. J. A. Robinson 4. Alkene und Alkine : Reaktionen und erstellung 4.1. Elektrophile Additionen an Alkene ; Regioselektivität Das Proton einer starken
6. Rechenübung Organik (27.01./ )
 1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
1 6. Rechenübung Organik (27.01./03.02.2009) Literatur: 2.) Mortimer : hemie Basiswissen hemie ISBN 3 13 484308 0 Paula Y. Bruice : Organische hemie ISBN 978 3 8273 7190 4 Gesättigtes Atom Atom, nur mit
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang
 Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
Lösung :Aromatische Kohlenwasserstoffe Kursleiter Klaus Bentz/ Kollegiat Andreas Maier Abiturjahrgang 2004 1985/IV/1 Zunächst wird Methan bei Licht bromiert: 4 2 3 Gemäß der FriedelraftSynthese unter Verwendung
π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!)
 . Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
. Alkene (lefine) Funktionelle Gruppe: C=C-Doppelbindung π-bindung: 264 kj/mol (s c hw äc he r als die σ-bindung!) => C=C-Doppelbindung: 612 kj/mol sp 2 -hybridisierung σ-bindung: 348 kj/mol Wieder eine
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - rganische hemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 4. Alkene: eaktionen und erstellung 4.1. Elektrophile Additionen an Alkene: egioselektivität Das Proton einer
E 102.1: Grundlagen der hemie - rganische hemie Prof Dr. E. Landau und Prof. Dr. J. A. obinson 4. Alkene: eaktionen und erstellung 4.1. Elektrophile Additionen an Alkene: egioselektivität Das Proton einer
Elektrophile Additionen von HX an die CC-Doppelbindung (Vollhardt, 3. Aufl., S , 4. Aufl., S ; Hart, S ; Buddrus, S.
 Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Vorlesung 19 Elektrophile Additionen von X an die -Doppelbindung (Vollhardt, 3. Aufl., S. 504-514, 4. Aufl., S. 566-577; art, S. 96-105; Buddrus, S. 149-155) Die Elektronenwolke der π-bindung verleiht
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Organische Chemie, Reaktionsmechanismen
 , Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
, Reaktionen, Teil 3-1 - hemieskript Dr. R. Steiger rganische hemie, Reaktionsmechanismen Das Lernziel dieser Unterrichtseinheit beinhaltet folgende Punkte: Wie können funktionelle Gruppen ineinander überführt
Alkohole Brüder des Wassers
 6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
6. Alkohole Brüder des Wassers 6.1 Alkohole Brüder des Wassers entsteht aus Zucker durch die alkoholische Gärung. Dabei werden Glucosemoleküle mit ilfe von efezellen in und Kohlendioxid umgewandelt. NS29
(Anmerkung: Es sind weitere möglich. Spektren zeigen Diradikal.)
 eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
eispielaufgaben IChO 2. Runde 2017 Aromaten, Lösungen Aromaten eispiel 1: a) b) (Zeichnungen hier und unten teilweise ohne Wasserstoff-Atome) c) Das Anion ist planar und hat ein cyclisch konjugiertes π-elektronensystem
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
8 Organische Verbindungen und ihre Reaktionswege
 Lösungen zu den Durchblick-Seiten 8 rganische Verbindungen und ihre Reaktionswege 8.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 a) 2 b) Es handelt sich um eine ydrierung. Die ydrierung gehört
Lösungen zu den Durchblick-Seiten 8 rganische Verbindungen und ihre Reaktionswege 8.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 a) 2 b) Es handelt sich um eine ydrierung. Die ydrierung gehört
Additionsreaktionen an die C=C-Doppelbindung
 Triolein C 57 H 104 O 6 Schmelzpunkt: 5 C Siedebereich: 235-240 C Tetradecan C 14 H 30 Quelle: bioltec.de Schmelzpunkt: 5,5 C Siedepunkt: 253 C Quelle: oerlikon.com Die Formeln in der Abbildung geben das
Triolein C 57 H 104 O 6 Schmelzpunkt: 5 C Siedebereich: 235-240 C Tetradecan C 14 H 30 Quelle: bioltec.de Schmelzpunkt: 5,5 C Siedepunkt: 253 C Quelle: oerlikon.com Die Formeln in der Abbildung geben das
E. Zusammenfassung. E. Zusammenfassung
 E. Zusammenfassung Seit den 1960er Jahren wird die Frage untersucht, ob elektronenreiche (insbesondere tetraaminosubstituierte) Alkene, an ihrer Doppelbindung dissoziieren können [99][100]. Spaltungsprodukte
E. Zusammenfassung Seit den 1960er Jahren wird die Frage untersucht, ob elektronenreiche (insbesondere tetraaminosubstituierte) Alkene, an ihrer Doppelbindung dissoziieren können [99][100]. Spaltungsprodukte
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 8. alogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen alogenalkane sind in der organischen
E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 8. alogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen alogenalkane sind in der organischen
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
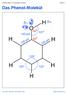 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Lösungen zum Übungsblatt zur Schulaufgabe. 0. Aufgaben aus dem Buch, S. 34
 Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Lösungen zum Übungsblatt zur Schulaufgabe 0. Aufgaben aus dem Buch, S. 34 A1 a) c) Br 5-Brom-2-methyl-hexa-2,3-dien 5-Brom-2-methyl-2,3-hexadien b) 3-Ethyl-3,4-dimethyldecan 3-Methylhexan A2 Butanmoleküle
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
8. Halogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen
 8. alogenalkane : ucleophile Substitutions- und Eliminationsreaktionen 69 alogenalkane sind in der organischen Synthese sehr wichtig, und werden auch in der Industrie als Lösungsmittel, im Krankenhaus
8. alogenalkane : ucleophile Substitutions- und Eliminationsreaktionen 69 alogenalkane sind in der organischen Synthese sehr wichtig, und werden auch in der Industrie als Lösungsmittel, im Krankenhaus
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Aufgaben zur Chemie der Alkohole und Ether (incl. deren Herstellung)
 Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Aufgaben zur Chemie der Alkohole und Ether (incl. deren erstellung) TGJ Nucleophile Substitution 1.1. Warum verlaufen nucleophile Substitutionen an Alkoholen leicht in saurer, nicht aber in basischer Lösung?
Selbsteinschätzungstest zum Vorkurs Organische Chemie
 WS 15/16 1/16 Selbsteinschätzungstest zum Vorkurs rganische hemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NIT die späteren Studieninhalte. Die Inhalte des Vorkurses
WS 15/16 1/16 Selbsteinschätzungstest zum Vorkurs rganische hemie Liebe Studierende! Der Vorkurs frischt Ihr Schulwissen auf, vermittelt aber NIT die späteren Studieninhalte. Die Inhalte des Vorkurses
Es wird bunt: Elektrophile Addition als Schnittstelle zwischen Reaktionsmechanismen und Farbstoffchemie
 1 von 20 Es wird bunt: Elektrophile Addition als Schnittstelle zwischen Reaktionsmechanismen und Farbstoffchemie Dirk Beyer, Würselen Niveau: Dauer: Sek. II 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards
1 von 20 Es wird bunt: Elektrophile Addition als Schnittstelle zwischen Reaktionsmechanismen und Farbstoffchemie Dirk Beyer, Würselen Niveau: Dauer: Sek. II 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Gruppe 3: Alkene, Alkine Versuch: omierung von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Gruppe 3: Alkene, Alkine Versuch: omierung von
Gruppe 3 Pflichtversuch. Umsetzung von Cyclohexan und Cyclohexen mit Bromwasser. Menge R-Sätze S-Sätze Gefahrensymbole. 300 ml /38
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 3 Pflichtversuch Umsetzung von Cyclohexan
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 3 Pflichtversuch Umsetzung von Cyclohexan
Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 Carbonylgruppen und eine C=C Doppelbindung.
 rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
9 Aromaten. 1 Elemente Chemie Oberstufe NRW Ernst Klett Verlag GmbH, Stuttgart Lösungen zu den Durchblick-Seiten
 Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Lösungen zu den Durchblick-Seiten 9.15 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 1. Aromaten sind ebene, cyclische Moleküle. 2. Das Ringmolekül weist ein durchgehendes System konjugierter
Übungen zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe. 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit
 O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
O II zu den Kapiteln Ungesättigte und aromatische Kohlenwasserstoffe 1. Wie lauten die allgemeinen Formeln für ungesättigte Kohlenwasserstoffe mit a) 2 Dreifachbindungen n 2n-6 b) 3 Dreifachbindungen n
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
Versuch: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung. keine Reaktion.
 Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Moleküle. Zweiatomige Moleküle: H 2+
 Moleküle Zweiatomige Moleküle: 2+ : zwei Kerne, ein Elektron Der Abstand zwischen den Atomkernen wird so klein gewählt, dass die 1s-Orbitale überlappen und durch Linearkombination Molekülorbitale gebildet
Moleküle Zweiatomige Moleküle: 2+ : zwei Kerne, ein Elektron Der Abstand zwischen den Atomkernen wird so klein gewählt, dass die 1s-Orbitale überlappen und durch Linearkombination Molekülorbitale gebildet
Reaktionstypen der Aromate
 Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Radikalische Reaktionspartner sind Atome bzw. Atomgruppen mit einem ungepaarten Elektron, wie z. B. das Chlorradikal Cl oder das Ethylradikal C 3 C 2. Radikale sind in der Regel sehr unbeständig, kurzlebig
Organische Chemie I. OC I Lehramt F. H. Schacher 1
 Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Organische Chemie I OC I Lehramt F. H. Schacher 1 Organisatorisches Kontakt: Felix H. Schacher IOMC, Lessingstr. 8, Raum 122 Email: felix.schacher@uni jena.de Termine: Vorlesung: Freitag 12 14 Uhr Hörsaal,
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Organische Chemie I SS 2018
 Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Organische Chemie I SS 2018 Organische Chemie I LA / J. C. Brendel 1 Organisatorisches Kontakt: Johannes C. Brendel ZAF, Philosophenweg 7, Raum 103 Email: johannes.brendel@uni-jena.de Felix H. Schacher,
Organik-Beispiel. Inhaltsverzeichnis
 Inhaltsverzeichnis I. Säure-Basen-Gleichungen... 2 a) Nach Arrhenius:... 2 b) Nach Broensted:... 2 c) Nach Lewis:... 2 II. H 2 O + HCl?... 4 a) Was ist in der Reaktion passiert? Welche Produkte entstehen?...
Inhaltsverzeichnis I. Säure-Basen-Gleichungen... 2 a) Nach Arrhenius:... 2 b) Nach Broensted:... 2 c) Nach Lewis:... 2 II. H 2 O + HCl?... 4 a) Was ist in der Reaktion passiert? Welche Produkte entstehen?...
Grundwissen Chemie 10. Klasse NTG
 Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Grundwissen Chemie 10. Klasse NTG Homologe Reihe der Alkane Methan, Ethan, Propan, Butan, Pentan, Hexan, Heptan, Octan, Nonan, Decan 10.1 C NTG Allg. Summenformel Alkane C n H 2n+2 (gesättigte Kohlenwasserstoffe,
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Elektrophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Signale für elektrophile Reak;onen Signale am organischen Molekül: π- Elektronen (Mehrfachbindungen), π- Elektronensysteme
Es wird bunt: Elektrophile Addition als Schnittstelle zwischen Reaktionsmechanismen und Farbstoffchemie
 Es wird bunt: Elektrophile Addition als Schnittstelle zwischen Reaktionsmechanismen und Farbstoffchemie Dirk Beyer, Wurselen Niveau: Dauer: Sek. II 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards
Es wird bunt: Elektrophile Addition als Schnittstelle zwischen Reaktionsmechanismen und Farbstoffchemie Dirk Beyer, Wurselen Niveau: Dauer: Sek. II 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards
Gruppe 2 vorgegebener Versuch Darstellung und Bromierung von Ethen
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 15.05.09 SS 09 Gruppe 2 vorgegebener Versuch Darstellung und omierung
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 15.05.09 SS 09 Gruppe 2 vorgegebener Versuch Darstellung und omierung
Halogenalkane. Radikalische Halogenierung von Alkanen. Addition von Halogenwasserstoffen an Alkene. H 3 C + HBr H C C C H.
 alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
alogenalkane erstellung: adikalische alogenierung von Alkanen + l + l + l l l + l Addition von alogenwasserstoffen an Alkene 3 Br + Br 3 Nucleophile Substitution an Alkylhalogeniden Nucleophil Elektrophil
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE
 SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE Wikipedia: Die organische Chemie (kurz: OC), häufig auch kurz Organik, ist ein Teilgebiet der
SÄUREN, BASE, SALZE GRUNDLAGEN CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE ORGANISCHE UND ANORGANISCHE CHEMIE Wikipedia: Die organische Chemie (kurz: OC), häufig auch kurz Organik, ist ein Teilgebiet der
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1. Grundwissen 10.Klasse NTG 2 Grundwissen 10.Klasse NTG 2
 Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Grundwissen 10.Klasse NTG 1 Grundwissen 10.Klasse NTG 1 Homologe Reihe: Reihe von Kohlenwasserstoffen, bei der jedes Molekül eine CH 2 -Gruppe mehr enthält als das vorhergehende. Gesättigte Kohlenwasserstoffe
Kapitel 10: Reaktionen in der organischen Chemie
 Kapitel 10: Den Aufbau von komplexeren organischen Molekülen aus einfachen Bausteinen oder den gezielten Umbau von bestehenden Molekülen nennt man chemische Synthese. Das Ziel ist meist die Eigenschaften
Kapitel 10: Den Aufbau von komplexeren organischen Molekülen aus einfachen Bausteinen oder den gezielten Umbau von bestehenden Molekülen nennt man chemische Synthese. Das Ziel ist meist die Eigenschaften
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Chemie. Elektrochemie, Alkane und Alkene
 Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Organische Chemie. Kapitel 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Organische Verbindungen enthalten Kohlenstoff
 rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
rganic Chemistry 4 th Edition Paula Yurkanis Bruice Kapitel 1 Elektronische Struktur und Bindung Säuren und Basen rganische Chemie rganische Verbindungen enthalten Kohlenstoff Kohlenstoff ist weder ein
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 5: )
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 5: 23.11.2005) Kovalente Bindung Atome können sich Valenzelektronen unter Ausbildung von Bindungen
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Übungsaufgaben: elektrophile Addition und radikalische Substitution. + Cl2
 Lösungsvorschlag mit Erläuterungen Übungsaufgaben: elektrophile Addition und radikalische Substitution In der folgenden Tabelle ist links ein Produkt benannt, das bei einer chemischen Reaktion entstehen
Lösungsvorschlag mit Erläuterungen Übungsaufgaben: elektrophile Addition und radikalische Substitution In der folgenden Tabelle ist links ein Produkt benannt, das bei einer chemischen Reaktion entstehen
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redox-Reaktion Oxidation Reduktion
Elektrostatik fachlicher Hintergrund und Unterrichtsvorschläge. Stiftung Bildungspakt Bayern
 Elektrostatik fachlicher Hintergrund und Unterrichtsvorschläge Stiftung Bildungspakt Bayern Florian Ziegler und Andreas Hartinger Universität Augsburg 04. Oktober 2012 1 Warum sollte man elektrostatischen
Elektrostatik fachlicher Hintergrund und Unterrichtsvorschläge Stiftung Bildungspakt Bayern Florian Ziegler und Andreas Hartinger Universität Augsburg 04. Oktober 2012 1 Warum sollte man elektrostatischen
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-OC-II Prof. R. Peters
 Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Uebungsklausur 2007, 1. Vordiplom (Basisprüfung) AC-C- Prof. R. Peters 1. Ergänzen Sie das folgende Schema durch Angabe der fehlenden Produkte oder Reagenzien! Bitte achten Sie auf die korrekte Darstellung
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bisher geschah Redoxreaktionen Oxidation/Reduktion
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
1/51. Protolysereaktion HCl + H2O + Protonenakzeptor: Ein H2O-Molekül. Protonendonator: Ein HCl-Molekül
 Protolysereaktion HCl + H2O + 1/51 - Protonendonator: Ein HCl-Molekül Protonenakzeptor: Ein H2O-Molekül Protolyse + 2/51 - Protolyse: Ein Proton "wandert" von einem Protonendonator zu einem Protonenakzeptor.
Protolysereaktion HCl + H2O + 1/51 - Protonendonator: Ein HCl-Molekül Protonenakzeptor: Ein H2O-Molekül Protolyse + 2/51 - Protolyse: Ein Proton "wandert" von einem Protonendonator zu einem Protonenakzeptor.
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
Rückblick Aufgaben. 4 Elemente Chemie Bayern 11
 Zu den Aufgaben A1 Im ydrogenchloridmolekül sind ein Wasserstoffatom und ein hloratom über eine Elektronenpaarbindung miteinander verbunden. Die Elektronenwolke ist dabei zum hloratom hin verschoben, da
Zu den Aufgaben A1 Im ydrogenchloridmolekül sind ein Wasserstoffatom und ein hloratom über eine Elektronenpaarbindung miteinander verbunden. Die Elektronenwolke ist dabei zum hloratom hin verschoben, da
Grundwissen Chemie Mittelstufe (10 MNG)
 Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 10. Aldehyde und Ketone 10.1 Nomenklatur ' Aldehyd Keton thanal "Formaldehyd" hanal
Prof. hristoffers, Vorlesung rganische hemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 10. Aldehyde und Ketone 10.1 Nomenklatur ' Aldehyd Keton thanal "Formaldehyd" hanal
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt
 Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 05.07.2014 NAME;
Chemisches Praktikum für Studierende der Humanmedizin, der Zahnheilkunde und Biologie/Lehramt Fachbereich Chemie der Philipps-Universität Marburg 1. Klausur zum 2. Praktikumsteil (OC) vom 05.07.2014 NAME;
1. Die folgenden Alkene liefern bei der elektrophilen Addition von Brom unterschiedliche kationische Zwischenstufen.
 Professor Lindhorst rganische Chemie 1: rganisch-chemische Reaktionsmechanismen chem303 WS 2008/09 ÜUNG 4 Addition an CC-hrfachbindungen - LÖSUNGEN - 1. Die folgenden Alkene liefern bei der elektrophilen
Professor Lindhorst rganische Chemie 1: rganisch-chemische Reaktionsmechanismen chem303 WS 2008/09 ÜUNG 4 Addition an CC-hrfachbindungen - LÖSUNGEN - 1. Die folgenden Alkene liefern bei der elektrophilen
Prof. Dr. P. Rademacher Organische Chemie IV
 Prof. Dr. P. Rademacher Organische hemie IV arbokationen 1. Nomenklatur arbokationen = alle kationischen -Verbindungen Beispiele:,, 2, 3, 4, 5. Im Massenspektrum von than bei hohem Druck findet man Peaks
Prof. Dr. P. Rademacher Organische hemie IV arbokationen 1. Nomenklatur arbokationen = alle kationischen -Verbindungen Beispiele:,, 2, 3, 4, 5. Im Massenspektrum von than bei hohem Druck findet man Peaks
3 Eliminierungen. 3.1 Begriffe und mechanistische Einteilung. Abspaltung zweier Atome bzw. Atomgruppen aus einem Molekül
 3 Eliminierungen 3.1 Begriffe und mechanistische Einteilung Abspaltung zweier Atome bzw. Atomgruppen aus einem Molekül Einteilung nach den Positionen der abgespaltenen Gruppen 1,1-Eliminierung (α-eliminierung)
3 Eliminierungen 3.1 Begriffe und mechanistische Einteilung Abspaltung zweier Atome bzw. Atomgruppen aus einem Molekül Einteilung nach den Positionen der abgespaltenen Gruppen 1,1-Eliminierung (α-eliminierung)
Prof. Dr. H. Hauptmann Übungen zur Vorlesung Organische Chemie II für Studierende des Lehramtes und der Biologie (3. Sem.)
 Prof. Dr.. auptmann Übungen zur Vorlesung rganische hemie II für tudierende des Lehramtes und der Biologie (3. em.) Lösungsbogen zu Übungsblatt 6, Additionsreaktionen an Alkenen 1.) Die Alkene c) werden
Prof. Dr.. auptmann Übungen zur Vorlesung rganische hemie II für tudierende des Lehramtes und der Biologie (3. em.) Lösungsbogen zu Übungsblatt 6, Additionsreaktionen an Alkenen 1.) Die Alkene c) werden
Chemie Carrella. Protokolle des Vorphysikums Herbst 2012
 Chemie Carrella Protokolle des Vorphysikums Herbst 2012 Protokoll 1 Atmosphäre: Alle sitzen an einem Tisch in einer Reihe, es wird im Uhrzeigersinn jedem eine Frage gestellt dann kommt der nächste dran
Chemie Carrella Protokolle des Vorphysikums Herbst 2012 Protokoll 1 Atmosphäre: Alle sitzen an einem Tisch in einer Reihe, es wird im Uhrzeigersinn jedem eine Frage gestellt dann kommt der nächste dran
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
REAKTIONEN DER ORGANISCHEN CHEMIE
 REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
Aufgaben zu ungesättigten Kohlenwasserstoffen und ihren Reaktionen
 Aufgaben zu ungesättigten Kohlenwasserstoffen und ihren eaktionen wichtige Fachbegriffe: positive und negative induktive Effekte, elektrophile Addition, egel von Markovnikov, Eliminierung, cis-trans-isomerie
Aufgaben zu ungesättigten Kohlenwasserstoffen und ihren eaktionen wichtige Fachbegriffe: positive und negative induktive Effekte, elektrophile Addition, egel von Markovnikov, Eliminierung, cis-trans-isomerie
Radikalische Substitution von Alkanen
 adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
adikalische Substitution von Alkanen KW mit sp³-hybridisierten C-Atomen (z.b. in Alkanen) und alogene Gemisch aus alogenalkanen und alogenwasserstoff Licht C n n à C n n1 eaktionsmechanismus z.b. Chlorierung
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
2. Verhalten der Elemente bei einer Reaktion: Warum funkt s bei unterschiedlichen
 1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
Versuchen Sie, die folgende Aufgabe nur mithilfe des Periodensystems zu lösen.
 hemie Vorkurs öhere achschulen für Gesundheitsberufe 1 Der Aufbau der Atome Aufgabe 10 Versuchen Sie, die folgende Aufgabe nur mithilfe des Periodensystems zu lösen. Zeichnen Sie mit dem Bohrmodell und
hemie Vorkurs öhere achschulen für Gesundheitsberufe 1 Der Aufbau der Atome Aufgabe 10 Versuchen Sie, die folgende Aufgabe nur mithilfe des Periodensystems zu lösen. Zeichnen Sie mit dem Bohrmodell und
Grundwissen Chemie 10 WSG/SG
 Grundwissen Chemie 10 WSG/SG Orbital Unter einem Orbital versteht man einen Raum, in dem sich ein Elektron mit einer bestimmten Wahrscheinlichkeit aufhält. Valenzelektronenpaarabstoßungsmodell (VEPA-Modell)
Grundwissen Chemie 10 WSG/SG Orbital Unter einem Orbital versteht man einen Raum, in dem sich ein Elektron mit einer bestimmten Wahrscheinlichkeit aufhält. Valenzelektronenpaarabstoßungsmodell (VEPA-Modell)
Organokatalytische Transferhydrierung. Von Mathias Ronellenfitsch und Christoph Krämer
 rganokatalytische Transferhydrierung Von Mathias Ronellenfitsch und Christoph Krämer 03.12.2009 Gliederung 1. Metallkatalysierte ydrierung von Doppelbindungen 2. Enantioselektive ydrierung in der atur
rganokatalytische Transferhydrierung Von Mathias Ronellenfitsch und Christoph Krämer 03.12.2009 Gliederung 1. Metallkatalysierte ydrierung von Doppelbindungen 2. Enantioselektive ydrierung in der atur
Chemie für Biologen, a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride?
 Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Chemie für Biologen, 2017 Übung 9 Organische Verbindungen (Thema 10.1 10.3) Aufgabe 1: a) Was ist Hybridisierung? Und aus welchen Orbitalen bestehen jeweils sp-, sp 2 - und sp 3 - Hybride? Hybridisierung,
Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie,
 Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
Wiederholung der letzten Vorlesungsstunde: Thema: Chemische h Bindungen Bindungen: Kräfte, die Atome zusammenhalten, Bindungsenergie, unterschiedliche Arten chemischer Bindungen, Atombindung, kovalente
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Summenformel Elektronenstrichformel Name Siedepunkt
 Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Die homologe Reihe der Alkene Summenformel Elektronenstrichformel Name Siedepunkt C 2 H 4 Ethen -104 C C 3 H 6 Propen -47 C C 4 H 8 1-Buten -6 C C 5 H 10 (...) 1-Penten 30 C C 6 H 12 (...) 1-Hexen 63 C
Nucleophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte
 Nucleophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Nucleophile Reak:onen Signale: Das organischen Molekül besitzt ein posi:v polarisiertes C- Atom in der KohlenstoKeLe.
Nucleophile Reaktionsmechanismen Erkennungsmerkmale und Reaktionsschritte H. Wünsch 2012 Nucleophile Reak:onen Signale: Das organischen Molekül besitzt ein posi:v polarisiertes C- Atom in der KohlenstoKeLe.
Der Estermechanismus ein individualisierter Einstieg in die Struktur-Eigenschaftsbeziehungen
 1 von 26 Der Estermechanismus ein individualisierter Einstieg in die Struktur-Eigenschaftsbeziehungen Jochen Hermanns, Würselen Niveau: Dauer: Sek. I/II (Übergangsphase) etwa 3 4 Unterrichtsstunden Kompetenzen:
1 von 26 Der Estermechanismus ein individualisierter Einstieg in die Struktur-Eigenschaftsbeziehungen Jochen Hermanns, Würselen Niveau: Dauer: Sek. I/II (Übergangsphase) etwa 3 4 Unterrichtsstunden Kompetenzen:
Chemie II. Vorlesung: Mo Uhr, HPT C103 Übungen: Mo Uhr, HCI H2.1, HCI J4
 hemie II Vorlesung: Mo 11-13 Uhr, PT 103 Übungen: Mo 14-16 Uhr, I 2.1, I J4 Literatur:.E. Mortimer, U. Müller: hemie, 11. Auflage Thieme-Verlag Stuttgart 2014 Dr. Wolfram Uhlig Laboratorium für Anorganische
hemie II Vorlesung: Mo 11-13 Uhr, PT 103 Übungen: Mo 14-16 Uhr, I 2.1, I J4 Literatur:.E. Mortimer, U. Müller: hemie, 11. Auflage Thieme-Verlag Stuttgart 2014 Dr. Wolfram Uhlig Laboratorium für Anorganische
