5. Versuche zur Synthese von Mn-Fe- und Mn-Cr-LDHs
|
|
|
- Klemens Morgenstern
- vor 5 Jahren
- Abrufe
Transkript
1 5. Versuche zur Synthese von Mn-Fe- und Mn-Cr-LDHs In den Systemen Mn-Fe und Mn-Cr wurde die Synthese von LDHs mit Nitrat, Chlorid, Karbonat und Sulfat als Zwischenschichtanion geprüft. Mn-Cr-LDHs Natürlich vorkommende LDHs mit Chrom als dreiwertigem Kation sind Barbertonit-2H [Mg 4 Cr 2 (OH) 12 ][CO 3 2,7H 2 O] und Stichtit-3R [Mg 4 Cr 2 (OH) 12 ][CO 3 2,7H 2 O]. Die Löslichkeitskurven von Mn(OH) 2 und [Cr(OH) 4 ] - schneiden sich bei ph = 10. Hier ist die Löslichkeit mit ca mol/l allerdings sehr gering. Trotz sorgfältiger, langsamer Fällung lieferte die Synthese nur schlecht kristalline Produkte für die Chlorid- und Nitrat-Verbindung. In Abbildung 106 sind zwei Röntgendiagramme von Mn-Cr-LDHs zusammengestellt in denen neben Mn(OH) 2 die Basisreflexe der LDHs ansatzweise erkennbar sind. Die Synthesen erfolgten bei ph = 10 und Raumtemperatur aus den Salzen MnCl 2 4H 2 0, CrCl 3 6H 2 O, Mn(NO 3 ) 2 9H 2 O und Cr(NO 3 ) 9H 2 O. Die Syntheseprodukte wurden 2 Wochen auf dem Schüttler alteriert. Auch eine längere Reaktionszeit führte zu keinen kristallineren Produkten, ebenso wenig wie eine saure Synthese aus MnO und den Cr-Salzen. counts Mn(OH) 2 Mn/Cr-Chlorid counts Mn(OH) 2 2θ Mn/Cr-Nitrat θ Abb. 106 Röntgendiagramme der Syntheseprodukte von Mn-Cr-Cl und Mn-Cr-NO 3 101
2 Abb. 107 Logarithmisches Diagramm zur Hydroxidfällung, nach SEEL (1970) 2 (003) Mn/Cr-Sulfat(K) 1 (009) (110) (113) (033) (030) Counts (006) (036) (309) (045) (03 15) (330) (333) (336) (22 18) (33 12) (066) (348) (615) Theta Abb. 108 Röntgendiagramm des Syntheseproduktes von Mn-Cr-Sulfat-K Die Synthese von Mn(SO 4 ) H 2 O und KCr(SO 4 ) 2 12H 2 O führte zu deutlich kristallineren Produkten (Abb. 107). Die Reflexe lassen sich analog denen von Shigait indizieren. Tabelle 46 zeigt einen Vergleich der Mn-Cr-Sulfat-K- und der Mn-Fe-Sulfat-K-, Mn-Al-Sulfat-K-Verbindungen. Die berechneten Gitterkonstanten weichen nur geringfügig voneinander ab. Der etwas größere a 0 Wert ist auf den größeren Ionenradius von Cr 3+ zurückzuführen. Leider erwies sich diese Phase gegenüber Trocknung als nicht stabil, was weitere Untersuchungen bezüglich chemischer 102
3 Zusammensetzung und Verhalten gegenüber thermischer Aufheizung unmöglich machte. Nach Trocknung waren nur Mn 3 O 4 Reflexe zu beobachten. Tabelle 46 Gitterparameter von Mn-Cr-Sulfat-K, Mn-Fe-Sulfat-K und Mn-Al-Sulfat-K bei 100 % r.f. a 0 [nm] c 0 [nm] c [nm] Mn/Cr-Sulfat(K) 0,9621 3,3698 1,1233 Mn/Fe-Sulfat(K) 0,9507 3,3362 1,1121 Mn/Al-Sulfat(K) 0,9531 3,3800 1,1267 Mn-Fe-LDHs Die Löslichkeitskurven von Mn(OH) 2 und [Fe(OH) 4 ] - verlaufen ähnlich wie die beim Chrom und schneiden sich bei einem ph-wert von etwa 10. Bei sorgfältiger, langsamer Fällung lieferte die Synthese schlecht kristalline Produkte für die Nitrat- und Sulfatverbindungen und besser kristalline Verbindungen für die Chlorid- und Karbonatderivate. In Abbildung 109 sind die Röntgendiagramme der Mn-Fe-LDHs mit Ausnahme der Sulfat-Na-Verbindung zusammengestellt. Reinphasige Verbindungen konnten nicht synthetisiert werden. Des Weiteren erwiesen sich alle Verbindungen gegenüber Trocknung instabil. Dies war aufgrund der geringen Kristallinität der Verbindungen und des Oxidationspotentials der nicht in der Kristallstruktur fixierten Eisen- und Manganionen zu erwarten. Die Synthesen erfolgten bei ph = 10 und Raumtemperatur aus den entsprechenden Mangan- und Eisensalzen. Die Syntheseprodukte wurden 2 Wochen auf dem Schüttler alteriert. Auch eine längere Reaktionszeit führte zu keinen kristallineren Produkten, ebenso wenig wie eine saure Synthese aus MnO und den Fe-Salzen. Tabelle 47 Gitterparameter von Mn-Fe-Cl, Mn-Fe-NO 3, Mn-Fe-CO 3 und Mn-Fe-Sulfat-K, -Na, -NH + 4 bei 100 % r.f. a 0 [nm] c 0 [nm] c [nm] Mn-Fe-Chlorid 0,3201 2,4246 0,8082 Mn-Fe-Nitrat 0,3202 2,3791 0,7930 Mn-Fe-Karbonat 0,3167 2,2909 0,7636 Mn-Fe-Sulfat-Na 0,9490 3,2939 1,0980 Mn-Fe-Sulfat-K 0,9507 3,3362 1, Mn-Al-Sulfat-NH 4 0,9531 3,3800 1,1267 Tabelle 47 zeigt die Ergebnisse der Gitterkonstantenverfeinerung der Mn-Fe-Verbindungen. Erwartungsgemäß ist bei der Karbonatverbindung der geringste Netzebenenabstand zu beobachten. Der Einbau unterschiedlicher einwertiger Kationen in die Zwischenschichten der Sulfatverbindungen führt auch bei den Mn-Fe-LDHs zu variierenden Netzebenenabständen. 103
4 Mn 3 O 4 Mn/Fe-Sulfat(NH 4 + ) 400 Mn/Fe-Sulfat(K) 300 Counts Mn/Fe-Chlorid 200 Mn(OH) 2 Mn/Fe-Karbonat 100 Mn/Fe-Nitrat Theta Abb. 109 Röntgendiagramme der Syntheseprodukte von Mn-Fe-LDHs (Offset der Diagramme je 100 counts) Um das Verhalten bezüglich des Einbaus von Mn 2+ /Mn 3+ und Fe 2+ /Fe 3+ in die Hauptschicht zu untersuchen, wurden Ansätze für die Sulfate-Na in allen 4 möglichen Kombinationen und mit unterschiedlichen molaren Verhältnissen hergestellt (Tabelle 48, Abbildungen ). Als Ausgangstoffe dienten Mn 2+ SO 4 0,95H 2 O, Mn 3+ (CH 3 COO) 3 2H 2 O, Fe 2+ SO 4 5,3H 2 O und Fe 3+ 2(SO 4 ) 3 5,3H 2 O. Sowohl bei dem Ansatz mit dreiwertigem Mangan und dreiwertigem Eisen als auch bei dem Syntheseversuch mit dreiwertigem Mangan und zweiwertigem Eisen treten keine Reflexe auf, die LDHs zuzuordnen wären. Bei den Mn 3+ /Fe 3+ -Mischungen mit höheren Mangangehalten konnten lediglich Manganhydroxide (Feitknechtit und Pyrochroit) und Hausmannit festgestellt werden. 104
5 Tabelle 48 Ausgangslösungen zur Herstellung von Mn/Fe-LDHs mit der Zusammensetzung [Mn 2+ 1-x Fe 3+ x (OH) 2 ] x+ [A x nh 2 O] - bzw. [Fe 2+ 1-x Mn 3+ x (OH) 2 ] x+ [A x nh 2 O] - Ansätze Mn 2+ Fe 2+ Verhältnis Mn/Fe c MnSO4 0,95H2O c FeSO4 5,3H2O g MnSO 4 0,95H 2 O g FeSO 4 5,3H 2 O x (mol/l) (mol/l) in 50 ml in 50 ml Mol.Masse (g/mol) / / / / / / Ansätze Mn 3+ Fe 3+ Verhältnis Mn/Fe c Mn(CH3COO)3 2H2O c Fe2(SO4)3 5,3H2O g Mn(CH 3 COO) 3 2H 2 O g Fe 2 (SO 4 ) 3 5,3H 2 O x (mol/l) (mol/l) in 50 ml in 50 ml Mol.Masse (g/mol) / / / Ansätze Mn 3+ Fe 2+ Verhältnis Mn/Fe c Mn(CH3COO)3 2H2O c FeSO4 * 5,3H2O g Mn(CH 3 COO) 3 2H 2 O g FeSO 4 * 5,3H 2 O x (mol/l) (mol/l) in 50 ml in 50 ml Mol.Masse (g/mol) / / / / / Ansätze Mn 2+ Fe 3+ Verhältnis Mn/Fe c MnSO4 0,95H2O c Fe2(SO4)3 5,3H2O g MnSO 4 0,95H 2 O g Fe 2 (SO 4 ) 3 5,3H 2 O x (mol/l) (mol/l) in 50 ml in 50 ml Mol.Masse (g/mol) / / / / Ähnliche Ergebnisse lieferten die Synthesen mit Mn 3+ /Fe 2+. Mit steigenden Mangangehalten kommt es kontinuierlich zur Bildung von Hausmannit. Anders sieht es bei den Ansätzen mit zweiwertigem Mangan aus. Nahezu nebenphasenfreie Synthesen konnten, wie zu erwarten, nur bei Mn 2+ /Fe 3+ Mischungen beobachtet werden. Die beste Kristallinität ist beim Ansatz mit einem Mn/Fe-Verhältnis von 2/1 zu verzeichnen. In diesem Verhältnis wurden auch alle Synthesen mit anderen Zwischenschichtanionen gemacht. Interessante Resultate lieferten die Ansätze mit zweiwertigem Mangan und zweiwertigem Eisen. Reflexe, die LDHs zuzuordnen sind, kann man in allen Syntheseversuchen sehen. Bei einem Mn/Fe-Verhältnis von 3/1 sind außer Spuren von Hausmannit keine Nebenphasen zu beobachten. 105
6 Tabelle 49 Reaktionsprodukte der Synthesen von Mn-Fe-LDHs LHD Hämatit Akaganeit Hausmannit Feitknechtit Pyrochroite Todorokit x Fe 2 O 3 β-feooh Mn 3 O 4 β-mnooh Mn(OH) 2 Mn 2 O 4 (H 2 O) Ansätze Mn 2+ Fe 2+ Verhältnis Mn/Fe Mol.Masse (g/mol) 3/ X - - X - X - 2/ X - - X - X - 3/ X X - 2/ X X X 2/ X X X X - X - 1/ X X X X - X - Ansätze Mn 3+ Fe 3+ Verhältnis Mn/Fe Mol.Masse (g/mol) 2/ (X) - - X X - 2/ X - - 2/ Ansätze Mn 3+ Fe 2+ Verhältnis Mn/Fe Mol.Masse (g/mol) 2/ X / X / X / X / X Ansätze Mn 2+ Fe 3+ Verhältnis Mn/Fe Mol.Masse (g/mol) 3/ X - - X / X - - X / X - X X / X - - X To Ak Ak Py Hä Ak To Py Hä Ha Intensity (counts) 4000 Ak Mn2+/Fe2+-Ansatz Ak Py To 0, ,33 0,40 0,50 0,60 0, Theta ( ) Abb. 110 Röntgendiagramme der Ansätze Mn 2+ /Fe 2+ in Abhängigkeit von x mit [Mn 2+ 1-x Fe 3+ x (OH) 2 ] x+ [A x nh 2 O] -, Nebenphasen gekennzeichnet (Farbcode siehe Tabelle) 106
7 Allerdings sind die Kristallinitäten hier auch geringer als beim Ansatz mit einem Verhältnis von 2/1. Hier kommt es zunächst zur Bildung von Pyrochroit. Todorokit tritt bei einem Mn/Fe-Verhältnis von 1/1 auf. Hohe Eisengehalte hingegen führen zur Bildung von Akaganeit und Hämatit. Intensity (counts) Ak Mn2+/Fe3+-Ansatz Ha 2 0,50 0,25 0,40 0,33 1 0,33 0,40 0,25 0, Theta ( ) Abb. 111 Röntgendiagramme der Ansätze Mn 2+ /Fe 3+ in Abhängigkeit von x mit [Mn 2+ 1-x Fe 3+ x (OH) 2 ] x+ [A x nh 2 O] -, Nebenphasen gekennzeichnet (Farbcode siehe Tabelle 49, Seite 106) Intensity (counts) Ha Ha Ha Ha 0,25 0,67 Mn3+/Fe2+-Ansatz 2 0,50 0,33 0,40 0,40 1 0,50 0,33 0,67 0, Theta ( ) Abb. 112 Röntgendiagramme der Ansätze Mn 3+ /Fe 2+ in Abhängigkeit von x mit [Mn 2+ 1-x Fe 3+ x (OH) 2 ] x+ [A x nh 2 O] -, Nebenphasen gekennzeichnet (Farbcode siehe Tabelle 49, Seite 106) 107
8 Intensity (counts) 2 Py Fe 0,60 0,33 Mn3+/Fe3+-Ansatz Ha 1 0,50 0,50 0,33 0, Theta ( ) Abb. 113 Röntgendiagramme der Ansätze Mn 3+ /Fe 3+ in Abhängigkeit von x mit [Mn 2+ 1-x Fe 3+ x (OH) 2 ] x+ [A x nh 2 O] -, Nebenphasen gekennzeichnet (Farbcode siehe Tabelle 49, Seite 106) 108
Synthese, Charakterisierung und Eigenschaften von manganhaltigen Layered Double Hydroxides (LDHs)
 Synthese, Charakterisierung und Eigenschaften von manganhaltigen Layered Double Hydroxides (LDHs) Dissertation zur Erlangung des akademischen Grades doctor rerum naturalium (Dr. rer. nat.) vorgelegt der
Synthese, Charakterisierung und Eigenschaften von manganhaltigen Layered Double Hydroxides (LDHs) Dissertation zur Erlangung des akademischen Grades doctor rerum naturalium (Dr. rer. nat.) vorgelegt der
Nachklausur zum Praktikum Allgemeine und Anorganische Chemie für Naturwissenschaftler Sommersemester 2007
 Nachklausur zum Praktikum Allgemeine und Anorganische Chemie für Naturwissenschaftler Sommersemester 2007 Name: Matr. Nr.: Studiengang (Bachelor/Diplom): Ergebnis: Punkte/Note: Aufg 1 2 3 4 5 6 7 8 9 10
Nachklausur zum Praktikum Allgemeine und Anorganische Chemie für Naturwissenschaftler Sommersemester 2007 Name: Matr. Nr.: Studiengang (Bachelor/Diplom): Ergebnis: Punkte/Note: Aufg 1 2 3 4 5 6 7 8 9 10
Analytische Chemie. B. Sc. Chemieingenieurwesen. 14. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie. B. Sc. Chemieingenieurwesen. 10. Juli Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 10. Juli 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 10. Juli 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
3. Synthese von ZnAl-LDHs mit anorganischen Anionen
 Synthese von ZnAl-LDHs mit anorganischen Anionen 3. Synthese von ZnAl-LDHs mit anorganischen Anionen LDHs können im basischen und sauren Milieu mit verschiedenen Methoden synthetisiert werden, die unter
Synthese von ZnAl-LDHs mit anorganischen Anionen 3. Synthese von ZnAl-LDHs mit anorganischen Anionen LDHs können im basischen und sauren Milieu mit verschiedenen Methoden synthetisiert werden, die unter
6. Zusammenfassung und Diskussion
 6. Zusammenfassung und Diskussion In dieser Dissertation wurden Synthesemethoden und Konzepte zur Untersuchung von manganhaltigen LDHs mit anorganischen und organischen Anionen (Mn-Al-Carboxylat-, Dicarboxylat-
6. Zusammenfassung und Diskussion In dieser Dissertation wurden Synthesemethoden und Konzepte zur Untersuchung von manganhaltigen LDHs mit anorganischen und organischen Anionen (Mn-Al-Carboxylat-, Dicarboxylat-
Anorganische-Chemie. Michael Beetz Arbeitskreis Prof. Bein. Grundpraktikum für Biologen 2017
 Michael Beetz Arbeitskreis Prof. Bein Butenandstr. 11, Haus E, E 3.027 michael.beetz@cup.uni-muenchen.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Trennungsgänge und Nachweise # 2 Trennungsgänge
Michael Beetz Arbeitskreis Prof. Bein Butenandstr. 11, Haus E, E 3.027 michael.beetz@cup.uni-muenchen.de Anorganische-Chemie Grundpraktikum für Biologen 2017 Trennungsgänge und Nachweise # 2 Trennungsgänge
Analytische Chemie. B. Sc. Chemieingenieurwesen. 22. September 2017, 13 bis 16 Uhr. Dr. Stephanie Möller & Prof. Dr. Thomas Jüstel.
 Analytische Chemie B. Sc. Chemieingenieurwesen 22. September 2017, 13 bis 16 Uhr Dr. Stephanie Möller & Prof. Dr. Thomas Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des
Analytische Chemie B. Sc. Chemieingenieurwesen 22. September 2017, 13 bis 16 Uhr Dr. Stephanie Möller & Prof. Dr. Thomas Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des
Analytische Chemie. B. Sc. Chemieingenieurwesen. 6. Juli 2016, Uhr. Prof. Dr. T. Jüstel & Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 6. Juli 2016, 10.30 13.30 Uhr Prof. Dr. T. Jüstel & Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 6. Juli 2016, 10.30 13.30 Uhr Prof. Dr. T. Jüstel & Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung
 Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
Übungsaufgaben zu Ionenreaktionen in wässriger Lösung 1) Berechnen Sie den phwert von folgenden Lösungen: a) 0.01 M HCl b) 3 10 4 M KOH c) 0.1 M NaOH d) 0.1 M CH 3 COOH (*) e) 0.3 M NH 3 f) 10 8 M HCl
Qualitative anorganische Analyse
 Dirk Häfner Arbeitsbuch Qualitative anorganische Analyse für Pharmazie- und Chemiestudenten unter Mitarbeit von Alice Stephan Gyyi Govi-Verlag Inhalt Vorwort zur 5. Auflage 9 Vorwort zur 4. Auflage 10
Dirk Häfner Arbeitsbuch Qualitative anorganische Analyse für Pharmazie- und Chemiestudenten unter Mitarbeit von Alice Stephan Gyyi Govi-Verlag Inhalt Vorwort zur 5. Auflage 9 Vorwort zur 4. Auflage 10
Analytische Chemie. B. Sc. Chemieingenieurwesen. 05. Februar Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 05. Februar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 05. Februar 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
3. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 3. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 3. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss
 1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
1 Uebungen zur Prüfungsvorbereitung 4.12.14 1) Redoxverhältnisse an einer Sediment-Wasser-Grenzfläche in einem Fluss Die folgenden Tiefenprofile von gelöstem Mangan, Eisen und Sulfid (S 2- ) sowie die
Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol]
![Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol] Aufgaben zum Umfeld: 7 Vergleichen Sie die Gitterenergien von NaF, NaCl und NaI bzw. MgO, CaO und BaO! Gitterenergien [kj/mol]](/thumbs/49/25486820.jpg) Seite 22 22 Auflösung von Si in NaOH-Lösung Weiterführende Infos Quarzsand und Alkalicarbonate werden bei ca. 1300 C zusammengeschmolzen und das Produkt ((Na/K) 2 O* n SiO 2 ) bei 150 C und 5 bar in Wasser
Seite 22 22 Auflösung von Si in NaOH-Lösung Weiterführende Infos Quarzsand und Alkalicarbonate werden bei ca. 1300 C zusammengeschmolzen und das Produkt ((Na/K) 2 O* n SiO 2 ) bei 150 C und 5 bar in Wasser
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP4 - Gesamtanalyse» Martin Wolf Betreuerin: Frau Sachse Datum: 05.05.2006 8:00 Uhr bis 12:00 Uhr
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP4 - Gesamtanalyse» Martin Wolf Betreuerin: Frau Sachse Datum: 05.05.2006 8:00 Uhr bis 12:00 Uhr
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7
 AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
AC2 ÜB12 Säuren und Basen LÖSUNGEN Seite 1 von 7 1. a) CH3COOH, C0=0.125 mol/l Schwache Säure pks = 4.75 (aus Tabelle) => ph = 0.5*(4.75-Log(0.125))= 2.83 b) H24, C0=0.1 mol/l Erste Protolysestufe starke
Analytische Chemie. B. Sc. Chemieingenieurwesen. 11. Februar Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 11. Februar 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Analytische Chemie B. Sc. Chemieingenieurwesen 11. Februar 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Allgemeine Grundlagen 2
 Allgemeine Grundlagen 2 1 Reaktionen und Bindung 1) Redox - Reaktionen 1. Semester 2) Säure - Base - Reaktionen 1. Semester 3) Komplexreaktionen (eigentlich kein neuer Reaktionstyp, sondern eine Säure
Allgemeine Grundlagen 2 1 Reaktionen und Bindung 1) Redox - Reaktionen 1. Semester 2) Säure - Base - Reaktionen 1. Semester 3) Komplexreaktionen (eigentlich kein neuer Reaktionstyp, sondern eine Säure
Prüfung zur Analytischen Chemie
 Prüfung zur Analytischen Chemie Datum: 10. Juli 2006 Punktzahl: Name: Matrikel-Nummer: Bitte verwenden Sie für die Lösung nur diese Aufgabenblätter (notfalls auch die Rückseite)! Aufgabe 1) Löslichkeit
Prüfung zur Analytischen Chemie Datum: 10. Juli 2006 Punktzahl: Name: Matrikel-Nummer: Bitte verwenden Sie für die Lösung nur diese Aufgabenblätter (notfalls auch die Rückseite)! Aufgabe 1) Löslichkeit
Analytische Chemie. B. Sc. Chemieingenieurwesen
 Analytische Chemie B. Sc. Chemieingenieurwesen 6. Februar 2018, 8.30 bis 11.30 Uhr Dr. Stephanie Möller und Prof. Dr. Thomas Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Analytische Chemie B. Sc. Chemieingenieurwesen 6. Februar 2018, 8.30 bis 11.30 Uhr Dr. Stephanie Möller und Prof. Dr. Thomas Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6
 Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Qualitative Analyse. - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch,
 - Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
- Identifikation von Ionen (häufig in einem Gemisch) - Charakterisierung der Analyse nach Farbe, Morphologie, Geruch, Löslichkeit - charakteristische Nachweisreaktionen für Einzelionen: - Fällungsreaktionen
Analytische Chemie. B. Sc. Chemieingenieurwesen. 15. März 2017, Uhr. Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller.
 Analytische Chemie B. Sc. Chemieingenieurwesen 15. März 2017, 12.30 15.30 Uhr Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 15. März 2017, 12.30 15.30 Uhr Prof. Dr. Thomas Jüstel, Dr. Stephanie Möller Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Name: Punktzahl: von 57 Note:
 Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
Testen Sie Ihr Wissen! Übungsprobe zu den Tertia-Themen und Säure-Base-Reaktionen Name: Punktzahl: von 57 Note: Für die folgenden Fragen haben Sie 60 Minuten Zeit. Viel Erfolg! Hilfsmittel: das ausgeteilte
4. Anorganisch-chemische Versuche
 4. Anorganisch-chemische Versuche o 4.4 Redoxreaktionen 4.4.1 Reduktion von Mangan(VII) in schwefelsaurer Lsg. 4.4.2 Oxidation von Mangan(II) in salpetersaurer Lsg. 4.4.3 Oxidation von Chrom(III) in alkalischer
4. Anorganisch-chemische Versuche o 4.4 Redoxreaktionen 4.4.1 Reduktion von Mangan(VII) in schwefelsaurer Lsg. 4.4.2 Oxidation von Mangan(II) in salpetersaurer Lsg. 4.4.3 Oxidation von Chrom(III) in alkalischer
4 LÖSLICHKEITSPRODUKT
 Arbeitsunterlagen zur Vorlesung CHEMISCHES RECHNEN 701.118 (Auflage November 005) Einheit 4 LÖSLICHKEITSPRODUKT und KOMPLEXBILDUNG Institut für Chemie Universität für Bodenkultur T. Prohaska 4 LÖSLICHKEITSPRODUKT
Arbeitsunterlagen zur Vorlesung CHEMISCHES RECHNEN 701.118 (Auflage November 005) Einheit 4 LÖSLICHKEITSPRODUKT und KOMPLEXBILDUNG Institut für Chemie Universität für Bodenkultur T. Prohaska 4 LÖSLICHKEITSPRODUKT
Metallische Baustoffe
 Metallische Baustoffe 1. Grundlagen / Eigenschaften. Eisen / Stahl 3. Schwermetalle / Korrosion 4. Korrosion 5. Elektrochemische Korrosion 6. Elektrochemie Metallische Baustoffe - Übersicht 1. Eisen Chemische
Metallische Baustoffe 1. Grundlagen / Eigenschaften. Eisen / Stahl 3. Schwermetalle / Korrosion 4. Korrosion 5. Elektrochemische Korrosion 6. Elektrochemie Metallische Baustoffe - Übersicht 1. Eisen Chemische
Analytische Chemie. B. Sc. Chemieingenieurwesen. 11. September Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 11. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 11. September 2013 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie. B. Sc. Chemieingenieurwesen. 19. März Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 19. März 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Analytische Chemie B. Sc. Chemieingenieurwesen 19. März 2014 Prof. Dr. T. Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der
Emder Wasser Trinkwasser-Analysewerte
 Emder Wasser Trinkwasser-Analysewerte Die Lust auf Wasser hat viele Gesichter. An heißen Sommertagen träumen wir von einer erfrischenden Dusche und einem Glas Wasser gegen den Durst. Im Winter verwöhnt
Emder Wasser Trinkwasser-Analysewerte Die Lust auf Wasser hat viele Gesichter. An heißen Sommertagen träumen wir von einer erfrischenden Dusche und einem Glas Wasser gegen den Durst. Im Winter verwöhnt
2. Teilklausur zum Chemischen Grundpraktikum im WS 2014/15 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2014/15 vom 21.01.2015 A1 A2 A3 F4 R5 E6 Note 8 12 5 9 8 8 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben Sie
2. Teilklausur zum Chemischen Grundpraktikum im WS 2014/15 vom 21.01.2015 A1 A2 A3 F4 R5 E6 Note 8 12 5 9 8 8 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben Sie
Prüfungsvorleistung zum Modul 13-BCH-0101 Aufgaben zum Praktikum "Allgemeine und Anorganische Chemie" , 08:00-09:00 Uhr.
 1 Prüfungsvorleistung zum Modul 13-BCH-0101 Aufgaben zum Praktikum "Allgemeine und Anorganische Chemie" 08.12.2008, 08:00-09:00 Uhr Name, Vorname: Matrikel-Nr.: Semester: Bitte schreiben Sie sauber und
1 Prüfungsvorleistung zum Modul 13-BCH-0101 Aufgaben zum Praktikum "Allgemeine und Anorganische Chemie" 08.12.2008, 08:00-09:00 Uhr Name, Vorname: Matrikel-Nr.: Semester: Bitte schreiben Sie sauber und
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2015/16 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2015/16 vom 18.09.2015 A1 A2 A3 A4 A5 Note 15 5 9 11 10 NAME:... VORNAME:...LÖSUNGSSTICHPUNKTE... Pseudonym für Ergebnisveröffentlichung:... Schreiben
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2015/16 vom 18.09.2015 A1 A2 A3 A4 A5 Note 15 5 9 11 10 NAME:... VORNAME:...LÖSUNGSSTICHPUNKTE... Pseudonym für Ergebnisveröffentlichung:... Schreiben
Analytische Chemie. B. Sc. Chemieingenieurwesen. 7. März 2016, Uhr. Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer:
 Analytische Chemie B. Sc. Chemieingenieurwesen 7. März 2016, 8.00 11.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 7. März 2016, 8.00 11.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Anhang Resultate DIN-Analytik Zulauf Grundwasserreinigungsanlage
 Anhang 11 1. Resultate DIN- Zulauf Grundwasserreinigungsanlage 2. Resultate DIN- Ablauf Grundwasserreinigungsanlage (einschließlich Ablauf 1. AK-Filter) Anhang 11 (1) Resultate DIN- Zulauf Grundwasserreinigungsanlage
Anhang 11 1. Resultate DIN- Zulauf Grundwasserreinigungsanlage 2. Resultate DIN- Ablauf Grundwasserreinigungsanlage (einschließlich Ablauf 1. AK-Filter) Anhang 11 (1) Resultate DIN- Zulauf Grundwasserreinigungsanlage
Grundlagen der Chemie für Nichtchemiker AUFGABENSAMMLUNG
 AUFGABENSAMMLUNG 1. Chemische Grundlagen: Masse -Berechnungen 1-1. Berechnen Sie die molaren Massen folgender Stoffe: a)caco 3 ; b)caso 4 2H 2 O; c)agcl; d)al 2 O 3 ; e)phenol C 6 H 5 OH; f)magnesiumammoniumphosphat-
AUFGABENSAMMLUNG 1. Chemische Grundlagen: Masse -Berechnungen 1-1. Berechnen Sie die molaren Massen folgender Stoffe: a)caco 3 ; b)caso 4 2H 2 O; c)agcl; d)al 2 O 3 ; e)phenol C 6 H 5 OH; f)magnesiumammoniumphosphat-
Anlage 2 (zu 3 Nr. 2, 4 Satz 1 und 5 Nr. 2, 3 und 5) Qualitätsanforderungen an zur Trinkwassergewinnung bestimmte Oberflächengewässer.
 Anlage 2 (zu 3 Nr. 2, 4 Satz 1 und 5 Nr. 2, 3 und 5) Qualitätsanforderungen an zur Trinkwassergewinnung bestimmte Oberflächengewässer Nummer Parameter Maßeinheit A 1 G 1) A 1 I 2) A 2 G 1) A 2 I 2) A 3
Anlage 2 (zu 3 Nr. 2, 4 Satz 1 und 5 Nr. 2, 3 und 5) Qualitätsanforderungen an zur Trinkwassergewinnung bestimmte Oberflächengewässer Nummer Parameter Maßeinheit A 1 G 1) A 1 I 2) A 2 G 1) A 2 I 2) A 3
Seminar zum Grundpraktikum Anorganische Chemie
 Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität Duisburg-Essen Analyse 2 (NH 4 ) 2 CO 3 -Gruppe Ba 2+ Sr 2+ Ca 2+ Lösliche Gruppe Na + Mg 2+ NH 4+ Eigenschaften
Seminar zum Grundpraktikum Anorganische Chemie Sommersemester 2012 Christoph Wölper Universität Duisburg-Essen Analyse 2 (NH 4 ) 2 CO 3 -Gruppe Ba 2+ Sr 2+ Ca 2+ Lösliche Gruppe Na + Mg 2+ NH 4+ Eigenschaften
Probe Entnahmestelle Probenahme Stadtwerke Rosenheim, Hochbehälter Kreut, Kammer :00
 / Labor, 80287 München Rosenheim labor@swro.de Martin.Winkler@swro.de Hubert.Paul@swro.de Besucheranschrift Labor Gebäude G Emmy-Noether-Str. 2 80287 München Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner:
/ Labor, 80287 München Rosenheim labor@swro.de Martin.Winkler@swro.de Hubert.Paul@swro.de Besucheranschrift Labor Gebäude G Emmy-Noether-Str. 2 80287 München Techn. Leiter: Hr. Dr. Hofmann Ansprechpartner:
Elektrochemie. Grundbegriffe. Oxidation: Ist die Teilreaktion bei der Elektronen abgegeben werden.
 Grundbegriffe Elektrochemische Reaktionen sind Redoxreaktionen, d.h Reaktionen mit Elektronenübergang. Sie können freiwillig ablaufen (galvanische Zelle) oder durch anlegen einer Spannung erzwungen werden
Grundbegriffe Elektrochemische Reaktionen sind Redoxreaktionen, d.h Reaktionen mit Elektronenübergang. Sie können freiwillig ablaufen (galvanische Zelle) oder durch anlegen einer Spannung erzwungen werden
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 23. April 2019 Inhalt: Volumetrische Messgeräte Säure-Base-Titration Analysenwaagen Fest-Flüssig-Trennverfahren Wasserlöslichkeit Verdünnung
Online Projektlabor Chemie. Durchführung für die Spurenanalytik in Wasser
 Online Projektlabor Chemie Technische Universität Berlin Durchführung für die Spurenanalytik in Wasser Leitung des Projektlabores: Prof. Dr. Th. Friedrich Ersteller des Dokumentes: Daniel Christian Brüggemann
Online Projektlabor Chemie Technische Universität Berlin Durchführung für die Spurenanalytik in Wasser Leitung des Projektlabores: Prof. Dr. Th. Friedrich Ersteller des Dokumentes: Daniel Christian Brüggemann
Reagenzien für Photometer
 Reagenzien für Photometer SERIE HI 937(00)-(00) Artikel : Reagenzien für Photometer, Cyanursäure (100 Tests) HI 93722-01 Parameter : Cyanursäure - Reagenzien für Photometer, Cyanursäure (300 Tests) HI
Reagenzien für Photometer SERIE HI 937(00)-(00) Artikel : Reagenzien für Photometer, Cyanursäure (100 Tests) HI 93722-01 Parameter : Cyanursäure - Reagenzien für Photometer, Cyanursäure (300 Tests) HI
Analytische Chemie. B. Sc. Chemieingenieurwesen. 23. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 23. März 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 23. März 2009 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Laborprotokoll Qualitative Analyse Ralph Koitz, Einzelsalz
 1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
1. Einzelsalz Aufgabenstellung: Nasschemische qualitative Analyse eines anorganischen Einzelsalzes. o Farblose, grobkörnige Kristalle o Flammenfärbung: leicht orange, nicht charakteristisch da vermutlich
Einführungskurs 3. Seminar
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG Einführungskurs 3. Seminar Prof. Dr. Christoph Janiak Literatur: Riedel, Anorganische Chemie Inhalt Reaktionstypen Gleichgewicht bei Säure/Base-Reaktionen ph-berechnungen
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG Einführungskurs 3. Seminar Prof. Dr. Christoph Janiak Literatur: Riedel, Anorganische Chemie Inhalt Reaktionstypen Gleichgewicht bei Säure/Base-Reaktionen ph-berechnungen
Übung 10 (Redox-Gleichgewichte und Elektrochemie)
 Übung 10 (Redox-Gleichgewichte und Elektrochemie) Verwenden Sie neben den in der Aufgabenstellung gegebenen Potenzialen auch die Werte aus der Potenzial-Tabelle im Mortimer. 1. Ammoniak kann als Oxidationsmittel
Übung 10 (Redox-Gleichgewichte und Elektrochemie) Verwenden Sie neben den in der Aufgabenstellung gegebenen Potenzialen auch die Werte aus der Potenzial-Tabelle im Mortimer. 1. Ammoniak kann als Oxidationsmittel
Bewehrungskorrosion. Stahl + Feuchte + Sauerstoff + (aggr. Medien) ---> Korrosionsprodukte. Fe + H 2 O + O 2 + (K) ---> 2FeO(OH) + H 2 O
 Bewehrungskorrosion Stahl + Feuchte + Sauerstoff + (aggr. Medien) ---> Korrosionsprodukte Fe + H 2 O + O 2 + (K) ---> 2FeO(OH) + H 2 O Bewehrungskorrosion Dauerhaftigkeit des Stahls im Beton in Abhängigkeit
Bewehrungskorrosion Stahl + Feuchte + Sauerstoff + (aggr. Medien) ---> Korrosionsprodukte Fe + H 2 O + O 2 + (K) ---> 2FeO(OH) + H 2 O Bewehrungskorrosion Dauerhaftigkeit des Stahls im Beton in Abhängigkeit
Vorpraktikum Grundoperationen im chemischen Laboratorium
 Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
Vorpraktikum Grundoperationen im chemischen Laboratorium Stand: 09. April 2018 Inhalt: Volumetrische Messgeräte Analysenwaagen Fest-Flüssig-Trennverfahren Flüssig-Flüssig-Trennverfahren Wasserlöslichkeit
VL Limnochemie
 VL Limnochemie Redoxreaktionen und -gleichgewichte WIEDERHOLUNG: SAUERSTOFF 1 Henry-Gesetz Massenwirkungsgesetz für den Fall: gasförmiger Stoff löst sich in Wasser A gas A fl K H = c(a fl ) c(a gas ) Henry-
VL Limnochemie Redoxreaktionen und -gleichgewichte WIEDERHOLUNG: SAUERSTOFF 1 Henry-Gesetz Massenwirkungsgesetz für den Fall: gasförmiger Stoff löst sich in Wasser A gas A fl K H = c(a fl ) c(a gas ) Henry-
2. Teilklausur zum Chemischen Grundpraktikum im WS 2012/13 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2012/13 vom 30.01.2013 A1 A2 A3 R4 F5 E6 Σ Note 8 9 8 9 8 8 50 NAME/VORNAME:... Matrikelnummer: Stichpunkte zu den Lösungen/AC... Pseudonym für Ergebnisveröffentlichung
2. Teilklausur zum Chemischen Grundpraktikum im WS 2012/13 vom 30.01.2013 A1 A2 A3 R4 F5 E6 Σ Note 8 9 8 9 8 8 50 NAME/VORNAME:... Matrikelnummer: Stichpunkte zu den Lösungen/AC... Pseudonym für Ergebnisveröffentlichung
Wasseranalyse - Prüfbericht
 101 Ww.Ausgang H Grenzwert 1,2-Dichlorethan < 0,000100 0,003000 mg/l DIN EN ISO 10301 (F4) 2,6-Dichlorbenzamid < 0,000030 0,003000 mg/l DIN EN ISO 11369 (F12) Aluminium (Al), gesamt < 0,0050 0,2000 mg/l
101 Ww.Ausgang H Grenzwert 1,2-Dichlorethan < 0,000100 0,003000 mg/l DIN EN ISO 10301 (F4) 2,6-Dichlorbenzamid < 0,000030 0,003000 mg/l DIN EN ISO 11369 (F12) Aluminium (Al), gesamt < 0,0050 0,2000 mg/l
Posten 1a. Was gilt immer. bei einer Oxidation?
 Posten 1a Was gilt immer bei einer Oxidation? a) Es werden Elektronen aufgenommen. (=> Posten 3c) b) Es wird mit Sauerstoff reagiert. (=> Posten 6b) c) Sie kann alleine in einer Reaktions- 9k) gleichungg
Posten 1a Was gilt immer bei einer Oxidation? a) Es werden Elektronen aufgenommen. (=> Posten 3c) b) Es wird mit Sauerstoff reagiert. (=> Posten 6b) c) Sie kann alleine in einer Reaktions- 9k) gleichungg
4. Quantitative Bestimmung von Eisen(II) durch Redoxtitration mit Kaliumpermanganat
 Redoxtitration 29. Quantitative Bestimmung von Eisen(II) durch Redoxtitration mit Kaliumpermanganat Einleitung Eisen ist das mit Abstand wichtigste Gebrauchsmetall. Aufgrund seines elektrochemisch sehr
Redoxtitration 29. Quantitative Bestimmung von Eisen(II) durch Redoxtitration mit Kaliumpermanganat Einleitung Eisen ist das mit Abstand wichtigste Gebrauchsmetall. Aufgrund seines elektrochemisch sehr
Analytische Chemie. B. Sc. Chemieingenieurwesen. 8. Juli 2015, Uhr. Prof. Dr. T. Jüstel, Stephanie Möller M. Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 8. Juli 2015, 12.30 15.30 Uhr Prof. Dr. T. Jüstel, Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Analytische Chemie B. Sc. Chemieingenieurwesen 8. Juli 2015, 12.30 15.30 Uhr Prof. Dr. T. Jüstel, Stephanie Möller M. Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges
Chemie Klausur SS Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren:
 Chemie Klausur SS14 1. Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren: b) Bestimmen Sie den isoelektrischen Punkt der Aminosäure Lysin (unterer Graph)! pks1 = 2,0 pks2 = 9,1
Chemie Klausur SS14 1. Aminosäuren (11.5 Punkte) a) Benennen Sie die unten stehenden Aminosäuren: b) Bestimmen Sie den isoelektrischen Punkt der Aminosäure Lysin (unterer Graph)! pks1 = 2,0 pks2 = 9,1
Redoxreaktionen. Elektrochemische Spannungsreihe
 Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Elektrochemische Spannungsreihe Eine galvanische Zelle bestehend aus einer Normal-Wasserstoffelektrode und einer anderen Halbzelle erzeugen eine Spannung, die, in 1-molarer Lösung gemessen, als Normal-
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP2 - Anionenreaktionen und Vorprobenanalyse» Martin Wolf Betreuerin: Frau Sachse Datum: 21.04.2006
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP2 - Anionenreaktionen und Vorprobenanalyse» Martin Wolf Betreuerin: Frau Sachse Datum: 21.04.2006
Analytische Chemie. B. Sc. Chemieingenieurwesen. 2. Februar 2016, Uhr. Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 2. Februar 2016, 14.00 17.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des
Analytische Chemie B. Sc. Chemieingenieurwesen 2. Februar 2016, 14.00 17.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des
Prüfbericht über Wasseruntersuchungen gemäß TrinkwV 2001
 Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
Zweckverband Wassererversorgung und Abwasserbeseitigung Grimmen Grellenberger Straße 6 1857 Grimmen Tel. ( 38326 ) 63- / Fax ( 38326 ) 63-12 Zweckverband Wasserversorgung und Abwasserbeseitigung Grimmen
6,
 ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
ph-wert 10,00 9,50 9,00 8,50 8,00 7,50 7,00 6,50 U:\13h\U135009_DGW_Änderung_Planfeststellung\02_Daten\Chemie\Wasser\Analyseberichte_neu\Sickerwasse_v03.xls Seite 1/18 Leitfähigkeit µs/cm 20000 15000 10000
Allgemeine Chemie I Herbstsemester 2011
 Lösung 2 Allgemeine Chemie I Herbstsemester 2011 1. Aufgabe Für die Berechnung der mittleren Atommasse m von Nickel sind die Massen m i der einzelnen Isotope i in ihrer Häufigkeit p i zu berücksichtigen.
Lösung 2 Allgemeine Chemie I Herbstsemester 2011 1. Aufgabe Für die Berechnung der mittleren Atommasse m von Nickel sind die Massen m i der einzelnen Isotope i in ihrer Häufigkeit p i zu berücksichtigen.
Anlage 3 zu Merkblatt Nr. 3.6/2 Stand: 01. Juli 2011
 Anlage 3 zu Merkblatt 3.6/2 Anlage 3 zu Merkblatt 3.6/2 Stand: 01. Juli 2011 Ansprechpartner: Referat 36 Wasserwirtschaftliche Überwachung von Abfallentsorgungsanlagen Parameterumfang / Analysenverfahren
Anlage 3 zu Merkblatt 3.6/2 Anlage 3 zu Merkblatt 3.6/2 Stand: 01. Juli 2011 Ansprechpartner: Referat 36 Wasserwirtschaftliche Überwachung von Abfallentsorgungsanlagen Parameterumfang / Analysenverfahren
Technisches Merkblatt
 Technisches Merkblatt Kaliumsulfat 93% K 2 SO 4 Kaliumsulfat K 2 SO 4 93 % Sonstige Sulfate (vorwiegend MgSO 4 ) MgSO 4 + 4 % Kaliumchlorid + Natriumchlorid KCl + NaCl 2 % Sonstiges vorwiegend H 2 O 1
Technisches Merkblatt Kaliumsulfat 93% K 2 SO 4 Kaliumsulfat K 2 SO 4 93 % Sonstige Sulfate (vorwiegend MgSO 4 ) MgSO 4 + 4 % Kaliumchlorid + Natriumchlorid KCl + NaCl 2 % Sonstiges vorwiegend H 2 O 1
Anhang 13. Resultate Oberflächenwasseranalysen. Ergebnistabellen sowie Grafiken N-Param. und TOC
 Anhang 13 Resultate Oberflächenwasseranalysen Ergebnistabellen sowie Grafiken N-Param. und Eigenkontrolle Rhein-Main Deponienachsorge GmbH Deponie Brandholz Oberflächenwassermessungen Betriebsjahr der
Anhang 13 Resultate Oberflächenwasseranalysen Ergebnistabellen sowie Grafiken N-Param. und Eigenkontrolle Rhein-Main Deponienachsorge GmbH Deponie Brandholz Oberflächenwassermessungen Betriebsjahr der
Maßanalyse. Bestimmung einer Schwefelsäure mit einer NaOH Maßlösung: bzw. n(naoh * 1 = n(h 2 SO 4 ) * 2 V [ml] * * t * 1 = n(h 2 SO 4 ) * 2
![Maßanalyse. Bestimmung einer Schwefelsäure mit einer NaOH Maßlösung: bzw. n(naoh * 1 = n(h 2 SO 4 ) * 2 V [ml] * * t * 1 = n(h 2 SO 4 ) * 2 Maßanalyse. Bestimmung einer Schwefelsäure mit einer NaOH Maßlösung: bzw. n(naoh * 1 = n(h 2 SO 4 ) * 2 V [ml] * * t * 1 = n(h 2 SO 4 ) * 2](/thumbs/79/78929570.jpg) Maßanalyse Bei der Maßanalyse (Volumetrie) wird zu der zu analysierenden Lösung unbekannten Gehaltes soviel einer Lösung bekannter Konzentration der Maßlösung zugegeben, bis ein Indikationssystem den Endpunkt
Maßanalyse Bei der Maßanalyse (Volumetrie) wird zu der zu analysierenden Lösung unbekannten Gehaltes soviel einer Lösung bekannter Konzentration der Maßlösung zugegeben, bis ein Indikationssystem den Endpunkt
Chemische-technische hygienische Parameter
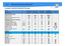 Chemische-technische hygienische Parameter Datum 13.04.2016 15.09.2016 12.04.2017 14.09.2017 Sensorische Prüfungen Färbung (vor Ort) farblos farblos farblos farblos Geruch (vor Ort) ohne ohne ohne ohne
Chemische-technische hygienische Parameter Datum 13.04.2016 15.09.2016 12.04.2017 14.09.2017 Sensorische Prüfungen Färbung (vor Ort) farblos farblos farblos farblos Geruch (vor Ort) ohne ohne ohne ohne
Kleine Formelsammlung Chemie
 Karl Schwister Kleine Forelsalung Cheie ISBN-1: 3-446-41545-9 ISBN-13: 978-3-446-41545-4 Leseprobe Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-41545-4 sowie i Buchhandel.
Karl Schwister Kleine Forelsalung Cheie ISBN-1: 3-446-41545-9 ISBN-13: 978-3-446-41545-4 Leseprobe Weitere Inforationen oder Bestellungen unter http://www.hanser.de/978-3-446-41545-4 sowie i Buchhandel.
Trinkwasseranalyse Qualitätsdaten des Trinkwassers aus der Kaufbeurer Wasserversorgung - Jahresmittelwerte
 Trinkwasseranalyse 2016 Qualitätsdaten des Trinkwassers aus der Kaufbeurer Wasserversorgung - Jahresmittelwerte Mikrobiologische Parameter, Anlage 1 - Teil 1 Escherichia coli (E.coli) Anzahl/100 ml 0 0
Trinkwasseranalyse 2016 Qualitätsdaten des Trinkwassers aus der Kaufbeurer Wasserversorgung - Jahresmittelwerte Mikrobiologische Parameter, Anlage 1 - Teil 1 Escherichia coli (E.coli) Anzahl/100 ml 0 0
Darstellung und Charakterisierung zweier Modifikationen von (CuI) 2 (µ 2-2-Ethylpyrazin-N,N )
 Versuch F3 Darstellung und Charakterisierung zweier Modifikationen von (CuI) 2 (µ 2-2-Ethylpyrazin-N,N ) Einführung Der Begriff Polymorphie bezeichnet die Eigenschaft chemischer Verbindung in mehreren
Versuch F3 Darstellung und Charakterisierung zweier Modifikationen von (CuI) 2 (µ 2-2-Ethylpyrazin-N,N ) Einführung Der Begriff Polymorphie bezeichnet die Eigenschaft chemischer Verbindung in mehreren
Rechnen mit Gehaltsgrößen
 Rechnen mit Gehaltsrößen Herstellen von Lösunen und Umrechnen von Gehaltsrößen 1. Es sollen 750 ml Natriumcarbonat-Lösun mit c= 0, /L herestellt werden. a Welche Masse an Na CO ist einzuwieen? b Welche
Rechnen mit Gehaltsrößen Herstellen von Lösunen und Umrechnen von Gehaltsrößen 1. Es sollen 750 ml Natriumcarbonat-Lösun mit c= 0, /L herestellt werden. a Welche Masse an Na CO ist einzuwieen? b Welche
Trinkwasseranalyse 2017
 Trinkwasseranalyse 2017 Qualitätsdaten des Trinkwassers aus der Kaufbeurer Wasserversorgung Jahresmittelwerte aus dem Verteilungsnetz Schieberkeller im Hochbehälter Oberbeuren Mikrobiologische Parameter,
Trinkwasseranalyse 2017 Qualitätsdaten des Trinkwassers aus der Kaufbeurer Wasserversorgung Jahresmittelwerte aus dem Verteilungsnetz Schieberkeller im Hochbehälter Oberbeuren Mikrobiologische Parameter,
6. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 6. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 6. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
Analytische Chemie. B. Sc. Chemieingenieurwesen. 13. September 2016, Uhr. Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc.
 Analytische Chemie B. Sc. Chemieingenieurwesen 13. September 2016, 8.00 11.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Analytische Chemie B. Sc. Chemieingenieurwesen 13. September 2016, 8.00 11.00 Uhr Prof. Dr. Thomas Jüstel, Stephanie Möller M.Sc. Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP1 - Vorprobenreaktionen» Martin Wolf Betreuerin: Frau Sachse Datum: 07.04.2006 8:00 Uhr bis 12:00
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP1 - Vorprobenreaktionen» Martin Wolf Betreuerin: Frau Sachse Datum: 07.04.2006 8:00 Uhr bis 12:00
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2012/13 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2012/13 vom 21.09.2012 A1 A2 A3 A4 A5 Σ Note 14 10 9 8 9 50 NAME/VORNAME:... Lösungsstichpunkte Pseudonym für Ergebnisveröffentlichung:... Schreiben
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2012/13 vom 21.09.2012 A1 A2 A3 A4 A5 Σ Note 14 10 9 8 9 50 NAME/VORNAME:... Lösungsstichpunkte Pseudonym für Ergebnisveröffentlichung:... Schreiben
Lösung Sauerstoff: 1s 2 2s 2 2p 4, Bor: 1s 2 2s 2 2p 1, Chlor: 1s 2 2s 2 2p 6 3s 2 3p 5 Neon: 1s 2 2s 2 2p 6
 1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
1 of 6 10.05.2005 10:56 Lösung 1 1.1 1 mol Natrium wiegt 23 g => 3 mol Natrium wiegen 69 g. 1 mol Na enthält N A = 6.02 x 10 23 Teilchen => 3 mol enthalten 1.806 x 10 24 Teilchen. 1.2 Ein halbes mol Wasser
Übung 6 Plausibilitätstest Gruppe 1, 4
 Übung 6 Plausibilitätstest Gruppe 1, 4 Gegeben ist folgende Wasseranalyse [Konzentrationen in mg/l]: LF 390 µs/cm temp 71.6 ph.1 pe 9.4 F.1 Cl 30 Br 0.17 N(+5) 0.018 as NO3- S(+6) 1350 as SO4- C(+4) 3.5
Übung 6 Plausibilitätstest Gruppe 1, 4 Gegeben ist folgende Wasseranalyse [Konzentrationen in mg/l]: LF 390 µs/cm temp 71.6 ph.1 pe 9.4 F.1 Cl 30 Br 0.17 N(+5) 0.018 as NO3- S(+6) 1350 as SO4- C(+4) 3.5
5. Seminar. Prof. Dr. Christoph Janiak. Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002
 ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 5. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
ALBERT-LUDWIGS- UNIVERSITÄT FREIBURG 5. Seminar Prof. Dr. Christoph Janiak Literatur: Jander,Blasius, Lehrb. d. analyt. u. präp. anorg. Chemie, 15. Aufl., 2002 Riedel, Anorganische Chemie, 5. Aufl., 2002
Universität Regensburg
 Universität Regensburg Fakultät für Chemie und Pharmazie 93040 Regensburg 14. März 2006 Institut für Anorganische Chemie Prof. Dr. R. Winter 1. Was besagt das Moseleysche Gesetz? Welche Größe kann man
Universität Regensburg Fakultät für Chemie und Pharmazie 93040 Regensburg 14. März 2006 Institut für Anorganische Chemie Prof. Dr. R. Winter 1. Was besagt das Moseleysche Gesetz? Welche Größe kann man
Grundwasser: chemische Vorgänge bei der Infiltration. Redoxprozesse im Grundwasser Transport reaktiver Spezies
 Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Übung 6 Plausibilitätstest Gruppe 1,4
 Übung 6 Plausibilitätstest Gruppe 1,4 Gegeben ist folgende Wasseranalyse [Konzentrationen in mg/l]: LF 1360 µs/cm temp 6.4 ph 3.4 pe 7.7 F 1.6 Cl 193 Br 0.69 N(+5) 0.018 as NO3- S(+6) 338 as SO4- C(+4)
Übung 6 Plausibilitätstest Gruppe 1,4 Gegeben ist folgende Wasseranalyse [Konzentrationen in mg/l]: LF 1360 µs/cm temp 6.4 ph 3.4 pe 7.7 F 1.6 Cl 193 Br 0.69 N(+5) 0.018 as NO3- S(+6) 338 as SO4- C(+4)
Trennungsgang. AC-I Seminar, B.
 Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Lernzielkontrolle Sekunda
 Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (15) Richtzeit: 25 Minuten 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) Manche
Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (15) Richtzeit: 25 Minuten 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) Manche
Universität des Saarlandes - Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum. Elektrochemie
 Universität des Saarlandes Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb der Chemie. Sie ist zum einen
Universität des Saarlandes Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb der Chemie. Sie ist zum einen
6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser
 Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 35 6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 6.1. Natriumsilikatglas Nach dem Ionenaustausch folgten Temperaturbehandlungen zwischen
Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 35 6. Temperaturbehandlung Ag/Na-ionenausgetauschter Gläser 6.1. Natriumsilikatglas Nach dem Ionenaustausch folgten Temperaturbehandlungen zwischen
Aufgabe Punkte (je 10) Anorganisches Grund-Praktikum (Lehramt/2-Fach Bachelor) Abschlußklausur (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt/2-Fach
Aufgabe 1 2 3 4 5 6 7 8 9 10 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Anorganisches Grund-Praktikum (Lehramt/2-Fach
Analytische Chemie. B. Sc. Chemieingenieurwesen. 17. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 17. März 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 17. März 2010 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Das 3 Seiten umfassende Gutachten bildet eine Einheit und darf ohne schriftliche Genehmigung nicht auszugsweise veröffentlicht werden.
 Gutachten 141441G Gutachten über die Trinkwasseruntersuchung für Gemeinde Feistritz bei Knittelfeld Das 3 Seiten umfassende Gutachten bildet eine Einheit und darf ohne schriftliche Genehmigung nicht auszugsweise
Gutachten 141441G Gutachten über die Trinkwasseruntersuchung für Gemeinde Feistritz bei Knittelfeld Das 3 Seiten umfassende Gutachten bildet eine Einheit und darf ohne schriftliche Genehmigung nicht auszugsweise
Übungen zum Kapitel I, Grundlagen chemischer Gleichungen
 Übungen zum Kapitel I, Grundlagen chemischer Gleichungen Übersicht der Übungen: Übung Nr. 1 (Bedeutungen und Ausgleichen von Gleichungen) Übung Nr. 2 (Bedeutungen und Ausgleichen von Gleichungen) Übung
Übungen zum Kapitel I, Grundlagen chemischer Gleichungen Übersicht der Übungen: Übung Nr. 1 (Bedeutungen und Ausgleichen von Gleichungen) Übung Nr. 2 (Bedeutungen und Ausgleichen von Gleichungen) Übung
Chemie aquatischer Systeme. Herbstsemester 2013
 Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Tonminerale. Technische Mineralogie, J. Majzlan
 Tonminerale Technische Mineralogie, J. Majzlan Tonminerale sind die Schichtsilikate, die in Partikeln kleiner als 2 µm vorkommen. Diese Denition ist operativ, d.h. dass sie auf keinen natürlichen Gesetzen,
Tonminerale Technische Mineralogie, J. Majzlan Tonminerale sind die Schichtsilikate, die in Partikeln kleiner als 2 µm vorkommen. Diese Denition ist operativ, d.h. dass sie auf keinen natürlichen Gesetzen,
2.Klausur Chemisches Rechnen 21. Januar 2013
 2.Klausur Chemisches Rechnen 21. Januar 2013 Name: Matrikelnr.: Dauer: 90 min. Maximal erreichbare Punkte: 40 Punkte 1 Sehr gut: 40 35.5 Punkte 2 Gut: 35 30.5 Punkte 3 Befriedigend: 30 25.5 Punkte 4 Genügend:
2.Klausur Chemisches Rechnen 21. Januar 2013 Name: Matrikelnr.: Dauer: 90 min. Maximal erreichbare Punkte: 40 Punkte 1 Sehr gut: 40 35.5 Punkte 2 Gut: 35 30.5 Punkte 3 Befriedigend: 30 25.5 Punkte 4 Genügend:
