|
|
|
- Katharina Schuler
- vor 5 Jahren
- Abrufe
Transkript
1
2
3
4
5
6
7
8
9
10 Regelwerk zur Norm DIN EN ISO 9001:2015 Inhaltsverzeichnis 0 Geforderte Nachweise nach DIN EN ISO 9001: Kontext der Organisation Verstehen der Organisation und ihres Kontextes Verstehen der Erfordernisse und Erwartungen interessierter Parteien Qualitätsmanagementsystem und dessen Prozesse Planung Maßnahmen zum Umgang mit Risiken und Chancen Kundenzufriedenheit Fortlaufende Verbesserung Geforderte Nachweise nach DIN EN ISO 9001:2015 Gefordert in DIN EN ISO 9001:2015 Anwendungsbereich des Qualitätsmanagementsystems Im Handbuch ISO realisiert in: Kapitel 1 Anwendungsbereich Notwendige Prozesse Qualitätspolitik Qualitätsziele Verwendete Ressourcen Kalibriernachweise Kompetenznachweise Dieses Regelwerk Kapitel 5.3 Qualitätspolitik Kapitel Qualitätsziele Kapitel 6.3 Infrastruktur Kapitel 7.6 Lenkung von Überwachungs- und Messmitteln Kapitel 6.2 Personelle Ressourcen Informationen zur Dokumentenlenkung Kapitel Lenkung von Dokumenten und Lenkung von Aufzeichnungen Dokumente zur betrieblichen Planung und Kapitel 7.1 Planung der Produktrealisierung Steuerung Ergebnisse der Auftragsprüfung Produkt- und Dienstleistungsanforderungen Entwicklungsnachweise, Entwicklungseingaben Kapitel 7.2 Kundenbezogene Prozesse Kapitel 7.5 Produktions- und Dienstleistungsrealisierung Kapitel Lenkung der Produktion und Dienstleistungsrealisierung Kapitel Sauberkeit von Produkten Kapitel Tätigkeiten bei der Installation Kapitel Tätigkeiten zur Instandhaltung Kapitel Produkterhaltung Kapitel 7.3 Entwicklung QM-Verlag, Revision 0, Seite 1 von 4, gültig ab xx.xx.xxxx
11 Regelwerk zur Norm DIN EN ISO 9001:2015 Gefordert in DIN EN ISO 9001:2015 Steuerungsmaßnahmen der Entwicklung Entwicklungsänderungen Maßnahmen aus Anbieteranfragen Produktions- und oder Dienstleistungsnachweise Informationen zur Rückverfolgbarkeit Maßnahmen aus Verlust und Beschädigung von Kunden- und Anbietereigentum Ergebnisse aus Prüfungen von Änderungen Produkt- und Dienstleistungsfreigaben Unterlagen zu Nichtkonformitäten Nachweise der Leistungsbewertung Methodennachweise zur Kundenzufriedenheitserfassung Ergebnisse der Managementbewertung Arten von Nichtkonformitäten, getroffene Maßnahmen und Ergebnisse Im Handbuch ISO realisiert in: Kapitel Entwicklungsplanung Kapitel Entwicklungseingaben Kapitel Entwicklungsergebnisse Kapitel Entwicklungsakten Kapitel 7.3 Entwicklung Kapitel Entwicklungsplanung Kapitel Lenkung von Entwicklungsänderungen Kapitel Beschaffungsangaben Kapitel Wareneingang / Verifizierung Beschaffung Kapitel Erfassung und Messung von Prozessen Kapitel Erfassung und Messung des Produktes Kapitel Identifikation Kapitel Rückverfolgbarkeit Kapitel Eigentum des Kunden Kapitel Planung des Qualitätsmanagements Kapitel Erfassung und Messung von Prozessen Kapitel Erfassung und Messung des Produktes Kapitel Maßnahmen als Reaktion auf vor der Auslieferung festgestellte nichtkonforme Produkte Kapitel Maßnahmen als Reaktion auf nach der Auslieferung festgestellte nichtkonforme Produkte Kapitel Nacharbeit Kapitel 8.4 Datenanalyse Dieses Regelwerk Kapitel Allgemeines Kapitel Eingaben für die Bewertung Kapitel Ergebnisse der Bewertung Kapitel Korrekturmaßnahmen 4 Kontext der Organisation 4 1 Verstehen der Organisation und ihres Kontextes Unsere wirtschaftlichen Rahmenbedingungen sind für die strategische Ausrichtung relevant. Die Themen zur Erreichung der beabsichtigten Ergebnisse sind in externe und interne Zusammenhänge unterteilt. Die Themen werden laufend, formell aber jährlich geprüft und überwacht. Werden zwischen den Überwachungen neue Themen erkannt, so werden diese umgehend umgesetzt. QM-Verlag, Revision 0, Seite 2 von 4, gültig ab xx.xx.xxxx
12 Dokumentationen Musterhandbuch Medizin DIN EN ISO 13485:2016 & DIN EN ISO 9001:2015 Prozesse
13 Weitere Prozesse auf der CD: Validierung Software Lenkung externer Dokumente Lenkung von Dokumenten Lenkung von Qualitätsaufzeichnungen Vertrauliche Informationen Qualitätspolitik Qualitätsziele Interne Kommunikation Managementbewertung Bereitstellung von Ressourcen Planung Produktionsmittel Einführung neuer Mitarbeiter Einstellung Erforderliche Ausbildung Schulungen Weiterbildung Externe Wartungen Interne Wartungen Erfassen von Arbeitsbedingungen Arbeitsvorbereitung Risikomanagement Produktion Angebotserstellung Auftragsabwicklung Auftragsänderung Vertrieb Risikomanagement Entwicklungsplanung Entwicklungseingaben Entwicklungsergebnisse Technische Dokumentation Übersetzung Entwicklungsbewertung Entwicklungsverifizierung Entwicklungsvalidierung Übertragung Entwicklung Entwicklungsänderung Auswahl Lieferanten Beschaffung Prüfmittel Beschaffung Lieferantenaudit Lieferantenbewertung Lieferantenkommunikation Rahmenverträge Wareneingang Dienstleistung Produktion / Installation Instandhaltung Sterilisation Prozessvalidierung Prozessvalidierung Sterilisation Anlieferung Identifizierung Rücklieferungen Rückverfolgbarkeit Eigentum des Kunden Einlagern Verpackung Versand Überwachung Messmittel Kundenzufriedenheit Rückmeldungen Reklamationsbearbeitung Internes Audit Besondere Prüfungen Externe Prüfung / Labor Planung Prüfungen Serienprüfung Verifizierung Produktion Lenkung nichtkonformer Produkte Rückruf Meldung Behörden Empfehlungen und Maßnahmen nach Auslieferung Nacharbeit Datenanalyse Planung Verbesserung Korrekturmaßnahmen Vorbeugemaßnahmen ISO Ermittlung Chancen und Risiken
14 4.2.4 Lenkung externer Dokumente Dokumentationen MW VA Ablauf / Tätigkeiten Dokumente Ablauf Hilfsmittel Start MA GF Zugang Externe Dokumente Scannen und Vorlage an Leitung. MA GF Prüfung Externe Dokumente Prüfen auf Relevanz und notwendige Maßnahmen. Maßnahme notwendig? MA GF Ja Korrekturmaßnahme Korrekturmaßnahmen / zugrunde liegendes Dokument Erstellung Korrekturmaßnahmen und Informieren der Beteiligten. Nein MA GF Schulung / Information Dokument Durchführung einer Schulung oder Information, wenn dies notwendig ist. MA GF Ablage Ablage Verwaltung Ablage gemäß Handbuch Kapitel Ende MW = Mitwirkung VA = Verantwortung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
15 Dokumentationen Qualitätsziele MW VA Ablauf / Tätigkeiten Dokumente Ablauf / Hilfsmittel Start GF Qualitätsziele erreicht? Prüfung alter / bestehender Qualitätsziele Nein PA Korrekturmaßnahmen Qualitätsziele PA Korrekturmaßnahmen Die qualifizierbaren Qualitätsziele werden auf ihre Erreichung überprüft. Bei der Überwachung wird geprüft, ob die gesetzten Ziele erreicht werden können. Verfahren gemäß PA Korrekturmaßnahmen. Abt.- Ja Abteilungen beteiligt? Informationssammlung Ja Nein Qualitätsziele, Managementbewertung, Verpflichtung der Leitung / Qualitätspolitik Qualitätsziele werden einmal jährlich anhand der beschriebenen Dokumente und Auswertungen erstellt. Befragung der Leitungsfunktionen. GF PA Korrekturmaßnahmen Abt.- Abt.- GF Abt.- GF Ziele im Einklang mit der Qualitätspolitik? Ja Verbesserung beachtet? Ja Stehen die Qualitätsziele im Einklang mit dem Produkt? Ja Erstellung der Qualitätsziele Abgabe der Qualitätsziele (Entwurf) Nein Nein Nein PA Korrekturmaßnahmen Qualitätsziele, ENTWURF PA Korrekturmaßnahmen Qualitätsziele, ENTWURF Qualitätsziele, ENTWURF Qualitätsziele, ENTWURF Vergleich mit der Qualitätspolitik und ggf. Rücksprache mit der GF. Die Qualitätsziele enthalten immer Verbesserungsziele Verfahren gemäß PA Korrekturmaßnahmen. Die Qualitätsziele müssen im Einklang mit der Produktstrategie stehen. Erstellung der Qualitätsziele im Entwurf unter Berücksichtigung der Machbarkeit. Der Entwurf wird 14 Tage zur Prüfung ausgegeben. Schweigen bedeutet, dass die Ziele angenommen wurden. Gegebenenfalls mit Absprache GF. GF Qualitätsziele sind realistisch und erreichbar? Ja Nein Der hängt die Qualitätsziele gut sichtbar aus. Die Leitungen schulen die Mitarbeiter, laufende Überwachung der Qualitätsziele. Abt.- Aushang / Verteilung / Überwachung Qualitätsziele ENDE MW = Mitwirkung VA = Verantwortung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
16 Dokumentationen Planung Produktionsmittel MW VA Ablauf / Tätigkeiten Dokumente Ablauf / Hilfsmittel Start Prod. Bedarf an notwendigen Produktionsmittel Korrekturmaßnahmen Bedarf durch Verschrottung, neue Prozesse, Folgemaßnahmen aus Fehlerauswertungen, Umsatzsteigerungen, Produktionsvorgaben etc.. Prod. Vorläufigen Finanzbedarf feststellen Investitionsplan, Geschäftsplan Unter Umständen aufgrund von Umfragen oder vorläufigen Kostenbedarfsanalysen. Entw. GF Prod. Mittel zur Beschaffung vorhanden? Ja Nein Anforderungen an Produktionsmittel festlegen Abgabe Entwicklung Korrekturmaßnahmen Korrekturmaßnahmen Die Entwicklung stellt fest, ob auch andere Möglichkeiten in Betracht gezogen werden können, wie z.b. andere Verfahren oder externe Vergabe. Die Anforderungen werden detailliert erfasst und bei einer erheblichen Investition in einem Lastenheft schriftlich niedergelegt. Prod. PA Auswahl Lieferanten PA Auswahl Lieferanten Verfahren gemäß PA Auswahl Lieferanten. Prod. PA Lieferantenbewertung PA Lieferantenbewertung Verfahren gemäß PA Lieferantenbewertung. GF Wird das Produktionsmittel beschafft? Nein Korrekturmaßnahmen In die Entscheidung fließen finanzielle, sicherheitstechnische, terminliche und praktizierbare Aspekte mit ein. Entw. Entw. Prod. Prod. Ja Validierung des Produktionsmittels Produktionsmittel für die Serie geeignet? Nein PA Korrekturmaßnahmen FB Wareneingang PA Korrekturmaßnahmen Nach bzw. während Entwicklung / Anlieferung des Produktionsmittels wird die Eigenschaft detailliert geprüft. Gegebenenfalls hat das Problem mehrere Maßnahmen zur Folge. Ja Prod. Datenpflege Alle Unterlagen Freigabe des Produktionsmittels, Abgabe Rechnung an Verwaltung, Erstellung der Wartungsanweisung, Einführung Mitarbeiter, ggf. Abschluss Wartungsvertrag etc.. ENDE MW = Mitwirkung VA = Verantwortung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
17 Dokumentationen Schulungen MW VA Ablauf / Tätigkeiten Dokumente Ablauf / Hilfsmittel Start MA Suche Ausbildungsträger Ausbildungs- & Befugnismatrix Gegebenenfalls durch bestehendes Angebot oder Ausschreibung, Suche nach internem Ausbilder. Abt. Ltg, Ma Träger geeignet? Nein Spezifizierung der Abteilung Angebote, Notizen Der Träger muss neben den Kosten auch die fachliche Kompetenz nachweisen, nähere Spezifizierung durch den Abteilungsleiter. Ja Vertragliche Bindung Vertrag Mit Definition des Ausbildungsziels und den Kosten. Bei internem Träger keine vertragliche Bindung. PA Korrekturmaßnahmen PA Korrekturmaßnahmen Verfahren gemäß PA Korrekturmaßnahmen. Externe / interne Träger Durchführung Schulung Schulungsunterlagen Durchführung der Schulung mit Erfassung Feedback. Abt. Ltg, Ma Ausbildungsziel erreicht? Ja Nein Maßnahmen erstellen Korrekturmaßnahmen Wenn das Schulungsziel nicht erreicht wurde, wird der Fehler durch den eingegrenzt und geeignete Maßnahmen festgelegt. Datenpflege Alle Unterlagen Nachweis der Ausbildung in der Personalakte, ggf. Aktualisierung der Ausbildungs- & Befugnismatrix. ENDE MW = Mitwirkung VA = Verantwortung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
18 Dokumentationen Risikomanagement Produktion MW VA Ablauf / Tätigkeiten Dokumente Ablauf / Hilfsmittel Start Entw. Prod. Produkte stehen erstmalig zur Produktion an Informationen aus der Entwicklung Zusammenstellen der Informationen. Entw. Prod. Gefahren ableiten Anweisungen, Datenblätter, Hinweise Mögliche Gefahren in Bezug auf die Produktqualität, der Gesundheit und Sicherheit ableiten und Listen. Entw. SiBe Prod. Risiken einschätzen Anweisungen, Datenblätter, Hinweise, Risiken Maßnahmen Ggf. mittels FMEA oder Befragung. Entw. Prod. Minderung des Risikos erforderlich? Ja Nein Risiken Maßnahmen Erforderlich ist die Minderung wenn zu vertretbaren Konditionen das Risiko minimiert werden kann. Entw. Prod. Risikokontrolle festlegen und aufzeichnen Risiken Maßnahmen Kurze Beschreibung wie das Risiko kontrolliert werden kann. Entw. Prod. Geeignete Maßnahmen durchführen Risiken Maßnahmen Beschreibung der Maßnahmen mit Anweisungen für die einzelnen Bereiche. SiBe Gesamtrisiko vertretbar? Ja Nein ENTWICKLUNG Risiken Maßnahmen Vertretbar bedeutet keine Gefahren in Bezug auf die Produktqualität, der Gesundheit und Sicherheit. Entw. Prod. Dokumentation Alle Unterlagen Dokumentation der Maßnahmen in Form von Umsetzungen in Arbeitsanweisungen, Prüfanweisungen, Schulungen. SiBe Prod. Prüfung der Informationen aus der Produktion Neubewertung erforderlich? Auswertungen Auswertung der laufenden Ergebnisse und Bewertung von neuen regulatorischen Anforderungen. Ja Nein MW = Mitwirkung VA = Verantwortung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
19 Dokumentationen Wareneingang MW VA Ablauf / Tätigkeiten Dokumente Ablauf / Hilfsmittel Start MA Anlieferung Lieferschein Ware ohne Lieferschein oder Anschreiben wird nicht angenommen. MA Bestimmung im Unternehmen festlegen Lieferschein Die Abteilung, welche die Ware erhalten soll, wird bestimmt. Einkauf MA Unterliegt die Ware einer Prüfung? Ja Nein Arbeitsanweisung Wareneingang Prod. MA MA Ist die Ware voll verwendungsfähig? Prüfung gemäß Prüfliste Ja Nein Reklamation der Ware Lieferschein, Matrix Wareneingang Lieferschein, Matrix Wareneingang Die Prüfungen werden gemäß der Matrix Wareneingangsprüfung durchgeführt. Die Ware ist voll verwendungsfähig, wenn die geforderten Prüfungen bestanden wurden. Beim Lieferant wird mittels Bericht schriftlich reklamiert. Verbringung Sperrlager Sperrzettel, Lieferschein Die Ware wird im Sperrlager gelagert bis der Vorgang bereinigt wurde. Einkauf MA Kennzeichnung / Buchung Lieferschein, Software Die Ware wird im Bestand gebucht. Einkauf MA Weiterleitung Unterlagen Lieferschein Übergabe der Unterlagen zur weiteren Verfolgung / Bezahlung. ENDE MW = Mitwirkung VA = Verantwortung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
20 Dokumentationen Musterhandbuch Medizin DIN EN ISO 13485:2016 & DIN EN ISO 9001:2015 Arbeitsanweisungen
21 Weitere Arbeitsanweisungen auf der CD: Erstellen von Dokumenten Verunreinigte Produkte Angebotserstellung Auswahl Lieferanten Regeln der Beschaffung Wareneingang Rückverfolgbarkeit Produkterhaltung Umgang mit Prüfmitteln
22 Dokumentation Arbeitsanweisung Erstellen von Dokumenten Inhaltsverzeichnis Grundlage...1 Gültigkeit...1 Ziel und Grund...1 Allgemeines...1 Abkürzungen...1 Forderungen...1 Grundlage Kapitel 4 Abschnitt "Lenkung von Dokumenten". Gültigkeit Die Anweisung umfasst den gesamten Betrieb. Ziel und Grund Ziel dieser Anweisung ist die Vereinheitlichung und eindeutige Regelung zur Erstellung und Pflege von Arbeitsanweisungen und Formblättern. Allgemeines Grundsätzlich ist die Geschäftsführung für die Erstellung von Arbeitsanweisungen und Formblättern zuständig. Die Freigabe der Dokumente wird durch den durchgeführt. Die Prüfung wird durch Handzeichen auf dem Skript dokumentiert. Wenn möglich, lässt der das Dokument von einer fachlich versierten Stelle gegenzeichnen. Diese Arbeitsanweisung dient als Muster. Abkürzungen GF Geschäftsführung Beauftragte(r) der Leitung Forderungen An ein Dokument / Formblatt in unserem Betrieb werden folgende formale Forderungen gestellt. Grundlagen Ein Dokument hat eine schriftliche Grundlage (in der Regel die zugrundeliegende Norm) und wird vom Verfasser für den individuellen Bereich begründet. Es definiert das angestrebte Ziel. Der Inhalt steht stets im Einklang mit den zugrundeliegenden Normen und wird somit vom auf die Verträglichkeit mit den Normenforderungen geprüft. QM-Verlag, Revision 0, Seite 1 von 2, gültig ab xx.xx.xxxx
23 Dokumentation Arbeitsanweisung Erstellen von Dokumenten Die Arbeitsanweisung bzw. das Formblatt sollen kurz, aber prägnant gehalten sein. Personen dürfen namentlich nicht erwähnt werden. Nur geläufige Abkürzungen sind geeignet. Zur einfachen Erkennung von Qualitätsaufzeichnungen, Arbeitsanweisungen und Formblättern unseres Unternehmens werden immer die Schriftarten Calibri verwendet, sofern ihre Gestaltung dies erlaubt. Alle anderen Unterlagen sowie persönliche Aufzeichnungen können in einer anderen Schriftart geschrieben werden. Alle wichtigen Listen werden in der Liste der Dokumente geführt. Sie wird im Firmennetzwerk zentral verwaltet und vom jeweiligen Bediener mit einem Passwort geschützt. Generell werden nur Leseberechtigungen vergeben. Erstellung Auftrags- und produktbezogene Dokumente werden von den jeweiligen Bereichen in Eigenverantwortung erstellt. Bereichsübergreifende Dokumente sind in Abstimmung mit allen betroffenen Bereichen zu erstellen. Bei Verwendung von EDV-Masken und -Formularen in Zusammenhang mit den verwendeten EDV-Systemen sind diese in den jeweiligen Systembeschreibungen aufzuführen. Jedes Dokument muss als Mindestangaben Titel, Dateiname und Ausgabestand enthalten. Der Dateiname entspricht gleichermaßen der Dokumentenkennzeichnung. Aus dem Dateinamen geht jeweils auch der Revisionstand hervor. Im Dateinamen wird auf Sonderzeichen wie Punkt, Komma, Ausrufezeichen usw. verzichtet. Prüfung/Freigabe Alle Managementdokumente (z.b. Kapitel des Managementhandbuchs, Verfahrens- und Arbeitsanweisungen, Checklisten, Formulare usw.) sind vor Verteilung von einer fachlich kompetenten und von der Dokumenterstellung unabhängigen Person auf inhaltliche Vollständigkeit und Praktizierbarkeit zu prüfen. Bei bereichsübergreifenden Dokumenten ist diese Prüfung von den Verantwortlichen aller betroffenen Bereiche durchzuführen. Die Freigabe von Dokumenten erfolgt durch die Geschäftsführung. Die Geschäftsführung kann hierzu einen Vertreter benennen (in der Regel den ). Der Ausgabestand wird fortgeführt und im Dateinamen sowie in der Liste der Dokumente geändert. Verteiler Für die Festlegung des Verteilers ist der / die verantwortlich. Der sofortige Einzug veralteter Dokumente unterliegt ebenfalls der Verantwortung der / dem. Entwicklungsdokumente werden gekennzeichnet und in der technischen Dokumentation abgelegt. Hier sind auch alle alten Versionen zu finden. Änderungen Auftrags- / produktbezogene Unterlagen dürfen nur vom Ersteller bzw. in Abstimmung mit dem erstellenden Bereich geändert werden. Die Ersteller der jeweiligen Dokumente sind verantwortlich für die Verteilung an alle betroffenen Bereiche. Geänderte Stellen sind in den Dokumenten deutlich zu kennzeichnen. Die Änderungen sind mit dem geänderten Dateinamen (Erhöhung des Revisionsstands) auf allen Seiten zu versehen. Veraltete Dokumente sind am Arbeitsplatz zu entfernen. Der archiviert jeweils ein Exemplar des vorherigen Revisionsstands. QM-Verlag, Revision 0, Seite 2 von 2, gültig ab xx.xx.xxxx
24 Dokumentationen Musterhandbuch Medizin DIN EN ISO 13485:2016 & DIN EN ISO 9001:2015 Formblätter Nachweise
25 Weitere Formblätter / Nachweise auf der CD: Dokumentationsebenen (eingebunden in Kapitel 4) QSV kritische Prozesse Softwarevalidierung Wechselwirkungen der Prozesse Liste der Dokumente Liste der Dokumente Produktakte Auflistung der Aufzeichnungen / Verpflichtung der Leitung / Qualitätspolitik Qualitätsziele Organisationsdiagramm Verantwortungen und Befugnisse Benennungsschreiben Liste Kommunikationswege Notfallplan Bewertung Aktualität Technische Dokumentation Managementbewertung Schweigepflicht Ausbildungs- und Befugnismatrix Einarbeitungsplan Personalgespräch Stellenbeschreibung Unterweisungsnachweis Infrastruktur Liste der Maschinen Wartungsaufzeichnung Wartungsnachweis Abfallplan Präventionskonzept Sauberkeitskonzept Prozesskette / Qualitätsplan Risiken Maßnahmen Liste der CE-gekennzeichneten Produkte Liste der aktuellen Entwicklungen Fehlermöglichkeits- & Einflussanalyse (FMEA) Verifizierungsplan Entwicklungsvalidierung Übertragung Entwicklung Checkliste Entwicklungsänderungen Ausgegliederte Prozesse Checkliste Lieferanten Lieferantenbewertung Chargenprotokoll Tätigkeiten Installation Instandhaltung Produkt Prozessänderungen Prozessvalidierung Begleitblatt Produktstatus Prüfgerätekartei Kundenzufriedenheit Reklamationen Rückmeldungen Auditabweichung Auditbericht Auditcheckliste Lieferanten Auditcheckliste Auditplan Auditprogramm Prüfplan Fehlerliste Lenkung konformer Produkte Sonderfreigaben Maßnahmenempfehlungen Nacharbeit / Nachbesserungen Datenanalyse Verbesserungen / Korrektur- und Vorbeugemaßnahmen ISO Kontext ISO Kontext Erfordernisse und Erwartungen ISO Chancen und Risiken
26 4.2.4 Liste der Dokumente Das Handbuch ist vorbelegt. Dokumentation Art Revision Kritisch? vom Ersteller/-in Verteiler Grund der letzten Änderung Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 Kapitel 3 Begriffe Abkürzungen 0 Kapitel 4 Qualitätsmanagementsystem 0 Kapitel 5 Verantwortung der Leitung 0 Kapitel 6 Management von Ressourcen 0 Kapitel 7 Produktions- und Dienstleistungserbringung 0 Kapitel 8 Messung, Analyse & Verbesserung 0 Prozessbeschreibung / Verfahren Validierung Software Lenkung externer Dokumente Lenkung von Dokumenten Lenkung von Qualitätsaufzeichnungen Vertrauliche Informationen Qualitätspolitik Qualitätsziele Interne Kommunikation Managementbewertung Bereitstellung von Ressourcen Planung Produktionsmittel Einführung neuer Mitarbeiter Einstellung Erforderliche Ausbildung Schulungen Weiterbildung Externe Wartungen Interne Wartungen 0 QM-Verlag, Revision 0, Seite 1 von 6, gültig ab xx.xx.xxxx
27 4.2.4 Liste der Dokumente Das Handbuch ist vorbelegt. Dokumentation Art Revision Kritisch? vom Ersteller/-in Verteiler Grund der letzten Änderung Erfassen von Arbeitsbedingungen Arbeitsvorbereitung Risikomanagement Produktion Angebotserstellung Auftragsabwicklung Auftragsänderung Vertrieb Risikomanagement Entwicklungsplanung Entwicklungseingaben Entwicklungsergebnisse Technische Dokumentation Übersetzung Entwicklungsbewertung Entwicklungsverifizierung Entwicklungsvalidierung Übertragung Entwicklung Entwicklungsänderung Auswahl Lieferanten Beschaffung Prüfmittel Beschaffung Lieferantenaudit Lieferantenbewertung Lieferantenkommunikation Rahmenverträge Wareneingang Dienstleistung Produktion / Installation Instandhaltung 0 QM-Verlag, Revision 0, Seite 2 von 6, gültig ab xx.xx.xxxx
28 4.2.4 Liste der Dokumente Das Handbuch ist vorbelegt. Dokumentation Art Revision Kritisch? vom Ersteller/-in Verteiler Grund der letzten Änderung Sterilisation Prozessvalidierung Prozessvalidierung Sterilisation Anlieferung Identifizierung Rücklieferungen Rückverfolgbarkeit Eigentum des Kunden Einlagern Verpackung Versand Überwachung Messmittel Kundenzufriedenheit Rückmeldungen Reklamationsbearbeitung Internes Audit Besondere Prüfungen Externe Prüfungen / Labor Planung Prüfungen Serienprüfungen Verifizierung Produktion Lenkung nichtkonformer Produkte Rückruf Meldung Behörden Empfehlungen und Maßnahmen nach Auslieferung Nacharbeit Datenanalyse Planung Verbesserung Korrekturmaßnahmen Vorbeugemaßnahmen 0 QM-Verlag, Revision 0, Seite 3 von 6, gültig ab xx.xx.xxxx
29 4.2.4 Liste der Dokumente Das Handbuch ist vorbelegt. Dokumentation Art Revision Kritisch? vom Ersteller/-in Verteiler Grund der letzten Änderung Arbeitsanweisung Erstellen von Dokumenten verunreinigte Produkte Angebotserstellung Auswahl Lieferanten Regeln der Beschaffung Wareneingang Rückverfolgbarkeit Produkterhaltung Umgang mit Prüfmitteln 0 Formblatt Dokumentationsebenen (eingebunden in Kapitel 4) QSV kritische Prozesse Softwarevalidierung Wechselwirkungen der Prozesse Liste der Dokumente (diese Datei) Liste der Dokumente Produktakte Auflistung der Aufzeichnungen / Verpflichtung der Leitung / Qualitätspolitik Qualitätsziele Organisationsdiagramm Verantwortungen und Befugnisse Benennungsschreiben Liste Kommunikationswege Notfallplan Bewertung Aktualität Technische Dokumentation Managementbewertung 0 QM-Verlag, Revision 0, Seite 4 von 6, gültig ab xx.xx.xxxx
30 4.2.4 Liste der Dokumente Das Handbuch ist vorbelegt. Dokumentation Art Revision Kritisch? vom Ersteller/-in Verteiler Grund der letzten Änderung Ausbildungs- und Befugnismatrix Einarbeitungsplan Personalgespräch Stellenbeschreibung Unterweisungsnachweis Schweigepflicht Infrastruktur Liste der Maschinen Wartungsaufzeichnung Wartungsnachweis Abfallplan Präventionskonzept Sauberkeitskonzept Prozesskette / Qualitätsplan Risiken Maßnahmen Liste der CE-gekennzeichneten Produkte Liste der aktuellen Entwicklungen Fehlermöglichkeits- & Einflussanalyse (FMEA) Verifizierungsplan Entwicklungsvalidierung Übertragung Entwicklung Checkliste Entwicklungsänderungen Ausgegliederte Prozesse Checkliste Lieferanten Lieferantenbewertung Chargenprotokoll Tätigkeiten Installation Instandhaltung Produkt Prozessänderungen 0 QM-Verlag, Revision 0, Seite 5 von 6, gültig ab xx.xx.xxxx
31 4.2.4 Liste der Dokumente Das Handbuch ist vorbelegt. Dokumentation Art Revision Kritisch? vom Ersteller/-in Verteiler Grund der letzten Änderung Prozessvalidierung Begleitblatt Produktstatus Prüfgerätekartei Kundenzufriedenheit Reklamationen Rückmeldungen Auditabweichung Auditbericht Auditcheckliste Lieferanten Auditcheckliste Auditplan Auditprogramm Prüfplan Fehlerliste Lenkung nichtkonformer Produkte Sonderfreigaben Maßnahmenempfehlungen Nacharbeit / Nachbesserungen Datenanalyse Verbesserungen / Korrektur- und Vorbeugemaßnahmen Korrekturmaßnahmen 0 Liste geprüft und freigegeben: Datum: Funktion, Unterschrift QM-Verlag, Revision 0, Seite 6 von 6, gültig ab xx.xx.xxxx
32 5.4.1 Qualitätsziele Beispiele in rot Dokumentation Qualitätsziele für das Jahr: XXXX Thema Soll Maßnahmen zur Erreichung Verantwortlich IST am: Kundenzufriedenheit Ziel: Besuch der wichtigen Kunden 1x per anno Besuchsplan erstellen. Vertrieb Führung Ziel: Einführung DIN EN ISO (Zertifizierung) 100% Aufbau Handbuch Zertifizierer vertraglich binden. BdL Mitarbeiter/-innenzufriedenheit Ziel: Kündigungen wegen Unzufriedenheit 0 Formlose Personalgespräche halbjährlich. Liste erstellen. GF Mitarbeiter/-innen Ziel: Maschinenausfall wegen mangelnder Wartung 0 Wartungsplan an jeder Maschine aushängen und überwachen. Prod. Leitung Qualität Produkt Ziel: Beanstandungen wegen Genauigkeit 0 Prüfplan erstellen und überwachen., Entwicklung, Produktion QM-Verlag, Revision 0, Seite 1 von 3, gültig ab xx.xx.xxxx
33 5.4.1 Qualitätsziele Beispiele in rot Dokumentation Thema Soll Maßnahmen zur Erreichung Verantwortlich IST am: Bereitstellung von Mitteln Ziel: Planung eines Neubaus 100% Planungsbüro beauftragen und überwachen. GF Verbesserung der Prozesse Ziel: Beschreibung der Prozesse im Rahmen des Qualitätsmanagementsystems Schulungskonzept Wartung Schulungskonzept erstellen, prüfen und freigeben. Entwicklung, Vertrieb Beziehungen zu unseren Lieferanten Ziel: Durchführung der Lieferantenbewertung 1x komplett Ermittlung der wichtigsten Lieferanten Einkauf Akquisition, Vertriebsziele Ziel: Aufbau neuer Stammkunden > 1 Messebesuch in Saarbrücken Vertrieb Vorkehrungen zum Schutz der Gesundheit und der Sicherheit am Arbeitsplatz Ziel: Durchführung der Erst- und Folgeunterweisungen im Rahmen des Arbeitsschutzes. 1x per anno Externen Arbeitsschützer beauftragen GF Umsetzung von Maßnahmen aus vorliegenden Bewertungen Ziel: nicht belegbar QM-Verlag, Revision 0, Seite 2 von 3, gültig ab xx.xx.xxxx
34 5.4.1 Qualitätsziele Beispiele in rot Dokumentation Thema Soll Maßnahmen zur Erreichung Verantwortlich IST am: Ausschluss von Haftungsrisiken, Risikominimierung Ziel: Ausführliche Einarbeitung von Auszubildenden und neuen Mitarbeitern/-innen Regulatorische Anforderungen 100% Ausbilder beauftragen und Bericht anfordern GF, Ausbilder Ziel: Prüfung auf Neuerungen durch die Entwicklung 2x per anno Überwachung Internetseiten und Informationen der benannten Stelle SiBe, Technische Dokumentationen Ziel: Prüfung der Produktakte auf Aktualität 2x per anno Prüfung halbjährlich und bei Anlässen wie Rückmeldungen, Fehler und vielem mehr. Entwicklung Freigegeben am: xx.xx.xxxx Unterschrift GF, Datum QM-Verlag, Revision 0, Seite 3 von 3, gültig ab xx.xx.xxxx
35 5.6.0 Bewertung Aktualität TD Beispiele in rot Dokumentation Die Technische Dokumentation des Produktes XXXXX wird wie folgt bewertet. Risikomanagement: Das Produkt hat keine unvertretbaren Risiken. Vernachlässigbare Risiken sind erkannt und werden jährlich neu bewertet. Die Akzeptanz von Risiken ist aufgrund der Eigenschaft und der Zweckbestimmung des Medizinproduktes bewertet. Es besteht kein Handlungsbedarf. Marktbeobachtung: Im Rahmen der Marktbeobachtung wurden Internetseiten ausgewertet (swissmedic, Wettbewerber, Fachpresse). Das Produkt oder vergleichbare Systeme hatten keine Vorkommnisse, die eine Abkündigung und oder Veränderung erfordern. Es besteht kein Handlungsbedarf. Normen: Die Norm EN ISO 13485:2016 wurde aktualisiert. Die Norm EN ISO 14971:2012 ist aktualisiert. Die Dokumentation des Managementsystems und der Technischen Dokumentation entsprechen den Norminhalten. Es besteht kein Handlungsbedarf. Gesetzliche Anforderungen: Die Internetseite swissmedic wurde ausgewertet auf neue gesetzliche Forderungen. Es wurden keine neuen oder veränderten Forderungen erkannt. Es besteht kein Handlungsbedarf. Klinische Bewertung: Die klinische Bewertung unseres Produktes ist sehr umfassend. Da noch kein Produkt verkauft wurde, sind keine weiteren Erkenntnisse bekannt. Wir sind der Auffassung, dass die klinische Bewertung vollständig und unser Produkt sicher ist. Es besteht kein Handlungsbedarf. Gebrauchsanweisungen: Die Gebrauchsanweisungen wurden von einem externen Büro übersetzt und intern geprüft. Siehe auch Prozessbeschreibung Übersetzung. Die Inhalte sind intern geprüft worden und wurden freigegeben. Es besteht kein Handlungsbedarf. Bewertung durchgeführt am xx.xx.xxxx Datum, Geschäftsführung QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
36 8.3.3 Maßnahmenempfehlungen Beispiele in rot Dokumentation Nr. Produkt Maßnahmen der Beseitigung Ursache Datum Verantwortlich 1 Aluhalter 72/4, verbogene Teile im Lager. Ware wird verschrottet, Lagerplatz wird optimiert, Ware kommt in Boxen Die Teile lagen lose im Lager was nicht geeignet war xxxx 2 Gerät 122sx, Reklamation von Kunden. Der Kunde hat die Inhalte der Gebrauchsanweisung nicht gelesen. Die Funktion wurde erklärt. Empfehlung an Kunde: Studium Gebrauchsanweisung. Unbekannt, wahrscheinlich wird nicht ausreichend auf die Gebrauchsanweisung hingewiesen xxxx 3 Umverpackung Transponder beschädigt (50 Stück). Die Transponder werden um verpackt und die Verpackung neu geprüft. Beschädigung bei dem Transport in das Lager xxxx QM-Verlag, Revision 0, Seite 1 von 1, gültig ab xx.xx.xxxx
Dokumentenübersicht Revision vom Ersteller/-in Verteiler Grund der letzten Änderung
 Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 BdoL BdoL Kapitel 3 Begriffe Abkürzungen 0 BdoL BdoL Kapitel 4 Qualitätsmanagementsystem 0 BdoL BdoL Kapitel 5 Verantwortung der Leitung
Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 BdoL BdoL Kapitel 3 Begriffe Abkürzungen 0 BdoL BdoL Kapitel 4 Qualitätsmanagementsystem 0 BdoL BdoL Kapitel 5 Verantwortung der Leitung
Produktvorstellung. Seiler. Musterbeispiel Medizin mit DIN EN ISO 13485:2015
 Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel Medizin mit DIN EN ISO 13485:2015 en Zielgruppe: Medizinprodukteherstellung Inverkehrbringung von Medizinprodukten Egal was Du tust, mach es
Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel Medizin mit DIN EN ISO 13485:2015 en Zielgruppe: Medizinprodukteherstellung Inverkehrbringung von Medizinprodukten Egal was Du tust, mach es
Inhaltsübersicht MH Medizin IBSN Inhalt der CD sortiert nach Normpunkten DIN EN ISO 9001:2000
 Seite 1 von 8 Seiten Inhaltsübersicht CD struktur Inhalt der CD sortiert nach punkten DIN EN ISO 9001:2000 Form Kapitel 1+2 2.0.0 1 und 2 Anwendungsbereich ative Verweise 424 Liste der en und Erlasse CD:\1
Seite 1 von 8 Seiten Inhaltsübersicht CD struktur Inhalt der CD sortiert nach punkten DIN EN ISO 9001:2000 Form Kapitel 1+2 2.0.0 1 und 2 Anwendungsbereich ative Verweise 424 Liste der en und Erlasse CD:\1
 Qualitätsmanagement Verlag Seiler Dokumentationen Musterhandbuch Medizin DIN EN ISO 13485:2016 & DIN EN ISO 9001:2015 Prozesse Weitere Prozesse auf der CD: 4.1.6 Validierung Software 4.2.4 Lenkung externer
Qualitätsmanagement Verlag Seiler Dokumentationen Musterhandbuch Medizin DIN EN ISO 13485:2016 & DIN EN ISO 9001:2015 Prozesse Weitere Prozesse auf der CD: 4.1.6 Validierung Software 4.2.4 Lenkung externer
4.2.3 Liste der Dokumente MH Gesundheitsvorsorge
 Interne Dokumente Kapitel- und Dokumentenbeschreibung Version vom Seitenanzahl 0 Einführung Deckblatt Musterhandbuch 1 Vorwort 2 Deckblatt Allgemeine Informationen 1 Abkürzungsverzeichnis 1 1 Managementhandbuch
Interne Dokumente Kapitel- und Dokumentenbeschreibung Version vom Seitenanzahl 0 Einführung Deckblatt Musterhandbuch 1 Vorwort 2 Deckblatt Allgemeine Informationen 1 Abkürzungsverzeichnis 1 1 Managementhandbuch
4.2.3 Liste der Dokumente
 Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 L LSG L LSG Kapitel 3 Begriffe Abkürzungen 0 L LSG L LSG Kapitel 4 Managementsystem Lebensmittelsicherheit 0 L LSG L LSG Kapitel 5 Verantwortung
Handbuch Kapitel 1 und 2 Anwendungsbereich & Normative Verweise 0 L LSG L LSG Kapitel 3 Begriffe Abkürzungen 0 L LSG L LSG Kapitel 4 Managementsystem Lebensmittelsicherheit 0 L LSG L LSG Kapitel 5 Verantwortung
Gegenüberstellung der Normkapitel
 Zuordnungstabelle ISO 9001: 2015 ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der Organisation 4.0 Qualitätsmanagementsystem 4.1 Verstehen der Organisation und Ihres 4.0 Qualitätsmanagementsystem
Zuordnungstabelle ISO 9001: 2015 ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der Organisation 4.0 Qualitätsmanagementsystem 4.1 Verstehen der Organisation und Ihres 4.0 Qualitätsmanagementsystem
Gegenüberstellung von DIN EN ISO 9001:2015. und DIN EN ISO 9001:2008
 Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 DIN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 DIN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Gegenüberstellung von DIN EN ISO 9001:2015. und DIN EN ISO 9001:2008
 Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 IN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Gegenüberstellung von DIN EN ISO 9001:2015 und DIN EN ISO 9001:2008 IN EN ISO 9001:2015 DIN EN ISO 9001:2008 4 Kontext der Organisation weitgehend neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen
Gegenüberstellung von ISO 9001:2015 und ISO 9001:2008
 von ISO 9001:2015 und ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der 4 Qualitätsmanagementsystem 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse und Erwartungen interessierter
von ISO 9001:2015 und ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der 4 Qualitätsmanagementsystem 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse und Erwartungen interessierter
Gegenüberstellung DIN EN 9100:2018 DIN EN 9100:2010
 Gegenüberstellung DIN EN 9100:2018 DIN EN 9100:2010 DIN EN 9100:2018 DIN EN 9100:2010 4 Kontext der 4 Qualitätsmanagementsystem 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse
Gegenüberstellung DIN EN 9100:2018 DIN EN 9100:2010 DIN EN 9100:2018 DIN EN 9100:2010 4 Kontext der 4 Qualitätsmanagementsystem 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse
7.5.1 Dokumentierte Informationen. Dokumentenübersicht Revision vom Ersteller/ in Verteiler Grund der letzten Änderung
 Handbuch Handbuch gesamt mit Kapitel 1 bis 10 0 QM QM Prozessbeschreibungen / Verfahren 6 1 0 Ermittlung Risiken Chancen 0 QM QM 6 2 0 Qualitätsziele 0 QM QM 6 3 0 Planung Änderungen 0 QM QM 7 1 3 Externe
Handbuch Handbuch gesamt mit Kapitel 1 bis 10 0 QM QM Prozessbeschreibungen / Verfahren 6 1 0 Ermittlung Risiken Chancen 0 QM QM 6 2 0 Qualitätsziele 0 QM QM 6 3 0 Planung Änderungen 0 QM QM 7 1 3 Externe
Management- Handbuch. Entwicklung, Produktion, Dienstleistung und Vertrieb. DIN EN ISO 9001:2015. Auflage 1.1
 Management- Handbuch Entwicklung, Produktion, Dienstleistung und Vertrieb. Auflage 1.1 Inhaltsverzeichnis 1 Anwendungsbereich... 5 2 Normative Verweisungen... 5 3 Begriffe (siehe Punkt 11)... 5 4 Kontext
Management- Handbuch Entwicklung, Produktion, Dienstleistung und Vertrieb. Auflage 1.1 Inhaltsverzeichnis 1 Anwendungsbereich... 5 2 Normative Verweisungen... 5 3 Begriffe (siehe Punkt 11)... 5 4 Kontext
Normrevision DIN EN ISO 9001:2015. Seite: 1
 Seite: 1 Qualitätsmanagement nach DIN EN ISO 9001 neu Inhalt: Zeitplan für Unternehmen und Organisationen Gegenüberstellung der Gliederung der Versionen 2008 und 2015 Die wichtigsten Neuerungen und deren
Seite: 1 Qualitätsmanagement nach DIN EN ISO 9001 neu Inhalt: Zeitplan für Unternehmen und Organisationen Gegenüberstellung der Gliederung der Versionen 2008 und 2015 Die wichtigsten Neuerungen und deren
QM nach DIN EN ISO 9001:2015. copyright managementsysteme Seiler Tel:
 QM nach DIN EN ISO 9001:2015 1 copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 2 Prozessplanung copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 3 Kennzahlen im Unternehmen 48 Lieferzeit
QM nach DIN EN ISO 9001:2015 1 copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 2 Prozessplanung copyright managementsysteme Seiler www.erfolgsdorf.de Tel: 3 Kennzahlen im Unternehmen 48 Lieferzeit
ISO 9001: Einleitung. 1 Anwendungsbereich. 2 Normative Verweisungen. 4 Qualitätsmanagementsystem. 4.1 Allgemeine Anforderungen
 DIN EN ISO 9001 Vergleich ISO 9001:2015 und ISO 9001:2015 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe 4 Kontext der Organisation 4.1 Verstehen der Organisation und ihres Kontextes
DIN EN ISO 9001 Vergleich ISO 9001:2015 und ISO 9001:2015 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe 4 Kontext der Organisation 4.1 Verstehen der Organisation und ihres Kontextes
DIN EN ISO 9001:2015 DIN EN ISO 1 Anwendungsbereich 1 Anwendungsbereich 1.1 Allgemeines 2 Normative Verweisungen 2 Normative Verweisungen Freie 3 Nutz
 DIN EN ISO 9001:2015 DIN EN ISO 1 Anwendungsbereich 1 Anwendungsbereich 1.1 Allgemeines 2 Normative Verweisungen 2 Normative Verweisungen Freie 3 Nutzung Begriffe kostenloser Tools 3 Begriffe und Experten-Links
DIN EN ISO 9001:2015 DIN EN ISO 1 Anwendungsbereich 1 Anwendungsbereich 1.1 Allgemeines 2 Normative Verweisungen 2 Normative Verweisungen Freie 3 Nutzung Begriffe kostenloser Tools 3 Begriffe und Experten-Links
Kapitel 4. Qualitätsmanagementsystem. 4. Qualitätsmanagementsystem Allgemeine Anforderungen Regulatorische Anforderungen...
 Kapitel 4 Qualitätsmanagementsystem Inhaltsverzeichnis 4. Qualitätsmanagementsystem...1 4.1. Allgemeine Anforderungen...1 4.1.1 Regulatorische Anforderungen...1 4.1.2 Risikobasierte Prozesse...2 4.1.3
Kapitel 4 Qualitätsmanagementsystem Inhaltsverzeichnis 4. Qualitätsmanagementsystem...1 4.1. Allgemeine Anforderungen...1 4.1.1 Regulatorische Anforderungen...1 4.1.2 Risikobasierte Prozesse...2 4.1.3
Inhaltsübersicht MH Brandmelde-Fachfirmen ISBN
 Seite 1 von 4 Seiten Inhaltsübersicht CD se auf CD Aufbau der CD Form Dateiname 0 Einleitung (Allgem. Informationen, Inhaltsverzeichnis usw.) 1 Kapitel (Alle Kapitel des Handbuches) CD:\0 Einleitung CD:\1
Seite 1 von 4 Seiten Inhaltsübersicht CD se auf CD Aufbau der CD Form Dateiname 0 Einleitung (Allgem. Informationen, Inhaltsverzeichnis usw.) 1 Kapitel (Alle Kapitel des Handbuches) CD:\0 Einleitung CD:\1
Werks-Anlagen und Einrichtungsplanung
 IATF 16949:2016 ISO/TS 16949:2009 1.1 Allgemeines 4.1 Verstehen der Organisation und ihres Kontextes 1.1 Allgemeines 4.2 Verstehen der Erfordernisse und Erwartungen interessierter Parteien 1.1 Anwendungen
IATF 16949:2016 ISO/TS 16949:2009 1.1 Allgemeines 4.1 Verstehen der Organisation und ihres Kontextes 1.1 Allgemeines 4.2 Verstehen der Erfordernisse und Erwartungen interessierter Parteien 1.1 Anwendungen
Musterhandbuch AZAV & ISO 9001
 Musterhandbuch AZAV & ISO 9001 DIN EN ISO 9001:2008 Prozessorientiert ISBN 978-3-942882-28-6 Auflage 2 Qualitätsmanagement Verlag Seiler Dokumentationen Kapitel 4 Qualitätsmanagementsystem Inhaltsverzeichnis
Musterhandbuch AZAV & ISO 9001 DIN EN ISO 9001:2008 Prozessorientiert ISBN 978-3-942882-28-6 Auflage 2 Qualitätsmanagement Verlag Seiler Dokumentationen Kapitel 4 Qualitätsmanagementsystem Inhaltsverzeichnis
ISO 9001: vom Praktiker für Praktiker. Bearbeitet von Norbert Waldy
 ISO 9001: 2015 vom Praktiker für Praktiker Bearbeitet von Norbert Waldy 1. Auflage 2015. Buch. 168 S. Hardcover ISBN 978 3 7323 3353 0 Format (B x L): 14 x 21 cm Gewicht: 385 g Wirtschaft > Management
ISO 9001: 2015 vom Praktiker für Praktiker Bearbeitet von Norbert Waldy 1. Auflage 2015. Buch. 168 S. Hardcover ISBN 978 3 7323 3353 0 Format (B x L): 14 x 21 cm Gewicht: 385 g Wirtschaft > Management
Musterhandbuch Qualitätsmanagementplan
 Musterhandbuch Leseprobe DIN ISO 10005:2009 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-25-5 Auflage 1 Grundlagen... 2 Gültigkeit... 2 Ziel und Grund... 2 Abkürzungen... 2 Informationen...
Musterhandbuch Leseprobe DIN ISO 10005:2009 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-25-5 Auflage 1 Grundlagen... 2 Gültigkeit... 2 Ziel und Grund... 2 Abkürzungen... 2 Informationen...
Qualitätsmanagement Verlag. Seiler. Dokumentationen. Vorlagen Technische Dokumentation. Gemäß VERORDNUNG (EU) 2017/745. Auflage 1
 Qualitätsmanagement Verlag Seiler Dokumentationen Vorlagen Technische Dokumentation Gemäß VERORDNUNG (EU) 2017/745 Auflage 1 Liste der Dokumente Produktakte Dokument Revision vom Ersteller/-in Verteiler
Qualitätsmanagement Verlag Seiler Dokumentationen Vorlagen Technische Dokumentation Gemäß VERORDNUNG (EU) 2017/745 Auflage 1 Liste der Dokumente Produktakte Dokument Revision vom Ersteller/-in Verteiler
Auftraggeber: QMB: Auditierte Bereiche: QMH-Kapitel: Auditleiter/in: Co-Auditor/in: Datum Auditdurchführung: Datum Berichterstellung:
 Audit-Nr. Auftraggeber: QMB: Normengrundlage / Referenzdokumente: Auditierte Bereiche: QMH-Kapitel: Auditleiter/in: Co-Auditor/in: Datum Auditdurchführung: Datum Berichterstellung: DIN EN ISO 9001:2015
Audit-Nr. Auftraggeber: QMB: Normengrundlage / Referenzdokumente: Auditierte Bereiche: QMH-Kapitel: Auditleiter/in: Co-Auditor/in: Datum Auditdurchführung: Datum Berichterstellung: DIN EN ISO 9001:2015
IATS 16949:2016 ISO/TS 16949:2009
 IATS 16949:2016 ISO/TS 16949:2009 4 Kontext der Organisation Zum Teil neu, siehe Anwendungsbereich 4.1 Verstehen der Organisation und ihres 1.1 Allgemeines Kontextes 4.2 Verstehen der Erfordernisse und
IATS 16949:2016 ISO/TS 16949:2009 4 Kontext der Organisation Zum Teil neu, siehe Anwendungsbereich 4.1 Verstehen der Organisation und ihres 1.1 Allgemeines Kontextes 4.2 Verstehen der Erfordernisse und
Gegenüberstellung IATF 16949:2016 und ISO/TS 16949:2009
 Gegenüberstellung IATF 16949:2016 und ISO/TS 16949:2009 4 Kontext der Organisation Teilweise neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen der Organisation und ihres 1.1 Allgemeines Kontextes
Gegenüberstellung IATF 16949:2016 und ISO/TS 16949:2009 4 Kontext der Organisation Teilweise neu, siehe aber auch 1 Anwendungsbereich 4.1 Verstehen der Organisation und ihres 1.1 Allgemeines Kontextes
Legende: Keine Aktion erforderlich! Anpassung erforderlich Neue Anforderung
 Legende: Keine Aktion erforderlich! Anpassung erforderlich Neue Anforderung Abschnitte der ISO 9001:2008 Abschnitte der ISO 9001:2015 Delta- Anforderungen, Bemerkungen 4 Qualitätsmanagementsystem 4.4 QMS
Legende: Keine Aktion erforderlich! Anpassung erforderlich Neue Anforderung Abschnitte der ISO 9001:2008 Abschnitte der ISO 9001:2015 Delta- Anforderungen, Bemerkungen 4 Qualitätsmanagementsystem 4.4 QMS
Handbuch / Regelwerk zur Norm DIN EN ISO 9001:2014 Entwurf
 Handbuch / Regelwerk zur Norm DIN EN ISO 9001:2014 Entwurf Inhaltsverzeichnis 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext der Organisation... 3 41
Handbuch / Regelwerk zur Norm DIN EN ISO 9001:2014 Entwurf Inhaltsverzeichnis 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext der Organisation... 3 41
Handbuch / Regelwerk zur Norm DIN EN ISO 9001:2014 Entwurf inkl. deutsches Manuskript 2015
 Inhaltsverzeichnis Handbuch / Regelwerk zur Norm DIN EN ISO 9001:2014 Entwurf inkl. deutsches Manuskript 2015 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext
Inhaltsverzeichnis Handbuch / Regelwerk zur Norm DIN EN ISO 9001:2014 Entwurf inkl. deutsches Manuskript 2015 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext
Produktvorstellung. Seiler. Regelwerk Medizin Handel mit DIN EN ISO 13485:2016. Zielgruppe: Medizinproduktehändler Importeure. Gliederung / Aufbau
 Produktvorstellung Qualitätsmanagement Verlag Regelwerk Medizin Handel mit DIN EN ISO 13485:2016 Seiler Dokumentationen Zielgruppe: Medizinproduktehändler Importeure Egal was Du tust, mach es mit Begeisterung!
Produktvorstellung Qualitätsmanagement Verlag Regelwerk Medizin Handel mit DIN EN ISO 13485:2016 Seiler Dokumentationen Zielgruppe: Medizinproduktehändler Importeure Egal was Du tust, mach es mit Begeisterung!
Das vollständige Dokument erhalten Sie nach der Bestellung.
 Auditbericht-NR.: Auditierte Organisation: Anschrift: Auditdatum: Mustermann GmbH Musterhausen xx.xx.xxxx Auditart: Internes Systemaudit nach DIN EN ISO 9001:2015 Anlass des Audits: Geplantes Audit gemäß
Auditbericht-NR.: Auditierte Organisation: Anschrift: Auditdatum: Mustermann GmbH Musterhausen xx.xx.xxxx Auditart: Internes Systemaudit nach DIN EN ISO 9001:2015 Anlass des Audits: Geplantes Audit gemäß
Release: 001 Stand 02.Juni 2003 Stand:
 Seite: 1/10 Inhaltsverzeichnis 1 Gliederung der Projektstruktur...1 1.1 Kapitel der Norm 9001:2000 (1) Aufbau und Struktur des QMH...2 1.2 Kapitel der Norm 9001:2000 (2) Vorstellen des Unternehmens...3
Seite: 1/10 Inhaltsverzeichnis 1 Gliederung der Projektstruktur...1 1.1 Kapitel der Norm 9001:2000 (1) Aufbau und Struktur des QMH...2 1.2 Kapitel der Norm 9001:2000 (2) Vorstellen des Unternehmens...3
Produktvorstellung. Seiler. Lieferung. Leseprobe. Besonderes. Qualitätsmanagement Verlag. Regelwerk Technische Dokumentation nach MDR 2017/745
 Produktvorstellung Qualitätsmanagement Verlag Regelwerk Technische Dokumentation nach MDR 2017/745 Seiler Dokumentationen Zielgruppe: Dieses Regelwerk ist für Inverkehrbringer von Medizinprodukten. Es
Produktvorstellung Qualitätsmanagement Verlag Regelwerk Technische Dokumentation nach MDR 2017/745 Seiler Dokumentationen Zielgruppe: Dieses Regelwerk ist für Inverkehrbringer von Medizinprodukten. Es
Musterhandbuch. Lerndienstleistung DIN ISO 29990:2010. Prozessorientiert ISBN Auflage 2
 Musterhandbuch Lerndienstleistung DIN ISO 29990:2010 Prozessorientiert ISBN 978 3 942882 16 3 Auflage 2 4.1 Dokumente und Aufzeichnungen Dokumentenübersicht Revision vom Ersteller/-in Verteiler Grund der
Musterhandbuch Lerndienstleistung DIN ISO 29990:2010 Prozessorientiert ISBN 978 3 942882 16 3 Auflage 2 4.1 Dokumente und Aufzeichnungen Dokumentenübersicht Revision vom Ersteller/-in Verteiler Grund der
Zuordnung der Anforderungen der DIN EN ISO 9001:2015 im QMS-Reha
 4. Kontext der Organisation Zuordnung der Anforderungen der DIN EN ISO 9001:2015 im QMS-Reha 4.1 Verstehen der Organisation und ihres Kontextes 4.2 Verstehen der Erfordernisse und Erwartungen interessierter
4. Kontext der Organisation Zuordnung der Anforderungen der DIN EN ISO 9001:2015 im QMS-Reha 4.1 Verstehen der Organisation und ihres Kontextes 4.2 Verstehen der Erfordernisse und Erwartungen interessierter
UMSTELLUNGSHILFE ISO 9001:2008 auf ISO 9001:2015
 UMSTELLUNGSHILFE ISO 9001:2008 auf ISO 9001:2015 Was ist wirklich NEU? Was ist zu tun? Was kann ich besser oder anders machen? Das nachfolgende Dokument beinhaltet eine Gegenüberstellung bzw. Zuordnung
UMSTELLUNGSHILFE ISO 9001:2008 auf ISO 9001:2015 Was ist wirklich NEU? Was ist zu tun? Was kann ich besser oder anders machen? Das nachfolgende Dokument beinhaltet eine Gegenüberstellung bzw. Zuordnung
4.2.4 Liste der Dokumente
 4.2.4 Liste der Dokumente Dokumentenübersicht Revision vom Ersteller/-in Verteiler Grund der letzten Änderung Managementhandbuch Kapitel 1 bis 8 0 BdoL BdoL Prozessbeschreibung / Verfahren 4.2.3 Lenkung
4.2.4 Liste der Dokumente Dokumentenübersicht Revision vom Ersteller/-in Verteiler Grund der letzten Änderung Managementhandbuch Kapitel 1 bis 8 0 BdoL BdoL Prozessbeschreibung / Verfahren 4.2.3 Lenkung
TEIL 1 allgemeiner Teil
 TEIL 1 allgemeiner Teil Einleitung 0 Einleitung 0 Einleitung 0 Einleitung Einleitung 0 Allgemeines 0.1 Hintergrund 0.1 Hintergrund 0.1 Allgemeines 0.1 Grundsätze des Qualitätsmanagements 0.2 Ziel eines
TEIL 1 allgemeiner Teil Einleitung 0 Einleitung 0 Einleitung 0 Einleitung Einleitung 0 Allgemeines 0.1 Hintergrund 0.1 Hintergrund 0.1 Allgemeines 0.1 Grundsätze des Qualitätsmanagements 0.2 Ziel eines
Kundencheckliste zur DIN EN ISO 9001
 Kundencheckliste zur Forderung der QM-System 4.1 Sind in Ihrem Unternehmen ausgegliederte Prozesse vorhanden, die sie für Ihr QM- System (die Produkt- /Dienstleistungsqualität benötigen? Wie stellen Sie
Kundencheckliste zur Forderung der QM-System 4.1 Sind in Ihrem Unternehmen ausgegliederte Prozesse vorhanden, die sie für Ihr QM- System (die Produkt- /Dienstleistungsqualität benötigen? Wie stellen Sie
Produktvorstellung. Seiler. Musterbeispiel DIN ISO 10005: QM-Plan. Zielgruppe: Große Unternehmen. Inhalte. Lieferung. Leseprobe.
 Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel DIN ISO 10005:2009 - Seiler Dokumentationen Zielgruppe: Große Unternehmen Egal was Du tust, mach es mit Begeisterung! Inhalte AA mit QMS, Prozessbeschreibungen
Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel DIN ISO 10005:2009 - Seiler Dokumentationen Zielgruppe: Große Unternehmen Egal was Du tust, mach es mit Begeisterung! Inhalte AA mit QMS, Prozessbeschreibungen
Interpretation der Anforderungen
 Interpretation der Anforderungen Canisha Teubert Online-Handbücher für Technik, IT, Produktentwicklung Medizinprodukte planen, entwickeln, realisieren digital Der CE-Routenplaner Strukturierte Produktentwicklung
Interpretation der Anforderungen Canisha Teubert Online-Handbücher für Technik, IT, Produktentwicklung Medizinprodukte planen, entwickeln, realisieren digital Der CE-Routenplaner Strukturierte Produktentwicklung
Musterhandbuch AZAV Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN Auflage 1
 Musterhandbuch AZAV Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-28-6 Auflage 1 4.2.4 Inhaltsübersicht Musterhandbuch AZAV Dokumentenübersicht Revision
Musterhandbuch AZAV Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-28-6 Auflage 1 4.2.4 Inhaltsübersicht Musterhandbuch AZAV Dokumentenübersicht Revision
Übersicht über ISO 9001:2000
 Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Übersicht über die ISO 9001:2000 0 Einleitung 1 Anwendungsbereich 2 Normative Verweisungen 3 Begriffe Übersicht über die ISO 9001:2000 4 Qualitätsmanagementsystem 5 Verantwortung der Leitung 6 Management
Musterhandbuch Lerndienstleistung
 Musterhandbuch Lerndienstleistung Leseprobe DIN ISO 29990:2010 DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-16-3 Auflage 1 4.2.4 Inhaltsübersicht QM-Handbuch Lerndienstleistung
Musterhandbuch Lerndienstleistung Leseprobe DIN ISO 29990:2010 DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-942882-16-3 Auflage 1 4.2.4 Inhaltsübersicht QM-Handbuch Lerndienstleistung
Integriertes Management-Handbuch
 Muster GmbH Integriertes Management-Handbuch Qualitätsmanagement (DIN EN ISO 9001) Umweltmanagement (DIN EN ISO 14001) Handbuch-Exemplar Nummer: 01-2014 Dieses Handbuch unterliegt dem Änderungsdienst:
Muster GmbH Integriertes Management-Handbuch Qualitätsmanagement (DIN EN ISO 9001) Umweltmanagement (DIN EN ISO 14001) Handbuch-Exemplar Nummer: 01-2014 Dieses Handbuch unterliegt dem Änderungsdienst:
Inhaltsübersicht MH ISO/TS 16949 ISBN 3-935388-12-8
 Seite 1 von 7 Seiten Inhaltsübersicht struktur Aufbau CD Form Dateiname 0 Einleitung (Allgem. Informationen, Inhaltsverzeichnis usw.) 1 Kapitel (Alle Kapitel des Handbuches) CD:\0 Einleitung CD:\1 Kapitel
Seite 1 von 7 Seiten Inhaltsübersicht struktur Aufbau CD Form Dateiname 0 Einleitung (Allgem. Informationen, Inhaltsverzeichnis usw.) 1 Kapitel (Alle Kapitel des Handbuches) CD:\0 Einleitung CD:\1 Kapitel
Vorschau. QM-Dokumentation Verzeichnis der Aufzeichnungen
 Vorschau Bitte beachten Sie, dieses Dokument ist nur eine Vorschau. Hier werden nur Auszüge dargestellt. Nach dem Erwerb steht Ihnen selbstverständlich die vollständige Version im offenen Dateiformat zur
Vorschau Bitte beachten Sie, dieses Dokument ist nur eine Vorschau. Hier werden nur Auszüge dargestellt. Nach dem Erwerb steht Ihnen selbstverständlich die vollständige Version im offenen Dateiformat zur
Vorstellung der Norm DIN EN ISO 9001:2008
 QM nach DIN EN ISO 9001 Vorstellung der Norm DIN EN ISO 9001:2008 Referent: Klaus Seiler, MSc managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See 1 Sinn und Zweck der Norm die ständige Verbesserung
QM nach DIN EN ISO 9001 Vorstellung der Norm DIN EN ISO 9001:2008 Referent: Klaus Seiler, MSc managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See 1 Sinn und Zweck der Norm die ständige Verbesserung
Regelwerk zur Norm DIN EN ISO 9001:2015
 Regelwerk zur Norm DIN EN ISO 9001:2015 Inhaltsverzeichnis 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext der Organisation... 3 41 Verstehen der Organisation
Regelwerk zur Norm DIN EN ISO 9001:2015 Inhaltsverzeichnis 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext der Organisation... 3 41 Verstehen der Organisation
ISO Qualitätsmanagement prozessorientiert umsetzen
 ISO 9001 - Qualitätsmanagement prozessorientiert umsetzen Bearbeitet von Michael Cassel 1. Auflage 2007. Buch. XII, 283 S. Hardcover ISBN 978 3 446 22731 6 Format (B x L): 17,4 x 24,7 cm Gewicht: 678 g
ISO 9001 - Qualitätsmanagement prozessorientiert umsetzen Bearbeitet von Michael Cassel 1. Auflage 2007. Buch. XII, 283 S. Hardcover ISBN 978 3 446 22731 6 Format (B x L): 17,4 x 24,7 cm Gewicht: 678 g
Musterhandbuch Medizin
 Musterhandbuch Medizin DIN EN ISO 13485:2012 unter Berücksichtigung der ISO 14971:2012 Prozessorientiert ISBN 978-3-935388-15-3 Auflage 10 4.2.4 Inhaltsübersicht QM-Handbuch Medizin Dokumentenübersicht
Musterhandbuch Medizin DIN EN ISO 13485:2012 unter Berücksichtigung der ISO 14971:2012 Prozessorientiert ISBN 978-3-935388-15-3 Auflage 10 4.2.4 Inhaltsübersicht QM-Handbuch Medizin Dokumentenübersicht
QM in der Zahnarztpraxis Muster-QM-Handbuch
 QM in der Zahnarztpraxis Muster-QM-Handbuch So führen Sie ein QM-System in Ihrer Praxis ein, das die Anforderungen der QM-Richtlinie des G-BA und der ISO 9001:2015 erfüllt - und verbessern damit Ihre Praxisprozesse!
QM in der Zahnarztpraxis Muster-QM-Handbuch So führen Sie ein QM-System in Ihrer Praxis ein, das die Anforderungen der QM-Richtlinie des G-BA und der ISO 9001:2015 erfüllt - und verbessern damit Ihre Praxisprozesse!
 Kapitel 4 Qualitätsmanagementsystem Inhaltsverzeichnis 4. Qualitätsmanagementsystem...1 4.1. Allgemeine Anforderungen...1 4.1.1 Regulatorische Anforderungen...1 4.1.2 Risikobasierte Prozesse...2 4.1.3
Kapitel 4 Qualitätsmanagementsystem Inhaltsverzeichnis 4. Qualitätsmanagementsystem...1 4.1. Allgemeine Anforderungen...1 4.1.1 Regulatorische Anforderungen...1 4.1.2 Risikobasierte Prozesse...2 4.1.3
ISO/TS Qualitätsmanagement in der Automobilindustrie umsetzen
 ISO/TS 16949 - Qualitätsmanagement in der Automobilindustrie umsetzen Michael Cassel ISBN 3-446-22729-6 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/3-446-22729-6
ISO/TS 16949 - Qualitätsmanagement in der Automobilindustrie umsetzen Michael Cassel ISBN 3-446-22729-6 Inhaltsverzeichnis Weitere Informationen oder Bestellungen unter http://www.hanser.de/3-446-22729-6
Petra Corbé Systemauditorin TQM Dozentin in der Fort- und Weiterbildung Inhouse - Fortbildungen. Auditbericht
 1. Allgemeines zum Audit Einrichtung Anschrift Geltungsbereich Nicht anwendbare Anforderungen Auditzeitraum Auditplan vom Auditform: Internes Systemaudit Internes Prozessaudit Nachaudit Wirksamkeitsaudit
1. Allgemeines zum Audit Einrichtung Anschrift Geltungsbereich Nicht anwendbare Anforderungen Auditzeitraum Auditplan vom Auditform: Internes Systemaudit Internes Prozessaudit Nachaudit Wirksamkeitsaudit
Revision der DIN EN ISO 9001 Dokumentierte Informationen. Ausschlüsse : nicht zutreffende Anforderungen begründen
 Seite 1 von 17 Dokumentationsanforderungen Anwendungsbereich 4 Kontext der Organisation 4.3 Festlegen des Anwendungsbereichs Bestehende Dokumente Kommentar verfügbar sein und aufrechterhalten werden Ausschlüsse
Seite 1 von 17 Dokumentationsanforderungen Anwendungsbereich 4 Kontext der Organisation 4.3 Festlegen des Anwendungsbereichs Bestehende Dokumente Kommentar verfügbar sein und aufrechterhalten werden Ausschlüsse
Qualitätsmanagement Verlag. Musterhandbuch. Brandmelde-Fachfirmen. Leseprobe DIN EN ISO 9001:2008 DIN 14675:2012
 Qualitätsmanagement Verlag Seiler Dokumentationen Musterhandbuch Brandmelde-Fachfirmen Leseprobe DIN EN ISO 9001:2008 DIN 14675:2012 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-935388-33-7
Qualitätsmanagement Verlag Seiler Dokumentationen Musterhandbuch Brandmelde-Fachfirmen Leseprobe DIN EN ISO 9001:2008 DIN 14675:2012 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-935388-33-7
Vorstellung der Norm DIN EN ISO 13485:2012 inkl. Entwurf 2015
 QM nach DIN EN ISO 13485 Vorstellung der Norm DIN EN ISO 13485:2012 inkl. Entwurf 2015 1 Sinn und Zweck der Norm die ständige Verbesserung DIN-Normen EN-Normen ISO-Standards Zertifizierer Dokumentationsumfang
QM nach DIN EN ISO 13485 Vorstellung der Norm DIN EN ISO 13485:2012 inkl. Entwurf 2015 1 Sinn und Zweck der Norm die ständige Verbesserung DIN-Normen EN-Normen ISO-Standards Zertifizierer Dokumentationsumfang
Regelwerk zur Norm DIN EN ISO 9001:2015 Kanzlei
 Inhaltsverzeichnis Regelwerk zur Norm DIN EN ISO 9001:2015 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext der Organisation... 3 4 1 Verstehen der Organisation
Inhaltsverzeichnis Regelwerk zur Norm DIN EN ISO 9001:2015 1 Anwendungsbereich... 3 2 Normative Verweisungen... 3 3 Begriffe (siehe Punkt 11)... 3 4 Kontext der Organisation... 3 4 1 Verstehen der Organisation
Inhalt. 2 Umsetzung der Einzelanforderungen Einleitung 49
 1 Projektplanung und Durchführung 1 1.1 Einleitung 1 1.2 Projektdurchführung, 4 1.2.1 Projektvorbereitung 5 1.2.1.1 Ziele des Projekts definieren 5 1.2.1.2 Projektteam bilden 6 1.2.2 Vorgehensplanung und
1 Projektplanung und Durchführung 1 1.1 Einleitung 1 1.2 Projektdurchführung, 4 1.2.1 Projektvorbereitung 5 1.2.1.1 Ziele des Projekts definieren 5 1.2.1.2 Projektteam bilden 6 1.2.2 Vorgehensplanung und
Musterhandbuch Beratung
 Musterhandbuch DIN EN ISO 9001:2008 Prozessorientiert ISBN 978 3 942882 27 9 Auflage 2 Inhaltsverzeichnis 1. Anwendungsbereich... 4 2. Normative Verweise... 4 4 Qualitätsmanagementsystem (QMS)... 4 4.1.
Musterhandbuch DIN EN ISO 9001:2008 Prozessorientiert ISBN 978 3 942882 27 9 Auflage 2 Inhaltsverzeichnis 1. Anwendungsbereich... 4 2. Normative Verweise... 4 4 Qualitätsmanagementsystem (QMS)... 4 4.1.
Audit-Bericht ISO 9001
 Audit-Art: 4. Wiederholungsaudit Audit-Grundlage / Standard / Ausgabedatum: ISO 9001:2008 ohne Produktentwicklung Handbuch / Revision / Datum 8; 9.12.2013 Audit-Zeitraum vor Ort (Solltermin): 2013-12-19-2013-12-19
Audit-Art: 4. Wiederholungsaudit Audit-Grundlage / Standard / Ausgabedatum: ISO 9001:2008 ohne Produktentwicklung Handbuch / Revision / Datum 8; 9.12.2013 Audit-Zeitraum vor Ort (Solltermin): 2013-12-19-2013-12-19
Die Anforderungen der DIN EN ISO 9001:2015 Eine erste Einschätzung
 Die Anforderungen der DIN EN ISO 9001:2015 Eine erste Einschätzung auf Grlage des DIS (Draft International Standard) 2014 1 Die (wesentlichen) neuen Inhalte (gegenüber der Version ISO 9001:2008) Eine neue
Die Anforderungen der DIN EN ISO 9001:2015 Eine erste Einschätzung auf Grlage des DIS (Draft International Standard) 2014 1 Die (wesentlichen) neuen Inhalte (gegenüber der Version ISO 9001:2008) Eine neue
Produktvorstellung. Seiler. Regelwerk 18001:2007 / OHSAS. Zielgruppe: Alle Unternehmen, welche ein Arbeitsschutzsystem aufbauen möchten
 Produktvorstellung Qualitätsmanagement Verlag Regelwerk 18001:2007 / OHSAS Seiler Dokumentationen Zielgruppe: Alle Unternehmen, welche ein Arbeitsschutzsystem aufbauen möchten Egal was Du tust, mach es
Produktvorstellung Qualitätsmanagement Verlag Regelwerk 18001:2007 / OHSAS Seiler Dokumentationen Zielgruppe: Alle Unternehmen, welche ein Arbeitsschutzsystem aufbauen möchten Egal was Du tust, mach es
Einleitung Audit - Fragenkatalog DIN EN ISO 13485:
 Einleitung Audit - Fragenkatalg DIN EN ISO 13485:2016-08 hier können Sie den gesamten Fragenkatalg bestellen QUMsult GmbH & C. KG Eisenbahnstraße 41 79098 Freiburg Tel. 07 61 / 29286-50 Fax 07 61 / 29286-77
Einleitung Audit - Fragenkatalg DIN EN ISO 13485:2016-08 hier können Sie den gesamten Fragenkatalg bestellen QUMsult GmbH & C. KG Eisenbahnstraße 41 79098 Freiburg Tel. 07 61 / 29286-50 Fax 07 61 / 29286-77
Vorstellung der Norm DIN EN ISO 13485:2012
 QM nach DIN EN ISO 13485 Vorstellung der Norm DIN EN ISO 13485:2012 Referent: Klaus Seiler, MSc. managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See 1 Sinn und Zweck der Norm die ständige Verbesserung
QM nach DIN EN ISO 13485 Vorstellung der Norm DIN EN ISO 13485:2012 Referent: Klaus Seiler, MSc. managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See 1 Sinn und Zweck der Norm die ständige Verbesserung
Gegenüberstellung DIN ISO 45001:2018 BS OHSAS 18001:2007
 Gegenüberstellung DIN ISO 45001:2018 BS OHSAS 18001:2007 1 Anwendungsbereich 1 Anwendungsbereich 2 Normative Verweisungen 2 Referenzen und Veröffentlichungen 3 Begriffe und Definitionen 3 Begriffe und
Gegenüberstellung DIN ISO 45001:2018 BS OHSAS 18001:2007 1 Anwendungsbereich 1 Anwendungsbereich 2 Normative Verweisungen 2 Referenzen und Veröffentlichungen 3 Begriffe und Definitionen 3 Begriffe und
Auditprotokoll prozessorientiert Audit-Nr.: 01/2017
 Auditprotokoll prozessorientiert Audit-Nr.: 01/2017 Auditierte Organisation: Anschrift: Mustermann GmbH Musterhausen Auditdatum: 01.02.2014 Auditart: Internes Systemaudit nach DIN EN ISO 9001 Anlass des
Auditprotokoll prozessorientiert Audit-Nr.: 01/2017 Auditierte Organisation: Anschrift: Mustermann GmbH Musterhausen Auditdatum: 01.02.2014 Auditart: Internes Systemaudit nach DIN EN ISO 9001 Anlass des
Informationsblatt zum Übergang eines bestehenden Zertifikates von der DIN EN ISO 9001:2008 auf die DIN EN ISO 9001:2015
 Informationsblatt zum Übergang eines bestehenden Zertifikates von der DIN EN ISO 9001:2008 auf die DIN EN ISO 9001:2015 Als offizieller Veröffentlichungstermin der DIN EN ISO 9001:2015 wurde der 15.09.2015
Informationsblatt zum Übergang eines bestehenden Zertifikates von der DIN EN ISO 9001:2008 auf die DIN EN ISO 9001:2015 Als offizieller Veröffentlichungstermin der DIN EN ISO 9001:2015 wurde der 15.09.2015
Umweltmanagement nach ISO 14001:2015
 Umweltmanagement nach ISO 14001:2015 Die Revision: Änderungen, Auswirkungen, Umsetzung 1. Auflage 2016. Buch. ISBN 978 3 8111 3611 3 Wirtschaft > Spezielle Betriebswirtschaft > Betriebliches Energie- und
Umweltmanagement nach ISO 14001:2015 Die Revision: Änderungen, Auswirkungen, Umsetzung 1. Auflage 2016. Buch. ISBN 978 3 8111 3611 3 Wirtschaft > Spezielle Betriebswirtschaft > Betriebliches Energie- und
ISO 13485:2016. TÜV SÜD Akademie GmbH Rev. <xx > / Stand: EN ISO 13485:2016 1
 ISO 13485:2016 Änderungen / Neue Anforderungen TÜV SÜD Akademie GmbH Rev. / Stand: 07 2016 EN ISO 13485:2016 1 ISO 13485:2016 Änderungen / Neue Anforderungen EN ISO 13485 DIN EN ISO 13485 TÜV SÜD
ISO 13485:2016 Änderungen / Neue Anforderungen TÜV SÜD Akademie GmbH Rev. / Stand: 07 2016 EN ISO 13485:2016 1 ISO 13485:2016 Änderungen / Neue Anforderungen EN ISO 13485 DIN EN ISO 13485 TÜV SÜD
Erläuterung zur Begrifflichkeit dokumentierte Information Dokumente und Aufzeichnungen werden in der DIN EN ISO 9001:2015 als dokumentierte Informatio
 Erläuterung zur Begrifflichkeit dokumentierte Information Dokumente und Aufzeichnungen werden in der DIN EN ISO 9001:2015 als dokumentierte Information zusammengefasst. Freie Die Unterscheidung Nutzung
Erläuterung zur Begrifflichkeit dokumentierte Information Dokumente und Aufzeichnungen werden in der DIN EN ISO 9001:2015 als dokumentierte Information zusammengefasst. Freie Die Unterscheidung Nutzung
Produktvorstellung. Seiler. Musterbeispiel DIN ISO 29990:2010 / Aus und Weiterbildung
 Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel DIN ISO 29990:2010 / Aus und Weiterbildung Seiler Dokumentationen Zielgruppe: Schulen Hochschulen sonstige Ausbildungsbetriebe mit Regelschulung
Produktvorstellung Qualitätsmanagement Verlag Musterbeispiel DIN ISO 29990:2010 / Aus und Weiterbildung Seiler Dokumentationen Zielgruppe: Schulen Hochschulen sonstige Ausbildungsbetriebe mit Regelschulung
Bereich. Datum. Zeit. Auditoren. Mitarbeiter. The spirit of good work. CL ISO-Bewertung Krankenhaus (06-0) TB GREEN & IBEX GmbH
 Bereich Datum Zeit Auditoren Mitarbeiter 1 Übersicht der Bewertung 4. Kontext der Organisation 1 2 3 4 5 4.1 Verstehen der Organisation und ihres Kontextes 4.2 Verstehen Erfordernisse/Erwartungen interessierter
Bereich Datum Zeit Auditoren Mitarbeiter 1 Übersicht der Bewertung 4. Kontext der Organisation 1 2 3 4 5 4.1 Verstehen der Organisation und ihres Kontextes 4.2 Verstehen Erfordernisse/Erwartungen interessierter
Gegenüberstellung ISO 9001:2015 ISO 9001:2008
 ISO 9001:2015 ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der Organisation 1.0 Anwendungsbereich 4.1 Verstehen der Organisation und ihres Kontextes 1.1 4.2 Verstehen der Erfordernisse und Erwartungen
ISO 9001:2015 ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der Organisation 1.0 Anwendungsbereich 4.1 Verstehen der Organisation und ihres Kontextes 1.1 4.2 Verstehen der Erfordernisse und Erwartungen
Vorstellung von Matrixzertifizierungen
 Vorstellung von Matrixzertifizierungen Klaus Seiler, MSc. in QM managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See Tel. +49 7551 949 7850 Fax +49 7551 949 7851 www.erfolgsdorf.de post@erfolgsdorf.de
Vorstellung von Matrixzertifizierungen Klaus Seiler, MSc. in QM managementsysteme Seiler Zum Salm 27 D-88662 Überlingen / See Tel. +49 7551 949 7850 Fax +49 7551 949 7851 www.erfolgsdorf.de post@erfolgsdorf.de
SCHUCHERT-Selbstcheck zu neuen Anforderungen der DIN EN ISO 9001:2015
 SCHUCHERT-Selbstcheck zu neuen Anforderungen der DIN EN ISO 9001:2015 Hinweise zur Nutzung Unternehmen und Organisationen haben bis zum 14.09.2018 Zeit, ihr QM-System auf die neue Norm umzustellen. Bei
SCHUCHERT-Selbstcheck zu neuen Anforderungen der DIN EN ISO 9001:2015 Hinweise zur Nutzung Unternehmen und Organisationen haben bis zum 14.09.2018 Zeit, ihr QM-System auf die neue Norm umzustellen. Bei
Qualitätsmanagement Änderungen in der ISO 9001 Entwurf 2007
 Qualitätsmanagement Änderungen in der ISO 9001 Entwurf 2007 30. Januar 2008 München Ablauf der Revision 2008 Start Systematic Review 15.12.2003 Ermittlung von Kundenfeedback 01/2004 Justification study
Qualitätsmanagement Änderungen in der ISO 9001 Entwurf 2007 30. Januar 2008 München Ablauf der Revision 2008 Start Systematic Review 15.12.2003 Ermittlung von Kundenfeedback 01/2004 Justification study
Schutzgebühr: 24,80 zzgl. 19 % MwSt. Die herausgebende Stelle. systemqm e.v. Barbarossa-Str Annweiler
 Manual internes Qualitätsmanagement für n in Orientierung an den Kriterien der nbetriebsordnung und der DIN EN ISO 9001:2015 Version 1.1 - Datum: 16.03.2016 Seite 1 von 26 Die herausgebende Stelle systemqm
Manual internes Qualitätsmanagement für n in Orientierung an den Kriterien der nbetriebsordnung und der DIN EN ISO 9001:2015 Version 1.1 - Datum: 16.03.2016 Seite 1 von 26 Die herausgebende Stelle systemqm
Vergleich ISO 9001:2008 zu ISO/DIS 9001:2014
 1 DIN EN ISO 9001:2008 pren ISO 9001:2014 (ISO/DIS 9001:2014) 4 4.1 Allgemeine Anforderungen 4.4 und dessen Prozesse 4.2. Dokumentationsanforderungen 7.5 Dokumentierte Information 4.2.1 Allgemeines 7.5.1
1 DIN EN ISO 9001:2008 pren ISO 9001:2014 (ISO/DIS 9001:2014) 4 4.1 Allgemeine Anforderungen 4.4 und dessen Prozesse 4.2. Dokumentationsanforderungen 7.5 Dokumentierte Information 4.2.1 Allgemeines 7.5.1
Präsentator. Markus Frei. avasis AG 9442 Berneck 2. Geschäftsführer
 ISO13485:2016 1 Präsentator Markus Frei Geschäftsführer avasis AG 9442 Berneck 2 Wer / Was ist medplm? avasis Siemens Industry Software 3 Dieses Webinar dauert ca. 30 Minuten zeigt die Teilnehmer nicht
ISO13485:2016 1 Präsentator Markus Frei Geschäftsführer avasis AG 9442 Berneck 2 Wer / Was ist medplm? avasis Siemens Industry Software 3 Dieses Webinar dauert ca. 30 Minuten zeigt die Teilnehmer nicht
Qualitätsmanagement-Handbuch gemäß den Anforderungen der Akkreditierungs- und Zulassungsverordnung AZAV
 Qualitätsmanagement-Handbuch gemäß den Anforderungen der Akkreditierungs- und Zulassungsverordnung AZAV Firma PA -Privater Arbeitsvermittler- PLZ Ort Handbuch-Version: 01 Datum Freigabe: 01.06.2012 x Unterliegt
Qualitätsmanagement-Handbuch gemäß den Anforderungen der Akkreditierungs- und Zulassungsverordnung AZAV Firma PA -Privater Arbeitsvermittler- PLZ Ort Handbuch-Version: 01 Datum Freigabe: 01.06.2012 x Unterliegt
VERANTWORTUNG DER LEITUNG
 Kapitel 1: VERANTWORTUNG DER LEITUNG INHALTSVERZEICHNIS 1 Ziel / Zweck 2 2 Begriffe 2 3 Vorgehen und Zuständigkeiten 2 3.1 Aufgaben der Geschäftsleitung 2 3.2. Ausrichtung auf den Kunden 2 3.3 Qualitätspolitik
Kapitel 1: VERANTWORTUNG DER LEITUNG INHALTSVERZEICHNIS 1 Ziel / Zweck 2 2 Begriffe 2 3 Vorgehen und Zuständigkeiten 2 3.1 Aufgaben der Geschäftsleitung 2 3.2. Ausrichtung auf den Kunden 2 3.3 Qualitätspolitik
Protokolle, Bericht der Managementbewertung, Übersicht der QM-Dokumente. Durchgeführt von/am: Max Mustermann am Freigegeben durch:
 MANAGEMENTBEWERTUNG Gültig für den Zeitraum: 01.01.2016 bis 12.12.2016 Prozess: Managementbewertung. Ziel: Bewertung des QM-Systems um dessen fortlaufende Eignung, Angemessenheit und Wirksamkeit sowie
MANAGEMENTBEWERTUNG Gültig für den Zeitraum: 01.01.2016 bis 12.12.2016 Prozess: Managementbewertung. Ziel: Bewertung des QM-Systems um dessen fortlaufende Eignung, Angemessenheit und Wirksamkeit sowie
DIN EN ISO 9001 : 2015 UMSETZEN. Pocket Power ANNI KOUBEK. Herausgegeben von Gerd F. Kamiske
 ANNI KOUBEK Herausgegeben von Gerd F. Kamiske DIN EN ISO 9001 : 2015 UMSETZEN Pocket Power Pocket Power Anni Koubek DIN EN ISO 9001:2015 umsetzen QM-System aufbauen und weiterentwickeln HANSER Die Wiedergabe
ANNI KOUBEK Herausgegeben von Gerd F. Kamiske DIN EN ISO 9001 : 2015 UMSETZEN Pocket Power Pocket Power Anni Koubek DIN EN ISO 9001:2015 umsetzen QM-System aufbauen und weiterentwickeln HANSER Die Wiedergabe
Modellierung ISO 9001 im Modell
 Modellierung 25.04.2018 Back to the roots Aktueller Stand MID GmbH 26.04.2018 Seite 3 Kontet Et. Stakeholder Wettbewerb AF Lieferanten Kunden Seite 4 muss dokumentiert werden Modellierungsansatz? Anforderung
Modellierung 25.04.2018 Back to the roots Aktueller Stand MID GmbH 26.04.2018 Seite 3 Kontet Et. Stakeholder Wettbewerb AF Lieferanten Kunden Seite 4 muss dokumentiert werden Modellierungsansatz? Anforderung
1 Ziel / Zweck 2. 2 Begriffe 2. 3 Vorgehen und Zuständigkeiten Allgemeines 2
 Kapitel 2: QUALITÄTSMANAGEMENTSYSTEM INHALTSVERZEICHNIS 1 Ziel / Zweck 2 2 Begriffe 2 3 Vorgehen und Zuständigkeiten 2 3.1 Allgemeines 2 3.2 Lenkung der Dokumente 3 3.2.1 Unser QM-Handbuch / Vorgabedokumente
Kapitel 2: QUALITÄTSMANAGEMENTSYSTEM INHALTSVERZEICHNIS 1 Ziel / Zweck 2 2 Begriffe 2 3 Vorgehen und Zuständigkeiten 2 3.1 Allgemeines 2 3.2 Lenkung der Dokumente 3 3.2.1 Unser QM-Handbuch / Vorgabedokumente
Musterhandbuch Kanzlei
 Musterhandbuch Kanzlei Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! Inhaltsübersicht Index: Vorwort Allgemeine Informationen Benutzerhinweise Verzeichnisstruktur Abkürzungsverzeichnis
Musterhandbuch Kanzlei Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! Inhaltsübersicht Index: Vorwort Allgemeine Informationen Benutzerhinweise Verzeichnisstruktur Abkürzungsverzeichnis
Eingesetzte Mittel Anlagen, Methoden, Fähigkeiten, Techniken, Geld, Kapital PROZESS. Bündel oder Folge von Aktivitäten
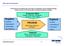 Was ist ein Prozess? Ein Prozess ist ein Bündel oder eine Folge von Aktivitäten, für die Vorgaben benötigt werden und die ein für den Kunden verwertbares Ergebnis erzeugen. Vorgaben Rohstoffe Halbfertigteile
Was ist ein Prozess? Ein Prozess ist ein Bündel oder eine Folge von Aktivitäten, für die Vorgaben benötigt werden und die ein für den Kunden verwertbares Ergebnis erzeugen. Vorgaben Rohstoffe Halbfertigteile
Vergleich der Anforderungen der RiliBÄK K 2008 mit denen der DIN EN ISO 15189
 Vergleich der der K 2008 mit denen der Petra Möller und Gerd Hafner Zentrum für Labormedizin und Mikrobiologie, Essen 5.1 Das Labor muss unter fachlich qualifizierter Leitung stehen???????? Es besteht
Vergleich der der K 2008 mit denen der Petra Möller und Gerd Hafner Zentrum für Labormedizin und Mikrobiologie, Essen 5.1 Das Labor muss unter fachlich qualifizierter Leitung stehen???????? Es besteht
Gegenüberstellung von ISO 9001:2015 und ISO 9001:2008
 von ISO 9001:2015 und ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der 4 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse und Erwartungen interessierter Parteien 4.3 Festlegen
von ISO 9001:2015 und ISO 9001:2008 ISO 9001:2015 ISO 9001:2008 4 Kontext der 4 4.1 Verstehen der und ihres Kontextes 4 5.6 4.2 Verstehen der Erfordernisse und Erwartungen interessierter Parteien 4.3 Festlegen
Qualitätsmanagement- Handbuch
 Qualitätsmanagement- Handbuch der ROTH KUNSTSTOFFTECHNIK GMBH Wolfgruben Lahnweg 35232 Dautphetal Datum der Erstausgabe: 01.01.1993 Datum dieser Revision: 2004-03-31 / Rev. 12 2004-03-31 2 (18) Inhaltsverzeichnis
Qualitätsmanagement- Handbuch der ROTH KUNSTSTOFFTECHNIK GMBH Wolfgruben Lahnweg 35232 Dautphetal Datum der Erstausgabe: 01.01.1993 Datum dieser Revision: 2004-03-31 / Rev. 12 2004-03-31 2 (18) Inhaltsverzeichnis
Die wichtigsten Änderungen
 DIN ISO 9001:2015 Die wichtigsten Änderungen und was heißt das für die dequs? Neue Gliederungsstruktur der Anforderungen Neue Querverweismatrix der dequs Stärkere Bedeutung der strategischen Ausrichtung
DIN ISO 9001:2015 Die wichtigsten Änderungen und was heißt das für die dequs? Neue Gliederungsstruktur der Anforderungen Neue Querverweismatrix der dequs Stärkere Bedeutung der strategischen Ausrichtung
DIN EN ISO - Normensystem
 1 v. 9 DIN EN ISO - Normensystem Nachweisstufen DIN EN ISO 9001 DIN EN ANFORDERUNGEN DIN EN ISO 9000 an das Qualitäts- ISO 9004 Grundlagen managementsystem und in LEITFADEN Begriffe -Qualitätsmanagement-
1 v. 9 DIN EN ISO - Normensystem Nachweisstufen DIN EN ISO 9001 DIN EN ANFORDERUNGEN DIN EN ISO 9000 an das Qualitäts- ISO 9004 Grundlagen managementsystem und in LEITFADEN Begriffe -Qualitätsmanagement-
Musterhandbuch Kinderbetreuung
 en Musterhandbuch Kinderbetreuung Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-935388-46-7 Auflage 3 Inhaltsübersicht Index: Vorwort Allgemeine Informationen
en Musterhandbuch Kinderbetreuung Leseprobe DIN EN ISO 9001:2008 Konditionen: 14 Tage Rückgaberecht! Kein Abo! ISBN 978-3-935388-46-7 Auflage 3 Inhaltsübersicht Index: Vorwort Allgemeine Informationen
Fragebogen. zur Beurteilung der Zertifizierungsfähigkeit des Betrieblichen Gesundheitsmanagements nach DIN SPEC
 zur Beurteilung der Zertifizierungsfähigkeit des Betrieblichen Gesundheitsmanagements nach 4 Umfeld der Organisation 1 Haben Sie die Interessierten Parteien (oder Kunden) bestimmt, die Bedeutung für Ihr
zur Beurteilung der Zertifizierungsfähigkeit des Betrieblichen Gesundheitsmanagements nach 4 Umfeld der Organisation 1 Haben Sie die Interessierten Parteien (oder Kunden) bestimmt, die Bedeutung für Ihr
Internes Audit. Beispiel
 Beispiel Verfahrensanweisung Dok.-Nr. 2.11 Internes Audit Revision 0 erstellt am 24.02.2010 Seite 1 von 5 Ziel und Zweck: Durch interne Audits werden alle betrieblichen Bereiche und Prozesse dahingehend
Beispiel Verfahrensanweisung Dok.-Nr. 2.11 Internes Audit Revision 0 erstellt am 24.02.2010 Seite 1 von 5 Ziel und Zweck: Durch interne Audits werden alle betrieblichen Bereiche und Prozesse dahingehend
