Übersicht über Eylea und Begründung für die Zulassung in der EU
|
|
|
- Anna Weiner
- vor 5 Jahren
- Abrufe
Transkript
1 EMA/481361/2018 EMEA/H/C/ Übersicht über Eylea und Begründung für die Zulassung in der EU Was ist Eylea und wofür wird es angewendet? Eylea ist ein Arzneimittel für Erwachsene zur Behandlung: der feuchten Form der altersabhängigen Makuladegeneration (AMD), einer Erkrankung, die sich auf den zentralen Teil der Netzhaut (als Makula bezeichnet) im Augenhintergrund auswirkt. Die feuchte Form der AMD wird durch choroidale Neovaskularisation (ein abnormales Wachstum der Blutgefäße unter der Makula) verursacht. Aus diesen Blutgefäßen können Flüssigkeit und Blut austreten und eine Schwellung hervorrufen; des beeinträchtigten Sehvermögens aufgrund eines Makulaödems (Schwellung der Makula) infolge der Blockierung der Hauptvene, die Blut von der Retina (Netzhaut) transportiert (bezeichnet als zentraler retinaler Venenverschluss (CRVO)), oder von kleineren Astvenen (bezeichnet als retinaler Astvenenverschluss (BRVO)); des beeinträchtigten Sehvermögens aufgrund eines durch Diabetes verursachten Makulaödems; des beeinträchtigten Sehvermögens aufgrund einer choroidalen Neovaskularisation infolge von Myopie (einer extremen Art von Kurzsichtigkeit, bei der der Augapfel beständig wächst und länger wird, als er sein sollte). Die Makula sorgt für das zentrale Sehvermögen, das für detailgenaues Sehen bei alltäglichen Aufgaben wie Autofahren, Lesen und das Erkennen von Gesichtern erforderlich ist. Die Erkrankungen führen bei den betroffenen Personen zu einem allmählichen Verlust des zentralen Sehvermögens. Eylea enthält den Wirkstoff Aflibercept. Wie wird Eylea angewendet? Eylea ist als Fertigspritzen oder Durchstechflaschen mit einer Lösung zur intravitrealen Injektion (Injektion in den Glaskörper, die gelartige Flüssigkeit im Inneren des Auges) erhältlich. Es ist nur auf ärztliche Verschreibung erhältlich und muss von einem qualifizierten Arzt verabreicht werden, der in der Durchführung intravitrealer Injektionen erfahren ist. 30 Churchill Place Canary Wharf London E14 5EU United Kingdom Telephone +44 (0) Facsimile +44 (0) Send a question via our website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 Eylea wird als 2-mg-Injektion in das betroffene Auge gegeben, die in geeigneten Abständen von einem Monat oder länger wiederholt wird. Die Injektionshäufigkeit hängt von der zu behandelnden Erkrankung und dem Ansprechen des Patienten auf die Behandlung ab. Die Injektion muss unter sterilen Bedingungen erfolgen. Die Fertigspritze und die Durchstechflasche sind nur für den einmaligen Gebrauch vorgesehen. Die Fertigspritze enthält mehr als die empfohlene Dosis; daher muss der Arzt bei der Vorbereitung der Injektion das überschüssige Volumen aus der Spritze herausdrücken und darauf achten, dass er die richtige Dosis injiziert. Nach der Injektion muss der Augeninnendruck überprüft werden. Weitere Informationen zur Anwendung von Eylea entnehmen Sie der Packungsbeilage, oder wenden Sie sich an Ihren Arzt oder Apotheker. Wie wirkt Eylea? Aflibercept ist ein biotechnologisch hergestelltes Protein, das so konzipiert ist, dass es an eine Substanz mit der Bezeichnung vaskulärer endothelialer Wachstumsfaktor A (vascular endothelial growth factor A, VEGF-A) bindet und dessen Wirkung blockiert. Es kann außerdem an andere Proteine, wie z. B. den plazentaren Wachstumsfaktor (placental growth factor, PlGF), binden. VEGF-A und PlGF sind an der Stimulierung des abnormalen Wachstums von Blutgefäßen bei Patienten mit AMD, bestimmten Arten von Makulaödemen und choroidaler Neovaskularisation infolge von Myopie beteiligt. Durch die Blockierung dieser Faktoren verringert Aflibercept das Wachstum der Blutgefäße und reguliert den Flüssigkeitsaustritt und die Schwellung. Welchen Nutzen hat Eylea in den Studien gezeigt? Feuchte AMD Eylea wurde in zwei Hauptstudien untersucht, an denen insgesamt etwa Patienten mit feuchter AMD teilnahmen. In den Studien wurde Eylea (in einer Dosierung von entweder 0,5 mg alle vier Wochen, 2 mg alle vier Wochen oder 2 mg alle acht Wochen, jeweils nach drei monatlichen Gaben zu Behandlungsbeginn) mit Ranibizumab verglichen, einem weiteren Arzneimittel zur Behandlung der AMD, das alle vier Wochen als Injektion ins Auge verabreicht wurde. Der Hauptindikator für die Wirksamkeit war der Anteil der Patienten, bei denen das Sehvermögen nach dem ersten Behandlungsjahr erhalten blieb (definiert als die Verschlechterung des Sehvermögens um weniger als 15 Buchstaben bei einem Standardsehtest). In beiden Studien wurde außerdem untersucht, inwieweit die Wirkung im zweiten Behandlungsjahr, in dem die Anzahl der Injektionen und der Zeitraum zwischen den Injektionen je nach Sehvermögen und Augenveränderungen angepasst wurden, erhalten blieb. Eylea hat sich im Hinblick auf die Erhaltung des Sehvermögens bei Patienten mit feuchter AMD als ebenso wirksam wie Ranibizumab erwiesen: In den zwei Studien zusammengenommen betrug der Anteil der Patienten, bei denen das Sehvermögen erhalten blieb, 96,1 % (517 von 538), 95,4 % (533 von 559) und 95,3 % (510 von 535) für 0,5 mg Eylea alle vier Wochen, 2 mg Eylea alle vier Wochen bzw. 2 mg Eylea alle acht Wochen im Vergleich zu 94,4 % (508 von 538) bei den Patienten, die mit Ranibizumab alle vier Wochen behandelt worden waren. Im zweiten Behandlungsjahr blieb die Wirkung im Allgemeinen erhalten. Der Großteil der Patienten erhielt die Injektionen in einem längeren Zeitabstand von 10 Wochen, wobei eine geringe Zahl von Patienten gelegentlich häufigere Injektionen (z. B. monatlich) benötigte. Anschließend gewonnene Ergebnisse aus einer unterstützenden Studie legten die Wirksamkeit verlängerter Behandlungsabstände bei Patienten mit feuchter AMD nahe. EMA/481361/2018 Seite 2/5
3 Makulaödem infolge eines retinalen Venenverschlusses Eylea wurde zudem in zwei weiteren Hauptstudien untersucht, an denen 366 Patienten mit Makulaödem infolge von CRVO teilnahmen. Dabei wurde eine monatliche Injektion von 2 mg Eylea mit einer Scheininjektion verglichen, bei der eine Spritze ohne Nadel verwendet wurde. In einer weiteren Hauptstudie mit 181 Patienten mit Makulaödem infolge von BRVO wurden die monatlichen Injektionen von 2 mg Eylea mit einer Laserbehandlung verglichen. In allen Studien war der Hauptindikator für die Wirksamkeit der Anteil der Patienten, die auf die Behandlung ansprachen und deren Sehvermögen sich bei einem Sehtest 24 Wochen nach der Behandlung um mindestens 15 Buchstaben verbessert hat. In den Studien mit Patienten mit Makulaödem infolge von CRVO wurden zudem die Wirkungen einer Bedarfsbehandlung nach 24 Wochen untersucht. Eylea führte zudem bei Patienten mit Makulaödem infolge von CRVO und BRVO zu einer erheblichen Verbesserung des Sehvermögens. Bei CRVO wiesen insgesamt 60 % der Patienten, denen Eylea verabreicht wurde, beim Sehtest in Woche 24 eine Verbesserung von mindestens 15 Buchstaben auf, verglichen mit 17 % der Patienten, die Scheininjektionen erhielten. Bei der Bedarfsbehandlung wurde der Nutzen bis zu 52 Wochen weitgehend aufrechterhalten, jedoch schien der Nutzen etwas abzunehmen, wenn Patienten über längere Zeiträume als diesen behandelt und überwacht wurden. Bei BRVO wiesen ca. 53 % der Patienten, denen Eylea verabreicht wurde, beim Sehtest in Woche 24 eine Verbesserung von mindestens 15 Buchstaben auf, verglichen mit 27 % der Patienten, die eine Laserbehandlung erhielten. Diese Wirkung wurde 52 Wochen aufrechterhalten, obwohl Eylea zwischen Woche 24 und Woche 52 weniger häufig gegeben wurde. Diabetisches Makulaödem In zwei weiteren Studien, an denen 872 Patienten mit diabetischem Makulaödem teilnahmen, wurde die Wirkung von Eylea im Vergleich mit einer Laserbehandlung untersucht. Dabei wurde Eylea entweder einmal pro Monat oder einmal alle zwei Monate nach vorangegangenen fünf monatlichen Injektionen verabreicht. Der Hauptindikator für die Wirksamkeit war in beiden Studien die Veränderung bei der Anzahl der Buchstaben, die die Patienten in einem Sehtest nach einem Jahr Behandlung lesen konnten. Bei Patienten mit diabetischem Makulaödem lag die Anzahl der Buchstaben, die sie in einem Sehtest vor der Behandlung lesen konnten, im Durchschnitt bei etwa 59 bis 60. Bei Patienten, denen Eylea monatlich verabreicht wurde, verbesserte sich diese Zahl um etwa 12 Buchstaben und bei denen, die Eylea alle zwei Monate erhielten, um etwa 11 Buchstaben. Demgegenüber lag die Verbesserung bei Patienten, die eine Laserbehandlung erhielten, nach einem Jahr bei nur etwa 1 Buchstaben. Choroidale Neovaskularisation infolge von Myopie Bei choroidaler Neovaskularisation infolge von Myopie wurde Eylea in einer Hauptstudie mit 122 Patienten untersucht, wobei Eylea mit einer Scheininjektion verglichen wurde. Der Hauptindikator für die Wirksamkeit war die Veränderung bei der Anzahl der Buchstaben, die die Patienten in einem Sehtest nach 24-wöchiger Behandlung lesen konnten. In der Studie über choroidale Neovaskularisation infolge von Myopie konnten die Patienten bei einem Sehtest vor der Behandlung durchschnittlich 56 Buchstaben lesen; Patienten, die Eylea erhielten, konnten nach einer Behandlung von 24 Wochen durchschnittlich 12 Buchstaben mehr lesen, und bei Patienten, die Scheininjektionen erhielten, sank die Gesamtanzahl der Buchstaben, die sie lesen konnten, um durchschnittlich 2. EMA/481361/2018 Seite 3/5
4 Welche Risiken sind mit Eylea verbunden? Sehr häufige Nebenwirkungen von Eylea (die mindestens 1 von 20 Patienten betreffen können) sind konjunktivale Hämorrhagie (Blutung aus den kleinen Blutgefäßen auf der Oberfläche des Auges an der Injektionsstelle), reduziertes Sehvermögen, Augenschmerzen, Glaskörperabhebung (Abhebung der gelartigen Substanz im Inneren des Auges), Katarakt (Linsentrübung), Glaskörperschlieren (kleine Partikel oder Flecken im Gesichtsfeld) und erhöhter Augeninnendruck. Schwerwiegende mit der Injektion verbundene Nebenwirkungen (die bei weniger als 1 von ca Injektionen auftraten) umfassen Erblindung, Endophthalmitis (schwerwiegende Infektion oder Entzündung im Inneren des Auges), Katarakt, erhöhten Augeninnendruck, Glaskörperblutung (Blutung in der gelartigen Flüssigkeit im Auge, die zu einem vorübergehenden Sehverlust führt) sowie Glaskörper- oder Netzhautabhebung. Die vollständige Auflistung der im Zusammenhang mit Eylea berichteten Nebenwirkungen ist der Packungsbeilage zu entnehmen. Eylea darf nicht bei Patienten angewendet werden, bei denen okuläre oder periokuläre Infektionen (Infektionen im Auge oder in der Umgebung des Auges) bestehen oder vermutet werden, bzw. bei Patienten, die unter einer schweren Entzündung im Auge leiden. Die vollständige Auflistung der Einschränkungen ist der Packungsbeilage zu entnehmen. Warum wurde Eylea in der EU zugelassen? Die Europäische Arzneimittel-Agentur stellte fest, dass Eylea bei feuchter AMD im Hinblick auf die Erhaltung des Sehvermögens der Patienten nach dem ersten Behandlungsjahr ebenso wirksam war wie Ranibizumab. Darüber hinaus war die Agentur der Ansicht, dass Eylea bei der Verbesserung des Sehvermögens von Patienten mit Makulaödem infolge von CRVO, BRVO oder Diabetes sowie bei Patienten mit choroidaler Neovaskularisation infolge von Myopie von Nutzen war. Die Agentur stellte weiter fest, dass es im Zusammenhang mit Eylea keine größeren oder unerwarteten Sicherheitsbedenken gab. Daher gelangte die Agentur zu dem Schluss, dass der Nutzen von Eylea gegenüber den Risiken überwiegt und dass es in der EU zugelassen werden kann. Welche Maßnahmen werden zur Gewährleistung der sicheren und wirksamen Anwendung von Eylea ergriffen? Das Unternehmen, das Eylea in Verkehr bring, wird aktuelles Informationsmaterial für Ärzte (zur Minimierung des Risikos, das mit Injektionen ins Auge verbunden ist) und Patienten (damit diese schwerwiegende Nebenwirkungen erkennen können und wissen, wann sie sich dringend in ärztliche Behandlung begeben müssen) zur Verfügung stellen. Darüber hinaus wird das Unternehmen eine Studie, bei der die verlängerten Behandlungsabstände von Eylea bei Makulaödem infolge von Diabetes untersucht werden, sowie eine Studie durchführen, bei der die Wirkungen von Eylea als Bedarfsbehandlung bei der feuchten AMD untersucht werden. Empfehlungen und Vorsichtsmaßnahmen zur sicheren und wirksamen Anwendung von Eylea, die von Angehörigen der Heilberufe und Patienten befolgt werden müssen, wurden auch in die Zusammenfassung der Merkmale des Arzneimittels und die Packungsbeilage aufgenommen. Wie bei allen Arzneimitteln werden Daten zur Anwendung von Eylea kontinuierlich überwacht. Gemeldete Nebenwirkungen von Eylea werden sorgfältig ausgewertet und alle notwendigen Maßnahmen zum Schutz der Patienten ergriffen. EMA/481361/2018 Seite 4/5
5 Weitere Informationen über Eylea Eylea erhielt am 22. November 2012 eine Genehmigung für das Inverkehrbringen in der gesamten EU. Weitere Informationen zu Eylea finden Sie auf den Internetseiten der Agentur: ema.europa.eu/find medicine/human medicines/european public assessment reports. Diese Übersicht wurde zuletzt im aktualisiert. EMA/481361/2018 Seite 5/5
des beeinträchtigten Sehvermögens aufgrund eines durch Diabetes verursachten Makulaödems;
 EMA/677928/2015 EMEA/H/C/002392 Zusammenfassung des EPAR für die Öffentlichkeit Aflibercept Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/677928/2015 EMEA/H/C/002392 Zusammenfassung des EPAR für die Öffentlichkeit Aflibercept Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
weitere Störungen des Sehvermögens, die auf eine choroidale Neovaskularisation zurückzuführen sind;
 EMA/704742/2016 EMEA/H/C/000715 Zusammenfassung des EPAR für die Öffentlichkeit Ranibizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/704742/2016 EMEA/H/C/000715 Zusammenfassung des EPAR für die Öffentlichkeit Ranibizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Stelara ist ein Arzneimittel, das zur Behandlung der folgenden Erkrankungen angewendet wird:
 EMA/636854/2016 EMEA/H/C/000958 Zusammenfassung des EPAR für die Öffentlichkeit Ustekinumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/636854/2016 EMEA/H/C/000958 Zusammenfassung des EPAR für die Öffentlichkeit Ustekinumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
PATIENT. Patienten-Ratgeber für die Behandlung mit EYLEA. (Aflibercept Injektionslösung)
 PATIENT Patienten-Ratgeber für die Behandlung mit EYLEA (Aflibercept Injektionslösung) Lesen Sie sich bitte vor Beginn Ihrer Behandlung mit EYLEA das gesamte Informationsmaterial, einschließlich der beiliegenden
PATIENT Patienten-Ratgeber für die Behandlung mit EYLEA (Aflibercept Injektionslösung) Lesen Sie sich bitte vor Beginn Ihrer Behandlung mit EYLEA das gesamte Informationsmaterial, einschließlich der beiliegenden
metastasiertes Mammakarzinom (Brustkrebs) in Kombination mit Paclitaxel oder Capecitabin;
 EMA/302947/2017 EMEA/H/C/000582 Zusammenfassung des EPAR für die Öffentlichkeit Bevacizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/302947/2017 EMEA/H/C/000582 Zusammenfassung des EPAR für die Öffentlichkeit Bevacizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Pradaxa ist ein Arzneimittel, das den Wirkstoff Dabigatranetexilat enthält. Es ist als Kapseln (75 mg, 110 mg und 150 mg) erhältlich.
 EMA/47517/2015 EMEA/H/C/000829 Zusammenfassung des EPAR für die Öffentlichkeit Dabigatranetexilat Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird
EMA/47517/2015 EMEA/H/C/000829 Zusammenfassung des EPAR für die Öffentlichkeit Dabigatranetexilat Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird
Xarelto ist ein Antikoagulans (Arzneimittel, das die Blutgerinnung verhindert), das bei Erwachsenen angewendet wird:
 EMA/708716/2017 EMEA/H/C/000944 Zusammenfassung des EPAR für die Öffentlichkeit Rivaroxaban Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/708716/2017 EMEA/H/C/000944 Zusammenfassung des EPAR für die Öffentlichkeit Rivaroxaban Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Keytruda ist ein Arzneimittel, das zur Behandlung der folgenden Krebserkrankungen angewendet wird:
 EMA/524789/2017 EMEA/H/C/003820 Zusammenfassung des EPAR für die Öffentlichkeit Pembrolizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/524789/2017 EMEA/H/C/003820 Zusammenfassung des EPAR für die Öffentlichkeit Pembrolizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Eylea 40 mg/ml Injektionslösung in einer Durchstechflasche
 Gebrauchsinformation: Information für Patienten Eylea 40 mg/ml Injektionslösung in einer Durchstechflasche Aflibercept Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor bei Ihnen dieses Arzneimittel
Gebrauchsinformation: Information für Patienten Eylea 40 mg/ml Injektionslösung in einer Durchstechflasche Aflibercept Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor bei Ihnen dieses Arzneimittel
Opdivo wird als Einzelarzneimittel zur Behandlung von Erwachsenen mit folgenden Erkrankungen angewendet:
 EMA/303208/2017 EMEA/H/C/003985 Zusammenfassung des EPAR für die Öffentlichkeit Nivolumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/303208/2017 EMEA/H/C/003985 Zusammenfassung des EPAR für die Öffentlichkeit Nivolumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Pneumokokkenpolysaccharid-Konjugatimpfstoff (13-valent, adsorbiert)
 EMA/90006/2015 EMEA/H/C/001104 Zusammenfassung des EPAR für die Öffentlichkeit Pneumokokkenpolysaccharid-Konjugatimpfstoff (13-valent, adsorbiert) Dies ist eine Zusammenfassung des Europäischen Öffentlichen
EMA/90006/2015 EMEA/H/C/001104 Zusammenfassung des EPAR für die Öffentlichkeit Pneumokokkenpolysaccharid-Konjugatimpfstoff (13-valent, adsorbiert) Dies ist eine Zusammenfassung des Europäischen Öffentlichen
Übersicht über Opdivo und Begründung für die Zulassung in der EU
 EMA/489091/2018 EMEA/H/C/003985 Übersicht über Opdivo und Begründung für die Zulassung in der EU Was ist Opdivo und wofür wird es angewendet? Opdivo ist ein Krebsarzneimittel, das zur Behandlung der folgenden
EMA/489091/2018 EMEA/H/C/003985 Übersicht über Opdivo und Begründung für die Zulassung in der EU Was ist Opdivo und wofür wird es angewendet? Opdivo ist ein Krebsarzneimittel, das zur Behandlung der folgenden
Lucentis (ranibizumab)
 Die Europäischen Gesundheitsbehörden haben bestimmte Bedingungen an die Vermarktung des Arnzeimittels LUCENTIS geknüpft. Der verbindliche Plan für Risikobeschränkung in Belgien, zu dem diese Informationen
Die Europäischen Gesundheitsbehörden haben bestimmte Bedingungen an die Vermarktung des Arnzeimittels LUCENTIS geknüpft. Der verbindliche Plan für Risikobeschränkung in Belgien, zu dem diese Informationen
Bei multiplem Myelom, einem Krebs eines Typs weißer Blutkörperchen, der sogenannten Plasmazellen, wird Revlimid angewendet:
 EMA/113870/2017 EMEA/H/C/000717 Zusammenfassung des EPAR für die Öffentlichkeit Lenalidomid Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/113870/2017 EMEA/H/C/000717 Zusammenfassung des EPAR für die Öffentlichkeit Lenalidomid Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Behandlung des Sehschärfenverlustes infolge eines diabetischen Makulaödems in der EU
 Aflibercept zur Injektion ins Auge: Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehsc Aflibercept zur Injektion ins Auge: Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehschärfenverlustes
Aflibercept zur Injektion ins Auge: Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehsc Aflibercept zur Injektion ins Auge: Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehschärfenverlustes
EYLEA 40 MG/ML. Injektionslösung. aflibercept PATIENTEN- INFORMATIONSPAKET
 Die europäischen Gesundheitsbehörden haben das Inverkehrbringen des Arzneimittels Eylea mit bestimmten Auflagen verbunden. Der vorgeschriebene Plan zur Risikominimierung in Belgien und Luxemburg, zu dem
Die europäischen Gesundheitsbehörden haben das Inverkehrbringen des Arzneimittels Eylea mit bestimmten Auflagen verbunden. Der vorgeschriebene Plan zur Risikominimierung in Belgien und Luxemburg, zu dem
Lucentis (ranibizumab)
 Um die Wirkungen des Arzneimittels LUCENTIS für Ihre Gesundheit optimal nutzen zu können, seine ordnungsgemäße Anwendung sicherzustellen und seine Nebenwirkungen zu begrenzen, sind bestimmte Maßnahmen/Sicherheitsvorkehrungen
Um die Wirkungen des Arzneimittels LUCENTIS für Ihre Gesundheit optimal nutzen zu können, seine ordnungsgemäße Anwendung sicherzustellen und seine Nebenwirkungen zu begrenzen, sind bestimmte Maßnahmen/Sicherheitsvorkehrungen
Übersicht über Opdivo und Begründung für die Zulassung in der EU
 EMA/55255/2019 EMEA/H/C/003985 Übersicht über Opdivo und Begründung für die Zulassung in der EU Was ist Opdivo und wofür wird es angewendet? Opdivo ist ein Krebsarzneimittel, das zur Behandlung der folgenden
EMA/55255/2019 EMEA/H/C/003985 Übersicht über Opdivo und Begründung für die Zulassung in der EU Was ist Opdivo und wofür wird es angewendet? Opdivo ist ein Krebsarzneimittel, das zur Behandlung der folgenden
Patienten-Ratgeber für die Behandlung der feuchten altersbedingten Makuladegeneration mit EYLEA. (Afl ibercept Injektionslösung)
 Patienten-Ratgeber für die Behandlung der feuchten altersbedingten Makuladegeneration mit EYLEA (Afl ibercept Injektionslösung) P Lesen Sie sich bitte vor Beginn Ihrer Behandlung mit EYLEA das gesamte
Patienten-Ratgeber für die Behandlung der feuchten altersbedingten Makuladegeneration mit EYLEA (Afl ibercept Injektionslösung) P Lesen Sie sich bitte vor Beginn Ihrer Behandlung mit EYLEA das gesamte
Bayer erhält Empfehlung für neue Behandlungsoption mit Aflibercept-Injektionslösung in der EU
 Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Bayer erhält Empfehlung für neue Behandlungsoption mit Aflibercept-Injektionslösung in der EU CHMP empfiehlt
Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Bayer erhält Empfehlung für neue Behandlungsoption mit Aflibercept-Injektionslösung in der EU CHMP empfiehlt
Aflibercept (Eylea) bei altersbedingter Makuladegeneration
 verstehen abwägen entscheiden Aflibercept (Eylea) bei altersbedingter Makuladegeneration Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) Inhaltsverzeichnis Überblick Einleitung
verstehen abwägen entscheiden Aflibercept (Eylea) bei altersbedingter Makuladegeneration Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) Inhaltsverzeichnis Überblick Einleitung
Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Signalen
 25 January 2018 EMA/PRAC/35610/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Verabschiedet im Rahmen
25 January 2018 EMA/PRAC/35610/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Verabschiedet im Rahmen
Heilsame Injektionen für das Auge Wie bringt man Medikamente sicher ins Innere des Augapfels? Wenn Augenärzte Augenleiden mit Medikamenten behandeln,
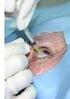 Augenärzte informieren: Intravitreale Injektion Operative Medikamenteneingabe in das Auge Berufsverband der Augenärzte Deutschlands e.v. (BVA) Deutsche Ophthalmologische Gesellschaft (DOG) Heilsame Injektionen
Augenärzte informieren: Intravitreale Injektion Operative Medikamenteneingabe in das Auge Berufsverband der Augenärzte Deutschlands e.v. (BVA) Deutsche Ophthalmologische Gesellschaft (DOG) Heilsame Injektionen
Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Signalen
 15 September 2016 EMA/PRAC/603548/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Verabschiedet im Rahmen
15 September 2016 EMA/PRAC/603548/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Verabschiedet im Rahmen
Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehschärfenverlustes infolge eines diabetischen Makulaödems in der EU
 Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Aflibercept zur Injektion ins Auge: Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehschärfenverlustes
Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Aflibercept zur Injektion ins Auge: Bayer erhält Empfehlung zur Zulassung für die Behandlung des Sehschärfenverlustes
Intravitreale Injektionen Empfehlungen für die Behandlung mit EYLEA
 ARZT Intravitreale Injektionen Empfehlungen für die Behandlung mit EYLEA Informationen für den behandelnden Arzt Weitere Informationen und Einzelheiten zu EYLEA entnehmen Sie bitte der Fachinformation.
ARZT Intravitreale Injektionen Empfehlungen für die Behandlung mit EYLEA Informationen für den behandelnden Arzt Weitere Informationen und Einzelheiten zu EYLEA entnehmen Sie bitte der Fachinformation.
Die altersabhängige Makuladegeneration
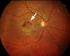 Die altersabhängige Makuladegeneration Die Makuladegeneration ist eine bei älteren Menschen sehr häufige Erkrankung der Netzhautmitte (Makula) und ist in den Industrieländern die häufigste Erblindungsursache
Die altersabhängige Makuladegeneration Die Makuladegeneration ist eine bei älteren Menschen sehr häufige Erkrankung der Netzhautmitte (Makula) und ist in den Industrieländern die häufigste Erblindungsursache
INFORMATIONEN FÜR DEN BEHANDELNDEN ARZT
 Intravitreale Injektionen Empfehlungen für die Behandlung mit EYLEA INFORMATIONEN FÜR DEN BEHANDELNDEN ARZT Weitere Informationen und Einzelheiten zu EYLEA entnehmen Sie bitte
Intravitreale Injektionen Empfehlungen für die Behandlung mit EYLEA INFORMATIONEN FÜR DEN BEHANDELNDEN ARZT Weitere Informationen und Einzelheiten zu EYLEA entnehmen Sie bitte
Investor News. Bayer erhält Zulassung für Eylea in China
 Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Bayer erhält Zulassung für Eylea in China Eylea erhält in China die Zulassung zur Behandlung des Sehschärfenverlusts
Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Bayer erhält Zulassung für Eylea in China Eylea erhält in China die Zulassung zur Behandlung des Sehschärfenverlusts
PATIENTENINFORMATION
 Die belgischen Gesundheitsbehörden haben bestimmte Voraussetzungen für das Inverkehrbringen des Arzneimittels Azzalure erlassen. Der in Belgien vorgeschriebene Plan zur Risikominimierung, zu dem diese
Die belgischen Gesundheitsbehörden haben bestimmte Voraussetzungen für das Inverkehrbringen des Arzneimittels Azzalure erlassen. Der in Belgien vorgeschriebene Plan zur Risikominimierung, zu dem diese
Gebrauchsinformation: Information für Patienten. Eylea 40 mg/ml Injektionslösung in einer Durchstechflasche Aflibercept
 Gebrauchsinformation: Information für Patienten Eylea 40 mg/ml Injektionslösung in einer Durchstechflasche Aflibercept Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Gebrauchsinformation: Information für Patienten Eylea 40 mg/ml Injektionslösung in einer Durchstechflasche Aflibercept Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Signalen
 17 December 2015 EMA/PRAC/835772/2015 Rev 1 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Verabschiedet im
17 December 2015 EMA/PRAC/835772/2015 Rev 1 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Verabschiedet im
Behandlung der feuchten altersabhängigen Makuladegeneration (feuchte AMD) mit VEGF-Hemmern durch operative Medikamenteneingabe in das Auge
 Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
Augenarztpraxis AltenKirchen Dr. med. Thomas Wehler Facharzt für Augenheilkunde Wilhelmstr. 32 Schlossweg 2 57610 Altenkirchen Tel 02681-1651 Fax 02681-6094 Mail info@ak-augenarzt.de Net www.ak-augenarzt.de
LUCENTIS. bei Visusbeeinträchtigung infolge eines diabetischen Makulaödems (DMÖ) Ihr Leitfaden für die Behandlung mit LUCENTIS
 LUCENTIS bei Visusbeeinträchtigung infolge eines diabetischen Makulaödems (DMÖ) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Die vorliegende Broschüre vermittelt Ihnen wichtige
LUCENTIS bei Visusbeeinträchtigung infolge eines diabetischen Makulaödems (DMÖ) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Die vorliegende Broschüre vermittelt Ihnen wichtige
Neue Einschränkungen zur Minimierung der Risiken für Auswirkungen auf den Herzrhythmus bei Hydroxyzin enthaltenden Arzneimitteln
 Freitag, 27. März 2015 EMA/149624/2015 Neue Einschränkungen zur Minimierung der Risiken für Auswirkungen auf den Herzrhythmus bei Hydroxyzin enthaltenden Arzneimitteln Die Anwendung ist bei Patienten mit
Freitag, 27. März 2015 EMA/149624/2015 Neue Einschränkungen zur Minimierung der Risiken für Auswirkungen auf den Herzrhythmus bei Hydroxyzin enthaltenden Arzneimitteln Die Anwendung ist bei Patienten mit
BAnz AT B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 3a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 3a SGB
Avastin wird zur Behandlung von Erwachsenen mit den folgenden Krebsarten in Kombination mit anderen Arzneimitteln gegen Krebs angewendet:
 EMA/175824/2015 EMEA/H/C/000582 Zusammenfassung des EPAR für die Öffentlichkeit Bevacizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/175824/2015 EMEA/H/C/000582 Zusammenfassung des EPAR für die Öffentlichkeit Bevacizumab Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
Übersicht über Metacam und Gründe für die Zulassung in der EU
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Übersicht über Metacam und Gründe für die Zulassung in der EU Was ist Metacam und wofür wird es angewendet? Metacam ist ein entzündungshemmendes Arzneimittel zur Anwendung
EMA/CVMP/259397/2006 EMEA/V/C/000033 Übersicht über Metacam und Gründe für die Zulassung in der EU Was ist Metacam und wofür wird es angewendet? Metacam ist ein entzündungshemmendes Arzneimittel zur Anwendung
Positive Studien-Ergebnisse mit VEGF Trap-Eye bei Zentralvenen- Verschluss des Auges und bei diabetischem Makulaödem
 Investor News Nur zur Verwendung außerhalb der USA Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Positive Studien-Ergebnisse mit VEGF Trap-Eye bei Zentralvenen- Verschluss
Investor News Nur zur Verwendung außerhalb der USA Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Positive Studien-Ergebnisse mit VEGF Trap-Eye bei Zentralvenen- Verschluss
Empfehlungen des PRAC zu Signalen für die Aktualisierung der Produktinformationen
 23 April 2015 EMA/PRAC/273924/2015 Pharmacovigilance Risk Assessment Committee Empfehlungen des PRAC zu Signalen für die Aktualisierung der Produktinformationen Verabschiedet im Rahmen der PRAC-Sitzung
23 April 2015 EMA/PRAC/273924/2015 Pharmacovigilance Risk Assessment Committee Empfehlungen des PRAC zu Signalen für die Aktualisierung der Produktinformationen Verabschiedet im Rahmen der PRAC-Sitzung
Wichtige sicherheitsrelevante Infor mationen für Patienten für die Behandlung mit LUCENTIS (Ranibizumab)
 Wichtige sicherheitsrelevante Infor mationen für Patienten für die Behandlung mit LUCENTIS (Ranibizumab) Die vorliegende Broschüre vermittelt Ihnen wichtige Informationen über die Behandlung mit diesem
Wichtige sicherheitsrelevante Infor mationen für Patienten für die Behandlung mit LUCENTIS (Ranibizumab) Die vorliegende Broschüre vermittelt Ihnen wichtige Informationen über die Behandlung mit diesem
LUCENTIS. bei feuchter altersbedingter Makuladegeneration (AMD) Ihr Leitfaden für die Behandlung mit LUCENTIS
 LUCENTIS bei feuchter altersbedingter Makuladegeneration (AMD) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Die vorliegende Broschüre vermittelt Ihnen wichtige Informationen über
LUCENTIS bei feuchter altersbedingter Makuladegeneration (AMD) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Die vorliegende Broschüre vermittelt Ihnen wichtige Informationen über
Erneut positive Studien-Ergebnisse in Phase III für VEGF Trap-Eye bei Zentralvenenverschluss der Netzhaut
 Investor News Nicht für US-Medien bestimmt Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Erneut positive Studien-Ergebnisse in Phase III für VEGF Trap-Eye bei Zentralvenenverschluss
Investor News Nicht für US-Medien bestimmt Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Erneut positive Studien-Ergebnisse in Phase III für VEGF Trap-Eye bei Zentralvenenverschluss
FRAGEBOGEN FÜR KINDER UND JUGENDLICHE
 Meinung in Bezug auf die Anwendung von Medikamenten Warum fragen wir? Der Pädiatrische Ausschuss (Paediatric Committee (PDCO)) arbeitet zusammen mit der Europäischen Arzneimittelagentur. Dieser Ausschuss
Meinung in Bezug auf die Anwendung von Medikamenten Warum fragen wir? Der Pädiatrische Ausschuss (Paediatric Committee (PDCO)) arbeitet zusammen mit der Europäischen Arzneimittelagentur. Dieser Ausschuss
Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen des PRAC zu Signalen
 10 November 2016 EMA/PRAC/738492/2016 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen Verabschiedet im Rahmen der
10 November 2016 EMA/PRAC/738492/2016 Corr 1 Pharmacovigilance Risk Assessment Committee (PRAC) Neufassung des Wortlauts der Produktinformationen Auszüge aus den Empfehlungen Verabschiedet im Rahmen der
AMD kann das scharfe Sehen zerstören, das notwendig ist für Aktivitäten wie Lesen, Autofahren und für das Erkennen von Gesichtern.
 Was ist AMD? AMD (Altersbedingte Makuladegeneration) ist eine Erkrankung des Auges, bei der im Alter zu einer Schädigung der Stelle des schärfsten Sehens (Makula) kommt. AMD kann zum Verlust der Sehkraft
Was ist AMD? AMD (Altersbedingte Makuladegeneration) ist eine Erkrankung des Auges, bei der im Alter zu einer Schädigung der Stelle des schärfsten Sehens (Makula) kommt. AMD kann zum Verlust der Sehkraft
LUCENTIS bei Visusbeeinträchtigung infolge eines Makulaödems aufgrund eines retinalen Venenverschlusses (RVV)
 DIE WELT IST WUNDERSCHÖN ANZUSEHEN LUCENTIS bei Visusbeeinträchtigung infolge eines Makulaödems aufgrund eines retinalen Venenverschlusses (RVV) Ihr Leitfaden für die Behandlung mit LUCENTIS Teil 1 Über
DIE WELT IST WUNDERSCHÖN ANZUSEHEN LUCENTIS bei Visusbeeinträchtigung infolge eines Makulaödems aufgrund eines retinalen Venenverschlusses (RVV) Ihr Leitfaden für die Behandlung mit LUCENTIS Teil 1 Über
Metacam. Meloxicam. Was ist Metacam und wofür wird es angewendet? Zusammenfassung des EPAR für die Öffentlichkeit
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Zusammenfassung des EPAR für die Öffentlichkeit Meloxicam Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
EMA/CVMP/259397/2006 EMEA/V/C/000033 Zusammenfassung des EPAR für die Öffentlichkeit Meloxicam Dies ist eine Zusammenfassung des Europäischen Öffentlichen Beurteilungsberichts (EPAR) für. Hierin wird erläutert,
LUCENTIS. bei Visusbeeinträchtigung infolge eines Makulaödems aufgrund eines retinalen Venenverschlusses (RVV)
 LUCENTIS bei Visusbeeinträchtigung infolge eines Makulaödems aufgrund eines retinalen Venenverschlusses (RVV) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Die vorliegende Broschüre
LUCENTIS bei Visusbeeinträchtigung infolge eines Makulaödems aufgrund eines retinalen Venenverschlusses (RVV) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Die vorliegende Broschüre
LUCENTIS bei Visusbeeinträchtigung infolge einer chorioidalen Neovaskularisation (CNV) aufgrund einer pathologischen Myopie (PM)
 LUCENTIS bei Visusbeeinträchtigung infolge einer chorioidalen Neovaskularisation (CNV) aufgrund einer pathologischen Myopie (PM) Ihr Leitfaden fu r die Behandlung mit LUCENTIS 3 Lud-13-107 PM RMP Patientenbroschuere_RZ_V4_131113.indd
LUCENTIS bei Visusbeeinträchtigung infolge einer chorioidalen Neovaskularisation (CNV) aufgrund einer pathologischen Myopie (PM) Ihr Leitfaden fu r die Behandlung mit LUCENTIS 3 Lud-13-107 PM RMP Patientenbroschuere_RZ_V4_131113.indd
BAnz AT 04.04.2014 B2. Beschluss
 Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Beschluss des Gemeinsamen Bundesausschusses über eine Änderung der Arzneimittel-Richtlinie (AM-RL): Anlage XII - Beschlüsse über die Nutzenbewertung von Arzneimitteln mit neuen Wirkstoffen nach 35a SGB
Anhang I. Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen
 Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Anhang I Wissenschaftliche Schlussfolgerungen und Gründe für die Änderung der Bedingungen der Genehmigung(en) für das Inverkehrbringen 1 Wissenschaftliche Schlussfolgerungen Unter Berücksichtigung des
Patientenaufklärung und Einverständniserklärung zur intravitrealen Injektion bei der feuchten altersbedingen Makuladegeneration (AMD)
 Patientendaten Arzt-/Klinikstempel Patientenaufklärung und Einverständniserklärung zur intravitrealen Injektion bei der feuchten altersbedingen Makuladegeneration (AMD) Die feuchte altersbedingte Makuladegeneration
Patientendaten Arzt-/Klinikstempel Patientenaufklärung und Einverständniserklärung zur intravitrealen Injektion bei der feuchten altersbedingen Makuladegeneration (AMD) Die feuchte altersbedingte Makuladegeneration
EINE INFORMATION FÜR PATIENTEN ÜBER DIE BEHANDLUNG MIT OZURDEX
 Die europäischen Gesundheitsbehörden haben für die Markteinführung des Arzneimittels OZURDEX Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information
Die europäischen Gesundheitsbehörden haben für die Markteinführung des Arzneimittels OZURDEX Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information
Aufklärungsbogen für Patienten zum Vertrag zur besonderen ambulanten augenchirurgischen
 Aufklärungsbogen für Patienten zum Vertrag zur besonderen ambulanten augenchirurgischen Versorgung Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist ein/e altersbedingte feuchte Makuladegeneration
Aufklärungsbogen für Patienten zum Vertrag zur besonderen ambulanten augenchirurgischen Versorgung Sehr geehrte Patientin, sehr geehrter Patient, bei Ihnen ist ein/e altersbedingte feuchte Makuladegeneration
NeuroBloc. Botulinumtoxin Typ B Injektionslösung 5000 E/ml. Wichtige Informationen zur Sicherheit für Ärzte
 NeuroBloc Botulinumtoxin Typ B Injektionslösung 5000 E/ml Wichtige Informationen zur Sicherheit für Ärzte Dieses Handbuch dient dazu, Ärzte, die für die Verschreibung und die Verabreichung von NeuroBloc
NeuroBloc Botulinumtoxin Typ B Injektionslösung 5000 E/ml Wichtige Informationen zur Sicherheit für Ärzte Dieses Handbuch dient dazu, Ärzte, die für die Verschreibung und die Verabreichung von NeuroBloc
Lucentis 10 mg/ml Injektionslösung
 Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel behandelt werden, denn
Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel behandelt werden, denn
LUCENTIS. bei Visusbeeinträchtigung infolge einer chorioidalen Neovaskularisation (CNV) aufgrund einer pathologischen Myopie (PM)
 LUCENTIS bei Visusbeeinträchtigung infolge einer chorioidalen Neovaskularisation (CNV) aufgrund einer pathologischen Myopie (PM) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Ihr
LUCENTIS bei Visusbeeinträchtigung infolge einer chorioidalen Neovaskularisation (CNV) aufgrund einer pathologischen Myopie (PM) Ihr Leitfaden für die Behandlung mit LUCENTIS Kapitel 1 Über LUCENTIS Ihr
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION
 ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
DIE MAKULASCHWELLUNG UND IHRE BEHANDLUNG
 DIE MAKULASCHWELLUNG UND IHRE BEHANDLUNG Lederhaut Regenbogenhaut (Iris) Netzhaut Hornhaut Aderhaut Linse Makula Sehnerv Glaskörperraum 5 4 3 2 1 Schematischer und tatsächlicher Schnitt durch eine gesunde
DIE MAKULASCHWELLUNG UND IHRE BEHANDLUNG Lederhaut Regenbogenhaut (Iris) Netzhaut Hornhaut Aderhaut Linse Makula Sehnerv Glaskörperraum 5 4 3 2 1 Schematischer und tatsächlicher Schnitt durch eine gesunde
Übersicht der Verträge zur der intravitrealen operativen Medikamentenapplikation (IVOM) Stand:
 Übersicht der Verträge zur der intravitrealen operativen Medikamentenapplikation (IVOM) Stand: 01.09.2017 Wichtiger Hinweis: Für Krankenkassen, die nicht in dieser Kurzübersicht aufgeführt sind und somit
Übersicht der Verträge zur der intravitrealen operativen Medikamentenapplikation (IVOM) Stand: 01.09.2017 Wichtiger Hinweis: Für Krankenkassen, die nicht in dieser Kurzübersicht aufgeführt sind und somit
PATIENTENINFORMATION
 Die belgischen Gesundheitsbehörden haben bestimmte Voraussetzungen für das Inverkehrbringen des Arzneimittels BOCOUTURE erlassen. Der in Belgien vorgeschriebene Plan zur Risikominimierung, zu dem diese
Die belgischen Gesundheitsbehörden haben bestimmte Voraussetzungen für das Inverkehrbringen des Arzneimittels BOCOUTURE erlassen. Der in Belgien vorgeschriebene Plan zur Risikominimierung, zu dem diese
AMD Die altersabhängige Makuladegeneration
 AMD Die altersabhängige Makuladegeneration 1 L.DE.SM.03.2014.2456 Eine Patientin berichtet 2 So sieht die Patientin Einschränkungen im zentralen Gesichtsfeld Peripheres (seitliches) Gesichtsfeld nicht
AMD Die altersabhängige Makuladegeneration 1 L.DE.SM.03.2014.2456 Eine Patientin berichtet 2 So sieht die Patientin Einschränkungen im zentralen Gesichtsfeld Peripheres (seitliches) Gesichtsfeld nicht
Gebrauchsinformation: Information für Patienten. Lucentis 10 mg/ml Injektionslösung Ranibizumab
 Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel behandelt werden, denn
Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel behandelt werden, denn
W. Spitzner Arzneimittelfabrik GmbH
 Seite: 1 von 5 3. Packungsbeilage Gebrauchsinformation Lesen Sie die gesamte Packungsbeilage/Gebrauchsinformation sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel
Seite: 1 von 5 3. Packungsbeilage Gebrauchsinformation Lesen Sie die gesamte Packungsbeilage/Gebrauchsinformation sorgfältig durch, denn sie enthält wichtige Informationen für Sie. Dieses Arzneimittel
Priv.-Doz. Dr. med. Monika Fleckenstein Universitäts-Augenklinik Bonn. Ophthalmologische Fortbildung für medizinische Fachangestellte 25.
 Neuigkeiten aus der IVOM-Sprechstunde Priv.-Doz. Dr. med. Monika Fleckenstein Universitäts-Augenklinik Bonn Ophthalmologische Fortbildung für medizinische Fachangestellte 25. März 2015 Altersabhängige
Neuigkeiten aus der IVOM-Sprechstunde Priv.-Doz. Dr. med. Monika Fleckenstein Universitäts-Augenklinik Bonn Ophthalmologische Fortbildung für medizinische Fachangestellte 25. März 2015 Altersabhängige
COVERSUM Arginin 2,5 mg Filmtabletten
 Gebrauchsinformation: Information für Patienten COVERSUM Arginin 2,5 mg Filmtabletten Perindopril-Arginin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten COVERSUM Arginin 2,5 mg Filmtabletten Perindopril-Arginin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
VEGF Trap-Eye verbessert Sehkraft bei altersbedingter Makula-Degeneration. Nachhaltige Sehkraftverbesserung über 52 Wochen in Phase-II-Studie
 Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de VEGF Trap-Eye verbessert Sehkraft bei altersbedingter Makula-Degeneration Nachhaltige Sehkraftverbesserung über
Investor News Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de VEGF Trap-Eye verbessert Sehkraft bei altersbedingter Makula-Degeneration Nachhaltige Sehkraftverbesserung über
EMA bestätigt Empfehlungen zur Minimierung des Risikos für die Hirninfektion PML im Zusammenhang mit Tysabri
 25/04/2016 EMA/266665/2016 EMA bestätigt Empfehlungen zur Minimierung des Risikos für die Hirninfektion PML im Bei Patienten mit hohem Risiko sollten häufigere MRT-Untersuchungen in Erwägung gezogen werden
25/04/2016 EMA/266665/2016 EMA bestätigt Empfehlungen zur Minimierung des Risikos für die Hirninfektion PML im Bei Patienten mit hohem Risiko sollten häufigere MRT-Untersuchungen in Erwägung gezogen werden
zugelassen Erfahrungen und neue Perspektiven mit Aflibercept: EYLEA jetzt auch bei Makulaödem infolge von ZVV
 Erfahrungen und neue Perspektiven mit Aflibercept: EYLEA jetzt auch bei Makulaödem infolge von ZVV Erfahrungen und neue Perspektiven mit Aflibercept EYLEA jetzt auch bei Makulaödem infolge von ZVV zugelassen
Erfahrungen und neue Perspektiven mit Aflibercept: EYLEA jetzt auch bei Makulaödem infolge von ZVV Erfahrungen und neue Perspektiven mit Aflibercept EYLEA jetzt auch bei Makulaödem infolge von ZVV zugelassen
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Lektinol-Ampullen. Wirkstoff: Mistelkraut-Flüssigextrakt
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Lektinol-Ampullen Wirkstoff: Mistelkraut-Flüssigextrakt Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Lektinol-Ampullen Wirkstoff: Mistelkraut-Flüssigextrakt Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
PATIENTENRATGEBER DAS DIABETISCHE MAKULAÖDEM (DMÖ)
 PATIENTENRATGEBER DAS DIABETISCHE MAKULAÖDEM (DMÖ) URSACHEN THERAPIE PRÄVENTION INHALTSVERZEICHNIS DAS DIABETISCHE MAKULAÖDEM 3 8 16 Das diabetische Makulaödem Behandlungsmöglichkeiten für das diabetische
PATIENTENRATGEBER DAS DIABETISCHE MAKULAÖDEM (DMÖ) URSACHEN THERAPIE PRÄVENTION INHALTSVERZEICHNIS DAS DIABETISCHE MAKULAÖDEM 3 8 16 Das diabetische Makulaödem Behandlungsmöglichkeiten für das diabetische
Informationen für Betroffene, Angehörige und Interessierte
 Informationen für Betroffene, Angehörige und Interessierte Giorgio Clementi Fotolia.com Eine Initiative der Österreichischen Diabetikervereinigung und der Hilfsgemeinschaft der Blinden und Sehschwachen
Informationen für Betroffene, Angehörige und Interessierte Giorgio Clementi Fotolia.com Eine Initiative der Österreichischen Diabetikervereinigung und der Hilfsgemeinschaft der Blinden und Sehschwachen
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten Toppoll 10 mg - Tabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten Toppoll 10 mg - Tabletten Wirkstoff: Loratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
RoACTEMRA (Tocilizumab) Patientenpass
 RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für Anwender Hylan 0,015%, Augentropfen Wirkstoff: Natriumhyaluronat (biotechnologisch hergestellt mit Hilfe
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für Anwender Hylan 0,015%, Augentropfen Wirkstoff: Natriumhyaluronat (biotechnologisch hergestellt mit Hilfe
Einschränkungen für die Anwendung von Domperidon enthaltenden Arzneimitteln
 1. September 2014 EMA/465179/2014 Einschränkungen für die Anwendung von Domperidon enthaltenden Arzneimitteln Am 23. April 2014 befürwortete die Koordinierungsgruppe für das Verfahren der gegenseitigen
1. September 2014 EMA/465179/2014 Einschränkungen für die Anwendung von Domperidon enthaltenden Arzneimitteln Am 23. April 2014 befürwortete die Koordinierungsgruppe für das Verfahren der gegenseitigen
Wichtige sicherheitsrelevante Informationen für Ärzte zur Handhabung von intravitrealen Injektionen bei einer LUCENTIS (Ranibizumab)-Behandlung
 Wichtige sicherheitsrelevante Informationen für Ärzte zur Handhabung von intravitrealen Injektionen bei einer LUCENTIS (Ranibizumab)-Behandlung Version 5.1 Ranibizumab Ärztebroschüre Genehmigung 06/2017,
Wichtige sicherheitsrelevante Informationen für Ärzte zur Handhabung von intravitrealen Injektionen bei einer LUCENTIS (Ranibizumab)-Behandlung Version 5.1 Ranibizumab Ärztebroschüre Genehmigung 06/2017,
Positive Ergebnisse von zwei Phase-III-Studien mit VEGF Trap-Eye bei feuchter altersbedingter Makula-Degeneration
 Positive Ergebnisse von zwei Phase-III-Studien mit VEGF Trap-Eye bei feuchter altersbedingter Makula-Degeneration - Präparat erreicht in allen Studienarmen inklusive der Dosierung von 2 mg alle zwei Monate
Positive Ergebnisse von zwei Phase-III-Studien mit VEGF Trap-Eye bei feuchter altersbedingter Makula-Degeneration - Präparat erreicht in allen Studienarmen inklusive der Dosierung von 2 mg alle zwei Monate
Empfehlungen des PRAC zu Signalen für die Aktualisierung der Produktinformation
 22. Januar 2015 EMA/PRAC/63324/2015 Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) Empfehlungen des PRAC zu Signalen für die Aktualisierung der Produktinformation Verabschiedet im
22. Januar 2015 EMA/PRAC/63324/2015 Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) Empfehlungen des PRAC zu Signalen für die Aktualisierung der Produktinformation Verabschiedet im
Früherkennung mit dem OCT schützen Sie Ihr Augenlicht Netzhauterkrankungen & Grüner Star. Patienteninformation
 Früherkennung mit dem OCT schützen Sie Ihr Augenlicht Netzhauterkrankungen & Grüner Star Patienteninformation Die Augen sind die wichtigsten Sinnesorgane. Mit ihrer Hilfe orientieren wir uns und nehmen
Früherkennung mit dem OCT schützen Sie Ihr Augenlicht Netzhauterkrankungen & Grüner Star Patienteninformation Die Augen sind die wichtigsten Sinnesorgane. Mit ihrer Hilfe orientieren wir uns und nehmen
2. WAS MÜSSEN SIE VOR DER ANWENDUNG VON LIVOCAB DIREKT AUGENTROPFEN BEACHTEN?
 Gebrauchsinformation: Information für den Anwender Livocab direkt Augentropfen 0,05 % Augentropfen, Suspension Zur Anwendung bei Kindern ab 1 Jahr, Jugendlichen und Erwachsenen Wirkstoff: Levocabastin
Gebrauchsinformation: Information für den Anwender Livocab direkt Augentropfen 0,05 % Augentropfen, Suspension Zur Anwendung bei Kindern ab 1 Jahr, Jugendlichen und Erwachsenen Wirkstoff: Levocabastin
Ozurdex R -Therapie bei besonderen Indikationen
 Ozurdex R -Therapie bei besonderen Indikationen J. Nasemann Makulaödem Definition: Extravaskuläre Schwellung, ausgelöst durch eine abnormale Permeabilität retinaler Kapillaren. Ursache: Durch unterschiedliche
Ozurdex R -Therapie bei besonderen Indikationen J. Nasemann Makulaödem Definition: Extravaskuläre Schwellung, ausgelöst durch eine abnormale Permeabilität retinaler Kapillaren. Ursache: Durch unterschiedliche
Patientenratgeber Das diabetische Makulaödem (DMÖ)
 Patientenratgeber Das diabetische Makulaödem (DMÖ) Ursachen Therapie Prävention Inhaltsverzeichnis 3 Das diabetische Makulaödem 8 Behandlungsmöglichkeiten für das diabetische Makulaödem 16 Häufig gestellte
Patientenratgeber Das diabetische Makulaödem (DMÖ) Ursachen Therapie Prävention Inhaltsverzeichnis 3 Das diabetische Makulaödem 8 Behandlungsmöglichkeiten für das diabetische Makulaödem 16 Häufig gestellte
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Eylea 40 mg/ml Injektionslösung in einer Fertigspritze 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Injektionslösung
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Eylea 40 mg/ml Injektionslösung in einer Fertigspritze 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Injektionslösung
Gebrauchsinformation: Information für Patienten. Essentiale forte-kapseln Wirkstoff: Phospholipide aus Sojabohnen
 Gebrauchsinformation: Information für Patienten Essentiale forte-kapseln Wirkstoff: Phospholipide aus Sojabohnen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Essentiale forte-kapseln Wirkstoff: Phospholipide aus Sojabohnen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
LERNEN SIE: Die Wissenschaft von AMD
 FEUCHTE AMD LERNEN SIE: Die Wissenschaft von AMD WAS IST AMD? Altersbedingte Makuladegeneration (AMD) ist eine Erkrankung welche mit zunehmendem Alter wahrscheinlicher wird. Sie zerstört nach und nach
FEUCHTE AMD LERNEN SIE: Die Wissenschaft von AMD WAS IST AMD? Altersbedingte Makuladegeneration (AMD) ist eine Erkrankung welche mit zunehmendem Alter wahrscheinlicher wird. Sie zerstört nach und nach
Gebrauchsinformation: Information für Patienten. Trobicin 2 g Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Spectinomycin
 Gebrauchsinformation: Information für Patienten Trobicin 2 g Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Spectinomycin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Patienten Trobicin 2 g Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Spectinomycin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
IVOM welches Medikament bei welcher Erkrankung
 IVOM welches Medikament bei welcher Erkrankung GIO IVOM - KURS 2016 Neumünster Arnd Bunse F.E.B.O. Augenärzte BEP Schwerpunktpraxis für Netzhaut- und Makulaerkrankungen 21029 Hamburg www.augenaerzte-bep-bergedorf.de
IVOM welches Medikament bei welcher Erkrankung GIO IVOM - KURS 2016 Neumünster Arnd Bunse F.E.B.O. Augenärzte BEP Schwerpunktpraxis für Netzhaut- und Makulaerkrankungen 21029 Hamburg www.augenaerzte-bep-bergedorf.de
Die Europäische Arzneimittel-Agentur empfiehlt Änderungen für die Anwendung von Metoclopramid
 20. Dezember 2013 EMA/13239/2014 Corr. 1 Die Europäische Arzneimittel-Agentur empfiehlt Änderungen für die Anwendung von Die Änderungen sollen vor allem das Risiko neurologischer Nebenwirkungen senken
20. Dezember 2013 EMA/13239/2014 Corr. 1 Die Europäische Arzneimittel-Agentur empfiehlt Änderungen für die Anwendung von Die Änderungen sollen vor allem das Risiko neurologischer Nebenwirkungen senken
Gebrauchsinformation: Information für Patienten. Lucentis 10 mg/ml Injektionslösung in einer Fertigspritze Ranibizumab
 Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung in einer Fertigspritze Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel
Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung in einer Fertigspritze Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel
Bayer und Regeneron erweitern augenheilkundliches Forschungsund Entwicklungsprogramm für VEGF Trap-Eye in Asien
 Investor News Nicht für US-Medien bestimmt Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Bayer und Regeneron erweitern augenheilkundliches Forschungsund Entwicklungsprogramm
Investor News Nicht für US-Medien bestimmt Bayer AG Investor Relations 51368 Leverkusen Deutschland www.investor.bayer.de Bayer und Regeneron erweitern augenheilkundliches Forschungsund Entwicklungsprogramm
20. September 2013 EMA/564255/ Westferry Circus Canary Wharf London E14 4HB United Kingdom
 20. September 2013 EMA/564255/2013 Die Genehmigung für das Inverkehrbringen für Numeta G13% E wird ausgesetzt und für Numeta G16% E werden neue Maßnahmen zur Risikominimierung eingeführt Die Koordinierungsgruppe
20. September 2013 EMA/564255/2013 Die Genehmigung für das Inverkehrbringen für Numeta G13% E wird ausgesetzt und für Numeta G16% E werden neue Maßnahmen zur Risikominimierung eingeführt Die Koordinierungsgruppe
Gebrauchsinformation: Information für Patienten. Lucentis 10 mg/ml Injektionslösung in einer Fertigspritze Ranibizumab
 Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung in einer Fertigspritze Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel
Gebrauchsinformation: Information für Patienten Lucentis 10 mg/ml Injektionslösung in einer Fertigspritze Ranibizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit dem Arzneimittel
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. EXACYL 500 mg/5 ml Injektionslösung
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN EXACYL 500 mg/5 ml Injektionslösung Tranexamsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN EXACYL 500 mg/5 ml Injektionslösung Tranexamsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
