Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution
|
|
|
- Paul Bachmeier
- vor 5 Jahren
- Abrufe
Transkript
1 14.01 Einfluß von Substituenten am Benzol auf Geschwindigkeit und Richtung der elektrophilen Substitution Substitutenten Geschwindigkeit (Reaktivität) Richtung (Regioselektivität) Interpretation 1. 2,, 3, beschleunigen ortho und para + M ( I) 3 + I 2. F, l, Br, I verzögern ortho und para + M / I 3., R, 2,, 2, verzögern stark meta M / I Stand SS 2010 Seite 131
2 14.02 Aromatische Sulfonsäuren und Derivate Benzolsulfonsäure (Benzensulfonsäure) 2 4-Aminobenzolsulfonsäure (Sulfanilsäure) 2 2 S 2 2 im rganismus 2 S 2 2 Sulfamidochrysoidin Prontosil (1. Sulfonamid) (Domagk, Medizin-obelpreis 1939) 4-Aminobenzolsulfonsäureamid (Sulfanilamid) (eigentlicher Wirkstoff) 2 S 2 2 4,4' -Diaminodiphenylsulfon (Dapson) gegen Dermatosen und Lepra Stand SS 2010 Seite 132
3 14.03 Vernetztes Polystyrol aus Styrol und 1,4-Divinylbenzol (5:1) Stand SS 2010 Seite 133
4 14.04 Kationenaustauscher auf Polystyrolbasis S Stand SS 2010 Seite 134
5 14.05 Phenole Phenol 1,2-Dihydroxybenzol (Brenzkatechin) 1,3-Dihydroxybenzol (Resorcin) 1,4-Dihydroxybenzol (ydrochinon) 1,2,3-Trihydroxybenzol (Pyrogallol) 1,3,5-Trihydroxybenzol (Phloroglucin) 1,2,4-Trihydroxybenzol (2-ydroxyhydrochinon) 1-aphthol 2-aphthol Stand SS 2010 Seite 135
6 14.06 Struktur von Phenol-Formaldehyd-Duroplasten Phenole mit weiteren funktionellen Gruppen 2 Salicylsäure (aus Weiden) 3 2 Acetylsalicylsäure (Aspirin) Analgetikum Antipyretikum 3 Paracetamol Analgetikum Antipyretikum 2 2 p-aminosalicylsäure (PAS) Tuberkulostatikum Stand SS 2010 Seite 136
7 14.08 hinone 1,2-Benzochinon (E 0 = V) 1,4-Benzochinon (E 0 = V) 1,2-aphthochinon (E 0 = V) 1,4-aphthochinon (E 0 = V) 9,10-Anthrachinon (E 0 = V) 1:1 Komplex aus hinon und ydrochinon = hinhydron Stand SS 2010 Seite 137
8 14.09 atürlich vorkommende hinone Ubichinone 3 3 (Atmungskette) 3 n n = 6 12 Vitamin K 3 (Blutgerinnung) n n = 6 9 Anthrachinon-Farbstoffe Alizarin (Wurzel der Färberröte, Krappwurzel) Komplex = Farblack mit Al 3+ karminrot Sn 2+ scharlachrot r 3+ braun Fe 3+ violett Indanthrenblau RS Stand SS 2010 Seite 138
9 14.10 Aromatische Polynitroverbindungen sind Explosivstoffe ,4,6-Trinitrophenol (Pikrinsäure) 2,4,6-Trinitrotoluol (TT),2,4,6-Tetranitro--methylanilin (Tetryl) exanitrodiphenylamin (exyl) Aromatische Amine Anilin -Methylanilin,-Dimethylanilin Siedepunkt [ ] Siedepunkt [ ] Schmp. [ ] Diphenylamin Triphenylamin Stand SS 2010 Seite 139
10 14.12 Azo-Farbstoffe 3 3 Methylorange 0/ a 0/ a 2 0/ a Kongorot 2 substantives Blau (für Baumwolle) 0/ a 0/ a 3 0/ a 3 S 2 0/ a 2 substantives Schwarz (für Baumwolle) Stand SS 2010 Seite 140
11 14.13 absorbiertes Licht sichtbare Farbe Wellenlänge [nm] Farbe < 400 (ultraviolett) (unsichtbar) violett gelbgrün blau gelb grünblau orange blaugrün rot grün purpur gelbgrün violett gelb blau orange grünblau rot blaugrün purpur grün > 800 (ultrarot, infrarot) (unsichtbar) Stand SS 2010 Seite 141
12 14.14 Küpen-Farbstoff Indigo Indigo (blau, unlöslich in Wasser) 0 Reduktion Diffusion und Adsorption Baumwollfaser (ellulose) 0 Leukoindigo (Indigweiß) (farblos, löslich in Wasser) Reduzierter Farbstoff (Leukoform) xidation durch Luft 2 Indigo Reoxidierter Farbstoff Vorstufe in der Indigopflanze: Indican (Färberwaid, Indigopflanze) Stand SS 2010 Seite 142
13 14.15 Kationische Triphenylmethan-Farbstoffe / konz. 2 S 4 2 / Triphenylmethanol (farblos) Triphenylmethylcarbenium-Ion (blaßgelb, λ max : 405, 428 nm) / 3 / 3 / (4-Dimethylaminophenyl)diphenylmethylcarbenium-Ion (orangegelb, λ max : 455 nm) / 3 3 / Malachitgrün-Kation Kristallviolett-Kation (λ max : 617, 425 nm) (λ max : 589 nm) 1 Stand SS 2010 Seite 143
14 14.16 Energieschema der Lichtabsorption, Fluoreszenz und Phophoreszenz (mit Schwingungs-Energieniveaus) angeregter Singulettzustand (S 1 ) (LUM) photochemische Reaktion mit anderen Molekülen S 13 S 12 S 11 S 10 Spinumkehr Triplettzustand ΔE Absorption strahlungslose Desaktivierung ( Wärme) ΔE Fluoreszenz ΔE Phosphoreszenz hv S 03 S 02 S 01 c S ΔE = h v = h 00 λ Grundzustand (S 0 ) (M) h = Plank'sches Wirkungsquantum v = Frequenz [z] λ = Wellenlänge c = Lichtgeschwindigkeit Stand SS 2010 Seite 144
15 Absorptions- und Fluoreszenzspektrum eines Fluoreszenzfarbstoffes (ptischer Aufheller) Absorption Emission Extinktion nahes UV sichtbares Licht [nm] Stand SS 2010 Seite 145
Übersicht 3 Aspekte: - Struktur - Farbe (λ, ε) - Wechselwirkung Farbstoff-Faser
 294 XVI Farbstoffe, Photochemie Übersicht 3 Aspekte: - Struktur - Farbe (λ, ε) - Wechselwirkung Farbstoff-Faser 1 Lichtabsorption, Fluoreszens Spektralbereiche und Komplementärfarben high high Frequency
294 XVI Farbstoffe, Photochemie Übersicht 3 Aspekte: - Struktur - Farbe (λ, ε) - Wechselwirkung Farbstoff-Faser 1 Lichtabsorption, Fluoreszens Spektralbereiche und Komplementärfarben high high Frequency
Spektroskopie-Seminar SS UV-Vis-Spektroskopie. UV-Vis-Spektroskopie
 UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
UV-Vis-Spektroskopie 7.1 Allgemeines UV-Vis-Spektroskopie verwendet elektromagnetische Strahlung im sichtbaren und UV-Bereich. 190 nm bis 700 nm. Dabei kommt es zur Anregung von Elektronen ( Elektronenspektroskopie
Umwandlung in substituierte Amide
 Umwandlung in substituierte Amide CI_folie356 R C 3 R C Cl - Cl 2 Carbonsäurechlorid Amid S Cl 3 Sulfonsäurechlorid - Cl S 2 Sulfonamid S Cl Benzolsulfonylchlorid 3 C S Cl Ts Cl p-toluolsulfonylchlorid
Umwandlung in substituierte Amide CI_folie356 R C 3 R C Cl - Cl 2 Carbonsäurechlorid Amid S Cl 3 Sulfonsäurechlorid - Cl S 2 Sulfonamid S Cl Benzolsulfonylchlorid 3 C S Cl Ts Cl p-toluolsulfonylchlorid
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden!
 Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Übung r. 8 Mi. 25.04.2012 bzw. Fr. 7.05.2 1. Umwandlung funktioneller Gruppen Geben Sie Reagenzien an, mit denen Sie die folgenden Umwandlungen durchführen würden! 2 CH 3 H a) b) I H c) d) C F e) f) H
Organische Farbstoffe und Pigmente
 rganische Farbstoffe und Pigmente Farbstoffe Pigmente Farbstoffe: sind löslich; Färben von Textilien Pigmente: sind unlöslich; Lacke, Farben, Anstriche Papiere Theorie der Farben absorbiertes Licht reflektiertes
rganische Farbstoffe und Pigmente Farbstoffe Pigmente Farbstoffe: sind löslich; Färben von Textilien Pigmente: sind unlöslich; Lacke, Farben, Anstriche Papiere Theorie der Farben absorbiertes Licht reflektiertes
Phenole (Nomenklatur)
 Phenole (omenklatur) I_folie377 Phenol: Schmp. 41 ; Sdp. 182 ; Lösl.: 9.3 g in 100 ml 2 Br 3 2 2 2 2 2 m-bromphenol p-kresol 2,4-Dinitrophenol Pikrinsäure (p-methylphenol) (2,4,6-Trinitrophenol) Salicylsäure
Phenole (omenklatur) I_folie377 Phenol: Schmp. 41 ; Sdp. 182 ; Lösl.: 9.3 g in 100 ml 2 Br 3 2 2 2 2 2 m-bromphenol p-kresol 2,4-Dinitrophenol Pikrinsäure (p-methylphenol) (2,4,6-Trinitrophenol) Salicylsäure
IUPAC muss das denn sein?
 IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
IUPAC muss das denn sein? Die Begriffe Methan, Aceton, Formaldehyd, Ameisensäure oder Zitronensäure haben alle schon einmal gehört. Diese Namen verraten nichts über den Aufbau der benannten Moleküle und
3-01. Triphenylmethan
 Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Stephen. Grundvoraussetzung: Die Moleküle müssen das Licht absorbieren! E = λ = Wellenlänge. Hashmi. ν = Frequenz
 Prof Dr ashmi, Sommersemester 2002 1 rganische Chemie für Technische Biologen, Teil 24 otochemie, Farbstoffe Bedeutung in der atur: - otosynthese - Sehvorgang - Zellschädigung durch energiereiches Licht
Prof Dr ashmi, Sommersemester 2002 1 rganische Chemie für Technische Biologen, Teil 24 otochemie, Farbstoffe Bedeutung in der atur: - otosynthese - Sehvorgang - Zellschädigung durch energiereiches Licht
Farbigkeit bei Molekülen Fluoreszenz Phosphoreszenz
 Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Farbigkeit bei Molekülen Im Unterschied zu einzelnen Atomen zeigen die Absorptionsspektren von Molekülen keine scharfen Linen, sondern breitere Absorptionsbanden. Die Moleküle absorbieren also nicht nur
Ableitung wieder aus einer einfachen anorganischen Verbindung, NH 3 :
 168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
168 X. Amine 1. Übersicht Ableitung wieder aus einer einfachen anorganischen Verbindung, 3 : primär sekündär tertiär Achtung: Ausdrücke primär, sekundär und tertiär beziehen sich auf, nicht auf wie bei
Wechselwirkung zwischen Licht und chemischen Verbindungen
 Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Photometer Zielbegriffe Photometrie. Gesetz v. Lambert-Beer, Metallkomplexe, Elektronenanregung, Flammenfärbung, Farbe Erläuterungen Die beiden Versuche des 4. Praktikumstages sollen Sie mit der Photometrie
Abiturprüfung Physik, Grundkurs
 Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
Seite 1 von 5 Abiturprüfung 2012 Physik, Grundkurs Aufgabenstellung: Aufgabe: Farbstoffmoleküle In der Spektroskopie unterscheidet man zwei grundsätzliche Typen von Spektren: Emissionsspektren, wie sie
3. Klausur zum Praktikum Organische Chemie I für Studierende der Chemie und der Biochemie im SS 2000
 Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Prof. Dr. B. König Prof. Dr. Th. Troll 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2000 am Donnerstag, dem 27. Juli 2000 ame: Mustermann...Vorname: Max...
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2018
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2018 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser und Dr. Martin Sumser September
P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger
 P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger Warum Spektroskopie auf dem Mars? Befindet sich Wasser auf dem Mars? Gibt es eine Atmosphäre? Aus welchen Elemente besteht sie? Gibt es Leben?
P H Y S I K - Spektroskopie - Helene Plank Stephan Giglberger Warum Spektroskopie auf dem Mars? Befindet sich Wasser auf dem Mars? Gibt es eine Atmosphäre? Aus welchen Elemente besteht sie? Gibt es Leben?
Seminar zum Organisch-Chemischen Praktikum für Biologen Sommersemester 2016
 Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Seminar zum rganisch-chemischen Praktikum für Biologen Sommersemester 2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Prof. Dr. asmus Linser September 2016 Gruppe A
Herstellung des Benzoldiazoniumchlorids aus Anilin, Natriumnitrit und Salzsäure. Benzoldiazonium-Ion
 Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
Vorlesung 34 Arendiazoniumsalze (Vollhardt, 3. Aufl., S. 1113-1117, 4. Aufl. 1191-1195; art, S. 412-418; Buddrus, S. 621-627) werden in gleicher Weise hergestellt wie die aliphatischen Diazonium-Salze.
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Chemie Stufe 13 / Aromaten / Phenol Folie 01. Das Phenol-Molekül. δ δ+ sp 3. sp 2
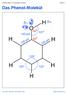 Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Chemie Stufe 13 / Aromaten / Phenol Folie 01 Das Phenol-Molekül δ δ+ sp 3 sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 02 Das Phenolat-Ion sp 3 H + sp 2 Chemie Stufe 13 / Aromaten / Phenol Folie 03 Grenzstrukturen
Br 1. Auch bei der folgenden Kombination, sind die Strukturen nicht identisch, sie lassen sich durch Drehung nicht ineinander überführen.
 Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Drill&Practice: Aufgaben und Lösungen, A. Dinter, KME Drill&Practice: Arene. Sind folgende Strukturpaare zueinander identisch? Die Frage ist möglicherweise nicht so simpel, wie sie sich anhört. Gemeint
Infrarot-Spektroskopie
 SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
SoSe 19 Infrarot-Spektroskopie E = h v = h c ሚθ E = Energie; h = Planck sches Wirkungsquantum; v = Frequenz; c = Lichtgeschwindigkeit, ሚθ = Wellenzahl 1 3.1 Schwingungsmodi T / % Moleküle werden mit Licht
Spektroskopische Methoden
 Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
Spektroskopische Methoden OCIfolie367 MS - Massenspektroskopie (Bestimmung von Molekulargewichten, charakteristischen Fragmentierungen von Molekülen) Absorptionsspektroskopische Methoden (Absorption =
» Konzepte, Fakten, Gliederung
 Kapitel 4: Funktionelle π-systeme Farbenchemie rganische Farbstoffe» Konzepte, Fakten, Gliederung Das elektromagnetische Spektrum Wechselwirkung zwischen Materie und elektromagnetischer Strahlung. Das
Kapitel 4: Funktionelle π-systeme Farbenchemie rganische Farbstoffe» Konzepte, Fakten, Gliederung Das elektromagnetische Spektrum Wechselwirkung zwischen Materie und elektromagnetischer Strahlung. Das
11 Organische Farbstoffe
 Lösungen zu den Durchblick-Seiten 11.11 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative
Lösungen zu den Durchblick-Seiten 11.11 Durchblick Zusammenfassung und Übung Zu den Aufgaben A1 Das Phenolmolekül ist reaktiver als das unsubstituierte Benzolmolekül, da in ihm durch Mesomerie negative
Spektroskopie-Seminar SS Infrarot-Spektroskopie. Infrarot-Spektroskopie
 Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
Infrarot-Spektroskopie 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden die absorbierten
2 Einführung in Licht und Farbe
 2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
2.1 Lernziele 1. Sie wissen, dass Farbe im Gehirn erzeugt wird. 2. Sie sind mit den drei Prinzipien vertraut, die einen Gegenstand farbig machen können. 3. Sie kennen den Zusammenhang zwischen Farbe und
Farbstoffe Zusammenfassung Klausur K2
 Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
Farbstoffe Zusammenfassung Klausur K2 aphael Michel 10. März 2013 Inhaltsverzeichnis 1 Allgemeines 1 1.1 Mesomeriemodell und Absorption.............................. 1 2 Farbstoffklassen 2 2.1 Indigo.............................................
2 Grundlagen der Photochemie
 folie191 2 Grundlagen der Photochemie 2.1 UV-Vis-Absorptionsspektren in organischen Verbindungen; Jablonski-Diagramm, Franck-Condon-Prinzip, Emissionsspektren (Fluoreszens, Phosphoreszens, Stokes-Verschiebung)
folie191 2 Grundlagen der Photochemie 2.1 UV-Vis-Absorptionsspektren in organischen Verbindungen; Jablonski-Diagramm, Franck-Condon-Prinzip, Emissionsspektren (Fluoreszens, Phosphoreszens, Stokes-Verschiebung)
Spektroskopie-Seminar WS 17/18 3 Infrarot-Spektroskopie. Infrarot-Spektroskopie
 WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
WS 17/18 Infrarot-Spektroskopie 1 3.1 Schwingungsmodi Moleküle werden mit Licht im Infrarot-Bereich (400-4000 cm -1 ) bestrahlt Durch Absorption werden Schwingungen im Molekül angeregt Im IR-Spektrum werden
SCHWEIZER JUGEND FORSCHT. Chemie und Materialwissenschaften
 SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
SCHWEIZER JUGEND FORSCHT Chemie und Materialwissenschaften Studie einer ultraschnellen Fotochemischen Reaktion mit Laserspektroskopie Gianluca Schmoll Widmer Betreuer: Dr. Sandra Mosquera Vazquez, Dr.
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Bilder Ton Zeit [s] Vorspann
![Bilder Ton Zeit [s] Vorspann Bilder Ton Zeit [s] Vorspann](/thumbs/62/47191146.jpg) Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Bilder Ton Zeit [s] Vorspann 4 Intro Man kennt es aus dem Alltag: 5 Gegenstände die unter Schwarzlicht leuchten. Aber welche Eigenschaften muss ein Stoff haben, um in Schwarzlicht leuchten zu können? 6
Quantitative Bestimmung von anorganischen Arznei-, Hilfs- und Schadstoffen
 Seminar zum Praktikum Quantitative Bestimmung von anorganischen Arznei-, Hilfs- und Schadstoffen im 2. Fachsemester Pharmazie. V. Photometrie Do, 24.4.2008 Komplexe/Koordinationsverbindungen: zentrales
Seminar zum Praktikum Quantitative Bestimmung von anorganischen Arznei-, Hilfs- und Schadstoffen im 2. Fachsemester Pharmazie. V. Photometrie Do, 24.4.2008 Komplexe/Koordinationsverbindungen: zentrales
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung)
 Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Aufstellung einiger Versuche zur Farbenchemie (Kurzfassung) Zusammenstellung der Versuche, die für Schulversuche als geeignet eingestuft wurden (zusammengestellt von Herrn Buchholz, TU Dresden) 1. Darstellung
Kinetik zusammengesetzter Reaktionen
 Kinetik zusammengesetzter Reaktionen Kap. 23 1 PC 2 SS 2016 Kinetik zusammengesetzter Reaktionen Kettenreaktionen Explosionen Polymerisationen Schrittweise Polymerisation Kettenpolymerisation Homogene
Kinetik zusammengesetzter Reaktionen Kap. 23 1 PC 2 SS 2016 Kinetik zusammengesetzter Reaktionen Kettenreaktionen Explosionen Polymerisationen Schrittweise Polymerisation Kettenpolymerisation Homogene
Seminar: Photometrie
 Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Seminar: Photometrie G. Reibnegger und W. Windischhofer (Teil II zum Thema Hauptgruppenelemente) Ziel des Seminars: Theoretische Basis der Photometrie Lambert-Beer sches Gesetz Rechenbeispiele Literatur:
Fragen aus dem ersten Abschnitt der pharmazeutischen Prüfung
 Agenda Molekül der Woche Fragen aus dem ersten Abschnitt der pharmazeutischen Prüfung Elektrophile und nucleophile Substitution am Aromaten Molekül der Woche Rolle von Kathepsin K bei der Knochenresorption
Agenda Molekül der Woche Fragen aus dem ersten Abschnitt der pharmazeutischen Prüfung Elektrophile und nucleophile Substitution am Aromaten Molekül der Woche Rolle von Kathepsin K bei der Knochenresorption
Elektronenspektroskopie
 Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Elektronenspektroskopie Die Elektronenspektroskopie befasst sich mit der Wechselwirkung elektromagnetischer Strahlung des Wellenlängenbereichs von etwa 100 bis 800 nm mit Materie. Es werden dabei Elektronen
Chemie für Biologen SS Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 11: Alkine / Polyene / Aromaten)
 hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
hemie für Biologen SS 2007 Georg Jansen AG Theoretische rganische hemie Universität Duisburg Essen (Teil 11: Alkine / Polyene / Aromaten) Bindungen mit sp ybridobitalen Bindungen mit sp ybridorbitalen
Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009
 Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 06.03.2009 Assistent: Esther Amstad E-Mail: zclaudio@student.ethz.ch
Versuch 5: Diazotierung und Azokupplung Chemieteil, Frühlingssemester 2009 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 06.03.2009 Assistent: Esther Amstad E-Mail: zclaudio@student.ethz.ch
Aromaten H H H C C C C C C C C H C H. Naphthalin: C 10 H 8. Benzol: C 6 H 6. Anthracen: C 14 H 10. Phenanthren: C 14 H 10.
 Aromaten Folie30 C C C C C C Benzol: C 6 6 C C C C C C C C C C aphthalin: C 10 8 7 6 8 8a 5 4a 1 4 3 7 6 8 8a 9 9a 5 10a 10 4a 1 4 3 Anthracen: C 14 10 1 10 9 3 8 4 5 7 6 Phenanthren: C 14 10 Benzpyren:
Aromaten Folie30 C C C C C C Benzol: C 6 6 C C C C C C C C C C aphthalin: C 10 8 7 6 8 8a 5 4a 1 4 3 7 6 8 8a 9 9a 5 10a 10 4a 1 4 3 Anthracen: C 14 10 1 10 9 3 8 4 5 7 6 Phenanthren: C 14 10 Benzpyren:
Organische Chemie für MST 5. Lienkamp/ Prucker/ Rühe
 Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Organische Chemie für MST 5 Lienkamp/ Prucker/ Rühe Inhalt 5 Aromaten Struktur und Bindung im Benzol, Hückel-Regel, mesomeregrenzstrukturen, ortho-, meta-, para-substitution, elektrophile Substitution
Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, Natriumsalz) - Azofarbstoff -
 Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Christina Sauermann 1 C- A- Praktikum Präparat 6: Darstellung von Methylorange (4 Dimethylaminoazobenzol-4 -sulfonsäure, atriumsalz) - Azofarbstoff - Die Darstellung von Methylorange erfolgt in zwei Teilschritten:
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Lösungen 3. Übungsblatt SS 2002
 Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
Lösungen 3. Übungsblatt SS 2002 1. Aufgabe: omenklatur und Stereochemie a) (E)-7-(S)-om-4-nonen-2-on b) H 3- Methoxy-4-methyl-benzaldehyd 2. Aufgabe: Alkene a) A B C D E Stabilitätsbeeinflussende Faktoren
9. GV: Atom- und Molekülspektren
 Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Physik Praktikum I: WS 2005/06 Protokoll zum Praktikum Dienstag, 25.10.05 9. GV: Atom- und Molekülspektren Protokollanten Jörg Mönnich Anton Friesen - Veranstalter Andreas Branding - 1 - Theorie Während
Gymnasium / Realschule. Atomphysik 2. Klasse / G8. Aufnahme und Abgabe von Energie (Licht)
 Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Aufnahme und Abgabe von Energie (Licht) 1. Was versteht man unter einem Elektronenvolt (ev)? 2. Welche physikalische Größe wird in Elektronenvolt gemessen? Definiere diese Größe und gib weitere Einheiten
Lehrbuchaufgaben Strahlung aus der Atomhülle
 LB S. 89, Aufgabe 1 Die Masse lässt sich mithilfe eines Massenspektrografen bestimmen. Der Radius von Atomen kann z.b. aus einmolekularen Schichten (Ölfleckversuch) oder aus Strukturmodellen (dichtgepackte
LB S. 89, Aufgabe 1 Die Masse lässt sich mithilfe eines Massenspektrografen bestimmen. Der Radius von Atomen kann z.b. aus einmolekularen Schichten (Ölfleckversuch) oder aus Strukturmodellen (dichtgepackte
Lernziele zu Farbigkeit von Stoffen
 Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Farbstoffe Lernziele zu Farbigkeit von Stoffen du verstehst, wie Farbigkeit mit der Absorption von EM-Strahlung zusammenhängt. du verstehst die Unterschiede zwischen Feuerwerksfarben und Textilfarbstoffen.
Vorlesung Chemie für Mediziner: Formeln OC
 Vorlesung hemie für Mediziner: Formeln In diesem Dokument sind die wichtigsten Formeln der Vorlesung zusammengestellt, die man für die Klausur kennen sollte. Die Zusammenstellung erhebt keinen Anspruch
Vorlesung hemie für Mediziner: Formeln In diesem Dokument sind die wichtigsten Formeln der Vorlesung zusammengestellt, die man für die Klausur kennen sollte. Die Zusammenstellung erhebt keinen Anspruch
Einführung Farbstoffe
 Einführung Farbstoffe Licht und Farbe Elektromagnetische Strahlung wird durch die Wellenlänge λ oder die Frequenz ν charakterisiert (Abb. 1). Ein Lichtquant der Frequenz ν bzw. der Wellenlänge λ hat die
Einführung Farbstoffe Licht und Farbe Elektromagnetische Strahlung wird durch die Wellenlänge λ oder die Frequenz ν charakterisiert (Abb. 1). Ein Lichtquant der Frequenz ν bzw. der Wellenlänge λ hat die
FLUORESZENZSPEKTROSKOPIE. Biophysik Vorlesung Gábor Talián
 FLUORESZENZSPEKTROSKOPIE Biophysik Vorlesung 05.02.2015. Gábor Talián ENTWURF Lumineszenz Fluoreszenzvorgang Fluorimeter Charakterisierung der Fluoreszenz Fluorophore, Biolumineszenz Lumineszenz Elektronenanregung
FLUORESZENZSPEKTROSKOPIE Biophysik Vorlesung 05.02.2015. Gábor Talián ENTWURF Lumineszenz Fluoreszenzvorgang Fluorimeter Charakterisierung der Fluoreszenz Fluorophore, Biolumineszenz Lumineszenz Elektronenanregung
Klausur: Chemie für Mediziner und Zahnmediziner SS
 Klausur: Chemie für Mediziner und Zahnmediziner SS 04 24.05.2005 Name:. Unterschrift:... Vorname:.. Matrikel-Nr.: Bitte ankreuzen: Medizien Zahnmedizin: Schreiben Sie bitte deutlich. Alle für die Korrektur
Klausur: Chemie für Mediziner und Zahnmediziner SS 04 24.05.2005 Name:. Unterschrift:... Vorname:.. Matrikel-Nr.: Bitte ankreuzen: Medizien Zahnmedizin: Schreiben Sie bitte deutlich. Alle für die Korrektur
Klausur zur Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Dr. Jens Christoffers 13. ktober 2005 Universität Stuttgart Klausur zur Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Vorname: ame: Matrikelnummer:
Prof. Dr. Jens Christoffers 13. ktober 2005 Universität Stuttgart Klausur zur Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler Vorname: ame: Matrikelnummer:
12 Organische Farbstoffe
 12 rganische Farbstoffe 12.1 Licht und Farbe vorläufige Fassung Zur Aufgabe A1 Das absorbierte Licht im Wellenlängenbereich 480 490 nm ist blau. Die Lösung hat folglich die Komplementärfarbe, d.h., sie
12 rganische Farbstoffe 12.1 Licht und Farbe vorläufige Fassung Zur Aufgabe A1 Das absorbierte Licht im Wellenlängenbereich 480 490 nm ist blau. Die Lösung hat folglich die Komplementärfarbe, d.h., sie
1.2 Vergleichen Sie die Reaktionsbedingungen für die Bromierung von A und B und begründen Sie unter Mitverwendung von Grenzformeln den Unterschied!
 Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Aufgabe II Die aromatischen Ringsysteme folgender Verbindungen sollen zu Monobromderivaten umgesetzt werden: Benzol (A), Anilin (B) und Aniliniumchlorid (C). 1.1 Erläutern Sie unter Mitverwendung von Strukturformeln
Theorie der Farbigkeit
 1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
1. Theorie der Farbigkeit 1.1 Theorie der Farbigkeit Chromophore Zentraler Bestandteil aller Farbstoffe sind die Chromophore. Als Chromophor (griech. Farbträger) bezeichnet man den Teil eines Farbstoffs,
M U S T E R L Ö S U N G
 Prof. Dr. B. König Prof. Dr.. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2001 am Donnerstag, dem 26. Juli 2001 M U S T E R L Ö S U G ame:...vorname:...
Prof. Dr. B. König Prof. Dr.. Geyer 3. Klausur zum Praktikum rganische hemie I für Studierende der hemie und der Biochemie im SS 2001 am Donnerstag, dem 26. Juli 2001 M U S T E R L Ö S U G ame:...vorname:...
Fluoreszenz. Abb. 1: Möglicher Versuchsaufbau
 Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Fluoreszenz Abb. 1: Möglicher Versuchsaufbau Geräteliste: UV-Lampe Geldscheintester, Schwarzlicht-Leuchtstofflampe, Halogenlampe, UV- Bandpass, Granulat mit fluoreszierendem Farbstoff, Fluoreszenzproben,
Prof. Christoffers, Vorlesung Organische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler
 Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Prof. Christoffers, Vorlesung rganische Chemie für Verfahrensingenieure, Umweltschutztechniker und Werkstoffwissenschaftler 6. Aromaten 6.1 Aromatizität Benzol ist eine Verbindung mit der Summenformel
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für öhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für öhlenmalereien. Diese Farben bestehen aus anorganischen
Grundkurs Farbstoffe 1983/II 1984/I 1984/IV 1985/IV
 Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Elektronenspektren Organischer Verbindungen (Vollhardt, 3. Aufl., S. 650-654, 4. Aufl. S. 725-729; Hart, S. 453-455; Buddrus, S. 41-45, S.
 Vorlesung 25 Elektronenspektren Organischer Verbindungen (Vollhardt, 3. Aufl., S. 650-654, 4. Aufl. S. 725-729; Hart, S. 453-455; Buddrus, S. 41-45, S. 310-312) Warum sind manche Substanzen farbig, andere
Vorlesung 25 Elektronenspektren Organischer Verbindungen (Vollhardt, 3. Aufl., S. 650-654, 4. Aufl. S. 725-729; Hart, S. 453-455; Buddrus, S. 41-45, S. 310-312) Warum sind manche Substanzen farbig, andere
Indanon ist das Produkt einer Friedel-Crafts-Acylierung Geben Sie die Reaktionsgleichung zu seiner Synthese an.
 Aromatenchemie für Fortgeschrittene 1.Wiederholung: Elektrophile aromatische Substitutionen 1.1. Geben Sie die Bruttogleichung für die zweistufige Synthese von Styren an. 1.2. Formulieren Sie die Reaktionsgleichung
Aromatenchemie für Fortgeschrittene 1.Wiederholung: Elektrophile aromatische Substitutionen 1.1. Geben Sie die Bruttogleichung für die zweistufige Synthese von Styren an. 1.2. Formulieren Sie die Reaktionsgleichung
Fluoreszenzlampenl. René Riedel. Bettina Haves
 Leuchtstoffe in Fluoreszenzlampenl René Riedel Bettina Haves Inhalt 1) Fluoreszenzlampen 2) Fluoreszenz 3) Geschichte der Leuchtstoffe 4) Leuchtstoffe in Fluoreszenzlampen 5) Weitere Anwendungsbereiche
Leuchtstoffe in Fluoreszenzlampenl René Riedel Bettina Haves Inhalt 1) Fluoreszenzlampen 2) Fluoreszenz 3) Geschichte der Leuchtstoffe 4) Leuchtstoffe in Fluoreszenzlampen 5) Weitere Anwendungsbereiche
Die Indigotinbottle. Zusammenfassung. Einordnung in den Unterricht 1
 V22 Die Indigotinbottle Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 20 Minuten Zusammenfassung Bei dem Versuch wird ein Redoxsystem erzeugt, dass seine Farbe ändert, je nachdem
V22 Die Indigotinbottle Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 20 Minuten Zusammenfassung Bei dem Versuch wird ein Redoxsystem erzeugt, dass seine Farbe ändert, je nachdem
Praktikum: Arzneimittelanalytik, Toxikologie, Drug monitoring und umweltrelevante Untersuchungen 8. Semester. Farbreaktionen
 1 FABEAKTIE Praktikum: Arzneimittelanalytik, Toxikologie, Drug monitoring und umweltrelevante Untersuchungen 8. Semester Farbreaktionen 2 1. elementaranalytische achweise 2. achweise funktioneller Gruppen
1 FABEAKTIE Praktikum: Arzneimittelanalytik, Toxikologie, Drug monitoring und umweltrelevante Untersuchungen 8. Semester Farbreaktionen 2 1. elementaranalytische achweise 2. achweise funktioneller Gruppen
Aufgaben ================================================================== 1. Ölfleckversuch
 Aufgaben ================================================================== 1. Ölfleckversuch Hans, Martin und Sandra führen gemeinsam den Öltröpfchenversuch durch, wobei ihnen aus Versehen anstelle eines
Aufgaben ================================================================== 1. Ölfleckversuch Hans, Martin und Sandra führen gemeinsam den Öltröpfchenversuch durch, wobei ihnen aus Versehen anstelle eines
Materialien- Handbuch Kursunterricht Chemie
 Materialien- Handbuch Kursunterricht Chemie Band 6 Farbstoffe - Waschmittel Herausgeber: Dr. Heinz Wambach unter Mitwirkung von Dr. Uwe HHgers Universitäts- und Landisbibliothek Darmstadt Bibliothek Biologie
Materialien- Handbuch Kursunterricht Chemie Band 6 Farbstoffe - Waschmittel Herausgeber: Dr. Heinz Wambach unter Mitwirkung von Dr. Uwe HHgers Universitäts- und Landisbibliothek Darmstadt Bibliothek Biologie
Spektroskopie im sichtbaren und UV-Bereich
 Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
Spektroskopie im sichtbaren und UV-Bereich Theoretische Grundlagen Manche Verbindungen (z.b. Chlorophyll oder Indigo) sind farbig. Dies bedeutet, dass ihre Moleküle sichtbares Licht absorbieren. Durch
6. LICHT UND MATERIE. Die Energie für ein Lichtquant berechnet sich zu ΔE = h ν = h c/λ (mit c = ν λ)
 6. LICHT UND MATERIE Elektromagnetische Strahlung weiteren Sinne: Licht kann mit Materie in Wechselwirkung treten. Dieses Prinzip nutzen wir im Alltag in vielfältiger Weise und oft nur unbewusst aus. Denken
6. LICHT UND MATERIE Elektromagnetische Strahlung weiteren Sinne: Licht kann mit Materie in Wechselwirkung treten. Dieses Prinzip nutzen wir im Alltag in vielfältiger Weise und oft nur unbewusst aus. Denken
Stark konz., Fluoreszierend
 hemie-protokoll 28.10.02, Seite 1 von 5 Lukman Iwan, 30.10.02 Stundenprotokoll vom Montag, 28. Oktober 2002 Es fehlen: keine VB: Lösungsmittel Extraktfarbe VD: Ethanol (Brennspiritus) Blaugrün, Stark konz.,
hemie-protokoll 28.10.02, Seite 1 von 5 Lukman Iwan, 30.10.02 Stundenprotokoll vom Montag, 28. Oktober 2002 Es fehlen: keine VB: Lösungsmittel Extraktfarbe VD: Ethanol (Brennspiritus) Blaugrün, Stark konz.,
10/6/2015. Licht IST FARBIG! DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE. Alle Objekte sind Reflektoren!
 DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE 1 WAS GENAU SIND OPTISCHE AUFHELLER? Optische Aufheller sind chemische Stoffe welche im elektromagnetischen Spektrum Licht
DAS UNSICHTBARE SICHTBAR MACHEN OPTISCHE AUFHELLER IN DER KUNSTSTOFF- INDUSTRIE 1 WAS GENAU SIND OPTISCHE AUFHELLER? Optische Aufheller sind chemische Stoffe welche im elektromagnetischen Spektrum Licht
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm.
 Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
Termschema des neutralen Natriumatoms. Die Zahlen bei den schrägen Strichen sind die Wellenlängen beobachteter Übergänge in nm. Prof. Dr. D. Winklmair Wechselwirkung 1/11 Symmetrische Valenzschwingung
 Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Farbstofflösung in einer Küvette absorbiert 90% des einfallenden Lichtes. Welche Extinktion hat diese Lösung? 0 0,9 1,9 keine der Aussagen ist richtig Eine Küvette mit einer wässrigen Farbstofflösung
Die Primärreaktion der Photosynthese
 Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
Die Primärreaktion der Photosynthese 1. Energetische Betrachtungen Wie ist es energetisch möglich, dass das so energiearme und stabile Wassermolekül in der Primärreaktion der Photosynthese zu Sauerstoff
Abschlussklausur zur Grundvorlesung Organische Chemie im SS 2007 Nachholtermin -
 Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Prof. Dr. H.-A. Wagenknecht Institut für rganische Chemie Universität Regensburg Abschlussklausur zur Grundvorlesung rganische Chemie im SS 2007 Nachholtermin - am Freitag, dem 12. ktober 2007... Vorname:...
Versuchsprotokoll A1 Photoeffekt. Johann Förster
 Versuchsprotokoll A1 Photoeffekt Johann Förster 519519 Versuchspartner Meikel Sobanski Messplatz 1 Humboldt Universität zu Berlin Institut für Physik 1 Inhaltsverzeichnis Seite 1) Physikalische Grundlagen
Versuchsprotokoll A1 Photoeffekt Johann Förster 519519 Versuchspartner Meikel Sobanski Messplatz 1 Humboldt Universität zu Berlin Institut für Physik 1 Inhaltsverzeichnis Seite 1) Physikalische Grundlagen
Die Natriumlinie. und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz
 Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Die Natriumlinie und Absorption, Emission, Dispersion, Spektren, Resonanz Fluoreszenz, Lumineszenz Absorption & Emissionsarten Absorption (Aufnahme von Energie) Atome absorbieren Energien, z.b. Wellenlängen,
Fluoreszenzspektroskopie
 A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
A 60 Fluoreszenzspektroskopie Aufgabe: Bestimmen Sie das Absorptions- und Fluoreszenzspektrum des Farbstoffs Rhodamin 6G in ethanolischer Lösung. Bestimmen Sie in beiden Spektren jeweils die Wellenlänge
Chemistry Department Cologne University. Photochemie 1 PC 2 SS Chemistry Department Cologne University. Photochemie
 Photochemie 1 PC 2 2016 Photochemie 2 PC 2 2016 1 Wichtige photophysikalische Prozesse 3 PC 2 2016 Der Grundzustand Boltzmann Verteilung: Alle Moleküle sind im elektronischen Grundzustand (0) chwingungsgrundzustand
Photochemie 1 PC 2 2016 Photochemie 2 PC 2 2016 1 Wichtige photophysikalische Prozesse 3 PC 2 2016 Der Grundzustand Boltzmann Verteilung: Alle Moleküle sind im elektronischen Grundzustand (0) chwingungsgrundzustand
Was sind die entscheidenden Prozesse?
 Was sind die entscheidenden Prozesse? Absorption angeregter Zustand Photochemie Thermalisierung Thermische Denaturierung Druck- und Zugwellen Phasenübergang biologische Reaktion Photoschäden Sonnenbrand
Was sind die entscheidenden Prozesse? Absorption angeregter Zustand Photochemie Thermalisierung Thermische Denaturierung Druck- und Zugwellen Phasenübergang biologische Reaktion Photoschäden Sonnenbrand
Was bedeutet Optik? Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel Definitionen erarbeiten Beispiele nennen Wellenspektrum beschriften Farben mit Wellenlängen versehen Wellenlängen verstehen und zuordnen Visualisieren Beispiele
Lehrerinformation 1/5 Arbeitsauftrag Ziel Definitionen erarbeiten Beispiele nennen Wellenspektrum beschriften Farben mit Wellenlängen versehen Wellenlängen verstehen und zuordnen Visualisieren Beispiele
Aromatische Kohlenwasserstoffe.
 Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Aromatische Kohlenwasserstoffe. Benzol und dessen Homologe. Mechanismus der S E 2-Ar-Reaktion. Orientierung in aromatischem Kern, abhängig vom ersten Substituent. Elektrophiler Mechanismus der Substitutionsreaktionen.
Färben von Stoffen in unserer Zeit! Eine Präsentation von: Carl B. Enno W. Malte M.
 Färben von Stoffen in unserer Zeit! Eine Präsentation von: Carl B. Enno W. Malte M. Gliederung 1.0 Einleitung 2.0 Farbstoffe - Eine Übersicht 2.1 Azofarbstoffe 2.1.1 Färben mit Azofarbstoffen 2.2 Indigo
Färben von Stoffen in unserer Zeit! Eine Präsentation von: Carl B. Enno W. Malte M. Gliederung 1.0 Einleitung 2.0 Farbstoffe - Eine Übersicht 2.1 Azofarbstoffe 2.1.1 Färben mit Azofarbstoffen 2.2 Indigo
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 GRUNDKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Sequenzierung inhaltlicher Aspekte Organische Reaktionsabläufe
CHEMIE QUALIFIKATIONSSPHASE 2 GRUNDKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Sequenzierung inhaltlicher Aspekte Organische Reaktionsabläufe
Anorganische Chemie für Biologen
 Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Arten chemischer Bindung Die entscheidende Größe für den
Anorganische Chemie für Biologen Nadja Giesbrecht AK Prof. Dr. Thomas Bein Raum: E3.005 Tel: 089/218077625 nadja.giesbrecht@cup.uni-muenchen.de Arten chemischer Bindung Die entscheidende Größe für den
Organische Experimentalchemie
 Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Dr. Franziska Thomas (fthomas@gwdg.de) Georg-August-Universität Göttingen SoSe 2018 Veranstaltungsnummer: 15 133 30200 Organische Experimentalchemie Für Studierende der Humanmedizin, Zahnmedizin und Biologie
Chemie in der Schule: www.chids.de. Vitamine
 Vitamine Übersicht 1. ahrung 2. Was ist ein Vitamin? 3. Klassifizierung 4. Wasserlösliche Vitamine 5. Fettlösliche Vitamine 6. Schulrelevanz 1. ahrung ahrung Aufgaben: Versorgung des Körpers mit Betriebsstoffen
Vitamine Übersicht 1. ahrung 2. Was ist ein Vitamin? 3. Klassifizierung 4. Wasserlösliche Vitamine 5. Fettlösliche Vitamine 6. Schulrelevanz 1. ahrung ahrung Aufgaben: Versorgung des Körpers mit Betriebsstoffen
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 4: Aromaten Versuch: Substituenteneinfluss
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 4: Aromaten Versuch: Substituenteneinfluss
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und Nebenfächer (
 Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Klausur zur Vorlesung Bioorganische Chemie für Studenten der Biologie, der Bioinformatik, Lehramt (L2) und ebenfächer ( 05.07.2012, 8 10 Uhr ) Erreichbare Punkte: max. 100 Prof. Dr. J. Engels / Dr. Th.
Seminarplan zum. Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie. (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE
 Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Seminarplan zum Chemischen Praktikum für Biologen ohne Prüfungsfach Chemie (Lehramt) TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE TEIL II: ORGANISCHE CHEMIE 1 TEIL I: ALLGEMEINE UND ANORGANISCHE CHEMIE Einführung
Quantenphysik. Der äußere Lichtelektrische Effekt (Photoeffekt)
 Quantenphysik Der äußere Lichtelektrische Effekt (Photoeffekt) 1. Experiment (qualitativ): Eine negativ geladene Zinkplatte wird mit UV-Licht bestrahlt. Licht als elektromagnetische Welle (so dachte man)
Quantenphysik Der äußere Lichtelektrische Effekt (Photoeffekt) 1. Experiment (qualitativ): Eine negativ geladene Zinkplatte wird mit UV-Licht bestrahlt. Licht als elektromagnetische Welle (so dachte man)
Seminar zum Organisch-Chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016. Aromatische Substitution. Dr. Florian Achrainer AK Zipse
 Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Seminar zum rganisch-chemischen Praktikum für Lehramtsstudierende Wintersemester 2015/2016 Aromatische Substitution Sicherheitsbelehrung: egeln für das Arbeiten im Labor Dr. Florian Achrainer AK Zipse
Übungen zur VL Chemie für Biologen und Humanbiologen
 Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
Übungen zur VL Chemie für Biologen und Humanbiologen 28.01.2011 1. Zeichnen Sie die Valenzstrichformeln folgender Verbindungen und benutzen Sie im Falle unbestimmter Alkylreste ein R: a) ein tertiärer
5. Elektronen- und Rotations- Spektren von Molekülen
 5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
5. Elektronen- und Rotations- Spektren von Molekülen Absorptionsspektren Optische Dichte Elektronischer Übergang S 0 S von Benzol: In der Gasphase: Rotations-Schwingungsstruktur Im Kristall: Spektrale
