Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
|
|
|
- Friedrich Boer
- vor 5 Jahren
- Abrufe
Transkript
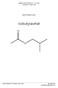
1 rganisch-chemisches Praktikum II WS 2008/2009 Gruppenpräparat Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Felix Bergler Benjamin Fröhlich Franziska Witterauf
2 Inhaltsverzeichnis 1. Aufgabenstellung Literaturrecherche Sicherheit und Entsorgung Versuchsdurchführung Darstellung von 1,3-Diphenylpropenon Ansatz Ansatz Darstellung von S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin Ansatz 1 unter Stickstoffatmosphäre Ansatz 2 ohne Stickstoffatmosphäre Darstellung von trans-1-benzoyl-2-phenylcyclopropan Ansatz 1 äquimolare Menge an gewaschenem NaH Ansatz 2 Überschuss an gewaschenem NaH Ansatz 3 Überschuss an 60%igem NaH Zusammenfassung Ausblick Literaturverzeichnis Anhang Spektren
3 1. Aufgabenstellung Im Rahmen dieses Gruppenpräparats sollte bei folgender Synthese von trans-1-benzoyl-2- phenylcyclopropan ein Weg gefunden werden, das Produkt zu isolieren, was zuvor im Praktikum mittels Sublimation noch nicht gelungen ist. CH 3 CH 3 CH 3 Na S N Cl + H 3 C S CH 3 CuCl 2 S N H3 C S CH 3 NaH DMS S N H2 C S CH 3 CH 3 + H NaH EtH DMS H 2. Literaturrecherche Zuerst wurden die im Praktikumsskript angegebenen Literaturangaben zur Synthese der Zwischenstufen und des Produkts benutzt. Die Synthesen von 1,3-Diphenylpropenon und S,S- Dimethyl-N-(p-tolylsulfonyl)sulfoximin bereiteten in der Vergangenheit kaum Probleme. Somit wurde 1,3-Diphenylpropenon gemäß der Vorschrift von Kohler und Chadwell [1] und S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin nach der Anleitung von Johnson et al. [2], auf die auch in dem Artikel von Heintzelmann und Swern [3] hingewiesen wurde, durchgeführt. 3
4 Die Umsetzung der beiden Substanzen zum gewünschten Produkt ist ebenso in der Literatur von Johnson et al. [2] beschrieben, wobei die Aufreinigung neben der Sublimation auch säulenchromatographisch erfolgen kann. 3. Sicherheit und Entsorgung 3.1 Sicherheit Tab. 1: Sicherheit eingesetzte Stoffe Gefahrensymbole Natriumhydroxid C Ethanol F Acetophenon Xn Benzaldehyd Xn 1,3-Diphenylpropenon T+ Chloramin-T-Trihydrat C Dimethylsulfoxid N Kupfer(II)chlorid Xn, N Natriumhydrid C, F S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin T+ trans-1-benzoyl-2-phenylcyclopropan T+ Essigsäureethylester F, Xi Petrolether F, Xn, N Nummern der R und S Sätze R35 S26-37/39-45 R11 S7-16 R22-36 S26 R22 S24 Stoff mit unbekannten Eigenschaften R S /37/39-45 R22-36/38-50/53 S R15 S7/8-24/ Stoff mit unbekannten Eigenschaften Stoff mit unbekannten Eigenschaften R S R11-38 S
5 3.2 Entsorgung Ethanol, Acetophenon, Benzaldehyd, 1,3-Diphenylpropenon, Dimethylsulfoxid, S,Sdimethyl-N-(p-tolylsulfonyl)sulfoximin, trans-1-benzoyl-2-phenylcyclopropan, Petrolether, Essigsäureethylester wurden als halogenfreie, organische Lösemittelabfälle entsorgt. Chloramin-T-Trihydrat wurde als halogenhaltiger, organischer Lösemittelabfall entsorgt. Natriumhydroxid, Kupferchlorid wurden neutralisiert und als wässrige Abfälle entsorgt. Natriumhydrid wurde in inertem Lösemittel vorgelegt, zuerst mit Isopropanol und anschließend langsam mit Wasser versetzt. Nach Abreaktion wurde die lösung neutralisiert und als wässrige Abfälle entsorgt. 4. Versuchsdurchführung Dimethylsulfoxid wurde unter Stickstoffatmosphäre destilliert und über Molsieb (4 Å) getrocknet. Acetophenon und Benzaldehyd wurden fraktionierend destilliert und die gereinigten Substanzen sofort verwendet. Hierbei sollte man eine 10 cm Vigreux-Kolonne verwenden. Brechungsindices [4] : n n 20 D 20 D ( Acetophenon) = ( Benzaldehyd) = Darstellung von 1,3-Diphenylpropenon bwohl die Synthese in der Vergangenheit gute Ergebnisse erzielt hat, wurden zwei Ansätze durchgeführt, da beim ersten Mal die Dauer der Reaktion ungewöhnlich lang war. Im Laufe der Reaktion stellte sich heraus, dass, wie schon in der Literatur von Kohler und Chadwell [1] beschrieben, eine optimale und vor allem schnelle Umsetzung bei einer Temperatur von C erfolgt. Bei der Filtration erhielt man eine geringe Ausbeute, was dazu veranlasste eine erneute Reaktion anzusetzen. Allerdings stellte sich im Nachhinein heraus, dass der größte Teil des Produktes des ersten Ansatzes noch in Lösung war. Ebenso wurde im zweiten Ansatz keine äquimolare Menge an Natriumhydroxid verwendet, sondern ein 1.2 molarer Überschuss eingesetzt. 5
6 4.1.1 Ansatz 1 In einen Kolben wurden 4.80 g (0.12 mol) NaH in 50 ml Wasser und 32 ml Ethanol vorgelegt. Unter Rühren mit einem KPG-Rührer bei 17 C wurden zuerst 14.4 g (0.12 mol) Acetophenon und anschließend 12.7 g (0.12 mol) Benzaldehyd zugegeben. Da nach zwei Tagen Rühren nur eine ölige Emulsion vorlag wurde die Reaktionsmischung mit einem Wasserbad auf 25 C erhitzt. Binnen zwei Stunden fiel ein gelber Feststoff aus und es wurden 5 ml 6N NaH zugeben. Nach weiteren zwei Stunden ergab die Reaktionskontrolle mittels Dünnschichtchromatographie (Kieselgel; Laufmittel: Petrolether/Diethylether 2:1) eine vollständige Umsetzung. Die Reaktionsmischung wurde für vier Tage bei -18 C gekühlt und man erhielt einen gelborangenen Feststoff in einer roten Lösung. Der Feststoff wurde über einen Büchnertrichter abfiltriert und mit gekühltem Wasser und gekühltem Ethanol gewaschen. Man erhielt einen gelben Feststoff in Form von kleinen Kügelchen. Die Mutterlauge wurde erneut abfiltriert und anschließend nur mit gekühltem Wasser gewaschen, wodurch man ein gelbes Pulver erhielt. Die Mutterlauge wurde eingeengt und es blieb ein gelbes Pulver zurück. Charakterisierung: Summenformel: C 15 H 12 Molmasse: g/mol Aussehen: gelbes Pulver Schmelzpunkt: C (Lit. [1] : C) Ausbeute: 97% (24.3 g; 117 mmol) (Lit. [1] : 85%) IR [cm -1 ]: = 3060 (=C-H); 1660 (C=); 1600, 1590, 1500 (Ring) 6
7 4.1.2 Ansatz 2 In einen Kolben wurden 1.15 g (28.3 mmol) NaH in 10 ml Wasser und 6 ml Ethanol vorgelegt. Unter Rühren mit einem KPG-Rührer bei 25 C wurden zuerst 2.88 g (24.0 mmol) Acetophenon und anschließend 2.54 g (24.0 mmol) Benzaldehyd zugegeben. Nach fünf Stunden ergab die Reaktionskontrolle mittels Dünnschichtchromatographie (Kieselgel; Laufmittel: Petrolether/Diethylether 2:1) eine vollständige Umsetzung. Die Reaktionsmischung wurde für vier Tage in der Tiefkühltruhe gekühlt und man erhielt einen gelborangenen Feststoff in einer roten Lösung. Der Feststoff wurde über einen Büchnertrichter abfiltriert und mit gekühltem Wasser und gekühltem Ethanol gewaschen. Die Mutterlauge wurde nun eingeengt und es blieb ein gelbes Pulver zurück. Charakterisierung: Summenformel: C 15 H 12 Molmasse: g/mol Aussehen: gelbes Pulver Schmelzpunkt: 54 C (Lit. [1] : C) Ausbeute: 93% (4.65 g; 22.3 mmol) (Lit. [1] : 85%) IR [cm -1 ]: = 3060 (=C-H); 1660 (C=); 1600, 1590, 1500 (Ring) 4.2 Darstellung von S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin Die Darstellung von S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin wurde analog der Vorschrift von Johnson et al. [2] durchgeführt, wobei die Reaktion unter Stickstoffatmosphäre gehalten wurde. Zum Vergleich wurde ein zweiter Ansatz ohne Stickstoffatmosphäre angesetzt und festgestellt, dass dieser die gleiche Ausbeute an Rohprodukt lieferte. 7
8 4.2.1 Ansatz 1 unter Stickstoffatmosphäre Zu 80 ml trockenem DMS wurden unter Stickstoffatmosphäre 2.00 g Kupferchlorid zugegeben, welches die Lösung grünlich färbte. Während der Zugabe von 28.5 g (101 mmol) Chloramtin-T 3H 2 färbte sich die Lösung zuerst dunkelrot und wechselte die Farbe nach grün, was darauf hindeutete, dass die Reaktion schon halb fertig war [2]. Nach 30 min Rühren, wurde drei Stunden unter Rückfluss erhitzt. Hierbei erhielt man nach zwei Stunden eine trübe olivegrüne Lösung und nach einer weiteren Stunde eine trübe orangene Lösung. Die Reaktionskontrolle mittels Dünnschichtchromatographie (Kieselgel; Laufmittel: Essigsäureethylester/Petrolether 1:5) zeigte eine vollständige Umsetzung an. Die Reaktionsmischung wurde in 500 ml Wasser und 80 ml gesättigte EDTA-Lösung gegeben und anschließend über einen Büchnertrichter abfiltriert. Man erhielt eine blaugrüne Mutterlauge und das Produkt als beiges Pulver. Charakterisierung: Summenformel: C 9 H 13 N 3 S 2 Molmasse: g/mol Aussehen: beiges Pulver Schmelzpunkt: C (Lit. [2] : C (aus Ethanol)) Ausbeute: 65% (16.1 g; 62.2 mmol) (Lit. [2] : 90%) IR [cm -1 ]: = 3060 (=C-H); 2930 (-CH 3 ); 1600 (Ring); 1400 (-CH 3 ); 1150 (-S 2 ); 1060 (-S=) Ansatz 2 ohne Stickstoffatmosphäre Zu 10 ml trockenem DMS wurden unter Stickstoffatmosphäre 0.20 g (1.49 mmol) Kupferchlorid zugegeben, was die Lösung grünlich färbte. Während dem Zugeben von 3.20 g (11.4 mmol) ChloramtinT 3H 2 färbte sich die Lösung zuerst dunkelrot und wechselte die Farbe in grün, was darauf deutete, dass die Reaktion schon halb fertig ist. Nach 30 min Rühren bei Raumtemperatur, wurde anschließend zwei Stunden unter Rückfluss erhitzt, wobei sich die Lösung zuerst olivegrün und anschließend orange färbte. Die Reaktionskontrolle mittels Dünnschichtchromatographie (Kieselgel; Laufmittel: Essigsäureethylester/Petrolether 1:5) ergab eine vollständige Umsetzung. Die 8
9 Reaktionsmischung wurde in 60 ml Wasser und 10 ml gesättigte EDTA-Lösung gegeben und anschließend über einen Büchnertrichter abfiltriert. Man erhielt eine blaugrüne Mutterlauge und 1.88 g eines weißgrauen Pulvers. Der Schmelzpunkt der Substanz betrug 165 C, wies vorher allerdings einen großen Schmelzbereich auf. Deshalb wurde das Rohprodukt aus Ethanol umkristallisiert. Charakterisierung: Summenformel: C 9 H 13 N 3 S 2 Molmasse: g/mol Aussehen: glitzernde, cremefarbene Kristalle Schmelzpunkt: C (aus Ethanol) (Lit. [2] : C (aus Ethanol)) Ausbeute: 46% (1.30 g; 5.26 mmol) nach Umkristallisation (Lit. [2] : 90%) IR [cm -1 ]: = 3020 (=C-H); 2940 (-CH 3 ); 1600 (Ring); 1405 (-CH 3 ); 1150 (-S 2 ); 1052 (-S=) 4.3 Darstellung von trans-1-benzoyl-2-phenylcyclopropan Die Synthese von trans-1-benzoyl-2-phenylcyclopropan wurde in Anlehnung an die Vorschrift von Johnson et al. [2] durchgeführt. Hier wurde im ersten Ansatz der eine Teil des erhaltenen gelben öligen Rohprodukts mittels Sublimation aufgereinigt und der andere Teil säulenchromatographisch (Kieselgel; Laufmittel: Essigsäureethylester/Petrolether 1:10) getrennt. Da durch die Sublimation kein reines Produkt isoliert werden konnte, jedoch die Chromatographie erfolgreich war, wurde in den folgenden Ansätzen die Säulenchromatographie als Reinigungsmethode gewählt. Es wurden drei Reaktionen, unter Stickstoffatmosphäre, angesetzt, die sich lediglich in der Menge und Reinheit des Natriumhydrids unterschieden. Der erste Ansatz wurde mit äquimolaren Mengen an gewaschenem Natriumhydrid und Edukt, der zweite Ansatz mit 1.4- fachem Überschuss an gewaschenem Natriumhydrid und der dritte Ansatz mit einem 1.4- fachem Überschuss einer 60%igen Dispersion Natriumhydrid durchgeführt. 9
10 Da kein Literaturspektrum für das Produkt verfügbar war und sich das Edukt und Produkt im IR-Spekrum aufgrund ihrer ähnlichen Struktur stark glichen wurde eine NMR-Messung durchgeführt, um zu bestimmen ob noch olefinische Protonen im Produkt vorhanden waren Ansatz 1 Äquimolare Menge an gewaschenem NaH Zuerst wurden 200 mg (5.00 mmol) einer 60%igen Dispersion Natriumhydrid fünfmal mit 10 ml Petrolether unter Stickstoffatmospähre mit einer Umkehrfritte gewaschen. Anschließend wurde unter Stickstoffatmosphäre 120 mg des gereinigten Natriumhydrids in 10 ml DMS vorgelegt, 1.24 g (5.01 mmol) S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin zugegeben und die Lösung drei Stunden bei Raumtemperatur gerührt. Nach der Zugabe von 1.04 g (5.01 mmol) 1,3-Diphenylpropenon ließ man die Reaktionsmischung über Nacht rühren und überführte sie am nächsten Tag in 50 ml Wasser. Die Lösung wurde viermal mit je 25 ml Diethylether extrahiert, die organische Phase über Magnesiumsulfat getrocknet und nach Entfernen des Lösemittels erhielt man 1.26 g eines gelben Öls als Rohprodukt g des Öls wurden mittels Sublimation mit einem Trockeneiskältefinger aufgereinigt. Allerdings erhielt man hierbei einen gelben öligen Feststoff, was auf Verunreinigungen hindeutete. Der Schmelzpunkt betrug 37 C. Charakterisierung: Summenformel: C 16 H 14 Molmasse: g/mol Aussehen: gelber öliger Feststoff Schmelzpunkt: 37 C (Lit. [2] : C) Ausbeute: 2% (4.70 mg; 0.02 mmol) (Lit. [2] : 88%) IR [cm -1 ]: = (=C-H), 1657 (C=), 1400 (C-H von Cyclopropan) 1 H-NMR (400MHz, CDCl 3 ): Das Spektrum wies keinerlei olefinsche Protonenpeaks mehr auf, jedoch war eine eindeutige Zuordnung der Peaks nicht möglich und man konnte noch Verunreinigungen erkennen. 10
11 0.98 g wurden säulenchromatographisch (Kieselgel; Laufmittel: Essigsäureethylester/Petrolether 1:10) aufgereinigt. Dabei erhielt man nach Trocknung im Vakuum einen weißen Feststoff. Charakterisierung: Summenformel: C 16 H 14 Molmasse: g/mol Aussehen: weißer Feststoff Schmelzpunkt: 43 C (Lit. [2] : C) Ausbeute: 1% (15.8 mg; 0.07 mmol) (Lit. [2] : 88%) IR [cm -1 ]: = (=C-H), 1657 (C=), 1400 (C-H von Cyclopropan) 1 H-NMR (400MHz, CDCl 3 ) [ppm]: δ = 7.91 (m, 2H, arom.), 7.49 (m, 1H, arom.), 7.40 (m, 2H, arom.), 7.25 (m, 1H, arom.), 7.17 (m, 1H, arom.), 7.15 (m, 1H, arom.), 7.12 (m, 1H, arom.), 7.10 (m, 1H, arom.), 2.84 (m, 1H, C-H), 2.63 (m, 1H, C-H), 1.85 (m, 1H, C-H) 1.48 (m, 1H, C-H) Ansatz 2 Überschuss an gewaschenem NaH Zuerst wurde eine 60%igen Dispersion Natriumhydrid fünfmal mit 10 ml Pentan unter Stickstoffatmospähre mit einer Umkehrfritte gewaschen. Anschließend wurden unter Stickstoffatmosphäre 0.30 g (7.00 mmol) Natriumhydrid in 10 ml DMS vorgelegt, 1.18 g (5.00 mmol) S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin zugegeben und die Lösung drei Stunden bei Raumtemperatur gerührt. Nach der Zugabe von 1.04 g (5.01 mmol) 1,3- Diphenylpropenon ließ man die Reaktionsmischung über Nacht rühren und überführte sie am nächsten Tag in 50 ml Wasser. Die Lösung wurde viermal mit je 25 ml Diethylether extrahiert, die organische Phase über Magnesiumsulfat getrocknet und nach Entfernen des Lösemittels erhielt man ein gelbes Öl als Rohprodukt. Das Öl wurde säulenchromatographisch (Kieselgel; Laufmittel: Essigsäureethylester/Petrolether 1:10) aufgereinigt. Dabei erhielt man 460 mg (2.07 mmol) eines weißen Feststoffes. 11
12 Charakterisierung: Summenformel: C 16 H 14 Molmasse: g/mol Aussehen: weißer Feststoff Schmelzpunkt: 42 C (Lit. [2] : C) Ausbeute: 41% (460 mg; 2.07 mmol) (Lit. [2] : 88%) IR [cm -1 ]: = (=C-H), 1657 (C=), 1400 (C-H von Cyclopropan) 1 H-NMR (400MHz, CDCl 3 ) [ppm]: δ = 7.97 (m, 2H, arom.), 7.53 (m, 1H, arom.), 7.45 (m, 2H, arom.), 7.28 (m, 2H, arom.), 7.20 (m, 3H, arom.), 2.84 (m, 1H, C-H), 2.65 (m, 1H, C-H), 1.90 (m, 1H, C-H), 1.52 (m, 1H, C-H) Ansatz 3 Überschuss an 60%igem NaH Unter Stickstoffatmosphäre wurden 0.28 g (7.00 mmol) Natriumhydrid, wobei hier eine 60%igen Dispersion eingesetzt wurde, in 20 ml DMS vorgelegt, 1.24 g (5.01 mmol) S,S- Dimethyl-N-(p-tolylsulfonyl)sulfoximin zugegeben und die Lösung drei Stunden bei Raumtemperatur gerührt. Nach der Zugabe von 1.04 g (5.01 mmol) 1,3-Diphenylpropenon ließ man die Reaktionsmischung über Nacht rühren und überführte sie am nächsten Tag in 50 ml Wasser überführt. Die Lösung wurde viermal mit je 25 ml Diethylether extrahiert, die organische Phase über Magnesiumsulfat getrocknet und nach Entfernen des Lösemittels erhielt man ein gelbes Öl als Rohprodukt. Das Öl wurde säulenchromatographisch (Kieselgel; Laufmittel: Essigsäureethylester/Petrolether 1:10) aufgereinigt. Dabei erhielt man 532 mg (2.38 mmol) eines weißen Feststoffes. Charakterisierung: Summenformel: C 16 H 14 Molmasse: g/mol Aussehen: weißer Feststoff Schmelzpunkt: 44 C (Lit. [2] : C) Ausbeute: 47% (532 mg; 2.38 mmol) (Lit. [2] : 88%) 12
13 IR [cm -1 ]: = (=C-H), 1657 (C=), 1400 (C-H von Cyclopropan) 1 H-NMR (DMS) δ [ppm]: δ = 8.01 (m, 2H, arom.), 7.55 (m, 1H, arom.), 7.46 (m, 2H, arom.), 7.32 (m, 2H, arom.), 7.21 (m, 3H, arom.), 2.91 (m, 1H, C-H), 2.71 (m, 1H, C-H), 1.93 (m, 1H, C-H), 1.57 (m, 1H, C-H) 5. Zusammenfassung Es ist im Rahmen des Gruppenpräparates gelungen das gewünschte Produkt zu isolieren. Anstelle der Aufreinigung durch Sublimation erzielte die Säulenchromatographie gute Erfolge. Allerdings erhielt man bei den durchgeführten Ansätzen nur die Hälfte der Literaturausbeute. Bei der Verwendung mit der äquimolaren Menge an gewaschenem Natriumhydrid lässt sich über die Ausbeute keine eindeutige Aussage treffen, da das Rohöl zur Aufreinigung aufgeteilt wurde. Es war kein großer Ausbeuteunterschied zwischen dem gewaschenen Natriumhydrid und der Dispersion, die beide im 1.4-fachem Überschuss eingesetzt wurden, zu erkennen. Neben der eigentlichen Aufgabenstellung konnte erarbeitet werden, dass es bei der Darstellung von 1,3-Diphenylpropenon wichtig ist, die Reaktionstemperatur von C einzuhalten. Bei der Synthese von S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin erhält man unter Schutzgas keine bessere Ausbeute. Allerdings wurde in den zwei Ansätzen nur die Hälfte der Literaturausbeute erzielt. 6. Ausblick Womöglich könnte man die Ausbeute dadurch verbessern, indem man einen noch größeren Überschuss an Natriumhydrid einsetzt. der man versucht durch Variieren der Reaktionszeiten eine bessere Umsetzung zu erlangen. 13
14 7. Literaturverzeichnis [1] E. P. Kohler, H. M. Chadwell, rg. Synth. Coll. Vol. 1941, 1, [2] C. R. Johnson et al., J. Am. Chem. Soc. 1973, 95, [3] R. W. Heintzelman, D. Swern, Synthesis 1976, [4] Fluka, laboratory chemicals 2001/2002, Riedel-de Haën. 14
15 8. Anhang Spektren Anhang 1: IR-Spektrum von S,S-Dimethyl-N-(p-tolylsulfonyl)sulfoximin = 3020 (=C-H); 2940 (-CH 3 ); 1600 (Ring); 1405 (-CH 3 ); 1150 (-S 2 ); 1052 (-S=) Anhang 2: IR-Spektrum von trans-1-benzoyl-2-phenylcyclopropan = (=C-H), 1657 (C=), 1400 (C-H von Cyclopropan) 15
16 Anhang 3 5: NMR-Spektren von trans-1-benzoyl-2-phenylcyclopropan 16
17 17
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan
 Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Mustervorschrift zu Versuch 6.3.4: trans-1-benzoyl-2-phenylcyclopropan Reaktion: Na N Cl + H 3 C CuCl 2 N H 3 C NaH DM N H 2 C CH 2 + H NaH EtH DM H Erstellt von: Felix Bergler Timo Duden Bettina Förster
Betreuer: Tobias Olbrich Literatur: Nach Organic Syntheses Coll. Vol. 10 (2004), 96.
 rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
rganisches Praktikum CP II Wintersemester 2009/10 Versuch 28 Salen-Ligand Betreuer: Tobias lbrich Literatur: ach rganic Syntheses Coll. Vol. 10 (2004), 96. Chemikalien: L-()-Weinsäure 1,2-Diaminocyclohexan
Protokoll zum Gruppenpra parat
 Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Protokoll zum Gruppenpra parat Versuche 5.4.1.2 und 4.4.4: Darstellung von 1 Naphthol 1. Darstellung von Anthranilsäure aus Phthalsäureimid 1.1. Literatur [1] www.merckmillipore.de/chemicals [2] sdbs.riodb.aist.go.jp/
Organisch chemisches Praktikum II
 18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
18.04.2010 rganisch chemisches Praktikum II WS 2009 / 2010 Gruppenpräparat 7.3.4: 1,3-Dibenzoylbenzimidazolon Heuler Dominik Sedlag Florian Inhaltsverzeichnis: 1 Einleitung 2 Literaturrecherche 3 Reaktionsgleichung
Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:
![Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer: Organisches Praktikum OCP II Wintersemester 2009/10. Versuch 30. 1,4-Diphenyl-6,7-dihydro-5H-cyclopenta[d]pyridazin. Betreuer:](/thumbs/55/37246535.jpg) Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Organisches Praktikum OCP II Wintersemester 2009/10 Versuch 30 1,4-Diphenyl-6,7-dihydro-5-cyclopenta[d]pyridazin Betreuer: Chemikalien: Benzonitril Tomahogh ydrazinhydrat achtraum (Kühlschrank) Schwefel
Gruppenpräparat 8.5. Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain
 Gruppenpräparat 8.5 Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain NaN 2,5nHCl H N Zn/HCl Cl NH 3 t-bu t-bu H C 14 H 22 206.33
Gruppenpräparat 8.5 Darstellung von 2,4,6 Triphenyl N (3,5 di tert. butyl 4 hydroxyphenyl) pyridinium tetrafluoroborat und entsprechendes Betain NaN 2,5nHCl H N Zn/HCl Cl NH 3 t-bu t-bu H C 14 H 22 206.33
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b
 3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
3.4.6 Cycloaddition von Anthracen und 1,4-Benzochinon unter Aluminiumchlorid- Katalyse zum 1:1-Addukt 6a und zum 2:1-Addukt 6b 1 : 1 6a + AlCl 3 C 2 Cl 2 2 : 1 6b C 14 10 (178.2) C 6 4 2 (108.1) AlCl 3
Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion)
 4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4.3.1.8 Disproportionierung von Furan-2-carbaldehyd (Furfural) mit Natronlauge zu Furan-2-carbonsäure und 2-Furylmethanol (Cannizzaro-Reaktion) H NaH konz. 8a H + 8b H H 4 2 (96.1) H 4 3 (112.1) H 6 2
4002 Synthese von Benzil aus Benzoin
 4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
4002 Synthese von Benzil aus Benzoin H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Klassifizierung Reaktionstypen und Stoffklassen xidation Alkohol, Keton, Schwermetallkatalysator
3021 Oxidation von Anthracen zu Anthrachinon
 xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
xidation von Anthracen zu Anthrachinon Ce(IV)(NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Literatur Tse-Lok Ho et al., Synthesis 97, 6. Klassifizierung Reaktionstypen und Stoffklassen xidation Aromat,
2. Herstellung der α,β-ungesättigten Kupplungskomponenten C H 3 H 33. Br 22 25
 2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
2. Herstellung der α,β-ungesättigten Kupplungskomponenten 2.1. E-3-(2-omphenyl)-propenal (25) C H 3 H 1 H H 33 1' 3 22 25 2' Eine Emulsion aus 1.85 g (10.0 mmol) 2-ombenzaldehyd (22), 616 mg (14.0 mmol)
3011 Synthese von erythro-9,10-dihydroxystearinsäure aus Ölsäure
 311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
311 Synthese von erythro-9,1-dihydroxystearinsäure aus Ölsäure COOH KMnO 4 /NaOH HO HO COOH C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Literatur A. Lapworth und E. N. Mottram,
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol
 4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4028 Synthese von 1-Bromdodecan aus 1-Dodecanol C 12 H 26 O (186.3) OH H 2 SO 4 konz. (98.1) + HBr (80.9) C 12 H 25 Br (249.2) Br + H 2 O (18.0) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
8.1 Durchführung gemäß Gruppenpräparat WS 2008/2009
 Inhalt: 1. Mustervorschrift aus dem WS2008/2009 2. Problemstellung 3. Literaturrecherche 4. Reaktionsgleichung 5. Gefahrenpotenzial 6. Entsorgung 7. Mechanismus 8. Durchgeführte Experimente 8.1 Durchführung
Inhalt: 1. Mustervorschrift aus dem WS2008/2009 2. Problemstellung 3. Literaturrecherche 4. Reaktionsgleichung 5. Gefahrenpotenzial 6. Entsorgung 7. Mechanismus 8. Durchgeführte Experimente 8.1 Durchführung
2017 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid
 217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
217 Umsetzung von Zimtsäurechlorid mit Ammoniak zu Zimtsäureamid O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) (17.) C 9 H 9 NO (147.2) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der Carbonylgruppe
4009 Synthese von Adipinsäure aus Cyclohexen
 4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4009 Synthese von Adipinsäure aus Cyclohexen C 6 H 10 (82.2) + Natriumwolframat-Dihydrat + 4 H 2 H 2 H + 4 H 2 (34.0) + Aliquat 336. Na 2 W 4 2 H 2 (329.9) C 25 H 54 ClN (404.2) C 6 H 10 4 (146.1) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol OH
 4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
4029 Synthese von Dodecylphenylether aus Bromdodecan und Phenol H C 12 H 25 Br (249.2) Br + + NaH (40.0) + Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 (94.1) C 18 H 30 (262.4) + NaBr (102.9) Klassifizierung
Organisch Chemisches Praktikum II. Gruppenpräparat: Darstellung von Z Crotonsäure
 Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
Organisch Chemisches Praktikum II Gruppenpräparat: 5.3.1.1 Darstellung von Z Crotonsäure Gruppe 5: Andreas Kraft Thomas Kramer Johannes Landmann Datum: 3.10.2009 Aufgabenstellung: Die Aufgabe bestand darin,
4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester
 NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4022 Synthese von (S)-(+)-3-Hydroxybuttersäureethylester Fermentierende Hefe, Saccharose H C 6 H 10 3 C 12 H 22 11 C 6 H 12 3 (130.1) (342.3) (132.2) Klassifizierung Reaktionstypen und Stoffklassen
Synthese von Benzalacetophenon
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von Benzalacetophenon Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 10. März 2008 page
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von Benzalacetophenon Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 10. März 2008 page
Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on
 Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
Praktikum Anorganische und rganische Chemie I Assistent: Matthias berli Synthese von eritreo- und reo-8,9,epoxy-p-menth-2-enl-on Dietikon, 24. April 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 Zusammenfassung
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol
 4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4026 Synthese von 2-Chlor-2-methylpropan (tert-butylchlorid) aus tert-butanol OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
NO 2 Rühren mit Magnetrührer, Extrahieren, Ausschütteln, Abrotieren, Umkristallisieren, Abfiltrieren,
 1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1003 Nitrierung von Benzaldehyd zu 3-Nitrobenzaldehyd H O H O HNO 3 /H 2 SO 4 + Nebenprodukte NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon)
 1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
1009 Intramolekulare Acylierung von 4-Phenylbuttersäure zu 1,2,3,4-Tetrahydronaphthalin-1-on (α-tetralon) H Polyphosphorsäure C 10 H 12 2 (164.2) C 10 H 10 (146.2) Klassifizierung Reaktionstypen und Stoffklassen
3012 Synthese von Adamantylidenadamantan aus Adamantanon
 Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von Adamantylidenadamantan aus Adamantanon O TiCl /Zn/THF C H O (.) TiCl Zn (9.) (.) C H (.) Literatur D. Lenoir, Synthesis, 99, -9 Klassifizierung Reaktionstypen und Stoffklassen McMurry-Reaktion,
Synthese von cis- und trans-stilben
 28. April 2008 eifer Manuel raktikum in Organischer Chemie (OC 1) Frühjahrssemester 2008 529-0230-00L eifer Manuel Synthese von cis- und trans-stilben Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich
28. April 2008 eifer Manuel raktikum in Organischer Chemie (OC 1) Frühjahrssemester 2008 529-0230-00L eifer Manuel Synthese von cis- und trans-stilben Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich
Ein Gemisch aus 13,2 g (0,1mol) 2,5-Dimethoxyterahydrofuran und 80ml 0,6 N Salzsäure werden erhitzt bis vollständige Lösung eintritt.
 1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
1.Acetondicarbonsäureanhydrid 40g (0,27mol)Acetondicarbonsäure werden in einer Lösung aus 100ml Eisessig und 43ml (0,45mol) Essigsäureanhydrid gelöst. Die Temperatur sollte 20 C nicht überschreiten und
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13
 Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Darstellung von 3,5-Diphenylisoxazol (1) Präparat 8 und Versuch der Umsetzung zu 2,5-Diphenyloxazol (1) Präparat 13 1. Reaktionstyp: (a) Cyclokondensation von 1,3-Diketonen mit ydroxylaminhydrochlorid
Chloro(salen*)mangan(III)
 Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
Chloro(salen*)mangan(III) [MnCl(salen*)] Asymmetrische Epoxidierung von Styrol Zürich, 31. Januar 2005 Raphael Aardoom, ACP 2 1 Synthese 1.1 Methode [1][2][3] Salen* reagiert mit Mangan(II)acetat und atriumchlorid
5007 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin
 57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
57 Synthese von Fluorescein aus Phthalsäureanhydrid und Resorcin CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Klassifizierung Reaktionstypen und Stoffklassen Reaktion der
5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester
 NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
NP 5013 Synthese von 2,6-Dimethyl-4-phenyl-1,4-dihydropyridin- 3,5-dicarbonsäure-diethylester NH 4 HC 3 + + 2 C 2 C 2 C 2 H CH 3 H 3 C N CH 3 H + 4 H 2 + C N 3 C 7 H 6 C 6 H 10 3 C 19 H 23 4 N C 2 (79.1)
Mustervorschrift 2.3.1
 Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
Christoph Böhm, Lisa Gutjahr, Philipp Hennig, Thorsten Scherpf, Junwen Shan, Verena Thyen Mustervorschrift 2.3.1 Darstellung von 1,2-Bis(trimethylsilyloxy)cyclohex-1-en: In einem trockenen und unter Schutzgas
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen
 3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
3003 Synthese von trans-2-chlorcyclohexanol aus Cyclohexen _ + SO 2 NCl Na OH H 2 SO 4 + x 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H
4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus
 NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
NP 4023 Synthese von Cyclopentanon-2-carbonsäureethylester aus Adipinsäurediethylester NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Klassifizierung Reaktionstypen und Stoffklassen
4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester
 NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
NP 4019 Synthese von Acetamidostearinsäuremethylester aus Ölsäuremethylester C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me C 21 H 41 N 3 (355.6) NH Klassifizierung
4006 Synthese von 2-(3-Oxobutyl)cyclopentanon-2- carbonsäureethylester
 4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
4006 Synthese von 2-(3-xobutyl)cyclopentanon-2- carbonsäureethylester CEt + FeCl 3 x 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Klassifizierung Reaktionstypen und Stoffklassen
Organisch-chemisches Praktikum Wintersemester 2005/06. 1-Phenyl-propan-1-ol. Stephan Steinmann
 Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Organisch-chemisches Praktikum Wintersemester 005/06 -Phenyl-propan--ol 08.. 005 Stephan Steinmann . Methode [] Benzaldehyd () wird über eine Grignard-Reaktion mit Ethylmagnesiumbromid (5) zum -Phenylpropan--ol
Synthese von 1-(p-Tolyl)butan-1,4-diol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1-(p-Tolyl)butan-1,4-diol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich, 07. April
4010 Synthese von p-methoxyacetophenon aus Anisol
 4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
4010 Synthese von p-methoxyacetophenon aus Anisol C 3 + 3 C C 3 Zeolith C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on)
 6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
6012 Aldol-Kondensation von Aceton und Benzaldehyd zu Dibenzalaceton (1,5-Diphenyl-1,4-pentadien-3-on) H 2 + KH H 2 /EtH/THF C 7 H 6 C 3 H 6 KH (56.1) C 17 H 14 (106.1) (58.1) (234.3) Klassifizierung Reaktionstypen
Benzol-d. Illumina-Chemie.de - Artikel
 Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
Illumina-Chemie.de - Artikel Synthesen Benzol-d 1 Dieser Versuch demonstriert eine häufig verwendete Möglichkeit zur gezielten Deuterierung von Molekülen, wie sie z.b. für die Mikrowellenspektroskopie
170 C C 2 H C C 11 H 10 (174.2) Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien
 3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3.4.2 Darstellung von Cyclopentadien durch thermische Spaltung von Dicyclopentadien. [4+2]-Cycloaddition von Cyclopentadien mit p-benzochinon zum 1:1- Addukt (2a) und zum 2:1-Addukt (2b) 170 C 2 C 10 12
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien
 3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
3009 Synthese von trans-5-norbornen-2,3-dicarbonsäure aus Fumarsäure und Cyclopentadien 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H 10 O 4 (182.2)
Gruppenpräparat: Versuch Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon
 P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch 7.4.1.1 Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan
P II Praktikum im WS 2008/2009 Gruppenpräparat: Versuch 7.4.1.1 Darstellung von 1,2-Diphenyl-2,2-(4-methylphenyl)- ethanon 1.Gruppe: Christoph Mann Marco Schott 2.Gruppe: Tim Walter Holger Hartleb Stefan
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol
 4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
4027 Synthese von 11-Chlorundec-1-en aus 10-Undecen-1-ol OH SOCl 2 Cl + HCl + SO 2 C 11 H 22 O C 11 H 21 Cl (170.3) (119.0) (188.7) (36.5) (64.1) Klassifizierung Reaktionstypen und Stoffklassen Nukleophile
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b).
 2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
2022 Reduktion von L-( )-Menthon mit Lithiumaluminiumhydrid zu einem Isomerengemisch ( )-Menthol (a) und (+)-Neomenthol (b). 3 O LiAl 4 tert-butylmethylether 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
1035 Synthese von p-methoxyacetophenon aus Anisol
 NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
NP 05 Synthese von p-methoxyacetophenon aus Anisol CH + CH CH Sc(Tf) + CH CH CH CH C 7 H 8 (08.) C 4 H 6 (02.) (CF S ) Sc (492.2) C 9 H 0 2 (50.2) C 2 H 4 2 (60.) Klassifizierung Reaktionstypen und Stoffklassen
Chloro(triphenylphosphin)gold(I)
 raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
raktikum Org. und Anorg. Chemie II D-CHAB Wintersemester 04/05 Zürich, den 1. März 2005 [(h 3 )] 1 1. SYNTHESE 1.1 Methode [1] Elementares Gold wird mit Königswasser aufgeschlossen und durch Zugabe von
(±)-4-Methyl-3- heptanon
 Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Synthese von (±)-4-Methyl-3- heptanon rganische Chemie Praktikum 1 Zürich, 14.12.2006 WS 2006 / 07 Maresa Afthinos Assistenz: Michael Schär Versuchsdurchführung: 12. Dezember 2006-1 - CP1 Synthese 5 Maresa
Gruppenpräparat zu V Cis-9-Methyl-2-decalon
 rganisch-chemisches-praktikum II WS 2007/2008 Gruppenpräparat zu V 6.2.2 Cis-9-Methyl-2-decalon Gruppe: E / F Jürgen Bauer Nadja Bertleff Daniel Ertler Johannes Klein Eva Siedler Johannes Wahler 1 Inhaltsverzeichnis:
rganisch-chemisches-praktikum II WS 2007/2008 Gruppenpräparat zu V 6.2.2 Cis-9-Methyl-2-decalon Gruppe: E / F Jürgen Bauer Nadja Bertleff Daniel Ertler Johannes Klein Eva Siedler Johannes Wahler 1 Inhaltsverzeichnis:
Praktikumsprotokoll OP II Gruppenpräparat. Synthese von 2S 3S Epoxygeraniol
 Praktikumsprotokoll P II 10.4.4.1 Gruppenpräparat Synthese von 2S 3S Epoxygeraniol Praktikanten: Christian Possiel und Kai Stephan Feichtner Bachelor Datum: 14.4.2010 Verwendete Literatur 1) L. M. Bradley,
Praktikumsprotokoll P II 10.4.4.1 Gruppenpräparat Synthese von 2S 3S Epoxygeraniol Praktikanten: Christian Possiel und Kai Stephan Feichtner Bachelor Datum: 14.4.2010 Verwendete Literatur 1) L. M. Bradley,
2-Methylcyclohexanon
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von 2-Methylcyclohexanon Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Das Ausgangsprodukt dieser
Indan-1,3-dion. Reaktionsgleichung. H- und P-Sätze. Für alle Reagenzien und Produkte. Ausformulierte H- und P-Sätze. Vor(Abschluss)protokoll
 Indan-1,3-dion Reaktionsgleichung H- und P-Sätze Substanz Gefahrensymbol Smp. ( C) Sdp. ( C) Phtalsäurediethylester Essigsäureethylester Flammpkt. ( C) H-Sätze P-Sätze - -40 302 150 - - Gefahr -83 77-4
Indan-1,3-dion Reaktionsgleichung H- und P-Sätze Substanz Gefahrensymbol Smp. ( C) Sdp. ( C) Phtalsäurediethylester Essigsäureethylester Flammpkt. ( C) H-Sätze P-Sätze - -40 302 150 - - Gefahr -83 77-4
Synthese von Acetessigsäureethylester
 Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Illumina-Chemie.de - Artikel Synthesen Synthese von Acetessigsäureethylester Acetessigsäureethylester ist der wohl bekannteste β-ketoester und durch seine CH-acide Methylengruppe (pk a = 11) leicht elektrophil
Gruppenpräparat im Rahmen des OPII-Praktikums an der Universität Würzburg
 Gruppenpräparat im Rahmen des OPII-Praktikums an der Universität Würzburg Versuch 4.3.3 Darstellung von cis-2,3,5-triphenylisoxazolidin Praktikanten Baus, Johannes Dück, Klaus Schilling, Daniel Assistenten
Gruppenpräparat im Rahmen des OPII-Praktikums an der Universität Würzburg Versuch 4.3.3 Darstellung von cis-2,3,5-triphenylisoxazolidin Praktikanten Baus, Johannes Dück, Klaus Schilling, Daniel Assistenten
1005 Bromierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol
 1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
1005 omierung von 1,2-Dimethoxybenzol zu 4,5-Dibrom-1,2- dimethoxybenzol H 3 H 3 K 3, H Essigsäure H 3 H 3 + Nebenprodukt 8 H 10 2 K 3 (167.0) 8 H 8 2 2 (138.2) H (80.9) (296.0) Klassifizierung Reaktionstypen
Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol
 Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
Praktikum in Organischer Chemie (OCP 1) Frühjahrssemester 2008 529-0230-00L Peifer Manuel Synthese von 1,4-Di-t-butyl-2,5-dimethoxybenzol Janosch Ehrenmann BSc Biotechnologie D CHAB, ETH Zürich Zürich,
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol
 7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
7.2.1 Nitrierung von Toluol zu 2-Nitrotoluol (1a), 4-Nitrotoluol (1b) und 2,4-Dinitrotoluol (1c) HNO 3, H 2 SO 4 + + C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1) 1a 1b 1c C 7 H 7 (137.1) C 7 H 6 N 2 O 4
Synthese von Dibenzalaceton (DBA) (1,5-Bisphenylpenta-1E,4E-dien-3-on)
 Praktikum rganische Chemie I Zürich, 08.01.2006 529-0229-00L (für Biol./arm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Dibenzalaceton (DBA)
Praktikum rganische Chemie I Zürich, 08.01.2006 529-0229-00L (für Biol./arm.Wiss) Wintersemester 05/06 Sylke öhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von Dibenzalaceton (DBA)
5 Chemisch-experimenteller Teil
 5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5 Chemisch-experimenteller Teil 113 5 Chemisch-experimenteller Teil 5.1 Allgemeine Angaben Schmelzpunkt-Bestimmung Lindström-Gerät (unkorrigiert) Elementaranalysen Elementar Vario EL IR-Spektren Perkin-Elmer
5009 Synthese von Kupferphthalocyanin
 P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
P 59 Synthese von Kupferphthalocyanin (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Literatur Klassiche
Gruppenpräparat im Organisch-Chemischen Praktikum II
 Gruppenpräparat im rganisch-chemischen Praktikum II WS 2007/2008 Versuch 6.2.3 Philipp Bissinger Alexander Damme Yvonne Göbel Inhaltsverzeichnis 1. Einleitung 2. Darstellungsmethoden 2.1 Darstellung von
Gruppenpräparat im rganisch-chemischen Praktikum II WS 2007/2008 Versuch 6.2.3 Philipp Bissinger Alexander Damme Yvonne Göbel Inhaltsverzeichnis 1. Einleitung 2. Darstellungsmethoden 2.1 Darstellung von
Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse
 Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Michael Seitz (aum 33.1.23, Tel.: 943-4647) Synthese eines chiralen Liganden Einsatz in einer enantioselektiven Katalyse Durchzuführende eaktionen: 1. NaH, DMS 2. MeI MeS NH 2 K 2 C 3 Glycerin / Ethylenglykol
Extraktion von Hesperidin aus Mandarinenschalen
 Extraktion von Hesperidin aus Mandarinenschalen Diese Arbeitsvorschrift für Sie ist eine Weiterentwicklung derjenigen aus Lit. [1]! HO H3 C HO 4 ''' 6 ''' 5 ''' 3 ''' O OH 2 ''' 1'' ' O OCH 2 3 6 '' '
Extraktion von Hesperidin aus Mandarinenschalen Diese Arbeitsvorschrift für Sie ist eine Weiterentwicklung derjenigen aus Lit. [1]! HO H3 C HO 4 ''' 6 ''' 5 ''' 3 ''' O OH 2 ''' 1'' ' O OCH 2 3 6 '' '
Oxidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) CO 2
 6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
6. xidations-, Reduktions-Reaktionen www.ioc-praktikum.de 6.1.4.2 xidation von p-xylol mit Kaliumpermanganat zu Terephthalsäure (2a) und Veresterung zu Terephthalsäurediethylester (2b) C 3 C 2 C 2 C 2
5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid
 NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
NP 5012 Synthese von Acetylsalicylsäure (Aspirin) aus Salicylsäure und Acetanhydrid CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Klassifizierung
Für das Praktikum muss ein Laborjournal (Kladde) geführt werden, und zwar handschriftlich. Kladde bitte mit Namen beschriften.
 Für das Praktikum muss ein Laborjournal (Kladde) geführt werden, und zwar handschriftlich. Kladde bitte mit Namen beschriften. Bitte über jeden Versuch dann ein Datum schreiben. Das zu führende Laborjournal
Für das Praktikum muss ein Laborjournal (Kladde) geführt werden, und zwar handschriftlich. Kladde bitte mit Namen beschriften. Bitte über jeden Versuch dann ein Datum schreiben. Das zu führende Laborjournal
3002 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure
 32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
32 Addition von Brom an Fumarsäure zu meso-dibrombernsteinsäure OOC COO Br 2 OOC Br Br COO C 4 4 O 4 (6.) (59.8) C 4 4 Br 2 O 4 (275.9) Literatur A. M. McKenzie, J. Chem. Soc., 92,, 96 M. Eissen, D. Lenoir,
6011 Hippursäure aus Glycin und Benzoylchlorid
 P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
P 6011 Hippursäure aus Glycin und Benzoylchlorid Cl + H 2 H H H C 7 H 5 Cl C 2 H 5 2 C 9 H 9 3 (140.6) (75.1) (179.2) Klassifizierung Reaktionstypen und Stoffklassen Benzoylierung, Reaktion der Carbonylgruppe
Organisches Praktikum I - SS 2006 Assistentin: Gabi Marti. Synthese von. Isobutylacetat. Zürich, Balzers & Eschen, Mai 2005
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von Isobutylacetat Zürich, Balzers & Eschen, Mai 2005 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1 Carbonsäure bilden mit Alkoholen
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol
 Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
Synthese von 4-tert-Butyl- 1,2-dimethylbenzol Name des/der Assistenten/in: Geyer Karolin Datum der Versuchsdurchführung: 5.12.2005 Rémy Denzler, D-Biol 1 1. Methode o-xylol wird in einer Friedel-Crafts
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid
 1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
1011 Synthese von 1,4-Di-tert-butylbenzol aus tert-butylbenzol und tert-butylchlorid + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Klassifizierung Reaktionstypen und Stoffklassen
Fachbereich Chemie. der Philipps-Universität Marburg
 Fachbereich Chemie der Philipps-Universität Marburg Skriptum zu den Versuchen Moderne präparative Methoden der organischen Chemie (1. Auflage, April 2004) Versuch 1: (AK Schrader) Enantioselektive Michael-Addition
Fachbereich Chemie der Philipps-Universität Marburg Skriptum zu den Versuchen Moderne präparative Methoden der organischen Chemie (1. Auflage, April 2004) Versuch 1: (AK Schrader) Enantioselektive Michael-Addition
2023 Reduktion von D-(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b).
 23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
23 Reduktion von -(+)-Campher mit Lithiumaluminiumhydrid zu einem Isomerengemisch (+)-Borneol (a) und (-)-Isoborneol (b). LiAlH 4 tert-butylmethylether H + OH O OH H C 1 H 16 O (152.2) LiAlH 4 (38.) a
1007 Synthese von 2,4,6-Tribromanilin aus 4-Bromacetanilid
 1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
1007 Synthese von 2,4,6-Tribromanilin aus 4-omacetanilid O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Klassifizierung Reaktionstypen und Stoffklassen
3016 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure
 6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
6 Oxidation von Ricinolsäure (aus Rizinusöl) mit KMnO 4 zu Azelainsäure CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.) C H 6 O 4 (.) Klassifizierung Reaktionstypen
β-binaphthol (1,1 -Binaphthyl-2,2 -diol)
 rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von β-binaphthol (1,1 -Binaphthyl-2,2 -diol) Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1, 2
rganisches Praktikum I - SS 2006 Assistentin: Gabi Marti Synthese von β-binaphthol (1,1 -Binaphthyl-2,2 -diol) Zürich, Balzers & Eschen, Juni 2006 Daniel Frick frickd@student.ethz.ch 1. Einleitung 1, 2
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid
 4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
4008 Synthese von 2-Dimethylaminomethyl-cyclohexanonhydrochlorid + + H 2 N(CH 3 H H EtH, H NH(CH 3 C 6 H 10 CH 2 C 2 H 8 N C 9 H 18 N (98.2) (30.0) (81.6) (191.7) Klassifizierung Reaktionstypen und Stoffklassen
Tris(acetylacetonato)cobalt(III)
 Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
Tris(acetylacetonato)cobalt(III) [Co(C5H7)3] Cobalt(III)acetylacetonat Zürich, 7. November 004 Raphael Aardoom, ACP 1 Synthese 1.1 Methode [1] Cobalt(II)carbonat reagiert mit Acetylaceton in Gegenwart
Darstellung von Chelidamsäure (gekürzte Version)
 CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
CF Assistent (Datum, Unterschrift): CF Auftraggeber (Datum, Unterschrift): Darstellung von Chelidamsäure (gekürzte Version) Protokoll zum rganischchemischen Praktikum für Fortgeschrittene Teil 1 unter
Kalium 13-vanadonickelat(IV) K 7 [NiV 13 O 38 ]*16 H 2 0
![Kalium 13-vanadonickelat(IV) K 7 [NiV 13 O 38 ]*16 H 2 0 Kalium 13-vanadonickelat(IV) K 7 [NiV 13 O 38 ]*16 H 2 0](/thumbs/79/80348146.jpg) K 7 [NiV 13 O 38 ]*16 H 0 Zürich, 03.0.004 1 SYNTHESE 1.1 Methode Kaliumcarbonat und Vanadiumpentoxid reagieren in Wasser zu Kaliummetavanadat. Kaliummetavanadat und Nickelsulfat in Wasser reagieren in
K 7 [NiV 13 O 38 ]*16 H 0 Zürich, 03.0.004 1 SYNTHESE 1.1 Methode Kaliumcarbonat und Vanadiumpentoxid reagieren in Wasser zu Kaliummetavanadat. Kaliummetavanadat und Nickelsulfat in Wasser reagieren in
Protokoll Versuch 2. Synthese von Bis[8-(dimethylamino)naphthyl]ditellurid. Versuchsprotokoll. Fachbereich 2: Chemie
![Protokoll Versuch 2. Synthese von Bis[8-(dimethylamino)naphthyl]ditellurid. Versuchsprotokoll. Fachbereich 2: Chemie Protokoll Versuch 2. Synthese von Bis[8-(dimethylamino)naphthyl]ditellurid. Versuchsprotokoll. Fachbereich 2: Chemie](/thumbs/74/70509027.jpg) Protokoll Versuch 2 Versuchsprotokoll Fachbereich 2: Chemie Autor: Marcus Knappert Studienbereich: Fachbereich 2: Chemie Matrikelnummer: 24 24 74 3 E-Mail: marcus.knappert@gmx.de Semester: Wintersemester
Protokoll Versuch 2 Versuchsprotokoll Fachbereich 2: Chemie Autor: Marcus Knappert Studienbereich: Fachbereich 2: Chemie Matrikelnummer: 24 24 74 3 E-Mail: marcus.knappert@gmx.de Semester: Wintersemester
Synthese von tert-butylchlorid (2-Chloro-2-methylpropan)
 Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Praktikum Organische Chemie I Zürich, 03.12.2005 529-0229-00L (für Biol./Pharm.Wiss) Wintersemester 05/06 Sylke Höhnel 04-921-664 3. Semester Assistent: Pascal Bindschädler Synthese von tert-butylchlorid
Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv)
 Cp2(H) Seite 1 Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv) [Cp 2 (H)] H (SCHWARTZ Reagens) Cp2(H) Seite 2 1. Synthese [1,2,3] 1.1 Methode Dicyclopentadien wird in einer Retro-DIELS-ALDER-Reaktion
Cp2(H) Seite 1 Chloro-bis(η 5 -cyclopentadienyl)- hydridozirkon(iv) [Cp 2 (H)] H (SCHWARTZ Reagens) Cp2(H) Seite 2 1. Synthese [1,2,3] 1.1 Methode Dicyclopentadien wird in einer Retro-DIELS-ALDER-Reaktion
2008 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester
 28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
28 Säurekatalysierte Veresterung von Propionsäure mit 1-Butanol zu Propionsäure-1-butylester H 3 C H 4-Toluolsulfonsäure + Cyclohexan H 3 C H CH 3 + CH 3 H 2 C 3 H 6 2 (74.1) C 4 H 1 (74.1) C 7 H 8 3 S
- 2 - Das folgende retrosynthetische Schema erwies sich als geeignet, die gewünschte Zielverbindung darzustellen. TEG. Abbildung 1
 - 1 - Protokoll ynthese von 4(3)-[4-(triethylenglykolmethylether)-3,5-dimetylphenyl]- cyclohepta-2,4,6-trienyl-[n-(triethylenglykolmethylether)-n- (methyl)-anilin] N rganisch-chemisches Fortgeschrittenenpraktikum
- 1 - Protokoll ynthese von 4(3)-[4-(triethylenglykolmethylether)-3,5-dimetylphenyl]- cyclohepta-2,4,6-trienyl-[n-(triethylenglykolmethylether)-n- (methyl)-anilin] N rganisch-chemisches Fortgeschrittenenpraktikum
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol
 1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
1001 Nitrierung von Toluol zu 4-Nitrotoluol, 2-Nitrotoluol und 2,4-Dinitrotoluol CH 3 CH 3 CH 3 NO 2 CH 3 NO 2 HNO 3 /H 2 SO 4 + + + Nebenprodukte NO 2 NO 2 C 7 H 8 (92.1) HNO 3 (63.0) H 2 SO 4 (98.1)
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013
 Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Fortgeschrittenen-Praktikum Organische Chemie Wintersemester 2012/2013 Universität Leipzig Fakultät für Chemie und Mineralogie Wasserdampfdestillation von Anisöl aus Anissamen Anton Werwein, Richard Cybik
Synthese von Diphenylmethanol
 FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
FS 2008 ET Zürich 23.06.2009 Praktikum Anorganische und Organische Chemie I Assistent: Matthias Oberli Synthese von Diphenylmethanol Dietikon, 18. März 2008 Jorge Ferreiro fjorge@student.ethz.ch 1 FS 2008
5001 Nitrierung von Phenol zu 2-Nitrophenol und 4-Nitrophenol
 00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
00 Nitrierung von Phenol zu -Nitrophenol und -Nitrophenol KNO, H SO NO + NO C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile Substitution an Aromaten,
Institut für Organische Chemie 1 Universität Würzburg
 Institut für Organische Chemie 1 Universität Würzburg Musterprotokoll Hinweise zur Erstellung des Protokolls 21.02.2018 Vorname, Name Datum und Name des Studenten angeben. Beide Angaben gehören natürlich
Institut für Organische Chemie 1 Universität Würzburg Musterprotokoll Hinweise zur Erstellung des Protokolls 21.02.2018 Vorname, Name Datum und Name des Studenten angeben. Beide Angaben gehören natürlich
Mustervorschrift Versuch
 Mustervorschrift Versuch 10.2.3 N-Acetylierung von D-/L- Methionin (1.Stufe) 5.20 g (34.86 mmol) D-/L- Methionin (racemisch) werden in 51.13 g (48.80 ml, 349 mmol) reiner Essigsäure (Eisessig) gelöst 1.
Mustervorschrift Versuch 10.2.3 N-Acetylierung von D-/L- Methionin (1.Stufe) 5.20 g (34.86 mmol) D-/L- Methionin (racemisch) werden in 51.13 g (48.80 ml, 349 mmol) reiner Essigsäure (Eisessig) gelöst 1.
2002 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan
 22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
22 Säurekatalysierte Acetalisierung von Acetessigsäureethylester mit Ethandiol zum entsprechenden Dioxolan 2 H 5 + H H Montmorillonit K 1 yclohexan 2 H 5 + H 2 6 H 1 3 (13.1) 2 H 6 2 (62.1) 8 H 14 4 (174.2)
OP II Praktikum. Gruppenpräparat: Versuch Diethylaminoanisol
 -1/23- OP II Praktikum Gruppenpräparat: Versuch 1.3.1 3- Diethylaminoanisol Gruppe π: Georg Hiltensperger Sebastian Völker Fabian Zieschang -2/23- Gliederung 1. Mustervorschrift 2. Problemstellung 3. Literaturrecherche
-1/23- OP II Praktikum Gruppenpräparat: Versuch 1.3.1 3- Diethylaminoanisol Gruppe π: Georg Hiltensperger Sebastian Völker Fabian Zieschang -2/23- Gliederung 1. Mustervorschrift 2. Problemstellung 3. Literaturrecherche
Leitfaden: Protokoll Routinestufe
 Leitfaden: Protokoll Routinestufe Musterprotokoll: OC-Website, Informationen für Studierende, F-Praktikum, Vordrucke und Formulare, Musterprotokoll_Routinestufe - Kopf-/Fußzeile: Name, Präparate-Nummer,
Leitfaden: Protokoll Routinestufe Musterprotokoll: OC-Website, Informationen für Studierende, F-Praktikum, Vordrucke und Formulare, Musterprotokoll_Routinestufe - Kopf-/Fußzeile: Name, Präparate-Nummer,
Synthese von Acetophenon
 Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
Illumina-Chemie.de - Artikel Synthesen Synthese von Geräte: 250 ml Zweihalskolben, Claisenaufsatz, 50 ml Tropftrichter mit Druckausgleich, Rückflusskühler, Eisbad, Trockenrohr, Thermometer, Magnetrührer,
1024 Eliminierung von Wasser aus 4-Hydroxy-4-methyl-2- pentanon
 0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
0 Eliminierung von Wasser aus -Hydroxy--methyl-- pentanon H I H H H H - H H + H H H H H I H 0 (.) (.8) (98.) Klassifizierung Reaktionstypen und Stoffklassen Eliminierung Alkohol, Alken, Keton, Säurekatalysator
1017 Azokupplung von Benzoldiazoniumchlorid mit 2-Naphthol zu 1-Phenylazo-2-naphthol
 OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
OP 1017 Azokupplung von Benzoldiazoniumchlorid mit 2-aphthol zu 1-Phenylazo-2-naphthol H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5 Cl 2 (140.6) C
1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid
 1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
1004 Nitrierung von Pyridin-N-oxid zu 4-Nitropyridin-N-oxid O N HNO 3 /H 2 SO 4 O N NO 2 C 5 H 5 NO (95.1) (63.0) (98.1) C 5 H 4 N 2 O 3 (140.1) Klassifizierung Reaktionstypen und Stoffklassen Elektrophile
Protokoll zum Gruppenpräparat Versuch / 8.5
 Protokoll zum Gruppenpräparat Versuch 3.3.2.2 / 8.5 Organisch-chemisches Praktikum 2 Julius-Maximilians-Universität Würzburg Fakultät für Chemie und Pharmazie Vorgelegt von: Julian Koeller, Carl Schiller,
Protokoll zum Gruppenpräparat Versuch 3.3.2.2 / 8.5 Organisch-chemisches Praktikum 2 Julius-Maximilians-Universität Würzburg Fakultät für Chemie und Pharmazie Vorgelegt von: Julian Koeller, Carl Schiller,
