4.2. Kohlenhydrate Aufbau und Bedeutung Physikalische Eigenschaften Stereoisomerie und Fischer-Projektion
|
|
|
- Hajo Brauer
- vor 8 Jahren
- Abrufe
Transkript
1 4.. Kohlenhydrate 4... Aufbau und Bedeutung Kohlenhydrate bilden mengenmäßig den größten Teil der auf der Erde vorkommenden organischen Naturstoffe. Neben Kohlenstoffatomen enthalten die meisten Kohlenhydrate Wasserstoffatome und Sauerstoffatome im Zahlenverhältnis :, ihre Summenformel ist daher n (H ) m. Diese Zusammensetzung führte zu der historisch bedingten Bezeichnung Kohlenhydrate". Kohlenhydrate dienen in Pflanzen (Stärke) und Tieren (Glykogen) als Energiespeicher. In Pflanzen und Insekten sind Kohlenhydrate außerdem wichtige Gerüstsubstanzen. Die Biosynthese der Kohlenhydrate erfolgt in Pflanzen durch die endotherme Photosynthese aus Kohlenstoffdioxid und Wasser. Die dazu benötigte Energie wird in Form von Licht zugeführt. Im tierischen rganismus werden die als Nahung aufgenommenen pflanzlichen Kohlenhydrate durch die exotherme Atmung (Glykolyse, itratzyklus und Atmungskette) wieder zu Kohlenstoffdioxid und Wasser abgebaut. Die dabei freiwerdende Energie wird für die Muskelarbeit, die Aufrechterhaltung der Körpertemperatur und die Biosynthese körpereigener Verbindungen bereitgestellt: hemisch gesehen sind Kohlenhydrate Polyhydroxylcarbonylverbindungen. Das häufigste und wichtigste Beispiel ist Traubenzucker (, R, 3S, 4R, R-Pentahydroxy- Hexanal bzw.d-glucose) H Übungen: Aufgaben zu Kohlenhydraten Aufgabe D-Glucose 4... Physikalische Eigenschaften Zucker und Mehl erhitzen, Zucker und Stärke in Wasser lösen Die Polarität der H-Bindung führt zu starken zwischenmolekularen Kräften (Wasserstoffbrücken) zwischen Molkülen mit Hydroxylgruppen. Die Anziehung von Polyhydroxycarbonylverbindungen untereinander führt zu hohen Schmelz- und Siedepunkten; Die meisten Zucker zersetzen sich schon beim Schmelzvorgang an der Luft. Die Anziehung zwischen Polyhydroxycarbonylverbindungen und Wasser führt zu der extrem guten Löslichkeit und dem hohen Wasserbindungsvermögen dieser Stoffe. Beispiele: Viskosität bei Glycerin und Honig, Glycerin als Feuchtigkeitsspeicher in remes, Stärkekleister, Gelbildung beim Kochen von Marmelade Stereoisomerie und Fischer-Projektion (Wiederholung: siehe... Stereoisomerie und Fischer-Projektion bei Halogenalkanen) Übungen: Aufgaben zu Kohlenhydraten Aufgabe
2 4..4. Polarimetrie Glucose-Lösung in Standzylinder mit zwei Polarisationsfolien auf P (Vorsicht!) betrachten hirale Verbindungen lassen sich durch ihre Verhalten gegenüber linear polarisiertem Licht charakterisieren. Linear polarisiertes Licht lässt sich z. B. durch Polarisationsfolien erzeugen, die aus parallel angeordneten Makromolekülen aufgebaut sind. Es wird nur solches Licht durchgelassen, dessen Schwingungsebene parallel zur Vorzugsrichtung der Moleküle in der Folie ist. (siehe rechts) Jedes asymmetrische -Atom dreht die Schwingungsebene des Lichtes um einen kleinen Winkel nach rechts (+) oder links ( ), der charakteristisch für dieses Atom ist. Je mehr asymmetrische -Atome das Licht auf seinem Weg durch die Lösung passiert, desto stärker wird die Schwingungsebene gedreht. Der Drehwinkel ist also proportional zur Konzentration c der asymmetrischen -Atome in der Lösung und zum Weg l, den das Licht durch die Lösung zurücklegt. Den Proportionalitätsfaktor [α] 0 D (siehe unten) bezieht man praktischerweise nicht auf einzelne asymmetrische -Atome, sonder auf die ganzen Moleküle wie z.b. D-Glucose, die eine charakteristische Kombination aus 4 asymmetrischen -Atomen enthält. Zur Messung des Drehwinkels verwendet man ein Polarimeter, das aus einer Natriumlampe als monochromatischer Lichtquelle, einem Polarisator zur Herstellung von linear polarisiertem Licht, einer Messzelle und einem Analysator zur Messung des Drehwinkels besteht. Wenn der Analysator α parallel zum Polarisator steht, gelangt das linear polarisierte Licht in das Auge des Betrachters. Steht jedoch der Analysator senkrecht zum Polarisator, so findet eine Auslöschung statt. Bringt man in dieser Stellung des Analysators die Lösung einer optisch aktiven Substanz in den Strahlengang zwischen Polarisator und Analysator, so tritt eine Aufhellung ein, weil die Ebene des polarisierten Lichtes gedreht wird. Der Drehwinkel wird dadurch gemessen, dass λ man den Analysator so weit dreht, bis wieder Auslöschung eintritt. Der Drehwert einer optisch aktiven Lösung ist proportional zur Konzentration c der Probelösung in g/cm 3 = g/ml und zur Länge l der Messzelle in dm (!): α = [α] D 0 c l, Der Proportionalitätsfaktor [α] 0 D der Einheit cm 3 g dm heißt spezifischer Drehwert und bezieht sich auf monochromatisches Licht der Wellenlänge = 89 nm, das von der D-Linie des Linienspektrums einer Natriumdampflampe erzeugt wird und eine Temperatur T = 0. α Übungen: Aufgaben zu Kohlenhydraten Aufgaben Keto-Enol-Tautomerie (siehe..3. Aldehyde und Ketone/ Keto-Enol-Tautomerie) Übungen: Aufgaben zu Kohlenhydraten Aufgabe 4... Nukleophile Addition an arbonylverbindungen (siehe..4. Aldehyde und Ketone/ Nukleophile Addition an die =-Doppelbindung) Übungen: Aufgaben zu Kohlenhydraten Aufgabe 7
3 4..7. Monosaccharide Kettenform der Monosaccharide Die einfachsten Kohlenhydrate sind die Monosaccharide, sie lassen sich nicht weiter hydrolytisch in kleinere Kohlenhydrat-Einheiten spalten. Kohlenhydrate, die bei der Hydrolyse in bis 0 Monosaccharid-Einheiten zerlegt werden, bezeichnet man als ligosaccharide. Polysaccharide sind Makromoleküle, die aus einigen tausend Monosaccharid-Einheiten aufgebaut sein können. Mono- und ligosaccharide werden auch als Zucker bezeichnet. Ihre Namen haben in der Regel die Endung -ose. Monosaccharide sind Polyhydroxylcarbonylverbindungen. Neben alkoholischen -Gruppen enthält jedes Molekül eine Aldehydgruppe oder eine Ketogruppe. Man unterscheidet daher Aldosen und Ketosen. Nach der Anzahl der -Atome im Molekül unterscheidet man außerdem Triosen, Tetrosen, Pentosen, Hexosen und Heptosen. D-Aldosen im Überblick D-Ketosen im Überblick Übungen: Aufgaben zu Kohlenhydraten Aufgabe 8 3
4 Gleichgewicht zwischen Ketten- und Ringformen der Glucose und Fructose in wässrigen Lösungen H H + / - H + / - H H H H + / - H + / - Halbacetal α-d-glucopyranose aus Ethanol Fp 47 [α] D 0 = +, ml g - dm - in Wasser 3 % Anteil Aldehyd + Alkohol: D-Glucose [α] D 0 = + ml g dm Halbacetal β-d-glucopyranose aus Eisessig Fp 0 [α] D 0 = +8,7 ml g - dm - in Wasser 4 % Anteil Aldehyd-Endiol-Keton-Tautomerie katalysiert durch H + (z.b. im Magen) oder - (z.b. in Fehling- oder Tollens-Lösung) H H H H + / - H + / - H + / - H + / - Halbacetal: α-d-fructopyranose bisher nicht isoliert Anteil in Wasser unbekannt Keton + Alkohol: D-Fructose [α] D 0 = 9 ml g dm Halbacetal: β-d-fructopyranose aus Aceton [a] D 0 = 33, ml g dm Anteil in Wasser unbekannt H α: -Gruppe des Halbacetals nach unten β: -Gruppe des Halbacetals nach oben -furanose: -Ring wie in Furan: -pyranose: -Ring wie in Pyran: H H + / - H + / - Halbacetal: β-d-fructofuranose Anteil in Wasser unbekannt Übungen: Aufgaben zu Kohlenhydraten Aufgabe 9 4
5 4..8. xidation der Monosaccharide Fehling-Test mit Glucose und Fructose Wiederholung Fehling-Reaktion: siehe... Aldehyde und Ketone/ Mechanismus der Fehling-Reaktion Die freie Aldehydgruppe der Kettenform lässt sich durch schwache xidationsmittel wie z.b. Ag + (Tollens) oder u + (Fehling) zur arboxylgruppe oxidieren. Die dabei entstehenden Säuren heißen -onsäuren wie z.b. Gluconsäure. Bei Anwesenheit des Enzyms Glucoseoxidase aus dem Schimmelpilz penicillium notatum ist diese xidation auch durch Luftsauerstoff möglich. Wird die Aldehydgruppe z.b. durch Bildung eines Vollacetals mit dem Nucleotid Uridin geschützt, so lässt sich die endständige Hydroxylgruppe oxidieren. Die dabei entstehenden Säuren nennt man -uronsäuren wie z.b. Glucuronsäure, die bei der Entgiftung von Schadstoffen in der Leber eine wichtige Rolle spielt. Durch stärkere xidationsmittel wie z.b. heißes u oder längere Einwirkung von Luftsauerstoff werden beide Gruppen oxidiert und man erhält Zuckersäuren wie z.b. Glucosesäure. H + H H α-d-glucopyranose - /H + H-Uridin H H D-Glucose -Uridin (Glucoseoxidase) 4 NAD + + H 4 NADH + 4 H + H H D-Gluconsäure H 0, H (Luftsauerstoff) H D-Glucosesäure H H-Uridin Uridin-Glucose D-Glucuronsäure Vergleicht man die Geschwindigkeit der Reaktion mit Fehling-Lösung bei Ethanal, Glucose und Fructose, so reagiert Fructose am schnellsten und Ethanal am langsamsten. Bei der Untersuchung der Reaktionsprodukte stellt man fest, dass die Ansätze mit Fructose und Glucose nicht nur Gluconsäure, sondern auch Dicarbonylverbindungen enthalten. Hydroxylgruppen in Nachbarschaft zu arbonylgruppen lassen sich also noch leichter oxidieren als Aldehydgruppen! Beispiel: Reaktion von Fructose mit Fehling: - /H + - /H + H u u + H β-d-fructopyranose D-Fructose (Fehling),4,,-Tetrahydroxohexandion-,3 Daneben findet in Fehling-Lösung natürlich auch die Umwandlung in Glucose durch Tautomerie und xidation zu Gluconsäure statt. Übungen: Aufgaben zu Kohlenhydraten Aufgaben 0 und Identifizierung der Monosaccharide GD- und Seliwanoff-Test jeweils mit Fructose und Glucose Fehling-Test: Basische Lösung von u + -Ionen werden durch primäre arbonylgruppen und Hydroxylgruppen in Nachbarschaft zu arbonylgruppen zu roten u reduziert.
6 Tollens-Test: Basische Lösungen von Ag + -Ionen werden durch primäre arbonylgruppen und Hydroxylgruppen in Nachbarschaft zu arbonylgruppen zu schwarzem Ag reduziert. Seliwanoff-Test: Eine salzsaure Lösung von Resorcin (,3-Dihydroxybenzol) bildet mit Fructose einen roten Farbstoff. Se -Test: Eine neutrale Lösung von Natriumselenit (Na-Salz der Selensäure H Se 3 ) wird durch Fructose zu rotem Selen reduziert. GD-Test: Das Enzym Glucoseoxidase (GD) katalysiert die xidation von Glucose zu Glucuronsäure durch Luftsauerstoff. Dabei entsteht H, das eine weitere organische Verbindung zu einem roten Farbstoff oxidiert. Dünnschichtchromatografie (vgl. Praktikumsversuch) Polarimetrie: (vgl ) Übungen: Aufgaben zu Kohlenhydraten Aufgabe Experimente mit Monosacchariden Disaccharide Wiederholung Nukleophile Addition an Alkoholen und Ethern, siehe... Bildung von Vollacetalen, siehe..4. Monosaccharide können als Halbacetale mit Alkoholen unter Abspaltung von Wasser zu Acetalen reagieren. Solche Zuckeracetale bezeichnet man allgemein als Glykoside. Je nach Monosaccharid spricht man von Glucosiden, Fructosiden, Galactosiden usw. In der Regel liegt das Gleichgewicht dieser Reaktionen auf der Seite der Hydrolyseprodukte Monosaccharid und Alkohol. In Gegenwart von hlorwasserstoff, das als Katalysator wirkt und gleichzeitig das freiwerdende Wasser bindet, läßt sich jedoch Glucose mit Methanol zu einem Gemisch der anomeren Glykoside α-methylglucosid und β-methylglucosid umsetzen. In Glykosiden bezeichnet man das ursprüngliche arbonyl--atom als glykosidisches -Atom und die von diesem Atom zum Alkohol ausgehende -Bindung als glykosidische Bindung. Wie alle Acetale sind auch Glykoside gegenüber Basen stabil. Vergleich der vier Disaccharide mit Geschmackstest (Süßkraft) Beispiele Maltose (Malzzucker) 4-(α-D-Glucopyranosyl)-D-glucopyranose ellobiose (Dimer der elluolse) 4-(β-D-Glucopyranosyl)-D-glucopyranose Saccharose (Rohrzucker) -(α-d-glucooopyranosyl)--β-d-fructofuranosid Lactose (Milchzucker) 4-(β-D-Galactoopyranosyl)-D-glucopyranose
7 Eigenschaften Fehling-Test mit Maltose und Saccharose mit und ohne vorherige Hydrolyse durch HL (anschließende Neutralisation mit Soda nicht vergessen!) Alle Disaccharide sind durch Vollacetale verknüpft und lassen sich daher in saurer Lösung hydrolytisch spalten. In neutraler und basischer Lösung sind sie stabil. Maltose, ellobiose und Lactose enthalten ein Halbacetal, das in saurer und basischer Lösung mit der offenkettigen Aldehydform im Gleichgewicht steht. Diese Disaccharide reagieren daher mit Fehling- und Tollens-Reagenz und heißen reduzierende Zucker. In der Saccharose sind beide Halbacetale an der Bildung des Vollacetals beteiligt. Da das Vollacetal nur durch Säuren gespalten wird, reagiert Saccharose mit den basischen Fehling- und Tollens Lösungen nicht. Es handelt sich um einen nichtreduzierenden Zucker. Bei der sauren Hydrolyse von Saccharose wechselt die Drehung des polarisierten Lichtes ihrer Richtung. Das Hydrolysat wird daher auch Invertzucker genannt: H + H H + H Saccharose D-Glucose + D-Fructose [α] 0 D = +, [α] 0 D = +,7 [α] 0 D = 9,4 Übungen: Aufgaben zu Kohlenhydraten Aufgaben 4 8 Experimente mit Di- und Polysacchariden 4... Polysaccharide Beispiele und Eigenschaften [α] D 0 = 0,9 Lugolsche Lösung mit Stärke, Stärke in heißem und kaltem Wasser, Tyndall-Effekt Polysaccharid Amylose Amylopektin Glykogen Pektin ellulose hitin Vorkommen Stärkekörner der Stärkekörner der Leber Früchte der Pflanzen Blätter der Panzer der Pflanzen (innen) Pflanzen (außen) Pflanzen Insekten, Algen Funktion Energiespeicher Gerüstsubstanz Energiespeicher Gerüstsubstanz Gerüstsubstanz Gerüstsubstanz Primär- α-,4 D-Glucose α-,4 D-Glucose α-,4 D-Glucose α-,4 D-Galacturon- β-,4 D-Glucose β-,4 N-acetylstruktur (00 E) (000 E) ( E) säure, zu 70% mit (3000 E) D--glucosamin unverzweigt mehrfach α-,- einfach α-,- Methanol verestert unverzweigt (00 E) verzweigt ( E) verzweigt (0 E) (000 E) unverzweigt unverzweigt Sekundär- Helix - - Faltblatt Fibrillen? (*) struktur in kaltem Gel - - Gel - - Wasser in heißem Wasser Kolloid Gel Gel Kolloid - - (*) Bei der Verpuppung und Häutung den Insekten besteht die Haut zunächst aus reinem elastischen hitin. Sobald die Haut ihre endgültige Form erreicht hat, wird sie durch Bildung von Skleroproteinen (Vgl. Haare und Nägel) ausgehärtet. Im Gegensatz zu der sehr ähnlichen ellulose kann hitin auch von höheren Tieren wie z.b. Schnecken verdaut werden. Nachweis von Amylose mit Iod-Kaliumiodid-Lösung (Lugolsche Lösung) Bei Anwesenheit von Iod und Iodidionen bilden sich Polyiodidionen wie z.b. I 3 und I, die in den Hohlraum der Helix eingelagert werden und sich dabei tiefblau färben. Löslichkeitseigenschaften der Stärke. Stärke ist eine weiße, geruch- und geschmacklose Substanz, die in kaltem Wasser unlöslich ist. Bei etwa 0 quillt Stärke in Wasser unter Bildung von Stärkekleister auf. Im Gegensatz zur klaren Lösung (Sol von Solution) bezeichnet man Feststoffe, die durch Flüssigkeitsaufnahme erweicht und gequollen sind, als Gel. In heißem Wasser geht ein Massenanteil von etwa 0 % kolloidal (s.u.) in Lösung. Der lösliche Bestandteil der Stärke wird wird als Amylose, der wasserunlösliche Anteil als Amylopektin bezeichnet. 7
8 Kolloidale Lösungen Als Kolloide bezeichnet man Teilchen, deren Durchmesser zwischen nm und 000 nm liegt. Eine kolloiddisperse oder kolloidale Lösung hat im Vergleich zu einer molekulardispersen, echten Lösung, in der die gelösten Teilchen kleiner als nm sind, und einer grobdispersen Suspension, in der die Teilchen größer als 000 nm sind, besondere Eigenschaften. Zur Erkennung von solchen kolloidalen Lösungen, die mit dem Auge nicht von echten Lösungen zu unterscheiden sind, eignet sich besonders der Tyndall-Effekt: Ein durch eine kolloidale Lösung tretendes Lichtbündel ist bei seitlicher Betrachtung als leuchtende Trübung zu erkennen. Dieser Effekt, der sich auch bei Sonnenstrahlen in staubiger Luft beobachten läßt, beruht auf der Streuung von Licht. Da Teilchen, die viel kleiner sind als die Wellenlänge von Licht, die geradlinige Ausbreitung von Licht nicht beeinflussen, zeigen echte Lösungen keinen Tyndall -Effekt. Übungen: Aufgaben zu Kohlenhydraten Aufgaben 8 und 9 Experimente zu Karamelisierung und Maillard-Reaktion 8
Material zur Vorbereitung der Prüfung im Fach Chemie
 Material zur Vorbereitung der Prüfung im Fach Chemie 1 Empfohlene Literatur Duden Basiswissen Schule: Abitur Chemie Schulbücher für die Sekundarstufe II: - Chemie im Kontext, CVK Verlag - Elemente Chemie
Material zur Vorbereitung der Prüfung im Fach Chemie 1 Empfohlene Literatur Duden Basiswissen Schule: Abitur Chemie Schulbücher für die Sekundarstufe II: - Chemie im Kontext, CVK Verlag - Elemente Chemie
Organische Chemie I Chemie am 16.11.2012. Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2
 Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Organische Chemie I Inhaltsverzeichnis Lewisformeln von Kohlenstoffverbindungen korrekt zeichnen!... 2 Verstehen was Organische Chemie heisst und die Entstehung von Kohlenstoffverbindungen kennen!... 2
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Chemie der Kohlenhydrate
 Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Chemie der Kohlenhydrate Grundlegendes Der Begriff Kohlenhydrate: Wurde ursprünglich aus der Formel für Glukose abgeleitet. C 6 H 12 O 6 = C 6 (H 2 O) 6 Bzw. allgemein: C n (H 2 O) m Diese missleitende
Spektroskopie. im IR- und UV/VIS-Bereich. Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) http://www.analytik.ethz.
 Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Kohlenhydrate (Zucker)
 Kohlenhydrate (Zucker) allgemein (früher): C n (H 2 O) n heute: Fischer-Projektions-Formel (FPF) Glucose: C 6 H 12 O 6 Glucose ist ein Polyhydroxyaldehyd (eine Aldose). Das beruht auf der Carbonyl- und
Kohlenhydrate (Zucker) allgemein (früher): C n (H 2 O) n heute: Fischer-Projektions-Formel (FPF) Glucose: C 6 H 12 O 6 Glucose ist ein Polyhydroxyaldehyd (eine Aldose). Das beruht auf der Carbonyl- und
Kohlenhydrate und ihre Funktionen
 Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Kohlenhydrate und ihre Funktionen Gliederung Monosaccharide Aufbau Nomenklatur Stereoisomerie/Konfiguration Zyklisierung O-glykosidische Bindung N-glykosidische Bindung Disaccharide Kohlenhydrate im Überblick
Optik: Teilgebiet der Physik, das sich mit der Untersuchung des Lichtes beschäftigt
 -II.1- Geometrische Optik Optik: Teilgebiet der, das sich mit der Untersuchung des Lichtes beschäftigt 1 Ausbreitung des Lichtes Das sich ausbreitende Licht stellt einen Transport von Energie dar. Man
-II.1- Geometrische Optik Optik: Teilgebiet der, das sich mit der Untersuchung des Lichtes beschäftigt 1 Ausbreitung des Lichtes Das sich ausbreitende Licht stellt einen Transport von Energie dar. Man
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
PCD Europe, Krefeld, Jan 2007. Auswertung von Haemoccult
 Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Auswertung von Haemoccult Ist das positiv? Nein! Ja! Im deutschen Krebsfrüherkennungsprogramm haben nur etwa 1 % der Frauen und 1,5 % der Männer ein positives Haemoccult -Ergebnis, da dieser Test eine
Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015
 Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015 Name: Vorname: Matrikel-Nr.: geborenam: in: Wiederholer dieser Klausur:
Studiengang Biowissenschaften Modulbegleitende Prüfung zum Praktikum in Organischer Chemie (gemäß MPO vom 12.09.2005) 21.07.2015 Name: Vorname: Matrikel-Nr.: geborenam: in: Wiederholer dieser Klausur:
Licht und Farbe - Dank Chemie!
 Licht und Farbe - Dank Chemie! Folie 1 Was verstehen wir eigentlich unter Licht? Licht nehmen wir mit unseren Augen wahr Helligkeit: Farbe: Schwarz - Grau - Weiß Blau - Grün - Rot UV-Strahlung Blau Türkis
Licht und Farbe - Dank Chemie! Folie 1 Was verstehen wir eigentlich unter Licht? Licht nehmen wir mit unseren Augen wahr Helligkeit: Farbe: Schwarz - Grau - Weiß Blau - Grün - Rot UV-Strahlung Blau Türkis
α- und β- Glucose können sich ineinander umwandeln
 Die Reaktionen der Zucker Zuckermoleküle können in verschiedenen Formen auftreten Zuckermoleküle zeigen, da sie in verschiedenen Formen auftreten können, ungewöhnliche Eigenschaften. Da diese auch für
Die Reaktionen der Zucker Zuckermoleküle können in verschiedenen Formen auftreten Zuckermoleküle zeigen, da sie in verschiedenen Formen auftreten können, ungewöhnliche Eigenschaften. Da diese auch für
REAKTIONEN BIOORGANISCHER VERBINDUNGEN. Lipide
 REAKTINEN BIRGANISHER VERBINDUNGEN Lipide Triglyceride Die Fette sind die Ester von langkettigen Fettsäuren und Glycerin (Triglyceride, oder Triacylglycerine). Die Öle enthalten ungesättigte langkettige
REAKTINEN BIRGANISHER VERBINDUNGEN Lipide Triglyceride Die Fette sind die Ester von langkettigen Fettsäuren und Glycerin (Triglyceride, oder Triacylglycerine). Die Öle enthalten ungesättigte langkettige
Lerntext Pflanzen 1. Was sind Pflanzen?
 Was sind Pflanzen? Lerntext Pflanzen 1 Pleurotus_ostreatus Ausschnitt eines Photos von Tobi Kellner, das er unter der Lizenz CC BY-SA 3.0 zur Verfügung stellte Der Körper eines Pilzes ist ein Fadengeflecht
Was sind Pflanzen? Lerntext Pflanzen 1 Pleurotus_ostreatus Ausschnitt eines Photos von Tobi Kellner, das er unter der Lizenz CC BY-SA 3.0 zur Verfügung stellte Der Körper eines Pilzes ist ein Fadengeflecht
Katalysatoren - Chemische Partnervermittlung im virtuellen Labor
 Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
BROTTEIG. Um Brotteig zu machen, mischt ein Bäcker Mehl, Wasser, Salz und Hefe. Nach dem
 UNIT BROTTEIG BROTTEIG Um Brotteig zu machen, mischt ein Bäcker Mehl, Wasser, Salz und Hefe. Nach dem Mischen wird der Teig für mehrere Stunden in einen Behälter gegeben, um den Gärungsprozess zu ermöglichen.
UNIT BROTTEIG BROTTEIG Um Brotteig zu machen, mischt ein Bäcker Mehl, Wasser, Salz und Hefe. Nach dem Mischen wird der Teig für mehrere Stunden in einen Behälter gegeben, um den Gärungsprozess zu ermöglichen.
Chemische Reaktionen
 Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
Ein paar Worte zuvor 7 Stoffe und ihre Eigenschaften 1 Reine Stoffe und Gemische 10 2 Aggregatzustände, Dichte, Löslichkeit, Brennbarkeit und Leitfähigkeit 12 3 Trennverfahren 19 Auf einen Blick: Stoffe
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Polarisation des Lichts
 PeP Vom Kerzenlicht zum Laser Versuchsanleitung Versuch 4: Polarisation des Lichts Polarisation des Lichts Themenkomplex I: Polarisation und Reflexion Theoretische Grundlagen 1.Polarisation und Reflexion
PeP Vom Kerzenlicht zum Laser Versuchsanleitung Versuch 4: Polarisation des Lichts Polarisation des Lichts Themenkomplex I: Polarisation und Reflexion Theoretische Grundlagen 1.Polarisation und Reflexion
2.8 Grenzflächeneffekte
 - 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
- 86-2.8 Grenzflächeneffekte 2.8.1 Oberflächenspannung An Grenzflächen treten besondere Effekte auf, welche im Volumen nicht beobachtbar sind. Die molekulare Grundlage dafür sind Kohäsionskräfte, d.h.
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Chemie Zusammenfassung KA 2
 Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Chemie Zusammenfassung KA 2 Wärmemenge Q bei einer Reaktion Chemische Reaktionen haben eine Gemeinsamkeit: Bei der Reaktion wird entweder Energie/Wärme frei (exotherm). Oder es wird Wärme/Energie aufgenommen
Festigkeit von FDM-3D-Druckteilen
 Festigkeit von FDM-3D-Druckteilen Häufig werden bei 3D-Druck-Filamenten die Kunststoff-Festigkeit und physikalischen Eigenschaften diskutiert ohne die Einflüsse der Geometrie und der Verschweißung der
Festigkeit von FDM-3D-Druckteilen Häufig werden bei 3D-Druck-Filamenten die Kunststoff-Festigkeit und physikalischen Eigenschaften diskutiert ohne die Einflüsse der Geometrie und der Verschweißung der
Gitterherstellung und Polarisation
 Versuch 1: Gitterherstellung und Polarisation Bei diesem Versuch wollen wir untersuchen wie man durch Überlagerung von zwei ebenen Wellen Gttterstrukturen erzeugen kann. Im zweiten Teil wird die Sichtbarkeit
Versuch 1: Gitterherstellung und Polarisation Bei diesem Versuch wollen wir untersuchen wie man durch Überlagerung von zwei ebenen Wellen Gttterstrukturen erzeugen kann. Im zweiten Teil wird die Sichtbarkeit
Würfelt man dabei je genau 10 - mal eine 1, 2, 3, 4, 5 und 6, so beträgt die Anzahl. der verschiedenen Reihenfolgen, in denen man dies tun kann, 60!.
 040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
040304 Übung 9a Analysis, Abschnitt 4, Folie 8 Die Wahrscheinlichkeit, dass bei n - maliger Durchführung eines Zufallexperiments ein Ereignis A ( mit Wahrscheinlichkeit p p ( A ) ) für eine beliebige Anzahl
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren
 Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
Lineargleichungssysteme: Additions-/ Subtraktionsverfahren W. Kippels 22. Februar 2014 Inhaltsverzeichnis 1 Einleitung 2 2 Lineargleichungssysteme zweiten Grades 2 3 Lineargleichungssysteme höheren als
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Lernpaket 3: Monosaccharide
 Lernpaket 3: Monosaccharide Saccharide Bei der Photosynthese werden aus Wasser und Kohlendioxid unter Freisetzung von Sauerstoff Kohlenhydrate (Zucker, Saccharide 1 ) hergestellt. Sie enthalten Kohlenstoff,
Lernpaket 3: Monosaccharide Saccharide Bei der Photosynthese werden aus Wasser und Kohlendioxid unter Freisetzung von Sauerstoff Kohlenhydrate (Zucker, Saccharide 1 ) hergestellt. Sie enthalten Kohlenstoff,
PO Doppelbrechung und elliptisch polarisiertes Licht
 PO Doppelbrechung und elliptisch polarisiertes Licht Blockpraktikum Herbst 27 (Gruppe 2b) 24. Oktober 27 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Polarisation.................................. 2 1.2 Brechung...................................
PO Doppelbrechung und elliptisch polarisiertes Licht Blockpraktikum Herbst 27 (Gruppe 2b) 24. Oktober 27 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Polarisation.................................. 2 1.2 Brechung...................................
COOH. Die Aminosäuren tragen laborübliche Abkürzungen, so stehen z. B. Gly für Glycin oder Phe für Phenylalanin.
 Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
Aminosäuren 1. Textentwurf Allgemeine Formel der Aminosäuren Aminosäuren sind die Grundbestandteile der Proteine. Neben der -Gruppe 1 enthalten sie als charakteristisches Merkmal die Aminogruppe N. Zwei
EINE KERZE INTERPRETATIONEN BEOBACHTUNGEN FLAMME REAKTIONEN WACHS DOCHT GASE. Reaktionsgleichungen Prozesse. Theorien
 Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Hydrierung von Kohlenmonoxid zu Methanol Kataly?sche Umsetzung von Ethen mit Wasser zu Ethanol
 Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Experimentiersatz Elektromotor
 Experimentiersatz Elektromotor Demonstration der Erzeugung von elektrischem Stromfluss durch Umwandlung von mechanischer Energie (Windrad) in elektrische Energie. Einführung Historisch gesehen hat die
Experimentiersatz Elektromotor Demonstration der Erzeugung von elektrischem Stromfluss durch Umwandlung von mechanischer Energie (Windrad) in elektrische Energie. Einführung Historisch gesehen hat die
Organische Moleküle. Verschiedene Ansichten des Methans
 Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Organische Räumlicher Bau, Elektronendichteverteilungen Verschiedene Ansichten des Methans Ansicht des Methans mit seiner Elektronenhülle (Solid-Darstellung) Ansicht des Methans mit seiner Elektronenhülle
Theoretische Grundlagen Physikalisches Praktikum. Versuch 12: Fotometrie und Polarimetrie
 Theoretische Grundlagen Physikalisches Praktikum Versuch 12: Fotometrie und Polarimetrie Licht als elektromagnetische Welle sichtbares Licht ist eine elektromagnetische Welle andere elektromagnetische
Theoretische Grundlagen Physikalisches Praktikum Versuch 12: Fotometrie und Polarimetrie Licht als elektromagnetische Welle sichtbares Licht ist eine elektromagnetische Welle andere elektromagnetische
Homologe Reihe. Alkane. Alkene. Alkine
 GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
GW Chemie 8.-10. NTG GA omologe eihe eihung von Stoffen, deren Moleküle sich durch eine sich wiederholende Einheit unterscheiden. Bsp.: Methan Ethan Propan Butan usw. unterscheiden sich durch je eine C
Professionelle Seminare im Bereich MS-Office
 Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Der Name BEREICH.VERSCHIEBEN() ist etwas unglücklich gewählt. Man kann mit der Funktion Bereiche zwar verschieben, man kann Bereiche aber auch verkleinern oder vergrößern. Besser wäre es, die Funktion
Die Sch. kennen die Zusammensetzung von Luft und können die verschiedenen Gase per Formel benennen.
 Anleitung LP Ziel: Die Sch. kennen die Zusammensetzung von Luft und können die verschiedenen Gase per Formel benennen. Arbeitsauftrag: Textblatt lesen lassen und Lücken ausfüllen mit Hilfe der zur Verfügung
Anleitung LP Ziel: Die Sch. kennen die Zusammensetzung von Luft und können die verschiedenen Gase per Formel benennen. Arbeitsauftrag: Textblatt lesen lassen und Lücken ausfüllen mit Hilfe der zur Verfügung
Abgestufte Lernhilfen
 Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Lichtbrechung an Linsen
 Sammellinsen Lichtbrechung an Linsen Fällt ein paralleles Lichtbündel auf eine Sammellinse, so werden die Lichtstrahlen so gebrochen, dass sie durch einen Brennpunkt der Linse verlaufen. Der Abstand zwischen
Sammellinsen Lichtbrechung an Linsen Fällt ein paralleles Lichtbündel auf eine Sammellinse, so werden die Lichtstrahlen so gebrochen, dass sie durch einen Brennpunkt der Linse verlaufen. Der Abstand zwischen
Funktionelle Gruppen Alkohol
 Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Alkohol Unter Alkohol versteht man (als hemiker) alle Verbindungen, in denen eine ydroxyl-gruppe an ein aliphatisches oder alicyclisches Kohlenstoffgerüst gebunden ist. ydroxylgruppe: funktionelle Gruppe
Administratives BSL PB
 Administratives Die folgenden Seiten sind ausschliesslich als Ergänzung zum Unterricht für die Schüler der BSL gedacht (intern) und dürfen weder teilweise noch vollständig kopiert oder verbreitet werden.
Administratives Die folgenden Seiten sind ausschliesslich als Ergänzung zum Unterricht für die Schüler der BSL gedacht (intern) und dürfen weder teilweise noch vollständig kopiert oder verbreitet werden.
ORGANISCHE CHEMIE TEIL 2 ORGANISCHE SAUERSTOFFVERBINDUNGEN FMS
 KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN FMS Skript rganische Chemie 2 (FMS) V1.0 10/13 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole...
KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN FMS Skript rganische Chemie 2 (FMS) V1.0 10/13 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole...
SUPERABSORBER. Eine Präsentation von Johannes Schlüter und Thomas Luckert
 SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
2 Physikalische Eigenschaften von Fettsäuren: Löslichkeit, Dissoziationsverhalten, Phasenzustände
 2 Physikalische Eigenschaften von Fettsäuren: Löslichkeit, Dissoziationsverhalten, Phasenzustände Als Fettsäuren wird die Gruppe aliphatischer Monocarbonsäuren bezeichnet. Der Name Fettsäuren geht darauf
2 Physikalische Eigenschaften von Fettsäuren: Löslichkeit, Dissoziationsverhalten, Phasenzustände Als Fettsäuren wird die Gruppe aliphatischer Monocarbonsäuren bezeichnet. Der Name Fettsäuren geht darauf
1.1 Auflösungsvermögen von Spektralapparaten
 Physikalisches Praktikum für Anfänger - Teil Gruppe Optik. Auflösungsvermögen von Spektralapparaten Einleitung - Motivation Die Untersuchung der Lichtemission bzw. Lichtabsorption von Molekülen und Atomen
Physikalisches Praktikum für Anfänger - Teil Gruppe Optik. Auflösungsvermögen von Spektralapparaten Einleitung - Motivation Die Untersuchung der Lichtemission bzw. Lichtabsorption von Molekülen und Atomen
1 Mathematische Grundlagen
 Mathematische Grundlagen - 1-1 Mathematische Grundlagen Der Begriff der Menge ist einer der grundlegenden Begriffe in der Mathematik. Mengen dienen dazu, Dinge oder Objekte zu einer Einheit zusammenzufassen.
Mathematische Grundlagen - 1-1 Mathematische Grundlagen Der Begriff der Menge ist einer der grundlegenden Begriffe in der Mathematik. Mengen dienen dazu, Dinge oder Objekte zu einer Einheit zusammenzufassen.
Eine solche Anordnung wird auch Fabry-Pérot Interferometer genannt
 Interferenz in dünnen Schichten Interferieren die an dünnen Schichten reflektierten Wellen miteinander, so können diese sich je nach Dicke der Schicht und Winkel des Einfalls auslöschen oder verstärken
Interferenz in dünnen Schichten Interferieren die an dünnen Schichten reflektierten Wellen miteinander, so können diese sich je nach Dicke der Schicht und Winkel des Einfalls auslöschen oder verstärken
Beispiele zur Multiple-Choice Prüfung in OC
 1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
1 Beispiele zur Multiple-Choice Prüfung in C 10 Fragen Typ A Einfachauswahl Bezeichnen Sie nur eine Wahlantwort durch Umkreisen des betreffenden Buchstabens: - bei positiver Formulierung die einzig richtige
Kulturelle Evolution 12
 3.3 Kulturelle Evolution Kulturelle Evolution Kulturelle Evolution 12 Seit die Menschen Erfindungen machen wie z.b. das Rad oder den Pflug, haben sie sich im Körperbau kaum mehr verändert. Dafür war einfach
3.3 Kulturelle Evolution Kulturelle Evolution Kulturelle Evolution 12 Seit die Menschen Erfindungen machen wie z.b. das Rad oder den Pflug, haben sie sich im Körperbau kaum mehr verändert. Dafür war einfach
2) In welcher Einheit wird die Energie (x-achse) im NMR-Spektrum angegeben und wie ist sie definiert?
 Aufgabe 1: Verständnisfragen 1) Welche Eigenschaften eines Atomkerns führen zu einem starken NMR-Signal? (man sagt der Kern hat eine große Empfindlichkeit) Ein Isotop eines Elements wird empfindlich genannt,
Aufgabe 1: Verständnisfragen 1) Welche Eigenschaften eines Atomkerns führen zu einem starken NMR-Signal? (man sagt der Kern hat eine große Empfindlichkeit) Ein Isotop eines Elements wird empfindlich genannt,
Wie sieht unsere Welt im Kleinen aus?
 Skriptum Wie sieht unsere Welt im Kleinen aus? 1 Wie sieht unsere Welt im Kleinen aus? Atom- und Quantenphysik für Kids Seminar im Rahmen der KinderUni Wien, 12. 7. 2005 Katharina Durstberger, Franz Embacher,
Skriptum Wie sieht unsere Welt im Kleinen aus? 1 Wie sieht unsere Welt im Kleinen aus? Atom- und Quantenphysik für Kids Seminar im Rahmen der KinderUni Wien, 12. 7. 2005 Katharina Durstberger, Franz Embacher,
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Vortrag 2: Kohärenz VON JANIK UND JONAS
 Vortrag 2: Kohärenz VON JANIK UND JONAS Vortrag 2: Kohärenz Inhalt: Kohärenz im Allgemeinen Kohärenzlänge Kohärenzbedingungen Zeitliche Kohärenz Räumliche Kohärenz MICHELSON Interferometer zum Nachweis
Vortrag 2: Kohärenz VON JANIK UND JONAS Vortrag 2: Kohärenz Inhalt: Kohärenz im Allgemeinen Kohärenzlänge Kohärenzbedingungen Zeitliche Kohärenz Räumliche Kohärenz MICHELSON Interferometer zum Nachweis
Endstoffe (Produkte) Aus dem Reaktionsgemisch entweichendes Gas, z. B. 2 Welche Informationen kann man einer Reaktionsgleichung entnehmen?
 Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Reaktionsgleichungen Reaktionsgleichungen Blatt 1/5 1 Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen, also einen chemischen Prozeß. Auf der einen Seite steht,
Anleitung über den Umgang mit Schildern
 Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Anleitung über den Umgang mit Schildern -Vorwort -Wo bekommt man Schilder? -Wo und wie speichert man die Schilder? -Wie füge ich die Schilder in meinen Track ein? -Welche Bauteile kann man noch für Schilder
Wasserkraft früher und heute!
 Wasserkraft früher und heute! Wasserkraft leistet heute einen wichtigen Beitrag zur Stromversorgung in Österreich und auf der ganzen Welt. Aber war das schon immer so? Quelle: Elvina Schäfer, FOTOLIA In
Wasserkraft früher und heute! Wasserkraft leistet heute einen wichtigen Beitrag zur Stromversorgung in Österreich und auf der ganzen Welt. Aber war das schon immer so? Quelle: Elvina Schäfer, FOTOLIA In
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Selbst-Test zur Vorab-Einschätzung zum Vorkurs Chemie für Mediziner
 Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Liebe Studierende der Human- und Zahnmedizin, mithilfe dieses Tests können Sie selbst einschätzen, ob Sie den Vorkurs besuchen sollten. Die kleine Auswahl an Aufgaben spiegelt in etwa das Niveau des Vorkurses
Optik. Optik. Optik. Optik. Optik
 Nenne das Brechungsgesetz! Beim Übergang von Luft in Glas (Wasser, Kunststoff) wird der Lichtstrahl zum Lot hin gebrochen. Beim Übergang von Glas (Wasser...) in Luft wird der Lichtstrahl vom Lot weg gebrochen.
Nenne das Brechungsgesetz! Beim Übergang von Luft in Glas (Wasser, Kunststoff) wird der Lichtstrahl zum Lot hin gebrochen. Beim Übergang von Glas (Wasser...) in Luft wird der Lichtstrahl vom Lot weg gebrochen.
FRAGENKATALOG ERNÄHRUNGSWISSEN. Themenbereich KOHLENHYDRATE. im Rahmen des Projektes. ein Projekt der ARGE Gänseblümchen auf Vogerlsalat
 FRAGENKATALOG ERNÄHRUNGSWISSEN Themenbereich KOHLENHYDRATE im Rahmen des Projektes ein Projekt der ARGE Gänseblümchen auf Vogerlsalat Ernährungswissen KOHLENHYDRATE Seite 2 VORBEMERKUNG Für diesen Bereich
FRAGENKATALOG ERNÄHRUNGSWISSEN Themenbereich KOHLENHYDRATE im Rahmen des Projektes ein Projekt der ARGE Gänseblümchen auf Vogerlsalat Ernährungswissen KOHLENHYDRATE Seite 2 VORBEMERKUNG Für diesen Bereich
Zwischenablage (Bilder, Texte,...)
 Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
Zwischenablage was ist das? Informationen über. die Bedeutung der Windows-Zwischenablage Kopieren und Einfügen mit der Zwischenablage Vermeiden von Fehlern beim Arbeiten mit der Zwischenablage Bei diesen
14. Minimale Schichtdicken von PEEK und PPS im Schlauchreckprozeß und im Rheotensversuch
 14. Minimale Schichtdicken von PEEK und PPS im Schlauchreckprozeß und im Rheotensversuch Analog zu den Untersuchungen an LDPE in Kap. 6 war zu untersuchen, ob auch für die Hochtemperatur-Thermoplaste aus
14. Minimale Schichtdicken von PEEK und PPS im Schlauchreckprozeß und im Rheotensversuch Analog zu den Untersuchungen an LDPE in Kap. 6 war zu untersuchen, ob auch für die Hochtemperatur-Thermoplaste aus
GEVITAS Farben-Reaktionstest
 GEVITAS Farben-Reaktionstest GEVITAS Farben-Reaktionstest Inhalt 1. Allgemeines... 1 2. Funktionsweise der Tests... 2 3. Die Ruhetaste und die Auslösetaste... 2 4. Starten der App Hauptmenü... 3 5. Auswahl
GEVITAS Farben-Reaktionstest GEVITAS Farben-Reaktionstest Inhalt 1. Allgemeines... 1 2. Funktionsweise der Tests... 2 3. Die Ruhetaste und die Auslösetaste... 2 4. Starten der App Hauptmenü... 3 5. Auswahl
Aufgaben verändern Beispiele zur Chemie
 A2-2-2 Aufgaben verändern Beispiele zur Chemie 1 Aufgaben verändern Beispiele zur Chemie Die folgenden beiden Varianten einer Aufgabe zeigen exemplarisch, wie unterschiedlich Frage- und Aufgabenstellungen,
A2-2-2 Aufgaben verändern Beispiele zur Chemie 1 Aufgaben verändern Beispiele zur Chemie Die folgenden beiden Varianten einer Aufgabe zeigen exemplarisch, wie unterschiedlich Frage- und Aufgabenstellungen,
Protokoll des Versuches 7: Umwandlung von elektrischer Energie in Wärmeenergie
 Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 7: Umwandlung von elektrischer Energie in ärmeenergie Verantwortlicher
Name: Matrikelnummer: Bachelor Biowissenschaften E-Mail: Physikalisches Anfängerpraktikum II Dozenten: Assistenten: Protokoll des Versuches 7: Umwandlung von elektrischer Energie in ärmeenergie Verantwortlicher
Info zum Zusammenhang von Auflösung und Genauigkeit
 Da es oft Nachfragen und Verständnisprobleme mit den oben genannten Begriffen gibt, möchten wir hier versuchen etwas Licht ins Dunkel zu bringen. Nehmen wir mal an, Sie haben ein Stück Wasserrohr mit der
Da es oft Nachfragen und Verständnisprobleme mit den oben genannten Begriffen gibt, möchten wir hier versuchen etwas Licht ins Dunkel zu bringen. Nehmen wir mal an, Sie haben ein Stück Wasserrohr mit der
Bundesverband Flachglas Großhandel Isolierglasherstellung Veredlung e.v. U g -Werte-Tabellen nach DIN EN 673. Flachglasbranche.
 Bundesverband Flachglas Großhandel Isolierglasherstellung Veredlung e.v. U g -Werte-Tabellen nach DIN EN 673 Ug-Werte für die Flachglasbranche Einleitung Die vorliegende Broschüre enthält die Werte für
Bundesverband Flachglas Großhandel Isolierglasherstellung Veredlung e.v. U g -Werte-Tabellen nach DIN EN 673 Ug-Werte für die Flachglasbranche Einleitung Die vorliegende Broschüre enthält die Werte für
Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch. Reinstoff, Element, Verbindung. Zweiatomige Elemente.
 1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
1 1 Einteilung der Stoffe: Stoff, Reinstoff, Gemisch, homogenes Gemisch, heterogenes Gemisch Stoff Reinstoff Mischen Gemisch Bei gleichen Bedingungen (Temperatur, Druck) immer gleiche Eigenschaften (z.b.
Überprüfe alkoholhaltige Getränke mit Hilfe eines AlcoTest- Röhrchens.
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77800) 4.3 Alco-Test-Röhrchen Experiment von: Anouch Gedruckt: 25.02.204 3:44:30 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77800) 4.3 Alco-Test-Röhrchen Experiment von: Anouch Gedruckt: 25.02.204 3:44:30 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Michelson-Interferometer & photoelektrischer Effekt
 Michelson-Interferometer & photoelektrischer Effekt Branche: TP: Autoren: Klasse: Physik / Physique Michelson-Interferometer & photoelektrischer Effekt Cedric Rey David Schneider 2T Datum: 01.04.2008 &
Michelson-Interferometer & photoelektrischer Effekt Branche: TP: Autoren: Klasse: Physik / Physique Michelson-Interferometer & photoelektrischer Effekt Cedric Rey David Schneider 2T Datum: 01.04.2008 &
Erstellen von x-y-diagrammen in OpenOffice.calc
 Erstellen von x-y-diagrammen in OpenOffice.calc In dieser kleinen Anleitung geht es nur darum, aus einer bestehenden Tabelle ein x-y-diagramm zu erzeugen. D.h. es müssen in der Tabelle mindestens zwei
Erstellen von x-y-diagrammen in OpenOffice.calc In dieser kleinen Anleitung geht es nur darum, aus einer bestehenden Tabelle ein x-y-diagramm zu erzeugen. D.h. es müssen in der Tabelle mindestens zwei
mentor Grundwissen Chemie. 5. bis 10. Klasse Usedom
 mentor Grundwissen mentor Grundwissen Chemie. 5. bis 10. Klasse Alle wichtigen Themen von Andreas Usedom 1. Auflage mentor Grundwissen Chemie. 5. bis 10. Klasse Usedom schnell und portofrei erhältlich
mentor Grundwissen mentor Grundwissen Chemie. 5. bis 10. Klasse Alle wichtigen Themen von Andreas Usedom 1. Auflage mentor Grundwissen Chemie. 5. bis 10. Klasse Usedom schnell und portofrei erhältlich
OECD Programme for International Student Assessment PISA 2000. Lösungen der Beispielaufgaben aus dem Mathematiktest. Deutschland
 OECD Programme for International Student Assessment Deutschland PISA 2000 Lösungen der Beispielaufgaben aus dem Mathematiktest Beispielaufgaben PISA-Hauptstudie 2000 Seite 3 UNIT ÄPFEL Beispielaufgaben
OECD Programme for International Student Assessment Deutschland PISA 2000 Lösungen der Beispielaufgaben aus dem Mathematiktest Beispielaufgaben PISA-Hauptstudie 2000 Seite 3 UNIT ÄPFEL Beispielaufgaben
Polarimetrie - Deutschlands nationales Metrologieinstitut
 Polarimetrie - Deutschlands nationales Metrologieinstitut - 1 - Anwendungen der Polarimetrie In vielen Bereichen wird Polarimetrie eingesetzt, um optisch aktive Substanzen nachzuweisen und deren Konzentration
Polarimetrie - Deutschlands nationales Metrologieinstitut - 1 - Anwendungen der Polarimetrie In vielen Bereichen wird Polarimetrie eingesetzt, um optisch aktive Substanzen nachzuweisen und deren Konzentration
Überlege du: Wann brauchen wir Strom. Im Haushalt In der Schule In Büros/Firmen Auf Straßen
 Jeden Tag verbrauchen wir Menschen sehr viel Strom, also Energie. Papa macht den Frühstückskaffee, Mama fönt sich noch schnell die Haare, dein Bruder nimmt die elektrische Zahnbürste zur Hand, du spielst
Jeden Tag verbrauchen wir Menschen sehr viel Strom, also Energie. Papa macht den Frühstückskaffee, Mama fönt sich noch schnell die Haare, dein Bruder nimmt die elektrische Zahnbürste zur Hand, du spielst
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Comenius Schulprojekt The sun and the Danube. Versuch 1: Spannung U und Stom I in Abhängigkeit der Beleuchtungsstärke E U 0, I k = f ( E )
 Blatt 2 von 12 Versuch 1: Spannung U und Stom I in Abhängigkeit der Beleuchtungsstärke E U 0, I k = f ( E ) Solar-Zellen bestehen prinzipiell aus zwei Schichten mit unterschiedlichem elektrischen Verhalten.
Blatt 2 von 12 Versuch 1: Spannung U und Stom I in Abhängigkeit der Beleuchtungsstärke E U 0, I k = f ( E ) Solar-Zellen bestehen prinzipiell aus zwei Schichten mit unterschiedlichem elektrischen Verhalten.
P9 Kunststoffe Moleküle ohne Ende
 SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
SLZB Fachbereich Naturwissenschaften Fachinternes Curriculum für das Fach Chemie Klasse 10 2014/15 P9 Kunststoffe Moleküle ohne Ende 10 Bedeutung Kunststoffe Monomer, Polymer, Makromoleküle Polymerisation
Das Hebelgesetz zur Lösung technischer Aufgaben
 Es gibt einseitige Hebel, zweiseitige Hebel und Winkelhebel. Mit allen Hebeln kann man die Größe und Richtung von Kräften ändern. In der Regel verwendet man Hebel zur Vergrößerung von Kräften. Das Hebelgesetz
Es gibt einseitige Hebel, zweiseitige Hebel und Winkelhebel. Mit allen Hebeln kann man die Größe und Richtung von Kräften ändern. In der Regel verwendet man Hebel zur Vergrößerung von Kräften. Das Hebelgesetz
Station 1: Säuren in Lebensmitteln (1)
 Station 1: Säuren in Lebensmitteln (1) An dieser Station testet ihr, welche Lebensmittel Säuren enthalten. Für den Säurenachweis benutzt man im Labor bestimmte chemische Stoffe, die man Indikatoren (Zeigerstoffe)
Station 1: Säuren in Lebensmitteln (1) An dieser Station testet ihr, welche Lebensmittel Säuren enthalten. Für den Säurenachweis benutzt man im Labor bestimmte chemische Stoffe, die man Indikatoren (Zeigerstoffe)
Thermodynamik. Basics. Dietmar Pflumm: KSR/MSE. April 2008
 Thermodynamik Basics Dietmar Pflumm: KSR/MSE Thermodynamik Definition Die Thermodynamik... ist eine allgemeine Energielehre als Teilgebiet der Chemie befasst sie sich mit den Gesetzmässigkeiten der Umwandlungsvorgänge
Thermodynamik Basics Dietmar Pflumm: KSR/MSE Thermodynamik Definition Die Thermodynamik... ist eine allgemeine Energielehre als Teilgebiet der Chemie befasst sie sich mit den Gesetzmässigkeiten der Umwandlungsvorgänge
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik
 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
POLARISATION. Von Carla, Pascal & Max
 POLARISATION Von Carla, Pascal & Max Die Entdeckung durch MALUS 1808 durch ÉTIENNE LOUIS MALUS entdeckt Blick durch einen Kalkspat auf die an einem Fenster reflektierten Sonnenstrahlen, durch Drehen wurde
POLARISATION Von Carla, Pascal & Max Die Entdeckung durch MALUS 1808 durch ÉTIENNE LOUIS MALUS entdeckt Blick durch einen Kalkspat auf die an einem Fenster reflektierten Sonnenstrahlen, durch Drehen wurde
WasserKreuzworträtsel
 Wasser als Lösungsmittel ARBEITSBLATT WasserKreuzworträtsel Teste dein WasserWissen! Um dir etwas zu helfen, haben wir dir ein paar Buchstaben bereits richtig eingesetzt. Tipp: Bei der WasserWerkstatt
Wasser als Lösungsmittel ARBEITSBLATT WasserKreuzworträtsel Teste dein WasserWissen! Um dir etwas zu helfen, haben wir dir ein paar Buchstaben bereits richtig eingesetzt. Tipp: Bei der WasserWerkstatt
Musterlösungen zur Linearen Algebra II Blatt 5
 Musterlösungen zur Linearen Algebra II Blatt 5 Aufgabe. Man betrachte die Matrix A := über dem Körper R und über dem Körper F und bestimme jeweils die Jordan- Normalform. Beweis. Das charakteristische
Musterlösungen zur Linearen Algebra II Blatt 5 Aufgabe. Man betrachte die Matrix A := über dem Körper R und über dem Körper F und bestimme jeweils die Jordan- Normalform. Beweis. Das charakteristische
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Prinzip der Zylinderdruckmessung mittels des piezoelektrischen Effektes
 Prinzip der Zylinderdruckmessung mittels des piezoelektrischen Effektes Messprinzip: Ein Quarz der unter mechanischer Belastung steht, gibt eine elektrische Ladung ab. Die Ladung (Einheit pc Picocoulomb=10-12
Prinzip der Zylinderdruckmessung mittels des piezoelektrischen Effektes Messprinzip: Ein Quarz der unter mechanischer Belastung steht, gibt eine elektrische Ladung ab. Die Ladung (Einheit pc Picocoulomb=10-12
Wärmebildkamera. Aufgabe 1. Lies ab, wie groß die Temperatur der Lippen (am Punkt P) ist. ca. 24 C ca. 28 C ca. 32 C ca. 34 C
 Wärmebildkamera Ob Menschen, Tiere oder Gegenstände: Sie alle senden unsichtbare Wärmestrahlen aus. Mit sogenannten Wärmebildkameras können diese sichtbar gemacht werden. Dadurch kann man die Temperatur
Wärmebildkamera Ob Menschen, Tiere oder Gegenstände: Sie alle senden unsichtbare Wärmestrahlen aus. Mit sogenannten Wärmebildkameras können diese sichtbar gemacht werden. Dadurch kann man die Temperatur
Parotis Pankreas. Dünndarm Bürstensaum. Amylose Amylopektin Glykogen. Maltose. Glucose. Isomaltose. Saccharose. Fructose. Lactose. Galaktose.
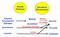 Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Parotis Pankreas Dünndarm Bürstensaum Amylose Amylopektin Glykogen Saccharose Lactose Maltose Isomaltose Saccharase (Sucrase) Lactase Maltase Isomaltase Glucose Fructose Galaktose Abbau von Stärke und
Warum kann ein Flugzeug fliegen?
 4. Dezember 2003 Warum kann ein Flugzeug fliegen? Wer oder was kann fliegen? Warum können Hexen und Harry Potter fliegen? Joanne K. Rowling / Carlsen Verlag GmbH Weil sie zaubern können! Wer oder was kann
4. Dezember 2003 Warum kann ein Flugzeug fliegen? Wer oder was kann fliegen? Warum können Hexen und Harry Potter fliegen? Joanne K. Rowling / Carlsen Verlag GmbH Weil sie zaubern können! Wer oder was kann
h- Bestimmung mit LEDs
 h- Bestimmung mit LEDs GFS im Fach Physik Nicolas Bellm 11. März - 12. März 2006 Der Inhalt dieses Dokuments steht unter der GNU-Lizenz für freie Dokumentation http://www.gnu.org/copyleft/fdl.html Inhaltsverzeichnis
h- Bestimmung mit LEDs GFS im Fach Physik Nicolas Bellm 11. März - 12. März 2006 Der Inhalt dieses Dokuments steht unter der GNU-Lizenz für freie Dokumentation http://www.gnu.org/copyleft/fdl.html Inhaltsverzeichnis
Inhalt. Allgemeine Einführung. Argumentationsvermögen. Räumliches Vorstellungsvermögen. Begabungen und Fähigkeiten messen
 Beispielheft Inhalt Allgemeine Einführung Test Eins: Test Zwei: Test Drei: Test Vier: Test Fünf: Argumentationsvermögen Auffassungsvermögen Zahlenvermögen Sprachverständnis Räumliches Vorstellungsvermögen
Beispielheft Inhalt Allgemeine Einführung Test Eins: Test Zwei: Test Drei: Test Vier: Test Fünf: Argumentationsvermögen Auffassungsvermögen Zahlenvermögen Sprachverständnis Räumliches Vorstellungsvermögen
Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn
 An die Redaktionen von Presse, Funk und Fernsehen 32 02. 09. 2002 Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn Das aktive Sparen ist nach wie vor die wichtigste Einflussgröße
An die Redaktionen von Presse, Funk und Fernsehen 32 02. 09. 2002 Vermögensbildung: Sparen und Wertsteigerung bei Immobilien liegen vorn Das aktive Sparen ist nach wie vor die wichtigste Einflussgröße
Lineare Funktionen. 1 Proportionale Funktionen 3 1.1 Definition... 3 1.2 Eigenschaften... 3. 2 Steigungsdreieck 3
 Lineare Funktionen Inhaltsverzeichnis 1 Proportionale Funktionen 3 1.1 Definition............................... 3 1.2 Eigenschaften............................. 3 2 Steigungsdreieck 3 3 Lineare Funktionen
Lineare Funktionen Inhaltsverzeichnis 1 Proportionale Funktionen 3 1.1 Definition............................... 3 1.2 Eigenschaften............................. 3 2 Steigungsdreieck 3 3 Lineare Funktionen
Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle Reaktion: Saccharose
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle Reaktion: Saccharose
