Der globale Kohlenstoffkreislauf
|
|
|
- Monika Breiner
- vor 7 Jahren
- Abrufe
Transkript
1 Der globale Kohlenstoffkreislauf Eine wesentliche Motivation für die Untersuchung des globalen Kohlenstoffkreislaufs ist der anthropogen bedingte Anstieg der atmosphärischen Konzentration von klimarelevanten Spurengasen, insbesondere CO und Methan (CH 4 ). Die atmosphärische CO - Konzentration stieg seit Beginn der Industrialisierung dramatisch and: zwischen 1750 und 1999 von 80ppm auf 67 ppm. Auch die atmosphärische Methankonzentration stieg seit 1750 um ca. 150% an. Das atmosphärische CO - Budget Abb. 1: Entwicklung der atmosphärischen CO - Konzentration auf unterschiedlichen Zeitskalen. (a): Direkte Messungen von atmosphärischem CO. (b): CO - Konzentration in Eisbohrkernen aus der Antarktis für das letzte Jahrtausend. (c): CO - Konzentration im Taylor Dome Eisbohrkern (Antarktis). (d): CO - Konzentration im Vostok Eisbohrkern (Antarktis) (unterschiedliche Farben sind Messungen unterschiedlicher Autoren). Quelle: IPCC-Report
2 Abb. : Entwicklung der atmosphärischen Methan- Konzentration (a): Aus Eisbohrkernen, Firn, und direkten Messungen von Methan. (b): Globales mittel der Methan- Konzentrationen von 198 bis (c): Jährlicher Anstieg der atmosphärischen Methan- Konzentration. Quelle: IPCC-Report 001.
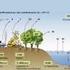
3 Abb. : Der globale Kohlenstoffkreislauf. Nach Produktion durch die Höhenstrahlung verteilt sich das 14 C auf alle Kohlenstoffreservoire. Fossile Brennstoffe enthalten kein 14 C (von B. Kromer) Wesentliche Flüsse von atmosphärischem CO in Einheiten von GtC/Jahr (10 15 g/jahr) sind (IPCC-Report 001): Anstieg in der Atmosphäre. ± 0.1. ± 0.1 Anthropogene Emissionen 5.4 ± ± 0.4 (Fossile Brennstoffe, Zement) Austausch Ozean- Atmosphäre -1.9 ± ± 0.5 Austausch Land- Atmosphäre -0. ± ± 0.7 Der Anstieg der atmosphärischen CO - Konzentration durch Verbrennung fossiler Brennstoffe kann teilweise durch die Aufnahme von CO durch Biomasse und den Ozean kompensiert werden.
4 Abb. 4: CO -Kreislauf zwischen Atmosphäre, Biosphäre und Ozean. Zahlen in umrandeten Kästchen: Gehalt an Kohlenstoff im jeweiligen Reservoir in GtC. Zahlen an den Pfeilen: Jährliche Flüsse (GtC/Jahr). Aus Rödel, S. 4. Die Rolle der Biosphäre im globalen Kohlenstoffkreislauf Die Gesamtmasse an Kohlenstoff in der Biosphäre ist von der gleichen Größenordnung wie die der Atmosphäre. Bezüglich der Pufferkapazität der Biosphäre (durch Erhöhte Aufnahme von CO bei steigender atmosphärischer CO - Konzentration) bestehen jedoch große Unsicherheiten. Neuere Abschätzungen ergaben, dass die Biosphäre trotz Änderung der Landnutzung (insbesondere die Rodung von Regenwald) und die damit Verbundenen CO - Emissionen netto eine Senke für CO ist. Der wahrscheinliche Grund hierfür ist die erhöhte Wachstumsrate und damit Aufnahme von CO bei ansteigender atmosphärischer CO - Konzentration. Während des Wachstums wandeln Pflanzen CO durch Photosynthese in Kohlehydrate um: CO + H O + h ν (CH O) n + O Daher ist die Aufnahme von CO durch lebende Biomasse höchstens proportional zum CO - Partialdruck p CO. Allerdings ist das Pflanzenwachstum meist auch durch andere Faktoren limitiert, z.b. die Verfügbarkeit von Sonnenlicht und Nährstoff. Abbildung 5 zeigt einen Vergleich der Photosyntheseraten von Mais und Sonnenblumen als Funktion der atmosphärischen CO - Konzentration. Bei der derzeitigen CO - Konzentration von 67ppm reagieren Sonnenblumen im Gegensatz zu Mais mit einem erhöhten Wachstum auf eine Steigerung des CO - Angebotes. 4
5 Abb. 5: Photosyntheseraten (Bildung von Kohlehydraten pro Zeiteinheit und pro Einheit bebauter Fläche) als Funktion des CO - Mischungsverhältnisses in der Luft. Aus Rödel, S. 45. Die Rolle des Ozeans im globalen Kohlenstoffkreislauf Der Ozean ist das größte Reservoir für Kohlendioxid. Seine Kapazität liegt um etwa Größenordnungen über der der Atmosphäre. Daher kontrolliert die Reaktion des Ozeans auf einen Anstieg CO - Konzentration in der Atmosphäre ganz wesentlich den effektiven Anstieg von atmosphärischem CO. Hierbei spielt vor allem die Chemie des im Ozean gespeicherten CO eine wichtige Rolle, aber auch dessen globale Verteilung durch innerozeanische Austauschprozesse. Die im Wasser gelöste CO - Konzentration, [CO ] aq, steht im Lösungsgleichgewicht mit dem gasförmigen CO, [CO ] g, über [CO ] aq = α [CO ] g Hierbei ist α die Oswald sche Löslichkeit. Mit dem Partialdruck p CO = [CO ] g R T und erhält man k = α 0 (1) R T [CO ] aq = k 0 p CO 5
6 bzw. [ CO ] aq k 0 = () p CO Zahlenwerte für Meerwasser (Salzgehalt.5%): α = 0.86 und k 0 = 0.08 Mol/l bei 0 C α = 0.55 und k 0 = 0.0 Mol/l bei 15 C Die Menge an physikalisch im Meerwasser gelöstem CO hängt also stark von der Temperatur ab (mit steigender Löslichkeit bei geringerer Temperatur). Im Meerwasser gelöstes CO (bzw. dessen Hydrat, CH O ) steht im Dissoziationsgleichgewicht mit Hydrogenkarbonat (HCO - ) und Karbonat (CO - ) gemäß mit den Gleichgewichtskonstanten CO + H O HCO - + H + CO - + H + und [ HCO + ] [ H ] k1 = () [ CO ] aq + [ CO ] [ H ] k = (4) [ HCO ] Zahlenwerte: k 1 = Mol/l und k = Mol/l bei 0 C k 1 = Mol/l und k = Mol/l bei 15 C Das Dissoziationsgleichgewicht hängt empfindlich von der Konzentration der H + - Ionen, und somit vom ph-wert des Meerwassers (zwischen 7.9 und 8.) ab, wobei bei zunehmender Azidität das Gleichgewicht nach links verschoben wird. Der gesamte im Ozean gelöste Kohlenstoff ( Summe CO ) ist: CO = [ CO ] [ aq + HCO ] + [ CO ] (5) Mit den Reaktionskonstanten aus Gleichungen (), () und (4) erhält man das gesamte im Ozean gelöste CO als Funktion des atmosphärischen CO - Partialdrucks: k0 k1 k0 k1 k CO = pco k (6) [ H ] [ H ] 6
7 Abb. 6: Relative Anteile von gelöstem CO, HCO -, und CO - als Funktion des ph- Wertes. Durchgezogene Kurven: Meerwasser; Gestrichelte Kurven: Süßwasser. Aus Rödel, S. 47. Hierbei bleibt als Unbekannte die Konzentration der H + - Ionen im Meerwasser. Diese ist bestimmt durch die Dissoziation der Kohlensäure, des Wassers (in H + und OH - - Ionen), sowie durch die Dissoziation von im Meerwasser vorhandener Borsäure: + H BO + H O B( OH ) 4 + H + OH + H O H mit den Reaktionskonstanten und k [ B( OH ) + 4 ] [ H ] = (7) [ H BO ] + k = [ OH ] [ H ] (8) 4 Mit diesen Reaktionskonstanten und dem Ionengleichgewicht erhält man dann eine Bestimmungsgleichung für die H + -Konzentration: H ] = [ HCO ] + [ CO ] + [ B( OH ) ] + [ OH + [ 4 und kann dann die im Ozean gelöste CO gemäß Gleichung (6) berechnen. ] Eine nützliche Größe zur Beschreibung der Aufnahmekapazität des Ozeans bezüglich CO ist der Puffer- oder Revelle- Faktor: dpco R = d CO p CO CO d(ln pco) = d(ln CO ) (9) 7
8 Der Revelle- Faktor beschreibt anschaulich, um wie viel Prozent die atmosphärische CO - Konzentration zunimmt, wenn das im Ozean gespeicherte CO um 1% zunimmt. Abb. 7: Revelle- Faktor als Funktion der Wassertemperatur. Die durchgezogene Linie gilt bei Gleichgewicht zwischen gasförmigem und gelöstem CO, die gestrichelten Linien den Variationsbereich bei Abweichungen vom Gleichgewicht. Aus Rödel, S. 49. Der Revelle- Faktor hängt stark von der Temperatur ab (Abb. 7), mit einem globalen Mittel von R 10, nimmt aber wegen der Ansäuerung des Ozeans mit steigendem atmosphärischem CO - Gehalt ab (Abb. 8). Abb. 8: Atmosphärischer Partialdruck von CO als Funktion der im Ozean gespeicherten Gesamtmenge an CO, bezogen auf die derzeitige Gesamtmenge an CO, 0 CO. Aus Rödel, S
9 Um zu bestimmen, wie viel des anthropogen in die Atmosphäre eingebrachten CO insgesamt vom Ozean aufgenommen werden kann, muss die Größe der einzelnen Reservoire miteinander in Beziehung gesetzt werden. Mit der in das Gesamtsystem eingebrachten Menge CO ( total ), der dabei in der Atmosphäre verbleibenden Menge CO ( Atm) und der vom Ozean aufgenommenen Menge CO ( Ozean ) ist der Anteil des vom Ozean aufgenommenen CO: x = CO ( Ozean) CO ( total) = CO ( Ozean) CO ( Atm) + CO ( Ozean) (10) Hierbei ist die Änderung der Konzentrationen proportional zur Größe der einzelnen Reservoire, wobei die Größe des atmosphärischen Reservoirs mit dem Revelle- Faktor R zu gewichten ist, da R mal soviel CO in die Atmosphäre geht wie in den Ozean. Es gilt also: N( Ozean) x = R N( Atm) + N( Ozean) (11) wobei N die jeweilige Größe des Reservoirs ist. Aus Abb. 4 entnimmt man hierfür: N(Atm) = tc N(Ozean) = tc Dies liefert aber nur eine obere Abschätzung, da nicht der gesamte Ozean gleichzeitig an der Aufnahme des CO beteiligt sein kann. Mit R=10 erhält man aus Gleichung (11) den maximalen Anteil des in die Atmosphäre injizierten CO, der vom Ozean aufgenommen werden kann: x = Durch die langsame Bildung von Tiefenwasser ist dieser Anteil jedoch in Wirklichkeit deutlich kleiner, ca %. Die Partialdrucke von CO in Luft und Wasser sind jedoch nicht immer im Gleichgewicht. Vielmehr ist der Ozean in den Tropen bezüglich CO tendenziell übersättigt, in höheren Breiten untersättigt (siehe Abb. 9). 9
10 Abb. 9: Nord/Süd- Breitenschnitt des CO -Partialdrucks im Oberflächenwasser. Die gestrichelte Kurve ist der zugehörigen atmosphärische Partialdruck. Aus Rödel, S
Feuerungen und Umwelt
 Feuerungen und Umwelt Der Kohlenstoffkreislauf Anstieg der CO 2 -Konzentration der Atmosphäre Der Treibhauseffekt Klimatische Auswirkungen von Feuerungen Gibt es einen Ausweg? Energiekosten und Energiepolitik
Feuerungen und Umwelt Der Kohlenstoffkreislauf Anstieg der CO 2 -Konzentration der Atmosphäre Der Treibhauseffekt Klimatische Auswirkungen von Feuerungen Gibt es einen Ausweg? Energiekosten und Energiepolitik
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lehrerhandreichungen zu: "Der Kohlenstoffkreislauf"
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Der Kohlenstoffkreislauf" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter Assimilation;
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lehrerhandreichungen zu: "Der Kohlenstoffkreislauf" Das komplette Material finden Sie hier: School-Scout.de Schlagwörter Assimilation;
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Ursachen, Amplituden und Raten langfristiger, natürlicher CO 2 -Schwankungen
 Ursachen, Amplituden und Raten langfristiger, natürlicher CO 2 -Schwankungen Hans R. Thierstein, D-ERDW, ETH & UniZ (thierstein@erdw.ethz.ch) Übersicht Planet Erde - ein Sonderfall Natürliche Quellen und
Ursachen, Amplituden und Raten langfristiger, natürlicher CO 2 -Schwankungen Hans R. Thierstein, D-ERDW, ETH & UniZ (thierstein@erdw.ethz.ch) Übersicht Planet Erde - ein Sonderfall Natürliche Quellen und
ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1
![ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 ph-wert Berechnung für starke Säuren / Basen starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1](/thumbs/33/16365353.jpg) ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
Biogeochemische Kreisläufe im globalen Klimasystem
 Biogeochemische Kreisläufe im globalen Klimasystem Martin Heimann Max-Planck-Institut für Biogeochemie Hans-Knöll Str. 10, PF 100164, 07701 Jena Tel.: (03641) 57 6350 Email: martin.heimann@bgc-jena.mpg.de
Biogeochemische Kreisläufe im globalen Klimasystem Martin Heimann Max-Planck-Institut für Biogeochemie Hans-Knöll Str. 10, PF 100164, 07701 Jena Tel.: (03641) 57 6350 Email: martin.heimann@bgc-jena.mpg.de
c C 2 K = c A 2 c B 2mol /l 2 0,5mol /l 2 4 mol /l K =4l /mol
 Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Berechnungen zum Massenwirkungsgesetz 1/13 Jakob 2010 Fall 1a: Gegeben: Gleichgewichtskonzentrationen aller Stoffe; Gesucht: Gleichgewichtskonstante Die Reaktion 2A + B 2C befindet sich im Gleichgewicht.
Klimawandel: Fakten, Optionen, Wirkungen
 Klimawandel: Fakten, Optionen, Wirkungen Fortunat Joos Klima- und Umweltphysik, Physikalisches Institut, Universität Bern Sidlerstr. 5, CH-3012 Bern Die Erwärmung des Klimasystems ist eindeutig und wird
Klimawandel: Fakten, Optionen, Wirkungen Fortunat Joos Klima- und Umweltphysik, Physikalisches Institut, Universität Bern Sidlerstr. 5, CH-3012 Bern Die Erwärmung des Klimasystems ist eindeutig und wird
Weniger CO 2 dem Klima zuliebe Lehrerinformation
 Lehrerinformation 1/8 Arbeitsauftrag Der CO 2- Kreislauf wird behandelt und die Beeinflussung des Menschen erarbeitet. Die Schülerberichte (Aufgabe 3) dienen als Grundlage zur Diskussion im Plenum. Ziel
Lehrerinformation 1/8 Arbeitsauftrag Der CO 2- Kreislauf wird behandelt und die Beeinflussung des Menschen erarbeitet. Die Schülerberichte (Aufgabe 3) dienen als Grundlage zur Diskussion im Plenum. Ziel
Neueste Ergebnisse der Treibhausgasmessungen am Blaserturm in Isny. Institut für Umweltphysik, Universität Heidelberg & NTA Isny
 Neueste Ergebnisse der Treibhausgasmessungen am Blaserturm in Isny Institut für Umweltphysik, Universität Heidelberg & NTA Isny Inhalt Der Treibhauseffekt Entwicklung der globalen vom Menschen verursachten
Neueste Ergebnisse der Treibhausgasmessungen am Blaserturm in Isny Institut für Umweltphysik, Universität Heidelberg & NTA Isny Inhalt Der Treibhauseffekt Entwicklung der globalen vom Menschen verursachten
Säure- und Base-Reaktion mit Wasser
 Säure- und Base-Reaktion mit Wasser K. Molt Fachgebiet Instrumentelle Analytik 15. Juni 2007 K. Molt (IAC) Säure/Base 15. Juni 2007 1 / 61 1 Anwendung des Massenwirkungsgesetzes Säure-/Baseexponent 2 Ostwaldsches
Säure- und Base-Reaktion mit Wasser K. Molt Fachgebiet Instrumentelle Analytik 15. Juni 2007 K. Molt (IAC) Säure/Base 15. Juni 2007 1 / 61 1 Anwendung des Massenwirkungsgesetzes Säure-/Baseexponent 2 Ostwaldsches
Elektrolytische Leitfähigkeit
 Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
Elektrolytische Leitfähigkeit 1 Elektrolytische Leitfähigkeit Gegenstand dieses Versuches ist der Zusammenhang der elektrolytischen Leitfähigkeit starker und schwacher Elektrolyten mit deren Konzentration.
B Chemisch Wissenwertes. Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden.
 -I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
-I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
Kleines Wasserlexikon
 Kleines Wasserlexikon Lösung von Kohlenstoffdioxid. Kohlenstoffdioxid CO 2 ist leicht wasserlöslich und geht mit manchen Inhaltsstoffen des Wassers auch chemische Reaktionen ein. In einem ersten Schritt
Kleines Wasserlexikon Lösung von Kohlenstoffdioxid. Kohlenstoffdioxid CO 2 ist leicht wasserlöslich und geht mit manchen Inhaltsstoffen des Wassers auch chemische Reaktionen ein. In einem ersten Schritt
Elektrochemie und Sauerstoffmessung mit LDO. Der gelöste Sauerstoff
 Elektrochemie und Sauerstoffmessung mit LDO Der gelöste Sauerstoff 2 Was ist gelöster Sauerstoff? Gelöster Sauerstoff beschreibt die Konzentration von freiem (nicht chemisch gebundenem) molekularem Sauerstoff
Elektrochemie und Sauerstoffmessung mit LDO Der gelöste Sauerstoff 2 Was ist gelöster Sauerstoff? Gelöster Sauerstoff beschreibt die Konzentration von freiem (nicht chemisch gebundenem) molekularem Sauerstoff
Demoseiten für
 Lineare Ungleichungen mit Variablen Anwendung (Vorübungen für das Thema Lineare Optimierung) Datei Nr. 90 bzw. 500 Stand 0. Dezember 009 INTERNETBIBLIOTHEK FÜR SCHULMATHEMATIK 90 / 500 Lineare Ungleichungen
Lineare Ungleichungen mit Variablen Anwendung (Vorübungen für das Thema Lineare Optimierung) Datei Nr. 90 bzw. 500 Stand 0. Dezember 009 INTERNETBIBLIOTHEK FÜR SCHULMATHEMATIK 90 / 500 Lineare Ungleichungen
LeWis» ph-wert Berechnungen «Kapitel 5
 Additum 5. Wässrige Lösungen mehrprotoniger Säuren und Basen Ziel dieses Kapitels ist es, eine weitere Anwendungsmöglichkeit des bisher erlernten Vorgehenskonzepts vorzustellen. Die Berechnung von ph-werten
Additum 5. Wässrige Lösungen mehrprotoniger Säuren und Basen Ziel dieses Kapitels ist es, eine weitere Anwendungsmöglichkeit des bisher erlernten Vorgehenskonzepts vorzustellen. Die Berechnung von ph-werten
Die Verweildauer des Kohlenstoffs in der Biomasse ist entscheidend
 Die Verweildauer des Kohlenstoffs in der Biomasse ist entscheidend Ein vereinfachtes Modell zur Beurteilung der Klimarelevanz menschlicher Aktivitäten Von Wolf von Fabeck 1 Wärmeabstrahlung in den Weltraum
Die Verweildauer des Kohlenstoffs in der Biomasse ist entscheidend Ein vereinfachtes Modell zur Beurteilung der Klimarelevanz menschlicher Aktivitäten Von Wolf von Fabeck 1 Wärmeabstrahlung in den Weltraum
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH + H 2 O Na + aq + OH starke
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Stand der Wissenschaft
 Der anthropogene Klimawandel Stand der Wissenschaft von Jan Hohlbein 1 Inhalt Def. Klima Natürlicher Treibhauseffekt Strahlungsbilanz Anthropogener Treibhauseffekt Indikatoren Beteiligte Gase Folgen des
Der anthropogene Klimawandel Stand der Wissenschaft von Jan Hohlbein 1 Inhalt Def. Klima Natürlicher Treibhauseffekt Strahlungsbilanz Anthropogener Treibhauseffekt Indikatoren Beteiligte Gase Folgen des
Übung 3. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) Verständnis des thermodynamischen Gleichgewichts
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen (Teil 2) adiabatische Flammentemperatur Verständnis des thermodynamischen Gleichgewichts Definition von K X, K c, K p Berechnung von K
Ein Puffer ist eine Mischung aus einer schwachen Säure/Base und ihrer Korrespondierenden Base/Säure.
 2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
Säuren und Basen nach Brönsted
 Säuren und Basen nach Brönsted Es gibt versch. Definitionen von Säuren und Basen. Nach Brönsted ist eine Säure (HA) ein Protonendonator und eine Base (B) ein Protonenakzeptor, d.h. eine Säure reagiert
Säuren und Basen nach Brönsted Es gibt versch. Definitionen von Säuren und Basen. Nach Brönsted ist eine Säure (HA) ein Protonendonator und eine Base (B) ein Protonenakzeptor, d.h. eine Säure reagiert
Ressourcenmanagement: Warum und wie die Sicht der Wissenschaft
 Zukunft der Entsorgungswirtschaft Ressourcenmanagement: Warum und wie die Sicht der Wissenschaft Paul H. Brunner und Brigitte Müller Technische Universität Wien Institut für Wassergüte, Ressourcenmanagement
Zukunft der Entsorgungswirtschaft Ressourcenmanagement: Warum und wie die Sicht der Wissenschaft Paul H. Brunner und Brigitte Müller Technische Universität Wien Institut für Wassergüte, Ressourcenmanagement
Kohlensäure Kalk-Kohlensäure-Gleichgewicht
 KalkGleichgewicht Das KalkGleichgewicht ist von rein technischer Bedeutung. Die Aufnahme von Kohlendioxid aus der Atmosphäre erfolgt durch Niederschlagswasser und bei der Passage durch den Boden und den
KalkGleichgewicht Das KalkGleichgewicht ist von rein technischer Bedeutung. Die Aufnahme von Kohlendioxid aus der Atmosphäre erfolgt durch Niederschlagswasser und bei der Passage durch den Boden und den
ph-wert Berechnung für starke Säuren / Basen
 ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
ph-wert Berechnung für starke Säuren / Basen 0.1 mol/l HCl: HCl + H 2 O H 3 O + + Cl starke Säure, vollständige Dissoziation [H 3 O + ] = 10 1 mol/l; ph = 1 0.1 mol/l NaOH: NaOH Na + aq + OH starke Base,
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Institut für hysikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum 0. Übungsblatt zur Vorlesung hysikalische Chemie I SS 04 rof. Dr. Bartsch 0. L Die freie Standardreaktionsenthalpie der
Übung 4. SS 2013 Übung - Einführung in die Verbrennung - Methling, Özuylasi 1
 Ziel: Grundlagen der chemischen Reaktionskinetik verstehen Verstehen qualitativer Reaktionsverläufe Aufstellung des Zeitgesetzes Umgang mit nicht reagierenden Stoßpartner (M) Berechnung Geschwindigkeitskoeffizient
Ziel: Grundlagen der chemischen Reaktionskinetik verstehen Verstehen qualitativer Reaktionsverläufe Aufstellung des Zeitgesetzes Umgang mit nicht reagierenden Stoßpartner (M) Berechnung Geschwindigkeitskoeffizient
Lösung Übungsserie 3
 Institut für Energietechnik Laboratorium für Aerothermochemie und Verbrennungssysteme Prof. Dr. onstantinos Boulouchos Lösung Übungsserie 3 Chemisches Gleichgewicht & Exergie Formeln Molare Entropie (ideales
Institut für Energietechnik Laboratorium für Aerothermochemie und Verbrennungssysteme Prof. Dr. onstantinos Boulouchos Lösung Übungsserie 3 Chemisches Gleichgewicht & Exergie Formeln Molare Entropie (ideales
Lösung 7. Allgemeine Chemie I Herbstsemester Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf.
 Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Lösung 7 Allgemeine Chemie I Herbstsemester 2012 1. Aufgabe Je nach Stärke einer Säure tritt eine vollständige oder nur eine teilweise Dissoziation auf. Chlorwasserstoff ist eine starke Säure (pk a = 7),
Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6
 Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 6 Säure-Base-Gleichgewichte E 1. Sie möchten 200 ml einer Pufferlösung mit ph = 5.00 mit dem Säure-Base-Paar Essigsäure
Wald, Holz und Kohlenstoff
 Wald, Holz und Kohlenstoff Dr. Uwe Paar Landesbetrieb HESSEN-FORST Nordwestdeutsche Forstliche Versuchsanstalt Gliederung Bedeutung des Waldes Leistungen nachhaltiger Forstwirtschaft Wie entsteht Holz?
Wald, Holz und Kohlenstoff Dr. Uwe Paar Landesbetrieb HESSEN-FORST Nordwestdeutsche Forstliche Versuchsanstalt Gliederung Bedeutung des Waldes Leistungen nachhaltiger Forstwirtschaft Wie entsteht Holz?
Fachbereich 1. Laborprotokoll Wechselwirkung Fels-Wasser
 Fachbereich 1 Laborprotokoll Wechselwirkung Fels-Wasser Schriftliche Versuchsbeschreibung und Protokollauswertung im Fortgeschrittenenpraktikum SS 2007 Dozent: Prof. Dr. Wolfgang Dreybrodt vorgelegt von:
Fachbereich 1 Laborprotokoll Wechselwirkung Fels-Wasser Schriftliche Versuchsbeschreibung und Protokollauswertung im Fortgeschrittenenpraktikum SS 2007 Dozent: Prof. Dr. Wolfgang Dreybrodt vorgelegt von:
Treibhausgase. Stefan Smidt. Bundesforschungs- und Ausbildungszentrum für Wald, Naturgefahren und Landschaft. Smidt / BFW
 Treibhausgase Stefan Smidt Bundesforschungs- und Ausbildungszentrum für Wald, Naturgefahren und Landschaft Direkte Treibhausgase absorbieren IR-Strahlung Wasserdampf (troposphärisch) Kohlendioxid Methan
Treibhausgase Stefan Smidt Bundesforschungs- und Ausbildungszentrum für Wald, Naturgefahren und Landschaft Direkte Treibhausgase absorbieren IR-Strahlung Wasserdampf (troposphärisch) Kohlendioxid Methan
1/6. Welche Antwort ist richtig: Wie entsteht aus organischen Kohlenstoffverbindungen das gasförmige Kohlendioxid?
 1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
Klimafakten: Aktualisierung Dezember 2018
 Klimafakten: Aktualisierung Dezember 2018 Die Klimakonferenz COP24 in Kattowitz (Katowice) sieht diese Woche ihrem Ende entgegen. Mit mehr als 20.000 Delegierten und Journalisten und einem medialen Dauerfeuer
Klimafakten: Aktualisierung Dezember 2018 Die Klimakonferenz COP24 in Kattowitz (Katowice) sieht diese Woche ihrem Ende entgegen. Mit mehr als 20.000 Delegierten und Journalisten und einem medialen Dauerfeuer
Der Treibhauseffekt Was bedeutet Treibhauseffekt?
 Der Treibhauseffekt 1.) Allgemein - Was bedeutet Treibhauseffekt? 2.) Ursachen Wie entsteht der Treibhauseffekt? 3.) Anteile der am Treibhauseffet beteiligten Gase 4.) Der Überschuss an Kohlendioxid 5.)
Der Treibhauseffekt 1.) Allgemein - Was bedeutet Treibhauseffekt? 2.) Ursachen Wie entsteht der Treibhauseffekt? 3.) Anteile der am Treibhauseffet beteiligten Gase 4.) Der Überschuss an Kohlendioxid 5.)
Chemie aquatischer Systeme. Herbstsemester 2013
 Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Chemie aquatischer Systeme Herbstsemester 2013 Ziele der Vorlesung Verständnis der chemischen Zusammensetzung der Gewässer aufgrund chemischer Prozesse Verknüpfung chemischer Prozesse mit biologischen
Treibhausgas-Messungen aus dem Weltraum mittels ENVISAT: Kohlendioxid und Methan
 Michael Buchwitz Bremen, 16. Juli 2009 Institut für Umweltphysik (IUP) Universität Bremen FB1 Otto Hahn Allee 1 28334 Bremen Tel.: (0421) 218-4475 Fax: (0421) 218-4555 E-mail: Michael.Buchwitz@iup.physik.uni-bremen.de
Michael Buchwitz Bremen, 16. Juli 2009 Institut für Umweltphysik (IUP) Universität Bremen FB1 Otto Hahn Allee 1 28334 Bremen Tel.: (0421) 218-4475 Fax: (0421) 218-4555 E-mail: Michael.Buchwitz@iup.physik.uni-bremen.de
1/37. Das Protolysegleichgewicht. Wie könnte man die Stärke einer Säure quantitativ definieren?
 Das Protolysegleichgewicht 1/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Das Protolysegleichgewicht 2/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Ein erster Ansatz
Das Protolysegleichgewicht 1/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Das Protolysegleichgewicht 2/37 Wie könnte man die Stärke einer Säure quantitativ definieren? Ein erster Ansatz
Elektrolyte. (aus: Goldenberg, SOL)
 Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Elektrolyte Elektrolyte leiten in wässriger Lösung Strom. Zu den Elektrolyten zählen Säuren, Basen und Salze, denn diese alle liegen in wässriger Lösung zumindest teilweise in Ionenform vor. Das Ostwaldsche
Auswirkungen von Querbauwerken auf die Stoffumsätze und Populationsbiologie von Fließgewässern
 Institut für Umweltwissenschaften Auswirkungen von Querbauwerken auf die Stoffumsätze und Populationsbiologie von Fließgewässern Andreas Lorke, Thomas Schmidt, Andreas Mäck Institute for Environmental
Institut für Umweltwissenschaften Auswirkungen von Querbauwerken auf die Stoffumsätze und Populationsbiologie von Fließgewässern Andreas Lorke, Thomas Schmidt, Andreas Mäck Institute for Environmental
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo
 Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Allgemeine Chemie für Studierende mit Nebenfach Chemie Andreas Rammo Allgemeine und Anorganische Chemie Universität des Saarlandes E-Mail: a.rammo@mx.uni-saarland.de innere Energie U Energieumsatz bei
Grundlagen der Chemie Säuren und Basen
 Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Säuren und Basen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Säure-Base-Theorien Die Begriffe Säure und Base
Makroökonomie I/Grundlagen der Makroökonomie
 Makroökonomie I/Grundzüge der Makroökonomie Page 1 1 Makroökonomie I/Grundlagen der Makroökonomie Kapitel 9: Geldmengenwachstum, Inflation und Produktion Günter W. Beck 1 Makroökonomie I/Grundzüge der
Makroökonomie I/Grundzüge der Makroökonomie Page 1 1 Makroökonomie I/Grundlagen der Makroökonomie Kapitel 9: Geldmengenwachstum, Inflation und Produktion Günter W. Beck 1 Makroökonomie I/Grundzüge der
Klimawandel. Inhalt. CO 2 (ppm)
 Klimawandel CO 2 (ppm) Sommersemester '07 Joachim Curtius Institut für Physik der Atmosphäre Universität Mainz Inhalt 1. Überblick 2. Grundlagen 3. Klimawandel heute: Beobachtungen 4. CO 2 5. Andere Treibhausgase
Klimawandel CO 2 (ppm) Sommersemester '07 Joachim Curtius Institut für Physik der Atmosphäre Universität Mainz Inhalt 1. Überblick 2. Grundlagen 3. Klimawandel heute: Beobachtungen 4. CO 2 5. Andere Treibhausgase
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Allgemeine Chemie I 2008/09 ÜBUNGSPRÜFUNG. Prof. J. Hulliger
 Allgemeine Chemie I 2008/09 ÜBUNGSPRÜFUNG Prof. J. Hulliger 15.10.08 Aufgabe 1 (1 Punkt) Vervollständigen Sie nachstehende Reaktionen, (stöchiometrische Koeffizienten, Pfeile, Zustände wie ionisch, aq,
Allgemeine Chemie I 2008/09 ÜBUNGSPRÜFUNG Prof. J. Hulliger 15.10.08 Aufgabe 1 (1 Punkt) Vervollständigen Sie nachstehende Reaktionen, (stöchiometrische Koeffizienten, Pfeile, Zustände wie ionisch, aq,
Definition Biosphäre, Kohlenstoffkreislauf
 Dynamik der Biosphäre Definition Biosphäre, Kohlenstoffkreislauf Wintersemester 2005/2006 Wolfgang Cramer Lehrstuhl "Globale Ökologie" http://portal.pik-potsdam.de/members/cramer -> "Teaching" Heute...
Dynamik der Biosphäre Definition Biosphäre, Kohlenstoffkreislauf Wintersemester 2005/2006 Wolfgang Cramer Lehrstuhl "Globale Ökologie" http://portal.pik-potsdam.de/members/cramer -> "Teaching" Heute...
Verbrennungstechnik. 1. Brennstoffe. 1.Brennstoffe. 2.Heizwert. 2.1 Oberer Heizwert 2.2 Unterer Heizwert. 3.Verbrennungsvorgang
 Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Verbrennungstechnik 1.Brennstoffe.Heizwert.1 Oberer Heizwert. Unterer Heizwert.Verbrennungsvorgang.1 Verbrennungsgleichungen 4.Ermittlung von Sauerstoff-, Luftbedarf u. Rauchgasmenge 5.Verbrennungskontrolle
Übung 1. Göksel Özuylasi Tel.: Torsten Methling Tel.
 Göksel Özuylasi Email: goeksel.oezuylasi@dlr.de Tel.: 0711 6862 8098 Torsten Methling Email: torsten.methling@dlr.de Tel.: 0711 6862 277 WS 2013/14 Übung - Einführung in die Verbrennung - Özuylasi, Methling
Göksel Özuylasi Email: goeksel.oezuylasi@dlr.de Tel.: 0711 6862 8098 Torsten Methling Email: torsten.methling@dlr.de Tel.: 0711 6862 277 WS 2013/14 Übung - Einführung in die Verbrennung - Özuylasi, Methling
+ - H3O(aq) + OH(aq) H2O(l) + H2O(l) 1/19. Autoprotolyse des Wassers
 Autoprotolyse des Wassers 1/19 Autoprotolyse des Wassers 2/19 c(h3o + ) = 10-7 mol/l c(h2o) = 55,4 mol/l c(oh - ) = 10-7 mol/l Autoprotolyse des Wassers 3/19 K = [H 3 O+ ][OH ] [H 2 O][H 2 O] Autoprotolyse
Autoprotolyse des Wassers 1/19 Autoprotolyse des Wassers 2/19 c(h3o + ) = 10-7 mol/l c(h2o) = 55,4 mol/l c(oh - ) = 10-7 mol/l Autoprotolyse des Wassers 3/19 K = [H 3 O+ ][OH ] [H 2 O][H 2 O] Autoprotolyse
a.) Wie beeinflussen in einer Verbrennungsreaktion Brennstoffe in fester bzw. flüssiger Phase das chemische Gleichgewicht? Begründung!
 Klausur F2004 (Grundlagen der motorischen Verbrennung) 2 Aufgabe 1.) ( 2 Punkte) Wie beeinflussen in einer Verbrennungsreaktion Brennstoffe in fester bzw. flüssiger Phase das chemische Gleichgewicht? Begründung!
Klausur F2004 (Grundlagen der motorischen Verbrennung) 2 Aufgabe 1.) ( 2 Punkte) Wie beeinflussen in einer Verbrennungsreaktion Brennstoffe in fester bzw. flüssiger Phase das chemische Gleichgewicht? Begründung!
Chemie für Geowissenschaftler. SSem Wiederholungsklausur. Datum
 Chemie für Geowissenschaftler SSem 2009 Wiederholungsklausur Datum 15.10.2009 Name: Vorname: Matr.-Nr.: Erreichte Punktzahl: 1. Am Ozeanboden wird Methangas durch sulfat-reduzierende Bakterien in Hydrogen-carbonat
Chemie für Geowissenschaftler SSem 2009 Wiederholungsklausur Datum 15.10.2009 Name: Vorname: Matr.-Nr.: Erreichte Punktzahl: 1. Am Ozeanboden wird Methangas durch sulfat-reduzierende Bakterien in Hydrogen-carbonat
Wasserchemie und Wasseranalytik SS 2015
 Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Kurstag 3. Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers
 Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Kurstag Pufferlösungen, Herstellung eines Essigsäure-Acetat-Puffers Stichworte zur Vorbereitung: Pufferlösungen, Henderson-Hasselbalch, Pufferkapazität, Pufferoptimum, Herstellen eines Puffers, physiologische
Hydrogeochemische Modellierung mit PhreeqC
 ( Blockkurs Geowissenschaftliches Modellieren (01. 03.04.2009) Aufgabe 1: Erhöhung CO 2 -Gehalt in der Atmosphäre durch Änderung der Lufttemperatur? Aus vielen Untersuchungen (z.b. an Eiskernen) wissen
( Blockkurs Geowissenschaftliches Modellieren (01. 03.04.2009) Aufgabe 1: Erhöhung CO 2 -Gehalt in der Atmosphäre durch Änderung der Lufttemperatur? Aus vielen Untersuchungen (z.b. an Eiskernen) wissen
Einführung in die Umweltwissenschaften
 Einführung in die Umweltwissenschaften Heribert Cypionka Mikrobiologische Grundlagen - Rolle der Mikroorganismen in der Natur - Beispiel Meer - Biogeochemie, Mikrobielle Ökologie, Umweltmikrobiologie -
Einführung in die Umweltwissenschaften Heribert Cypionka Mikrobiologische Grundlagen - Rolle der Mikroorganismen in der Natur - Beispiel Meer - Biogeochemie, Mikrobielle Ökologie, Umweltmikrobiologie -
Treibhausgasemissionen nach der Düngung mit Gülle und Gärresten
 Treibhausgasemissionen nach der Düngung mit Gülle und Gärresten J. Augustin, U. Hagemann, M. Drösler, S. Glatzel, H. Kage, A. Pacholski, K.H. Mühling, u.a. Gülletag Landmaschinenschule Triesdorf, 21. Mai
Treibhausgasemissionen nach der Düngung mit Gülle und Gärresten J. Augustin, U. Hagemann, M. Drösler, S. Glatzel, H. Kage, A. Pacholski, K.H. Mühling, u.a. Gülletag Landmaschinenschule Triesdorf, 21. Mai
Energie und Umwelt. Klimaverträgliche Nutzung von Energie. Dr. rer. nat. Klaus Heinloth Professor für Physik an der Universität Bonn
 Energie und Umwelt Klimaverträgliche Nutzung von Energie Dr. rer. nat. Klaus Heinloth Professor für Physik an der Universität Bonn 3 vdf B. G. Teubner Stuttgart Hochschulverlag AG an der ETH Zürich Vorwort
Energie und Umwelt Klimaverträgliche Nutzung von Energie Dr. rer. nat. Klaus Heinloth Professor für Physik an der Universität Bonn 3 vdf B. G. Teubner Stuttgart Hochschulverlag AG an der ETH Zürich Vorwort
Kapitel 2.2 Kardiopulmonale Homöostase. Kohlendioxid
 Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
Kapitel 2.2 Kardiopulmonale Homöostase Kohlendioxid Transport im Plasma Bei der Bildung von im Stoffwechsel ist sein Partialdruck höher als im Blut, diffundiert folglich ins Plasmawasser und löst sich
CO 2 im Klimasystem. F. Joos & Urs Lauterburg (Experimente) Klima- und Umweltphysik Oeschger Zentrum für Klimaforschung Universität Bern
 CO 2 im Klimasystem F. Joos & Urs Lauterburg (Experimente) Klima- und Umweltphysik Oeschger Zentrum für Klimaforschung Universität Bern CO 2 Konzentration (ppm) Beispiellos: CO 2 der letzen 800 000 Jahre
CO 2 im Klimasystem F. Joos & Urs Lauterburg (Experimente) Klima- und Umweltphysik Oeschger Zentrum für Klimaforschung Universität Bern CO 2 Konzentration (ppm) Beispiellos: CO 2 der letzen 800 000 Jahre
Lösung der Aufgaben. / Baum] = 405 [Baum]
![Lösung der Aufgaben. / Baum] = 405 [Baum] Lösung der Aufgaben. / Baum] = 405 [Baum]](/thumbs/51/28785678.jpg) Lösung der Aufgaben 1 Lösen Sie die Aufgabe in Abbildung 1A! 3000[Liter/Jahr]*,7[kg/Liter] = 8100 [kg CO / Jahr] 8100 [kg CO / Jahr] / 0 [kg CO / Baum] = 405 [Baum] Wie viel CO entsteht bei der Verbrennung
Lösung der Aufgaben 1 Lösen Sie die Aufgabe in Abbildung 1A! 3000[Liter/Jahr]*,7[kg/Liter] = 8100 [kg CO / Jahr] 8100 [kg CO / Jahr] / 0 [kg CO / Baum] = 405 [Baum] Wie viel CO entsteht bei der Verbrennung
Venndiagramm, Grundmenge und leere Menge
 Venndiagramm, Grundmenge und leere Menge In späteren Kapitel wird manchmal auf die Mengenlehre Bezug genommen. Deshalb sollen hier die wichtigsten Grundlagen und Definitionen dieser Disziplin kurz zusammengefasst
Venndiagramm, Grundmenge und leere Menge In späteren Kapitel wird manchmal auf die Mengenlehre Bezug genommen. Deshalb sollen hier die wichtigsten Grundlagen und Definitionen dieser Disziplin kurz zusammengefasst
Energetische Nutzung von Biomasse erhöht die CO2-Konzentration in der Atmosphäre
 Energetische Nutzung von Biomasse erhöht die CO2-Konzentration in der Atmosphäre Ein einfaches Modell zur Beurteilung der energetischen Nutzung von Biomasse Von Wolf von Fabeck 1 Unter dem Stichwort Kohlenstoffzyklus
Energetische Nutzung von Biomasse erhöht die CO2-Konzentration in der Atmosphäre Ein einfaches Modell zur Beurteilung der energetischen Nutzung von Biomasse Von Wolf von Fabeck 1 Unter dem Stichwort Kohlenstoffzyklus
4 Gleichungen und Ungleichungen
 In diesem Kapitel werden Techniken zur Bestimmung der Lösungsmengen von Gleichungen und Ungleichungen rekapituliert. 4.1 Eindimensionale Gleichungen und Ungleichungen Eine Gleichung oder Ungleichung ohne
In diesem Kapitel werden Techniken zur Bestimmung der Lösungsmengen von Gleichungen und Ungleichungen rekapituliert. 4.1 Eindimensionale Gleichungen und Ungleichungen Eine Gleichung oder Ungleichung ohne
Konfidenzintervall für den Anteilswert θ. Konfidenzintervalle. Jost Reinecke. Universität Bielefeld. 13. Juni 2005
 Universität Bielefeld 13. Juni 2005 Einführung Einführung Wie kann die Kenntnis der Wahrscheinlichkeitsverteilung der Parameter einer Stichprobe dazu verhelfen auf die wahren Werte der Grundgesamtheit
Universität Bielefeld 13. Juni 2005 Einführung Einführung Wie kann die Kenntnis der Wahrscheinlichkeitsverteilung der Parameter einer Stichprobe dazu verhelfen auf die wahren Werte der Grundgesamtheit
CO -Konzentration 2 April 2014
 CO 2 -Konzentration April 2014 CO 2 -Konzentration Thüringer Landesanstalt für Umwelt und Geologie - Thüringer Klimaagentur - Göschwitzer Str. 41 07745 Jena Email: klimaagentur@tlug.thueringen.de Internet:
CO 2 -Konzentration April 2014 CO 2 -Konzentration Thüringer Landesanstalt für Umwelt und Geologie - Thüringer Klimaagentur - Göschwitzer Str. 41 07745 Jena Email: klimaagentur@tlug.thueringen.de Internet:
Ü b u n g s b l a t t 15
 Einführung in die Stochastik Sommersemester 07 Dr. Walter Oevel 2. 7. 2007 Ü b u n g s b l a t t 15 Hier ist zusätzliches Übungsmaterial zur Klausurvorbereitung quer durch die Inhalte der Vorlesung. Eine
Einführung in die Stochastik Sommersemester 07 Dr. Walter Oevel 2. 7. 2007 Ü b u n g s b l a t t 15 Hier ist zusätzliches Übungsmaterial zur Klausurvorbereitung quer durch die Inhalte der Vorlesung. Eine
Aufgaben. 2 Physikalische Grundlagen
 Der Verdampfungs- oder Kondensationspunkt jedes Stoffes ist von der Temperatur und dem Druck abhängig. Für jede Verdampfungstemperatur gibt es nur einen zugehörigen Verdampfungsdruck und für jeden Verdampfungsdruck
Der Verdampfungs- oder Kondensationspunkt jedes Stoffes ist von der Temperatur und dem Druck abhängig. Für jede Verdampfungstemperatur gibt es nur einen zugehörigen Verdampfungsdruck und für jeden Verdampfungsdruck
Globaler Kohlenstoff-Haushalt
 Globaler Kohlenstoff-Haushalt 1 Lernziele Sie kennen die grossen globalen Kohlenstoffspeicher und wissen, wie sie zusammenhängen. Sie verstehen den Treibhauseffekt und die Rolle von CO 2 im Wärmehaushalt
Globaler Kohlenstoff-Haushalt 1 Lernziele Sie kennen die grossen globalen Kohlenstoffspeicher und wissen, wie sie zusammenhängen. Sie verstehen den Treibhauseffekt und die Rolle von CO 2 im Wärmehaushalt
Dynamik der Biosphäre. Definition Biosphäre, Kohlenstoffkreislauf
 Dynamik der Biosphäre Definition Biosphäre, Kohlenstoffkreislauf Wintersemester 2006/2007 Wolfgang Cramer Lehrstuhl "Globale Ökologie" http://www.pik-potsdam.de/~cramer -> "Teaching" Heute... Biosphäre
Dynamik der Biosphäre Definition Biosphäre, Kohlenstoffkreislauf Wintersemester 2006/2007 Wolfgang Cramer Lehrstuhl "Globale Ökologie" http://www.pik-potsdam.de/~cramer -> "Teaching" Heute... Biosphäre
Nährstoffkreislauf in den Tropen
 Nährstoffkreislauf in den Tropen Manuel Zak 3. Juni 2005 1) Standort 2) Nährstoffvorkommen Boden Biomasse 3) Nährstoffkreislauf 4) Einfluss des Menschen Manuel Zak 2 Standort 3 große Regenwaldgebiete:
Nährstoffkreislauf in den Tropen Manuel Zak 3. Juni 2005 1) Standort 2) Nährstoffvorkommen Boden Biomasse 3) Nährstoffkreislauf 4) Einfluss des Menschen Manuel Zak 2 Standort 3 große Regenwaldgebiete:
Interpretation der chemischen und physikalischen Untersuchungen
 Interpretation der chemischen und physikalischen Untersuchungen in Fliessgewässern Für die Interpretation der chemischen (ph, Nitrat, Sauerstoff, Alkalinität), physikalischen (Temperatur, Transparenz,
Interpretation der chemischen und physikalischen Untersuchungen in Fliessgewässern Für die Interpretation der chemischen (ph, Nitrat, Sauerstoff, Alkalinität), physikalischen (Temperatur, Transparenz,
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Fächerübergreifender Teil Biologie
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Schwerpunktfach Teil BIOLOGIE UND CHEMIE Fächerübergreifender Teil Biologie Verfasser: Richtzeit: Hilfsmittel: Hinweise: G. Rutz, M. Lüscher 30 Minuten (von
Gruppe / Kandidat/in Nr:... Name/Vorname:... Schwerpunktfach Teil BIOLOGIE UND CHEMIE Fächerübergreifender Teil Biologie Verfasser: Richtzeit: Hilfsmittel: Hinweise: G. Rutz, M. Lüscher 30 Minuten (von
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler
 Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 4: Isomerie, Gibbs-Helmholtz-Gleichung, Katalysator, Addition an Alkene, funktionelle Gruppen, Säure/Base 1) Ordnen Sie die folgenden
Formelsammlung Chemie
 1 Formelsammlung Chemie Joachim Jakob, Kronberg-Gymnasium Aschaffenburg chemie-lernprogramme.de/daten/programme/js/formelsammlung/ Inhaltsverzeichnis 1 Avogadro Konstante N A 2 2 Molare Masse M 2 3 Molares
1 Formelsammlung Chemie Joachim Jakob, Kronberg-Gymnasium Aschaffenburg chemie-lernprogramme.de/daten/programme/js/formelsammlung/ Inhaltsverzeichnis 1 Avogadro Konstante N A 2 2 Molare Masse M 2 3 Molares
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie
 Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Übersicht. Emissionen. 1 Klimaökonomische Modelle. 2 Abbildung von wirtschaftlicher Entwicklung und
 Vorlesung 3: Modellierung von Klimawandel 1/17 Übersicht 1 Klimaökonomische Modelle 2 Abbildung von wirtschaftlicher Entwicklung und Emissionen 3 Abbildung des Klimasystems und des CO 2 -Kreislaufs 4 Abbildung
Vorlesung 3: Modellierung von Klimawandel 1/17 Übersicht 1 Klimaökonomische Modelle 2 Abbildung von wirtschaftlicher Entwicklung und Emissionen 3 Abbildung des Klimasystems und des CO 2 -Kreislaufs 4 Abbildung
b) Hydrostatik, Aerostatik (Fortsetzung) Schweredruck:
 b) Hydrostatik, Aerostatik (Fortsetzung) Schweredruck: = Druck einer senkrecht über einer Fläche A Stehenden Substanz (auch Flächen innerhalb der Flüssigkeit, nicht nur am Boden) Schweredruck steigt linear
b) Hydrostatik, Aerostatik (Fortsetzung) Schweredruck: = Druck einer senkrecht über einer Fläche A Stehenden Substanz (auch Flächen innerhalb der Flüssigkeit, nicht nur am Boden) Schweredruck steigt linear
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6
 Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übungen zur VL Chemie für Biologen und Humanbiologen 05.12.2011 Lösung Übung 6 Thermodynamik und Gleichgewichte 1. a) Was sagt die Enthalpie aus? Die Enthalpie H beschreibt den Energiegehalt von Materie
Übersicht. 1 Klimasystem und Klimawandel. 2 Emissionen von Treibhausgasen. 3 Impacts von Klimawandel. Vorlesung 2: Grundlagen 1/33
 Vorlesung 2: Grundlagen 1/33 Übersicht 1 Klimasystem und Klimawandel 2 Emissionen von Treibhausgasen 3 Impacts von Klimawandel Vorlesung 2: Grundlagen 2/33 Strahlungshaushalt der Erde Alle Körper mit einer
Vorlesung 2: Grundlagen 1/33 Übersicht 1 Klimasystem und Klimawandel 2 Emissionen von Treibhausgasen 3 Impacts von Klimawandel Vorlesung 2: Grundlagen 2/33 Strahlungshaushalt der Erde Alle Körper mit einer
4. Wässrige Lösungen schwacher Säuren und Basen
 4. Wässrige Lösungen schwacher Säuren und Basen Ziel dieses Kapitels ist es, das Vorgehenskonzept zur Berechnung von ph-werten weiter zu entwickeln und ph-werte von wässrigen Lösungen einprotoniger, schwacher
4. Wässrige Lösungen schwacher Säuren und Basen Ziel dieses Kapitels ist es, das Vorgehenskonzept zur Berechnung von ph-werten weiter zu entwickeln und ph-werte von wässrigen Lösungen einprotoniger, schwacher
Übungen zu Physik 1 für Ingenieure Musterlösung Blatt 6
 Übungen zu Physik 1 für Ingenieure Musterlösung Blatt 6 Aufgabe 1 Hook sches Gesetz für ein Federpendel Bei einer Feder, für die das Hook sche Gesetz gilt, ist die rücktreibende Kraft F F proportional
Übungen zu Physik 1 für Ingenieure Musterlösung Blatt 6 Aufgabe 1 Hook sches Gesetz für ein Federpendel Bei einer Feder, für die das Hook sche Gesetz gilt, ist die rücktreibende Kraft F F proportional
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der Treibhauseffekt. Treibhausgase. Sonnenstrahlen
 Der Treibhauseffekt Sonnenstrahlen Treibhausgase 18 ºC +15 ºC Die kurzwelligen Sonnenstrahlen erwärmen die Erdoberfläche. Diese gibt langwellige Infrarotstrahlung ab, welche von den Treibhausgasen aufgenommen
Der Treibhauseffekt Sonnenstrahlen Treibhausgase 18 ºC +15 ºC Die kurzwelligen Sonnenstrahlen erwärmen die Erdoberfläche. Diese gibt langwellige Infrarotstrahlung ab, welche von den Treibhausgasen aufgenommen
Letzte Woche. Auswirkung chemischer Bestandteile der Atmosphäre auf das Klima Energiehaushalt Treibhausgase Das atmosphärische IR-Fenster GWPs
 Letzte Woche. Auswirkung chemischer Bestandteile der Atmosphäre auf das Klima Energiehaushalt Treibhausgase Das atmosphärische IR-Fenster GWPs Der anthropogene Treibhauseffekt Feedbacks 0 Fließender Übergang
Letzte Woche. Auswirkung chemischer Bestandteile der Atmosphäre auf das Klima Energiehaushalt Treibhausgase Das atmosphärische IR-Fenster GWPs Der anthropogene Treibhauseffekt Feedbacks 0 Fließender Übergang
Makroökonomie I/Grundlagen der Makroökonomie
 Makroökonomie I/Grundzüge der Makroökonomie Page 1 1 Makroökonomie I/Grundlagen der Makroökonomie Kapitel 10 Wachstum Stilisierte Fakten Günter W. Beck 1 Makroökonomie I/Grundzüge der Makroökonomie Page
Makroökonomie I/Grundzüge der Makroökonomie Page 1 1 Makroökonomie I/Grundlagen der Makroökonomie Kapitel 10 Wachstum Stilisierte Fakten Günter W. Beck 1 Makroökonomie I/Grundzüge der Makroökonomie Page
Einführung in die Modellierung: Statische und dynamische Bilanzgleichungen
 Einführung in die Modellierung: Statische und dynamische Bilanzgleichungen Mengenbilanzen: Beispiel 1: Kessel Wirkungsgraph Flussdiagramm Modellgleichungen Statische Mengenbilanz Deispiel 2: Chemische
Einführung in die Modellierung: Statische und dynamische Bilanzgleichungen Mengenbilanzen: Beispiel 1: Kessel Wirkungsgraph Flussdiagramm Modellgleichungen Statische Mengenbilanz Deispiel 2: Chemische
Fragen der Schüler der Birkenau-Volksschule
 Fragen der Schüler der Birkenau-Volksschule Warum gibt es Klima? Warum gibt es Wärme? Wissenschaftler können die tiefe Frage, warum es etwas überhaupt gibt, meist gar nicht beantworten. Wir befassen uns
Fragen der Schüler der Birkenau-Volksschule Warum gibt es Klima? Warum gibt es Wärme? Wissenschaftler können die tiefe Frage, warum es etwas überhaupt gibt, meist gar nicht beantworten. Wir befassen uns
Fehlerrechnung EXPERIMENTELLE FEHLER ANALYTIK II IAAC, TU-BS, 2004 ANALYTIK II IAAC, TU-BS, 2004. Dr. Andreas Martens a.mvs@tu-bs.
 Fehlerrechnung ANALYTIK II Dr. Andreas Martens a.mvs@tu-bs.de Institut f. Anorg.u. Analyt. Chemie, Technische Universität Braunschweig, Braunschweig, Germany EXPERIMENTELLE FEHLER ANALYTIK II - 2 - Signifikante
Fehlerrechnung ANALYTIK II Dr. Andreas Martens a.mvs@tu-bs.de Institut f. Anorg.u. Analyt. Chemie, Technische Universität Braunschweig, Braunschweig, Germany EXPERIMENTELLE FEHLER ANALYTIK II - 2 - Signifikante
Kohlenstoffkreislauf
 Globale Ökologie Kohlenstoffkreislauf Wintersemester 2009/2010 Heute: Christoph Müller Wolfgang Cramer Univ. Potsdam, Geoökologie, Globale Ökologie http://www.pik-potsdam.de/~cramer -> Lehre / "Teaching
Globale Ökologie Kohlenstoffkreislauf Wintersemester 2009/2010 Heute: Christoph Müller Wolfgang Cramer Univ. Potsdam, Geoökologie, Globale Ökologie http://www.pik-potsdam.de/~cramer -> Lehre / "Teaching
Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier.
 Ache2 Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier. Bsp. ph berechnen einer 0.085 mol/l salpetriger
Ache2 Kapitel 17: Weitere Aspekt. wässriger Gleichgew. Einfluss gleicher Ionen: Gleichioniger Zusatz, Verschiebung des Gleichgewichtes nach Le-Châtelier. Bsp. ph berechnen einer 0.085 mol/l salpetriger
Neue Studie zur CO2 Konzentration: Anthropogener Anteil irgendwo zwischen 0 und max 30 % -Vortrag von Prof. Murry Salby am 13.3.
 Neue Studie zur CO2 Konzentration: Anthropogener Anteil irgendwo zwischen 0 und max 30 % -Vortrag von Prof. Murry Salby am 13.3.15 in Essen Zur Zeit stellt er sich in Australien einem Tribunal, das die
Neue Studie zur CO2 Konzentration: Anthropogener Anteil irgendwo zwischen 0 und max 30 % -Vortrag von Prof. Murry Salby am 13.3.15 in Essen Zur Zeit stellt er sich in Australien einem Tribunal, das die
Expertenpuzzle Quadratische Funktionen
 Phase 1 Aufgaben für die Expertengruppe I Im Folgenden sollen die in IR definierten Funktionen a : x x, b : x x 0,5, c : x x und d: x x 3 untersucht werden. Die Abbildung zeigt den Graphen G a von a, also
Phase 1 Aufgaben für die Expertengruppe I Im Folgenden sollen die in IR definierten Funktionen a : x x, b : x x 0,5, c : x x und d: x x 3 untersucht werden. Die Abbildung zeigt den Graphen G a von a, also
CO 2 -Dynamik von Bio- und Atmosphäre in Basismodellen
 CO 2 -Dynamik von Bio- und Atmosphäre in Basismodellen R. Hohmann Otto-von-Guericke-Universität Magdeburg, ISG 39106 Magdeburg, Universitätsplatz 2 hohmann@isg.cs.uni-magdeburg.de Zusammenfassung: In einer
CO 2 -Dynamik von Bio- und Atmosphäre in Basismodellen R. Hohmann Otto-von-Guericke-Universität Magdeburg, ISG 39106 Magdeburg, Universitätsplatz 2 hohmann@isg.cs.uni-magdeburg.de Zusammenfassung: In einer
die Wachstumsrate ist proportional zur Anzahl der vorhandenen Individuen.
 Exponentielles Wachstum und Zerfall Angenommen, man möchte ein Modell des Wachstums oder Zerfalls einer Population erarbeiten, dann ist ein Gedanke naheliegend: die Wachstumsrate ist proportional zur Anzahl
Exponentielles Wachstum und Zerfall Angenommen, man möchte ein Modell des Wachstums oder Zerfalls einer Population erarbeiten, dann ist ein Gedanke naheliegend: die Wachstumsrate ist proportional zur Anzahl
