Physikalische Chemie 0 Klausur, 22. Oktober 2011
|
|
|
- Leon Busch
- vor 7 Jahren
- Abrufe
Transkript
1 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden maximal 5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden, und 50 Punkte sind notwendig, um zu bestehen. Zu keiner Frage werden negative Punkte vergeben. Nur das kann berücksichtigt werden, was abgegeben wird! Punkte Note Punkte Note Punkte Note ab bis 49 n.b Name: Matrikelnummer: Platznummer: 1
2 Für Notizen, Zwischenrechnungen, etc. 2
3 Name: Matrikelnummer: Platznummer: Frage 1. Ein Körper mit einer Masse von 400 g, einer Molenmasse von 32 g/mol, einer molaren Wärmekapazität von 4 kj/(mol K) und einer Temperatur von 80 C wird in einer Flüssigkeit mit Temperatur 20 C gebracht. Die Flüssigkeit hat eine molare Wärmekapazität von 6 kj/(mol K). Wie viele Mol der Flüssigkeit braucht man, damit die Gleichgewichtstemperatur 35 C wird? Frage 2. Betrachten Sie ein ideales Gas in einem Behälter mit Volumen V 0, Druck P 0 und Temperatur T 0. In einem isochoren Prozess wird der Druck verdoppelt. Anschließend wird das Volumen halbiert in einem isobaren Prozess. Und zuletzt in einem isothermen Prozess wird der Druck halbiert. Welche Werte haben Druck, Volumen und Temperatur (ausgedruckt mit Hilfe von V 0, P 0 und T 0 ) am Ende der drei Prozesse? 3
4 Frage 3. Betrachten Sie die Größe Z = nrt PV dp und dv aus. für ein van der Waals Gas. Drucken Sie dz mit Hilfe von Frage 4. Bestimmen Sie ( ) V P T ( P ) ( T ) T V V P für ein ideales Gas. Frage 5. Betrachten Sie eine Mischung aus drei idealen Gase, A, B und C. Der Partialdruck vom A ist gleich 2 bar, und der vom C ist gleich 0.8 bar. Der Molenbruch von B ist gleich x B = 0.3. Bestimmen Sie den Gesamtdruck sowie die Molenbrüche von A und C. 4
5 Name: Matrikelnummer: Platznummer: Frage 6. Erläutern Sie kurz, wie Gay-Lussac herausfand, dass ( ) U V T = 0 für ein ideales Gas gilt. Frage 7. Betrachten Sie eine flüssige Mischung bestehend aus 200 mol vom Stoff A und 300 mol vom Stoff B. Durch Zugabe von 0.01 mol vom Stoff A ändert sich das Gesamtvolumen um 0.03 l, während die Zugabe von 0.02 mol vom Stoff B zu einer Änderung des Gesamtvolumens um 0.04 l führt. Bestimmen Sie daraus die partiellen molaren Volumina vom Stoff A und Stoff B für die Mischung. 5
6 Frage 8. 4 mol von Stoff A werden mit 2 mol von Stoff B gemischt. Sie reagieren miteinander laut der chemischen Reaktion A + 2 B C. Im Gleichgewicht ist der Molenbruch vom Stoff C gleich 0.2. Bestimmen Sie daraus die Stoffmengen von A, B und C. Frage 9. Für die drei chemischen Reaktionen A + 2 B 2 C, B + D A und B + D C sind die Reaktionsenthalpien gleich 150, 200 und 400 kj/mol. Bestimmen Sie daraus die Reaktionsenthalpie für die Reaktion D B. Frage 10. Die Reaktionsenthalpie für die Reaktion A + 2 B 2 C beträgt bei 25 C 150 kj/mol. Die molaren Wärmekapazitäten der drei Stoffe A, B und C sind gleich 500, 400 und 300 J/(mol K). Bestimmen Sie daraus die Reaktionsenthalpie für die Reaktion 1 2 A + B C bei 50 C. 6
7 Name: Matrikelnummer: Platznummer: Frage 11. Erläutern Sie den Begriff Verbrennungsenthalpie. Frage 12. Was muss für einen beliebigen Kreisprozess gelten, damit sein thermischer Nutzeffekt so groß ist wie der eines Carnot Kreisprozesses? Begründen Sie die Antwort. 7
8 Frage 13. Betrachten Sie ein System bestehend aus zwei nicht-mischbaren Lösungsmitteln. In beiden Phasen läuft die chemische Reaktion A + B 2 C ab. Im Gleichgewicht ist das chemische Potential vom Stoff A in der einen Phase gleich 20 J/mol, während das chemische Potential vom Stoff C in der anderen Phase gleich 40 J/mol ist. Bestimmen Sie daraus das chemische Potential für alle drei Stoffe in den beiden Phasen. Frage 14. Benutzen Sie das Gesetz der Gleichverteilung der Energie, um die molare Wärmekapazitäten von H 2 O und (linearem) CO 2 zu bestimmen. Die Ergebnisse sollen mit Hilfe der Gaskonstante ausgedruckt werden. Frage 15. Betrachten Sie ein Gas aus Teilchen bei einer Temperatur T 0. Die einzelnen Teilchen können die Energie kt 0, 0 und +kt 0 besitzen (k ist die Boltzmann Konstante). Bestimmen Sie daraus die durchschnittliche Energie der Teilchen. 8
9 Name: Matrikelnummer: Platznummer: Frage 16. Vergleichen Sie graphisch das Gesetz von Dulong und Petit mit den Vorhersagen der Modelle von Einstein und Debye und mit experimentellen Befunden. Worum geht es überhaupt? Frage 17. Was beschreibt der Welle-Teilchen Dualismus? 9
10 Frage 18. Erläutern Sie den Zusammenhang zwischen Spektren und Quantentheorie. Frage 19. Betrachten Sie ein Teilchen in einem ein-dimensionalen Kasten, 0 x a. Bei welchen x Werten hat das Teilchen die größte Wahrscheinlichkeit, sich aufzuhalten, wenn das Teilchen sich im Grundzustand, n = 1, bzw. im ersten angeregten Zustand, n = 2, befindet? Begründen Sie die Antwort. Frage 20. Für ein Teilchen (Masse gleich kg) in einem ein-dimensionalen Kasten mit Kastenlänge 1 nm ist die Energie für den Übergang n = 2 n = 3 gleich 4 ev. Wie groß ist dann die Energie für den Übergang n = 2 n = 4, wenn sich die Kastenlänge auf 2 nm ändert? 10
11 Name: Matrikelnummer: Platznummer: Frage 21. Erklären Sie den Begriff Nullpunktsenergie. Frage 22. Betrachten Sie die 1s Wellenfunktion des Wasserstoffatoms. Wo hat diese Funktion ihr Maximum, und wo ist die radiale Verteilung dieser Funktion am größten? 11
12 Frage 23. Erläutern Sie kurz Hund s Regeln. Frage 24. Vergleichen Sie bindende und antibindende σ und π Orbitale am Beispiel des N 2 Moleküls. Frage 25. Betrachten Sie zwei Reaktionen A + 2 B 2 C und C + D B, die gleichzeitig ablaufen. Die Geschwindigkeitskonstanten der beiden Reaktionen werden gleich k 1 und k 2 genannt. Stellen Sie Ausdrucke für [X] t auf mit X gleich A, B, C und D. 12
Repetitorium Physikalische Chemie für Lehramt
 Repetitorium Physikalische Chemie für Lehramt Anfangstext bei der Prüfung. Hier nicht relevant. Zu jeder der 10 Fragen werden maximal 12,5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Repetitorium Physikalische Chemie für Lehramt Anfangstext bei der Prüfung. Hier nicht relevant. Zu jeder der 10 Fragen werden maximal 12,5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Physikalische Chemie für Bioinformatik. Frühere Klausuraufgaben
 Physikalische Chemie für Bioinformatik. Frühere Klausuraufgaben Bei jeder Klausur gibt es 25 Fragen. Zu jeder der 25 Fragen werden maximal 5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Physikalische Chemie für Bioinformatik. Frühere Klausuraufgaben Bei jeder Klausur gibt es 25 Fragen. Zu jeder der 25 Fragen werden maximal 5 Punkte vergeben. Höchstens 100 Punkte können erreicht werden,
Klausur zu Grundlagen der Physikalischen Chemie (21371) - Teil 1
 Klausur zu Grundlagen der Physikalischen Chemie (21371) - Teil 1 Name: Mat.Nr.: Punkte: /50 Zur Bearbeitung der folgenden Aufgaben haben Sie 90 Minuten Zeit. Antworten dürfen in Form von Stichpunkten gegeben
Klausur zu Grundlagen der Physikalischen Chemie (21371) - Teil 1 Name: Mat.Nr.: Punkte: /50 Zur Bearbeitung der folgenden Aufgaben haben Sie 90 Minuten Zeit. Antworten dürfen in Form von Stichpunkten gegeben
a) Welche der folgenden Aussagen treffen nicht zu? (Dies bezieht sind nur auf Aufgabenteil a)
 Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Aufgabe 1: Multiple Choice (10P) Geben Sie an, welche der Aussagen richtig sind. Unabhängig von der Form der Fragestellung (Singular oder Plural) können eine oder mehrere Antworten richtig sein. a) Welche
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Erreichte Punktzahlen: Die Bearbeitungszeit beträgt 3 Stunden.
 Fakultät für Physik der LMU München Prof. Ilka Brunner Michael Kay Vorlesung T4, WS11/12 Klausur am 18. Februar 2012 Name: Matrikelnummer: Erreichte Punktzahlen: 1 2 3 4 5 6 Hinweise Die Bearbeitungszeit
Fakultät für Physik der LMU München Prof. Ilka Brunner Michael Kay Vorlesung T4, WS11/12 Klausur am 18. Februar 2012 Name: Matrikelnummer: Erreichte Punktzahlen: 1 2 3 4 5 6 Hinweise Die Bearbeitungszeit
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13. Klausur PC 1. Sommersemester :15 bis 11:45.
 Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13 Klausur PC 1 Sommersemester 2009 03.08.2007 10:15 bis 11:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) SS09 - Blatt 1 von 13 Klausur PC 1 Sommersemester 2009 03.08.2007 10:15 bis 11:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti.
 (c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
(c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
Klausur Bachelorstudiengang CBI / CEN / LSE. Physikalische Chemie
 Bachelorstudiengang CBI / CEN/ LSE - Physikalische Chemie SS12 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / CEN / LSE Physikalische Chemie 24.09.2012 Name: Vorname: geb. am: in: Studienfach: Matrikelnummer:
Bachelorstudiengang CBI / CEN/ LSE - Physikalische Chemie SS12 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / CEN / LSE Physikalische Chemie 24.09.2012 Name: Vorname: geb. am: in: Studienfach: Matrikelnummer:
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen!
 1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
1. Klausur ist am 5.12.! (für Vets sowie Bonuspunkte für Zahni-Praktikum) Jetzt lernen! http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ****** Druck und Volumen Gesetz von Boyle-Mariotte:
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Name, Vorname (bitte leserlich) Studiengang Matr. Nr. oder Pseudonym Σ
 Name, Vorname (bitte leserlich) Studiengang Matr. Nr. oder Pseudonym... LA CHE DS BIO... 1 2 3 4 5 6 7 8 Σ bestanden (7) (4) (4) (3) (10) (6) (6) (4) Klausur zum Grundpraktikum Physikalische Chemie im
Name, Vorname (bitte leserlich) Studiengang Matr. Nr. oder Pseudonym... LA CHE DS BIO... 1 2 3 4 5 6 7 8 Σ bestanden (7) (4) (4) (3) (10) (6) (6) (4) Klausur zum Grundpraktikum Physikalische Chemie im
Physik III im Studiengang Elektrotechnik
 Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Physik III im Studiengang Elektrotechnik - Einführung in die Wärmelehre - Prof. Dr. Ulrich Hahn WS 2008/09 Entwicklung der Wärmelehre Sinnesempfindung: Objekte warm kalt Beschreibung der thermische Eigenschaften
Probeklausur STATISTISCHE PHYSIK PLUS
 DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
DEPARTMENT FÜR PHYSIK, LMU Statistische Physik für Bachelor Plus WS 2011/12 Probeklausur STATISTISCHE PHYSIK PLUS NAME:... MATRIKEL NR.:... Bitte beachten: Schreiben Sie Ihren Namen auf jedes Blatt; Schreiben
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) WS09/10 - Blatt 1 von 13. Klausur PC 1
 Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) WS09/10 - Blatt 1 von 13 Klausur PC 1 Wintersemester 2009/10-20.10.2009 Hörsaal H2 15:15 bis 16:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift:
Physikalische Chemie 1 (Thermodyn. u. Elektrochemie) WS09/10 - Blatt 1 von 13 Klausur PC 1 Wintersemester 2009/10-20.10.2009 Hörsaal H2 15:15 bis 16:45 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift:
PC-Übung Nr.3 vom
 PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
Klausur Thermodynamik E2/E2p SoSe 2019 Braun. Formelsammlung Thermodynamik
 Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene)
 Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Vorbemerkung. [disclaimer]
![Vorbemerkung. [disclaimer] Vorbemerkung. [disclaimer]](/thumbs/97/130802699.jpg) orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Der Zustand eines Systems ist durch Zustandsgrößen charakterisiert.
 Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Klausur Physikalische Chemie für TUHH (Chemie III)
 07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Grundlagen der Physik II
 Grundlagen der Physik II Othmar Marti 05. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 05. 07. 2007 Klausur Die Klausur
Grundlagen der Physik II Othmar Marti 05. 07. 2007 Institut für Experimentelle Physik Physik, Wirtschaftsphysik und Lehramt Physik Seite 2 Wärmelehre Grundlagen der Physik II 05. 07. 2007 Klausur Die Klausur
Musterlösung Thermodynamik 3 Besprechung in der Woche vom bis
 E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Musterlösung 3 Musterlösung Thermodynamik 3 Besprechung in der Woche vom 30.04.18 bis 04.05.18 Anmerkung: Es wird jede Aufgabe bepunktet, nicht jede
E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Musterlösung 3 Musterlösung Thermodynamik 3 Besprechung in der Woche vom 30.04.18 bis 04.05.18 Anmerkung: Es wird jede Aufgabe bepunktet, nicht jede
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Klausur Bachelorstudiengang CBI / LSE Prüfung Modul Physikalische Chemie und Thermodynamik. Physikalische Chemie
 Bachelorstudiengang CBI / LSE - Teil Physikalische Chemie - SS09 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / LSE Prüfung Modul Physikalische Chemie und Thermodynamik Physikalische Chemie 25.03.2010
Bachelorstudiengang CBI / LSE - Teil Physikalische Chemie - SS09 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / LSE Prüfung Modul Physikalische Chemie und Thermodynamik Physikalische Chemie 25.03.2010
PC I Thermodynamik und Transportprozesse
 20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
20.06.2006 15:19 1 PC I Thermodynamik und Transportprozesse Kapitel 5 20.06.2006 15:19 2 V. Lösungen und Mischungen Im Winter des Jahres 1729 setzte ich Bier, Wein, Essig und Salzwasser in großen offenen
3 Der 1. Hauptsatz der Thermodynamik
 3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
Klausur Bachelorstudiengang Prüfung Modul Physikalische Chemie und Thermodynamik. Teil 1: Physikalische Chemie
 Bachelorstudiengang / Diplomstudiengang CBI - Teil Physikalische Chemie - WS0809 - Blatt 1 / 16 Klausur Bachelorstudiengang Prüfung Modul Physikalische Chemie und Thermodynamik Teil 1: Physikalische Chemie
Bachelorstudiengang / Diplomstudiengang CBI - Teil Physikalische Chemie - WS0809 - Blatt 1 / 16 Klausur Bachelorstudiengang Prüfung Modul Physikalische Chemie und Thermodynamik Teil 1: Physikalische Chemie
Physikdepartment. Ferienkurs zur Experimentalphysik 4. Daniel Jost 10/09/15
 Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Bernhard Härder. Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik W/ WESTAR.P WISSENSCHAFTEN. Skripte, Lehrbücher Band 2
 Bernhard Härder Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik Skripte, Lehrbücher Band 2 W/ WESTAR.P WISSENSCHAFTEN Inhaltsverzeichnis Vorwort zur ersten Auflage Vorwort zur
Bernhard Härder Einführung in die PHYSIKALISCHE CHEMIE ein Lehrbuch Chemische Thermodynamik Skripte, Lehrbücher Band 2 W/ WESTAR.P WISSENSCHAFTEN Inhaltsverzeichnis Vorwort zur ersten Auflage Vorwort zur
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Modelle zur Beschreibung von Gasen und deren Eigenschaften
 Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Prof. Dr. Norbert Hampp 1/7 1. Das Ideale Gas Modelle zur Beschreibung von Gasen und deren Eigenschaften Modelle = vereinfachende mathematische Darstellungen der Realität Für Gase wollen wir drei Modelle
Grundlagen der Quantentheorie
 Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Grundlagen der Quantentheorie Ein Schwarzer Körper (Schwarzer Strahler, planckscher Strahler, idealer schwarzer Körper) ist eine idealisierte thermische Strahlungsquelle: Alle auftreffende elektromagnetische
Musterlösung Klausur Physikalische Chemie I: Thermodynamik
 Musterlösung Klausur Physikalische Chemie I: hermodynamik Aufgabe : Dimerisierung von Stickstoffdioxid a Nach dem Prinzip des kleinsten Zwanges von LeChatelier sollte der Druck p möglichst klein und die
Musterlösung Klausur Physikalische Chemie I: hermodynamik Aufgabe : Dimerisierung von Stickstoffdioxid a Nach dem Prinzip des kleinsten Zwanges von LeChatelier sollte der Druck p möglichst klein und die
Thermodynamik I Formeln
 Thermodynamik I Formeln Tobi 4. September 2006 Inhaltsverzeichnis Thermodynamische Systeme 3. Auftriebskraft........................................ 3 2 Erster Hauptsatz der Thermodynamik 3 2. Systemenergie........................................
Thermodynamik I Formeln Tobi 4. September 2006 Inhaltsverzeichnis Thermodynamische Systeme 3. Auftriebskraft........................................ 3 2 Erster Hauptsatz der Thermodynamik 3 2. Systemenergie........................................
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14,
 ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
ÜBUNGEN ZUR VORLESUNG Physikalische Chemie I (PC I) (Prof. Meerholz, Hertel, Klemmer) Blatt 14, 12.02.2016 Aufgabe 1 Kreisprozesse Mit einem Mol eines idealen, monoatomaren Gases (cv = 3/2 R) wird, ausgehend
1. Klausur zur Vorlesung Physikalische Chemie I
 1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
Physikalische Chemie Physikalische Chemie I SoSe 2009 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas. Thermodynamik
 Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Prof. Dr. Norbert Hampp 1/9 1. Das Ideale Gas Thermodynamik Teilgebiet der klassischen Physik. Wir betrachten statistisch viele Teilchen. Informationen über einzelne Teilchen werden nicht gewonnen bzw.
Übung 2. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Lehrbuch der Thermodynamik
 Ulrich Nickel Lehrbuch der Thermodynamik Eine verständliche Einführung Ж HANSER Carl Hanser Verlag München Wien VII Inhaltsverzeichnis 1 GRUNDBEGRIFFE DER THERMODYNAMIK 1 Einführung 1 Systeme 3 offene
Ulrich Nickel Lehrbuch der Thermodynamik Eine verständliche Einführung Ж HANSER Carl Hanser Verlag München Wien VII Inhaltsverzeichnis 1 GRUNDBEGRIFFE DER THERMODYNAMIK 1 Einführung 1 Systeme 3 offene
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludigs-Universität Freiburg Lösungen zum 4. Übungsblatt zur orlesung Physikalische Chemie I SS 00 Prof. Dr. Bartsch 4. (6 Punkte) In einem Behälter mit der Grundfläche
Institut für Physikalische Chemie Albert-Ludigs-Universität Freiburg Lösungen zum 4. Übungsblatt zur orlesung Physikalische Chemie I SS 00 Prof. Dr. Bartsch 4. (6 Punkte) In einem Behälter mit der Grundfläche
Klausur Bachelorstudiengang CBI / LSE. Physikalische Chemie
 Bachelorstudiengang CBI / LSE - Teil Physikalische Chemie SS10 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / LSE Physikalische Chemie 27.09.2010 Name: Vorname: geb. am: in: Studienfach: Matrikelnummer:
Bachelorstudiengang CBI / LSE - Teil Physikalische Chemie SS10 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / LSE Physikalische Chemie 27.09.2010 Name: Vorname: geb. am: in: Studienfach: Matrikelnummer:
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Reale Gase. Versuch: RG. Inhaltsverzeichnis. Fachrichtung Physik. Erstellt: E. Beyer Aktualisiert: am Physikalisches Grundpraktikum
 Versuch: RG Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: E. Beyer Aktualisiert: am 01. 10. 2010 Bearbeitet: J. Kelling F. Lemke S. Majewsky M. Justus Reale Gase Inhaltsverzeichnis 1 Aufgabenstellung
Versuch: RG Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: E. Beyer Aktualisiert: am 01. 10. 2010 Bearbeitet: J. Kelling F. Lemke S. Majewsky M. Justus Reale Gase Inhaltsverzeichnis 1 Aufgabenstellung
Klausur Wärmelehre E2/E2p SoSe 2016 Braun. Formelsammlung Thermodynamik
 Klausur Wärmelehre E2/E2p SoSe 2016 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Wärmelehre E2/E2p SoSe 2016 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Bachelorstudiengang CBI / CEN / LSE. Physikalische Chemie
 Bachelorstudiengang CBI / CEN/ LSE - Physikalische Chemie SS14 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / CEN / LSE Physikalische Chemie 12.09.2014 Name: Vorname: geb. am: in: Studienfach: Matrikelnummer:
Bachelorstudiengang CBI / CEN/ LSE - Physikalische Chemie SS14 - Blatt 1 / 15 Klausur Bachelorstudiengang CBI / CEN / LSE Physikalische Chemie 12.09.2014 Name: Vorname: geb. am: in: Studienfach: Matrikelnummer:
Die innere Energie and die Entropie
 Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Die innere Energie and die Entropie Aber fangen wir mit der Entropie an... Stellen Sie sich ein System vor, das durch die Entropie S, das Volumen V und die Stoffmenge n beschrieben wird. U ' U(S,V,n) Wir
Physikalisches Anfaengerpraktikum. Zustandsgleichung idealer Gase und kritischer Punkt
 Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Physikalisches Anfaengerpraktikum Zustandsgleichung idealer Gase und kritischer Punkt Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe 37) Freitag, 18. März 005 email: Marcel.Engelhardt@mytum.de
Q i + j. dτ = i. - keine pot. und kin. Energien: depot. - adiabate ZÄ: Q i = 0 - keine technische Arbeit: Ẇ t,j = 0
 Institut für hermodynamik hermodynamik - Formelsammlung. Hauptsätze der hermodynamik (a. Hauptsatz der hermodynamik i. Offenes System de = de pot + de kin + du = i Q i + j Ẇ t,j + ein ṁ ein h tot,ein aus
Institut für hermodynamik hermodynamik - Formelsammlung. Hauptsätze der hermodynamik (a. Hauptsatz der hermodynamik i. Offenes System de = de pot + de kin + du = i Q i + j Ẇ t,j + ein ṁ ein h tot,ein aus
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009)
 Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
Musterlösung Klausur Physikalische Chemie I: Thermodynamik (Januar 2009) Aufgabe 1: Reaktionsthermodynamik a) möglichst niedrige Temeratur (begünstigt exotherme Reaktionen) möglichst hoher Druck (begünstigt
Thermodynamik 1 Klausur 08. September 2016
 Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
Thermodynamik 1 Klausur 08. September 2016 Bearbeitungszeit: 150 Minuten Umfang der Aufgabenstellung: 7 nummerierte Seiten Alle Unterlagen zur Vorlesung und Übung sowie Lehrbücher und Taschenrechner sind
1. Klausur: Veranstaltung Allgemeine und Anorganische Chemie
 1. Klausur: Veranstaltung Allgemeine und Anorganische Chemie Geowissenschaften (BSc, Diplom), Mathematik (BSc, Diplom), Informatik mit Anwendungsfach Chemie und andere Naturwissenschaften 1. Klausur Modulbegleitende
1. Klausur: Veranstaltung Allgemeine und Anorganische Chemie Geowissenschaften (BSc, Diplom), Mathematik (BSc, Diplom), Informatik mit Anwendungsfach Chemie und andere Naturwissenschaften 1. Klausur Modulbegleitende
Temperatur. Temperaturmessung. Grundgleichung der Kalorik. 2 ² 3 2 T - absolute Temperatur / ºC T / K
 Temperatur Temperatur ist ein Maß für die mittlere kinetische Energie der Teilchen 2 ² 3 2 T - absolute Temperatur [ T ] = 1 K = 1 Kelvin k- Boltzmann-Konst. k = 1,38 10-23 J/K Kelvin- und Celsiusskala
Temperatur Temperatur ist ein Maß für die mittlere kinetische Energie der Teilchen 2 ² 3 2 T - absolute Temperatur [ T ] = 1 K = 1 Kelvin k- Boltzmann-Konst. k = 1,38 10-23 J/K Kelvin- und Celsiusskala
Die Zustandsgleichung realer Gase
 Die Zustandsgleichung realer Gase Grolik Benno, Kopp Joachim 2. Januar 2003 1 Grundlagen des Versuchs Der Zustand eines idealen Gases wird durch die drei elementaren Zustandsgrößen Druck p, Temperatur
Die Zustandsgleichung realer Gase Grolik Benno, Kopp Joachim 2. Januar 2003 1 Grundlagen des Versuchs Der Zustand eines idealen Gases wird durch die drei elementaren Zustandsgrößen Druck p, Temperatur
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 12.12.2014 Gase Flüssigkeiten Feststoffe Wiederholung Teil 2 (05.12.2014) Ideales Gasgesetz: pv Reale Gase: Zwischenmolekularen Wechselwirkungen
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Aufgaben zur Experimentalphysik II: Thermodynamik
 Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5//8 1. 1. Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 +
Van der Waals-Theorie und Zustandsgleichung
 Van der Waals-Theorie und Zustandsgleichung Eine verbesserte Zustandsgleichung für klassische Gase bei höheren Dichten liefert die Van der Waals-Gleichung. Diese Gleichung beschreibt auch den Phasenübergang
Van der Waals-Theorie und Zustandsgleichung Eine verbesserte Zustandsgleichung für klassische Gase bei höheren Dichten liefert die Van der Waals-Gleichung. Diese Gleichung beschreibt auch den Phasenübergang
2 Wärmelehre. Reibungswärme Reaktionswärme Stromwärme
 2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
f) Ideales Gas - mikroskopisch
 f) Ideales Gas - mikroskopisch i) Annahmen Schon gehabt: Massenpunkte ohne Eigenvolumen Nur elastische Stöße, keine Wechselwirkungen Jetzt dazu: Wände vollkommen elastisch, perfekte Reflektoren Zeitliches
f) Ideales Gas - mikroskopisch i) Annahmen Schon gehabt: Massenpunkte ohne Eigenvolumen Nur elastische Stöße, keine Wechselwirkungen Jetzt dazu: Wände vollkommen elastisch, perfekte Reflektoren Zeitliches
Höhere Experimentalphysik 1
 Höhere Experimentalphysik 1 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 9. Vorlesung 20.01.2017 Was bisher geschah Thermodynamik Thermodynamische Systeme und Zustandsgrößen Gleichgewichtszustand
Höhere Experimentalphysik 1 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 9. Vorlesung 20.01.2017 Was bisher geschah Thermodynamik Thermodynamische Systeme und Zustandsgrößen Gleichgewichtszustand
2 Grundbegriffe der Thermodynamik
 2 Grundbegriffe der Thermodynamik 2.1 Thermodynamische Systeme (TDS) Aufteilung zwischen System und Umgebung (= Rest der Welt) führt zu einer Klassifikation der Systeme nach Art der Aufteilung: Dazu: adiabatisch
2 Grundbegriffe der Thermodynamik 2.1 Thermodynamische Systeme (TDS) Aufteilung zwischen System und Umgebung (= Rest der Welt) führt zu einer Klassifikation der Systeme nach Art der Aufteilung: Dazu: adiabatisch
E2: Wärmelehre und Elektromagnetismus 4. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 4. Vorlesung 19.04.2018 Heute: - Freiheitsgrade realer Gase - Adiabatische Volumenänderungen - Kurze Einführung in die Quantenmechanik - Freiheitsgrade & Wärmekapazität
E2: Wärmelehre und Elektromagnetismus 4. Vorlesung 19.04.2018 Heute: - Freiheitsgrade realer Gase - Adiabatische Volumenänderungen - Kurze Einführung in die Quantenmechanik - Freiheitsgrade & Wärmekapazität
Physikalische Aspekte der Respiration
 Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
Physikalische Aspekte der Respiration Christoph Hitzenberger Zentrum für Biomedizinische Technik und Physik Themenübersicht Physik der Gase o Ideale Gasgleichung o Atmosphärische Luft o Partialdruck Strömungsmechanik
1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus.
 1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus. kann mit der Umgebung Energie austauschen. kann mit der Umgebung Entropie
1) Ein offenes System zeichnet sich immer durch eine konstante Temperatur aus. zeichnet sich immer durch eine konstante Masse aus. kann mit der Umgebung Energie austauschen. kann mit der Umgebung Entropie
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
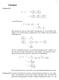 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
E2: Wärmelehre und Elektromagnetismus 3. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 3. Vorlesung 16.04.2018 https://xkcd.com/1978/ Heute: - Gleichverteilungssatz - 1. Hauptsatz - Volumenarbeit - Wärmekapazität - Wärmekapazität des idealen Gases -
E2: Wärmelehre und Elektromagnetismus 3. Vorlesung 16.04.2018 https://xkcd.com/1978/ Heute: - Gleichverteilungssatz - 1. Hauptsatz - Volumenarbeit - Wärmekapazität - Wärmekapazität des idealen Gases -
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I Dr. Helge Klemmer
 Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Mathematisch-Naturwissenschaftliche Grundlegung WS 2014/15 Chemie I 05.12.2014 Wiederholung Teil 1 (28.11.2014) Fragenstellungen: Druckanstieg im Reaktor bei Temeraturerhöhung und Produktbildung? Wie groß
Karlsruher Institut für Technologie Festkörperphysik. Übungen zur Theoretischen Physik F SS 10
 Karlsruher Institut für Technologie Institut für Theoretische Festkörperphysik Übungen zur Theoretischen Physik F SS 10 Prof. Dr. G. Schön Lösungsvorschlag zu Blatt 2 Dr. J. Cole 30.04.2010 1. Van-der-Waals
Karlsruher Institut für Technologie Institut für Theoretische Festkörperphysik Übungen zur Theoretischen Physik F SS 10 Prof. Dr. G. Schön Lösungsvorschlag zu Blatt 2 Dr. J. Cole 30.04.2010 1. Van-der-Waals
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg
 Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Institut für Physikalische Chemie Albert-Ludwigs-Universität Freiburg Lösungen zum Übungsblatt 4 zur Vorlesung Physikalische Chemie II WS 2008/09 Prof. E. Bartsch 4.1 Der Siedepunkt einer flüssigen Mischung
Nachklausur zum Modul Physikalische Chemie 1
 Nachklausur zum Modul Physikalische Chemie 1 Sommersemester 2007 Wintersemester 2007 / 08 29. Januar 2008 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort...
Nachklausur zum Modul Physikalische Chemie 1 Sommersemester 2007 Wintersemester 2007 / 08 29. Januar 2008 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort...
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen
 Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen Lennart Schmidt 08.09.2011 Inhaltsverzeichnis 1 Grundlagen 3 1.1 Temperatur und Wärme............................ 3 1.2 0. und 1. Hauptsatz..............................
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht
 8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
8.2 Thermodynamische Gleichgewichte, insbesondere Gleichgewichte in Mehrkomponentensystemen Mechanisches und thermisches Gleichgewicht 8.2-1 Stoffliches Gleichgewicht Beispiel Stickstoff Sauerstoff: Desweiteren
Schriftliche Leistungsüberprüfung PC/CBI
 Abschlusstest - Physikalische Chemie CBI/LSE - SS08 - Blatt 1 Schriftliche Leistungsüberprüfung PC/CBI SS08-25.07.2008 Hörsaal H1/H2 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die Beantwortung
Abschlusstest - Physikalische Chemie CBI/LSE - SS08 - Blatt 1 Schriftliche Leistungsüberprüfung PC/CBI SS08-25.07.2008 Hörsaal H1/H2 Name: Vorname: geb. am: in: Matrikelnummer: Unterschrift: Für die Beantwortung
Formelzeichen Bedeutung Wert / SI-Einheit
 CHEMISCHE THERMODYNAMI SYMBOLE UND ONSTANTEN PROF. DR. WOLFGANG CHRISTEN Formelzeichen Bedeutung Wert / SI-Einheit AA Fläche m 2 AA Freie Energie, Helmholtz-Energie Nm = aa Beschleunigung m aa ii CC pp
CHEMISCHE THERMODYNAMI SYMBOLE UND ONSTANTEN PROF. DR. WOLFGANG CHRISTEN Formelzeichen Bedeutung Wert / SI-Einheit AA Fläche m 2 AA Freie Energie, Helmholtz-Energie Nm = aa Beschleunigung m aa ii CC pp
Klausur zur Vorlesung Physikalische Chemie II: Aufbau der Materie / Kinetik
 Name:... Vorname:... Matrikelnummer:. geb. am:... in:... Klausur zur Vorlesung Physikalische Chemie II: Aufbau der Materie / Kinetik WS 2007/2008 am 5.02.2008 Zugelassene Hilfsmittel: Taschenrechner. Naturkonstanten
Name:... Vorname:... Matrikelnummer:. geb. am:... in:... Klausur zur Vorlesung Physikalische Chemie II: Aufbau der Materie / Kinetik WS 2007/2008 am 5.02.2008 Zugelassene Hilfsmittel: Taschenrechner. Naturkonstanten
Die Zusammensetzung am Ausgang der 1. Verdampfereinheit (0) kann aus dem beigefügten T, x-diagramm abgelesen werden zu
 Fragenteil : Aufgabe 1 Phasengleichgewichte 15 P a Eine binäre Mischung wird in einer Verdamfereinheit kontinuierlich teilweise verdamft. Messtechnisch wurden für die Ausgangsströme der Temeratur, der
Fragenteil : Aufgabe 1 Phasengleichgewichte 15 P a Eine binäre Mischung wird in einer Verdamfereinheit kontinuierlich teilweise verdamft. Messtechnisch wurden für die Ausgangsströme der Temeratur, der
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Lösungsvorschlag zu Übung 11
 PCI Thermodynamik G. Jeschke FS 2015 Lösungsvorschlag zu Übung 11 (Version vom 28.04.2015) Aufgabe 1 Alle Reaktionsgleichgewichte stellen sich bei 1000 K ein, damit sind alle Komponenten stets gasförmig.
PCI Thermodynamik G. Jeschke FS 2015 Lösungsvorschlag zu Übung 11 (Version vom 28.04.2015) Aufgabe 1 Alle Reaktionsgleichgewichte stellen sich bei 1000 K ein, damit sind alle Komponenten stets gasförmig.
Klausur Wärmelehre E2/E2p, SoSe 2012 Braun. Formelsammlung Thermodynamik
 Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg
![2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg 2. Fluide Phasen. 2.1 Die thermischen Zustandsgrößen Masse m [m] = kg](/thumbs/75/72774995.jpg) 2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
2. Fluide Phasen 2.1 Die thermischen Zustandsgrößen 2.1.1 Masse m [m] = kg bestimmbar aus: Newtonscher Bewegungsgleichung (träge Masse): Kraft = träge Masse x Beschleunigung oder (schwere Masse) Gewichtskraft
Spezifische Wärme fester Körper
 1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
1 Spezifische ärme fester Körper Die spezifische, sowie die molare ärme von Kupfer und Aluminium sollen bestimmt werden. Anhand der molaren ärme von Kupfer bei der Temperatur von flüssigem Stickstoff soll
Lösungsvorschlag Übung 1
 Lösungsvorschlag Übung Aufgabe : Physikalische Einheiten a) Es existieren insgesamt sieben Basisgrössen im SI-System. Diese sind mit der zugehörigen physikalischen Einheit und dem Einheitenzeichen in der
Lösungsvorschlag Übung Aufgabe : Physikalische Einheiten a) Es existieren insgesamt sieben Basisgrössen im SI-System. Diese sind mit der zugehörigen physikalischen Einheit und dem Einheitenzeichen in der
E2: Wärmelehre und Elektromagnetismus 7. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 7. Vorlesung 30.04.2018 Heute: - 2. Hauptsatz - Boltzmann-Verteilung https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 30.04.2018 Prof. Dr. Jan Lipfert
E2: Wärmelehre und Elektromagnetismus 7. Vorlesung 30.04.2018 Heute: - 2. Hauptsatz - Boltzmann-Verteilung https://xkcd.com/1166/ Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de 30.04.2018 Prof. Dr. Jan Lipfert
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
Musterlösung Übung 10
 Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Musterlösung Übung 10 Aufgabe 1: Phasendiagramme Abbildung 1-1: Skizzen der Phasendiagramme von Wasser (links) und Ethanol (rechts). Die Steigung der Schmelzkurven sind zur besseren Anschaulichkeit überzogen
Erreichte Punktzahlen: Die Bearbeitungszeit beträgt 3 Stunden.
 Fakultät für Physik der LMU München Prof. Ilka Brunner Vorlesung T4p, WS08/09 Klausur am 11. Februar 2009 Name: Matrikelnummer: Erreichte Punktzahlen: 1.1 1.2 1.3 2.1 2.2 2.3 2.4 Hinweise Die Bearbeitungszeit
Fakultät für Physik der LMU München Prof. Ilka Brunner Vorlesung T4p, WS08/09 Klausur am 11. Februar 2009 Name: Matrikelnummer: Erreichte Punktzahlen: 1.1 1.2 1.3 2.1 2.2 2.3 2.4 Hinweise Die Bearbeitungszeit
Beispielaufgaben IChO 2. Runde 2019 Grundlagen der Thermodynamik, Lösungen. = -0,900 kj/k (21,84 22,15) K / 13,16 g = 0,279 kj / 13,16 g
 Lösung Beispiel 1 Erhaltung der Energie a) ZnSO 4(s) ZnSO 4(aq): Lösungsenthalpie Lsg (ZnSO 4) = -0,900 kj/k (23,52 22,55) K / 1,565 g = -0,873 kj / 1,565 g mit (ZnSO 4) = 161,48 g/mol: Lsg (ZnSO 4) =
Lösung Beispiel 1 Erhaltung der Energie a) ZnSO 4(s) ZnSO 4(aq): Lösungsenthalpie Lsg (ZnSO 4) = -0,900 kj/k (23,52 22,55) K / 1,565 g = -0,873 kj / 1,565 g mit (ZnSO 4) = 161,48 g/mol: Lsg (ZnSO 4) =
6.2 Temperatur und Boltzmann Verteilung
 222 KAPITEL 6. THERMODYNAMIK UND WÄRMELEHRE 6.2 Temperatur und Boltzmann Verteilung Im letzten Abschnitt haben wir gesehen, dass eine statistische Verteilung von Atomen eines idealen Gases in einem Volumen
222 KAPITEL 6. THERMODYNAMIK UND WÄRMELEHRE 6.2 Temperatur und Boltzmann Verteilung Im letzten Abschnitt haben wir gesehen, dass eine statistische Verteilung von Atomen eines idealen Gases in einem Volumen
Übungen zu Theoretische Physik IV
 Physikalisches Institut Übungsblatt 4 Universität Bonn 02. November 2012 Theoretische Physik WS 12/13 Übungen zu Theoretische Physik IV Priv.-Doz. Dr. Stefan Förste http://www.th.physik.uni-bonn.de/people/forste/exercises/ws1213/tp4
Physikalisches Institut Übungsblatt 4 Universität Bonn 02. November 2012 Theoretische Physik WS 12/13 Übungen zu Theoretische Physik IV Priv.-Doz. Dr. Stefan Förste http://www.th.physik.uni-bonn.de/people/forste/exercises/ws1213/tp4
