Glycolyse und Gluconeogenese
|
|
|
- Stephanie Kohl
- vor 7 Jahren
- Abrufe
Transkript
1 Glycolyse und Gluconeogenese Arbeiten, deren Beginn sich auf die Zeit um 1905 datieren lässt, führten dazu, dass in den 1940er Jahren alle Schritte der Glycolyse bekannt waren. Durchsicht der aktuellen Lehrwerke erweckt den Eindruck, dass es seit dieser Zeit nicht an Versuchen gemangelt hat, das Verständnis dieses vielleicht wichtigsten Stoffwechselwegs künstlich zu verkomplizieren. Da werden gut etablierte und verständliche Substanzbezeichnungen wie z.b. Glycerinaldehyd- 3-phosphat durch halbsystematische Namen wie Glyceral-3-phosphat ersetzt und komplizierte Regulationsmechanismen zum Standardwissen erhoben. Intermediate werden als stereochemisch korrekte, aber nur für ausgewiesene hemiker interpretierbare Keilstrichformeln geschrieben, und Übersichtsschemata mit Details enzymatischer Katalysemechanismen ausgeschmückt. Die Funktion der Glycolyse... Die Funktion der Gluconeogenese... Die Reaktionen der Glycolyse... Exkurs: Alkoholische Gärung... Exkurs: Die Spaltung von Fructose-1,6-bisphosphat ist die Umkehrreaktion einer Aldol- Addition... Exkurs: Bei der Bildung von 1,3-Bisphosphoglycerat entsteht eine energiereiche hosphorsäureanhydrid-bindung... Exkurs: Die Bildung der äußerst energiereichen Verbindung hosphoenolpyruvat ermöglicht den zweiten AT-liefernden Schritt... Die Reaktionen der Gluconeogenese... Der ori-yclus... Exkurs: xalacetat entsteht in den Mitochondrien und wird als Malat ins ytoplasma exportiert... Regulation der Glycolyse und Gluconeogenese in der Leber... Allgemeine rinzipien... Erster Kontrollpunkt: exokinase, Glucokinase, Glucose-6-phosphatase... Zweiter Kontrollpunkt: hosphofructokinase 1, hosphofructokinase 2, Fruktose- 1,6-bisphosphatase... Dritter Kontrollpunkt: yruvatkinase, yruvatcarboxylase, E-arboxykinase... Regulation der Glycolyse in den Skelettmuskeln und im erzmuskel
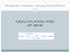
2 Die Funktion der Glycolyse Als Glycolyse bezeichnet man die Umwandlung von Glucose in yruvat. Die Glycolyse dient in erster Linie dem Energiegewinn. Sämtliche Reaktionen laufen im Zytoplasma ab. ro umgesetztem Glucosemolekül werden zwei Moleküle AT gewonnen. Unter aeroben Bedingungen wird yruvat über den itratcyclus und die Atmungskette vollständig zu 2 und 2 oxidiert, verbunden mit dem zusätzlichen Gewinn von ca. 30 AT-Molekülen. Unter anaeroben Bedingungen, z.b. während intensiver Muskelarbeit, wird yruvat in Lactat umgewandelt (Milchsäuregärung). Der Energiegewinn bleibt in diesem Fall auf die zwei Moleküle AT beschränkt. Zahlreiche Mikroorganismen, z.b. die Bäckerhefe, wandeln unter anaeroben Bedingungen yruvat in Ethanol und 2 um (alkoholische Gärung). Dabei werden ebenfalls nur zwei Moleküle AT gewonnen. Die Funktion der Gluconeogenese Bei der Gluconeogenese wird unter Energieverbrauch Glucose aus yruvat, Lactat und einigen anderen Metaboliten gewonnen. Die Mehrzahl der Reaktionen der Gluconeogenese sind mit denen der Glycolyse identisch, laufen aber in umgekehrter Richtung ab. Diese Reaktionen werden in der Glycolyse und Gluconeogenese durch die selben Enzyme katalysiert. Drei Reaktionen der Glycolyse sind stark exergonisch und können deshalb unter physiologischen Bedingungen nicht in umgekehrter Richtung ablaufen. Für diese Reaktionen existieren in der Gluconeogenese spezielle Umgehungsreaktionen. Während die Glycolyse in allen Zellen ablaufen kann, erfolgt die Gluconeogenese hauptsächlich in den rganen, deren Aufgabe in der omöostase des Blutglucosespiegels besteht, nämlich in der Leber und zu geringerem Anteil in der Niere und der Darmschleimhaut. Die Reaktionen der Glycolyse Im ersten Teilabschnitt der Glycolyse wird Glucose in Fructose-1,6-bisphosphat umgewandelt (Abb. 1). Dabei treten ausschließlich 6-Körper auf. Im zweiten Teilabschnitt wird Fructose- 1,6-bisphosphat in zwei 3-Körper gespalten, die in yruvat umgewandelt werden. Im ersten Abschnitt werden pro Glucosemolekül zwei Moleküle AT verbraucht. Im zweiten Abschnitt werden pro 3-Körper zwei Moleküle AT gewonnen. Da aus jedem Glucosemolekül zwei 3-Körper entstehen, werden effektiv zwei Moleküle AT gewonnen. Glucose tritt über Glucosetransporter, von denen verschiedene Typen existieren, in die Zelle ein und wird unter AT-Verbrauch zu Glucose-6-phosphat phosphoryliert. Glucose-6- phosphat kann die Zelle nicht mehr verlassen, da es die Glucosetransporter nicht passieren kann. Nach Isomerisierung zu Fructose-6-phosphat erfolgt eine weitere AT-abhängige hosphorylierung zu Fructose-1,6-bisphosphat. Fructose-1,6-bisphosphat wird in Glycerinaldehyd-3-phosphat und Dihydroxyacetonphosphat gespalten. Allerdings ist nur Glycerinaldehyd-3-phosphat Substrat für die folgenden Reaktionen. Deshalb wird das entstandene Dihydroxyacetonphosphat durch Isomerisierung ebenfalls in Glycerinaldehyd-3- phosphat umgewandelt. Aus Glycerinaldehyd-3-phosphat entsteht durch xidation mit NAD + und Anlagerung eines anorganischen hosphats 1,3-Bisphosphoglycerat. Die beiden hosphatgruppen des 1,3- Bisphosphoglycerats sind über zwei unterschiedliche Bindungstypen gebunden. Bei der hosphatgruppe in osition 3 handelt es sich um einen wenig energiereichen 2
3 hosphorsäureester. Die hosphatgruppe in osition 1 dagegen ist ein energiereiches hosphorsäureanhydrid. Übertragung dieser hosphatgruppe auf AD ist der erste ATliefernde Schritt der Glycolyse. Das entstandene 3-hosphoglycerat wird zur 2- hosphoglycerat isomerisiert und durch Eliminierung eines Wassermoleküls in hosphoenolpyruvat (E) umgewandelt, das eine sehr energiereiche Verbindung darstellt. Als zweiter AT-liefernder Schritt wird die hosphatgruppe des hosphoenolpyruvats auf AD übertragen. Das dabei entstehende yruvat ist das Endprodukt der Glycolyse. Unter aeroben Bedingungen gelangt das yruvat in die Mitochondrien, wo es nach Umwandlung in Acetyl-oA in den itratcyclus eingespeist wird. Auch das in der Glycolyse gebildete NAD wird in die Mitochondrien übertragen und für den Energiegewinn genutzt. Unter anaeroben Bedingungen wird durch die Reduktion von yruvat zu Lactat das NAD in NAD + zurückverwandelt, um für die Glycerinaldehyd-3-phosphat-Dehydrogenase- Reaktion zur Verfügung zu stehen. Die Energiebilanz von 2 AT-Molekülen pro umgesetztem Glucosemolekül unter anaeroben Bedingungen ergibt sich daraus, dass zur Bildung von Fructose-1,6-bisphosphat zunächst 2 AT-Moleküle investiert werden müssen. Fructose-1,6-bisphosphat wird in zwei 3-Körper gespalten, deren Umsetzung jeweils 2 AT-Moleküle (also insgesamt 4 AT-Moleküle) liefert. Nach Subtraktion der beiden investierten AT-Moleküle bleiben 2 AT-Moleküle übrig. Der Mechanismus der beiden AT-liefernden Schritte der Glycolyse wird als Substratkettenphosphorylierung bezeichnet. Der Begriff beschreibt die Übertragung von hosphatgruppen von energiereichen Substraten mir hohem hosphatgruppen- Übertragungspotential auf AD. Dagegen bezeichnet man den unter aeroben Bedingungen in den Mitochondrien ablaufende Mechanismus der AT-Synthese als Atmungskettenphosphorylierung oder oxidative hosphorylierung. Exkurs: Alkoholische Gärung Bei der für die Wein- und Bierherstellung verwendeten Bäckerhefe sowie bei vielen anderen Mikroorganismen erfolgt die unter anaeroben Bedingungen notwendige Rückverwandlung von NAD zu NAD + durch die Umwandlung von yruvat in Ethanol. Die zweistufige Reaktionsfolge ist unten dargestellt. Bei ausreichender Sauerstoffzufuhr erfolgt auch bei der efe die Energiegewinnung über den itratcyclus und die Atmungskette. 2 NAD + NAD yruvat Acetaldehyd Ethanol Abb. 1 (nächste Seite). Die Reaktionen der Glycolyse und Gluconeogenese. hosphatreste sind als dargestellt. 3
4 AT exokinase od. Glucokinase AD 2 Glucose 2 Glucose-6-phosphat Glucose-6-phosphatase Glucose-6-phosphat-Isomerase AT hosphofructokinase Fructose-6-phosphat Fructose-1,6-bisphosphatase AD 2 2 Fructose-1,6-bisphosphat 2 2 Fructose-1,6-bisphosphat (offenkettige Form) Glycerinaldehyd-3-phosphat 2 Aldolase Triosephosphat-Isomerase 2 2 Dihydroxyacetonphosphat NAD + Glycerinaldehyd-3-phosphat-Dehydrogenase NAD AD 2 1,3-Bisphosphoglycerat = Glycerinsäure-1,3-bisphosphat hosphoglyceratkinase AT 2 3-hosphoglycerat = Glycerinsäure-3-phosphat hosphoglyceratmutase 2 2-hosphoglycerat = Glycerinsäure-2-phosphat Enolase 2 2 GD GT 3 Lactat = Milchsäure NAD + NAD Lactatdehydrogenase AD yruvatkinase AT 2 hosphoenolpyruvat (E) 3 yruvat = Brenztraubensäure 4 E-arboxykinase AD AT 2 yruvatcarboxylase NAD + NAD yruvat-dehydrogenase S-oA 2 2 xalacetat S oa Acetyl-oA 3
5 Exkurs: Die Spaltung von Fructose-1,6-bisphosphat ist die Umkehrreaktion einer Aldol- Addition Die Spaltung von Fructose-1,6-bisphosphat in Glycerinaldehyd-3-phosphat und Dihydroxyacetonphosphat ist die Umkehrreaktion einer Aldol-Addition. Deshalb heißt das entsprechende Enzym Aldolase. Die Aldol-Addition ist eine allgemeine Reaktion von arbonyl- Verbindungen, also Aldehyden und Ketonen. Da der Mechanismus kompliziert ist, wird zunächst das klassische Beispiel einer Aldol-Addition zweier Moleküle Acetaldehyd erläutert (linker Teil der untenstehenden Abb.). Die elektronenziehende Wirkung des Sauerstoffatoms der arbonylgruppe des ersten Acetaldehyd-Moleküls ermöglicht die Deprotonierung des benachbarten -Atoms. Es liegt damit der ungewöhnliche Fall vor, dass ein an ein Kohlenstoffatom gebundenes Wasserstoffatom als roton abgespalten werden kann; man spricht von einer --aciden Verbindung. Die entstehende Spezies kann als mesomere Grenzstruktur zwischen dem arbanion und dem Enolat-Ion beschrieben werden. Die weitere Reaktion lässt sich am leichtesten aus der Struktur des arbanions verstehen. Das freie Elektronenpaar greift den positiv polarisierten arbonyl-kohlenstoff des zweiten Acetaldehyd- Moleküls an (nucleophiler Angriff). Das rodukt trägt den Trivialnamen Aldol. Unter bestimmten Bedingungen kann die Eliminierung eines Wassermoleküls folgen, so dass eine Doppelbindung entsteht; man spricht dann von einer Aldol-Kondensation. Aldol-Kondensationen spielen eine Rolle bei der Quervernetzung von Kollagen-Fibrillen. Die Reaktion von Dihydroxyacetonphosphat und Glycerinaldehyd-3-phosphat zu Fructose-1,6-bisphosphat (rechter Teil der untenstehenden Abb.) erfolgt formal nach dem selben Mechanismus wie die Reaktion zwischen den beiden Acetaldehyd- Molekülen. 2 + Acetaldehyd Dihydroxyacetonphosphat arbanion Enolat-Ion Mesomerie n nucleophiler Angriff δ δ + + Acetaldehyd 2 Glycerinaldehyd-3-phosphat 2 2 trans-2-butenal 3-ydroxybutanal Trivialname: (Acet-) Aldol 2 Fructose-1,6-bisphosphat 5
6 Exkurs: Bei der Bildung von 1,3-Bisphosphoglycerat entsteht eine energiereiche hosphorsäureanhydrid-bindung Treibende Kraft für den ersten AT-liefernden Schritt ist die xidation eines Aldehyds (Glycerinaldehyd-3-phosphat) zu einer Säure (3-hosphoglycerat = Anion des Glycerinsäure- 3-phosphats). Die frei werdende Energie wird zunächst zur Bildung der energiereichen hosphorsäureanhydrid-bindung des 1,3-Bisphosphoglycerats genutzt, bevor in der Folgereaktion AT entsteht. Der katalytische Mechanismus der Glycerinaldehyd-3-phosphat- Dehydrogenase ist ein typisches Beispiel dafür, wie die bei einer Reaktion frei werdende Energie in Form einer Verbindung mit hohem hosphatgruppen-übertragungspotential für den Stoffwechsel nutzbar gemacht wird. Im aktiven Zentrum bildet Glycerinaldehyd-3- phosphat mit einem ystein-rest ein Thio-albacetal. Durch Übertragung eines ydrid-ions ( - ) auf NAD + entsteht unter Bildung von NAD ein Thioester-Zwischenprodukt. Da die Thioester-Bindung energiereich ist, kann sie unter Anlagerung eines anorganischen hosphats gespalten werden, so dass die energiereiche hosphorsäureanhydrid-bindung entsteht. ystein-rest S Glycerinaldehyd-3-phosphat 2 Glycerinaldehyd-3-phosphat- Dehydrogenase Thio-albacetal S 2 Glycerinaldehyd-3-phosphat- Dehydrogenase NAD + NAD + + Thioester S 2 Glycerinaldehyd-3-phosphat- Dehydrogenase S 1,3-Bisphosphoglycerat 2 Glycerinaldehyd-3-phosphat- Dehydrogenase 6
7 Exkurs: Die Bildung der äußerst energiereichen Verbindung hosphoenolpyruvat ermöglicht den zweiten AT-liefernden Schritt hosphoenolpyruvat ist eine der energiereichsten in der Biochemie bekannten Verbindungen. Da hosphoenolpyruvat deutlich energiereicher ist als AT, ist die AT-Synthese durch die Übertragung der hosphatgruppe auf AD ohne weiteres möglich. Der Grund für den hohen Energiegehalt des hosphoenolpyruvats ergibt sich aus dem hänomen der Keto-Enol- Tautomerie. Als Tautomerie bezeichnet man allgemein das Auftreten von Konstitutionsisomeren (Strukturisomeren), die durch Verschiebung einzelner Gruppen hervorgehen. Bei den in der Biochemie relevanten Beispielen handelt es sich um die Verschiebung von Wasserstoffresten. Allgemein liegen Ketone in wässriger Lösung in einem Gleichgewicht zwischen der Keto-Form und der Enol-Form vor. R R R R Keton Keto-Enol- Tautomerie Beim yruvat ist der Anteil der Enol-Form sehr gering (wie bei den meisten Ketonen). Das Gleichgewicht liegt also stark auf der Seite der Keto-Form, die der allgemein üblichen Strukturformel des yruvats entspricht. Das hosphoenolpyruvat stellt die mit einem hosphorsäurerest veresterte Enol-Form des yruvats dar. Dieser hosphatrest verhindert die spontane Umwandlung in die Keto-Form. Erst nach der an die AT-Synthese gekoppelten Abgabe der hosphatgruppe kann die wesentlich stabilere Keto-Form angenommen werden. Die treibende Kraft für das hohe hosphatgruppen-übertragungspotential des hosphoenolpyruvats ist also das Bestreben der Enol-Form des yruvats in die Keto-Form überzugehen. R Enol R hosphorsäure-enol-ester AD AT hosphoenolpyruvat yruvat (Enol-Form) yruvat (Keto-Form) 7
8 Die Reaktionen der Gluconeogenese Folgende Reaktionen sind für die Gluconeogenese spezifisch und stellen keine Umkehrreaktionen der Glycolyse dar: (1) die Umwandlung von yruvat in hosphoenolpyruvat (2) die Umwandlung von Fructose-1,6-bisphosphat in Fructose-6-phosphat (3) die Umwandlung von Glucose-6-phosphat in Glucose. Der Grund, warum die Umwandlung von yruvat in hosphoenolpyruvat nicht durch Umkehr der glycolytischen Reaktion möglich ist, wird offensichtlich, wenn man bedenkt, dass hosphoenolpyruvat deutlich energiereicher ist als AT. Es muss also mehr Energie aufgewandt werden, als durch den Verbrauch eines AT-Moleküls freigesetzt würde. In der Gluconeogenese wird daher das yruvat zunächst durch Anlagerung eines 2 -Moleküls unter AT-Verbrauch zu xalacetat carboxyliert. Anschließend wird das 2 -Molekül unter GT-Verbrauch wieder abgespalten. Dabei entsteht hosphoenolpyruvat. Da AT und GT energetisch gleichwertig sind, werden zwei AT-Äquivalente verbraucht. Die durch die AT- Spaltung frei werdende Energie des ersten Teilschritts wird in der relativ labilen arboxylgruppe des xalacetats zwischengespeichert. Die Abspaltung dieser arboxylgruppe als 2 im zweiten Teilschritt bei gleichzeitiger Spaltung von GT ermöglicht die Bildung des hosphoenolpyruvats. Ebenfalls leicht verständlich ist, warum die Bildung von Fructose-6-phosphat aus Fructose- 1,6-bisphosphat bzw. Glucose aus Glucose-6-phosphat nicht durch Umkehrreaktionen der Glycolyse erfolgen kann. Die formale Umkehrung der glycolytischen Reaktionen würde bedeuten, dass die an den Zuckern gebundenen hosphatgruppen auf AD übertragen würden, so dass AT entstünde. Dies ist nicht möglich, da diese hosphatgruppen als energiearme hosphorsäureester gebunden sind. Daher werden in der Gluconeogenese die hosphatgruppen durch hosphatasen (Fructose-1,6-bisphosphatase und Fructose-6- phosphatase) hydrolytisch ohne Energiegewinn abgespalten. Die Bildung der freien Glucose im letzten Schritt der Gluconeogenese erfolgt im Endoplasmatischen Retikulum. Dazu gelangt Glucose-6-phosphat zunächst über einen Transporter in das Lumen des Endoplasmatischen Retikulums, wo es durch die mit der Membran assoziierte Glucose-6-phosphatase gespalten wird. Die Glucose kann so direkt in den Extrazellulärraum und schließlich ins Blut gelangen. 8
9 Der ori-yclus Bei intensiver Arbeit findet im Muskel zur Energieversorgung anaerobe Glycolyse statt (Abb. 2). Das gebildete Lactat (Milchsäuregärung) gelangt über das Blut in die Leber. Dort wird es über die Gluconeogenese in Glucose verwandelt. Die Glucose wird über das Blut wieder dem Muskel zur Verfügung gestellt. Diese Zusammenhänge werden nach den Entdeckern Gerty ori und arl ori ori-yclus genannt. Muskel Glucose Glucose Leber 2 AT Gluconeogenese Glycolyse yruvat LD Lactat Lactat LD yruvat Abb. 2. ori-yclus. LD = Lactat-Dehydrogenase. 9
10 Exkurs: xalacetat entsteht in den Mitochondrien und wird als Malat ins ytoplasma exportiert Die Umwandlung von yruvat in hosphoenolpyruvat erfordert bei detaillierterer Betrachtung zwei weitere Teilreaktionen. Da die yruvatcarboxylase ein mitochondriales Enzym ist, muss das gebildete xalacetat ins ytoplasma ausgeschleust werden. Dazu wird das xalacetat zu Malat reduziert, das die innere Mitochondrienmembran durch einen spezifischen Transporter passieren kann. Die äußere Mitochondrienmembran enthält große oren und stellt daher keine Diffusionsbarriere für kleine Moleküle dar. Im ytoplasma wird das Malat wieder zu xalacetat oxidiert. Da bei der intramitochondrialen Reduktion von xalacetat zu Malat NAD verbraucht und bei der cytoplasmatischen xidation von Malat zu xalacetat NAD freigesetzt wird, hat dieser Exportmechanismus zur Folge, dass in der Stoffbilanz NAD aus den Mitochondrien in das ytoplasma transportiert wird, wo es für die Umwandlung von 1,3- Bisphosphoglycerat in Glycerinaldehyd-3-phosphat benötigt wird. GD GT NAD + + NAD + hosphoenolpyruvat xalacetat Malat 2 ytoplasma Mitochondrien-Matrix AT NAD AD NAD + yruvat xalacetat Malat 10
11 Regulation der Glycolyse und Gluconeogenese in der Leber Allgemeine rinzipien In der Leber werden Glycolyse und Gluconeogenese abhängig von der aktuellen Stoffwechselsituation so reguliert, dass innerhalb einer Zelle im Wesentlichen nur einer der beiden Wege abläuft. Kontrollpunkte sind die charakteristischen irreversiblen Reaktionen. Der wichtigste Mechanismus ist die allosterische Regulation der entsprechenden Enzyme. Als weiterer Mechanismus wird die Aktivität eines Teils dieser Enzyme hormonabhängig durch hosphorylierung beeinflusst (Interkonversion). Ebenfalls hormonabhängig kann die Konzentration der aktuell benötigten Enzyme durch Aktivierung der Genexpression erhöht werden (Induktion). Allosterische Regulation, Interkonversion und Induktion wirken typischerweise innerhalb von Millisekunden, wenigen Sekunden bzw. Stunden. Im Detail ist die Regulation der Glycolyse und Gluconeogenese der Leber ausgesprochen komplex und nicht vollständig verstanden. Die übergeordneten rinzipien der Regulation spiegeln die besondere Aufgabe der Leber bei der omöostase des Blutglucosespiegels wider. Bei hohem Blutglucosespiegel findet praktisch keine Gluconeogenese statt, und die Glycolyse wird stimuliert. Das entstehende yruvat kann in Acetyl-oA und weiter in Fettsäuren umgewandelt werden, die nach Veresterung zu Triacylglyceriden mit den Lipoproteinen sehr geringer Dichte (VLDL) über das Blut u.a. ins Fettgewebe exportiert werden. Gleichzeitig wird die Glycolyse durch verschiedene Rückkopplungsmechanismen so weit gedrosselt, dass kein übermäßiger Glucoseverbrauch stattfindet und das Anlegen von Glycogenspeichern ermöglicht wird. Bei geringem Blutglucosespiegel überwiegt die Gluconeogenese, so dass aus verschiedenen Metaboliten Glucose gebildet und ans Blut abgegeben werden kann. Die allosterische Regulation erlaubt eine schnelle Reaktion auf die Verfügbarkeit von Substraten, den Bedarf an rodukten und den Energiestatus innerhalb einer Zelle. Eine Anpassung an die physiologische Situation des Gesamtorganismus ist durch die hormonabhängigen Mechanismen gewährleistet. Glucagon, Adrenalin und ortisol hemmen die Glycolyse der Leber und aktivieren die Gluconeogenese. Als Gegenspieler aktiviert Insulin die Glycolyse und hemmt die Gluconeogenese. Glucagon wird als ungersignal gebildet und dient in allererster Linie der Erhöhung des Blutglucosespiegels. Zielorgan des Glucagons ist fast ausschließlich die Leber. Adrenalin zeigt zum Teil sehr unterschiedliche Wirkungen an verschiedenen rganen mit dem übergeordneten Zweck, den rganismus kurzfristig in eine erhöhte Leistungsfähigkeit zu versetzten. Die molekulare Wirkung von sowohl Glucagon als auch Adrenalin in den Leberzellen erfolgt über eine Erhöhung der cam-konzentration. Durch cam wird die roteinkinase A aktiviert, die wiederum bestimmte Enzyme phosphoryliert (Interkonversion). Außerdem existieren cam-abhängige Mechanismen, die zu einer erhöhten Expression der Gene führen, die für die Enzyme der Gluconeogenese codieren (Induktion). Eine der vielen Funktionen des ortisols als ormon zur längerfristigen Anpassung an Belastungssituationen besteht in der Steigerung der Gluconeogenese zur Stabilisierung des Blutglucosespiegels trotz Nahrungsmangels. ortisol wirkt wie alle Steroidhormone primär über die Induktion der Zielenzyme. Die Funktion des Insulins besteht darin, die mit einer Mahlzeit aufgenommenen Nährstoffe einer Verwertung zum Aufbau von Körperstrukturen bzw. zum Anlegen von Speichern (Fett, Glycogen) zuzuführen. Der molekulare Wirkmechanismus des Insulins besteht u.a. in einer Verringerung der cam-konzentration, so dass sich ein zu Glucagon und Adrenalin antagonistischer Effekt ergibt. Außerdem wirkt Insulin über Induktion der Schüsselenzyme der Glycolyse. 11
12 Erster Kontrollpunkt: exokinase, Glucokinase, Glucose-6-phosphatase Die Reaktion von Glucose zu Glucose-6-phosphat wird in allen Geweben durch das Enzym exokinase katalysiert (Abb. 3). Die Regulation der exokinase erfolgt durch negative Rückkopplung, indem das Enzym durch sein rodukte (Glucose-6-phosphat) gehemmt wird (feedback-emmung). harakteristisch für die Leber ist das zusätzliche Vorkommen eines zweiten Enzyms, der Glucokinase, das die selbe Reaktion katalysiert. Die Substratspezifität der exokinase ist gering, so dass neben Glucose auch andere 6 -Zucker (exosen) phosphoryliert werden können. Dagegen akzeptiert die Glucokinase nur Glucose als Substrat. Außerdem ist der K M -Wert der Glucokinase wesentlich höher (ca. 50fach) als der K M -Wert der exokinase. Als weiterer Unterschied wird die Glucokinase nicht durch Glucose-6- phosphat gehemmt. Stattdessen existieren für die Glucokinase kompliziertere Regulationsmechanismen unter Beteiligung des sog. Glucokinase-regulierenden roteins (hier nicht beschrieben). Als Folge dieser doppelten Enzymausstattung findet in der Leber bei niedrigem Blutglucosespiegel nur eine niedrige glycolytische Basisaktivität vorwiegend über die exokinase statt. Dadurch können bei knappem Glucoseangebot zuerst das Gehirn und andere rgane versorgt werden. Erst bei hohen Blutglucosespiegeln kommt die Aktivität der Glucokinase zum Tragen, so dass größere Mengen Glucose durch die Leber umgesetzt und zur Fettsäure- und Glycogensynthese genutzt werden können. Im Gegensatz zur exokinase ist die Glucokinase durch Insulin induzierbar. Die Glucose-6-phosphatase wird durch Glucagon, Adrenalin und ortisol induziert. Außer in der Leber kommt die Glucokinase auch in den β-zellen der Bauchspeicheldrüse vor. Dadurch findet in den β-zellen erst bei hohen Glucosekonzentrationen ein intensiver glycolytischer Umsatz statt. Der resultierende Anstieg der AT-Konzentration ist ein Auslöser der Insulin-Ausschüttung. Zweiter Kontrollpunkt: hosphofructokinase 1, hosphofructokinase 2, Fruktose-1,6- bisphosphatase Die hosphorylierung von Fructose-6-phosphat zu Fructose-1,6-bisphosphat durch die hosphofructokinase 1 ist der erste irreversible Schritt, der ausschließlich bei der Glycolyse stattfindet. Im Gegensatz dazu wird das in der exokinase- bzw. Glucokinase-Reaktion erzeugte Glucose-1-phosphat auch als Ausgangssubstanz für die Glycogensynthese und den entosephosphatweg benötigt. Allgemein wird die erste irreversible Reaktion, die für einen Stoffwechselweg charakteristisch ist, als Schrittmacherreaktion (committed step) bezeichnet. Das Enzym, das die Schrittmacherreaktion katalysiert, ist in der Regel der wichtigste Kontrollpunkt. Eine zentrale Rolle bei der Regulation der hosphofructokinase 1 spielt das Signalmolekül Fructose-2,6-bisphosphat. Außer der Regulation der Glycolyse und Gluconeogenese sind keine weiteren Funktionen dieses Moleküls bekannt. Fructose-2,6- bisphosphat wird mit ilfe eines speziellen Enzyms, der hosphofructokinase 2, durch hosphorylierung von Fructose-6-phosphat gebildet. Daher ist die Konzentration von Fructose-2,6-bisphosphats ein Maß für die Verfügbarkeit von Fructose-6-phosphat. Fructose- 2,6-bisphosphat ist ein allosterischer Aktivator der hosphofructokinase 1. Einen derartiger Regulationsmechanismus, bei dem ein Metabolit ein Enzym aktiviert, das einen späteren Schritt in der Reaktionsfolge katalysiert, bezeichnet man als feedforward-aktivierung. (Dieses Beispiel ist allerdings ungewöhnlich kompliziert, da die feedforward-aktivierung der hosphofructokinase 1 durch Fructose-6-phosphat indirekt über Fructose-2,6-bisphosphat geschieht.) 12
13 Die hosphofructokinase 2 der Leber wird unter der Wirkung von Glucagon oder Adrenalin phosphoryliert (Interkonversion). Dadurch verliert das Enzym seine Kinase-Aktivität und gewinnt eine hosphatase-aktivität, so dass es die Dephosphorylierung von Fructose-2,6- bisphosphat zu Fructose-6-phosphat katalysiert und damit indirekt die Glycolyse hemmt. Deshalb wird die hosphofructokinase 2 auch als hosphofructokinase-2/fructose-2,6- bisphosphatase oder einfach nur das Bifunktionelle Enzym bezeichnet. Außer durch Fructose-2,6-bisphosphat wird die hosphofructokinase 1 durch AM als Signal für eine niedrige Energieladung der Zelle aktiviert. Gehemmt wird die hosphofructokinase 1 durch Moleküle, die eine hohe Energieladung anzeigen, nämlich AT und itrat. Das in der Gluconeogenese aktive Enzym Fructose-1,6-bisphosphatase wird durch die selben Signalmoleküle reguliert wie die hosphofructokinase 1, allerdings im umgekehrten Sinn. Dritter Kontrollpunkt: yruvatkinase, yruvatcarboxylase, E-arboxykinase Die yruvatkinase wird durch Fructose-1,6-bisphosphat aktiviert, so dass auch dieses Enzym über eine feedforward-aktivierung reguliert wird. Außerdem unterliegt die yruvatkinase einer feedback-emmung durch AT und Alanin als Indikatoren für eine hohe Energieladung. Alanin steht über eine reversible Reaktion (eine Transaminierungsreaktion) im Gleichgewicht mit yruvat und ist daher auch eine wichtige Ausgangssubstanz der Gluconeogenese. Unter der Wirkung von Glucagon oder Adrenalin wird die yruvatkinase der Leber durch hosphorylierung (Interkonversion) inaktiviert. Die beiden in der Gluconeogenese aktiven Enzyme yruvatcarboxylase und E- arboxykinase werden durch AD als Signal für eine niedrige Energieladung gehemmt. Die yruvatcarboxylase wird außerdem durch Acetyl-oA aktiviert. Acetyl-oA entsteht aus yruvat in einer irreversiblen Reaktion durch die yruvatdehydrogenase und wird in den itratcyclus eingespeist. Außerdem wird Acetyl-oA beim Abbau von Fettsäuren gebildet. Acetyl-oA (neben AT und NAD) hemmt die yruvatdehydrogenase, so dass insbesondere bei vorherrschendem Fettabbau yruvat für die Gluconeogenese genutzt werden kann. Die yruvatdehydrogenase-reaktion wird nicht als Teil der Glycolyse angesehen, ist aber im Zusammenhang mit der Regulation der Glycolyse und Gluconeogenese interessant. 13
14 Glucokinase nur in Leber und β-zellen des ankreas; hohe Spezifität, geringe Affinität (hohe K M ) Leber: erz-muskel: hosphorylierung der FK2 bewirkt hosphatase-aktivität (Abbau von F2,6B) hosphorylierung der FK2 bewirkt Verstärkung der Kinase-Aktivität (vermehrte Bildung von F2,6B) Skelett-Muskel: FK2 kann nicht phosphoryliert werden (kein Effekt durch cam) FK2 Glucokinase exokinase Glucose AT AD G6 ER Glucose-6- phosphatase Glycogensynthese entosephosphatweg F2,6B Insulin Glucagon, Adrenalin F6 FK2 AM FK1 AT AD Fructose-1,6- bisphosphatase AT itrat F1,6B GA3 DA AD 1,3BG AT Alanin AT 3G 2G Regulation der yruvatkinase durch hosphorylierung nur in der Leber yruvatkinase Insulin inaktiv Glucagon Adrenalin AD AT yruvatkinase Mito yruvatdehydrogenase E yruvat 2 Alanin E-arboxykinase GD GT xalacetat AD 2 AT Biotin Mito yruvatcarboxylase Lactat AD AcoA Induktion der Schlüsselenzyme der Glycolyse durch Insulin itrat Induktion der Schlüsselenzyme der Gluconeogenese durch Glucagon, Adrenalin und ortisol Abb. 3. Regulation der Glycolyse und Gluconeogenese. 14
15 Regulation der Glycolyse in den Skelettmuskeln und im erzmuskel Auch in den Skelettmuskeln und im erzmuskel ist die Glycolyse durch Mechanismen, die im Detail noch Gegenstand aktueller Forschung sind, reguliert. Die Gluconeogenese spielt in diesen Geweben keine wichtige Rolle. Die allosterische Regulation erfolgt nach ähnlichen Mechanismen wie in der Leber. ffensichtliche Unterschiede gibt es vor allem bei der hormonellen Regulation, insbesondere durch Adrenalin. In der Leber bewirkt Adrenalin eine emmung der Glycolyse und eine Aktivierung der Gluconeogenese, so dass Glucose ans Blut abgegeben und den Muskeln als Energielieferant zur Verfügung gestellt wird. Um die Glucose für den Energiegewinn nutzen zu können, darf die Glycolyse in den Muskelzellen nicht gehemmt werden. Dies wird dadurch erreicht, dass im Muskel eine Variante der hosphofructokinase 2 vorkommt, die nicht phosphoryliert werden kann und daher unter Adrenalinwirkung nicht den Abbau von Fructose-2,6-bisphosphat katalysiert. Ebenso kann die yruvatkinase des Muskels nicht durch hosphorylierung inaktiviert werden. Wegen der Nichtexistenz dieser negativen Regulationsmechanismen und dem erhöhten Glucoseangebot wird die Glycolyse im Muskel unter Adrenalinwirkung effektiv stimuliert. Im erzmuskel kommt eine weitere Variante der hosphofructokinase 2 vor, die unter Adrenalinwirkung an einer anderen Stelle phosphoryliert wird als das entsprechende Enzym der Leber. Als Folge kommt es zu einer Erhöhung der Kinaseaktivität, so dass vermehrt Fructose-2,6-bisphosphat gebildet und die Glycolyse stimuliert wird. Allgemein bezeichnet man Enzyme, die dieselben Reaktionen katalysieren, sich jedoch in ihren kinetischen Eigenschaften (V max, K M ) und/oder ihrer Regulierbarkeit durch verschiedene Effektormoleküle unterscheiden, als Isoenzyme oder Isozyme. ft entstehen Isoenzyme durch alternatives Spleißen des Transkripts eines einzigen Gens oder durch Expression verschiedener Gene, die evolutionär durch Genduplikationen entstanden sind. Isoenzyme werden meist gewebs- oder organellspezifisch oder in unterschiedlichen Entwicklungsphasen gebildet. Quellen: Berg, J. M.; Tymoczko, J. L.; Stryer, L. Biochemie. 6. Auflage. Spektrum Akademischer Verlag, Elsevier Gmb, München Löffler, G.; etrides,. E.; einrich,.. Biochemie und athobiochemie. 8. Auflage. Springer Medizin Verlag, eidelberg Rider M, Bertrand L, Vertommen D, Michels A, Rousseau GG, ue L. 6-phosphofructo-2- kinase/fructose-2,6-bisphosphatase: head-to-head with a bifunctional enzyme that controls glycolysis. Biochem J Aug 1;381(t 3): abgerufen am
Pharmazeutische Biologie Grundlagen der Biochemie
 harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Asmaa Mebrad Caroline Mühlmann Gluconeogenese
 Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
Gluconeogenese Asmaa Mebrad Caroline Mühlmann 06.12.2004 Definition: wichtiger Stoffwechselweg, bei dem Glucose aus Nicht-Kohlenhydrat-Vorstufen synthetisiert wird Ablauf bei längeren Hungerperioden dient
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Die Wege des Kohlenstoffes
 Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Z11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung. Proteine aus der Nahrung werden
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Praktikumsreferat Biochemie
 Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse
Praktikumsreferat Biochemie Thema: Glycolyse und Gluconeogenese 1. Glycolyse im Überblick Die Glycolyse (gr.: glykys = süß, lysis = auflösen) beschreibt den Abbau von Glucose zu Pyruvat (aerobe Glycolyse
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
Wiederholungsklausur zur Vorlesung Biochemie I im WS 2004/05
 Wiederholungsklausur zur Vorlesung Biochemie I im WS 2004/05 am 09.05.2005 von 08.00-09.30 Uhr Mensa & 2 Lösungen in rot unkte in grün Aufgabe : Formulieren Sie drei unterschiedliche Reaktionswege, wie
Wiederholungsklausur zur Vorlesung Biochemie I im WS 2004/05 am 09.05.2005 von 08.00-09.30 Uhr Mensa & 2 Lösungen in rot unkte in grün Aufgabe : Formulieren Sie drei unterschiedliche Reaktionswege, wie
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue rüfungsordnung Dauer Std.),. 4. 203, 8:30-9:30 Uhr, Mensa -3, sowie Biochemische Teilklausur zum Grundmodul 07
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue rüfungsordnung Dauer Std.),. 4. 203, 8:30-9:30 Uhr, Mensa -3, sowie Biochemische Teilklausur zum Grundmodul 07
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
KOHLENHYDRATE. Die Glykolyse
 Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Zellen verwandeln Zucker in Energie
 Zellen verwandeln Zucker in Energie Kohlenhydrate sind äusserst wichtige Brennstofflieferanten. Pflanzen können Zucker selber herstellen (vgl. autotrophe Organismen); Tiere hingegen müssen Zucker (und
Zellen verwandeln Zucker in Energie Kohlenhydrate sind äusserst wichtige Brennstofflieferanten. Pflanzen können Zucker selber herstellen (vgl. autotrophe Organismen); Tiere hingegen müssen Zucker (und
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Abbauwege im Energiestoffwechsel (Katabolismus)
 5.2.2. Abbauwege im Energiestoffwechsel (Katabolismus) 5.2.1. Enzyme 5.2.1.1. Definition der Enzyme Enzyme sind roteine, die als Biokatalysatoren wirken, d.h., Sie beschleunigen bestimmte Reaktionen durch
5.2.2. Abbauwege im Energiestoffwechsel (Katabolismus) 5.2.1. Enzyme 5.2.1.1. Definition der Enzyme Enzyme sind roteine, die als Biokatalysatoren wirken, d.h., Sie beschleunigen bestimmte Reaktionen durch
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten.
 Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Inhaltsverzeichnis - Kapitel
 Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
BIOCHEMIE des Stoffwechsels ( )
 BIEMIE des Stoffwechsels (772.113) 9. Einheit und oxidativer entosephosphatweg Metabolismus des Menschen Einige Fakten: Täglicher Bedarf von 160 + 20 g Glucose. Davon konsumiert das Gehirn etwa 75%. Gehirn
BIEMIE des Stoffwechsels (772.113) 9. Einheit und oxidativer entosephosphatweg Metabolismus des Menschen Einige Fakten: Täglicher Bedarf von 160 + 20 g Glucose. Davon konsumiert das Gehirn etwa 75%. Gehirn
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Mucosazelle. Mucosazelle
 Saccharase, Lactase Mucosazelle Mucosazelle Na-abhängiger Na-abhängiger Glucosetransporter (SGLT; (SGLT; aktiv): aktiv): nur nur in in Mucosazellen Mucosazellen (luminal) (luminal) und und Zellen Zellen
Saccharase, Lactase Mucosazelle Mucosazelle Na-abhängiger Na-abhängiger Glucosetransporter (SGLT; (SGLT; aktiv): aktiv): nur nur in in Mucosazellen Mucosazellen (luminal) (luminal) und und Zellen Zellen
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Claisen-Kondensation
 Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Praktikum Biochemie B.Sc. Water Science WS Enzymregulation. Marinja Niggemann, Denise Schäfer
 Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Praktikum Biochemie B.Sc. Water Science WS 2011 Enzymregulation Marinja Niggemann, Denise Schäfer Regulatorische Strategien 1. Allosterische Wechselwirkung 2. Proteolytische Aktivierung 3. Kovalente Modifikation
Versuchsprotokoll: Leitenzyme
 Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Versuchsprotokoll: Leitenzyme Aufschluss von Lebergewebe / Fraktionierte Zentrifugation / Aufschluss von Mitochondrien / Nachweis von Leitenzymen im Cytosol und 1.1. Einleitung Für die Trennung der Organellen
Die Verknüpfung zweier kleinerer Bausteine zu einem größeren läuft in diesem Fall über eine sogenannte Aldoladdition.
 Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Glykogenstoffwechsel. Glykogensynthese und Glykogenolyse
 Glykogenstoffwechsel Glykogensynthese und Glykogenolyse Glykogen lykogen ist das Speicher- bzw. Reserve-Kohlenhydrat bei Tieren Vergleichbar dem Amylopektin, ist Glykogen ein nichtlineares Polymer aus
Glykogenstoffwechsel Glykogensynthese und Glykogenolyse Glykogen lykogen ist das Speicher- bzw. Reserve-Kohlenhydrat bei Tieren Vergleichbar dem Amylopektin, ist Glykogen ein nichtlineares Polymer aus
ENZYME. Teil 1: Grundlagen und Substratbestimmungen
 ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
ENZYME Teil 1: Grundlagen und Substratbestimmungen Metastabiler Zustand Beispiel: Glucose-6-Phosphat + H 2 O [Glc6P] [H 2 0] K = = 1.135 x 10 [Glc] [Pi] -3 Gleichgewicht stark auf Seite von Glc + Pi Glucose
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Hauptwege des Stoffwechsels
 Hauptwege des Stoffwechsels Auf- und Abbau der Stoffgruppen Kohlenhydrate 1 Enzyme Hauptklassen 1 2 3 4 5 6 Biochemie 08/2 Enzyme 1. Erhöhung der Reaktionsgeschwindigkeit ΔΔG kat = ΔG unkat - ΔG kat Erniedrigung
Hauptwege des Stoffwechsels Auf- und Abbau der Stoffgruppen Kohlenhydrate 1 Enzyme Hauptklassen 1 2 3 4 5 6 Biochemie 08/2 Enzyme 1. Erhöhung der Reaktionsgeschwindigkeit ΔΔG kat = ΔG unkat - ΔG kat Erniedrigung
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Der Fettsäurestoffwechsel. Basierend auf Stryer Kapitel 22
 Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Der Fettsäurestoffwechsel Basierend auf Stryer Kapitel 22 1 CoA 2 3 Überblick 4 Ein paar Grundlagen... Carbonsäure Alkohol Carbonsäureester Eine Acyl-Gruppe 5 Eine Acyl-Gruppe H O Formyl H 3 C O Acetyl
Einführung in die Biochemie Gärung anaerober Abbau
 Gärungen sind ATP liefernde Energiestoffwechsel, die ohne Sauerstoff als xidationsmittel ablaufen. Ein Grund zur Nutzung der Gärung kann ein plötzlich anstehender Bedarf an rasch verfügbarerer Energie
Gärungen sind ATP liefernde Energiestoffwechsel, die ohne Sauerstoff als xidationsmittel ablaufen. Ein Grund zur Nutzung der Gärung kann ein plötzlich anstehender Bedarf an rasch verfügbarerer Energie
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
6.3 Phospholipide und Signaltransduktion. Allgemeines
 6.3 Phospholipide und Signaltransduktion Allgemeines Bei der Signaltransduktion, das heißt der Weiterleitung von Signalen über die Zellmembran in das Innere der Zelle, denkt man zuerst einmal vor allem
6.3 Phospholipide und Signaltransduktion Allgemeines Bei der Signaltransduktion, das heißt der Weiterleitung von Signalen über die Zellmembran in das Innere der Zelle, denkt man zuerst einmal vor allem
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
2. Klausur. 1. Aufgabe
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Bei der abschließenden
Primärstoffwechsel. Prof. Dr. Albert Duschl
 Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
Primärstoffwechsel Prof. Dr. Albert Duschl Aufgaben Der Primärstoffwechsel sorgt für Aufbau (Anabolismus) und Abbau (Katabolismus) biologischer Moleküle, wie Aminosäuren, Lipide, Kohlenhydrate und Nukleinsäuren.
BIOCHEMIE des Stoffwechsels (772.113)
 Glycolyse 6. Reaktion: Glycerinaldehyd-3- phosphat-dehydrogenase BIEMIE des Stoffwechsels (772.113) 5. Einheit Glycerinaldehyd-3- + NAD + + i 1,3-Bisphosphoglycerat + NAD + + Enzym: xidoreductase Glycerinaldehyd-3-phosphat-Dehydrogenase
Glycolyse 6. Reaktion: Glycerinaldehyd-3- phosphat-dehydrogenase BIEMIE des Stoffwechsels (772.113) 5. Einheit Glycerinaldehyd-3- + NAD + + i 1,3-Bisphosphoglycerat + NAD + + Enzym: xidoreductase Glycerinaldehyd-3-phosphat-Dehydrogenase
Bioenergetik. Technische Universität Ilmenau, FG Nanotechnologie. Zentrum für Mikro- und Nanotechnologien
 Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
schnell und portofrei erhältlich bei
 Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 Carbonylgruppen und eine C=C Doppelbindung.
 rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
Benjamin Franklin Beer is proof that God loves us and wants us to be happy.
 Benjamin Franklin 1706-1790 Beer is proof that God loves us and wants us to be happy. Warum entsteht ausgerechnet Ethanol beim Vergären von fermentiertem Getreide (= Kohlenhydraten)? Benjamin Franklin
Benjamin Franklin 1706-1790 Beer is proof that God loves us and wants us to be happy. Warum entsteht ausgerechnet Ethanol beim Vergären von fermentiertem Getreide (= Kohlenhydraten)? Benjamin Franklin
Versuchsprotokoll. 1.) Versuch 2a: Quantitative Bestimmung der Atmung
 Versuchsprotokoll 1.) Versuch 2a: Quantitative Bestimmung der Atmung 1.1. Einleitung: Bei der aeroben Atmung, also dem oxidativen Abbau der Kohlenhydrate, entsteht im Citratzyklus und bei der oxidativen
Versuchsprotokoll 1.) Versuch 2a: Quantitative Bestimmung der Atmung 1.1. Einleitung: Bei der aeroben Atmung, also dem oxidativen Abbau der Kohlenhydrate, entsteht im Citratzyklus und bei der oxidativen
I. Zellatmung. =Abbau von Kohlenhydraten unter Sauerstoffverbrauch (aerob) KH + O 2 --> CO 2 + H 2 O + Energie
 KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
 hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
hemie-protokoll 11.11.02, Seite 1 von 5 Lukman Iwan, 12.11.02 Stundenprotokoll vom Montag, 11. ovember 2002 Es fehlen: Janine und Jeannette Zettel 1&2: Aromatische eterocyclen http://www.oci.unizh.ch/edu/lectures/material/a_bii/kap6/kap6.html
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000
 Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
VL Kurs 7: Kohlenhydrate. Angelika Stöcklinger
 VL Kurs 7: Kohlenhydrate Angelika Stöcklinger Kohlenhydrate Produkte der Photosynthese Mono- Di-und Polysaccharide stellen zusammen mit Lipiden und Proteinen den größten Teil der Nahrung dar Monosaccharide
VL Kurs 7: Kohlenhydrate Angelika Stöcklinger Kohlenhydrate Produkte der Photosynthese Mono- Di-und Polysaccharide stellen zusammen mit Lipiden und Proteinen den größten Teil der Nahrung dar Monosaccharide
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Clinical definition of the metabolic syndrome
 Metabolismus: Lehrbuch der Biochemie: Voet/Voet Kapitel 13: Einführung in den Stoffwechsel Kapitel 14: Glucose Katabolismus Kapitel 15: Glycogen Metabolismus und Gluconeogenese Kapitel 16: Citratcyclus
Metabolismus: Lehrbuch der Biochemie: Voet/Voet Kapitel 13: Einführung in den Stoffwechsel Kapitel 14: Glucose Katabolismus Kapitel 15: Glycogen Metabolismus und Gluconeogenese Kapitel 16: Citratcyclus
Angelika Stöcklinger. Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate
 Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
5.2. Fragen zu Abbauwegen im Energiestoffwechsel (Katabolismus)
 5.2. Fragen zu Abbauwegen im Energiestoffwechsel (Katabolismus) Stoffwechselwege (16) In der folgenden Abbildung sind mehrere Stoffwechselwege dargestellt: 1 1 NAD + + NADH + H 2 3 4 2 a) Um welche Stoffwechselwege
5.2. Fragen zu Abbauwegen im Energiestoffwechsel (Katabolismus) Stoffwechselwege (16) In der folgenden Abbildung sind mehrere Stoffwechselwege dargestellt: 1 1 NAD + + NADH + H 2 3 4 2 a) Um welche Stoffwechselwege
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
a) Zeichnen Sie den Mechanismus für die säure-katalysierte Esterhydrolyse des unten gezeigten Carbonsäureesters.
 1. Aufgabe a) Zeichnen Sie den Mechanismus für die säure-katalysierte Esterhydrolyse des unten gezeigten Carbonsäureesters. 2 -shift - 2 P wenn nur die Produkte richtig sind: + b) Ein wichtiger Essigsäureester
1. Aufgabe a) Zeichnen Sie den Mechanismus für die säure-katalysierte Esterhydrolyse des unten gezeigten Carbonsäureesters. 2 -shift - 2 P wenn nur die Produkte richtig sind: + b) Ein wichtiger Essigsäureester
Fruktose ist Fruchtzucker gesünder als normaler Zucker?
 Fruktose ist Fruchtzucker gesünder als normaler Zucker? Fruchtzucker galt lange und gilt heute immer noch bei vielen als gesunde Alternative zum normalen Haushaltszucker. Immer noch bewerben Hersteller
Fruktose ist Fruchtzucker gesünder als normaler Zucker? Fruchtzucker galt lange und gilt heute immer noch bei vielen als gesunde Alternative zum normalen Haushaltszucker. Immer noch bewerben Hersteller
Verlauf der Blutzuckerkonzentration nach der Mahlzeit. Thinkstock /istockphoto. Konzentration. Thinkstock /istockphoto VORANSICHT.
 S 6 Art der Mahlzeit Verlauf der Blutzuckerkonzentration nach der Mahlzeit Abbildung 1 Graph 1 Abbildung 2 Graph 2 Abbildung 3 www.colourbox.de Graph 3 Die verschiedenen Mahlzeiten lassen den Blutzuckerspiegel
S 6 Art der Mahlzeit Verlauf der Blutzuckerkonzentration nach der Mahlzeit Abbildung 1 Graph 1 Abbildung 2 Graph 2 Abbildung 3 www.colourbox.de Graph 3 Die verschiedenen Mahlzeiten lassen den Blutzuckerspiegel
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Basiswissen Ernährungslehre
 Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Basiswissen Ernährungslehre Hauptnährstoffgruppen und bioaktive Substanzen Ergänze folgende Übersicht zu den natürlichen Bestandteilen der Nahrung Natürliche Bestandteile der Nahrung Nährstoffe Funktionsgruppen
Glykogen. 1,6-glykosidisch verbunden sind. Die Verzweigungen dienen dazu das Molekül an vielen Stellen gleichzeitig ab- oder aufzubauen.
 Glykogen Glykogen stellt die Speicherform der Glucose dar. Der menschliche Körper kann Glucose nicht speichern (Osmose). Es können ca. 400g Glucose als Glykogen aufbewahrt werden. Chemischer Aufbau: Glykogen
Glykogen Glykogen stellt die Speicherform der Glucose dar. Der menschliche Körper kann Glucose nicht speichern (Osmose). Es können ca. 400g Glucose als Glykogen aufbewahrt werden. Chemischer Aufbau: Glykogen
1. Die Bildung von Methan durch Mikroorganismen erfolgt (2 Punkte)
 Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Einführung in die Biochemie Wirkungsweise von Enzymen
 Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Wirkungsweise von en Am Aktiven Zentrum kann ein nur in einer ganz bestimmten Orientierung anlegen, wie ein Schlüssel zum Schloss. Dieses Prinzip ist die Ursache der spezifität von en. Dies resultiert
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Tyrosinkinase- Rezeptoren
 Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Tyrosinkinase- Rezeptoren für bestimmte Hormone gibt es integrale Membranproteine als Rezeptoren Aufbau und Signaltransduktionsweg unterscheiden sich von denen der G- Protein- gekoppelten Rezeptoren Polypeptide
Anaerobe NADH-Regeneration: Gärung
 Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Fettstoffwechsel - Stoffwechsel beim Sportler
 Fettstoffwechsel - Stoffwechsel beim Sportler Sonja Schmitz-Harwardt Heilpraktikerin und Sporttherapeutin Naturheilpraxis Alles in Balance in Velbert Muskelstoffwechsel Muskelstoffwechsel Quelle:http://de.wikipedia.org/wiki/Energiebereitstellung
Fettstoffwechsel - Stoffwechsel beim Sportler Sonja Schmitz-Harwardt Heilpraktikerin und Sporttherapeutin Naturheilpraxis Alles in Balance in Velbert Muskelstoffwechsel Muskelstoffwechsel Quelle:http://de.wikipedia.org/wiki/Energiebereitstellung
Jetzt-nehm-ich-mal-ab.de
 Hunger haben und satt werden Wie funktioniert das eigentlich mit dem Gefühl Hunger zu haben und satt zu werden? Der Körper hat da einen sehr komplizierten Regelmechanismus, der noch nicht so richtig vollständig
Hunger haben und satt werden Wie funktioniert das eigentlich mit dem Gefühl Hunger zu haben und satt zu werden? Der Körper hat da einen sehr komplizierten Regelmechanismus, der noch nicht so richtig vollständig
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Inhaltsverzeichnis zu Kapitel 10. Aldehyde und Ketone
 Inhaltsverzeichnis zu Kapitel 10. Aldehyde und Ketone 10. Aldehyde und Ketone 106 10.1 Nomenklatur 106 10.2 Die arbonylgruppe 106 10.3 Darstellung 107 10.3.1 xidation von Alkoholen 107 10.3.2 eduktion
Inhaltsverzeichnis zu Kapitel 10. Aldehyde und Ketone 10. Aldehyde und Ketone 106 10.1 Nomenklatur 106 10.2 Die arbonylgruppe 106 10.3 Darstellung 107 10.3.1 xidation von Alkoholen 107 10.3.2 eduktion
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
Testsysteme zur Bestimmung der Aktivität verschiedener Enzyme
 Testsysteme zur Bestimmung der Aktivität verschiedener Enzyme Einleitung: Das Ziel der Versuche ist es, Enzymaktivitäten verschiedener Stoffwechselwege in Geweben zu messen und dadurch Rückschlüsse auf
Testsysteme zur Bestimmung der Aktivität verschiedener Enzyme Einleitung: Das Ziel der Versuche ist es, Enzymaktivitäten verschiedener Stoffwechselwege in Geweben zu messen und dadurch Rückschlüsse auf
Beckers Welt der Zelle 8., aktualisierte Auflage. Jeff Hardin Gregory Bertoni Lewis Kleinsmith. Deutsche Bearbeitung von Wolf-Michael Weber
 Beckers Welt der Zelle 8., aktualisierte Auflage Jeff Hardin Gregory Bertoni Lewis Kleinsmith Deutsche Bearbeitung von Wolf-Michael Weber 9 Chemotropher Energiemetabolismus I: Glykolyse und Fermentation
Beckers Welt der Zelle 8., aktualisierte Auflage Jeff Hardin Gregory Bertoni Lewis Kleinsmith Deutsche Bearbeitung von Wolf-Michael Weber 9 Chemotropher Energiemetabolismus I: Glykolyse und Fermentation
Hemmung der Enzym-Aktivität
 Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Enzym - Inhibitoren Wie wirkt Penicillin? Wie wirkt Aspirin? Welche Rolle spielt Methotrexat in der Chemotherapie? Welche Wirkstoffe werden gegen HIV entwickelt? Hemmung der Enzym-Aktivität Substrat Kompetitiver
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
