Löslichkeit und Mischbarkeit von Stoffen
|
|
|
- Carl Breiner
- vor 7 Jahren
- Abrufe
Transkript
1 Löslichkeit und Mischbarkeit von Stoffen Fragestellung: Wie lösen sich unterschiedliche Stoffe in Wasser und Benzin? Chemikalien: Zucker, Kreidepulver (Kalkstein), Kochsalz, Soda, Sand, Öl, Wasser, Benzin Geräte: 5 Bechergläser (150 ml), Reagenzgläser, Reagenzglasständer, Stopfen, Trichter, Glasstab, Spatel, Schutzbrille Durchführung: Jeweils ein Spatel der Stoffprobe wird unter Rühren in ein halb mit Wasser gefülltes 150-ml-Becherglas gegeben. Die Löslichkeit in Benzin wird in einem Reagenzglas mit Stopfen untersucht. Befülle dazu das Reagenzglas ca. 2cm hoch mit Benzin und gib 1 / 2 Spatel des zu untersuchenden Stoffes in das Reagenzglas. Verschließe es dann mit dem Stopfen und schüttle um. Die Ergebnisse werden in die Tabelle eingetragen. Entsorgung: Die Bechergläser mit Wasser können in den Abfluss entsorgt werden. Ungelöste Feststoffe dabei bitte zurückhalten! Die Reagenzgläser mit Benzin werden vorne auf dem Lehrertisch gesammelt. Bitte nicht zusammenkippen! Stoff Zucker Löslich, schwerlöslich oder unlöslich? In Wasser In Benzin Kreidepulver(Kalkstein) Kochsalz Soda Sand Öl m L Becherglas Reagenzglasständer mit Reagenzgläsern Trichter Pistill Mörser
2 Löslichkeit und Mischbarkeit von Stoffen Lösung Fragestellung: Wie lösen sich unterschiedliche Stoffe in Wasser und Benzin? Chemikalien: Zucker, Kreidepulver (Kalkstein), Kochsalz, Soda, Sand, Öl, Wasser, Benzin Geräte: 5 Bechergläser (150 ml), Reagenzgläser, Reagenzglasständer, Stopfen, Trichter, Glasstab, Spatel, Schutzbrille Durchführung: Jeweils ein Spatel der Stoffprobe wird unter Rühren in ein halb mit Wasser gefülltes 150-ml-Becherglas gegeben. Die Löslichkeit in Benzin wird in einem Reagenzglas mit Stopfen untersucht. Befülle dazu das Reagenzglas ca. 2cm hoch mit Benzin und gib 1 / 2 Spatel des zu untersuchenden Stoffes in das Reagenzglas. Verschließe es dann mit dem Stopfen und schüttle um. Die Ergebnisse werden in die Tabelle eingetragen. Entsorgung: Die Bechergläser mit Wasser können in den Abfluss entsorgt werden. Ungelöste Feststoffe dabei bitte zurückhalten! Die Reagenzgläser mit Benzin werden vorne auf dem Lehrertisch gesammelt. Bitte nicht zusammenkippen! Stoff Löslich, schwerlöslich oder unlöslich? In Wasser In Benzin Zucker gut löslich nicht löslich Kreidepulver(Kalkstein) nicht löslich nicht löslich Kochsalz gut löslich nicht löslich Soda gut löslich nicht löslich Sand nicht löslich nicht löslich Öl nicht löslich gut löslich m L Becherglas Reagenzglasständer mit Reagenzgläsern Trichter Pistill Mörser
3 Schmelztemperaturbestimmung von Stearinsäure Fragestellung: Wie verhält sich ein fester Stoff beim Erwärmen? Material: Stearinsäure, Becherglas, Reagenzglas, Thermometer, Stativmaterial, Gasbrenner, Keramiknetz, Stoppuhr, Schutzbrille Gib etwas von der zu untersuchenden Substanz in ein Reagenzglas. Stelle ein Thermometer hinein und erwärme das Reagenzglas vorsichtig in einem Wasserbad. Führe dabei ein Protokoll. Zum Aufbau: Das Becherglas und das Reagenzglas werden mit einem Stativ befestigt. Der Aufbau ist auf nebenstehendem Foto dargestellt. a) Miss die Temperatur der Substanz im Minutenabstand und trage die Temperatur der Substanz gegen die Zeit in eine Tabelle ein. b) Wenn alles geschmolzen ist, nimm das Reagenzglas aus dem Wasserbad heraus und lasse es abkühlen. Dabei rühre so lange es geht immer wieder mal mit dem Thermometer um. Miss die Temperatur der Substanz erneut im Minutenabstand und trage sie gegen die Zeit in die Tabelle ein. c) Trage nun die Messwerte der Temperatur gegen die Zeit in ein Koordinatensystem. Verwende folgenden Maßstab: 10 C = 1cm, 1min = 1cm (Das unten dargestellte Koordinatensystem ist dafür nicht geeignet, es dient nur der Anschauung). Temperatur in C Zeit in Minuten
4 Schmelztemperaturbestimmung von Stearinsäure - Lösung Fragestellung: Wie verhält sich ein fester Stoff beim Erwärmen? Material: Stearinsäure, Becherglas, Reagenzglas, Thermometer, Stativmaterial, Gasbrenner, Keramiknetz, Stoppuhr, Schutzbrille Gib etwas von der zu untersuchenden Substanz in ein Reagenzglas. Stelle ein Thermometer hinein und erwärme das Reagenzglas vorsichtig in einem Wasserbad. Führe dabei ein Protokoll. Zum Aufbau: Das Becherglas und das Reagenzglas werden mit einem Stativ befestigt. Der Aufbau ist auf nebenstehendem Foto dargestellt. a) Miss die Temperatur der Substanz im Minutenabstand und trage die Temperatur der Substanz gegen die Zeit in eine Tabelle ein. b) Wenn alles geschmolzen ist, nimm das Reagenzglas aus dem Wasserbad heraus und lasse es abkühlen. Dabei rühre so lange es geht immer wieder mal mit dem Thermometer um. Miss die Temperatur der Substanz erneut im Minutenabstand und trage sie gegen die Zeit in die Tabelle ein. c) Trage nun die Messwerte der Temperatur gegen die Zeit in ein Koordinatensystem. Verwende folgenden Maßstab: 10 C = 1cm, 1min = 1cm (Das unten dargestellte Koordinatensystem ist dafür nicht geeignet, es dient nur der Anschauung). Temperatur in C Heizphase Abkühlphase Zeit in Minuten
5 Verhalten von Stoffen beim Erhitzen Fragestellung: Gibt es Unterschiede im Verhalten unterschiedlicher Stoffe beim Erhitzen? Geräte: Tiegelzange, Bunsenbrenner, Magnesiarinne, Schutzbrille Chemikalien: Salz, Zucker, Holzkohle, Eisennagel, Kupferblech Durchführung: Halte die vorliegenden Stoffe mit Hilfe der Tiegelzange in die nicht leuchtende Flamme des Bunsenbrenners. Bei Zucker und Salz musst du die Magnesiarinne zu Hilfe nehmen. Beobachtung: Tiegelzange Verhalten von Stoffen beim Erhitzen Fragestellung: Gibt es Unterschiede im Verhalten unterschiedlicher Stoffe beim Erhitzen? Geräte: Tiegelzange, Bunsenbrenner, Magnesiarinne, Schutzbrille Chemikalien: Salz, Zucker, Holzkohle, Eisennagel, Kupferblech Durchführung: Halte die vorliegenden Stoffe mit Hilfe der Tiegelzange in die nicht leuchtende Flamme des Bunsenbrenners. Bei Zucker und Salz musst du die Magnesiarinne zu Hilfe nehmen. Beobachtung: Tiegelzange
6 Verhalten von Stoffen beim Erhitzen Lösung Fragestellung: Gibt es Unterschiede im Verhalten unterschiedlicher Stoffe beim Erhitzen? Geräte: Tiegelzange, Bunsenbrenner, Magnesiarinne, Schutzbrille Chemikalien: Salz, Zucker, Holzkohle, Eisennagel, Kupferblech Durchführung: Halte die vorliegenden Stoffe mit Hilfe der Tiegelzange in die nicht leuchtende Flamme des Bunsenbrenners. Bei Zucker und Salz musst du die Magnesiarinne zu Hilfe nehmen. Beobachtung: Tiegelzange Stoff Salz Zucker Holzkohle Eisennagel Kupferblech Beobachtung springt, schmilzt eventuell, wenn die Magnesiarinne 800 C heiß wird schmilzt, verfärbt sich schwarz und stinkt glüht und verbrennt glüht, nach dem Abkühlen keine Veränderung sichtbar glüht, nach dem Abkühlen schwarz Manche Stoffe verändern ihre Eigenschaften durch das Erhitzen (Zucker, Kupfer), andere liegen nach dem Abkühlen so vor wie vor dem Erhitzen (Eisennagel, Salz).
7 DIE DICHTE Cola-Party Für ihre Party hat Janna Cola und Cola light in Dosen besorgt. Um die Getränke zu kühlen, füllt sie einen großen Behälter mit kaltem Wasser und gibt die Dosen hinein. Der Behälter wird unter einen Tisch gestellt und die Gäste greifen hinein, ohne die einzelnen Dosen sehen zu können. Die meisten Gäste trinken das zuerst herausgezogene Getränk, da sie kein Getränk dem anderem vorziehen. Nach kurzer Zeit befindet sich keine Dose Cola light mehr im Behälter. Dieser bei der Party beobachtete Effekt liegt an der unterschiedlichen Dichte von Cola und Cola light. Die Dichte ist eine wichtige Stoffeigenschaft. Sie ist für jeden Stoff spezifisch (ein Stoff hat immer dieselbe Dichte, egal welche Form er hat) und kann zur Identifizierung herangezogen werden. Das folgende Experiment soll dies verdeutlichen: Bei dem Experiment wirkt sich die Kohlensäure des Getränkes störend aus. Daher wurde die Kohlensäure ausgetrieben, indem die Cola kurz unter rühren aufgekocht wurde. Dabei entwich die Kohlensäure. Nimm einen Messzylinder und bestimme seine Masse (Umgangssprachlich: bestimme das Gewicht). Die Masse des leeren Messzylinders wird notiert. Fülle nun eine beliebige Menge Cola in den Messzylinder, notiere das abgefüllte Volumen und bestimme erneut die Masse des gefüllten Messzylinders. Aus der Differenz der beiden Massen kann die Masse der Cola berechnet werden. Wiederhole dies für mindestens drei beliebige Volumina. Führe den gleichen Versuch mit Cola light durch. Die Ergebnisse werden in der Tabelle zusammengetragen und dann in einem Diagramm dargestellt: Cola Volumen in ml Masse in g Cola light Volumen in ml Masse in g Volumen in ml Aufgaben 1. Das Diagramm ist eine proportionale Zuordnung. Aus der Mathematik weißt du, wie die Formel für solche Zuordnungen lautet (y = ). Die Dichte ist hier die Steigung des Graphen. Stelle die Formel für die Dichte auf (Lernhilfen sind bei der Lehrkraft erhältlich). 2. Besteht die 5-Cent-Münze aus Kupfer? Diese Frage sollt Ihr experimentell klären, ohne die Münze zu beschädigen! Wiege zehn Münzen sorgfältig ab. Fülle einen 100ml-Meßzylinder mit 50 ml Wasser und bestimme jetzt das Volumen der Münzen. Berechne die Dichte und vergleiche sie mit dem Literaturwert aus einem Buch. Masse in g
8 Lernhilfen zur Dichte Lernhilfe 1: Wenn die Werte korrekt bestimmt und aufgetragen wurden, ergibt sich sowohl für die Cola als auch für die Cola-light jeweils eine Gerade: Cola Cola light Lernhilfe 2: Aus der Mathematik kennst du proportionale Zuordnungen. Die Formel für proportionale Zuordnungen lautet y = m x. m ist dabei die Steigung. Lernhilfe 3: Die Formel für die allgemeine Geradengleichung lautet y = m x, wobei m die Steigung der Geraden ist. Die Steigung der Geraden ist in diesem Fall die Dichte Lernhilfe 4: Die Masse m ist auf der y-achse aufgetragen, das Volumen V ist auf der x-achse aufgetragen. Lernhilfe5: Als Körper bezeichnet man in der Physik alle Gegenstände, die untersucht werden. Die Luft im Luftballon ist ebenso ein Körper wie ein Hammer oder die Milch in der Flasche. Alle Körper bestehen aus Stoffen, die Raum benötigen. Masse und Volumen sind zueinander proportional. Wo ein Körper ist, kann kein zweiter sein. Eine Holzkugel und eine Eisenkugel haben bei gleichem Volumen unterschiedliche Massen. Wir sagen, die Stoffe Holz und Eisen haben eine unterschiedliche Dichte. Für Körper aus ein und demselben Stoff ist die Masse m proportional zum Volumen V. Den Quotienten m V bezeichnet man als Dichte (Rho). Sie ist von Stoff zu Stoff verschieden. Die Formel für die Dichte lautet also: Masse Rho = Volumen m V
9 DIE DICHTE - LÖSUNG Cola-Party Für ihre Party hat Janna Cola und Cola light in Dosen besorgt. Um die Getränke zu kühlen, füllt sie einen großen Behälter mit kaltem Wasser und gibt die Dosen hinein. Der Behälter wird unter einen Tisch gestellt und die Gäste greifen hinein, ohne die einzelnen Dosen sehen zu können. Die meisten Gäste trinken das zuerst herausgezogene Getränk, da sie kein Getränk dem anderem vorziehen. Nach kurzer Zeit befindet sich keine Dose Cola light mehr im Behälter. Dieser bei der Party beobachtete Effekt liegt an der unterschiedlichen Dichte von Cola und Cola light. Die Dichte ist eine wichtige Stoffeigenschaft. Sie ist für jeden Stoff spezifisch (ein Stoff hat immer dieselbe Dichte, egal welche Form er hat) und kann zur Identifizierung herangezogen werden. Das folgende Experiment soll dies verdeutlichen: Bei dem Experiment wirkt sich die Kohlensäure des Getränkes störend aus. Daher wurde die Kohlensäure ausgetrieben, indem die Cola kurz unter rühren aufgekocht wurde. Dabei entwich die Kohlensäure. Nimm einen Messzylinder und bestimme seine Masse (Umgangssprachlich: bestimme das Gewicht). Die Masse des leeren Messzylinders wird notiert. Fülle nun eine beliebige Menge Cola in den Messzylinder, notiere das abgefüllte Volumen und bestimme erneut die Masse des gefüllten Messzylinders. Aus der Differenz der beiden Massen kann die Masse der Cola berechnet werden. Wiederhole dies für mindestens drei beliebige Volumina. Führe den gleichen Versuch mit Cola light durch. Die Ergebnisse werden in der Tabelle zusammengetragen und dann in einem Diagramm dargestellt: Cola Volumen in ml 6,5 10, , Masse in g 6,6 11,1 17,6 21, ,2 97,9 Cola light Volumen in ml 7, Masse in g 7,5 14,7 23,7 49,7 73,9 84,7 94,9 Aufgaben 1. Das Diagramm ist eine proportionale Zuordnung. Aus der Mathematik weißt du, wie die Formel für solche Zuordnungen lautet (y = ). Die Dichte ist hier die Steigung des Graphen. Stelle die Formel für die Dichte auf (Lernhilfen sind bei der Lehrkraft erhältlich). Dichte = Masse Volumen bzw. in Formelzeichen: = m V 2. Besteht die 5-Cent-Münze aus Kupfer? Diese Frage sollt Ihr experimentell klären, ohne die Münze zu beschädigen! Wiege zehn Münzen sorgfältig ab. Fülle einen 100ml-Meßzylinder mit 50 ml Wasser und bestimme jetzt das Volumen der Münzen. Berechne die Dichte und vergleiche sie mit dem Literaturwert aus einem Buch. 10 Münzen wiegen 39,44g und verdrängen ein Volumen von 5ml. Es gilt also: m = 39,44g, V = 5cm³. Die Dichte ist also = m V = 39,44g g 5cm³ = 7,89 cm³. g Literaturwert: (Kupfer) = 8,96 cm³ Die Münzen können nicht aus Kupfer bestehen, da sie eine geringere Dichte besitzen als Kupfer. Aus der Untersuchung des Magnetismus wissen wir, dass die 5-Cent- Münze einen Eisenkern besitzt.
10 Hausaufgabe Aufgabe 1 Oliver hat sich sehr viel Mühe mit seiner Hausaufgabe gegeben. Er hat die Experimente zum Thema Dichtebestimmung sorgfältig durchgeführt und das die Ergebnisse in dem folgenden Diagramm dargestellt. Trotzdem ist sein Lehrer nicht ganz zufrieden. a) Überprüfe das Diagramm auf fachliche Korrektheit. b) Erkläre das von Oliver erstellte Diagramm. Ermittle die durchgeführten Versuche. Aufgabe 2 Bestimme die Dichte einer Zwiebel mit den Möglichkeiten in deiner Küche zu Hause. Beschreibe dein experimentelles Vorgehen. Hilfe zum Lösen der Aufgaben findest du auf dem Arbeitsblatt Die Dichte aus deinem Scienceunterricht.. Zusatzaufgabe für künftige Nobelpreisträger Wie unterscheiden sich die Dichten von rohen und gekochten Eiern? Begründe deine Antwort!
11 Hausaufgabe Aufgabe 1 Lösung A B C a) Überprüfe das Diagramm auf fachliche Korrektheit. Es fehlt die Beschriftung der Achse: V in cm 3, es fehlt eine Legende. b) Erkläre das von Oliver erstellte Diagramm. Ermittle die durchgeführten Versuche. Es wurden Massen und Volumina dreier Stoffe ermittelt. Mit Hilfe des Diagramms kann man die Dichten dieser Stoffe bestimmen: A 10 cm 3 80g g haben eine Masse von 80 g (eventuell Eisen) cm 10cm B 60 cm 3 49g g haben eine Masse von 49 g 0, (eventuell Holz) cm 60cm C 70 cm 3 25g g haben eine Masse von 25 g 0, (eventuell Kork) cm 70cm Aufgabe 2 Bestimme die Dichte einer Zwiebel mit den Möglichkeiten in deiner Küche zu Hause. Beschreibe dein experimentelles Vorgehen. Masse der Zwiebel: Volumen der Zwiebel: Ausführliche Beschreibung der Ermittlung der Daten Ergebnis: Zwiebeln schwimmen auf Wasser folglich muss die Dichte kleiner als 1g/cm 3 sein (0,89g/cm 3 ). Zusatzaufgabe für künftige Nobelpreisträger Wie unterscheiden sich die Dichten von rohen und gekochten Eiern? Begründe deine Antwort! Nur wenn Volumen oder Masse sich ändern, verändert sich die Dichte. Das Volumen des Eies wird durch das Kochen nicht beeinflusst. Eventuell verliert es etwas Gas aus der Luftblase, die es enthält. Das hätte eine geringfügige Änderung der Masse zur Folge.
12 Siedetemperatur und Druck Schließt man Wasser in ein Gefäß ein, so gehen Wasserteilchen in den Raum über der Flüssigkeit über, bis er mit Wasserdampf gesättigt ist. Diese Verdunstung führt zur Zunahme des Druckes im Inneren des Gefäßes. Der Druck, der auf das verdunstete Wasser zurückzuführen ist, wird Dampfdruck genannt. Temperatur in C Dampfdruck in hpa Die nebenstehende Tabelle zeigt den Zusammenhang zwischen dem Dampfdruck des Wassers in Abhängigkeit von der Temperatur. d) Der Extrembergsteiger Gerd Gipfel versucht in 5000 m Höhe Kartoffeln zu kochen. Es gelingt nicht, sie werden einfach nicht gar. Erkläre Gerd Gipfel die Vorgänge beim Kochen in dieser Höhe. e) Wasser siedet in einem Schnellkochtopf bei 120 C. Erkläre diesen Sachverhalt. f) Stelle die verschiedenen Aggregatzustände im Teilchenmodell dar. g) Benenne die Übergänge der einzelnen Aggregatzustände. a) Stelle den Zusammenhang zwischen Dampfdruck und Temperatur grafisch dar. b) Bestimme mit Hilfe der Grafik den Dampfdruck des Wassers bei 95 C und bei 25 C. c) Untersuche den Zusammenhang zwischen dem Luftdruck und der Siedetemperatur. flüssig
13 a) Stelle den Zusammenhang zwischen Dampfdruck und Temperatur grafisch dar. Siedetemperatur und Druck Lösung es erreicht auch nur diese Temperatur. Diese reicht nicht aus, um Kartoffeln gar zu bekommen. e) Wasser siedet in einem Schnellkochtopf bei 120 C. Erkläre diesen Sachverhalt. Ein Schnellkochtopf ist sehr fest verschlossen. Es baut sich, wenn Wasser darin erhitzt wird ein höherer Druck auf. Wasserdampf kann nur über das Sicherheitsventil, das sich erst bei einem Druck von über 1300 hpa öffnet. entweichen. Die Siedetemperatur des Wassers ist deshalb höher. f) Stelle die verschiedenen Aggregatzustände im Teilchenmodell dar. g) Benenne die Übergänge der einzelnen Aggregatzustände. b) Bestimme mit Hilfe der Grafik den Dampfdruck des Wassers bei 95 C und bei 25 C. Bei 95 C beträgt der Druck ungefähr 800 hpa und bei 25 C ca 30 hpa. c) Untersuche den Zusammenhang zwischen dem Luftdruck und der Siedetemperatur. Je höher der Luftdruck, desto höher ist die Siedetemperatur des Wassers. d) Der Extrembergsteiger Gerd Gipfel versucht in 5000 m Höhe Kartoffeln zu kochen. Es gelingt nicht, sie werden einfach nicht gar. Erkläre Gerd Gipfel die Vorgänge beim Kochen in dieser Höhe. Der Luftdruck in 5000 m Höhe beträgt 500 hpa. Das Wasser siedet bei diesem Druck bereits bei 80 C. Das heißt flüssig
14 Übungsaufgaben I Aufgabe 1: a) Stelle die verschiedenen Aggregatzustände im Teilchenmodell dar. b) Benenne die Übergänge der einzelnen Aggregatzustände flüssig Aufgabe 2: Die Abbildung der nebenstehenden Reagenzgläser zeigt die folgenden Gemische: Zucker mit Benzin Wasser mit Zucker Pflanzenöl mit Wasser Pflanzenöl mit Benzin Ordne die Mischungen den Reagenzgläsern 1 bis 4 zu. Aufgabe 3: Welche der folgenden Aussagen ist richtig? Die Teilchen eines Stoffes A besitzen den kleinsten Abstand, wenn der betreffende Stoff gasförmig ist, B ziehen sich gegenseitig an, C besitzen eine für den jeweiligen Stoff charakteristische Farbe, D sind im festen Zustand meistens dichter gepackt als im flüssigen Zustand, E bewegen sich bei niedrigen Temperaturen langsamer als bei hohen Temperaturen.
15 Übungsaufgaben I - Lösung Aufgabe 1: gasförmig a) Stelle die verschiedenen Aggregatzustände im Teilchenmodell dar. b) Benenne die Übergänge der einzelnen Aggregatzustände resublimieren sublimieren flüssig fest Aufgabe 2: Die Abbildung der nebenstehenden Reagenzgläser zeigt die folgenden Gemische: 3 Zucker mit Benzin 1 Wasser mit Zucker 2 Pflanzenöl mit Wasser 4 Pflanzenöl mit Benzin Ordne die Mischungen den Reagenzgläsern 1 bis 4 zu. Aufgabe 3: Welche der folgenden Aussagen ist richtig? Die Teilchen eines Stoffes A besitzen den kleinsten Abstand, wenn der betreffende Stoff gasförmig ist, B ziehen sich gegenseitig an, C besitzen eine für den jeweiligen Stoff charakteristische Farbe, D sind im festen Zustand meistens dichter gepackt als im flüssigen Zustand, E bewegen sich bei niedrigen Temperaturen langsamer als bei hohen Temperaturen.
16 Übungsaufgabe II In der Chemie kommt es häufig vor, dass Stoffe identifiziert werden müssen. In einem chemischen Labor werden beim Aufräumen 3 Gefäße mit farblosen Flüssigkeiten gefunden, deren Etiketten abgefallen sind. Die stark verschmutzten Etikette liegen auf dem Labortisch. Man kann mühsam die Worte Wasser Alkohol, Alkohollösung und Salzlösung entziffern. Ein Laborant bekommt die Aufgabe, die Substanzen zu identifizieren und ordnungsgemäß zu beschriften. Er untersucht das Verhalten der Stoffe beim Erhitzen und erhält die in der folgenden Abbildung dargestellten Kurven. a b c d a) Beschreibe das Diagramm. b) Beschrifte die Flaschen korrekt. Begründe Deine Entscheidung. c) Stelle die Vorgänge beim Sieden eines Stoffes im Teilchenmodell dar. d) Erkläre den unter schiedlichen Verlauf der Siedekurven.
17 Übungsaufgabe II Lösung a b c d a) Beschreibe das Diagramm. Es ist die Entwicklung der Temperatur in Abhängigkeit von der Zeit von drei Stoffen dargestellt. Die Stoffe c und a erreichen eine konstante Temperatur, bei der sich der Stoff nicht weiter erwärmt. Das bedeutet der Stoff siedet, a bei 78 C und c bei 100 C. B nähert sich beim erhitzen dem Stoff c an, während d stetig wärmer wird und am Ende des Experimentes bei 110 C liegt. b) Beschrifte die Flaschen korrekt. Begründe Deine Entscheidung. An Hand der Siedetemperatur (100 C) kann der Stoff c Wasser zugeordnet werden. Wasser ist ein Reinstoff mit einer festen Siedetemperatur. Auch Alkohol ist ein Reinstoff, folglich handelt es sich bei a um den Alkohol. Die Temperaturentwicklung von b bewegt sich zwischen Alkohol und Wasser, es handelt sich um das Alkohollösung. Dann bleibt für d nur noch die Salzlösung. c) Stelle die Vorgänge beim Sieden eines Stoffes im Teilchenmodell dar. erwärmen erwärmen Bei niedrigen Temperaturen befinden sich nur wenige Teilchen des Stoffes im Raum darüber. Je höher die Temperatur wird, desto mehr Teilchen befinden sich in der Gasphase über der Flüssigkeit. Beim Sieden bilden sich in der Flüssigkeit Gasblasen und sehr viele Teilchen verlassen die Flüssigkeit. d) Erkläre den unter schiedlichen Verlauf der Siedekurven. Reinstoffe haben eine feste Siedetemperatur. Das bedeutet, wenn diese erreicht ist ändert der Stoff bis keine Flüssigkeit mehr vorhanden ist seinen Aggregatzustand, während der Dauer dieses Vorganges ändert sich die Temperatur nicht mehr. Bei Gemischen verlässt der Stoff mit der niedrigeren Siedetemperatur zuerst die Flüssigkeit. Die Konzentration der Teilchen des höher siedenden Stoffes wird größer und die Temperatur steigt stetig an (z.b. Alkohollösung).
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften
 Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Steckbrief-Test. 1 Überprüfe, ob die Stoff-Steckbriefe richtig sind. Wenn nicht, fertige einen überarbeiteten Steckbrief im Heft an.
 Steckbrief-Test Emma soll für die Schule Stoff-Steckbriefe zu vier verschiedenen Stoffen erstellen. Im Internet hat sie folgende Stoff-Steckbriefe gefunden. Bei manchen Angaben hat sie aber Zweifel, ob
Steckbrief-Test Emma soll für die Schule Stoff-Steckbriefe zu vier verschiedenen Stoffen erstellen. Im Internet hat sie folgende Stoff-Steckbriefe gefunden. Bei manchen Angaben hat sie aber Zweifel, ob
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Kultusministerium. Name, Vorname: Klasse: Schule: Seite 1 von 6
 Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Chemie ist wie die Biologie und die Geschichte eine auf Erfahrungen und Befragungen beruhende
Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Chemie ist wie die Biologie und die Geschichte eine auf Erfahrungen und Befragungen beruhende
Wir untersuchen einige Flammen auf ihre Temperatur
 Station 1 Wir untersuchen einige Flammen auf ihre Temperatur Du benötigst den Graphikrechner, das CBL2 und das Thermoelement. Verbinde das Thermoelement mit dem CBL2. Verbinde das CBL2 mit dem Rechner.
Station 1 Wir untersuchen einige Flammen auf ihre Temperatur Du benötigst den Graphikrechner, das CBL2 und das Thermoelement. Verbinde das Thermoelement mit dem CBL2. Verbinde das CBL2 mit dem Rechner.
Temperaturabhängigkeit, Schmelzund Siedetemperatur
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelzund Siedetemperatur Kurzprotokoll Auf einen Blick: Im Folgenden
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelzund Siedetemperatur Kurzprotokoll Auf einen Blick: Im Folgenden
8. Löslichkeit verschiedener Salze bestimmen
 Praktikum Chemie N 8 Classe : Date de la remise : Note sur 10 : Nom(s) : 8. Löslichkeit verschiedener Salze bestimmen Video Löslichkeit Die Löslichkeit eines Stoffes gibt an, in welchem Umfang ein Reinstoff
Praktikum Chemie N 8 Classe : Date de la remise : Note sur 10 : Nom(s) : 8. Löslichkeit verschiedener Salze bestimmen Video Löslichkeit Die Löslichkeit eines Stoffes gibt an, in welchem Umfang ein Reinstoff
Untersuche die ausgegebenen Stoffe auf Brennbarkeit und Schmelztemperatur.
 Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt: 07.2.205 :7:33 intertess (Version
Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt: 07.2.205 :7:33 intertess (Version
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Kernaussagen zum Teilchenmodell
 Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Wie wirkt sich die Zugabe von Salz auf den Schmelz- und Siedepunkt von Wasser aus?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Stoffeigenschaften auf der Spur
 Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Klassenarbeitsaufgaben
 Klassenarbeitsaufgaben Untersuchung von Limonade und wasser 1. Erik möchte seine Lieblingslimonade untersuchen. Zuerst muss er das störende Kohlenstoffdioxid ( Kohlensäure ) entfernen. Dazu stehen ihm
Klassenarbeitsaufgaben Untersuchung von Limonade und wasser 1. Erik möchte seine Lieblingslimonade untersuchen. Zuerst muss er das störende Kohlenstoffdioxid ( Kohlensäure ) entfernen. Dazu stehen ihm
1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE VORÜBERLEGUNGEN
 1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE Chemie beschäftigt sich mit Materie. Die Aggregatzustände (s, l und g) sind Formen der Materie. Materie besteht aus
1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE Chemie beschäftigt sich mit Materie. Die Aggregatzustände (s, l und g) sind Formen der Materie. Materie besteht aus
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Untersuche die ausgegebenen Stoffe auf Brennbarkeit und Schmelztemperatur.
 Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt:.0.203 2:44:57 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - Stoffeigenschaften (P750200).2 Stoffeigenschaften - Brennbarkeit, Schmelztemperatur Experiment von: Phywe Gedruckt:.0.203 2:44:57 intertess (Version 3.06
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Dichtebestimmung flüssiger Körper (Artikelnr.: P )
 Lehrer-/Dozentenblatt Gedruckt: 22.08.207 :6:57 P0998600 Dichtebestimmung flüssiger Körper (Artikelnr.: P0998600) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema:
Lehrer-/Dozentenblatt Gedruckt: 22.08.207 :6:57 P0998600 Dichtebestimmung flüssiger Körper (Artikelnr.: P0998600) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema:
2.1 Eigenschaften von Stoffgemischen. Aufgabe. Welche Eigenschaften haben Stoffgemische?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750600) 2. Eigenschaften von Stoffgemischen Experiment von: Phywe Gedruckt:.0.203 2:49:48 intertess (Version 3.06 B200, Export 2000)
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750600) 2. Eigenschaften von Stoffgemischen Experiment von: Phywe Gedruckt:.0.203 2:49:48 intertess (Version 3.06 B200, Export 2000)
Unterrichtsmaterial. Die Unterrichtssequenz enthält drei verschiedene Teile/ Experimente:
 Unterrichtsmaterial Die Unterrichtssequenz enthält drei verschiedene Teile/ Experimente: I. Mit dem Abkühlungsprozess vertraut werden Idee: Gegebenes Experiment / Beobachtung des Abkühlungsprozesses von
Unterrichtsmaterial Die Unterrichtssequenz enthält drei verschiedene Teile/ Experimente: I. Mit dem Abkühlungsprozess vertraut werden Idee: Gegebenes Experiment / Beobachtung des Abkühlungsprozesses von
Die vorliegenden Arbeitsblätter enthalten vor allem experimentelle Zugänge zum Projektthema.
 Hinweise für die Lehrkräfte Der Inhalt der Arbeitsblätter orientiert sich vor allem am Lehrplan des G8 für die 8. und 9. Klasse Chemie im Rahmen der Unterrichtsgegenstände Teilchenmodell und Aggregatzustandsänderungen
Hinweise für die Lehrkräfte Der Inhalt der Arbeitsblätter orientiert sich vor allem am Lehrplan des G8 für die 8. und 9. Klasse Chemie im Rahmen der Unterrichtsgegenstände Teilchenmodell und Aggregatzustandsänderungen
Umschmelzen und Tiefziehen von Polystyrol
 Umschmelzen und Tiefziehen von Heißluftgebläse, Keramiknetz, Tiegelzange, Saugflasche mit Gummiring, Glasfritte, Wasserstrahlpumpe, Stativ mit Muffe und Klammer Joghurtbecher aus (PS) Schutzbrille! Das
Umschmelzen und Tiefziehen von Heißluftgebläse, Keramiknetz, Tiegelzange, Saugflasche mit Gummiring, Glasfritte, Wasserstrahlpumpe, Stativ mit Muffe und Klammer Joghurtbecher aus (PS) Schutzbrille! Das
Versuch 1. Baue ein Thermometer. Nun erwärme das Wasser im Erlenmeyerkolben auf einem Stövchen. Was geschieht?
 Versuch 1 Nun erwärme das Wasser im Erlenmeyerkolben auf einem Stövchen. Was geschieht? Baue ein Thermometer Fülle den Erlenmeyerkolben mit Wasser und verschließe ihn mit dem Stopfen. Im Stopfen befindet
Versuch 1 Nun erwärme das Wasser im Erlenmeyerkolben auf einem Stövchen. Was geschieht? Baue ein Thermometer Fülle den Erlenmeyerkolben mit Wasser und verschließe ihn mit dem Stopfen. Im Stopfen befindet
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat
 1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
1. Chemie ist da wo es stinkt und kracht Die chemische Reaktion zwischen Zucker und Kaliumnitrat Geräte/Chemikalien: Mörser mit Pistill, feuerfeste Unterlage, Zucker, Kaliumnitrat, Zünder: Kaliumpermanganat
1.5 Stoffeigenschaften - Dichtebestimmung. Aufgabe. Wie bestimmt man die Dichte von Feststoffen?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 1 Stoffeigenschaften (P7150500) 1.5 Stoffeigenschaften - Dichtebestimmung Experiment von: Phywe Gedruckt: 11.10.2013 12:48:42 intertess (Version 13.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 1 Stoffeigenschaften (P7150500) 1.5 Stoffeigenschaften - Dichtebestimmung Experiment von: Phywe Gedruckt: 11.10.2013 12:48:42 intertess (Version 13.06
Schmelz- und Erstarrungskurve von watriumthiosulfat
 Lehrer-/Dozentenblatt Schmelz- und Erstarrungskurve von watriumthiosulfat (Artikelnr.: P044600) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema:
Lehrer-/Dozentenblatt Schmelz- und Erstarrungskurve von watriumthiosulfat (Artikelnr.: P044600) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema:
Die Kleinsten unter den Kleinen. - Einführung eines Teilchenmodells
 Carl-von-Ossietzky-Universität Oldenburg Fakultät V Institut für reine und angewandte Chemie Didaktik der Chemie Arbeitsmaterialien Chemie Die Kleinsten unter den Kleinen - Einführung eines Teilchenmodells
Carl-von-Ossietzky-Universität Oldenburg Fakultät V Institut für reine und angewandte Chemie Didaktik der Chemie Arbeitsmaterialien Chemie Die Kleinsten unter den Kleinen - Einführung eines Teilchenmodells
Schmelzpunktserniedrigung und Siedepunktserhöhung
 Lehrer-/Dozentenblatt Schmelzpunktserniedrigung und Siedepunktserhöhung Aufgabe und Material Lehrerinformationen Lernziele Lösungen haben einen höheren Siedepunkt und einen niedrigeren Schmelzpunkt als
Lehrer-/Dozentenblatt Schmelzpunktserniedrigung und Siedepunktserhöhung Aufgabe und Material Lehrerinformationen Lernziele Lösungen haben einen höheren Siedepunkt und einen niedrigeren Schmelzpunkt als
B E I S P I E L A R B E I T / Aufgaben. Kultusministerium. Name, Vorname: Klasse: Schule: Seite 1 von 6
 B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
Merkmale chemischer Reaktionen
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale chemischer Reaktionen Kurzprotokoll Auf einen Blick: Im Folgenden werden weitere Versuche zum Thema Merkmale einer
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 7 & 8 Merkmale chemischer Reaktionen Kurzprotokoll Auf einen Blick: Im Folgenden werden weitere Versuche zum Thema Merkmale einer
1-2 Unterrichtsstunden
 Lernziele Scaffolding und Differenzierung im Biologieunterricht (Praktikum) - Die Schüler sollen Material/Stoff, respektiv Form eines Körpers unterscheiden können, und mithilfe von Fachbegriffen verschiedene
Lernziele Scaffolding und Differenzierung im Biologieunterricht (Praktikum) - Die Schüler sollen Material/Stoff, respektiv Form eines Körpers unterscheiden können, und mithilfe von Fachbegriffen verschiedene
Sicher experimentieren
 Sicher experimentieren A1 Das Experimentieren im Labor kann gefährlich sein. Deswegen muss man sich an Regeln im Labor halten. Lies dir die 6 wichtigsten Regeln im Labor durch. 1. Kein Essen und Trinken
Sicher experimentieren A1 Das Experimentieren im Labor kann gefährlich sein. Deswegen muss man sich an Regeln im Labor halten. Lies dir die 6 wichtigsten Regeln im Labor durch. 1. Kein Essen und Trinken
Untersuche, ob Wasser gelöste Gase enthält und wovon die Löslichkeit der Gase abhängt.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Wie verändern sich die Eigenschaften der Alkohole bei Zunahme der Kohlenstoffzahl?
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77200) 4.6 Eigenschaften der homologen Reihe Experiment von: Phywe Gedruckt: 20.07.206 3:58:38 intertess (Version 3.2 B24, Export 2000) Aufgabe
Jeder Gegenstand Stoff Jeder Stoff Eigenschaften
 Stoffe Jeder Gegenstand der Welt, die euch umgibt, besteht aus einem chemischen Stoff. Jeder Stoff hat ganz spezielle Eigenschaften, die bestimmen, wie er verwendet wird. Die Chemie hat die Aufgabe die
Stoffe Jeder Gegenstand der Welt, die euch umgibt, besteht aus einem chemischen Stoff. Jeder Stoff hat ganz spezielle Eigenschaften, die bestimmen, wie er verwendet wird. Die Chemie hat die Aufgabe die
Klassenarbeit - Mechanik
 5. Klasse / Physik Klassenarbeit - Mechanik Aggregatszustände; Geschwindigkeit; Geradlinige Bewegung; Volumen; Physikalische Größen; Masse; Dichte Aufgabe 1 Welche 3 Arten von Stoffen kennst Du? Nenne
5. Klasse / Physik Klassenarbeit - Mechanik Aggregatszustände; Geschwindigkeit; Geradlinige Bewegung; Volumen; Physikalische Größen; Masse; Dichte Aufgabe 1 Welche 3 Arten von Stoffen kennst Du? Nenne
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
Physik 7 Lernbuffet Teilchenmodell und thermisches Verhalten von Körpern Damköhler
 Physik 7 Lernbuffet Teilchenmodell und thermisches Verhalten von Körpern Damköhler Aufgabe 1 (Aggregatzustände nennen und Aufbau und Bewegung beschreiben) N1: Betrachte aufmerksam die Bilder und benenne
Physik 7 Lernbuffet Teilchenmodell und thermisches Verhalten von Körpern Damköhler Aufgabe 1 (Aggregatzustände nennen und Aufbau und Bewegung beschreiben) N1: Betrachte aufmerksam die Bilder und benenne
Veranstaltung 5: Chemie macht hungrig!
 Veranstaltung 5: Chemie macht hungrig! Station 1: Kohlenhydrate E1 Gummibärchen gehen baden! E2 Ist Zucker gleich Zucker? E3 Was macht eine Kartoffel stark? Station 2: Fette E4 Können Fette verschwinden?
Veranstaltung 5: Chemie macht hungrig! Station 1: Kohlenhydrate E1 Gummibärchen gehen baden! E2 Ist Zucker gleich Zucker? E3 Was macht eine Kartoffel stark? Station 2: Fette E4 Können Fette verschwinden?
Versuch Nr.53. Messung kalorischer Größen (Spezifische Wärmen)
 Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
Versuch Nr.53 Messung kalorischer Größen (Spezifische Wärmen) Stichworte: Wärme, innere Energie und Enthalpie als Zustandsfunktion, Wärmekapazität, spezifische Wärme, Molwärme, Regel von Dulong-Petit,
In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz
 Name: Datum: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz Geräte Becherglas, Spatel, Alu-Teelichtschale, Heizplatte, Pipette, Tiegelzange, Glasstab, Lupe Materialien Kochsalz
Name: Datum: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Kochsalz Geräte Becherglas, Spatel, Alu-Teelichtschale, Heizplatte, Pipette, Tiegelzange, Glasstab, Lupe Materialien Kochsalz
Brenner Streichhölzer Eis
 Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
4.1 Vergleich von physikalischem Vorgang und chemischer Reaktion. Aufgabe. Woran lassen sich chemische Reaktionen erkennen? (1)
 Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
Kohlenhydrate in Lebensmitteln - Nachweis von Zucker
 Name: Datum: Kohlenhydrate in Lebensmitteln - Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter, schwarzer Stift Materialien Glucose,
Name: Datum: Kohlenhydrate in Lebensmitteln - Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter, schwarzer Stift Materialien Glucose,
Temperaturabhängigkeit, Schmelz- und Siedetemperatur
 Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelz- und Siedetemperatur Auf einen 1 Beschreibung Blick: des Themas
Schulversuchspraktikum Isabelle Faltiska Sommersemester 2015 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit, Schmelz- und Siedetemperatur Auf einen 1 Beschreibung Blick: des Themas
02. Was kann man über die Teilchen eines schmelzenden Stoffes aussagen?
 01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser
 HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser DIE ZERDRÜCKTE ALUDOSE LEERE Alu-Getränkedose (1/2 Liter!) Tiegelzange Schüssel mit kaltem Wasser 1. Fülle die leere Getränkedose mit wenig Wasser 2. Stelle die
HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser DIE ZERDRÜCKTE ALUDOSE LEERE Alu-Getränkedose (1/2 Liter!) Tiegelzange Schüssel mit kaltem Wasser 1. Fülle die leere Getränkedose mit wenig Wasser 2. Stelle die
Wir untersuchen Mineralwasser
 Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Junior-Laborführerschein für die Orientierungsstufe
 Junior-Laborführerschein für die Orientierungsstufe Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in
Junior-Laborführerschein für die Orientierungsstufe Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in
Aggregatzustände und deren Temperaturabhängigkeit
 Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Besteht die 5-Cent-Münze eigentlich aus Kupfer?
 Besteht die 5-Cent-Münze ERPROBUNGSFASSUNG eigentlich aus Kupfer? Die 5-Cent-Münze sieht aus, als ob sie aus Kupfer gefertigt ist. Aber ist sie das wirklich? Die Münze wird von einem Magneten angezogen.
Besteht die 5-Cent-Münze ERPROBUNGSFASSUNG eigentlich aus Kupfer? Die 5-Cent-Münze sieht aus, als ob sie aus Kupfer gefertigt ist. Aber ist sie das wirklich? Die Münze wird von einem Magneten angezogen.
Physik 7 Lernbuffet Masse, Volumen und Dichte Damköhler
 Physik 7 Lernbuffet Masse, Volumen und Dichte Damköhler Aufgabe 1 (Masse definieren, Formelzeichen und Einheit angeben) N1: Definiere die physikalische Größe Masse! Gib außerdem das Formelzeichen und die
Physik 7 Lernbuffet Masse, Volumen und Dichte Damköhler Aufgabe 1 (Masse definieren, Formelzeichen und Einheit angeben) N1: Definiere die physikalische Größe Masse! Gib außerdem das Formelzeichen und die
Institut für Anorganische Chemie (Materialchemie)
 1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker
 Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Stoffkreislauf: - Atmung und Kohlenstoffdioxid - Inhalt
 : - Atmung und Kohlenstoffdioxid - Inhalt Versuch 1 Kohlenstoffdioxidnachweis mit Kalkwasser 2 Versuch 2.1 Kohlenstoffdioxid in der Atemluft 3 Versuch 2.2 Kohlenstoffdioxid als Produkt der Verbrennung
: - Atmung und Kohlenstoffdioxid - Inhalt Versuch 1 Kohlenstoffdioxidnachweis mit Kalkwasser 2 Versuch 2.1 Kohlenstoffdioxid in der Atemluft 3 Versuch 2.2 Kohlenstoffdioxid als Produkt der Verbrennung
Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit Empfohlene Gruppengröße. {time:2} 20 Minuten. Versuchsvarianten:
 Lehrer-/Dozentenblatt Gedruckt: 2.8.27 6::24 P753 Siedetemperatur Lehrerinformationen Einführung Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit Empfohlene Gruppengröße {complexity:3} mittel {time:}
Lehrer-/Dozentenblatt Gedruckt: 2.8.27 6::24 P753 Siedetemperatur Lehrerinformationen Einführung Schwierigkeitsgrad Vorbereitungszeit Durchführungszeit Empfohlene Gruppengröße {complexity:3} mittel {time:}
Veranstaltung 1: Ist Luft nichts?
 Veranstaltung 1: Ist Luft nichts? Station 1: Wer verdrängt hier wen? E1 Verdrängen von Wasser durch Luft E2 Verdrängen von Luft durch Wasser Station 2: Luft kann sich bewegen! E3 Bewegung von Luft durch
Veranstaltung 1: Ist Luft nichts? Station 1: Wer verdrängt hier wen? E1 Verdrängen von Wasser durch Luft E2 Verdrängen von Luft durch Wasser Station 2: Luft kann sich bewegen! E3 Bewegung von Luft durch
Löslichkeit gesättigte Lösung kaltgesättigte heissgesättigte
 Löslichkeit - In welcher Einheit wird die Löslichkeit eines Stoffes angegeben? - In welchem Grössenordnungsbereich schwankt die Löslichkeit von Feststoffen? - Wie sieht es mit der Löslichkeit von Gasen
Löslichkeit - In welcher Einheit wird die Löslichkeit eines Stoffes angegeben? - In welchem Grössenordnungsbereich schwankt die Löslichkeit von Feststoffen? - Wie sieht es mit der Löslichkeit von Gasen
Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden?
 Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden? Beschrifte die Kästchen mit je einem Aggregatzustand. Benenne die Nummern, es handelt sich dabei um Fachbegriffe für die Übergänge
Arbeitsblatt Sollte eine Wasserflasche aus Glas im Gefrierfach gekühlt werden? Beschrifte die Kästchen mit je einem Aggregatzustand. Benenne die Nummern, es handelt sich dabei um Fachbegriffe für die Übergänge
Schulversuchspraktikum. Isabel Böselt. Sommersemester Klassenstufen 5 & 6. Aggregatzustände. und deren Temperaturabhängigkeit
 Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Schulversuchspraktikum Isabel Böselt Sommersemester 2014 Klassenstufen 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden einfache
Fachhochschule Flensburg. Die spezifische Wärmekapazität fester Körper
 Name : Fachhochschule Flensburg Fachbereich Technik Institut für Physik und Werkstoffe Name: Versuch-Nr: W4 Die spezifische Wärmekapazität fester Körper Gliederung: Seite Einleitung 1 Berechnung 1 Versuchsbeschreibung
Name : Fachhochschule Flensburg Fachbereich Technik Institut für Physik und Werkstoffe Name: Versuch-Nr: W4 Die spezifische Wärmekapazität fester Körper Gliederung: Seite Einleitung 1 Berechnung 1 Versuchsbeschreibung
Masse, Volumen und Dichte
 Masse, Volumen und Dichte Ziel: Uns umgeben zahlreiche Gegenstände, die in der Physik als Körper bezeichnet werden. Diese Körper haben eine Reihe von grundlegenden Eigenschaften: Sie nehmen einen Raum
Masse, Volumen und Dichte Ziel: Uns umgeben zahlreiche Gegenstände, die in der Physik als Körper bezeichnet werden. Diese Körper haben eine Reihe von grundlegenden Eigenschaften: Sie nehmen einen Raum
B E I S P I E L A R B E I T / Aufgaben. Kultusministerium
 B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
Illustrierende Aufgaben zum LehrplanPLUS. Fachoberschule, Chemie, Jahrgangsstufe 11. Dosenimplosion
 Dosenimplosion Jahrgangsstufen 11 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material Chemie Technische Bildung 90 min leere Getränkedose (Plastik-)Pipette mit Graduierung
Dosenimplosion Jahrgangsstufen 11 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material Chemie Technische Bildung 90 min leere Getränkedose (Plastik-)Pipette mit Graduierung
Bestimmung des Massenverhältnisses bei der Reaktion von Magnesium mit Sauerstoff
 8 0 6 0 4 0 2 0 0 0 0 1 0 8 0 6 0 4 0 2 0 L m 1.1 Konstante Massenproportionen Untersuche, welches Volumen Sauerstoff für die Reaktion mit verschiedenen Massen Magnesium jeweils benötigt wird. Geräte 2
8 0 6 0 4 0 2 0 0 0 0 1 0 8 0 6 0 4 0 2 0 L m 1.1 Konstante Massenproportionen Untersuche, welches Volumen Sauerstoff für die Reaktion mit verschiedenen Massen Magnesium jeweils benötigt wird. Geräte 2
Ausdehnung von Luft bei konstantem Volumen
 Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Volumen (Artikelnr.: P042800) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Volumen (Artikelnr.: P042800) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Wärmeleitung in Flüssigkeiten (Artikelnr.: P )
 Lehrer-/Dozentenblatt Wärmeleitung in Flüssigkeiten (Artikelnr.: P1043400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Wärmetransport
Lehrer-/Dozentenblatt Wärmeleitung in Flüssigkeiten (Artikelnr.: P1043400) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Wärmetransport
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
HERFORD. Dichte - Ein spannendes oder langweiliges Thema. ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht.
 ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht HERFORD Dichte - Ein spannendes oder langweiliges Thema Jannik Rönsch Schule: Königin-Mathilde-Gymnasium Vlothoer Straße 1 32049 Herford
ZfP-Sonderpreis der DGZfP beim Regionalwettbewerb Jugend forscht HERFORD Dichte - Ein spannendes oder langweiliges Thema Jannik Rönsch Schule: Königin-Mathilde-Gymnasium Vlothoer Straße 1 32049 Herford
Chemie-Labothek zur Photochemie
 Fluoreszenz und Phosphoreszenz, Echtfarbenemissionsspektren (EFES) V1: Fluoreszenz und Phosphoreszenz Arbeitsmaterialien: Waage Mörser mit Pistill Porzellanschale Bunsenbrenner UV-Handlampe 7 Reagenzgläser
Fluoreszenz und Phosphoreszenz, Echtfarbenemissionsspektren (EFES) V1: Fluoreszenz und Phosphoreszenz Arbeitsmaterialien: Waage Mörser mit Pistill Porzellanschale Bunsenbrenner UV-Handlampe 7 Reagenzgläser
Was kannst Du (schon)? Stoffe und Eigenschaften D
 Falte zunächst das Blatt entlang des Pfeils nach hinten. Mache Dir zunächst alleine Gedanken über Deine Fähigkeiten und kreuze an. Tausche Dich im Folgenden mit Deinem Nachbar aus bzw. falte das Blatt
Falte zunächst das Blatt entlang des Pfeils nach hinten. Mache Dir zunächst alleine Gedanken über Deine Fähigkeiten und kreuze an. Tausche Dich im Folgenden mit Deinem Nachbar aus bzw. falte das Blatt
Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser?
 http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
http://www.kostenloseausmalbilder.de/media/.gallery/main606.jpg (02.08.2015) Arbeitsblatt Pip und Lucky: Was atmen Tiere im Wasser? Pip, die kleine Maus, benötigt zum Atmen Luft, vor allem den Sauerstoff,
Übungsprüfung A zur Physik-Prüfung vom 19. April 2012
 Übungsprüfung A zur Physik-Prüfung vom 19. April 2012 1. Temperatur-Umrechnung (6 Punkte) a) Die tiefste natürliche Temperatur, die jemals auf der Erde gemessen wurde, beträgt 89.2 C (Wostok-Station in
Übungsprüfung A zur Physik-Prüfung vom 19. April 2012 1. Temperatur-Umrechnung (6 Punkte) a) Die tiefste natürliche Temperatur, die jemals auf der Erde gemessen wurde, beträgt 89.2 C (Wostok-Station in
Stoffeigenschaften: Dichte und Löslichkeit
 Grundlagenfach Chemie 4. Kl. 1/5 Stoffeigenschaften: Dichte und Löslichkeit Einleitung Chemie ist die Lehre von Stoffen. Eine wichtige Unterscheidung ist die Einteilung in Reinstoffe und Gemische. Gemische
Grundlagenfach Chemie 4. Kl. 1/5 Stoffeigenschaften: Dichte und Löslichkeit Einleitung Chemie ist die Lehre von Stoffen. Eine wichtige Unterscheidung ist die Einteilung in Reinstoffe und Gemische. Gemische
Versuche zu Stärke. AGENS Arbeitsgemeinschaft NaturStoffe Leipzig
 Versuche zu Stärke Versuch 1 - Stärkegewinnung aus Kartoffeln Geräte: 2 Kunststoffschüssel groß 1 Kunststoffschüssel klein 1 Kartoffelreibe 1 Baumwoll- oder Leinentuch 2 Kartoffeln 1 Löffel 1 Trichter
Versuche zu Stärke Versuch 1 - Stärkegewinnung aus Kartoffeln Geräte: 2 Kunststoffschüssel groß 1 Kunststoffschüssel klein 1 Kartoffelreibe 1 Baumwoll- oder Leinentuch 2 Kartoffeln 1 Löffel 1 Trichter
Rezepte: 1. Brause herstellen
 1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
INHALTSVERZEICHNIS. 7 Temperatur und Zustandsänderungen 48 V1 Einfaches Flüssigkeitsthermometer 48 V2 Bimetallthermometer 50 Warm und kalt 52
 INHALTSVERZEICHNIS Verhaltensregeln 3 Einführung in das Praxisbuch 4 1 Physik bestimmt unser Leben 6 V1 Längenmessung 6 V2 Messung des Volumens 8 Exp Schwingunsdauer 10 Mein Zeigefinger! 12 2 Alles in
INHALTSVERZEICHNIS Verhaltensregeln 3 Einführung in das Praxisbuch 4 1 Physik bestimmt unser Leben 6 V1 Längenmessung 6 V2 Messung des Volumens 8 Exp Schwingunsdauer 10 Mein Zeigefinger! 12 2 Alles in
Verbrennung einer Kerze
 Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Schmelz- und Siedetemperaturen
 Schmelz- und Siedetemperaturen 1) Schmelztemperatur einiger fester Stoffe und Siedetemperatur von Wasser: Chemikalien: Geräte: Stearinsäure (=Octadecansäure), Fixiersalz (=Natriumthiosulfat-pentahydrat),
Schmelz- und Siedetemperaturen 1) Schmelztemperatur einiger fester Stoffe und Siedetemperatur von Wasser: Chemikalien: Geräte: Stearinsäure (=Octadecansäure), Fixiersalz (=Natriumthiosulfat-pentahydrat),
Ausdehnung von Luft bei konstantem Druck
 Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Druck (Artikelnr.: P042700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Lehrer-/Dozentenblatt Ausdehnung von Luft bei konstantem Druck (Artikelnr.: P042700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-0 Lehrplanthema: Wärmelehre Unterthema: Wärmeausdehnung
Experimente Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Die SuS experimentieren mit Salz und lernen es von der chemischen Seite her besser kennen. Dabei lernen sie in Modellversuchen wichtige Merkmale von Salz kennen. Ziel
Lehrerinformation 1/7 Arbeitsauftrag Die SuS experimentieren mit Salz und lernen es von der chemischen Seite her besser kennen. Dabei lernen sie in Modellversuchen wichtige Merkmale von Salz kennen. Ziel
A Sie ist weniger als 1 kg/dm 3. B E F D A G C. Zusammengesetzte Grössen 15
 1. Richtig oder falsch? A Stoffe mit einer Dichte unter 1 kg/dm 3 schwimmen in Wasser. Richtig B Die Dichte von kleinen Körpern ist immer kleiner als die Dichte von grossen Körpern. Falsch C Schwere Körper
1. Richtig oder falsch? A Stoffe mit einer Dichte unter 1 kg/dm 3 schwimmen in Wasser. Richtig B Die Dichte von kleinen Körpern ist immer kleiner als die Dichte von grossen Körpern. Falsch C Schwere Körper
Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann.
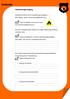 Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Spezifische Schmelzwärme von wis (Artikelnr.: P )
 Lehrer-/Dozentenblatt Spezifische Schmelzwärme von wis (Artikelnr.: P1044700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Schmelzen,
Lehrer-/Dozentenblatt Spezifische Schmelzwärme von wis (Artikelnr.: P1044700) Curriculare Themenzuordnung Fachgebiet: Physik Bildungsstufe: Klasse 7-10 Lehrplanthema: Wärmelehre Unterthema: Schmelzen,
N & T 1 Stoffeigenschaften 01 Name: Vorname: Datum:
 N & T 1 Stoffeigenschaften 01 Name: Vorname: Datum: Aufgabe 1: Natur und Technik wird aufgeteilt in drei Teilbereiche: diese sind jedoch nicht immer ganz klar abgetrennt: Wasser kann zum Kochen und zum
N & T 1 Stoffeigenschaften 01 Name: Vorname: Datum: Aufgabe 1: Natur und Technik wird aufgeteilt in drei Teilbereiche: diese sind jedoch nicht immer ganz klar abgetrennt: Wasser kann zum Kochen und zum
Kupfersteckbrief 06 AB1 MS
 Um einen Stoff und seine Eigenschaften genauer beschreiben zu können, ist es wichtig verschiedene Versuche durchzuführen und genau zu beobachten. Aufgabe: Erstelle einen Steckbrief für, indem du verschiedene
Um einen Stoff und seine Eigenschaften genauer beschreiben zu können, ist es wichtig verschiedene Versuche durchzuführen und genau zu beobachten. Aufgabe: Erstelle einen Steckbrief für, indem du verschiedene
Schwimmen, Schweben, Sinken
 Schulversuchspraktikum Patricia Hiller Sommersemester 2015 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Kurzprotokoll Auf einen Blick: In diesem Kurzprotokoll werden weitere Versuche rund um das Thema
Schulversuchspraktikum Patricia Hiller Sommersemester 2015 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Kurzprotokoll Auf einen Blick: In diesem Kurzprotokoll werden weitere Versuche rund um das Thema
Sonne wärmt A Papier. 1 Metall. 4 Holz
 Sonne wärmt A 20 An einem schönen sonnigen Tag treffen die Strahlen der Sonne auf Platten aus unterschiedlichen Materialien, die im Hof gelagert sind. 1 Metall 2 Papier 3 Mamor 4 Holz a) Ordne die Platten
Sonne wärmt A 20 An einem schönen sonnigen Tag treffen die Strahlen der Sonne auf Platten aus unterschiedlichen Materialien, die im Hof gelagert sind. 1 Metall 2 Papier 3 Mamor 4 Holz a) Ordne die Platten
DARUM GEHT S IN DIESER LernBOX. Mit dieser LernBOX kannst du folgendes lernen: A1 -wie man Kohlenstoffdioxid von Sprudel abtrennt. erledigt?
 Kohlenstoffdioxid (Teil1) Im Sprudel und in vielen Erfrischungsgetränken sorgen kleine Gasbläschen für ein angenehmes Kribbeln auf der Zunge. Sie bestehen aus Kohlenstoffdioxid, ein Gas, das nicht nur
Kohlenstoffdioxid (Teil1) Im Sprudel und in vielen Erfrischungsgetränken sorgen kleine Gasbläschen für ein angenehmes Kribbeln auf der Zunge. Sie bestehen aus Kohlenstoffdioxid, ein Gas, das nicht nur
Schüler und Schülerinnen im Labor in Rechtenthal. 4 weiße Stoffe
 Schüler und Schülerinnen im Labor in Rechtenthal 4 weiße Stoffe Chemische Laborgeräte (www.seilnacht.com) Chemische Stoffe unterscheiden sich durch ihre Eigenschaften 4 weiße Stoffe: Von außen sind sie
Schüler und Schülerinnen im Labor in Rechtenthal 4 weiße Stoffe Chemische Laborgeräte (www.seilnacht.com) Chemische Stoffe unterscheiden sich durch ihre Eigenschaften 4 weiße Stoffe: Von außen sind sie
prozessbezogene Kompetenzen E = Erkenntnisgewinnung K = Kommunikation B = Bewertung beachten Sicherheitsaspekte (E)
 Helene-Lange-Schule Hannover Fachcurriculum Chemie Jahrgang 5+6 Unterrichtsinhalte und inhaltsbezogene Kompetenzen (Die Schülerinnen und Schüler...) Klasse 5 prozessbezogene Kompetenzen E = Erkenntnisgewinnung
Helene-Lange-Schule Hannover Fachcurriculum Chemie Jahrgang 5+6 Unterrichtsinhalte und inhaltsbezogene Kompetenzen (Die Schülerinnen und Schüler...) Klasse 5 prozessbezogene Kompetenzen E = Erkenntnisgewinnung
Warum kann eine Büroklammer schwimmen?
 ARBEITSBLATT 1.1 Warum kann eine Büroklammer schwimmen? Warum kann eine Büroklammer schwimmen? Eigentlich schwimmt Metall nicht es kommt aber darauf an, wie geschickt man sich anstellt Ñ eine Büroklammer
ARBEITSBLATT 1.1 Warum kann eine Büroklammer schwimmen? Warum kann eine Büroklammer schwimmen? Eigentlich schwimmt Metall nicht es kommt aber darauf an, wie geschickt man sich anstellt Ñ eine Büroklammer
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Physik kompetenzorientiert: Mechanik 1
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Physik kompetenzorientiert: Mechanik 1 Das komplette Material finden Sie hier: Download bei School-Scout.de Eigenschaften von Körpern
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Physik kompetenzorientiert: Mechanik 1 Das komplette Material finden Sie hier: Download bei School-Scout.de Eigenschaften von Körpern
Chemische Grundlagen und Handgriffe
 Chemische Grundlagen und Handgriffe Beim chemischen Arbeiten gibt es viele spezielle Werkzeuge und Handgriffe. Drei davon wollen wir zu Beginn besonders gut erlernen. Es sind: das Heizen mit dem Gasbrenner
Chemische Grundlagen und Handgriffe Beim chemischen Arbeiten gibt es viele spezielle Werkzeuge und Handgriffe. Drei davon wollen wir zu Beginn besonders gut erlernen. Es sind: das Heizen mit dem Gasbrenner
Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz
 Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Name: Datum: Versuch: In der Natur verschwindet nichts - Lösen und Auskristallisieren von Salz Material: Kochsalz (NaCl), Leitungswasser, Mineralwasser, Becherglas, Spatel, destilliertes Wasser, Alu-Teelichtschalen,
Echt ätzend! - Was ist und wie wirkt Abflussreiniger?
 Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
Echt ätzend! - Was ist und wie wirkt Abflussreiniger? Versuch 1: Zusammensetzung von festem Abflussreiniger (Analyse nach Prof. Pick ): fester Abflussreiniger (z.b. Drano Rohrfrei) Petrischale, Holzstab
7. Themenfeld: Stoffe im Alltag 6. Klasse
 1 Stoffe und Stoffeigenschaften 2 Sicherheit http://www.elmar-kiessling.info/fachsem/sicher/labor.htm http://famona.bildung-rp.de/fileadmin/user_upload/famona.bildungrp.de/materialien/nawi/tf7/sicherheit.zip
1 Stoffe und Stoffeigenschaften 2 Sicherheit http://www.elmar-kiessling.info/fachsem/sicher/labor.htm http://famona.bildung-rp.de/fileadmin/user_upload/famona.bildungrp.de/materialien/nawi/tf7/sicherheit.zip
