Bundesrealgymnasium Imst. Chemie Klasse 7. Einführung in die Chemie
|
|
|
- Axel Auttenberg
- vor 7 Jahren
- Abrufe
Transkript
1 Bundesrealgymnasium Imst Chemie Klasse 7 Einführung in die Chemie Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter aufgearbeitet wird, als dies im Skriptum der Fall ist. Ergänzungen zum Skriptum werden während des Unterrichts durchgeführt. In diesem Skriptum sind nur wenige Diagramme und Zeichnungen enthalten. Die fehlenden Diagramme werden im Unterricht erarbeitet. Inhalt 1 Einführung in die Chemie Chemie als Naturwissenschaft Was ist Chemie Unterschiede zur Physik Fachgebiete der Chemie Historische Entwicklung Aufbau der Materie Aggregatszustände Trennen von Stoffgemischen Gemische und Reinstoffe Trennverfahren Moderne Methoden der Stofftrennung... 7 Aufgaben 9
2 1 Einführung in die Chemie 1.1 Chemie als Naturwissenschaft Was ist Chemie Chemie ist die Lehre von den Stoffen. Unter Stoff versteht man alle Arten von Materie. Die Chemie behandelt aber auch die Reaktionen, also die Stoffumwandlungen, untereinander. Darüber hinaus ist es die einzige Wissenschaft, die uns lehrt, aus bekannten Substanzen neue, in der Natur nicht vorkommende Stoffe herzustellen. Um das zu erreichen, müssen Aufbau und innere Strukturen der Stoffe bekannt sein damit mit wissenschaftlicher Präzision Stoffe verändert und somit den gestellten Anforderungen angepasst werden können. Werkstoffe, Baumaterialien, unsere Nahrungsmittel und Bekleidung, moderne Medikamente und Reinigungsmittel währen ohne diese Kenntnisse nicht denkbar. Alle diese Stoffe werden aber letztendlich aus natürlichen Stoffen aufgebaut Unterschiede zur Physik Chemische und physikalische Vorgänge sind oft miteinander Verbunden. Oft wird Physik als die Lehre von Vorgängen, bei denen keine stofflichen Veränderungen stattfinden, definiert. Entsprechend ist die Chemie die Wissenschaft, die sich eben mit diesen stofflichen Veränderungen beschäftigt. Betrachtet man allerdings die kleinsten Teilchen (im chemischen Sinn), die Atome, können physikalische oder chemische Prozesse nicht mehr eindeutig getrennt werden. Da chemische Reaktionen letztendlich auf einer elektrischen (physikalischen) Wechselwirkung beruhen, sind auch hier Überschneidungen üblich. Trotzdem gibt es genügend Prozess, die als typisch physikalisch oder typisch chemisch bezeichnet werden. Einige Beispiele: physikalisch Aggregatszustand Siedepunkt Schmelzpunkt Härte Leitfähigkeit Farbe, Glanz chemisch Erhalten gegenüber anderen Stoffen Verhalten bei Energiezufuhr (Verbrennen, Zersetzung) Physiologische Wirkung (z. B. Gift) Fachgebiete der Chemie Die Allgemeine und physikalische Chemie erforscht allgemein gültige Gesetzmäßigkeiten im Verhalten der Stoffe, ohne auf Besonderheiten bestimmter Stoffe einzugehen. Hierzu gehören Schmelz- und Siedevorgänge der Stoffe, Atombau und chemische Bindungen oder Geschwindigkeiten chemischer Reaktionen uvm. Die Anorganische Chemie befasst sich mit allen Elementen und allen Kombinationen dieser Elemente mit Ausnahme der Kohlenwasserstoffe und deren Derivate. Zu den anorganischen Stoffen gehören z. B. Metalle, Wasser, Erze,. Die Chemie der Kohlenwasserstoffe wird in der Organischen Chemie behandelt. Zu diesen Stoffen gehören Erdöl, Gas und Kohle wie auch Zucker, Proteine oder Enzyme. In der Biochemie werden Wechselwirkungen in der belebten Natur zusammengefasst. Um die Zusammensetzung der Stoffe zu klären unterscheidet man in der Analytische Chemie die quantitative Analytik (bestimmt die mengenmäßige Zusammensetzung der Bestandteile eines Stoffes) von der qualitativen Analytik (bestimmt, aus welchen Bestandteilen ein Stoff besteht). Dr. K.-H. Offenbecher Seite 2
3 Chemisches Wissen in die Praxis und in Produktionsverfahren umzusetzen ist Gegenstand der Technischen Chemie. Vorwiegend mit mathematischen Modellen und Simulationen berechnet die Theoretische Chemie Eigenschaften von Stoffen Historische Entwicklung Physikalische, chemische und biologische Prozesse laufen seit Urzeiten in der Natur ab, auch ohne den Menschen. Mit Hilfe der Wissenschaften erkannte der Mensch die Naturzusammenhänge und konnte diese in zunehmendem Maße zur Verbesserung seiner Lebensgrundlage nutzen. Die historische Entwicklung der Chemie als Wissenschaft begann mit den Naturphilosophen in der Antike. Auf sie gehen viele noch heute genutzte Begriffe wie Atom, Element, Elektron oder Verbindung zurück. Einige Meilensteine: BC. Entdeckung des Feuers BC. Verwendung anorganischer Pigmente zum Färben (Höhlenmalereien von Altamira und Lascaux) BC. Beginn der Bronzezeit zuerst in Mesopotamien, später in Europa 400 BC. Leukipp und Demokrit entwickeln die erste Atomtheorie und führen den Atombegriff ein AC. Symbole für damals bekannte Metalle und einige chemische Fachbegriffe entstsehen G. E. Stahl findet eine systematische Erklärung für chemische Reaktionen 1792/93 J. B. Richter begründet die Stöchiometrie 1824 F. Wöhler synthetisiert Harnstoff und begründet damit die organische Chemie 1869 L. J. Meyer und D. Mendelejew stellen das Periodensystem der Elemente auf 1911 E. Rutherford stellt eine Theorie zur Atomstruktur auf 2005 verschiedene Arbeitsgruppen entschlüsseln die DNA-Sequenz des menschlichen X-Chromosoms 1.2 Aufbau der Materie Aggregatszustände Aggregatszustand ist die allgemeine Bezeichnung für einen der drei Zustände, in denen Körper vorliegen können. Ein fester Körper besitzt ein bestimmtes Volumen und eine bestimmte Gestalt. Zwischen den Teilchen wirken sehr starke Anziehungskräfte wodurch sich Gitterstrukturen bilden. Dabei sind die Atome regelmäßig angeordnet. Bleiben die Atome ungeordnet, spricht man von amorphen Stoffen (z. B. Glas). Führt man einem Festkörper Wärmeenergie zu bis die Gitterkräfte nicht mehr ausreichen um die Struktur des Kristalls aufrecht zu halten, schmilzt der Festkörper. Ein flüssiger Körper besitzt ein bestimmtes Volumen aber keine bestimmte Gestalt. Er nimmt die Form des Gefäßes an in dem er sich befindet und bildet dabei eine Oberfläche. Dr. K.-H. Offenbecher Seite 3
4 Chemie Klasse 7 Einführung Zwischen den Teilchen wirkenn Anziehungskräfte (Kohäsion).. Die Kohäsion ist Ursache der Oberflächenspannung. Abb. 1-1: Zustandekommen einer Oberflächenspannung Ein gasförmiger Körper hatt weder ein bestimmtes Volumen noch eine bestimmte Gestalt. Er nimmt jeden ihm zur Verfügung stehenden Raum ein und bildet dabei keine Oberfläche. Zwischen den Teilchen wirkenn (fast) keine Kräfte. Gase besitzen einen Druck Der Druck p (Pa), den eine bestimmte Gasmenge auf den Behälter ausübt, ist vom Volumen des Behälters und von der Temperatur abhängig. Der Druck in einem Gasbehälter hängt bei allen Gasen linear von der Temperatur ab. Werden diese Geraden extrapoliert, erhält man einen gemeinsamen Schnittpunkt bei 273,15 C dem absolutenn Nullpunkt. Die Bewegung der Gasmoleküle hat aufgehört. Die Beziehung zwischen Druck, Temperatur und Volumen wirdd durch das allgemeine Gasgesetz eines idealen Gases wiedergegeben. p1 V1 p2 V2 = = konst. T T 1 2 Abb. 1-2: Temperaturabhängigkeit des Drucks und Herleitung des absoluten Nullpunkts Umwandlungswärme Schmelz und Kristallisationswärme einer Stoffmenge sind gleich groß! Verdampfungs und Kondensationswärme einer Stoffmenge sind gleichh groß! Sublimationswärme und Resublimationswärme eines Stoffes sind gleich groß! Abb. 1-3: Umwandlungswärme Dr. K.-H. Offenbecher Seite 4
5 Chemie Klasse 7 Einführung Verdampfen Die Bewegungsenergien der einzelnen Teilchen in einer Flüssigkeit sind unterschiedlich. Bei einigen Teilchen sind sie groß genug um die Kohäsionskräfte zu überwinden. Weil dadurch die energiereichsten Teilchen aus der Flüssigkeit entfernt werden, sinkt die Temperatur der Flüssigkeit. Abb. 1-4: Theorie einer verdampfenden Flüssigkeit. Verdunsten Bei Raumtemperatur entweichen ebenfalls nur die Teilchen, deren Bewegungsenergie ausreicht, um die Kohäsions-kräfte zu überwinden. Die sinkende Temperatur entzieht der Umgebung Wärme und es entsteht Verdunstungskälte. Abb. 1-5: Statistische Verteilung der Bewegungsenergie der Teilchen einer Flüssigkeit Dampfdruck Der Druck des Dampfes, der sich bei gegebener Temperatur im Gleichgewicht mit einer Flüssigkeit befindet. Abb. 1-6: Vergleich Verdampfen - Verdunsten Der Dampfdruck einer Flüssigkeit wird nur durch die Temperatur festgelegt. Änderungen des Dampfvolumens beeinflussen ihn nicht. Abb. 1-7: Dampfdruckkurven verschiedener Flüssigkeiten. Dr. K.-H. Offenbecher Seite 5
6 Chemie Klasse 7 Einführung Siedepunkt Der Siedepunkt Kp einer Flüssigkeit ist jene Temperatur, bei der der Dampfdruck der Flüssigkeit dem Luftdruck entspricht. Die Temperatur einer siedenden Flüssigkeit bleibt konstant, bis die gesamtee Menge verdampft ist. 1.3 Trennen von Stoffgemischen Fast alle Stoffe des täglichen Lebens sind keine Reinstoffe. Die Auftrennung dieser Gemische und die damit verbundene Gewinnung von Reinstoffen sind wichtige Arbeitsgebiete der Chemiker Gemische und Reinstoffe Reinstoffe besitzen eine einheitliche Zusammensetzung und Eigenschaften, die nur dieser Stoff besitzt, d. h. für diesen Stoff charakteristisch sind. Dazu gehören: Masse Gewicht Dichte Stoffzustand (Aggregatszustand bei Standardbedingungen) Siedetemperatur Teilchengröße Magnetische Eigenschaften Elektrische Eigenschaften Löslichkeit Verhalten bei Reaktionen mit anderen Stoffen Bei Mischungen hängen die Eigenschaften von der Zusammensetzung ab. Bei manchen Stoffen unserer Umwelt erkennt man sofort, dass sie aus Anteilen mit unterschiedlichen Eigenschaften bestehen (z. B. Gesteine mit unterschiedlich farbigen Bestandteilen). Solche optisch uneinheitlichen Stoffe werden als heterogen bezeichnet. Sie bestehen aus mehreren Phasen. Bei anderen Stoffen (z. B. Luft) erkennt man keine unterschiedlichenn Bestandteile. Sie bestehen aus einer Phase und werden als homogen bezeichnet. Als Phase bezeichnet man homogene Bereiche eines Stoffes. Reinstoffe und Mischungen können mit Hilfe des Siedediagramms (Abb. 1-8) leicht unterschieden werden. Abb. 1-8: Siedediagramm eines Reinstoffes und eines Gemisches. Dr. K.-H. Offenbecher Seite 6
7 1.3.2 Trennverfahren Um Reinstoffe aus Mischungen zu erhalten, werden fast immer die unterschiedlichen physikalischen Eigenschaften zur Trennung der Komponenten ausgenützt. Die Trennung von Gemischen erfolgt aus zwei Gründen: Gewinnung von Reinstoffen zur Anwendung oder Weiterverwendung Feststellung der Zusammensetzung einer Mischung (Analyse). Sieben Filtrieren Sedimentieren Zentrifugieren Fällen Extrahieren Destillieren, Verdampfen Die Teilchengröße der zu trennenden Stoffe muss unterschiedlich sein. Getrennt werden Feststoffe (z. B. Gemenge) Die zu trennende Suspension (fest-flüssig) läuft durch einen Filter (Textilfasern, Papier). Die festen Teilchen werden vom Filter zurückgehalten, die Flüssigkeit (Filtrat) läuft durch den Filter. Die in der Flüssigkeit aufgeschlämmten schweren festen Stoffe setzen sich ab, die klare Flüssigkeit wird vom abgesetzten Stoff abgegossen (dekantiert). Trennung von Suspensionen oder Emulsionen unter Ausnutzung der unterschiedlichen Dichte Ein Bestandteil einer Lösung wird durch eine chemische Reaktion mit einem zugesetzten Stoff (Fällungsmittel) in einen schwer löslichen Niederschlag überführt und filtriert. Bestimmte Bestandteile fester oder flüssiger Stoffe werden mithilfe geeigneter Lösungsmittel herausgelöst (Kaffee- oder Teekochen) Ein Flüssigkeitsgemisch wird erhitzt bis ein Anteil siedet. Der entstehende Dampf (Destillat) wird aufgefangen und kondensiert an einem Kühler. Chromatographie Unterschiedliche Adsorptions- und Lösungseigenschaften führen zu unterschiedlichen Geschwindigkeiten beim Transport durch eine mobile Phase durch eine stationäre Phase Elektrophorese Trennung aufgrund unterschiedlicher Geschwindigkeiten in einem elektrischen Feld Moderne Methoden der Stofftrennung Durch chromatographische Methoden ist es heute möglich, verschiedenste Stoffe, wie kleinste Rückstände von Pflanzenschutzmitteln, Schwermetallspuren oder geringste Mengen von Luftverunreinigungen mit hoher Sicherheit und Genauigkeit nachzuweisen. Standard sind Nachweisgrenzen von 10-9 kg/kg (Einheit ppb, parts per billion). Das bedeutet, dass ein Teilchen unter Teilchen entdeckt wird. Unter guten Voraussetzungen sind aber auch Nachweise von kg/kg oder darunter möglich. Die chromatographische Trennanordnung (Analysemethode) besteht immer aus einer unbeweglichen (stationären) Phase (z. B. Papier) und einer beweglichen (mobilen) Phase (z. B. Wasser), die die Trennanordnung durchströmt. Je länger ein Bestandteil einer Mischung von der stationären Phase zurückgehalten wird, umso langsamer wandert er durch die Trennanordnung. Dr. K.-H. Offenbecher Seite 7
8 Hochdruckflüssigkeitschromatographie (HPLC) Das Lösungsmittel, die mobile Phase, wird aus einem Vorratsgefäß mittels einer Hochdruckpumpe durch die Trennsäule gepresst. Durch eine Dosiereinheit bringt man die Probe in den Fluss der mobilen Phase ein. Die einzelnen Probenkomponenten werden in der Trennsäule aufgetrennt und verlassen diese mit unterschiedlicher Verzögerung. Sie durchströmen nacheinander einen Detektor, der für jede Komponente ein elektrisches Signal liefert Gaschromatographie (GC) Hier strömt ein Trägergas als mobile Phase durch eine Trennsäule oder Trennkapillare. In ihr befindet sich als stationäre Phase eine Flüssigkeit mit hohem Siedepunkt. In Trennsäulen wird diese Flüssigkeit in den Poren eines Feststoffes festgehalten. In Trennkapillaren bildet sie einen dünnen Film an der Innenseite der Kapillare. Die Länge von Trennkapillaren kann bis zu 100 m betragen. Dr. K.-H. Offenbecher Seite 8
9 Aufgaben 1. Geben Sie an, ob es sich bei folgenden Stoffen um ein chemisches Element oder um eine Verbindung handelt: a) Kohlendioxid; b) Schwefel; c) Luft; d) Wasser; e) Kochsalz; Schwefelsäure 2. Geben Sie an, ob es sich bei folgenden Stoffen um ein chemisches Element, ein Verbindung oder ein Gemisch handelt: a) Wasser; b) Eisen; c) Schwefel; d) Luft; e) Leitungswasser; f) Traubenzucker; g) Wein 3. Geben Sie an, ob es sich bei folgenden Stoffen um homogene oder heterogene Stoffgemische handelt: a) Sand in Wasser; b) Kochsalz, in Wasser gelöst; c) Luft; d) Milch; e) Staub 4. Ordnen Sie folgende Eigenschaften den Stoffkategorien Element, Verbindung, und Gemisch zu: a) Zusammensetzung ist variabel; b) besitzt eine chemische Formel; c) durch physikalische Methoden in andersartige Stoffe zerlegbar; d) durch chemische Methoden in andersartige Stoffe zerlegbar; e) durch keine Methode zerlegbar; f) kann gasförmig sein; g) kann in der Natur vorkommen. 5. Durch welche der folgenden Trennmethoden kann eine wässrige Kochsalzlösung in Kochsalz und Wasser getrennt werden? a) Filtrieren; b) Zentrifugieren; c) Sedimentieren; d) Destillieren; e) Dekantieren 6. Schlagen Sie Wege vor, wie man die Gemische Salz/Pfeffer und Sand/Sägespäne in die Bestandteile zerlegen kann! 7. Beschreiben Sie ein Beispiel für die praktische Anwendung der Extraktion, Filtration, Destillation! Dr. K.-H. Offenbecher Seite 9
Materie ist die Gesamtheit aller Stoffe: Energie bei chemischen Reaktionen:
 A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt eine Masse m (Einheit: kg) Dichte = Masse / Volumen
A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt eine Masse m (Einheit: kg) Dichte = Masse / Volumen
Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt.
 1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
1 Definition: Chemie ist eine naturwissenschaftliche Disziplin, welche sich mit den Stoffen, den Stoffeigenschaften und den Stoffumwandlungen beschäftigt. 2 Erscheinungsformen der Materie Homogen oder
Bundesrealgymnasium Imst. Chemie 2010-11. Klasse 4. Einführung Stoffe
 Bundesrealgymnasium Imst Chemie 2010-11 Einführung Stoffe Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 Einführung Stoffe Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Buch Seite 3-5. WIW - HTL St. Pölten
 Aufbau der Materie Aggregatzustände Buch Seite 3-5 A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt
Aufbau der Materie Aggregatzustände Buch Seite 3-5 A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Trennverfahren (c) by Gerald Trutschl
 Trennverfahren (c) by Gerald Trutschl Inhalt Einteilung der Materie Homogene vs. Heterogene Gemische Trennverfahren Materie Materie by GT Gemische Reinstoffe heterogene Elemente homogene Verbindungen Gemische
Trennverfahren (c) by Gerald Trutschl Inhalt Einteilung der Materie Homogene vs. Heterogene Gemische Trennverfahren Materie Materie by GT Gemische Reinstoffe heterogene Elemente homogene Verbindungen Gemische
Gase sind in Wasser löslich Solche Lösungen können auch gesättigt sein
 4. TRENNEN UND MISCHEN ARBEITSBLATT 4.1 DIE LÖSLICHKEIT VON GASEN IN FLÜSSIGKEITEN Können sich Gase wie Festkörper in Flüssigkeiten lösen? Was lässt sich über die Löslichkeit von Kohlendioxid in Wasser
4. TRENNEN UND MISCHEN ARBEITSBLATT 4.1 DIE LÖSLICHKEIT VON GASEN IN FLÜSSIGKEITEN Können sich Gase wie Festkörper in Flüssigkeiten lösen? Was lässt sich über die Löslichkeit von Kohlendioxid in Wasser
3. STOFFE MISCHEN UND TRENNEN
 CHEMIE / 4.0S Seite - 3.1-3. STOFFE MISCHEN UND TRENNEN 3.1. Herstellung von Gemischen: Die genaue Mischung von Farben, Kosmetika, Reinigungsmitteln u.s.w. sind wohlgehütete Betriebsgeheimnisse der Herstellerfirmen.
CHEMIE / 4.0S Seite - 3.1-3. STOFFE MISCHEN UND TRENNEN 3.1. Herstellung von Gemischen: Die genaue Mischung von Farben, Kosmetika, Reinigungsmitteln u.s.w. sind wohlgehütete Betriebsgeheimnisse der Herstellerfirmen.
Chemische Reaktionen ergeben neue Stoffe mit neuen Eigenschaften
 1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
Gegenstand genau zu beschreiben? Antworten: a) Geschmack & Form (=> Posten 2a) b) Dichte & Form (=> Posten 3d) c) Stoff & Form
 Posten 1a Was muss man alles angeben, um einen Gegenstand genau zu beschreiben? a) Geschmack & Form (=> Posten 2a) b) Dichte & Form (=> Posten 3d) c) Stoff & Form (=> Posten 4j) d) Dichte & Stoff (=> Posten
Posten 1a Was muss man alles angeben, um einen Gegenstand genau zu beschreiben? a) Geschmack & Form (=> Posten 2a) b) Dichte & Form (=> Posten 3d) c) Stoff & Form (=> Posten 4j) d) Dichte & Stoff (=> Posten
Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? Antworten: a) es entsteht Wasserdampf (Wasser-
 Posten 1a Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? a) es entsteht Wasserdampf (Wasser- (=> Posten 5l) tropfen kondensieren am Streifen) b) der Schwefeldampf wird
Posten 1a Was passiert, wenn Schwefeldampf über einen heissen Kupferblechstreifen streicht? a) es entsteht Wasserdampf (Wasser- (=> Posten 5l) tropfen kondensieren am Streifen) b) der Schwefeldampf wird
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kovalente Bindung Oktett-Regel Valence-Bond-Theorie
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kovalente Bindung Oktett-Regel Valence-Bond-Theorie
Anorganische Chemie! der unbelebten Natur keine Kohlenstoffverbindung (Kohlenstoffatome C) Metall Nichtmetallverbindungen Ionenbindung
 3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3. Stoffgemische und Ihre Zerlegung
 3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
Individualisierung im Naturwissenschaftlichen Unterricht DI Dr. mont. Monika Grasser, HTBLVA Ferlach 2. Jahrgang HTL Naturwissenschaften
 Individualisierung im Naturwissenschaftlichen Unterricht DI Dr. mont. Monika Grasser, HTBLVA Ferlach 2. Jahrgang HTL Naturwissenschaften Thema: Trennverfahren. Unterrichtsziel Anhand der vorbereiteten
Individualisierung im Naturwissenschaftlichen Unterricht DI Dr. mont. Monika Grasser, HTBLVA Ferlach 2. Jahrgang HTL Naturwissenschaften Thema: Trennverfahren. Unterrichtsziel Anhand der vorbereiteten
prozessbezogene Kompetenzen E = Erkenntnisgewinnung K = Kommunikation B = Bewertung beachten Sicherheitsaspekte (E)
 Helene-Lange-Schule Hannover Fachcurriculum Chemie Jahrgang 5+6 Unterrichtsinhalte und inhaltsbezogene Kompetenzen (Die Schülerinnen und Schüler...) Klasse 5 prozessbezogene Kompetenzen E = Erkenntnisgewinnung
Helene-Lange-Schule Hannover Fachcurriculum Chemie Jahrgang 5+6 Unterrichtsinhalte und inhaltsbezogene Kompetenzen (Die Schülerinnen und Schüler...) Klasse 5 prozessbezogene Kompetenzen E = Erkenntnisgewinnung
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
Chemie. Die Chemie beschäftigt sich mit materiellen Dingen; Sie ist die Lehre von den Stoffen.
 Chemie Die Chemie beschäftigt sich mit materiellen Dingen; Sie ist die Lehre von den Stoffen. Stoffeinteilung: Stoffdefinition: Ein Stoff liegt dann vor, wenn dieser ein Volumen einnimmt und eine Masse
Chemie Die Chemie beschäftigt sich mit materiellen Dingen; Sie ist die Lehre von den Stoffen. Stoffeinteilung: Stoffdefinition: Ein Stoff liegt dann vor, wenn dieser ein Volumen einnimmt und eine Masse
Vorlesung Allgemeine Chemie: Die lange Odyssee zur konsistenten Stöchiometrie
 Vorlesung Allgemeine Chemie: Die lange Odyssee zur konsistenten Stöchiometrie Inhalte Grundbegriffe der Stöchiometrie (Element, Verbindung, Formeln, Stoffmenge), klassische Gesetze (G. d. Erhaltung der
Vorlesung Allgemeine Chemie: Die lange Odyssee zur konsistenten Stöchiometrie Inhalte Grundbegriffe der Stöchiometrie (Element, Verbindung, Formeln, Stoffmenge), klassische Gesetze (G. d. Erhaltung der
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften
 Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Löslichkeit gesättigte Lösung kaltgesättigte heissgesättigte
 Löslichkeit - In welcher Einheit wird die Löslichkeit eines Stoffes angegeben? - In welchem Grössenordnungsbereich schwankt die Löslichkeit von Feststoffen? - Wie sieht es mit der Löslichkeit von Gasen
Löslichkeit - In welcher Einheit wird die Löslichkeit eines Stoffes angegeben? - In welchem Grössenordnungsbereich schwankt die Löslichkeit von Feststoffen? - Wie sieht es mit der Löslichkeit von Gasen
Modelle helfen Erscheinungen und Vorgänge zu beschreiben und Wesentliches zu erkennen, geben jedoch die Wirklichkeit nie vollständig wieder.
 I. Stoffen auf der Spur 1. Eigenschaften von Stoffen erkennen Farbe Geruch Geschmack Kristallform Klang Zustandsform 2. Eigenschaften von Stoffen ermitteln/ messen Wärmeleitfähigkeit Elektrische Leitfähigkeit
I. Stoffen auf der Spur 1. Eigenschaften von Stoffen erkennen Farbe Geruch Geschmack Kristallform Klang Zustandsform 2. Eigenschaften von Stoffen ermitteln/ messen Wärmeleitfähigkeit Elektrische Leitfähigkeit
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung der allgemeinen chemischen Grundlagen und Aspekte, die für alle Bereiche der Chemie notwendig sind; Modellvorstellungen Inhaltsübersicht:
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung der allgemeinen chemischen Grundlagen und Aspekte, die für alle Bereiche der Chemie notwendig sind; Modellvorstellungen Inhaltsübersicht:
Der Chemielehrer wettet um eine Tafel Schokolade, dass kein Schüler länger als zwei Minuten ohne chemische Reaktion auskommen kann.
 1 Einleitung Wozu Chemie? Der Chemielehrer wettet um eine Tafel Schokolade, dass kein Schüler länger als zwei Minuten ohne chemische Reaktion auskommen kann. Überprüfung: Wer kann länger als zwei Minuten
1 Einleitung Wozu Chemie? Der Chemielehrer wettet um eine Tafel Schokolade, dass kein Schüler länger als zwei Minuten ohne chemische Reaktion auskommen kann. Überprüfung: Wer kann länger als zwei Minuten
Stoffeigenschafte n, Trennmethoden und Verbindungen
 Stoffeigenschafte n, Trennmethoden und Verbindungen Linus Metzler Stoffeigenschaften, Trennmethoden und Verbindungen L i m e n e t L i n u s M e t z l e r W a t t s t r a s s e 3 9 3 0 6 F r e i d o r
Stoffeigenschafte n, Trennmethoden und Verbindungen Linus Metzler Stoffeigenschaften, Trennmethoden und Verbindungen L i m e n e t L i n u s M e t z l e r W a t t s t r a s s e 3 9 3 0 6 F r e i d o r
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
Extraktion. Extraktion: Unter Extrahieren versteht man das Herauslösen eines oder mehrerer Stoffe aus einem festen Gemisch oder einer Lösung.
 Extraktion Extraktion: Unter Extrahieren versteht man das Herauslösen eines oder mehrerer Stoffe aus einem festen Gemisch oder einer Lösung. a) Festkörper Zum Extrahieren gut löslicher Substanzen genügt
Extraktion Extraktion: Unter Extrahieren versteht man das Herauslösen eines oder mehrerer Stoffe aus einem festen Gemisch oder einer Lösung. a) Festkörper Zum Extrahieren gut löslicher Substanzen genügt
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Arbeitsauftrag: Destillation
 Abfalltrennung Arbeitsauftrag: Destillation Aufgabe: Baue eine Destillationsapparatur auf (Lass dir dabei von deinem Lehrer helfen) und fertige eine Skizze in deinem Laborbuch dazu an. Verfolge, wie sich
Abfalltrennung Arbeitsauftrag: Destillation Aufgabe: Baue eine Destillationsapparatur auf (Lass dir dabei von deinem Lehrer helfen) und fertige eine Skizze in deinem Laborbuch dazu an. Verfolge, wie sich
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
8.4.5 Wasser sieden bei Zimmertemperatur ******
 8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
8.4.5 ****** 1 Motivation Durch Verminderung des Luftdrucks siedet Wasser bei Zimmertemperatur. 2 Experiment Abbildung 1: Ein druckfester Glaskolben ist zur Hälfte mit Wasser gefüllt, so dass die Flüsigkeit
Allgemeine Chemie WS 04/05
 Allgemeine Chemie WS 04/05 Vorlesung: Dienstag 8:30-10:00, Beginn 19. 10. 2004 Grüner Hörsaal D5104 Übungen: Mittwoch 8:30-9:00, Beginn 20. 10. 2004 Grüner Hörsaal D5104 Gez. Prof. A. J. Meixner für die
Allgemeine Chemie WS 04/05 Vorlesung: Dienstag 8:30-10:00, Beginn 19. 10. 2004 Grüner Hörsaal D5104 Übungen: Mittwoch 8:30-9:00, Beginn 20. 10. 2004 Grüner Hörsaal D5104 Gez. Prof. A. J. Meixner für die
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen.
 Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Kapitel 1: Einfache Laborarbeiten
 Kapitel 1: Einfache Laborarbeiten Handhabung von Chemikalien und Geräten Bearbeitung von Glas Pipetten, kleine Reagenzgläser, Gaseinleitungsrohr keine Protokolle notwendig, Durchführung wird nicht testiert
Kapitel 1: Einfache Laborarbeiten Handhabung von Chemikalien und Geräten Bearbeitung von Glas Pipetten, kleine Reagenzgläser, Gaseinleitungsrohr keine Protokolle notwendig, Durchführung wird nicht testiert
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
LB1 Stoffe. LB1 Stoffe. LB1 Stoffe. Womit beschäftigt sich die Chemie?
 Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Lösung. Gasgemisch. Legierung. Suspension. Ein löslicher Stoff (z.b. Salz) ist in einem Lösungsmittel (z.b. Wasser) gelöst.
 Ein löslicher Stoff (z.b. Salz) ist in einem Lösungsmittel (z.b. Wasser) gelöst. Lösung 8C1 Jede Lösung ist ein homogenes Stoffgemisch: Feststofflösung: Feststoff ist in Flüssigkeit gelöst (Zuckerwasser)
Ein löslicher Stoff (z.b. Salz) ist in einem Lösungsmittel (z.b. Wasser) gelöst. Lösung 8C1 Jede Lösung ist ein homogenes Stoffgemisch: Feststofflösung: Feststoff ist in Flüssigkeit gelöst (Zuckerwasser)
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
 Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Lösungen flüchtiger Stoffe - Stofftrennung http://ac16.uni-paderborn.de/lehrveranstaltungen/_aac/vorles/skript/kap_7/kap7_5/ Für Lösungen flüchtiger Stoffe ist der Dampfdruck des Gemischs ebenfalls von
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Jeder Gegenstand Stoff Jeder Stoff Eigenschaften
 Stoffe Jeder Gegenstand der Welt, die euch umgibt, besteht aus einem chemischen Stoff. Jeder Stoff hat ganz spezielle Eigenschaften, die bestimmen, wie er verwendet wird. Die Chemie hat die Aufgabe die
Stoffe Jeder Gegenstand der Welt, die euch umgibt, besteht aus einem chemischen Stoff. Jeder Stoff hat ganz spezielle Eigenschaften, die bestimmen, wie er verwendet wird. Die Chemie hat die Aufgabe die
Destillation. Erdöl: durch die Trennung von Erdöl kann man verschiedene Benzine gewinnen. Z.B.: Diesel, Schweröl und Asphalt.
 Destillation Erklärung: Destillation ist ein Verfahren, bei dem verschiedene, meistens flüssige Stoffe, getrennt werden. Die Emulsion, die du trennen möchtest, wird in einem Kolben zum Sieden gebracht.
Destillation Erklärung: Destillation ist ein Verfahren, bei dem verschiedene, meistens flüssige Stoffe, getrennt werden. Die Emulsion, die du trennen möchtest, wird in einem Kolben zum Sieden gebracht.
Trennmethoden: fest/flüssig
 Kapitel 3: Trenn und Reinigungsmethoden Verschiedene Methoden, je nach Aufgabenstellung dekantieren, filtrieren, abnutschen, zentrifugieren : Wahl der Methode je nach Niederschlag und Ziel Zustand des
Kapitel 3: Trenn und Reinigungsmethoden Verschiedene Methoden, je nach Aufgabenstellung dekantieren, filtrieren, abnutschen, zentrifugieren : Wahl der Methode je nach Niederschlag und Ziel Zustand des
Einführung in die Chromatographie
 Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/32 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Einführung in die Chromatographie Vorlesung WS 2007/2008 VAK 02-03-5-AnC2-1 Johannes Ranke Einführung in die Chromatographie p.1/32 Programm 23. 10. 2007 Trennmethoden im Überblick und Geschichte der Chromatographie
Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung)
 Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Versuch Nr. 57 Dampfdruck von Flüssigkeiten (Clausius-Clapeyron' sche Gleichung) Stichworte: Dampf, Dampfdruck von Flüssigkeiten, dynamisches Gleichgewicht, gesättigter Dampf, Verdampfungsenthalpie, Dampfdruckkurve,
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I
 Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
Institut für Anorganische Chemie Prof. Dr. R. Streubel Modul BCh 1.2 Praktikum Anorganische und Analytische Chemie I Vorlesung für die Studiengänge Bachelor Chemie und Lebensmittelchemie Im WS 08/09 Die
B E I S P I E L A R B E I T / Aufgaben. Kultusministerium. Name, Vorname: Klasse: Schule: Seite 1 von 6
 B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
Modul: Allgemeine Chemie
 Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
Modul: Allgemeine Chemie 5. Grundlagen der chemischen Bindung Ionenbindung Eigenschaften, Ionengitter, Kugelpackung Strukturtypen, Kreisprozesse Kovalente Bindung Lewis Formeln, Oktettregel, Formalladungen
7. Themenfeld: Stoffe im Alltag 6. Klasse
 1 Stoffe und Stoffeigenschaften 2 Sicherheit http://www.elmar-kiessling.info/fachsem/sicher/labor.htm http://famona.bildung-rp.de/fileadmin/user_upload/famona.bildungrp.de/materialien/nawi/tf7/sicherheit.zip
1 Stoffe und Stoffeigenschaften 2 Sicherheit http://www.elmar-kiessling.info/fachsem/sicher/labor.htm http://famona.bildung-rp.de/fileadmin/user_upload/famona.bildungrp.de/materialien/nawi/tf7/sicherheit.zip
Charakteristisch für die Denkweise in der Naturwissenschaft Chemie sind zwei Betrachtungsebenen:
 Charakteristisch für die Denkweise in der Naturwissenschaft Chemie sind zwei Betrachtungsebenen: Stoffebene: Teilchenebene: Stoffgemische: Betrachtungen an Stoffportionen und Reaktionen (Fakten, Phänomene)
Charakteristisch für die Denkweise in der Naturwissenschaft Chemie sind zwei Betrachtungsebenen: Stoffebene: Teilchenebene: Stoffgemische: Betrachtungen an Stoffportionen und Reaktionen (Fakten, Phänomene)
02. Was kann man über die Teilchen eines schmelzenden Stoffes aussagen?
 01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
Praktikum Allgemeine Chemie SS 2013
 Praktikum Allgemeine Chemie SS 2013 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Kapitel 1: Einfache Laborarbeiten
Praktikum Allgemeine Chemie SS 2013 Dr. Lars Birlenbach Physikalische Chemie, Universität Siegen Raum AR-F0102 Tel.: 0271 740 2817 email: birlenbach@chemie.uni-siegen.de Kapitel 1: Einfache Laborarbeiten
Was kannst Du (schon)? Stoffe und Eigenschaften D
 Falte zunächst das Blatt entlang des Pfeils nach hinten. Mache Dir zunächst alleine Gedanken über Deine Fähigkeiten und kreuze an. Tausche Dich im Folgenden mit Deinem Nachbar aus bzw. falte das Blatt
Falte zunächst das Blatt entlang des Pfeils nach hinten. Mache Dir zunächst alleine Gedanken über Deine Fähigkeiten und kreuze an. Tausche Dich im Folgenden mit Deinem Nachbar aus bzw. falte das Blatt
Trenne ein Gemisch aus Sand und Kochsalz sowie ein Gemisch aus Sand und Eisen.
 Naturwissenschaften - Chemie - Allgemeine Chemie - 3 Trennverfahren (P750900) 3.2 Gemischtrennungen - Filtrieren, Magnetscheidung Experiment von: Phywe Gedruckt:.0.203 2:53:30 intertess (Version 3.06 B200,
Naturwissenschaften - Chemie - Allgemeine Chemie - 3 Trennverfahren (P750900) 3.2 Gemischtrennungen - Filtrieren, Magnetscheidung Experiment von: Phywe Gedruckt:.0.203 2:53:30 intertess (Version 3.06 B200,
Flüssigkeitsthermometer Bimetallthermometer Gasthermometer Celsius Fahrenheit
 Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Teilchenmodell: * Alle Stoffe bestehen aus Teilchen (Atomen, Molekülen). * Die Teilchen befinden sich in ständiger Bewegung.
 Teilchenmodell Teilchenmodell: * Alle Stoffe bestehen aus Teilchen (Atomen, Molekülen). * Die Teilchen befinden sich in ständiger Bewegung. *Zwischen den Teilchen wirken anziehende bzw. abstoßende Kräfte.
Teilchenmodell Teilchenmodell: * Alle Stoffe bestehen aus Teilchen (Atomen, Molekülen). * Die Teilchen befinden sich in ständiger Bewegung. *Zwischen den Teilchen wirken anziehende bzw. abstoßende Kräfte.
1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE VORÜBERLEGUNGEN
 1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE Chemie beschäftigt sich mit Materie. Die Aggregatzustände (s, l und g) sind Formen der Materie. Materie besteht aus
1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE Chemie beschäftigt sich mit Materie. Die Aggregatzustände (s, l und g) sind Formen der Materie. Materie besteht aus
Mit Tandemkarten in der Sekundarstufe I wiederholen
 38. Mit Tandemkarten in der Sekundarstufe I wiederholen 1 von 12 Mit Tandemkarten in der Sekundarstufe I wiederholen Birte Bathen, Duisburg Niveau: Sek. I Dauer: 1 Unterrichtsstunde Bezug zu den KMK-Bildungsstandards
38. Mit Tandemkarten in der Sekundarstufe I wiederholen 1 von 12 Mit Tandemkarten in der Sekundarstufe I wiederholen Birte Bathen, Duisburg Niveau: Sek. I Dauer: 1 Unterrichtsstunde Bezug zu den KMK-Bildungsstandards
Kondensationswärme. Verdampfungswärme. Resublimationswärme. Sublimationswärme. Erstarrungswärme. Schmelzwärme. Energie (Enthalpie) Energie (Enthalpie)
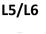 A. Soi 2017 18 81 Energie (Enthalpie) Energie (Enthalpie) Gasförmig Flüssig Schmelzwärme (Schmelzenthalpie) Verdampfungswärme (Schmelzenthalpie) Sublimationswärme (Sublimationsenthalpie) Fest Gasförmig
A. Soi 2017 18 81 Energie (Enthalpie) Energie (Enthalpie) Gasförmig Flüssig Schmelzwärme (Schmelzenthalpie) Verdampfungswärme (Schmelzenthalpie) Sublimationswärme (Sublimationsenthalpie) Fest Gasförmig
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Stoffe und ihre Eigenschaften
 Stoffe und ihre Eigenschaften 1.) Welche Stoffeigenschaften kennen Sie? Zählen Sie auf. Aussehen, Geruch, Geschmack, Verformbarkeit, elektr. LF, Magnetismus, Härte, Verhalten beim Erhitzen, Brennbarkeit;
Stoffe und ihre Eigenschaften 1.) Welche Stoffeigenschaften kennen Sie? Zählen Sie auf. Aussehen, Geruch, Geschmack, Verformbarkeit, elektr. LF, Magnetismus, Härte, Verhalten beim Erhitzen, Brennbarkeit;
Definiere den Begriff Chemischer Vorgang! Definiere den Begriff Physikalischer Vorgang!
 Chemischer Vorgang! Stoffänderung, keine Zustandsänderung, mit Energiebeteiligung Physikalischer Vorgang! Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Erkläre die Begriffe heterogenes
Chemischer Vorgang! Stoffänderung, keine Zustandsänderung, mit Energiebeteiligung Physikalischer Vorgang! Zustandsänderung, keine Stoffänderung (z.b. Lösen, Aggregatzustände,...) Erkläre die Begriffe heterogenes
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Das Salz in unserer Suppe
 Das Salz in unserer Suppe Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung C2.3 Physikalische Trennverfahren und deren Anwendung W1 Ich kann Vorgänge und Phänomene in Natur, Umwelt und Technik
Das Salz in unserer Suppe Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung C2.3 Physikalische Trennverfahren und deren Anwendung W1 Ich kann Vorgänge und Phänomene in Natur, Umwelt und Technik
LMPG1 ÜB1 Phasendiagramme & Dampfdruck Lösungen Seite 1 von 6
 LMPG1 ÜB1 Phasendiagramme & Dampfdruck Lösungen Seite 1 von 6 Aufgabe 1: Phasendiagramm reiner Stoffe. Die Abbildung zeigt das allgemeingültige Phasendiagramm reiner Stoffe. a) Beschriften Sie das Diagramm
LMPG1 ÜB1 Phasendiagramme & Dampfdruck Lösungen Seite 1 von 6 Aufgabe 1: Phasendiagramm reiner Stoffe. Die Abbildung zeigt das allgemeingültige Phasendiagramm reiner Stoffe. a) Beschriften Sie das Diagramm
Aufgabe: Erkläre folgende Tatsache mit Hilfe des Teilchenmodells! An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen.
 An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen. Bei einem Flüssigkeitsthermometer kann die Temperatur an der Höhe des Flüssigkeitsstandes im Röhrchen abgelesen werden. 1827
An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen. Bei einem Flüssigkeitsthermometer kann die Temperatur an der Höhe des Flüssigkeitsstandes im Röhrchen abgelesen werden. 1827
Flüssiggasfeuerzeug BIFIE
 Flüssiggasfeuerzeug Flüssiggasfeuerzeuge sind mit Butan befüllt. Seite 1 1. Ein solches Flüssiggasfeuerzeug wird vor dem Gebrauch gewogen (Bild 1) und gezündet (Bild 2). Bild 1 Bild 2 Wenn man es 20 Sekunden
Flüssiggasfeuerzeug Flüssiggasfeuerzeuge sind mit Butan befüllt. Seite 1 1. Ein solches Flüssiggasfeuerzeug wird vor dem Gebrauch gewogen (Bild 1) und gezündet (Bild 2). Bild 1 Bild 2 Wenn man es 20 Sekunden
B E I S P I E L A R B E I T / Aufgaben. Kultusministerium
 B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
B E I S P I E L A R B E I T / Aufgaben Kultusministerium Name, Vorname: Klasse: Schule: Seite 1 von 6 B E I S P I E L A R B E I T / Aufgaben Aufgabe 1: Stoffe und ihre Eigenschaften a) Die Naturwissenschaft
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen.
 Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Thermodynamik. Wechselwirkung mit anderen Systemen Wärme, Arbeit, Teilchen
 18a Temperatur 1 Thermodynamik Thermodynamik ist eine phänomenologische Wissenschaft Sie beschreibt die Wechselwirkung von Systemen mit ihrer Umgebung Aus der Erfahrung und durch zahllose Beobachtungen
18a Temperatur 1 Thermodynamik Thermodynamik ist eine phänomenologische Wissenschaft Sie beschreibt die Wechselwirkung von Systemen mit ihrer Umgebung Aus der Erfahrung und durch zahllose Beobachtungen
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov #12 am 26.01.2007 Folien im PDF Format unter: http://www.physik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Grundwissen Chemie 8I
 1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
Textverständnis Strukturieren von Fachbegriffen Text Ggf. Demonstrationsbeispiele. Umgang mit Fachsprache Verstehendes Lesen von Fachtexten
 Methode: Aktivierung mit der Methode Partnerpuzzle Fach: Naturwissenschaften Thema des Unterrichtsbeispiels: Stoffgemisch Klassenstufe: 5-6 Kompetenzbereich: Textverarbeitung Ziele Materialien (Raum-)ausstattung
Methode: Aktivierung mit der Methode Partnerpuzzle Fach: Naturwissenschaften Thema des Unterrichtsbeispiels: Stoffgemisch Klassenstufe: 5-6 Kompetenzbereich: Textverarbeitung Ziele Materialien (Raum-)ausstattung
Formelsammlung Abfallwirtschaft Seite 1/6 Wärmekapazität Prof. Dr. Werner Bidlingmaier & Dr.-Ing. Christian Springer
 Formelsammlung Abfallwirtschaft Seite 1/6 1 Energiebedarf zur Erwärmung von Stoffen Der Energiebetrag, der benötigt wird, um 1 kg einer bestimmten Substanz um 1 C zu erwärmen, wird als die (auch: Spezifische
Formelsammlung Abfallwirtschaft Seite 1/6 1 Energiebedarf zur Erwärmung von Stoffen Der Energiebetrag, der benötigt wird, um 1 kg einer bestimmten Substanz um 1 C zu erwärmen, wird als die (auch: Spezifische
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Das Salz in unserer Suppe
 Das Salz in unserer Suppe Aufgabe 1 In der Küche verwendet man oft zwei Arten von Salz. Das eine ist Steinsalz und das andere ist Meersalz. Das Meerwasser im Mittelmeer enthält 3,8 % Salz, im Toten Meer
Das Salz in unserer Suppe Aufgabe 1 In der Küche verwendet man oft zwei Arten von Salz. Das eine ist Steinsalz und das andere ist Meersalz. Das Meerwasser im Mittelmeer enthält 3,8 % Salz, im Toten Meer
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 9. Kl. SG - WSG 1 / 56 ) ( 9. Kl. SG - WSG 2 / 56 ) ( 9. Kl.
 Stoffgemisch ( 9. Kl. SG - WSG 1 / 56 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 9. Kl.
Stoffgemisch ( 9. Kl. SG - WSG 1 / 56 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 9. Kl.
Station 9: Expertenwissen 1.1
 Station 9: Expertenwissen 1.1 Das Wasser aus Kläranlagen muss bestimmten Messwerten entsprechen, um in Flüsse eingeleitet werden zu dürfen. Viele Verunreinigungen sind mit bloßem Auge erkennbar, für andere
Station 9: Expertenwissen 1.1 Das Wasser aus Kläranlagen muss bestimmten Messwerten entsprechen, um in Flüsse eingeleitet werden zu dürfen. Viele Verunreinigungen sind mit bloßem Auge erkennbar, für andere
Grundlagen der Allgemeinen und Anorganischen Chemie. Atome
 Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Grundlagen der Allgemeinen und Anorganischen Chemie Atome Elemente Chemische Reaktionen Energie Verbindungen 361 4. Chemische Reaktionen 4.1. Allgemeine Grundlagen (Wiederholung) 4.2. Energieumsätze chemischer
Kurze Einführung in die Thermodynamik mit Begriffsklärungen
 Kurze Einführung in die Thermodynamik mit Begriffsklärungen Gliederung 1. Begriffsklärungen 2. Energieumwandlungen 3. Molare Volumenarbeit 4. Hauptsätze der Thermodynamik 5. Quellen 1. Begriffsklärungen
Kurze Einführung in die Thermodynamik mit Begriffsklärungen Gliederung 1. Begriffsklärungen 2. Energieumwandlungen 3. Molare Volumenarbeit 4. Hauptsätze der Thermodynamik 5. Quellen 1. Begriffsklärungen
P1: Die Welt der Stoffe
 Schulinternes Curriculum Chemie auf der Grundlage des brandenburgischen Rahmenplanes Jahrgangsstufe 7 ( 2 Stunden / 40 Wochen / 80 Stunden ) P1: Die Welt der Stoffe 1.1. Chemie ist überall 1.1.1. Was ist
Schulinternes Curriculum Chemie auf der Grundlage des brandenburgischen Rahmenplanes Jahrgangsstufe 7 ( 2 Stunden / 40 Wochen / 80 Stunden ) P1: Die Welt der Stoffe 1.1. Chemie ist überall 1.1.1. Was ist
VORANSICHT. Hinweise zu den Materialien
 Hinweise zu den Materialien M 1 Heterogen oder homogen könnt ihr es unterscheiden? Das Arbeitsblatt dient zur aktiven Wiederholung von bereits Gelerntem und behandelt heterogene und homogene Stoffgemische.
Hinweise zu den Materialien M 1 Heterogen oder homogen könnt ihr es unterscheiden? Das Arbeitsblatt dient zur aktiven Wiederholung von bereits Gelerntem und behandelt heterogene und homogene Stoffgemische.
VORANSICHT I/A. Hinweise zu den Materialien
 2 von 18 Hinweise zu den Materialien M 1 Heterogen oder homogen könnt ihr es unterscheiden? Das Arbeitsblatt dient zur aktiven Wiederholung von bereits Gelerntem und behandelt heterogene und homogene Stoffgemische.
2 von 18 Hinweise zu den Materialien M 1 Heterogen oder homogen könnt ihr es unterscheiden? Das Arbeitsblatt dient zur aktiven Wiederholung von bereits Gelerntem und behandelt heterogene und homogene Stoffgemische.
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen.
 Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Chemielaborant 1. Ausbildungsjahr 1,5 Tage Unterricht pro Woche
 BS2 Augsburg FG Chemie Chemielaborant 1. Ausbildungsjahr 1,5 Tage Unterricht pro Woche Allgemeiner Allgemeiner Unterricht Unterricht 1 Stunde Deutsch 1 Stunde Religion 1 Stunde Religion 1 Stunde Sozialkunde
BS2 Augsburg FG Chemie Chemielaborant 1. Ausbildungsjahr 1,5 Tage Unterricht pro Woche Allgemeiner Allgemeiner Unterricht Unterricht 1 Stunde Deutsch 1 Stunde Religion 1 Stunde Religion 1 Stunde Sozialkunde
3.4 Änderung des Aggregatzustandes
 34 Änderung des Aggregatzustandes Man unterscheidet 3 Aggregatzustände: Fest Flüssig Gasförmig Temperatur: niedrig mittel hoch Molekülbindung: Gitter lose Bindung keine Bindung schmelzen sieden erstarren
34 Änderung des Aggregatzustandes Man unterscheidet 3 Aggregatzustände: Fest Flüssig Gasförmig Temperatur: niedrig mittel hoch Molekülbindung: Gitter lose Bindung keine Bindung schmelzen sieden erstarren
Partnerpuzzle zu Trennverfahren
 Partnerpuzzle zu Trennverfahren 1. Lies den Text durch. 2. Lies den Text ein zweites Mal durch und unterstreiche dabei wichtige Begriffe und die dazugehörige Erklärung. 3. Beantwortet innerhalb eurer Zweiergruppe
Partnerpuzzle zu Trennverfahren 1. Lies den Text durch. 2. Lies den Text ein zweites Mal durch und unterstreiche dabei wichtige Begriffe und die dazugehörige Erklärung. 3. Beantwortet innerhalb eurer Zweiergruppe
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Überblick Inhalt. Grundlagen Chromatographie. Gaschromatographie. Aufbau. Probenaufgabesysteme. Einsatzgebiete der Gaschromatographie
 Überblick Inhalt Grundlagen Chromatographie Gaschromatographie Aufbau Probenaufgabesysteme Einsatzgebiete der Gaschromatographie Beispielchromatogramm Seite 2 Warum Chromatographie? Zu untersuchende Proben
Überblick Inhalt Grundlagen Chromatographie Gaschromatographie Aufbau Probenaufgabesysteme Einsatzgebiete der Gaschromatographie Beispielchromatogramm Seite 2 Warum Chromatographie? Zu untersuchende Proben
Analytische Chemie (für Biol. / Pharm. Wiss.)
 Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Analytische Chemie (für Biol. / Pharm. Wiss.) Teil: Trenntechniken (Chromatographie, Elektrophorese) Dr. Martin Pabst Laboratory of Organic Chemistry HCI D323 martin.pabst@org.chem.ethz.ch http://www.analytik.ethz.ch/
Endersch, Jonas 09./
 Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
Endersch, Jonas 09./10.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Gruppe 3, Platz 53 Versuchsprotokoll Versuch 1.2: Destillation 1 Versuch 1.3: Destillation 2 Einleitung und Theorie: In diesen Versuchen
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
