Patientinneninformation und Einwilligungserklärung
|
|
|
- Franz Sebastian Schäfer
- vor 7 Jahren
- Abrufe
Transkript
1 Patientinneninformation und Einwilligungserklärung Titel der Studie Blasenfunktion vor und nach Operation bei tief-infiltrierender Endometriose Sehr geehrte, liebe Patientin, Wir möchten Ihnen die wichtigsten Informationen zur laufenden Studie bezüglich Endometriose und Blasenfunktion mit diesem Informationsblatt erklären. Endometriose ist eine häufige, gutartige, oft schmerzhafte chronische Erkrankung von Frauen, bei der Gebärmutterschleimhaut außerhalb der Gebärmutterhöhle vorkommt. 1. Auswahl der Personen, die an der Studie teilnehmen können Teilnehmen dürfen Frauen mit Verdacht auf tief-infiltrierende Endometriose, die eine Operation wegen endometriosebedingten Symptomen (z.b. Schmerzen, Infertilität) erfordern. Nicht teilnehmen hingegen dürfen Frauen, die früher eine Darmentfernung bekommen haben oder eine Strahlentherapie wegen einem bösartigen Geschwulst. Auch nicht teilnehmen dürfen Personen, die an psychiatrischen oder neurologischen Krankheiten leiden, Neuroleptika bekommen, einen grösseren Scheidenvorfall haben oder unter wiederholten Harnwegsinfektionen leiden. 2. Ziel der Studie Ziel des Projektes ist den möglichen Zusammenhang zwischen Blasenfunktion und Endometriose genauer zu verstehen, insbesondere ob und wie Endometriose die Blasenfunktion bereits vor einer Operation für Endometriose beeinflusst. 3. Allgemeine Informationen zur Studie Blasenfunktionsstörungen werden bei bis zu 30% der Patientinnen nach einer Operation für tiefinfiltrierende Endometriose beobachtet. Es stellt sich die Frage ob und wie Endometriose die Nervenversorgung und somit die Blasenfunktion bereits vor einer Operation beeinflussen kann; Deshalb möchten wir vor und nach einer Operation die Häufigkeit einer gestörter Blasensfunktion erfassen und die Nervenfasern am Gewebe untersuchen. Drei Konsultationen sind vorgesehen. Vor, 6 und 12 Wochen nach der Operation. Bei den zwei ersten Konsultationen wird eine klinische und urodynamische Untersuchung durchgeführt und Sie werden einen einfachen Fragebogen zur Blasenfunktion ausfüllen. Bei der letzten Konsultation wird eine Restharnmessung durchgeführt. Wir möchten, dass 50 Frauen teilnehmen und schätzen die gesamte Dauer der Studie auf zwei Jahre. Die Ergebnisse der Studien werden erwartungsgemäss ca. zwei Jahre nach Studienbeginn veröffentlicht werden. Wir führen die Studie nach den Gesetzen der Schweiz durch. Ausserdem beachten wir alle international anerkannten Richtlinien. Die zuständige Kantonale Ethikkommission hat die Studie geprüft und bewilligt. 4. Ablauf für die Teilnehmenden Die Studiendauer für Sie beträgt 12 Wochen. Die Konsultationen mit den Untersuchungen sind in der Tabelle aufgelistet. 1
2 Visiten Zeit (Woche) Vor der 6 12 Operation Ort Frauenklinik Frauenklinik Frauenklinik Klinische Untersuchung X x eventuell Urodynamische X x Untersuchung Restharn-Messung X x x IPSS Fragebogen X x x Je nach klinischem Verlauf werden eventuell noch zusätzliche nicht studienbedingte Konsultationen erforderlich sein. Fragebogen: Fragebogen bestehend aus sieben Fragen zur Blasenfunktion und einer Frage zur Lebensqualität. Dadurch wird eine gestörte Blasenfunktion erfasst. Ausserdem erhalten Sie einen Fragenbogen zur Erfassung der empfundenen Stärke Ihrer Schmerzen. Urodynamische Untersuchung: Sie dauert ca. 45 Minuten und ist eine Untersuchungsmethode, bei der mit Hilfe von Drucksonden und Elektroden die Funktionsweise der Harnblase untersucht wird (Blasendruckmessung). Bei der Untersuchung wird ein spezieller Katheter in die Blase eingeführt. Nach initialer Entleerung der Blase wird diese anschließend durch den Katheter mit warmer Infusionslösung gefüllt und gleichzeitig der Druck innerhalb der Blase gemessen. Ein weiterer Drucksensor, der in den After eingeführt wird, misst den Druck, der von außen auf die Blase einwirkt, z.b. wenn die Patientin presst oder hustet. Die Untersuchung findet auf einem speziellen Toilettenstuhl statt. Die gesamten Messwerte werden kontinuierlich dokumentiert und aufgezeichnet. Die so erhaltenen Druck- und Flusskurven werden über ein Computersystem ausgewertet und vom Arzt interpretiert. Keine sonstigen Untersuchungen wie z.b. Blutentnahmen sind im Rahmen der Studie vorgesehen. 5. Rechte der Teilnehmenden Sie nehmen nur dann an dieser Studie teil, wenn Sie es wollen. Niemand darf Sie dazu in irgendeiner Weise drängen oder dazu überreden. Ihre laufende medizinische Behandlung geht genau gleich weiter, wenn Sie nicht mitmachen. Sie müssen nicht begründen, warum Sie nicht mitmachen wollen. Wenn Sie sich entscheiden mitzumachen, können Sie diesen Entscheid jederzeit zurücknehmen. Sie müssen ebenfalls nicht begründen, wenn Sie aus der Studie aussteigen wollen. Sie dürfen jederzeit alle Fragen zur Studie stellen. Wenden Sie sich dazu bitte an die Person, die am Ende dieser Studieninformation genannt ist. 6. Pflichten der Teilnehmenden Wenn Sie bei der Studie mitmachen, müssen Sie bestimmte Regeln beachten. Dies ist notwendig für Ihre Sicherheit und Gesundheit. Wir werden Sie dabei so gut wir können unterstützen. Als Studienteilnehmende sind Sie verpflichtet, den medizinischen Anweisungen Ihres Studienarztes zu folgen und sich an den Studienplan zu halten. Ihren Studienarzt über den Verlauf der Erkrankung zu informieren und neue Symptome, neue Beschwerden und Änderungen im Befinden zu melden. Ihren Studienarzt über die gleichzeitige Behandlung und Therapien bei einem anderen Arzt und über die Einnahme von Medikamenten zu informieren. 7. Nutzen für die Teilnehmenden Klinische Studien gewährleisten eine qualitativ hoch stehende Durchführung und Bewertung der Behandlung. Alle Patienten, die an Studien teilnehmen, werden zusätzlich zur Routine intensiv untersucht, besonders sorgfältig überwacht und werden auch nach Beendigung der Studie weiter betreut. 2
3 Ausserdem können die Resultate wichtig sein für andere, die nach Ihnen dieselbe Krankheit haben. Es kann aber auch durchaus sein, dass Sie selber keinen Nutzen aus dieser Studie haben werden. 8. Risiken und Belastungen für die Teilnehmenden Es besteht kein Risiko für Sie durch Ihre Teilnahme an der Studie. Gewisse kleine Unannehmlichkeiten bei den urodynamischen Untersuchungen sind eventuell zu erwarten. Manchmal ist die Blase nach der Untersuchung für 1-2 Tage etwas irritiert. Wenn Sie bei dieser Studie mitmachen, so sind die studienrelevanten Untersuchungen sowohl für Sie als auch für die Krankenkasse kostenlos. 9. Andere Behandlungsmöglichkeiten Ihre Behandlung wird unabhängig der Studie zusammen mit Ihrem betreuenden Arzt ausgewählt. Diese ändert sich nicht durch Ihre Teilnahme an der Studie. 10. Ergebnisse aus der Studie Der Studienarzt wird Sie während der Studie über alle neuen Erkenntnisse informieren, die den Nutzen der Studie oder Ihre Sicherheit und somit Ihr Einwilligung zur Teilnahme an der Studie beeinflussen können. Sie werden die Information mündlich und schriftlich erhalten. 11. Vertraulichkeit der Daten Wir werden für diese Studie Ihre persönlichen und medizinischen Daten erfassen. Diese Daten werden wir verschlüsseln. Verschlüsselung bedeutet, dass alle Angaben, die Sie identifizieren könnten (z.b. Name, Geburtsdatum usw.), durch einen Code (Schlüssel) ersetzt sind, sodass für Personen, die den Code nicht kennen, keine Rückschlüsse auf Ihre Person mehr möglich sind. Innerhalb der Institution können die Daten durch berechtigte und klar bezeichnete Personen auch ohne Verschlüsselung eingesehen werden. Der Schlüssel bleibt immer in der Institution. Es kann sein, dass die Studie während des Ablaufs überprüft wird. Dies können die Behörden tun, die sie vorab kontrolliert und bewilligt haben. Sie alle sorgen dafür, dass die Regeln eingehalten werden und Ihre Sicherheit nicht gefährdet wird. Dazu muss der Leiter der Studie eventuell Ihre persönlichen und medizinischen Daten für solche Kontrollen offenlegen. Ebenso kann es sein, dass im Fall eines Schadens ein Vertreter der Versicherung Ihre Daten ansehen muss. Das darf dann aber nur die Daten betreffen, die unbedingt gebraucht werden, um den Schadensfall zu erledigen. Alle Personen, die mit der Studie in irgendeiner Weise zu tun haben, müssen absolute Vertraulichkeit wahren. Wir werden Ihren Namen nirgends, in keinem Bericht, keiner Publikation, nicht gedruckt und nicht im Internet, veröffentlichen. Es ist möglich, dass Ihre gesundheitsbezogene Daten und biologisches Material zu einem späteren Zeitpunkt an eine andere Biobank in der Schweiz zu Analysezwecken übersandt werden. Diese muss die gleichen Standards einhalten wie die vorliegende Biobank. Verantwortlich für die Einhaltung der nationalen und internationalen Richtlinien zum Datenschutz ist der Sponsor in der Schweiz. 12. Weitere Verwendung von Material und Daten Sie können jederzeit aus der Studie aussteigen, wenn Sie dies wünschen. Die medizinischen Daten, die wir bis dahin erhoben haben, und das biologische Material (Gewebe) von Ihnen werden wir trotzdem auswerten, weil sonst die ganze Studie ihren Wert verlieren würde. Wenn Sie Ihre Einwilligung widerrufen, werden Ihre Daten, nach Abschluss der Datenauswertung anonymisiert. 3
4 13. Entschädigung für Teilnehmende Wenn Sie bei dieser Studie mitmachen, bekommen Sie dafür keine Entschädigung. 14. Deckung von Schäden Falls Sie durch die Studie einen gesundheitlichen Schaden erleiden, haftet die Institution, die für die Durchführung der Studie verantwortlich ist. Diese Haftung gilt aber nur dann, wenn Sie nachweisen können, dass der Schaden auf Forschungshandlungen (z.b. Untersuchungen) zurückzuführen ist. Ausserdem gilt die Haftpflicht nur, wenn sonstige Standardintervention in neuer Weise angewendet und getestet wird, wenn die Anwendung nicht als medizinischer Standard gilt, oder wenn ein vergleichbarer Schaden nicht auch bei einer üblichen Therapie hätte eintreten können. 15. Finanzierung der Studie Die Studie wird vollständig von der finanziert. 16. Kontaktperson(en) Bei allen Unklarheiten, Befürchtungen oder Notfällen, die während der Studie oder danach auftreten, können Sie sich jederzeit an eine dieser Kontaktpersonen wenden. Dr. med. K. Nirgianakis, Oberarzt Prof. M. Mueller, Chefarzt Prof. A. Kuhn, Leiterin Urogynäkologie Frau J. Wanner, Study Nurse/ Studienkoordinatorin Tel: Glossar (erklärungsbedürftige Begriffe) Nicht zutreffend. 4
5 Schriftliche Einwilligungserklärung zur Teilnahme an einer Studie Bitte lesen Sie dieses Formular sorgfältig durch. Bitte fragen Sie, wenn Sie etwas nicht verstehen oder wissen möchten. Nummer der Studie: 131/15 Titel der Studie: verantwortliche Institution (Sponsor) Ort der Durchführung: Leiter der Studie Teilnehmerin Name und Vorname in Druckbuchstaben: Geburtsdatum: Blasenfunktion vor und nach Operation für tiefinfiltrierende Endometriose. Tel: Dr. med. Konstantinos Nirgianakis Ich wurde vom unterzeichnenden Arzt mündlich und schriftlich über den Zweck, den Ablauf der Studie, über mögliche Vor- und Nachteile sowie über eventuelle Risiken informiert. Meine Fragen im Zusammenhang mit der Teilnahme an dieser Studie sind mir zufriedenstellend beantwortet worden. Ich kann die schriftliche Studieninformation behalten und erhalte eine Kopie meiner schriftlichen Einwilligungserklärung. Ich akzeptiere den Inhalt der zur oben genannten Studie abgegebenen schriftlichen Studieninformation. Ich nehme an dieser Studie freiwillig teil. Ich kann jederzeit und ohne Angabe von Gründen meine Zustimmung zur Teilnahme widerrufen, ohne dass ich deswegen Nachteile bei der weiteren medizinischen Betreuung erleide. Ich hatte genügend Zeit, meine Entscheidung zu treffen. Ich weiss, dass meine persönlichen Daten und Körpermaterialien nur in verschlüsselter Form zu Forschungszwecken weitergegeben werden können. Ich bin einverstanden, dass die zuständigen Fachleute des Auftraggebers der Studie, der Behörden und der Kantonalen Ethikkommission zu Prüf- und Kontrollzwecken in meine Originaldaten Einsicht nehmen dürfen, jedoch unter strikter Einhaltung der Vertraulichkeit. Ich bin mir bewusst, dass die in der Teilnehmerinformation genannten Pflichten während der Studie einzuhalten sind. Im Interesse meiner Gesundheit kann mich der Leiter / die Leiterin jederzeit von der Studie ausschliessen. Ort, Datum Unterschrift der Studienteilnehmerin Bestätigung des Studienarztes: Hiermit bestätige ich, dass ich dieser Teilnehmerin Wesen, Bedeutung und Tragweite der Studie erläutert habe. Ich versichere, alle im Zusammenhang mit dieser Studie stehenden Verpflichtungen gemäss dem geltenden Recht zu erfüllen. Sollte ich zu irgendeinem Zeitpunkt während der Durchführung der Studie von Aspekten erfahren, welche die Bereitschaft der Teilnehmerin zur Teilnahme an der Studie beeinflussen könnten, werde ich sie umgehend darüber informieren. Ort, Datum Unterschrift der Studienärztin/des Studienarztes 5
Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen
 Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen Sehr geehrte Patientin, sehr geehrter Patient Wir laden Sie ein, an der
Information und Einverständniserklärung für Patienten und Patientinnen, die an der Schweizerischen HIV-Kohortenstudie teilnehmen Sehr geehrte Patientin, sehr geehrter Patient Wir laden Sie ein, an der
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Telehealthcare vs. standard care in COPD an international randomised controlled trial
 Telehealthcare vs. standard care in COPD an international randomised controlled trial Sehr geehrte Dame, sehr geehrter Herr Wir sind Mitarbeitende der des Kantonsspitals St. Gallen. Mein Name ist Dr. med.
Telehealthcare vs. standard care in COPD an international randomised controlled trial Sehr geehrte Dame, sehr geehrter Herr Wir sind Mitarbeitende der des Kantonsspitals St. Gallen. Mein Name ist Dr. med.
für die Erstellung einer schriftlichen Studieninformation für schwangere Studienteilnehmerinnen oder schwangere Partnerinnen von Studienteilnehmern
 Template von swissethics für die Erstellung einer schriftlichen Studieninformation für schwangere Studienteilnehmerinnen oder schwangere Partnerinnen von Studienteilnehmern Zur folgenden Vorlage: schwarz
Template von swissethics für die Erstellung einer schriftlichen Studieninformation für schwangere Studienteilnehmerinnen oder schwangere Partnerinnen von Studienteilnehmern Zur folgenden Vorlage: schwarz
PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie
 PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie... (Vollständiger Titel der klinischen Studie) Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer! Wir laden
PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie... (Vollständiger Titel der klinischen Studie) Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer! Wir laden
Weiterverwendung von Patientendaten und biologischen Proben für die Forschung
 Forschungskommission KSW Weiterverwendung von Patientendaten und biologischen Proben für die Forschung Sehr geehrte Patientin Sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat in den
Forschungskommission KSW Weiterverwendung von Patientendaten und biologischen Proben für die Forschung Sehr geehrte Patientin Sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat in den
Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie
 Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie APRES: Angemessenheit der Antibiotika -Verschreibungen in der hausärztlichen Praxis in Europa im Hinblick
Patienten-/Patientinneninformation und Einwilligungserklärung zur Teilnahme an der Beobachtungsstudie APRES: Angemessenheit der Antibiotika -Verschreibungen in der hausärztlichen Praxis in Europa im Hinblick
Information für Eltern von Studienteilnehmenden Schweizer Kohorte von Personen mit Varianten der Geschlechtsentwicklung (Schweizer DSD Kohorte)
 Information für Eltern von Studienteilnehmenden Schweizer Kohorte von Personen mit Varianten der Geschlechtsentwicklung (Schweizer DSD Kohorte) Dieses Projekt wird durchgeführt durch die Kinderklinik am
Information für Eltern von Studienteilnehmenden Schweizer Kohorte von Personen mit Varianten der Geschlechtsentwicklung (Schweizer DSD Kohorte) Dieses Projekt wird durchgeführt durch die Kinderklinik am
Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD)
 Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD) In diesem Text wird der Einfachheit halber nur die männliche Form verwendet. Die weibliche Form ist selbstverständlich immer miteingeschlossen.
Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD) In diesem Text wird der Einfachheit halber nur die männliche Form verwendet. Die weibliche Form ist selbstverständlich immer miteingeschlossen.
Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD)
 Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD) In diesem Text wird der Einfachheit halber nur die männliche Form verwendet. Die weibliche Form ist selbstverständlich immer miteingeschlossen.
Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD) In diesem Text wird der Einfachheit halber nur die männliche Form verwendet. Die weibliche Form ist selbstverständlich immer miteingeschlossen.
PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie
 PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie Der Einfluss von kontrollierter Bewegung und balneologischer Therapie bei PatientInnen mit chronischen unspezifischen
PatientInneninformation 1 und Einwilligungserklärung zur Teilnahme an der klinischen Studie Der Einfluss von kontrollierter Bewegung und balneologischer Therapie bei PatientInnen mit chronischen unspezifischen
Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD)
 Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD) In diesem Text wird der Einfachheit halber nur die männliche Form verwendet. Die weibliche Form ist selbstverständlich immer miteingeschlossen.
Schweizer Register für neuromuskuläre Erkrankungen (Swiss-Reg-NMD) In diesem Text wird der Einfachheit halber nur die männliche Form verwendet. Die weibliche Form ist selbstverständlich immer miteingeschlossen.
Weiterverwendung von Patientendaten
 FORSCHUNGSKOMMISSION KSW KANTONSSPITAL WINTERTHUR Brauerstrasse 15 Postfach 834 8401 Winterthur Tel. 052 266 21 21 info@ksw.ch www.ksw.ch Weiterverwendung von Patientendaten Kontakt Zentrale Studienkoordination
FORSCHUNGSKOMMISSION KSW KANTONSSPITAL WINTERTHUR Brauerstrasse 15 Postfach 834 8401 Winterthur Tel. 052 266 21 21 info@ksw.ch www.ksw.ch Weiterverwendung von Patientendaten Kontakt Zentrale Studienkoordination
Sehr geehrte Studienteilnehmerin Im Folgenden erhalten Sie wichtige Informationen zur Studie. Über eine Teilnahme würden wir uns sehr freuen.
 Studieninformation Studie: Postpartale Depression und der Einfluss psychosozialer Risikofaktoren Dieses Projekt ist organisiert durch: Prof. Dr. rer. nat. Ulrike Ehlert, Universität Zürich,. Sehr geehrte
Studieninformation Studie: Postpartale Depression und der Einfluss psychosozialer Risikofaktoren Dieses Projekt ist organisiert durch: Prof. Dr. rer. nat. Ulrike Ehlert, Universität Zürich,. Sehr geehrte
Information und Einwilligung für Eltern / Erziehungsberechtige zur Durchführung genetischer Analysen bei Kindern und Jugendlichen
 Information und Einwilligung für Eltern / Erziehungsberechtige zur Durchführung genetischer Analysen bei Kindern und Jugendlichen Studienstelle: Klinik für Nephrologie Universitätsklinikum Düsseldorf Moorenstr.
Information und Einwilligung für Eltern / Erziehungsberechtige zur Durchführung genetischer Analysen bei Kindern und Jugendlichen Studienstelle: Klinik für Nephrologie Universitätsklinikum Düsseldorf Moorenstr.
Erläuterungen zur Einwilligungserklärung
 Erläuterungen zur Einwilligungserklärung Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die Ärzte und Wissenschaftler der
Erläuterungen zur Einwilligungserklärung Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die Ärzte und Wissenschaftler der
Patienteninformation:
 Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
Patienteninformation: Synthetisches Netz versus kein Netz bei Nabelbrüchen: eine prospektive, doppelblinde, randomisierte, kontrollierte Studie Synthetic mesh versus no mesh for umbilical hernias: a prospective
PATIENTENINFORMATION. Caregiver Burden bei betreuenden Angehörigen schwer betroffener Parkinsonpatienten
 Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Version 1.2 Neurologische Klinik mit Klinischer Neurophysiologie Kommissarischer Direktor: Prof. Dr. med. M. Stangel PD Dr. med. F. Wegner Telefon: (0511) 532-3110 Fax: (0511) 532-3115 Carl-Neuberg-Straße
Klinik für Geburtshilfe und Schwangerschaftsmedizin. Vibwife Studie
 Vibwife Studie Die Vibwife Studie ist eine Sicherheits-Studie welche die Sicherheit, Praktikabilität und Akzeptanz von Vibwife One prüft, ein Medizinprodukt, welches die Mobilisierung von Frauen unter
Vibwife Studie Die Vibwife Studie ist eine Sicherheits-Studie welche die Sicherheit, Praktikabilität und Akzeptanz von Vibwife One prüft, ein Medizinprodukt, welches die Mobilisierung von Frauen unter
Erläuterungen zur Einwilligungserklärung mit zusätzlicher Blutentnahme
 Erläuterungen zur Einwilligungserklärung mit zusätzlicher Blutentnahme Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die
Erläuterungen zur Einwilligungserklärung mit zusätzlicher Blutentnahme Leisten Sie einen Beitrag zur medizinischen Forschung Liebe Patientin, Lieber Patient Dank der medizinischen Forschung leisten die
Patientinnen-/ Patienten-Information für die Studie Neurofeedback-Behandlung bei akustischen Halluzinationen
 Universitäre Psychiatrische Dienste Bern (UPD) Universitätsklinik für Psychiatrie und Psychotherapie Prof. Dr. Thomas Koenig Bolligenstrasse 111, CH-3000 Bern 60 Tel. 031 930 91 69, Fax 031 930 99 58 email:
Universitäre Psychiatrische Dienste Bern (UPD) Universitätsklinik für Psychiatrie und Psychotherapie Prof. Dr. Thomas Koenig Bolligenstrasse 111, CH-3000 Bern 60 Tel. 031 930 91 69, Fax 031 930 99 58 email:
PatientInneninformation und Einwilligungserklärung zur Teilnahme an der Pilotstudie
 PatientInneninformation und Einwilligungserklärung zur Teilnahme an der Pilotstudie Effekt einer Reduktion von tierischem Eiweiß auf den Verlauf einer bestehenden Krebserkrankung Sehr geehrte Teilnehmerin,
PatientInneninformation und Einwilligungserklärung zur Teilnahme an der Pilotstudie Effekt einer Reduktion von tierischem Eiweiß auf den Verlauf einer bestehenden Krebserkrankung Sehr geehrte Teilnehmerin,
Information für Eltern
 Kinder- und Jugendpsychiatrischer Dienst des Kantons Zürich Zentrum für Kinder- und Jugendpsychiatrie Universität Zürich Ärztliche Direktorin Prof. Dr. med. Dipl.-Psych. Susanne Walitza ZKJP Poliklinik
Kinder- und Jugendpsychiatrischer Dienst des Kantons Zürich Zentrum für Kinder- und Jugendpsychiatrie Universität Zürich Ärztliche Direktorin Prof. Dr. med. Dipl.-Psych. Susanne Walitza ZKJP Poliklinik
Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen
 Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Prüfstelle: Schriftliche Einwilligung und datenschutzrechtliche Erklärung zur Teilnahme an der Studie mit dem Namen Simultaneous Study of Docetaxel Based Anthracycline Free Adjuvant Treatment Evaluation,
Mit Ihnen einen Schritt weiter in der Forschung
 Mit Ihnen einen Schritt weiter in der Forschung Informationen zur Verwendung von Patientendaten und -proben Sehr geehrte Patientin, sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat
Mit Ihnen einen Schritt weiter in der Forschung Informationen zur Verwendung von Patientendaten und -proben Sehr geehrte Patientin, sehr geehrter Patient Die Erkennung und Behandlung von Krankheiten hat
Diese Broschüre fasst die wichtigsten Informationen zusammen, damit Sie einen Entscheid treffen können.
 Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Aufklärung über die Weiterverwendung/Nutzung von biologischem Material und/oder gesundheitsbezogen Daten für die biomedizinische Forschung. (Version V-2.0 vom 16.07.2014, Biobanken) Sehr geehrte Patientin,
Template von swissethics
 Template von swissethics für die Erstellung einer schriftlichen Studieninformation für Projekte unter Einbezug von Personen gemäss HFG/HFV 2.Kapitel (nicht: KlinV oder HFV 3.Kapitel Weiterverwendung ).
Template von swissethics für die Erstellung einer schriftlichen Studieninformation für Projekte unter Einbezug von Personen gemäss HFG/HFV 2.Kapitel (nicht: KlinV oder HFV 3.Kapitel Weiterverwendung ).
Beobachtungsstudie für Patienten mit Vorhofflimmern in der Schweiz [Swiss Atrial Fibrillation Cohort Study]
![Beobachtungsstudie für Patienten mit Vorhofflimmern in der Schweiz [Swiss Atrial Fibrillation Cohort Study] Beobachtungsstudie für Patienten mit Vorhofflimmern in der Schweiz [Swiss Atrial Fibrillation Cohort Study]](/thumbs/59/42767108.jpg) Patienteninformation Beobachtungsstudie für Patienten mit Vorhofflimmern in der Schweiz [Swiss Atrial Fibrillation Cohort Study] Kurzfassung der Patienteninformation Beobachtungsstudie für Patienten mit
Patienteninformation Beobachtungsstudie für Patienten mit Vorhofflimmern in der Schweiz [Swiss Atrial Fibrillation Cohort Study] Kurzfassung der Patienteninformation Beobachtungsstudie für Patienten mit
Probandeninformation zur Studie
 Zentrum für Chronobiologie Universitäre Psychiatrische Kliniken Basel www.chronobiology.ch Probandeninformation zur Studie Jugendliche benutzen Multimedia-Bildschirme, welche den Schlaf tief in die Nacht
Zentrum für Chronobiologie Universitäre Psychiatrische Kliniken Basel www.chronobiology.ch Probandeninformation zur Studie Jugendliche benutzen Multimedia-Bildschirme, welche den Schlaf tief in die Nacht
Biologicaregister für entzündliche rheumatische Erkrankungen e.v. BioReg. ZVR-Zahl Zahl p.a. Schloßhoferstrasse 4/4/12, 1210 Wien
 Biologicaregister für entzündliche rheumatische Erkrankungen e.v. BioReg ZVR-Zahl Zahl 295050213 p.a. Schloßhoferstrasse 4/4/12, 1210 Wien Patientenaufklärung und Patientendatenschutzrechtliche Zustimmungserklärung
Biologicaregister für entzündliche rheumatische Erkrankungen e.v. BioReg ZVR-Zahl Zahl 295050213 p.a. Schloßhoferstrasse 4/4/12, 1210 Wien Patientenaufklärung und Patientendatenschutzrechtliche Zustimmungserklärung
PatientInneninformation zum Projekt
 PatientInneninformation zum Projekt Erstellung eines gesamtösterreichischen Registers zur Erfassung der Familiären Hypercholesterinämie Pilotprojekt Wien, Graz und Innsbruck 1 von5 Lieber Patient, liebe
PatientInneninformation zum Projekt Erstellung eines gesamtösterreichischen Registers zur Erfassung der Familiären Hypercholesterinämie Pilotprojekt Wien, Graz und Innsbruck 1 von5 Lieber Patient, liebe
Patienteninformation zur klinischen Studie:
 UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
UniversitätsKlinikum Heidelberg Universitätsklinikum Heidelberg INF 400 69120 Heidelberg Radiologische Klinik Abteilung RadioOnkologie und Strahlentherapie -Czernyklinik- Patienteninformation zur klinischen
PATIENTENINFORMATION. Nationales Klinisches Amyloidose-Register
 UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
Einverständniserklärung:
 Zum Verbleib beim Patienten Einverständniserklärung: Name, Vorname...geb. am... wohnhaft in... Ich wurde ausreichend in mündlicher und schriftlicher Form über die klinische Studie Phase II Studie zur Therapie
Zum Verbleib beim Patienten Einverständniserklärung: Name, Vorname...geb. am... wohnhaft in... Ich wurde ausreichend in mündlicher und schriftlicher Form über die klinische Studie Phase II Studie zur Therapie
Patienten-Information und Einwilligung zur Durchführung einer klinischen Untersuchung mit volljährigen einwilligungsfähigen Patienten 1
 Patienten-Information und Einwilligung zur Durchführung einer klinischen Untersuchung mit volljährigen einwilligungsfähigen Patienten 1 Prüfstelle: Prüfarzt: Petrus-Krankenhaus Wuppertal Prof. Dr. med.
Patienten-Information und Einwilligung zur Durchführung einer klinischen Untersuchung mit volljährigen einwilligungsfähigen Patienten 1 Prüfstelle: Prüfarzt: Petrus-Krankenhaus Wuppertal Prof. Dr. med.
Informationsschrift. Momentum Projekt Heidelberg Aktiver Umgang mit einer Krebserkrankung
 Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Studieninformation SCHOCO-Studie für Patienten / Patientinnen / Teilnehmer und Teilnehmerinnen Kontrollgruppe
 Verantwortlicher Prüfarzt Prof. Dr. med. Jürg H. Beer Studieninformation SCHOCO-Studie für Patienten / Patientinnen / Teilnehmer und Teilnehmerinnen Kontrollgruppe Sponsor und Hauptprüfer: Prof. Dr. med.
Verantwortlicher Prüfarzt Prof. Dr. med. Jürg H. Beer Studieninformation SCHOCO-Studie für Patienten / Patientinnen / Teilnehmer und Teilnehmerinnen Kontrollgruppe Sponsor und Hauptprüfer: Prof. Dr. med.
Patienteninformation Teil 2 Untersuchung der Erbsubstanz (genetische und epigenetische Untersuchung) der Blutproben für das
 Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
Technische Universität München Leiter des Forschungsvorhaben Univ.-Prof. Dr. Wolfgang Dott Direktor des Instituts für Hygiene und Umweltmedizin Pauwelsstr. 30 D 52074 Aachen Telefon (+49) 0241 80 88 385
Besondere Versorgung Teilnahmeerklärung. Teilnahmeerklärung. Augenärztliche Vorsorgeuntersuchung von Kindern AB71IV DA002
 Besondere Versorgung Teilnahmeerklärung AB71IV057 121712DA002 Bitte senden Sie die Teilnahmeerklärung an folgende Adresse: DAK-Gesundheit, Fachzentrum Ambulante Abrechnungen, Balinger Str. 80, 72336 Balingen.
Besondere Versorgung Teilnahmeerklärung AB71IV057 121712DA002 Bitte senden Sie die Teilnahmeerklärung an folgende Adresse: DAK-Gesundheit, Fachzentrum Ambulante Abrechnungen, Balinger Str. 80, 72336 Balingen.
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie, Robert-Koch-Str. 40, D-37075 Göttingen Institut für Neuropathologie Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472
Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie, Robert-Koch-Str. 40, D-37075 Göttingen Institut für Neuropathologie Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472
Versicherteninformation. Versicherteninformation. Besondere Versorgung (DAK-Spezialisten-Netzwerk) BC72IV028 / DA003
 Besondere Versorgung (DAK-Spezialisten-Netzwerk) Anlage 8 zum Diabetes-Vertrag mit der Kassenärztlichen Vereinigung Berlin Vertrags-Nr.: BC72IV028 / 171722DA003 Versicherteninformation Versicherteninformation
Besondere Versorgung (DAK-Spezialisten-Netzwerk) Anlage 8 zum Diabetes-Vertrag mit der Kassenärztlichen Vereinigung Berlin Vertrags-Nr.: BC72IV028 / 171722DA003 Versicherteninformation Versicherteninformation
PTT2.0 INFORMATIONSBROSCHÜRE FÜR KINDER (6-12 JAHRE)
 UniversitätsKlinikum Heidelberg Universitätsklinik für Kinder- und Jugendmedizin Abt. III Im Neuenheimer Feld 430 69120 Heidelberg PTT2.0 INFORMATIONSBROSCHÜRE FÜR KINDER (6-12 JAHRE) - Personalisierte
UniversitätsKlinikum Heidelberg Universitätsklinik für Kinder- und Jugendmedizin Abt. III Im Neuenheimer Feld 430 69120 Heidelberg PTT2.0 INFORMATIONSBROSCHÜRE FÜR KINDER (6-12 JAHRE) - Personalisierte
DR. MARGARETE FISCHER-BOSCH-INSTITUT FÜR KLINISCHE PHARMAKOLOGIE. Informationsblatt
 Informationsblatt für Interessentinnen und Interessenten an Klinischen Studien zum Aufbau eines Probandenregisters am Dr. Margarete Fischer-Bosch-Institut für Klinische Pharmakologie Sehr geehrte Interessentinnen
Informationsblatt für Interessentinnen und Interessenten an Klinischen Studien zum Aufbau eines Probandenregisters am Dr. Margarete Fischer-Bosch-Institut für Klinische Pharmakologie Sehr geehrte Interessentinnen
Information Dimensionen der Bedeutsamkeit / Spiritualität bei Menschen mit Down-Syndrom
 ( Die folgenden 3 Seiten bitte entweder per Post oder per Email zusenden!) Sehr geehrte Damen und Herren, im Rahmen eines Promotionsvorhabens an der Universität Witten/Herdecke möchten wir Menschen mit
( Die folgenden 3 Seiten bitte entweder per Post oder per Email zusenden!) Sehr geehrte Damen und Herren, im Rahmen eines Promotionsvorhabens an der Universität Witten/Herdecke möchten wir Menschen mit
Studie zur Sicherheit von Flugreisen bei Patienten mit Pulmonaler Hypertonie (jeglicher Genese)
 Prüfstelle: Abteilung Pneumologie und Intensivmedizin der Medizinischen Klinik II Uniklinik Gießen und Marburg Standort Gießen Klinikstr. 33, 35392 Gießen Telefon: 0641 985 42352 Prüfärzte: Prof. Dr. A.
Prüfstelle: Abteilung Pneumologie und Intensivmedizin der Medizinischen Klinik II Uniklinik Gießen und Marburg Standort Gießen Klinikstr. 33, 35392 Gießen Telefon: 0641 985 42352 Prüfärzte: Prof. Dr. A.
Patienteninformation zur Teilnahme an der Registerstudie NEOCYST Netzwerk zur Erforschung zystischer Nierenerkrankungen im Kindesalter
 Patienteninformation und Einwilligungserklärung zur Teilnahme an der Registerstudie NEOCYST Patienten von 6 17 Jahren Registerleitung: Univ.-Prof. Dr. med. Martin Konrad Klinik und Poliklinik für Kinder-
Patienteninformation und Einwilligungserklärung zur Teilnahme an der Registerstudie NEOCYST Patienten von 6 17 Jahren Registerleitung: Univ.-Prof. Dr. med. Martin Konrad Klinik und Poliklinik für Kinder-
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG
 PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Nicht-interventionelle Studie zu Edoxaban für die Behandlung des nicht-valvulären Vorhofflimmerns in der klinischen Routine (ETNA-AF-Europe) Nummer der klinischen
PATIENTENINFORMATION UND EINWILLIGUNGSERKLÄRUNG Nicht-interventionelle Studie zu Edoxaban für die Behandlung des nicht-valvulären Vorhofflimmerns in der klinischen Routine (ETNA-AF-Europe) Nummer der klinischen
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Informationsschrift. Momentum Projekt Heidelberg Aktiver Umgang mit einer Krebserkrankung
 Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
Informationsschrift Sehr geehrte Teilnehmerin, sehr geehrter Teilnehmer, Zweck der Studie Der Umgang mit einer Krebserkrankung kann sehr unterschiedlich ausfallen: Jede/r Betroffene findet andere Wege,
PATIENTENINFORMATION. Nationales Klinisches Amyloidose-Register
 UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
UniversitätsKlinikum Heidelberg Medizinische Klinik Universitätsklinikum Heidelberg Im Neuenheimer Feld 410 69120 Heidelberg Medizinische Klinik (Krehl-Klinik) Abteilung Innere Medizin V Hämatologie, Onkologie
2. Um welche Art von Biomaterialien und Daten handelt es sich?
 150701 Biobank Augenklinik Version 1_modek.docx Klinik für Augenheilkunde Universitätsklinikum Freiburg Killianstraße 5 D-79106 Freiburg Spende, Einlagerung und Nutzung von Biomaterialien sowie Erhebung,
150701 Biobank Augenklinik Version 1_modek.docx Klinik für Augenheilkunde Universitätsklinikum Freiburg Killianstraße 5 D-79106 Freiburg Spende, Einlagerung und Nutzung von Biomaterialien sowie Erhebung,
Einfluss von Erythropoetin (Epo) auf exekutive Funktionen bei frühgeborenen Kindern (EpoKids)
 Teilnehmerinformation für Eltern Einfluss von Erythropoetin (Epo) auf exekutive Funktionen bei frühgeborenen Kindern (EpoKids) Wissenschaftlicher Titel der Studie: Long-term neuroprotective effect of erythropoietin
Teilnehmerinformation für Eltern Einfluss von Erythropoetin (Epo) auf exekutive Funktionen bei frühgeborenen Kindern (EpoKids) Wissenschaftlicher Titel der Studie: Long-term neuroprotective effect of erythropoietin
Patienteninformation und Einverständniserklärung zur Teilnahme an der ARPKD Registerstudie ARegPKD
 Patienteninformation und Einverständniserklärung zur Teilnahme an der ARPKD Registerstudie ARegPKD Registerleitung: Stellvertreter: Dr. med. Max C. Liebau Dr. med. Markus Feldkötter Kinderklinik Zentrum
Patienteninformation und Einverständniserklärung zur Teilnahme an der ARPKD Registerstudie ARegPKD Registerleitung: Stellvertreter: Dr. med. Max C. Liebau Dr. med. Markus Feldkötter Kinderklinik Zentrum
Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms)
 Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms) Die Anwendung kurz andauernder magnetischer Reize über dem intakten Schädeldach bewirkt auf der Grundlage der elektromagnetischen
Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms) Die Anwendung kurz andauernder magnetischer Reize über dem intakten Schädeldach bewirkt auf der Grundlage der elektromagnetischen
Management von Hepatitis C in Drogensubstitutionsprogrammen - Kanton Aargau
 Infektiologie/Spitalhygiene Kantonsspital Aarau AG Tellstrasse 5001 Aarau Teilnehmerinnen- / Teilnehmerinformation Management von Hepatitis C in Drogensubstitutionsprogrammen - Kanton Aargau Sponsor: Kantonsspital
Infektiologie/Spitalhygiene Kantonsspital Aarau AG Tellstrasse 5001 Aarau Teilnehmerinnen- / Teilnehmerinformation Management von Hepatitis C in Drogensubstitutionsprogrammen - Kanton Aargau Sponsor: Kantonsspital
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des ZNS im Rahmen des MS-Spenderprogramms Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie,
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des ZNS im Rahmen des MS-Spenderprogramms Universitätsmedizin Göttingen, 37099 Göttingen Institut für Neuropathologie,
Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
 Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Telefon : ++49 (0)551 / 39-22700 Fax : ++49 (0)551 / 39-8472 Patienteninformation Information zur Einrichtung einer Gewebebank von chronisch entzündlichen Erkrankungen des Nervensystems im Rahmen des MS-Spenderprogramms
Einfluss von Erythropoetin (Epo) auf exekutive Funktionen bei frühgeborenen Kindern (EpoKids)
 Teilnehmerinformation für Eltern Einfluss von Erythropoetin (Epo) auf exekutive Funktionen bei frühgeborenen Kindern (EpoKids) Wissenschaftlicher Titel der Studie: Long-term neuroprotective effect of erythropoietin
Teilnehmerinformation für Eltern Einfluss von Erythropoetin (Epo) auf exekutive Funktionen bei frühgeborenen Kindern (EpoKids) Wissenschaftlicher Titel der Studie: Long-term neuroprotective effect of erythropoietin
Protokoll Abschlussarbeit
 Protokoll Abschlussarbeit Sandra Kaspar Ziegelstrasse 6 8038 Zürich Tel: 01 450 36 28 Fax: 01 450 36 29 Email:sandrak1@bluewin.ch Brigitte van Dulmen Hintermettlen 9 6318 Walchwil Tel: 041 711 67 70 Fax:
Protokoll Abschlussarbeit Sandra Kaspar Ziegelstrasse 6 8038 Zürich Tel: 01 450 36 28 Fax: 01 450 36 29 Email:sandrak1@bluewin.ch Brigitte van Dulmen Hintermettlen 9 6318 Walchwil Tel: 041 711 67 70 Fax:
Teilnehmerinneninformation. Die Entwicklung der Kinder von der Geburt bis zum 2. Geburtstag
 HEILPÄDAGOGISCHES INSTITUT DER UNIVERSITÄT FREIBURG (SCHWEIZ) PD Dr. phil. Dagmar Orthmann Bless Lehr- und Forschungsrätin Petrus-Kanisius-Gasse 21 CH-1700 Freiburg Teilnehmerinneninformation Studie: Die
HEILPÄDAGOGISCHES INSTITUT DER UNIVERSITÄT FREIBURG (SCHWEIZ) PD Dr. phil. Dagmar Orthmann Bless Lehr- und Forschungsrätin Petrus-Kanisius-Gasse 21 CH-1700 Freiburg Teilnehmerinneninformation Studie: Die
Patientenaufklärungs- und Informationshinweise
 Patientenaufklärungs- und Informationshinweise ZIELSETZUNG DER STUDIE Ihnen wird hiermit die Teilnahme an einer klinischen Studie angeboten. Ziel dieser Studie ist der klinische Ausgang und der Wirksamkeitsnachweis
Patientenaufklärungs- und Informationshinweise ZIELSETZUNG DER STUDIE Ihnen wird hiermit die Teilnahme an einer klinischen Studie angeboten. Ziel dieser Studie ist der klinische Ausgang und der Wirksamkeitsnachweis
ANMELDUNG FÜR PRIVATPATIENTEN
 ANMELDUNG FÜR PRIVATPATIENTEN Name Vorname Namenszusatz Akad. Titel Geburtsdatum Straße / Hausnummer PLZ Ort Tel. privat Tel. mobil Tel. tagsüber/arbeit Beruf Arbeitgeber Privatversichert wo: Selbstzahler
ANMELDUNG FÜR PRIVATPATIENTEN Name Vorname Namenszusatz Akad. Titel Geburtsdatum Straße / Hausnummer PLZ Ort Tel. privat Tel. mobil Tel. tagsüber/arbeit Beruf Arbeitgeber Privatversichert wo: Selbstzahler
Fragebogen zum vermuteten Behandlungsfehler
 Fragebogen zum vermuteten Behandlungsfehler Persönliche Angaben Angaben zum Kunden, dessen Behandlung überprüft werden soll Name, Vorname: Geburtsdatum: Versicherungsnummer: Telefon: Fax: E-Mail: Angaben
Fragebogen zum vermuteten Behandlungsfehler Persönliche Angaben Angaben zum Kunden, dessen Behandlung überprüft werden soll Name, Vorname: Geburtsdatum: Versicherungsnummer: Telefon: Fax: E-Mail: Angaben
Anamnesebogen. Liebe Patienten, bitte füllen Sie diesen Bogen leserlich und in Druckbuchstaben aus. Erziehungsberechtigter: Gewicht, Größe: Beruf:
 Liebe Patienten, bitte füllen Sie diesen Bogen leserlich und in Druckbuchstaben aus. Anamnesebogen Patient Name, Vorname: Geb. Datum: Adresse: Ort: Telefonnummer: E-Mailadresse: Erziehungsberechtigter:
Liebe Patienten, bitte füllen Sie diesen Bogen leserlich und in Druckbuchstaben aus. Anamnesebogen Patient Name, Vorname: Geb. Datum: Adresse: Ort: Telefonnummer: E-Mailadresse: Erziehungsberechtigter:
Liebe Patientin, lieber Patient,
 30.8/066-09/14 Liebe Patientin, lieber Patient, wir freuen uns, dass Sie sich für das TK-Angebot Besondere ambulante ärztliche Versorgung interessieren. Hier erfahren Sie mehr darüber und wie Sie daran
30.8/066-09/14 Liebe Patientin, lieber Patient, wir freuen uns, dass Sie sich für das TK-Angebot Besondere ambulante ärztliche Versorgung interessieren. Hier erfahren Sie mehr darüber und wie Sie daran
Patienteninformation. zur Teilnahme an
 Prüfstelle: Patienteninformation zur Teilnahme an Randomisierte endokrine Therapieintervention bei postmenopausalen, hormonrezeptorpositiven Patientinnen mit dem Nachweis zirkulierender Tumorzellen im
Prüfstelle: Patienteninformation zur Teilnahme an Randomisierte endokrine Therapieintervention bei postmenopausalen, hormonrezeptorpositiven Patientinnen mit dem Nachweis zirkulierender Tumorzellen im
Patienteninformation
 Patienteninformation zum MS-Register der DMSG, Bundesverband e.v. Sehr geehrte Patientin, sehr geehrter Patient, wir möchten Sie um Ihre Einwilligung zur Teilnahme an dem MS-Register der DMSG, Bundesverband
Patienteninformation zum MS-Register der DMSG, Bundesverband e.v. Sehr geehrte Patientin, sehr geehrter Patient, wir möchten Sie um Ihre Einwilligung zur Teilnahme an dem MS-Register der DMSG, Bundesverband
EINVERSTÄNDNISERKLÄRUNG ZUR SCHUTZIMPFUNG
 EINVERSTÄNDNISERKLÄRUNG ZUR SCHUTZIMPFUNG MMR Impfung BITTE BEANTWORTEN SIE DIE NACHSTEHENDEN FRAGEN: ( Zutreffendes bitte ankreuzen) Sollte die zu impfende Person zwischen dem Ausfüllen der Einverständniserklärung
EINVERSTÄNDNISERKLÄRUNG ZUR SCHUTZIMPFUNG MMR Impfung BITTE BEANTWORTEN SIE DIE NACHSTEHENDEN FRAGEN: ( Zutreffendes bitte ankreuzen) Sollte die zu impfende Person zwischen dem Ausfüllen der Einverständniserklärung
Studieninformation. Machbarkeit & Akzeptanz des Pilotprojekts zur Vermeidung Frühkindlicher Karies in Pirmasens-Zweibrücken (Rheinland-Pfalz)
 Team Pirmasens GbR Studienleiter: Prof. Dr. Christian Splieth Team Pirmasens GbR Gesterdingstr. 23, 17489 Greifswald, Telefax: 03834 931 913 2 team-pirmasens@gmx.de Studieninformation Machbarkeit & Akzeptanz
Team Pirmasens GbR Studienleiter: Prof. Dr. Christian Splieth Team Pirmasens GbR Gesterdingstr. 23, 17489 Greifswald, Telefax: 03834 931 913 2 team-pirmasens@gmx.de Studieninformation Machbarkeit & Akzeptanz
Klinik für Anästhesiologie Departement für Anästhesie, Operative Intensivbehandlung, Präklinische Notfallmedizin und Schmerztherapie
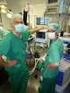 Kurzfassung der Studieninformation Wirkung von Pabal (Carbetocin) auf die Gebärmutter beim Kaiserschnitt: Vergleich einer langsamen Bolusgabe mit einer Gabe als Kurzinfusion Details auf Seite Offizieller
Kurzfassung der Studieninformation Wirkung von Pabal (Carbetocin) auf die Gebärmutter beim Kaiserschnitt: Vergleich einer langsamen Bolusgabe mit einer Gabe als Kurzinfusion Details auf Seite Offizieller
1. Nachtrag zum Vertrag nach 73 c SGB V über die Durchführung eines ergänzenden Hautkrebsvorsorge-Verfahrens
 TK-Vertragsnummer: 500015 1. Nachtrag zum Vertrag nach 73 c SGB V über die Durchführung eines ergänzenden Hautkrebsvorsorge-Verfahrens zwischen der Kassenärztlichen Vereinigung Hamburg Humboldtstr. 56
TK-Vertragsnummer: 500015 1. Nachtrag zum Vertrag nach 73 c SGB V über die Durchführung eines ergänzenden Hautkrebsvorsorge-Verfahrens zwischen der Kassenärztlichen Vereinigung Hamburg Humboldtstr. 56
WENN SOGAR UMARMUNGEN WEHTUN DIE NÄCHSTEN SCHRITTE. Informationen für Patienten. besuchen Sie
 DIE NÄCHSTEN SCHRITTE Wir danken Ihnen, dass Sie sich die Zeit genommen haben, sich über diese wichtige Studie zu informieren. Wenn Sie teilnehmen möchten, kontaktieren Sie uns bitte, damit wir einen Besuchstermin
DIE NÄCHSTEN SCHRITTE Wir danken Ihnen, dass Sie sich die Zeit genommen haben, sich über diese wichtige Studie zu informieren. Wenn Sie teilnehmen möchten, kontaktieren Sie uns bitte, damit wir einen Besuchstermin
Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen
 Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen Informationsbroschüre für männliche Patienten und Patientinnen, die nicht im gebärfähigen Alter sind Diese Informationsbroschüre wurde
Therapie mit Acitretin-haltigen Arzneimitteln: Was Sie wissen müssen Informationsbroschüre für männliche Patienten und Patientinnen, die nicht im gebärfähigen Alter sind Diese Informationsbroschüre wurde
Patienten/Patientinnen Vereinbarung. Gesundheitsdialog
 Patienten/Patientinnen Vereinbarung Gesundheitsdialog Inhalt 1 PRÄAMBEL... 3 2 ZUSTIMMUNG ZUR TEILNAHME... 3 3 NUTZUNG DER SYSTEME DURCH DEN/DIE PATIENTEN/PATIENTIN... 3 4 BEREITSTELLUNG EINES SYSTEMS
Patienten/Patientinnen Vereinbarung Gesundheitsdialog Inhalt 1 PRÄAMBEL... 3 2 ZUSTIMMUNG ZUR TEILNAHME... 3 3 NUTZUNG DER SYSTEME DURCH DEN/DIE PATIENTEN/PATIENTIN... 3 4 BEREITSTELLUNG EINES SYSTEMS
Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms)
 Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms) Die Anwendung kurz andauernder magnetischer Reize über dem intakten Schädeldach bewirkt auf der Grundlage der elektromagnetischen
Aufklärung über die neuronavigierte Transkranielle Magnetische Stimulation (ntms) Die Anwendung kurz andauernder magnetischer Reize über dem intakten Schädeldach bewirkt auf der Grundlage der elektromagnetischen
Leberresektion eine randomisierte kontrollierte Studie zum Vergleich von zwei chirurgischen Techniken
 UniversitätsKlinikum Heidelberg Chirurgische Universitätsklinik Im Neuenheimer Feld 110 D-69120 Heidelberg Studienleitung Prof. Dr. med. Jürgen Weitz Studiendurchführung Dr. med. Nuh N. Rahbari Heike Elbers
UniversitätsKlinikum Heidelberg Chirurgische Universitätsklinik Im Neuenheimer Feld 110 D-69120 Heidelberg Studienleitung Prof. Dr. med. Jürgen Weitz Studiendurchführung Dr. med. Nuh N. Rahbari Heike Elbers
Einwilligungserklärung zur Teilnahme an der Studie. Intelligenzminderung und syndromale Krankheitsbilder mit Mutationen im SWI/SNF-Komplex"
 Institut für Humangenetik Universitätsklinikum Düsseldorf Universitätsstr. 1, Gebäue 23.12.03, 40225 Düsseldorf Prof. Dr. med. Dagmar Wieczorek Telefon: +49 211 81 12350 Telefax: +49 211 81 12538 E-Mail:
Institut für Humangenetik Universitätsklinikum Düsseldorf Universitätsstr. 1, Gebäue 23.12.03, 40225 Düsseldorf Prof. Dr. med. Dagmar Wieczorek Telefon: +49 211 81 12350 Telefax: +49 211 81 12538 E-Mail:
Teilnahme- und Einwilligungserklärung für Versicherte der AOK Nordost Berliner Projekt Die Pflege mit dem Plus
 Krankenkasse bzw. Kostenträger Name, Vorname des Versicherten geb. am Kostenträgerkennung Versicherten-Nr. Status Betriebsstätten-Nr. Arzt-Nr. Datum Tel.-Nr. (Angabe freiwillig) Teilnahme- und Einwilligungserklärung
Krankenkasse bzw. Kostenträger Name, Vorname des Versicherten geb. am Kostenträgerkennung Versicherten-Nr. Status Betriebsstätten-Nr. Arzt-Nr. Datum Tel.-Nr. (Angabe freiwillig) Teilnahme- und Einwilligungserklärung
STUDIENTEILNEHMER/-INNEN GESUCHT
 STUDIENTEILNEHMER/-INNEN GESUCHT Körperliche Fitness und Gefässgesundheit bei Patienten mit rheumatoiden Erkrankungen Wir suchen Sie, wenn Sie eine rheumatische Erkrankung haben, deren Diagnosezeitpunkt
STUDIENTEILNEHMER/-INNEN GESUCHT Körperliche Fitness und Gefässgesundheit bei Patienten mit rheumatoiden Erkrankungen Wir suchen Sie, wenn Sie eine rheumatische Erkrankung haben, deren Diagnosezeitpunkt
Dringender Sicherheitshinweis Chargenrückruf des gabcontrol D-Dimer Schnelltests (M09DD02) vom Markt
 Am Wassermann 28 50829 Köln Adressat: Anwender, Betreiber, Vertreiber des gabcontrol D-Dimer Schnelltests (M09DD02) Praxis- & Drogendiagnostik Am Wassermann 28 D-50829 Köln Telefon: 02 21 56 97 3-0 Fax:
Am Wassermann 28 50829 Köln Adressat: Anwender, Betreiber, Vertreiber des gabcontrol D-Dimer Schnelltests (M09DD02) Praxis- & Drogendiagnostik Am Wassermann 28 D-50829 Köln Telefon: 02 21 56 97 3-0 Fax:
Ein sorgfältig gepflegter Garten strahlt Schönheit aus und bereitet Freude. (Das gilt auch für die Gesundheit Ihrer Knochen.)
 Ein sorgfältig gepflegter Garten strahlt Schönheit aus und bereitet Freude. (Das gilt auch für die Gesundheit Ihrer Knochen.) Die Erhaltung Ihrer Knochen erfordert Ihre Pflege und Aufmerksamkeit. Wenn
Ein sorgfältig gepflegter Garten strahlt Schönheit aus und bereitet Freude. (Das gilt auch für die Gesundheit Ihrer Knochen.) Die Erhaltung Ihrer Knochen erfordert Ihre Pflege und Aufmerksamkeit. Wenn
Die Betreuungsverfügung
 Die Was ist das? In der benennt der volljährige Verfasser eine Person des eigenen Vertrauens für den Fall, dass das Vormundschaftsgericht wegen Entscheidungs- und Handlungsunfähigkeit einen gesetzlichen
Die Was ist das? In der benennt der volljährige Verfasser eine Person des eigenen Vertrauens für den Fall, dass das Vormundschaftsgericht wegen Entscheidungs- und Handlungsunfähigkeit einen gesetzlichen
Checkliste (nicht AMG-Studie)
 Checkliste (nicht AMG-Studie) 1. Basisdaten 1.1 Vollständiger Titel der Studie 1.2 Studienleiter/Studienleiterin vor Ort (Vor- und Zuname, Beruf, Akademischer Titel, Anschrift, Telefon, Fax, Email) 1.3
Checkliste (nicht AMG-Studie) 1. Basisdaten 1.1 Vollständiger Titel der Studie 1.2 Studienleiter/Studienleiterin vor Ort (Vor- und Zuname, Beruf, Akademischer Titel, Anschrift, Telefon, Fax, Email) 1.3
Informationen für die Eltern und Kinder der Ernährung-und Allergie-Studie. Kurzfassung der Studieninformation
 Informationen für die Eltern und Kinder der Ernährung-und Allergie-Studie Ostschweizer Kinderspital Claudiusstrasse 6 9006 St. Gallen Kurzfassung der Studieninformation Kind, Allergie und Ernährung (CARE)
Informationen für die Eltern und Kinder der Ernährung-und Allergie-Studie Ostschweizer Kinderspital Claudiusstrasse 6 9006 St. Gallen Kurzfassung der Studieninformation Kind, Allergie und Ernährung (CARE)
Antrag zur Durchführung einer epidemiologischen Studie
 Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
Absender/ Begleitschreiben: Antrag zur Durchführung einer epidemiologischen Studie 1. Bezeichnung der Studie 2. Ziel der Studie Fragestellung (einschl. Formulierung der Forschungshypothese) Relevanz für
SAKK 41/14 ACTIVE-2 Ein Bewegungsprogramm während der Chemotherapie für Patienten mit fortgeschrittenem Darmkrebs eine randomisierte Studie
 A) Kurzfassung der Studieninformation Version 2.0 vom 07.12.2015 SAKK 41/14 ACTIVE-2 Ein Bewegungsprogramm während der Chemotherapie für Patienten mit fortgeschrittenem Darmkrebs eine randomisierte Studie
A) Kurzfassung der Studieninformation Version 2.0 vom 07.12.2015 SAKK 41/14 ACTIVE-2 Ein Bewegungsprogramm während der Chemotherapie für Patienten mit fortgeschrittenem Darmkrebs eine randomisierte Studie
Transparenz in der Zusammenarbeit mit Ärzten
 Transparenz in der Zusammenarbeit mit Ärzten Offenlegung von Zahlungen an Ärzte und andere Heilberufe Die Pharmaindustrie und Angehörige medizinischer Fachkreise arbeiten in vielen Bereichen zusammen:
Transparenz in der Zusammenarbeit mit Ärzten Offenlegung von Zahlungen an Ärzte und andere Heilberufe Die Pharmaindustrie und Angehörige medizinischer Fachkreise arbeiten in vielen Bereichen zusammen:
Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf
 Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, im Folgenden möchten wir Sie um Ihr Einverständnis bitten,
Patienteninformation und Einverständniserklärung zur Biobank des Universitätsklinikums Düsseldorf Sehr geehrte Patientin, sehr geehrter Patient, im Folgenden möchten wir Sie um Ihr Einverständnis bitten,
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept
 PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
Was Sie tun können, um richtig vorzusorgen Durch einen Unfall, eine schwere Krankheit oder Altersabbau kann jeder Mensch in eine Situation kommen, in
 1BUJFOUFOWFSGÛHVOH 7PSTPSHFWPMMNBDIU #FUSFVVOHTWFSGÛHVOH Was Sie tun können, um richtig vorzusorgen Durch einen Unfall, eine schwere Krankheit oder Altersabbau kann jeder Mensch in eine Situation kommen,
1BUJFOUFOWFSGÛHVOH 7PSTPSHFWPMMNBDIU #FUSFVVOHTWFSGÛHVOH Was Sie tun können, um richtig vorzusorgen Durch einen Unfall, eine schwere Krankheit oder Altersabbau kann jeder Mensch in eine Situation kommen,
Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1
 Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1 Das Programm für Ihre Gesundheit 2 AOK-Curaplan Diabetes mellitus Typ 1 Was ist AOK-Curaplan? An den strukturierten Behandlungsprogrammen für chronisch
Patienteninformation AOK-Curaplan Diabetes mellitus Typ 1 Das Programm für Ihre Gesundheit 2 AOK-Curaplan Diabetes mellitus Typ 1 Was ist AOK-Curaplan? An den strukturierten Behandlungsprogrammen für chronisch
für die Patienten-Information und -Einwilligung zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten
 PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
PROSTATITIS, ENTZÜNDUNG UND FRUCHTBARKEIT für die zur Durchführung einer klinischen Studie mit volljährigen einwilligungsfähigen Patienten Prüfstelle: Klinik für Urologie, Kinderurologie und Andrologie,
An die Eltern der Kindergartenkinder
 U NIVERSITÄT F REIBURG (SCHWEIZ) D EPARTEMENT F ÜR PSYCHOLOGIE PROF. D R. N ADINE M ESSERLI-BÜ RGY An die Eltern der Kindergartenkinder Studie STERN: Stresserleben, Stressregulation und Gesundheit bei
U NIVERSITÄT F REIBURG (SCHWEIZ) D EPARTEMENT F ÜR PSYCHOLOGIE PROF. D R. N ADINE M ESSERLI-BÜ RGY An die Eltern der Kindergartenkinder Studie STERN: Stresserleben, Stressregulation und Gesundheit bei
Ethikkommissionen an Universitätskliniken Beispiele aus der Praxis
 Ethikkommissionen an Universitätskliniken Beispiele aus der Praxis Prof. Dr. H.D. Tröger Vorsitzender der Ethikkommission Carl-Neuberg-Str. 1 30625 Hannover Quelle: http://www.bundesaerztekammer.de/downloads/deklhelsinki2013.pdf
Ethikkommissionen an Universitätskliniken Beispiele aus der Praxis Prof. Dr. H.D. Tröger Vorsitzender der Ethikkommission Carl-Neuberg-Str. 1 30625 Hannover Quelle: http://www.bundesaerztekammer.de/downloads/deklhelsinki2013.pdf
Patienteninformation. Sehr geehrte Patientin, sehr geehrter Patient,
 und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
und Biomaterialbank Biomaterialsammlung und prospektive Datenerfassung zu Diagnostik, Behandlung und Krankheitsverlauf der ALL des Erwachsenen Patienteninformation Sehr geehrte Patientin, sehr geehrter
