Benjamin Franklin Beer is proof that God loves us and wants us to be happy.
|
|
|
- Margarethe Rothbauer
- vor 7 Jahren
- Abrufe
Transkript
1 Benjamin Franklin Beer is proof that God loves us and wants us to be happy.
2 Warum entsteht ausgerechnet Ethanol beim Vergären von fermentiertem Getreide (= Kohlenhydraten)? Benjamin Franklin Beer is proof that God loves us and wants us to be happy.
3 Alkoholische Gärung Amylose (Bestandteil der Stärke; ein Polysaccharid) Quelle: zg-raiffeisen.de Gärungen sind mikrobielle Abbauprozesse zur Energiegewinnung in Abwesenheit von Sauerstoff. Sie sind allerdings deutlich weniger energieeffizient als die biochemischen Abbauprozesse in Gegenwart von 2. Ein bekanntes Beispiel dafür ist die alkoholische Gärung, die beim Bierbrauen eine Rolle spielt.
4 Alkoholische Gärung ydrolyse Amylose (Bestandteil der Stärke; ein Polysaccharid) Maltose (= Malzzucker; ein Disaccharid) Quelle:
5 Alkoholische Gärung ydrolyse Amylose (Bestandteil der Stärke; ein Polysaccharid) Maltose (= Malzzucker; ein Disaccharid) ydrolyse 2 D-Glucose (offenkettige Aldehydform) Quelle: gsn-donau.de
6 Alkoholische Gärung Quelle: motor-talk.de ydrolyse Amylose (Bestandteil der Stärke; ein Polysaccharid) Maltose (= Malzzucker; ein Disaccharid) ydrolyse C 2 (Katalysator: Enzyme der efe) 2 Ethanol Kohlendioxid D-Glucose (offenkettige Aldehydform)
7 P 2 P P D-Glycerinaldehyd-3-phosphat D-Glucose D-Fructose-1,6-bisphosphat Der Abbau des Traubenzuckers erfolgt über sein Isomeres, nämlich den Fruchtzucker (= D-Fructose), und zwar in dessen zweifach phosphorylierter Form (d.h. die -Gruppen an den C-Atomen 1 und 6 der D-Fructose sind mit Phosphorsäure verestert). Der ame dieses Zwischenprodukts lautet D-Fructose-1,6-bisphosphat.
8 P 2 P P D-Glycerinaldehyd-3-phosphat D-Glucose D-Fructose-1,6-bisphosphat Die folgende Folie soll uns einen Überblick geben, auf welchem Weg vom Spaltprodukt des D-Fructose-1,6-bisphosphats, nämlich dem Glycerinaldehyd-3-phosphat, ausgehend, in einer Kaskade von Reaktionsschritten Ethanol entsteht.
9 xidation Salz der 3-Phospho-glycerinsäure (= 3-Phosphoglycerat) 1 2-Phosphoglycerat Isomerisierung P 2 3 P Ethanol Phosphoenolpuruvat [gemischter Ester aus dem Salz der (anorganischen) Phosphorsäure und dem Salz der (organischen) Enolform der Brenztraubensäure] Dehydratisierung (= Abspaltung von Wasser) P 4 ydrolyse P Glycerinaldehyd-3-phosphat Reduktion 7 Decarboxylierung 6 5 Isomerisierung (hier: Keto-Enol- Tautomerie) Ethanal (= Acetaldehyd) Salz der 2-xopropansäure (= Salz der Brenztraubensäure = = Pyruvat) Salz der 2-ydroxy- -propensäure (= Salz der Enolform der Brenztraubensäure)
10 Salz der 3-Phospho-glycerinsäure (= 3-Phosphoglycerat) P Im ersten Reaktionsschritt wird die Aldehydgruppe zur Carbonsäuregruppe (bzw. deren Salz) oxidiert. xidation 1 Welche Verbindung fungiert in diesem Schritt als xidationsmittel? (dieses grün umrandete Dreieck zeigt uns die beiden C-Atome und das -Atom des späteren Ethanol-Moleküls) P Glycerinaldehyd-3-phosphat
11 ? Kann das xidationsmittel im Fall der alkoholischen Gärung der Luftsauerstoff sein? (Man beachte im Übrigen die korrekte Wiedergabe des Sauerstoff-Moleküls als diradikalische Spezies!)
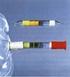
12 Quelle: chemie-master.de ein denn die alkoholische Gärung ist ein anaerober Prozeß. Um das Eindringen von Luftsauerstoff in den Gärbottich zu verhindern, setzen Winzer beim Vergären von Traubensaft ein sogenanntes Gärröhrchen (siehe Abbildung) auf den Bottich. Das Gärröhrchen erlaubt zwar das Entweichen von Kohlendioxid (C 2 ) und somit einen Druckausgleich, aber es verhindert das Eindringen von Luft und damit auch des Sauerstoffs in der Luft (Anteil: 20,9%).
13 Quelle: wikipedia.de Ein weiterer Beleg dafür, daß es auch energieliefernde Prozesses ohne utzung von Luftsauerstoff als xidationsmittel gibt, ist die Tatsache, daß in sauerstoffarmen Regionen wie z.b. der Tiefsee Leben existiert, und zwar ohne Glykolyse (so bezeichnet man den energieliefernden Stoffwechsel, der auf dem Umsetzen eines Kohlenhydrats mit Sauerstoff basiert). Da diese Tiere offenbar in Abwesenheit von Sauerstoff leben können, muß ihr energieliefernder Stoffwechsel eine Alternative zum Sauerstoff als xidans entwickelt haben.
14 2 P 2 P Das xidationsmittel für die energieliefernde Umwandlung von Glycerinaldehyd-phosphat zum Salz der Phosphoglycerinsäure ist die hier abgebildete Verbindung namens icotinsäureamid-adenin-dinucleotid AD +.
15 2 P 2 P Der ame der Verbindung leitet sich ab vom icotinsäureamid (siehe Rechteck in der Abbildung).
16 2 Das -Atom im Pyridin-Ring ist vierbindig und daher positiv geladen. Daher stammt auch das + in der Abkürzung AD +.
17 Diese Struktur zeigt den aturstoff icotin, welcher der amensgeber für die
18 icotinsäure
19 2 bzw. das hier abgebildete icotinsäureamid ist.
20 2 Die Struktur des Restes, der mit dem -Atom des Pyridin-Rings verbunden ist, können wir der Abbildung des AD + auf der vorhergehenden Folie r. 15 entnehmen. Er spielt für die Wiedergabe des entscheidenden Schritts der Redoxreaktion allerdings keine Rolle.
21 2 Zur Verdeutlichung des Redoxprozesses geben wir eines der -Atome am aromatischen Ring gesondert wieder, nämlich das -Atom am C-Atom r. 4, welches in para-position zum -Atom steht (also dem -Atom gegenüber).
22 2 Da das AD + das xidationsmittel ist, muß es im Rahmen der Redoxreaktion logischerweise reduziert werden, also Elektronen aufnehmen. Eine klassische Form dieser Elektronenaufnahme ist die Anlagerung von Wasserstoff, und zwar mit den entsprechenden Elektronen (andernfalls wäre es definitionsgemäß keine Reduktion!).
23 katalytische ydrierung + (E)-2-Butensäure Butansäure 2 Der obere Teil der Abbildung zeigt uns die drei ptionen: a) Anlagerung von Wasserstoff als Molekül (wie z.b. bei der katalytischen ydrierung von ungesättigten Fettsäuren zu den entsprechenden gesättigten Fettsäuren);
24 ydrierung mit -Atomen itrobenzol 2 Aminobenzol = Anilin b) Anlagerung von zwei Atomen Wasserstoff (= nascierender Wasserstoff, falls diese -Atome im Reaktionsgefäß durch die Aufnahme je eines Elektrons durch je ein Proton hergestellt wurden, wie z.b. bei der Reduktion von itrobenzol zu Anilin in einem Gemisch aus Eisenschrott und Salzsäure die Protonen + der Salzsäure werden dabei durch Aufnahme je eines Elektrons des metallischen Eisens zu -Atomen reduziert);
25 Reduktion mit ydrid-ionen 2 c) Letztendlich können die beiden Elektronen auch so aufgeteilt werden, daß ein Wasserstoff beide Elektronen erhält (wir sprechen in dem Fall von einem ydrid-ion) und der andere Wasserstoff leer ausgeht und als Proton + übrigbleibt. In diesem Fall kann logischerweise nur das ydrid-ion als Reduktionsmittel fungieren, da es im Gegensatz zum Proton über Elektronen verfügt.
26 2 Dieser Fall c) tritt, zumindest rein formal, bei der Reduktion des AD + ein. Beim Angriff des Wasserstoffs auf das C-Atom r. 4 des Rings werden beide Elektronen mitgenommen. De facto greift hier also ein ydrid-ion an.
27 2 Übrig bleiben das Proton + und die reduzierte Form des icotinsäureamid-adenin-dinucleotids, welche als AD abgekürzt wird.
28 2 2 ier nochmals die reduzierte und die oxidierte Form des icotinsäureamid-adenin-dinucleotids im Vergleich.
29 Die bei der xidation von AD freigesetzten Elektronen (hier in Form der Elektronen im 1s-rbital von -Atomen vorliegend; siehe obere Reaktionsgleichung rechts) werden im Fall von aeroben Prozessen letzten Endes, nach einer Kaskade von Elektronenübergängen auf andere Moleküle und Elektronenabgängen von den entsprechenden reduzierten Formen jener Verbindungen, von einem Sauerstoff-Molekül aufgenommen (siehe untere Reaktionsgleichung in der Abbildung). Das Sauerstoff-Molekül wird dabei zu zwei Äquivalenten Wasser reduziert. 2 xidation Reduktion 4 + Reduktion 2 xidation
30 Auf dieser abschließenden Aufnahme der Elektronen durch Sauerstoff und der Bildung von Wasser beruht unsere Atmung. Dieser Vorgang ist essentiell für den Stoffwechsel und somit unser Leben, denn nur durch eine abschließende Fixierung der Elektronen im Fall der normalen Atmung im Wasser-Molekül kann das AD + wieder regeneriert werden, so daß es erneut ein Molekül Glycerinaldehyd-phosphat oxidieren und die Energiegewinnung im menschlichen Körper aufrecht erhalten kann. 2 xidation Reduktion 4 + Reduktion 2 xidation
31 Steht der Sauerstoff als ultimativer Fixierer jener Elektronen aber nicht zur Verfügung (wie im Fall der alkoholischen Gärung), dann muß das System eine andere Art und Weise der abschließenden Fixierung dieser Elektronen entwickeln. Im Fall der Gärung hat die Evolution den Aldehyd Ethanal dazu auserkoren, für diesen letztendlichen Einfang von Elektronen zu sorgen. Das Endprodukt jener lebensnotwendigen Elektronenfixierung ist Ethanol (andernfalls wären die Reserven an AD + rasch aufgebraucht) Ethanal Ethanol
32 Die Evolution hat in einigen Spezies (z.b. bei den Tintenfischen der Tiefsee) einen alternativen Elektronenfänger entwickelt. Diese Tintenfische setzen Brenztraubensäure (= 2-xo-propansäure) ein, um die Elektronen abschließend zu binden. Das Endprodukt ist Milchsäure (= 2-ydroxy-propansäure) Brenztraubensäure Milchsäure
33 Der gleiche Vorgang spielt sich in unserem Körper ab, wenn Energie freigesetzt werden muß, obwohl nicht genügend Sauerstoff zur Verfügung steht. Ein Beispiel dafür ist ein 200-Meter-Sprint
34 Wir müssen dabei im ersten Schritt der Glykolyse so viel Glycerinaldehyd-phosphat mit AD + oxidieren, daß der eingeatmete Sauerstoff mit der Fixierung der Elektronen nicht mehr nachkommt. Der Körper wird gezwungen, auf Brenztraubensäure als Elektronenfixierer umzustellen. Dies kann nach Sprints oder vergleichbaren Anstrengungen unter Sauerstoffschuld durch die Messung des Lactat-Werts bestimmt werden ( Lactat = Salz der Milchsäure)
35 Auch dieses Tier lebte lange Zeit unentdeckt in tieferen Bereichen der zeane und muß aufgrund des dortigen Sauerstoffmangels Brenztraubensäure als ultimativen Elektronenakzeptor für die Verbrennungsvorgänge im Körper bereitstellen. Quelle: wikipedia Quelle: wikipedia
36 Ethanol Was passiert mit dem Ethanol beim Stoffwechsel in unserem Körper? Man könnte auch fragen: was passiert mit dem Ethanol im Wein, wenn wir den Wein längere Zeit an der Luft stehen lassen? In beiden Fällen passiert das Gleiche: Das Ethanol wird oxidiert im Körper durch das körpereigene xidationsmittel AD + (icotinsäureamidadenin-dinucleotid, positiv geladene oxidierte Form), welches dadurch zu AD reduziert wird (icotinsäureamid-adenin-dinucleotid, ungeladene reduzierte Form).
37 Ethanol Beim Stehenlassen von Wein an der Luft passiert zunächst einmal nichts. ier müssen erst Essigsäurebakterien hinzukommen und ihre Wirkung entfalten. Dabei ist anzunehmen, daß deren Enzyme ebenfalls Cofaktoren wie AD + benötigen und letzten Endes, wie beim menschlichen Stoffwechsel, der Luftsauerstoff durch seine xidationswirkung über mehrere Zwischenstufen hinweg das AD + wieder regeneriert.
38 Ethanol Ethanal Das xidationsprodukt des Ethanols ist Ethanal (Trivialname: Acetaldehyd). Der Trivialname leitet sich vom lateinischen Ausdruck acetum (Essig) ab.
39 Ethanol Ethanal Es fällt auf, daß der Begriff xidation (lat.: oxygenium dare = Sauerstoff hinzugeben) nicht zwingend wörtlich anzuwenden ist. Das Ethanal enthält nämlich genau wie das Ethanol auch nur ein -Atom. Es wurde demnach kein Sauerstoff hinzugefügt. Aber: Dem Ethanol wurden bei der xidation zwei -Atome weggenommen (siehe Kreise in der Abbildung) wohlgemerkt: -Atome, keine Protonen!! Jedes dieser -Atome hat auch jeweils ein Elektron mitgenommen, und genau darauf kommt es bei einer xidation an: Eine xidation ist nicht anderes als eine Abgabe bzw. ein Verlust von Elektronen.
40 Ethanol Ethanal Ethansäure Das xidationsprodukt des Ethanals ist Ethansäure (Trivialname: Essigsäure). Sie ist in einer Konzentration von ca. 3% im aushaltsessig enthalten. In diesem Fall dürfen wir das oxygenium dare ausnahmsweise wörtlich nehmen. Ethansäure enthält ein -Atom mehr als Ethanal. Wie ist dies mit unserer Definition der xidation als Abgabe bzw. Verlust von Elektronen unter einen ut zu bringen?
41 Ethanol Ethanal Ethansäure Die Antwort darauf lautet: Die Abgabe bzw. der Verlust jener Elektronen muß für das betreffende Atom (hier: das C-1 im Ethanal) nicht immer vollständig sein (d.h. das Elektron muß den Molekülverband nicht zwingend verlassen). Auch ein gewisser Verlust an Elektronendichte, bedingt durch den stark elektronegativen Sauerstoff als Bindungspartner, ist eine Form der xidation.
42 Ethanol Ethanal Ethansäure Dieses Prinzip können wir auch auf die xidation des Ethanols zum Ethanal anwenden. Im Ethanol leidet das C-1 unter dem Elektronenzug über eine Bindung zu einem -Atom. Im Ethanal sind es hingegen zwei Bindungen zu diesem -Atom, über die Elektronendichte näher hin zum -Atom transferiert wird, nämlich die - und die -Bindung der C=-Doppelbindung.
43 Ethanol Ethanal Ethansäure 2-Propanol Wie sieht es mit der xidierbarkeit eines sekundären Alkohols wie z.b. 2-Propanol aus? In einem sekundären Alkohol ist das C-Atom, welches die -Gruppe trägt, mit zwei weiteren C-Atomen verbunden. (ota bene: In einem primären Alkohol wie dem Ethanol ist das C-Atom, welches die -Gruppe trägt, mit einem weiteren C-Atom verbunden).
44 Ethanol Ethanal Ethansäure 2-Propanol Propanon Auch in diesem Fall läuft die xidation analog ab: Dem Alkohol werden zwei -Atome weggenommen (Atome heißt: hier geht nicht nur ein Proton ab, sondern auch ein Elektron wird mitgenommen!), und es entsteht das entsprechende Keton (in diesem Fall Propanon, welches eher unter seinem Trivialnamen Aceton bekannt ist und gerne als Reinigungs- und Lösungsmittel verwendet wird).
45 Ethanol Ethanal Ethansäure 2-Propanol Propanon Im Gegensatz zum Aldehyd ist das Keton nicht weiter oxidierbar (zumindest nicht mit den üblichen xidationsmitteln).
46 Ethanol Ethanal Ethansäure 2-Propanol Propanon Kann ein tertiärer Alkohol wie 2-Methyl-2-propanol oxidiert werden? 2-Methyl-2-propanol (In einem tertiären Alkohol ist das C-Atom, welches die -Gruppe trägt, mit drei weiteren C-Atomen verbunden).
47 Ethanol Ethanal Ethansäure 2-Propanol Propanon Die Antwort lautet: nein. 2-Methyl-2-propanol
48 ier ein Überblick über die auf den letzten Folien betrachteten Verbindungsklassen: Primärer Alkohol Aldehyd Carbonsäure Sekundärer Alkohol Keton Tertiärer Alkohol
49 Dort, wo eine xidation möglich ist, ist mit geeigneten Reagenzien selbstverständlich auch die Rückreaktion (= Reduktion) durchführbar: xidation xidation Reduktion Reduktion Primärer Alkohol Aldehyd Carbonsäure xidation Sekundärer Alkohol Reduktion Keton Tertiärer Alkohol
Die Verknüpfung zweier kleinerer Bausteine zu einem größeren läuft in diesem Fall über eine sogenannte Aldoladdition.
 Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Quelle: www.helpster.de Quelle: www.fotocommunity.de Quelle: www.hobbybrauer.de Das Gehirn benötigt ständig Traubenzucker als Energieträger. Im Fall von Traubenzuckermangel kann der Körper über die Gluconeogenese
Einführung in die Biochemie Glykolyse
 Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Glykolyse Der Abbau der Glukose beginnt beim aeroben und beim anaeroben Abbau nach dem gleichen rinzip, der Glykolyse. Dabei wird Brenztraubensäure (2-Ketopropansäure) gebildet. Die Glykolyse ist die erste
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Organische Chemie für Mediziner WS 2016/2017. Übungsblatt 3: Ausgewählte Substanzklassen
 1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
1 rganische hemie für Mediziner WS 2016/2017 Übungsblatt 3: Ausgewählte Substanzklassen 01 Die Siedetemperatur von Alkoholen unterscheidet sich deutlich von der ungefähr gleich schwerer Alkane (z.b. 3
Claisen-Kondensation
 Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Quelle: gerlicher.de In dieser Datei soll der Mechanismus der Biosynthese wichtiger Bausteine von Ölen und festen Fetten näher betrachtet werden, nämlich die Biosynthese der Fettsäuren. Quelle: gerlicher.de
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
GRUNDWISSEN CHEMIE 10. KLASSE
 Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
Grundwissen der 10. Klasse hemie GRUNDWISSEN EMIE 10. KLASSE (LS Marquartstein Sept. 2013) 2009 Zannantonio/Wagner LS Marquartstein 1 Grundwissen der 10. Klasse hemie Alkane= gesättigte KW: In ihren Molekülen
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Z 11 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: 2) ÜBERSICHT ÜBER DEN ENERGIESTOFFWECHSEL
 GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
GRUNDLAGEN DER BIOCHEMIE STOFFWECHSELWEGE Zusammenfassung Zusammenfassung Kapitel 11 1) DIE WICHTIGSTEN STOFFWECHSELWEGE: Fette und Kohlenhydrate aus der Nahrung nutzt der Körper hauptsächlich zur Energiegewinnung.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Aldehyde, Ketone und Kohlenhydrate
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Aldehyde, Ketone und Kohlenhydrate Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Aldehyde,
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Aldehyde, Ketone und Kohlenhydrate Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Aldehyde,
Ketone gehären zu den Carbonylverbindungen. Sie tragen als funktionelle Gruppe eine nicht endståndige Carbonylgruppe. R 1 R 2
 rganische Chemie Ri 12 2.5. Ketone Ketone gehären zu den Carbonylverbindungen. Sie tragen als funktionelle Gruppe eine nicht endståndige Carbonylgruppe. R 1 C R 2 R 1 C R 2 R 1 C R 2 Strukturformel Elektronenstrichformel
rganische Chemie Ri 12 2.5. Ketone Ketone gehären zu den Carbonylverbindungen. Sie tragen als funktionelle Gruppe eine nicht endståndige Carbonylgruppe. R 1 C R 2 R 1 C R 2 R 1 C R 2 Strukturformel Elektronenstrichformel
1. Homologe Reihe der Alkansäuren
 1. omologe Reihe der Alkansäuren 2 Mit Zunahme der Kettenlänge verlängern sich die unpolaren Teile (Alkylgruppen) der Alkansäuremoleküle, dadurch steigen die van-der-waals-kräfte zwischen den Molekülen
1. omologe Reihe der Alkansäuren 2 Mit Zunahme der Kettenlänge verlängern sich die unpolaren Teile (Alkylgruppen) der Alkansäuremoleküle, dadurch steigen die van-der-waals-kräfte zwischen den Molekülen
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
b) Sauerstoff-Nucleophile: Wasser H 2 O => Hydrate
 b) Sauerstoff-Nucleophile: Wasser 2 => ydrate [ - ] [ + ] Basenkatalyse Säurekatalyse - + R 1 + R 2 + 2 + 2 -[ - ] -[ + ] Aldehydhydrat R 1 und/oder R 2 = Ketonhydrat R 1 und R 2 = Gleichgewichtslage:
b) Sauerstoff-Nucleophile: Wasser 2 => ydrate [ - ] [ + ] Basenkatalyse Säurekatalyse - + R 1 + R 2 + 2 + 2 -[ - ] -[ + ] Aldehydhydrat R 1 und/oder R 2 = Ketonhydrat R 1 und R 2 = Gleichgewichtslage:
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Versuchsprotokoll. 1.) Versuch 2a: Quantitative Bestimmung der Atmung
 Versuchsprotokoll 1.) Versuch 2a: Quantitative Bestimmung der Atmung 1.1. Einleitung: Bei der aeroben Atmung, also dem oxidativen Abbau der Kohlenhydrate, entsteht im Citratzyklus und bei der oxidativen
Versuchsprotokoll 1.) Versuch 2a: Quantitative Bestimmung der Atmung 1.1. Einleitung: Bei der aeroben Atmung, also dem oxidativen Abbau der Kohlenhydrate, entsteht im Citratzyklus und bei der oxidativen
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen Chemie Mittelstufe (10 MNG)
 Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Grundwissen hemie Mittelstufe (10 MNG) Marie-Therese-Gymnasium Erlangen Einzeldateien: GW8 Grundwissen für die 8. Jahrgangsstufe GW9 Grundwissen für die 9. Jahrgangsstufe (MNG) GW9a Grundwissen für die
Z 8 EINFÜHRUNG IN DIE ORGANISCHE CHEMIE 1) DEFINITIONEN 2) ELEMENTE UND BINDUNGEN. Organische Chemie. Kunstoffe. Farbstoffe
 EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
EINFÜRUNG IN DIE RGANISCE CEMIE 1) DEFINITINEN Die C beschäftigt sich mit Molekülen, die ein Kohlenstoffgerüst haben. Die Fähigkeit des Kohlenstoffs Einfach-, Zweifach- und Dreifachbindungen (mit seinen
Übungsaufgaben: Alkohole und Aldehyde/Ketone
 Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
Grundwissen Chemie Klasse
 Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
13.1. Struktur der Carbonyl-Gruppe, Prinzipielle Reaktivität
 13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
13. arbonyl -Verbindungen 13.1. Struktur der arbonyl-gruppe, Prinzipielle Reaktivität 13.2. Aldehyde & Ketone 13.2.1 Nomenklatur 13.2.2 Darstellungen xidationen 13.2.3 Reaktionen Additionen an der = Acetale
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Fragen zum Thema funktionelle Gruppen Alkohol und Phenol
 1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
1. Was sind Derivate? 2. Was sind Substituenten? 3. Wann werden neu angehängte Atome oder Gruppen als Substituent bezeichnet? 4. Warum sind Substituenten so wichtig für organische Verbindungen? Alkohol
Einführung in die Biochemie Gärung anaerober Abbau
 Gärungen sind ATP liefernde Energiestoffwechsel, die ohne Sauerstoff als xidationsmittel ablaufen. Ein Grund zur Nutzung der Gärung kann ein plötzlich anstehender Bedarf an rasch verfügbarerer Energie
Gärungen sind ATP liefernde Energiestoffwechsel, die ohne Sauerstoff als xidationsmittel ablaufen. Ein Grund zur Nutzung der Gärung kann ein plötzlich anstehender Bedarf an rasch verfügbarerer Energie
ORGANISCHE CHEMIE TEIL 2 ORGANISCHE SAUERSTOFFVERBINDUNGEN
 KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN Skript rganische Chemie 2 (GF) V2.0 02/14 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole... 02 1.1
KS RGANISCE CEMIE TEIL 2 RGANISCE SAUERSTFFVERBINDUNGEN Skript rganische Chemie 2 (GF) V2.0 02/14 Marc Borer 1 INALTSVERZEICNIS "RGANISCE SAUERSTFFVERBINDUNGEN" 1. Die Stoffgruppe der Alkohole... 02 1.1
Kohlenwasserstoffe. Alkane. Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind.
 2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
2 2 Kohlenwasserstoffe Kohlenwasserstoffe sind brennbare und unpolare Verbindungen, die aus Kohlenstoff- und Wasserstoffatomen aufgebaut sind. 4 4 Alkane Alkane sind gesättigte Kohlenwasserstoffverbindungen
O H H 3 C. Methanol. Molekulargewicht Siedepunkt Löslichkeit in Wasser H 3 C-OH. unbegrenzt H 3 C-Cl. 7.4 g/l H 3 C-CH 3 -24/C -88/C
 Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
Struktur und Eigenschaften 3 C 3 C C 3 105 109 112 Wasser Methanol Dimethylether Vektoraddition der einzelnen Dipolmomente eines Moleküls zum Gesamtdipolmoment Anmerkung zu aktuellen Ereignissen: itrofen
REAKTIONEN DER ORGANISCHEN CHEMIE
 REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
REAKTIONEN DER ORGANISCHEN CHEMIE 1) ÜBERSICHT VON DEN REAKTIONEN AUSGEHEND: Die Reaktion der OC lassen sich auf 4 Grundtypen zurückführen: Grundtyp Addition Substitution Eliminierung Umlagerung allg A
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Versuch: Alkoholtest mit Dichromat. Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz:
 Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Grundkurs Chemie anaerober Abbau aerober Abbau 1977/I 1983/II 1984/IV 1986/IV 1987/II
 Grundkurs Chemie anaerober Abbau aerober Abbau 1977/I 3.2 Beschreiben Sie die Struktur eines Fett-, eines Polysaccharidund eines Proteinmoleküls mit Hilfe einer Strukturformel bzw. eines Strukturformelausschnittes
Grundkurs Chemie anaerober Abbau aerober Abbau 1977/I 3.2 Beschreiben Sie die Struktur eines Fett-, eines Polysaccharidund eines Proteinmoleküls mit Hilfe einer Strukturformel bzw. eines Strukturformelausschnittes
Alkane. homologe Reihe. homologe Reihe der Alkane Nomenklatur. Isomerie. Gesättigte, kettenförmige Kohlenwasserstoffe
 Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
Gesättigte, kettenförmige Kohlenwasserstoffe Alkane gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane : n 2n+2 (n N) Alle Alkane erhalten
a81 a Carbonylverbindungen (I)
 Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Ω Amine können als formale -Substitutionsprodukte des Ammoniaks (Ersatz von -Atomen am Stickstoff durch Alkylgruppen) betrachtet werden.sie sind durch das freie Elektronenpaar am N-Atom, genauso wie Ammoniak,
Einige Aufgaben zu Kohlenhydraten
 Einige Aufgaben zu Kohlenhydraten Manchmal unterscheidet sich die Nummerierung auf dem kopierten Arbeitsblatt und der online-version unter www.laborberufe.de. In der online-version sind häufig am Ende
Einige Aufgaben zu Kohlenhydraten Manchmal unterscheidet sich die Nummerierung auf dem kopierten Arbeitsblatt und der online-version unter www.laborberufe.de. In der online-version sind häufig am Ende
Chemie-Tutorien zur Vorbereitung auf das Praktikum
 Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Seite 1 von 7 LMU Co.Med (Curriculumsoptimierung Medizin) Chemie-Tutorien zur Vorbereitung auf das Praktikum 07.03.-18.03.2017 Dienstag, 07.03.2017 18.00-20.00 Uhr Grundlagen der Chemie I Donnerstag, 09.03.2017
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Aldehyde und Ketone. Aldehyde C 2 H 5 H 3 C. H Propanal Propionaldehyd. H Ethanal Acetaldehyd. H Methanal Formaldehyd. Benzaldehyd.
 Aldehyde und Ketone Aldehyde Methanal Formaldehyd 3 Ethanal Acetaldehyd 2 5 Propanal Propionaldehyd Benzaldehyd Ketone 3 3 2 5 Propanon Aceton 3 2 5 2-Butanon 2 5 3-Pentanon Acetophenon 3 Natürliche Aldehyde
Aldehyde und Ketone Aldehyde Methanal Formaldehyd 3 Ethanal Acetaldehyd 2 5 Propanal Propionaldehyd Benzaldehyd Ketone 3 3 2 5 Propanon Aceton 3 2 5 2-Butanon 2 5 3-Pentanon Acetophenon 3 Natürliche Aldehyde
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
Grundzüge des Energiestoffwechsels I
 Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
Grundzüge des Energiestoffwechsels I 4.5 Grundzüge des Energiestoffwechsels 4.5.2 Glykolyse 4.5.3 Pyruvatdecarboxylierung 4.5.4 Citratzyklus 4.5.5 Glyoxylatzyklus und Gluconeogenese 4.5.6 Atmung, Endoxidation
III. Saure, basische und neutrale Lösungen
 III. Saure, basische und neutrale Lösungen Säure/Base-Reaktionen sind Reaktionen bei denen Protonen ausgetauscht werden. Säuren sind immer Protonendonatoren, d.h. sie geben Protonen ab. So bilden sich
III. Saure, basische und neutrale Lösungen Säure/Base-Reaktionen sind Reaktionen bei denen Protonen ausgetauscht werden. Säuren sind immer Protonendonatoren, d.h. sie geben Protonen ab. So bilden sich
Aufgaben zu Aldehyden und Ketonen
 Aufgaben zu Aldehyden und Ketonen 1. Formulieren Sie jeweils die Reaktionsgleichungen! a) erstellung von Ethanal aus einem Alkanol mit Sauerstoff (mit Ag als Katalysator) b) erstellung von yclohexanon
Aufgaben zu Aldehyden und Ketonen 1. Formulieren Sie jeweils die Reaktionsgleichungen! a) erstellung von Ethanal aus einem Alkanol mit Sauerstoff (mit Ag als Katalysator) b) erstellung von yclohexanon
Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )
![Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 ) Beobachtung [Jeweils] exotherme Reaktion unter Gasentwicklung (H 2 )](/thumbs/74/69784240.jpg) 1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
1 25.01.2006 0.1 Alkohole Alkohole enthalten neben den Elementen C und H auch O. Sie leiten sich aber dennoch von den Kohlenwasserstoffen ab. Beispiel: C 2 H 6 O als Summenformel Strukturformel: C C O
im Molekül eine Dreifachbindung (eine σ-bindung,
 1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
1 14.03.2006 0.1 Grundwissen Alkane Gesättigte Kohlenwasserstoffe, die keine Mehrfachbindungen, sondern nur Einfachbindungen (σ-bindungen) zwischen den Kohlenstoffatomen im Molekül aufweisen. Die allgemeine
Hydrierung von Kohlenmonoxid zu Methanol Kataly?sche Umsetzung von Ethen mit Wasser zu Ethanol
 Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Organische Chemie 10C1. Funktionelle Gruppen 10C2. Homologe Reihe der Alkane 10C3. Nomenklatur der Alkane (gesättigte Kohlenwasserstoffe) 10C4
 Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
Organische Chemie 10C1 Chemie der Kohlenstoffverbindungen (C und v.a. H, N, O, S) C-Atome immer vierbindig Funktionelle Gruppen 10C2 Alkan: nur Einfachbindungen Alken: mindestens eine Doppelbindung Alkin:
LÖSUNGEN DER AUFGABEN ZUM 5. PRAKTIKUM
 LÖUNGEN DER AUFGABEN ZUM 5. PRAKTIKUM 1. Elektrophile und nukleophile Teilchen Elektrophile Teilchen: Es handelt sich um Elektronenpaarakzeptoren, also LEWI-äuren. Beispiele sind: +, Br +, I +, BF3, All3,
LÖUNGEN DER AUFGABEN ZUM 5. PRAKTIKUM 1. Elektrophile und nukleophile Teilchen Elektrophile Teilchen: Es handelt sich um Elektronenpaarakzeptoren, also LEWI-äuren. Beispiele sind: +, Br +, I +, BF3, All3,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Autotrophe und heterotrophe Organismen
 Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
Grundlagen der Umwelttechnik 5. Biomoleküle und Grundlagen des Stoffwechsels Vorlesung an der ochschule Augsburg Dr. Siegfried Kreibe 1 Autotrophe und heterotrophe rganismen Autotrophe rganismen: bauen
1.9. Aldehyde und Ketone (Carbonylverbindungen)
 1.9. Aldehyde und Ketone (arbonylverbindungen) omenklatur: achsilbe al on Funktionelle Gruppe arbonylgruppe xogruppe Aldehyd Alkohol dehydrogenatus Keton xidationsstufe II 3 3 3 2 3 3 Methanal Formaldehyd
1.9. Aldehyde und Ketone (arbonylverbindungen) omenklatur: achsilbe al on Funktionelle Gruppe arbonylgruppe xogruppe Aldehyd Alkohol dehydrogenatus Keton xidationsstufe II 3 3 3 2 3 3 Methanal Formaldehyd
α- und β- Glucose können sich ineinander umwandeln
 Die Reaktionen der Zucker Zuckermoleküle können in verschiedenen Formen auftreten Zuckermoleküle zeigen, da sie in verschiedenen Formen auftreten können, ungewöhnliche Eigenschaften. Da diese auch für
Die Reaktionen der Zucker Zuckermoleküle können in verschiedenen Formen auftreten Zuckermoleküle zeigen, da sie in verschiedenen Formen auftreten können, ungewöhnliche Eigenschaften. Da diese auch für
Grundwissen der 10.Klasse NTG
 Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Grundwissen der 10.Klasse NTG 1. Kohlenwasserstoffe 1.1 Alkane 1.1.1 Organische Stoffe = Verbindungen, die Kohlenstoffatome enthalten Ausnahme: Kohlenstoffoxide, Kohlensäure, Carbonate 1.1.2 Kohlenwasserstoffe
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Grundwissen: Chemie für Biologen (Sek II)
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Grundwissen: Chemie für Biologen (Sek II) Das komplette Material finden Sie hier: School-Scout.de Titel: Grundwissen: Chemie für Biologen
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Grundwissen: Chemie für Biologen (Sek II) Das komplette Material finden Sie hier: School-Scout.de Titel: Grundwissen: Chemie für Biologen
Organische Chemie. Kohlenwasserstoffe. Alkane. Alkane
 1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
1 1 Organische Chemie beschäftigt sich mit Verbindungen, die C- Atome enthalten 2 2 Kohlenwasserstoffe bestehen ausschließlich aus C- und H- Atomen 3 3 es existieren nur C-H Einfachbindungen C-C Einfachbindung
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
Alkoholische Gärung von Zuckern
 KantonsSchuleOlten Fachschaft Chemie Alkoholische Gärung von Zuckern Aufgabe: Jede Gruppe führt die Gärungsversuche mit einer Zuckerart (Glucose, Fructose, Maltose, Saccharose oder Lactose) durch. Die
KantonsSchuleOlten Fachschaft Chemie Alkoholische Gärung von Zuckern Aufgabe: Jede Gruppe führt die Gärungsversuche mit einer Zuckerart (Glucose, Fructose, Maltose, Saccharose oder Lactose) durch. Die
c) Gleichzeitiger Bruch der C-X-Bindung und der C-H-Bindung
 Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Eliminierungen Das Nucleophil mit seinem freien Elektronenpaar muß nicht am Kohlenstoffatom der C-- Bindung angreifen, es kann auch am nächsten Kohlenstoffatom ein Proton abstrahieren und somit als Base
Bioenergetik. Technische Universität Ilmenau, FG Nanotechnologie. Zentrum für Mikro- und Nanotechnologien
 Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
Bioenergetik Quellen: 1. Physiologie des Menschen (mit Pathophysiologie) R.F. Schmidt, F. Lang, G. Thews, 29. Auflage Springer Medizin Verlag Heidelberg (2005), ISBN 3-540-21882-3. 2. www.cg.bnv bamberg.de/t3/fileadmin/images/fachbereiche/biologie/dateien/kh-abbau.ppt
Pentosephosphatzyklus. Synonym: Hexosemonophosphatweg
 Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Pentosephosphatzyklus Synonym: Hexosemonophosphatweg Gliederung Funktion & Lokalisation Grundgerüst des Ablaufs Anpassung an Stoffwechselsituation Regelung Beispielreaktion Funktion & Lokalisation Gewinnung
Molekülstruktur und Stoffeigenschaften
 10.Klasse Chemie Grundwissen OlympiaMorataGymnasium Schweinfurt Molekülstruktur und Stoffeigenschaften Räumlicher Bau von Molekülen Möglicher Molekülbau: tetraedrisch; trigonalpyrimidal; gewinkelt; linear;
10.Klasse Chemie Grundwissen OlympiaMorataGymnasium Schweinfurt Molekülstruktur und Stoffeigenschaften Räumlicher Bau von Molekülen Möglicher Molekülbau: tetraedrisch; trigonalpyrimidal; gewinkelt; linear;
Orbital. Atombindung, Bindung. Elektronegativität. Dipol
 GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
GW Chemie 10. SG GA rbital aum, in dem sich Elektronen mit 99%iger Wahrscheinlichkeit aufhalten; in einem rbital halten sich maximal 2 Elektronen auf; man unterscheidet Atom- und Molekülorbitale Atombindung,
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Vorlesung Chemie für Mediziner: Formeln OC
 Vorlesung hemie für Mediziner: Formeln In diesem Dokument sind die wichtigsten Formeln der Vorlesung zusammengestellt, die man für die Klausur kennen sollte. Die Zusammenstellung erhebt keinen Anspruch
Vorlesung hemie für Mediziner: Formeln In diesem Dokument sind die wichtigsten Formeln der Vorlesung zusammengestellt, die man für die Klausur kennen sollte. Die Zusammenstellung erhebt keinen Anspruch
Grundlagen der Physiologie
 Grundlagen der Physiologie Gärungen und anaerobe Atmungsprozesse www.icbm.de/pmbio Glykolyse C 6 H 12 O 6 2 C 3 H 4 O 3 + 4 [H] (+ 2 ATP) Entsorgung überschüssiger Reduktionsequivalente durch Übertragung
Grundlagen der Physiologie Gärungen und anaerobe Atmungsprozesse www.icbm.de/pmbio Glykolyse C 6 H 12 O 6 2 C 3 H 4 O 3 + 4 [H] (+ 2 ATP) Entsorgung überschüssiger Reduktionsequivalente durch Übertragung
Organische Chemie für Biologen und Nebenfächler Übungsaufgaben für die Klausur
 rganische Chemie für Biologen und Nebenfächler Übungsaufgaben für die Klausur Aufgabe 1: Sie wollen Fettflecken von ihrem Kleidungsstück entfernen. Man gibt Ihnen als Fleckenentferner folgende Chemikalien
rganische Chemie für Biologen und Nebenfächler Übungsaufgaben für die Klausur Aufgabe 1: Sie wollen Fettflecken von ihrem Kleidungsstück entfernen. Man gibt Ihnen als Fleckenentferner folgende Chemikalien
Zugrunde gelegt wird ein Chemie-Unterricht mit zwei Wochenstunden. September. Oktober
 Vorschlag für einen Jahresplan Chemie-Unterricht im fünften Jahr mit dem Unterrichtswerk PRISMA Zugrunde gelegt wird ein Chemie-Unterricht mit zwei Wochenstunden Monat September Oktober Chemische Bindungen
Vorschlag für einen Jahresplan Chemie-Unterricht im fünften Jahr mit dem Unterrichtswerk PRISMA Zugrunde gelegt wird ein Chemie-Unterricht mit zwei Wochenstunden Monat September Oktober Chemische Bindungen
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Biochemie/Monosaccharide1. Kohlenhydrate:
 Biochemie/Monosaccharide1 Kohlenhydrate: Unter Kohlenhydraten versteht man Stoffe, deren Moleküle neben Kohlenstoff die Elemente Wasserstoff und Sauerstoff im Verhältnis 2:1 enthalten. Zu den Kohlenhydraten
Biochemie/Monosaccharide1 Kohlenhydrate: Unter Kohlenhydraten versteht man Stoffe, deren Moleküle neben Kohlenstoff die Elemente Wasserstoff und Sauerstoff im Verhältnis 2:1 enthalten. Zu den Kohlenhydraten
Vom Alkohol zum Oxidationsprodukte der Alkohole
 Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Vom Alkohol zum xidationsprodukte der Alkohole Wiederholung: Alkohole und Aldehyde sind wichtige organische Stoffklassen. Sie spielen sowohl in der organischen hemie, als auch im Alltag eine wichtige Rolle.
Kohlenhydrate Einleitung
 Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
Einleitung Kohlenhydrate (Saccharide) sind Polyhydroxycarbonyl-Verbindungen, die neben Kohlenstoff noch Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 enthalten. Der Begriff Kohlenhydrate ist
P Station 1: Darstellung der Carbonsäuren
 P Station 1: Darstellung der Carbonsäuren Carbonsäuren lassen sich durch Oxidation der entsprechenden Aldehyde darstellen. Die Oxidation der Aldehyde kann in einem Versuch mit heißem Kupferoxid im Abzug
P Station 1: Darstellung der Carbonsäuren Carbonsäuren lassen sich durch Oxidation der entsprechenden Aldehyde darstellen. Die Oxidation der Aldehyde kann in einem Versuch mit heißem Kupferoxid im Abzug
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Chemie der Kohlenwasserstoffe
 hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
hemie der Kohlenwasserstoffe Alkane Gesättigte, kettenförmige Kohlenwasserstoffe gesättigt = nur Einfachbindungen kettenförmig = keine inge Kohlenwasserstoff = nur - und -Atome Summenformel der Alkane
Aldehyde und Ketone Carbonylverbindungen
 Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Aldehyde und Ketone Carbonylverbindungen Prof. Dr. Ivo C. Ivanov 1 Prof. Dr. Ivo C. Ivanov 2 Die Siedepunkte liegen höher als bei den jeweils zugrundeliegenden Alkanen, eine Folge des polaren Charakters
Prüfungsvorbereitung organische Chemie
 Prüfungsvorbereitung organische hemie 2L Alle diese Aufgaben lehnen sich an Aufgaben zur gestreckten Abschlussprüfung für hemielaboranten Teil 1 an. Sie sind jedoch umformuliert und von den Stoffsystemen/Zahlenwerten
Prüfungsvorbereitung organische hemie 2L Alle diese Aufgaben lehnen sich an Aufgaben zur gestreckten Abschlussprüfung für hemielaboranten Teil 1 an. Sie sind jedoch umformuliert und von den Stoffsystemen/Zahlenwerten
b) Zeichnen Sie die beiden möglichen Isomere der Aldol-Kondensation und bezeichnen Sie die Stereochemie der Produkte.
 1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
1. Aufgabe a) Formulieren Sie den Mechanismus der durch ydroxid-ionen katalysierten Aldol- Addition und Aldol-Kondensation zwischen den beiden unten gezeigten Molekülen. + 2 2 b) Zeichnen Sie die beiden
Kapitel 9. Reaktionen von Carbonylverbindungen
 Kapitel 9 Reaktionen von Carbonylverbindungen Die Struktur der Carbonylgruppe Eine der wichtigsten funktionellen Gruppen überhaupt, besonders in Biologie und Medizin alle wichtigen Naturstoffklassen weisen
Kapitel 9 Reaktionen von Carbonylverbindungen Die Struktur der Carbonylgruppe Eine der wichtigsten funktionellen Gruppen überhaupt, besonders in Biologie und Medizin alle wichtigen Naturstoffklassen weisen
Kohlenhydrate. spielen in der Natur eine sehr wichtige Rolle. dienen als Energiespeicher: Stärke, Glykogen
 Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Kohlenhydrate spielen in der Natur eine sehr wichtige Rolle dienen als Energiespeicher: Stärke, Glykogen sind Bestandteile von DNA bzw. RNA, Zellwänden,... gebunden an Proteine und Lipide Einteilung der
Stoffverteilungsplan
 Stoffverteilungsplan für Chemie Klasse 10 in Bayern für sprachliche, humanistische, musische, Wirtschafts- und sozialwissenschaftliche Gymnasien 934.339 für das 8-jährige Gymnasium C 10.1 Molekülstruktur
Stoffverteilungsplan für Chemie Klasse 10 in Bayern für sprachliche, humanistische, musische, Wirtschafts- und sozialwissenschaftliche Gymnasien 934.339 für das 8-jährige Gymnasium C 10.1 Molekülstruktur
Klausur zur Vorlesung "Grundzüge der Chemie" für Studierende des Maschinenbaus BITTE AUSFÜLLEN BITTE HALTEN SIE IHREN STUDENTAUSWEIS BEREIT
 1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
1 PUNKTZAL NTE Klausur zur Vorlesung "Grundzüge der hemie" für Studierende des Maschinenbaus Termin: 17. Juni 2003 rt: Z 10 Zeit: 9.30-11.30 Uhr Dauer: 120 Minuten BITTE AUSFÜLLEN BITTE ALTEN SIE IREN
Fakultät Mathematik und Naturwissenschaften, Anorganische Chemie Professur AC I. Seminar zum Brückenkurs 2016 TU Dresden, 2017 Folie 1
 Seminar zum Brückenkurs 2016 TU Dresden, 2017 Folie 1 Seminar zum Brückenkurs Chemie 2017 Chemische Bindung, Molekülbau, Stöchiometrie Dr. Jürgen Getzschmann Dresden, 19.09.2017 Zeichnen von Valenzstrichformeln
Seminar zum Brückenkurs 2016 TU Dresden, 2017 Folie 1 Seminar zum Brückenkurs Chemie 2017 Chemische Bindung, Molekülbau, Stöchiometrie Dr. Jürgen Getzschmann Dresden, 19.09.2017 Zeichnen von Valenzstrichformeln
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
a) Vervollständigen Sie das Freie-Enthalpie-Diagramm der Reaktion, indem Sie den zutreffenden Buchstaben A D in die leeren Kreise setzen:
 1. Aufgabe Für die Reaktion R-X + u R-u + X findet man folgendes Reaktionsdiagramm: a) Vervollständigen Sie das Freie-Enthalpie-Diagramm der Reaktion, indem Sie den zutreffenden Buchstaben A D in die leeren
1. Aufgabe Für die Reaktion R-X + u R-u + X findet man folgendes Reaktionsdiagramm: a) Vervollständigen Sie das Freie-Enthalpie-Diagramm der Reaktion, indem Sie den zutreffenden Buchstaben A D in die leeren
Chemische Bindung, Molekülbau, Stöchiometrie
 Seminar zum Brückenkurs Chemie 2016 Chemische Bindung, Molekülbau, Stöchiometrie Dr. Jürgen Getzschmann Dresden, 20.09.2016 Zeichnen von Valenzstrichformeln 1. Zeichnen Sie die Strukturformeln der folgenden
Seminar zum Brückenkurs Chemie 2016 Chemische Bindung, Molekülbau, Stöchiometrie Dr. Jürgen Getzschmann Dresden, 20.09.2016 Zeichnen von Valenzstrichformeln 1. Zeichnen Sie die Strukturformeln der folgenden
Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 Carbonylgruppen und eine C=C Doppelbindung.
 rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
rganische hemie I Lösungen zur Übung 23 Aufgabe 1 Funktionelle Gruppen: Progesteron hat 2 arbonylgruppen und eine = Doppelbindung. 3 () 3 3 Progesteron Das Molekül hat 6 hiralitätszentren (mit * bezeichnet).
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Multiple Choice Fragen zum Üben Organische Chemie (J. Fuhrhop / B. Kirste)
 1 Multiple Choice Fragen zum Üben rganische Chemie (J. Fuhrhop / B. Kirste) 1) Mit Ausnahme der Kohlensäure und mancher ihrer Derivate sind alle organischen Verbindungen verbrennbar. 2) Biologische Zellen
1 Multiple Choice Fragen zum Üben rganische Chemie (J. Fuhrhop / B. Kirste) 1) Mit Ausnahme der Kohlensäure und mancher ihrer Derivate sind alle organischen Verbindungen verbrennbar. 2) Biologische Zellen
Aufstellen von Redoxgleichungen
 Aufstellen von Redoxgleichungen Mit Tabellenbuch (Küster-Thiel, 105. Auflage) Formulieren Sie jeweils getrennt die Reduktion und die xidation. Bilden Sie dann die Redoxreaktion. 1. In alkalischer Lösung
Aufstellen von Redoxgleichungen Mit Tabellenbuch (Küster-Thiel, 105. Auflage) Formulieren Sie jeweils getrennt die Reduktion und die xidation. Bilden Sie dann die Redoxreaktion. 1. In alkalischer Lösung
Kohlenwasserstoffe. Homologe Reihe. Alkane. Alkene. HGA-Grundwissen Chemie-10. Klasse NTG
 GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
GA-Grundwissen Chemie-10. Klasse NTG Kohlenwasserstoffe Sind eine Stoffgruppe von chemischen Verbindungen, die nur aus C- und - Atomen bestehen. Aufgrund des unpolaren Molekülbaus sind sie lipophil und
Angelika Stöcklinger. Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate
 Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Angelika Stöcklinger Molekulare Biologie und Biochemie Teil 7: Kohlenhydrate Kohlenhydrate und das Immunsystem z.b. Mannosen Bindungspartner für Lektine Mannose Aufnahme von Pathogenen Dendritische Zelle
Die Abbildung auf dieser ersten Folie mag Erinnerungen an das Weihnachtsessen aufkommen lassen.
 Die Abbildung auf dieser ersten Folie mag Erinnerungen an das Weihnachtsessen aufkommen lassen. Da Landwirtschaft und Ernährung eng zusammenhängen, sollten wir uns für die chemischen Grundlagen dessen
Die Abbildung auf dieser ersten Folie mag Erinnerungen an das Weihnachtsessen aufkommen lassen. Da Landwirtschaft und Ernährung eng zusammenhängen, sollten wir uns für die chemischen Grundlagen dessen
