1) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P)
|
|
|
- Regina Fischer
- vor 7 Jahren
- Abrufe
Transkript
1 1. Klausur zum Modul 5.3 Biochemie WS 09/ ) Erklären sie die Begriffe Primär Sekundär und Tertiärstruktur von Proteinen. Nennen Sie drei typische Sekundärstrukturelemente (6P) 2) Welche Funktion hat das Protein PDI bei der Proteinfaltung? (2P) 3) Was ist der Unterschied zwischen integralen und peripheren Membranproteinen? (2P) 4) Geben Sie für die folgenden Kofaktoren den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (8P) TPP CoA Fe S Cluster 5) Die Erzeugung von metabolischer Energie aus Glukose besteht aus der Glykolyse, dem Citrat Zyklus und der Oxidativen Phosphorylierung. Beschreiben Sie: a) Welche Reaktionen laufen grob in den drei Teilschritten ab? (6P) b) Wo sind die drei Bereiche in einer Säugetierzelle lokalisiert? (3P) c) Welche dieser Reaktionen laufen in Abwesenheit von Sauerstoff ab? Wie stark verändert sich dabei die Menge an produziertem ATP? (4P) d) Wie sind Sauerstoffverbrauch und ATP Synthese miteinander verbunden? (3P) 6) Unter welchen Bedingungen wird die Glukoneogenese aktiviert? Welche Reaktionen der Glykolyse werden dabei umgangen? (6P) 7) Bescheiben Sie die Vorgänge im Umfeld der Replikationsgabel im Zuge der DNA Replikation. (10P) 8) Zusatzaufgabe: Sie füttern einer Zellkultur 2 Ketoglutarat, das an Position 2 14 C markiert ist. Nach längerer Inkubation isolieren Sie die Proteine und zerlegen sie in die einzelnen Aminosäuren. Welche Aminosäuren finden Sie in radioaktiver Form vor und wie kommt das 14 C in die jeweilige Aminosäure? Beachten Sie, daß 2 Ketosäuren reversibel durch die sogenannte Transaminase Reaktion in die entsprechende 2 Aminosäure umgewandelt werden können. (8P) 1
2 2. Klausur zum Modul 5.3 Biochemie WS 09/ ) Was ist eine Proteindomäne, was ist ein Proteinmotif? Nennen Sie je drei typische Beispiele (8P) 2) Welche Funktion haben die Heat shock Proteine HSP70 und HSP60/HSP10 bei der Proteinfaltung? Erläutern Sie kurz den jeweiligen Wirkmechanismus. (6P) 4) Geben Sie für die folgenden Kofaktoren den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (10P) PLP Fe S Cluster 5) Beschreiben Sie die Reaktion, die durch den Pyruvat Dehydrogenase Komplex katalysiert wird. Zerlegen Sie die Reaktion in Einzelschritte E1 bis E3 und benennen Sie die Kofaktoren, die für jeden Einzelschritt benötigt werden. (6P) 6) Wo sind folgende Reaktionswege in einer eukaryontischen Zelle lokalisiert? (6P) Glykolyse Gluconeogenese Citrat Cyclus Glyoxalat Cyclus Pentosephosphat Weg Atmungskette 7) Wie funktioniert die Polymerase Kettenreaktion (PCR)? Welche Eigenschaft der Polymerase macht die PCR überhaupt erst möglich? (5P) 8) Durch welche Mechanismen erreicht die DNA Replikation ihre niedrige Fehlerrate? (5P) 9) Zusatzaufgabe: Sie füttern einer Zellkultur Oxaloacetat, das an Position 2 14 C markiert ist. Nach längerer Inkubation homogenisieren Sie die Zellkultur und zerlegen sie in Protein, Kohlenhydrate, Lipide und Nukleinsäuren. Welche dieser Verbindungsklassen enthalten Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung? Beachten Sie, daß 2 Ketosäuren reversibel durch die sogenannte Transaminase Reaktion in die entsprechende 2 Aminosäure umgewandelt werden können. (8P) 2
3 1. Klausur zum Modul 5.3 Biochemie WS 2010/ Name: Matrikelnummer: 1) Was sind Primär, Sekundär und Tertiärstruktur eines Proteins? (3P) 2) Beschreiben Sie die Vorgänge bei der Faltung eines Proteins in seine aktive Konformation. Welche Funktion haben dabei die Heat shock Proteine HSP70 und HSP60/HSP10? (6P) 4) Geben Sie für die folgenden Kofaktoren den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (5P) TPP Fe S Cluster 5) Zeichnen Sie Zitrat Zyklus auf (Nur Reaktanden, 4P) Ordnen Sie die Einzelreaktionen den EC Klassen zu (Oxidoreduktasen, Transferasen, Hydrolasen, Synthasen/Lyasen, Isomerasen, Synthetasen) (4P). Wie ist der Zyklus mit der oxidativen Phosphorylierung verbunden? (3P)? Welche Zusatzreaktionen benötigen Pflanzen, die aus Acetyl CoA Zucker aufbauen, und wie heißt der resultierende Reaktionsweg? (3P). 6) Wo sind folgende Reaktionswege in einer eukaryontischen Zelle lokalisiert? (6P) Glykolyse Gluconeogenese Citrat Cyclus ATP Synthese Pentosephosphat Weg Atmungskette 7) Wie funktioniert die Polymerase Kettenreaktion (PCR)? Welche Eigenschaft der Polymerase macht die PCR überhaupt erst möglich? (5P) 8) Beschreiben Sie die Vorgänge, die sich bei der DNA Replikation an der Replikationsgabel abspielen (8P) 9) Beim Öffnen einer Ampulle mit 14 C markiertem Bariumcarbonat atmen Sie versehentlich freigesetztes CO2 ein.. In welcher der wichtigsten Verbindungsklassen Protein, Kohlenhydrate, Lipide und Nukleinsäuren ihres Körpers finden Sie Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung? Beachten Sie, daß 2 Ketosäuren reversibel durch die sogenannte Transaminase Reaktion in die entsprechende 2 Aminosäure umgewandelt werden können. Welche Resultate liefert die gleiche Analyse in ihrer gleichfalls markierten Laborpflanze? (8P) 3
4 2. Klausur zum Modul 5.3 Biochemie WS 2010/ Name: Matrikelnummer: Was versteht man unter integralen und peripheren Membranproteinen? Wie können integrale Membranproteine in der Membran verankert werden? (3P) 2) Erläutern Sie anhand der Hexokinase das Prinzip des Induced fit Mechanismus in einer enzymatischen Reaktion. Welchen Vorteil bietet dieser Mechanismus für die Kinasereaktion? (6P) 4) Geben Sie für die folgenden Kofaktoren den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (5P) TPP Fe S Cluster 5) Zeichnen Sie den Stoffwechselweg der Glykolyse auf (Reaktanden einschließlich der Kofaktoren/Kosubstrate) (4P). Ordnen Sie die Einzelreaktionen den EC Klassen zu (Oxidoreduktasen, Transferasen, Hydrolasen, Synthasen/Lyasen, Isomerasen, Synthetasen) (4P). Welches sind die wichtigen allosterisch regulierten Schritte (3P)? Welche Zusatzreaktionen werden für die Umkehrung des Weges benötigt und wie heißt der resultierende Reaktionsweg? (3P). 6) In welchem Organell/Kompartiment sind folgende Funktionen oder Stoffwechselwege in einer eukaryontischen Zelle lokalisiert? (6P) Glykolyse DNA Replikation Citrat Cyclus Protein Abbau Speicherung von Neutrallipiden Atmungskette 7) Wie funktioniert die Polymerase Kettenreaktion (PCR)? Welche Eigenschaft der Polymerase macht die PCR überhaupt erst möglich? (5P) 8) Beschreiben Sie die Vorgänge, die sich bei der DNA Replikation an der Replikationsgabel abspielen (8P) 4
5 9) Zusatzaufgabe: Sie füttern einer Leberzellkultur Oxaloacetat, das an Position 2 14 C markiert ist. Nach längerer Inkubation homogenisieren Sie die Zellkultur und zerlegen sie in Protein, Kohlenhydrate, Lipide und Nukleinsäuren. Welche dieser Verbindungsklassen enthalten Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung (Schematische Angabe des Reaktionsweges)? Beachten Sie, daß 2 Ketosäuren reversibel durch die sogenannte Transaminase Reaktion in die entsprechende 2 Aminosäure umgewandelt werden können. (8P) 5
6 1. Klausur zum Modul 5.3 Biochemie WS 11/ ) Was ist eine Proteindomäne, was ist ein Proteinmotif? Nennen Sie je zwei typische Beispiele (6P) 2) Wie konnte Anfinsen zeigen, dass die Information für die korrekte Faltung eines Proteins in der Primärsequenz enthalten ist? (3P). Nennen Sie drei Proteine, die in der Säuger Zelle die Faltung unterstützen und beschreiben Sie kurz deren Funktion. (3P) 4) Geben Sie für die folgenden Kofaktoren den jeweiligen Typ der Reaktion, an der sie beteiligt sind, an und nennen Sie je ein Beispielenzym (10P) PLP Fe S Cluster 5) Beschreiben Sie den Ablauf der Glykolyse von der Glukose bis zum Pyruvat (Verbindungsnamen ohne Strukturformel, Namen der beteiligten Enzyme) (10P). Geben Sie für jedes Enzym die EC Klasse an (Oxidoreduktasen, Transferasen, Hydrolasen, Lyasen/Synthasen, Isomerasen, Ligasen/Synthetasen) (5P). 6) Beschreiben Sie anhand je eines Beispiels die Regulation eines Stoffwechselweges durch Feed Forward Stimulation und durch Feed Back Inhibition. 7) Beschreiben Sie die Vorgänge bei der Replikation bakterieller DNA (Zeichnung!) (8P) 8) Durch welche Mechanismen erreicht die DNA Replikation ihre niedrige Fehlerrate? (4P) 9) Zusatzaufgabe: Sie füttern einer Zellkultur Glutamat, das an Position 2 14 C markiert ist. Nach längerer Inkubation homogenisieren Sie die Zellkultur und zerlegen sie in Protein, Kohlenhydrate, Lipide und Nukleinsäuren. Welche dieser Verbindungsklassen enthalten Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung? Beachten Sie, daß 2 Ketosäuren reversibel durch die sogenannte Transaminase Reaktion in die entsprechende 2 Aminosäure umgewandelt werden können. (4P) 6
7 2. Klausur zum Modul 5.3 Biochemie WS 11/ Name: Matrikelnummer: Was versteht man unter integralen und peripheren Membranproteinen? Wie können integrale Membranproteine in der Membran verankert werden? (4P) 2) Erläutern Sie anhand der Hexokinase das Prinzip des Induced fit Mechanismus in einer enzymatischen Reaktion. Welchen Vorteil bietet dieser Mechanismus für die Kinasereaktion? (3P) 3) In welchem Stoffwechselweg spielt das Enzym Rubisco eine Schlüsselrolle (2P) Wie ist dieser Weg mit der Gluconeogenese verknüpft? (2P) 4) Geben Sie für die folgenden Kofaktoren den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (10P) TPP CoA Pyridoxalphosphat 5) Zeichnen Sie den Zitrat Zyklus auf (Namen und Strukturformeln der Reaktanden, Namen der Enzyme, 12P). Wie ist der Zyklus mit der oxidativen Phosphorylierung verbunden? (2P)? Welche Zusatzreaktionen benötigen Pflanzen, die aus Acetyl CoA Zucker aufbauen, und wie heißt der resultierende Reaktionsweg? (3P). 6) Beschreiben Sie Struktur und Funktion der mitochondrialen ATP Synthase (4P). Wie kann man die Funktion anschaulich in einem Experiment demonstrieren? (2P) 7) Beschreiben Sie anhand einer Zeichnung die Vorgänge im Umfeld der Replikationsgabel im Zuge der DNA Replikation. (8P) 8) Was sind Telomere? (2P) Was haben Telomerasen mit der Entstehung von Krebs zu tun? (2P) 9) Zusatzaufgabe: Beim Öffnen einer Ampulle mit 14 C markiertem Bariumcarbonat atmen Sie versehentlich freigesetztes CO 2 ein. In welcher der wichtigsten Verbindungsklassen Protein, Kohlenhydrate, Lipide und Nukleinsäuren ihres Körpers finden Sie Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung? Beachten Sie, daß 2 Ketosäuren reversibel durch die sogenannte Transaminase Reaktion in die entsprechende 2 Aminosäure umgewandelt werden können. (4P) 7
8 1. Klausur zum Modul 5.3 Biochemie WS 2012/ Name: Matrikelnummer: 1) Was sind Primär, Sekundär und Tertiärstruktur eines Proteins? (3P) 2) Wie können Sie experimentell integrale und periphere Membranproteine unterscheiden (2P)? Nennen Sie drei Typen von Membranverankerungen integraler Membranproteine (3P). 4) Geben Sie für die folgenden Kofaktoren/prosthetischen Gruppen den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (5P) NADH CoA Häm TPP 5) Zeichnen Sie den Zitrat Zyklus auf (Substrate, Produkte, Cofaktoren, Enzyme, 12P) Ordnen Sie die Einzelreaktionen den EC Klassen zu (Oxidoreduktasen, Transferasen, Hydrolasen, Synthasen/Lyasen, Isomerasen, Synthetasen) (4P). Welche Zusatzreaktionen benötigen Pflanzen, die aus Acetyl CoA Zucker aufbauen, und wie heißt der resultierende Reaktionsweg? (2P). 6) Wo sind folgende Reaktionswege in einer eukaryontischen Zelle lokalisiert? (6P) Glykolyse Gluconeogenese Citrat Cyclus ATP Synthese Pentosephosphat Weg Proteinbiosynthese 7) Sie führen die aerobe Verstoffwechselung von Glucose in Gegenwart von 18 O 2 als Marker durch. In welchem Hauptprodukt finden Sie den markierten Sauerstoff? (1P) Begründung? (2P) 8) Beschreiben Sie die Vorgänge, die sich bei der bakteriellen DNA Replikation an der Replikationsgabel abspielen (8P) 9) Sie inkubieren Leberzellen für eine Stunde mit Alanin, das an Position 1 mit 14 C markiert ist. In welcher der wichtigsten Verbindungsklassen Protein, Kohlenhydrate, Lipide und Nukleinsäuren dieser Zellen finden Sie Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung? (4P) 8
9 2. Klausur zum Modul 5.3 Biochemie WS 2012/ Name: Matrikelnummer: 1) Beschreiben Sie Anfinsens Experiment, mit dem er bewies, dass die Primärsequenz eine Proteins die Tertiärstruktur bestimmt. Warum war die Wahl des "richtigen" Proteins entscheidend für das Gelingen des Experiments? (8P) 2) Was versteht man in der Enzymologie unter Feed Forward Stimulation und Feed Back Inhibition? (4P) Nennen Sie je ein Beispiel (2P). 4) Geben Sie für die folgenden Kofaktoren/prosthetischen Gruppen den jeweiligen Typ der Reaktion an, an der sie beteiligt sind und nennen Sie je ein Beispielenzym (5P) Pyridoxalphosphat Fe S cluster Liponsäure 5) Zeichnen Sie den Stoffwechselweg zum anaeroben Abbau von Glukose in Hefe auf (Substrate, Produkte, Cofaktoren, Enzyme, 14P). Ordnen Sie die Einzelreaktionen den EC Klassen zu (Oxidoreduktasen, Transferasen, Hydrolasen, Synthasen/Lyasen, Isomerasen, Synthetasen) (4P). Nennen Sie zwei wichtige Regulationspunkte und mindesten 4 allosterisch wirksame Regulatoren (6P) 6) Wo sind folgende Reaktionswege in einer eukaryotischen Zelle lokalisiert? (6P) ATP Synthase Proteinabbau Citrat Cyclus Peroxidase Reaktonen DNA Replikation Proteinbiosynthese 7) Glyceraldehyd 3 Phosphatdehydrogenase lässt sich durch 2 Iodessigsäureamid hemmen. Begründen Sie dies anhand des Reaktionsmechanismus? (3P) Dasselbe Enzym spielt eine wichtige Rolle bei als Angriffspunkt der Vergiftung mit Arsenaten. Beschreiben Sie einen möglichen Mechanismus. (2P) 8) Beschreiben Sie die Vorgänge, die sich bei der bakteriellen DNA Replikation an der Replikationsgabel abspielen (8P) 9
10 9) Sie inkubieren Leberzellen für eine Stunde mit Alanin, das an Position 2 mit 14 C markiert ist. In welcher der wichtigsten Verbindungsklassen Protein, Kohlenhydrate, Lipide und Nukleinsäuren dieser Zellen finden Sie Radioaktivität und wie kommt das 14 C in die jeweilige Verbindung? (4P) Zusatzaufgabe: Beim Auftrag der initialen Reaktionsgeschwindigkeit V gegen die Substratkonzentration S einer enzymatisch katalysierten Reaktion erhalten Sie den abgebildeten Graphen. Wie kann es dazu kommen? Lässt sich der Effekt sinnvoll nutzen? Kennen Sie ein Beispiel? (4P) 10
Klausur zur Vorlesung Biochemie I im WS 1993/1994. am 18. Februar Nachklausur zur Vorlesung Biochemie I im WS 1993/1994. am 30. Mai 1994.
 Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Biochemie 1, WS 93 http://www.uni-kl.de/fb-biologie/fs/klausur/chemie/biochem/bc1ws93.htm 1 von 2 17.07.01 20:50 Klausur zur Vorlesung Biochemie I im WS 1993/1994 am 18. Februar 1994 1 (16 Punkte) Formulieren
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur ( )
 Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Grundlagen der Biochemie (BCh 5.3) Prof. Dr. Christoph Thiele WS 2014/15 1. Klausur (6.2.2015) Aufgabe 1: Erläutern Sie die Primär-, Sekundär- und die Tertiärstruktur von Proteinen. [3 P] Aufgabe 2: Erklären
Klausur zur Vorlesung Biochemie I im WS 2001/02
 (insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
(insgesamt 100 Punkte, mindestens 40 erforderlich) Klausur zur Vorlesung Biochemie I im WS 2001/02 am 18.02.2002 von 08.15 09.45 Uhr Gebäude 52, Raum 207 Bitte Namen, Matrikelnummer und Studienfach unbedingt
Was bisher geschah 1
 Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Was bisher geschah 1 Zellatmung (Übersicht) Der Citratcyclus ist die erste Stufe der Zellatmung 2 Citratzyklus Synonyme: Tricarbonsäurezyklus (TCA-Zyklus) Krebszyklus, Zitronensäurezyklus Der Zyklus ist
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8,
Johann Wolfgang Goethe-Universität Frankfurt am Main
 Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Teilklausur Biochemie Studiengang Biowissenschaften Modul BSc-Biowiss-7 Studiengang Bioinformatik Modul BSc-Bioinf-8.Studiengang
Um welches Molekül handelt es sich? Was ist dessen Funktion? Benennen Sie die funktionellen Gruppen. (2)
 Prüfungsfragen Biochemie; Teil Schroeder Ad Einheit 1 Vergleichen Sie die Stärke von molekularen Wechselwirkungen in kj/mol. In welcher Größenordnung ist der Abstand dieser Wechselwirkungen? Im Vergleich
Prüfungsfragen Biochemie; Teil Schroeder Ad Einheit 1 Vergleichen Sie die Stärke von molekularen Wechselwirkungen in kj/mol. In welcher Größenordnung ist der Abstand dieser Wechselwirkungen? Im Vergleich
Citratzyklus. Biochemie Maria Otto,Bo Mi Ok Kwon Park
 Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Citratzyklus Biochemie 13.12.2004 Maria Otto,Bo Mi Ok Kwon Park O CH 3 C Acetyl-CoA + H 2 O HO C COO C NADH O C H Citrat Cis-Aconitat H C Malat Citratzyklus HO C H Isocitrat CH H 2 O Fumarat C = O FADH
Kataboler und Anaboler Stoffwechsel
 Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Vorlesung Vom Molekül zur Zelle Ao.Univ.Prof. Dr. Georg Weitzer Fortsetzung von Block 3 nach Prof. Müllner, ab 8.1. Kataboler und Anaboler Stoffwechsel Aktuelle Folien unter http://homepage.univie.ac.at/georg.weitzer/lectures.html
Stoffwechsel. Metabolismus (3)
 Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
Vorlesung Zell- und Molekularbiologie Stoffwechsel Metabolismus (3) Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien 1 Glykolyse 1 Glucose und in der Glykolyse daraus gebildete
- der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen
 Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die Aufgabe des Citratcyklus ist: - der oxidative Abbau von Acetyl-CoA (und die somit gebildeten Reduktionsäquivalente) - Lieferung von Substraten für verschiedene Synthesen Die Aufgabe des Citratcyklus
Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat
 Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Der Malat-Shuttle Die innere Mitochondrienmebran ist durchlässig für: 1. Pyruvat 2. Malat 3. Aspartat 4. Citrat Die innere Mitochondrienmembran ist undurchlässig für: 1. Wasserstoffatomen > 2. Acetyl-
Regulation der Glykolyse: Phosphofructokinase
 Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Regulation der Glykolyse: Phosphofructokinase Abbauwege des Pyruvats Weitere Oxidation (zu CO 2 ) Alkoholische Gärung Pyruvat- Decarboxylase Alkohol- Dehydrogenase NAD + wird bei der Gärung regneriert,
Vertiefendes Seminar zur Vorlesung Biochemie
 Vertiefendes Seminar zur Vorlesung Biochemie 24.10.2014 Vorbesprechung und Organisation Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Vertiefendes Seminar zur Vorlesung Biochemie 24.10.2014 Vorbesprechung und Organisation Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/abteilung-van-echten-deckert/abt-van-echten-deckert-startseite/
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 16.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Das Sinnloseste: der Zitronensäurezyklus
 Vortrag zum Thema Das Sinnloseste: der Zitronensäurezyklus von Daniel Metzsch 1 Inhalte 1. Zuerst ein paar Strukturformeln 2. Einordnung in den Metabolismus 3. Überblick über den Zitronensäurezyklus 4.
Vortrag zum Thema Das Sinnloseste: der Zitronensäurezyklus von Daniel Metzsch 1 Inhalte 1. Zuerst ein paar Strukturformeln 2. Einordnung in den Metabolismus 3. Überblick über den Zitronensäurezyklus 4.
Der Energiestoffwechsel eukaryotischer Zellen
 Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Der Energiestoffwechsel eukaryotischer Zellen Der Abbau (Katabolismus/Veratmung/Verbrennung) reduzierter Kohlenstoffverbindungen (Glukose, Fettsäuren, Aminosäuren) bzw. deren makromolekularer Speicher
Atmung Übersicht. Atmung der Mitochondrien
 Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Atmung der Mitochondrien Atmung Übersicht e - Transportkette REAKTION: C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O + Energie (Glucose) (Sauerstoff) (Kohlendioxid) (Wasser) Nur ca. 40% der Energie wird zu ATP Der
Der Stoffwechsel. Wir zeigen dir wie er funktioniert.
 Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Der Stoffwechsel. Wir zeigen dir wie er funktioniert. Guter Stoffwechsel, schlechter Stoffwechsel, der Stoffwechsel schläft, den Stoffwechsel ankurbeln,
Klausur zur Vorlesung Biochemie III im WS 2000/01
 Klausur zur Vorlesung Biochemie III im WS 2000/01 am 15.02.2001 von 15.30 17.00 Uhr (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte Name, Matrikelnummer und Studienfach unbedingt angeben (3 1.
Klausur zur Vorlesung Biochemie III im WS 2000/01 am 15.02.2001 von 15.30 17.00 Uhr (insgesamt 100 Punkte, mindestens 40 erforderlich) Bitte Name, Matrikelnummer und Studienfach unbedingt angeben (3 1.
Biochemie II - Tutorium
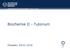 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 04.01.2016 Zellkern Lipidtröpfchen Nucleotidmetabolismus Glykogen- Stoffwechsel Pentosephosephatweg Glucose Glucose
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase
 Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Atmungskette ( Endoxidation) Reaktionen und ATP-Synthase Einleitung Aufrechterhaltung von Struktur und Funktion aller Lebensformen hängt von einer ständigen Energiezufuhr ab Höchste Energieausbeute liefert
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 09.01.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
-Klausur Biochemie Name: Matrikelnr.: 1. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist.
 4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
4.07.205 Name: Matrikelnr.:. a) Erklären Sie, warum ist Wasser gutes Lösungsmittel von Salzen und polaren Biomolekülen ist. 2. Was bedeutet es, wenn eine schwache Säure einen pks von 5 hat? 3. Nennen Sie
Gluconeognese Neusynthese von Glucose aus Pyruvat
 Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
Gluconeognese Neusynthese von Glucose aus Pyruvat Warum notwendig? Das Gehirn ist auf eine konstante Versorgung mit Glucose angewiesen. Eine Unterzuckerung (< 3 4 mmol/l) führt unweigerlich zur Bewußtlosigkeit
1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt.
 Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Übung und Lösung zur Übung Aminosäuren 1. Zeichnen und beschriften Sie die stereochemische Struktur von L- Threonin. Geben Sie an, ob R- oder S-Konfiguration vorliegt. 2. Das Tripeptid Glutathion ( -Glu-Cys-Gly)
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau. (Biomoleküle allgemein)
 Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Übungsfragen zur Vorlesung Einführung in die Biologie, Zell- und Molekularbiologie Teil Biochemie PD Dr. Udo Rau (Biomoleküle allgemein) 1) Aus welchen Elementen besteht die Zelle zu 99%? 2) Warum ist
Musterlösung. Frage Summe Note Punkte 1, ,5 1,0
 Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Biochemische Teilklausur zum Grundmodul 0 im Bachelor-Studiengang Biowissenschaften (neue Prüfungsordnung Dauer Std.), 2. 2. 203, 8:00-9:00 Uhr, Sporthalle, sowie Biochemische Teilklausur zum Grundmodul
Schrittweise Oxidation und Decarboxylierung von Glucose-6-phosphat zu Ribulose-5- phosphat
 1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
1. Der plastidäre oxidative Pentosephosphatweg Abbau von Hexose unter NADPH+H + -Synthese Schlüsselenzym=Glucose-6-phosphat-Dehydrogenase Glucose-6-phosphat-Dehydrogenase wird durch Thioredoxin im reduzierten
Biochemie II. im Wintersemester 2009/2010. Joachim Wegener. Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg
 Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Biochemie II im Wintersemester 2009/2010 Joachim Wegener Institut für Analytische Chemie, Chemo- und Biosensorik Universität Regensburg 18.10.2010 1/14 Biochemie II im WS 2010 / 2011 All Dozenten auf einen
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
9. Abbau der Glukose zum Pyruvat
 9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
9. Abbau der Glukose zum Pyruvat 236 9.1. Übersicht: Abbau von Glucose Pentosephosphate Pathway (PPP) NADP + NADPH Glucose Glycolysis Oxidative Phosphorylation PDH Complex Citric Acid Citric Acid Cycle
Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 23.11.2016 Ablauf des Tutoriums Einführung und Wiederholung Vorlesungszusammenfassung Übungsaufgaben Selbststudium
Pharmazeutische Biologie Grundlagen der Biochemie
 harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
harmazeutische Biologie Grundlagen der Biochemie A Enzyme E1 E2 E3 E4 Biosynthese A B D E B E7 E2 E6 E1 E3 E5 E4 E1 E2 E5 E4 rof. Dr. Theo Dingermann Institut für harmazeutische Biologie Goethe-Universität
Bachelorstudiengang Biologie. Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18
 Bachelorstudiengang Biologie Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18 1. (a) Welche Aminosäuren mit positiv geladenen Seitenketten kennen Sie? Bitte geben Sie die Strukturformel
Bachelorstudiengang Biologie Vorlesung Biochemie I Klausur am 11. Oktober 2012, 9:00 11:00, H18 1. (a) Welche Aminosäuren mit positiv geladenen Seitenketten kennen Sie? Bitte geben Sie die Strukturformel
KOHLENHYDRATE. Die Glykolyse
 Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
Die Glykolyse Hexokinase Glucose Kostet 1ATP Mg 2+ Glucose-6-P Die Glucokinase kann durch Insulin induziert werden in : 1) Den Fettzellen 2) Den ß-Zellen des Pankreas 3) Der Nierenrinde 4) Der Leber Die
schnell und portofrei erhältlich bei
 Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
Kurzlehrbuch Biochemie Kurzlehrbuch Biochemie Bearbeitet von Melanie Königshoff, Timo Brandenburger 2. überarb. Aufl. 2007. Taschenbuch. 46 S. Paperback ISBN 978 3 13 136412 8 Format (B x L): 24 x 17 cm
KOHLENHYDRATE PYRUVAT-DEHYDROGENASE
 PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
PYRUVAT-DEHYDROGENASE PYRUVAT-DEHYDROGENASE: Um ein Optimum Beute garantieren zu können, Wird das entstandene Pyruvat (bei der aeroben) Glykolyse, durch die PDH in Acetyl-CoA umgewandelt, um dann, Teil
Citratzyklus. Citratzyklus
 Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Der hat in der Zelle verschiedene Aufgaben. Teilschritte werden z.b. bei manchen Gärungen eingesetzt (Methyl-Malonyl-CoA-Weg). Er ist wichtig zur Bereitstellung verschiedener Vorstufen für Biosynthesen,
Inhaltsverzeichnis. a. Chemie der Aminosäuren und Peptide
 Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
Inhaltsverzeichnis 1 Zelluläre Grundlagen der Biochemie Typen lebender Zellen 2 Typen biochemischer Präparationen 2 Subzelluläre Fraktionierung 3 Biochemische Funktionen der Zellorganellen 4 2 Proteine
- Biochemieklausur Name: Matrikelnr.:
 08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
08.07.20 Name: Matrikelnr.: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus)
 Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
Der Citratzyklus (= Trikarbonsäurezyklus, Krebszyklus) Biochemischer Kreisprozeß Ablauf in der mitochondrialen Matrix Glykolyse β-oxidation Atmungskette AS-Abbau Der Citratzyklus Der Citratzyklus: Übersicht
1 Vom Organismus zum Molekül... 3
 I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
I Stoffwechsel... 1 1 Vom Organismus zum Molekül... 3 1.1 Aufbau des Organismus... 4 1.2 Chemische Grundlagen des Stoffwechsels... 8 1.3 Informationsübertragung in lebenden Systemen... 17 1.4 Funktion
Kohlenhydrate C n. O) n (H 2. z.b. C 6 O 6 O) 6 H 12 : C 6. Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Monosaccharide
 Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Kohlenhydrate C n (H 2 O) n z.b. C 6 (H 2 O) 6 : C 6 H 12 O 6 Monosaccharide Di- und Oligosaccharide Polysaccharide (Glykane) Vortragender: Dr. W. Helliger Monosaccharide Reaktionen der Monosaccharide
Unterrichtsvorhaben Biologie - Sekundarstufe II Jahrgangsstufe EF ab 2017/2018
 Unterrichtsvorhaben Biologie - Sekundarstufe II Jahrgangsstufe EF ab 2017/2018 Thema/ fachlicher Kontext: Kein Leben ohne Zelle Teil 1 Wie sind Zellen aufgebaut und organsiert? Zellaufbau und Stofftransport
Unterrichtsvorhaben Biologie - Sekundarstufe II Jahrgangsstufe EF ab 2017/2018 Thema/ fachlicher Kontext: Kein Leben ohne Zelle Teil 1 Wie sind Zellen aufgebaut und organsiert? Zellaufbau und Stofftransport
Pentosephosphat-Weg: alternativer Abbau von Glucose. Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet.
 Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Pentosephosphat-Weg: alternativer Abbau von Glucose Wird auch als Hexosemonophosphatweg (HMW) oder Phosphogluconat-Cyclus bezeichnet. Er liefert NADPH und Ribose-5-phosphat. NADPH ist die 2. Währung der
Kapitel 5: 1. Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D.
 Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Kapitel 5: 1 Siderophore assistieren dem Transfer welcher der folgenden Makronährstoffe über Membranen? A. Stickstoff B. Phosphor C. Eisen D. Kalium Kapitel 5: 2 Welcher der folgenden Makronährstoffe ist
Grundlagen der Physiologie
 Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Grundlagen der Physiologie Abbau eines Zuckermoleküls www.icbm.de/pmbio Lebensweise eines heterotrophen Aerobiers 1 Überblick Stoffwechsel Glykolyse Citratcyklus Chemiosmotische Prinzipien Anabolismus
Wirkungsmechanismen regulatorischer Enzyme
 Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Wirkungsmechanismen regulatorischer Enzyme Ein Multienzymsystem ist eine Aufeinanderfolge von Enzymen, bei der das Produkt eines vorstehenden Enzyms das Substrat des nächsten Enzyms wird. Ein regulatorisches
Anaerobe NADH-Regeneration: Gärung
 Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Anaerobe NADH-egeneration: Gärung Milchsäure-Gärung H 3 Lactat-DH H H H 3 Pyruvat Lactat Alkoholische Gärung H 3
Die Wege des Kohlenstoffes
 Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
Die Wege des Kohlenstoffes 1. Licht vs. Dunkelreaktionen Lichtgetriebene Reaktionen o Dunkle -Reaktionen laufen nicht im Dunklen ab reduzieren CO 2-Zucker für Pflanzen zum Wachsen und für uns zum Nutzen
1.Frankfurter Consilium in 2015
 Regulationsmechanismen der Glykolyse und Tumorstoffwechsel Glykolyse leicht gemacht 1.Frankfurter Consilium in 2015 Alfons Meyer Facharzt f. Allgemeinmedizin Notfallmedizin, Naturheilverfahren, Akupunktur,
Regulationsmechanismen der Glykolyse und Tumorstoffwechsel Glykolyse leicht gemacht 1.Frankfurter Consilium in 2015 Alfons Meyer Facharzt f. Allgemeinmedizin Notfallmedizin, Naturheilverfahren, Akupunktur,
Inhaltsfeld 1: Biologie der Zelle (KLP, Seite 22 ff) Vorschläge für mögliche Kontexte: Erforschung der Biomembranen Zellkulturen
 Einführungsphase S II Nordrhein-Westfalen Biologie Stoffverteilung: Zuordnung von Kompetenzen im Kernlehrplan (KLP) Biologie zu den Inhaltsfeldern Inhaltsfelder Reihenfolge Inhaltlicher Schwerpunkt laut
Einführungsphase S II Nordrhein-Westfalen Biologie Stoffverteilung: Zuordnung von Kompetenzen im Kernlehrplan (KLP) Biologie zu den Inhaltsfeldern Inhaltsfelder Reihenfolge Inhaltlicher Schwerpunkt laut
Beschreiben Sie in Stichworten zwei der drei Suppressormutationen, die man in Hefe charakterisiert hat. Starzinski-Powitz, 6 Fragen, 53 Punkte Name
 Starzinski-Powitz, 6 Fragen, 53 Punkte Name Frage 1 8 Punkte Nennen Sie 2 Möglichkeiten, wie der Verlust von Heterozygotie bei Tumorsuppressorgenen (Z.B. dem Retinoblastomgen) zum klompletten Funktionsverlust
Starzinski-Powitz, 6 Fragen, 53 Punkte Name Frage 1 8 Punkte Nennen Sie 2 Möglichkeiten, wie der Verlust von Heterozygotie bei Tumorsuppressorgenen (Z.B. dem Retinoblastomgen) zum klompletten Funktionsverlust
I. Zellatmung. =Abbau von Kohlenhydraten unter Sauerstoffverbrauch (aerob) KH + O 2 --> CO 2 + H 2 O + Energie
 KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
KATABOLISMUS Abbau komplexer organischer Moleküle (reich an Energie) zu einfacheren (mit weniger Energie). Ein Teil der Energie wird genutzt um Arbeit zu verrichten (Zelle erhalten, Wachstum) I. Zellatmung
BIOCHEMIE. Teil 2: Aminosäuren, Proteine, Enzyme. Urheberrechtlich geschütztes Material. Lernkarteikarten Veterinärmedizin - BIOCHEMIE
 Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Lernkarteikarten Veterinärmedizin - BIOCHEMIE BIOCHEMIE 2014 Teil 2: Aminosäuren, Proteine, Enzyme Vetbrainfood - Tiermedizinische Lernkarteikarten - Diplombiologin und Tierärztin G. Glück Liebe/r Biochemie-Interessierte,
Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten.
 Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
Glukose hilft uns, auch bei intensiven Belastungen zu überleben. Wieso? Um diesen Prozess zu verstehen, müssen wir die Wege der Glukose genauer betrachten. In diesem Artikel geht es nicht nur um den Abbau
12. Oxidative Phosphorylierung
 12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
12. Oxidative Phosphorylierung 303 Zweck: Gewinnung von ATP Regeneration von NAD + und FAD Gesamtreaktionen: 3 ADP + 3 P i 3 ATP NADH + 0,5 O 2 + H + NAD + + H-O-H 2 ADP + 2 P i 2 ATP FADH 2 + 0,5 O 2
Vertiefendes Seminar zur Vorlesung Biochemie I. Bearbeitung Übungsblatt 10
 Vertiefendes Seminar zur Vorlesung Biochemie I 22.01.2016 Bearbeitung Übungsblatt 10 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Vertiefendes Seminar zur Vorlesung Biochemie I 22.01.2016 Bearbeitung Übungsblatt 10 Gerhild van Echten-Deckert Fon. +49-228-732703 Homepage: http://www.limes-institut-bonn.de/forschung/arbeitsgruppen/unit-3/
Einführung in die Biochemie Antworten zu den Übungsaufgaben
 Einführung in die Biochemie Antworten zu den Übungsaufgaben Dank Die vorliegenden Antworten zu den Übungsaufgaben für das Seminar zum Modul Einführung in die Biochemie wurden im Wintersemester 2014/2015
Einführung in die Biochemie Antworten zu den Übungsaufgaben Dank Die vorliegenden Antworten zu den Übungsaufgaben für das Seminar zum Modul Einführung in die Biochemie wurden im Wintersemester 2014/2015
Mechanismen der ATP Synthese in Mitochondrien
 Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Mechanismen der ATP Synthese in Mitochondrien Übersicht Die Bedeutung von ATP Aufbau eines Mitochondriums ATP Synthese: Citratzyklus Atmungskette ATP Synthase Regulation der ATP Synthese Die Bedeutung
Enzyme SPF BCH am
 Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Enzyme Inhaltsverzeichnis Ihr kennt den Aufbau von Proteinen (mit vier Strukturelementen) und kennt die Kräfte, welche den Aufbau und die Funktion von Enzymen bestimmen... 3 Ihr versteht die Einteilung
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O O 2 6 CO H 2 O G kj
 Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Biologische Oxidation: Atmung (Dissimilation) C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O G 0-2872 kj Hydrolyse der Stärke Ausgangssubstrate: Glucose, Fructose Stärkehydrolyse: Amylasen Endo- ( -Amylase) und
Nennen Sie die unterschiedlichen rrnas der A.) prokaryotischen und B.) eukaryotischen Ribosomen.
 Averhoff, 9 Fragen, 39 Punkte Frage 1 Erläutern Sie kurz die Bezeichnungen 5-Ende und 3-Ende der RNA. 2 Punkte Frage 2 7 Punkte Nennen Sie die unterschiedlichen rrnas der A.) prokaryotischen und B.) eukaryotischen
Averhoff, 9 Fragen, 39 Punkte Frage 1 Erläutern Sie kurz die Bezeichnungen 5-Ende und 3-Ende der RNA. 2 Punkte Frage 2 7 Punkte Nennen Sie die unterschiedlichen rrnas der A.) prokaryotischen und B.) eukaryotischen
1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog.
 FRAGENKATALOG 1 1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog. 3) Bei der schriftlichen Prüfung kommt je eine Frage aus 10 der 11 Kapitel (10 Hauptfragen), plus eine Zusatzaufgabe.
FRAGENKATALOG 1 1) Zu jedem der 11 Kapitel gibt es 10 Fragen in diesem Fragenkatalog. 3) Bei der schriftlichen Prüfung kommt je eine Frage aus 10 der 11 Kapitel (10 Hauptfragen), plus eine Zusatzaufgabe.
BIOCHEMIE. Prof. Manfred SUSSITZ. über(be)arbeitet und zusammengestellt nach Internetvorlagen:
 BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
BIOCHEMIE Prof. Manfred SUSSITZ über(be)arbeitet und zusammengestellt nach Internetvorlagen: Medizinische Fakultät, Universität Erlangen http://www2.chemie.uni-erlangen.de/projects/vsc/chemie-mediziner-neu/start.html
Versuch 6. Leitenzyme
 Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Versuch 6 Leitenzyme Protokollant: E-mail: Studiengang: Gruppen-Nr: Semester: Betreuer: Max Mustermann max@quantentunnel.de X X X Dr. Kojro Einleitung Ziel dieses Versuches ist der Nachweis von bestimmten
Inhaltsverzeichnis. I Stoffwechsel. 1 Vom Organismus zum Molekül Aminosäuren Peptide und Proteine Enzyme...
 XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
XI I Stoffwechsel 1 Vom Organismus zum Molekül...................... 2 1.1 Aufbau des Organismus.............................. 2 1.2 Chemische Grundlagen des Stoffwechsels.................. 6 1.3 Informationsübertragung
Seminare Biochemie (2. Semester)
 Seminare Biochemie (2. Semester) im SoSe 2017: 1/1 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 1) 1/2 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 2) 2/1 Molekulare Funktion
Seminare Biochemie (2. Semester) im SoSe 2017: 1/1 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 1) 1/2 Molekulare Funktion und Bedeutung von Nucleinsäuren (Teil 2) 2/1 Molekulare Funktion
Punkte 1. a) Erklären Sie wieso das Wassermolekül ein Dipol ist (gerne mit Zeichnung).
 -Klausur Biochemie - 20.07.6 Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie - 20.07.6 Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
Inhaltsverzeichnis - Kapitel
 Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Inhaltsverzeichnis - Kapitel 1. Einleitung: Die Chemie des Lebens 2. Kohlenhydrate 3. Lipide und Membranen 4. Nukleinsäuren 5. Aminosäuren und Proteine 6. Enzyme und Katalyse 7. Vitamine & Kofaktoren 8.
Reaktionen der Zellatmung (1)
 ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
ARBEITSBLATT 1 Reaktionen der Zellatmung (1) 1. Benennen Sie den dargestellten Stoffwechselweg und die beteiligten Substanzen! CoA-S Acetyl-CoA Citrat Oxalacetat Isocitrat Malat Citratzyklus α-ketoglutarat
1. Die Bildung von Methan durch Mikroorganismen erfolgt (2 Punkte)
 Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Modul: Einführung in die Biochemie und Genetik Prüfungsleistung: Einführung in die Biochemie Welches Enzym katalysiert die dargestellte Reaktion? (2 Punkte) a) Hexokinase b) Glyceratkinase c) Mitogen-aktivierte
Präsentation STOFFWECHSEL STOFFWECHSEL. Fettstoffwechsel im Sport. Biologische Oxidation Zitratzyklus und Atmungskette
 STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
STOFFWESEL GRUNDLAGEN STÖRUNGEN:Diagnose, Therapie, Prävention 6 Bedeutung der körperlichen Aktivität Präsentation Fettstoffwechsel im Sport Glukose exokinase 1ATP -> 1ADP Glukose-6-Phosphat Phosphohexoisomerase
Scheinbedingungen für die Lehrveranstaltung Praktikum der Biochemie/ Molekularbiologie
 Scheinbedingungen für die Lehrveranstaltung Praktikum der Biochemie/ Molekularbiologie gültig ab: Wintersemester 2011/12 verantwortlicher Fachvertreter: Prof. K.-D. Fischer, Institut für Biochemie und
Scheinbedingungen für die Lehrveranstaltung Praktikum der Biochemie/ Molekularbiologie gültig ab: Wintersemester 2011/12 verantwortlicher Fachvertreter: Prof. K.-D. Fischer, Institut für Biochemie und
Frühjahr 2012 Organische Chemie S.1. Staatsexamensklausur Frühjahr 2012 Chemie für das Lehramt an Gymnasien. Teil II: Organische Chemie
 Frühjahr 2012 rganische Chemie S.1 Staatsexamensklausur Frühjahr 2012 Chemie für das Lehramt an Gymnasien Teil II: rganische Chemie Aufgabe 1: Polymere (10 P) 1. Polymere a. Zeichnen Sie Ausschnitte aus
Frühjahr 2012 rganische Chemie S.1 Staatsexamensklausur Frühjahr 2012 Chemie für das Lehramt an Gymnasien Teil II: rganische Chemie Aufgabe 1: Polymere (10 P) 1. Polymere a. Zeichnen Sie Ausschnitte aus
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000
 Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
Wiederholungsklausur zur Vorlesung Biochemie IV im SS 2000 am 15.11.2000 von 13.45 15.15 Uhr (insgesamt 100 Punkte, mindestens 50 erforderlich) Bitte Name, Matrikelnummer und Studienfach 1. Wie erfolgt
Zum Klausurbogen der Teilprüfung (Mikrobiologie) zum Modul 10 des Bachelorstudiengangs Biowissenschaften vom
 Deckblatt Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Zum Klausurbogen der Teilprüfung (Mikrobiologie) zum Modul 10 des Bachelorstudiengangs Biowissenschaften vom
Deckblatt Johann Wolfgang Goethe-Universität Frankfurt am Main Fachbereich Biowissenschaften Zum Klausurbogen der Teilprüfung (Mikrobiologie) zum Modul 10 des Bachelorstudiengangs Biowissenschaften vom
Schulinternes Curriculum für die Einführungsphase
 Schulinternes Curriculum für die Einführungsphase Einführungsphase Unterrichtsvorhaben I: Thema/Kontext: Kein Leben ohne Zelle I Wie sind Zellen aufgebaut und organisiert? UF1 Wiedergabe UF2 Auswahl K1
Schulinternes Curriculum für die Einführungsphase Einführungsphase Unterrichtsvorhaben I: Thema/Kontext: Kein Leben ohne Zelle I Wie sind Zellen aufgebaut und organisiert? UF1 Wiedergabe UF2 Auswahl K1
-Klausur Biochemie Name:
 -Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
-Klausur Biochemie -03.02.5 Name: Nur vollständige Reaktionsgleichungen, Berechnungen und Antworten werden als Lösung der Aufgaben gewertet, das Ergebnis alleine genügt nicht. Der Rechengang muß ersichtlich
52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat
 2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
2. Testat Biochemie 93/94 - Teil B (Leider ist dies nur ein Teil der Fragen!) 52: Welche der Coenzyme sind an der oxidativen Decarboxylierung von Pyruvat beteiligt? 1) Thiaminpyrophosphat 3) Biotin 2)
«Ausdauertraining» Naturwissenschaftliche Aspekte
 EHSM / Trainerbildung Jost Hegner Was verstehen wir unter «Leistung» im pädagogischen Sinne? unter «Leistung» im physikalischen Sinne: Power (in Joule/s; Watt)? unter «Leistung» im physiologischen Sinne:
EHSM / Trainerbildung Jost Hegner Was verstehen wir unter «Leistung» im pädagogischen Sinne? unter «Leistung» im physikalischen Sinne: Power (in Joule/s; Watt)? unter «Leistung» im physiologischen Sinne:
Energie, Enzyme und Stoffwechsel
 Energie, Enzyme und Stoffwechsel 1 Physikalische Prinzipien der biologischen Energieumwandlung Physik: Energie Fähigkeit, Arbeit zu verrichten Biochemie: Energie Fähigkeit, Materie zu verändern 1 Physikalische
Energie, Enzyme und Stoffwechsel 1 Physikalische Prinzipien der biologischen Energieumwandlung Physik: Energie Fähigkeit, Arbeit zu verrichten Biochemie: Energie Fähigkeit, Materie zu verändern 1 Physikalische
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte
 Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
Biochemie und Stoffwechsel Biochemie Aufklärung der Stoffwechselwege und -teilschritte Identifikation der Ausgangs-, Zwischen- und Endprodukte (Stoffwechselprodukte) Enzyme sind Proteine mit Katalysatorwirkung.
LIPIDE. Periphere Gruppe mit Cysteinylrest. FS-Synthase. Zentrale Gruppe Phosphopanthetinarm kovalente Bindung
 Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Periphere Gruppe mit Cysteinylrest FS-Synthase Zentrale Gruppe Phosphopanthetinarm kovalente Bindung Die FS-Biosynthse aus Acetyl-CoA und Malonyl-CoA, wird komplett an dem dimeren Multienzymkomplex FETTSÄURESYNTHETASE
Klausur zur Vorlesung Biochemie I im WS 2004/05
 Klausur zur Vorlesung Biochemie I im W 2004/05 am 9.03.2005 von 0.00 -.30 Uhr Gebäude 42, örsaal 5 Lösungen in rot Punkte in grün Aufgabe : Formulieren ie die repetitiven chritte in der -xidation von Fettsäuren
Klausur zur Vorlesung Biochemie I im W 2004/05 am 9.03.2005 von 0.00 -.30 Uhr Gebäude 42, örsaal 5 Lösungen in rot Punkte in grün Aufgabe : Formulieren ie die repetitiven chritte in der -xidation von Fettsäuren
10.2 Der Citratzyklus 203
 10.2 Der Citratzyklus 203 Ketonkörper-Biosynthese. Bei den Ketonkörpern handelt es sich um die verschiffbare Form von Acetyl-CoA. Staut sich viel Acetyl-CoA in der Leber an im Hungerzustand, dann werden
10.2 Der Citratzyklus 203 Ketonkörper-Biosynthese. Bei den Ketonkörpern handelt es sich um die verschiffbare Form von Acetyl-CoA. Staut sich viel Acetyl-CoA in der Leber an im Hungerzustand, dann werden
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!!
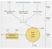 Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Glykolyse! Pyruvat-! dehydrogenase! Citronensäure-! Zyklus!! Indirekte ATP synthese! Protonen können in wässriger Lösung sehr! schnell transportiert werden.! Ionen können biologische Membranen nicht spontan
Vorname: Frage 1. Nennen Sie drei Metalle, die :für den Menschen essentiell sind und als Mengenelemente Körper vorkommen (3 P) Frage 2
 1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
1\.1 Matrikelnummer: Name: Vorname: Bitte eintragen Bitte ankreuzen: Fachsemester: Fachrichtung: Chemie Sonstige Bitte prüfen Sie Ihre Klausur sofort auf Vollständigkeit (Seiten fortlaufend nummeriert
Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte)
 Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Datum: 07.02.2011 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 2. Klausur (50 Punkte) Modulnr.: FMI-BI0027 Hiermit bestätige ich meine Prüfungstauglichkeit.
Biochemie. Kurzes Lehrbuch der. für Mediziner und Naturwissenschaftler. Von Peter Karlson. 12., völlig neubearbeitete Auflage
 Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler Von Peter Karlson 12., völlig neubearbeitete Auflage 177 Abbildungen 323 Formelbilder und Schemata 37 Tabellen 2008 AGI-Information
Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom
 Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Johann Wolfgang Goethe-Universität Frankfurt am Main Deckblatt Fachbereich Biowissenschaften Klausurbogen im Studiengang B.Sc. Biologie Modul BSc-Bio-7, Teilklausur Biochemie vom 08.12.2008 Name: Vorname:
Testsysteme zur Bestimmung der Aktivität verschiedener Enzyme
 Testsysteme zur Bestimmung der Aktivität verschiedener Enzyme Einleitung: Das Ziel der Versuche ist es, Enzymaktivitäten verschiedener Stoffwechselwege in Geweben zu messen und dadurch Rückschlüsse auf
Testsysteme zur Bestimmung der Aktivität verschiedener Enzyme Einleitung: Das Ziel der Versuche ist es, Enzymaktivitäten verschiedener Stoffwechselwege in Geweben zu messen und dadurch Rückschlüsse auf
Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05
 16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
16.02.2005 Abschlussklausur zur Vorlesung Biomoleküle II WS 2004/05 Name: Studienfach: Matrikelnummer: Fachsemester: Hinweise: 1. Bitte tragen Sie Ihren Namen, Matrikelnummer, Studienfach und Semesterzahl
Biochemie der Pflanzen
 Helmut Kindl Biochemie der Pflanzen Dritte Auflage Mit 323 größtenteils zweifarbigen Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris Tokyo HongKong Barcelona Budapest Inhaltsverzeichnis
Helmut Kindl Biochemie der Pflanzen Dritte Auflage Mit 323 größtenteils zweifarbigen Abbildungen Springer-Verlag Berlin Heidelberg New York London Paris Tokyo HongKong Barcelona Budapest Inhaltsverzeichnis
Wiederholungsklausur zur Vorlesung Biochemie I im WS 2004/05
 Wiederholungsklausur zur Vorlesung Biochemie I im WS 2004/05 am 09.05.2005 von 08.00-09.30 Uhr Mensa & 2 Lösungen in rot unkte in grün Aufgabe : Formulieren Sie drei unterschiedliche Reaktionswege, wie
Wiederholungsklausur zur Vorlesung Biochemie I im WS 2004/05 am 09.05.2005 von 08.00-09.30 Uhr Mensa & 2 Lösungen in rot unkte in grün Aufgabe : Formulieren Sie drei unterschiedliche Reaktionswege, wie
Glucose-6-Phosphat > Glucose-1-Phosphat Glucose-1-Phosphat + UTP UTP > > UDP-Glucose + PPi PPi
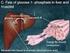 Phosphoglucomutase Phosphoglucomutase Glucose-6-Phosphat -------------------> Glucose-1-Phosphat Glucose-1-Phosphat + UTP UTP -------> -------> UDP-Glucose + PPi PPi fehlt fehlt bei bei Galactoseseintolleranz
Phosphoglucomutase Phosphoglucomutase Glucose-6-Phosphat -------------------> Glucose-1-Phosphat Glucose-1-Phosphat + UTP UTP -------> -------> UDP-Glucose + PPi PPi fehlt fehlt bei bei Galactoseseintolleranz
