Verfahren zur Stofftrennung
|
|
|
- Matilde Klein
- vor 7 Jahren
- Abrufe
Transkript
1 Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Verfahren zur Stofftrennung
2 Auf einen Blick: Dieses Protokoll enthält 3 Schülerversuche und 3 Lehrerversuche für die Klassenstufen 5 und 6 zum Thema Reinstoffe, Stoffgemische und Verfahren zur Stofftrennung. Den SuS kann mittels dieser Versuche verdeutlicht werden, dass sich stoffspezifische Eigenschaften ausnutzen lassen, um Stoffgemische wieder zu trennen oder Stoffe voneinander zu unterscheiden. Hierzu werden ausschließlich Stoffe verwendet, die die SuS bereits aus ihrem Alltag kennen, um ihnen den Zugang zu diesem Thema zu erleichtern. Außerdem sollen den SuS die Begrifflichkeiten der Unterscheidung von Stoffen verdeutlicht werden, indem in den Versuchen besonders auf das Gemenge und die Lösung eingegangen wird. Ein Arbeitsblatt zum Trennen von Sand, Salz und Eisenspänen rundet das Protokoll ab und kann die Erarbeitung des Versuches unterstützen. Inhalt 1 Beschreibung des Themas und zugehörige Lernziele Relevanz des Themas für SuS der 5. und 6. Jahrgangsstufe und didaktische Reduktion Lehrerversuch - Das Salz in der Suppe Schülerexperiment - Trennen von Sand, Salz und Eisenspänen Didaktischer Kommentar zum Arbeitsblatt Erwartungshorizont (Kerncurriculum) Erwartungshorizont (Inhaltlich)... 12
3 1 Beschreibung des Themas und zugehörige Lernziele 1 Beschreibung des Themas und zugehörige Lernziele Die Materialien aus denen ein Körper aufgebaut ist, werden in der Chemie als Stoff bezeichnet. Jeder Stoff besteht aus vielen Teilchen und besitzt für ihn charakteristische Eigenschaften, so dass er von anderen Stoffen unterschieden werden kann. Diese Unterschiede können optisch wahrgenommen werden wie Farbe und Teilchengröße oder können gemessen werden wie Schmelz- und Siedepunkt. Stoffe können in Reinstoffe und Gemische unterteilt werden. Ein Reinstoff ist nur aus einer Teilchensorte aufgebaut, während ein Gemisch sich mindestens aus zwei Reinstoffen zusammensetzt. Diese beiden Kategorien der Stoffe lassen sich noch weiter unterteilen. Reine Stoffe können sowohl chemische Verbindungen sein (z.b. Wasser), als auch Elemente (z.b. Sauerstoff). Stoffgemische lassen sich mit Hilfe von verschiedenen Methoden wieder voneinander trennen, wobei die Eigenschaften der jeweiligen Reinstoffe ausgenutzt werden, die beim Mischen erhalten blieben. In homogenen Stoffgemischen sind die beteiligten Stoffe bis zu den kleinsten Teilchen miteinander vermischt, während sie es in heterogenen Stoffgemischen nicht sind. In heterogenen Stoffgemischen können die Teilchen noch mit dem bloßen Auge oder optischen Hilfsmitteln voneinander unterschieden werden. Legierungen, Lösungen und Gasgemische werden aus diesem Grund zu den homogenen Stoffgemischen gezählt. Gemenge, Suspensionen, Emulsionen, Rauch und Nebel hingegen gehören zu den heterogenen Stoffgemischen. Das Thema Reinstoffe, Stoffgemische und Verfahren zur Stofftrennung findet sich im niedersächsischen Kerncurriculum (KC) im Basiskonzept Stoff-Teilchen wieder. Hierbei werden Reinstoffe und Stoffgemische unter dem Oberbegriff Stoffe zusammengefasst. Ein Lernziel ist es, dass die SuS in der Lage sein sollen Stoffe anhand von, mit den Sinnen erfahrbaren aber auch messbaren, Eigenschaften zu unterschieden. Darüber hinaus sollen diese Eigenschaften angewandt werden, um Trennverfahren verschiedener Stoffe zu erklären und zu entwickeln. Als ergänzende Differenzierung wird neben der Destillation auch die Chromatographie als Trennverfahren explizit aufgeführt. Außerdem sollen die SuS Kenntnisse über die Löslichkeit, die Schmelztemperatur und den Umgang mit dem Bunsenbrenner gewinnen. Am Ende der Unterrichtseinheit sollen die SuS einen Überblick über die Unterteilung von Stoffen bekommen haben und verschiedene Verfahren zur Stofftrennung kennengelernt und selbst durchgeführt haben. Hierbei können die SuS ihr Vorwissen über Stoffeigenschaften wie Löslichkeit, Dichte, Magnetismus, Siedetemperatur und Teilchengröße anwenden. Im Lehrerversuch erkennen die SuS, dass es sich bei der Gemüsebrühe um ein Gemisch aus mehreren Stoffen handelt. Die SuS können Vermutungen darüber anstellen, aus welchen Stoffen sich Gemüsebrühe zusammensetzt. Dies kann z.b. durch genaues Betrachten (Gemüsestücke)
4 1 Beschreibung des Themas und zugehörige Lernziele des Feststoffes oder durch ihr Vorwissen hinsichtlich des Geschmacks (salzig) erfolgen. Im Vordergrund der Trennverfahren steht jedoch die Extraktion des Kochsalzes. Die SuS stellen fest, dass sich Stoffeigenschaften ausnutzen lassen, um Gemische wieder zu trennen (größere Teilchen wie die Gemüsestücke bleiben im Filter zurück). Im Schülerversuch wenden die SuS ihre Kenntnisse über verschiedene Trennverfahren selbstständig an und verwenden, neben den im LV gezeigten Trennverfahren, außerdem das Magnetscheiden und das Dekantieren.
5 2 Relevanz des Themas für SuS der 5. und 6. Jahrgangsstufe und didaktische Reduktion 2 Relevanz des Themas für SuS der 5. und 6. Jahrgangsstufe und didaktische Reduktion Das Verständnis, dass Stoffe in Gemische und reine Stoffe unterteilt werden können ist besonders wichtig in Hinblick auf die Einführung des Teilchenmodells in den höheren Jahrgansstufen. Aus diesem Grund sollte bereits in der 5. und 6. Jahrgangsstufe darauf geachtet werden, dass dieses grundlegende Konzept verstanden wurde. Um den SuS den Einstieg zu erleichtern wird zunächst nur die makroskopische Ebene betrachtet, die in den Experimenten fast ausschließlich mit Alltagsstoffen dargestellt wird. Die Verwendung von ungefährlichen Alltagsgegenständen ist gerade in den unteren Klassenstufen zu empfehlen, wenn fundamentale Experimentierfertigkeiten gelernt und trainiert werden sollen. Die angewandten Trennverfahren stellen einen geeigneten Bezug zur Lebenswelt der SuS dar. Die SuS erkennen, dass sie bereits Verfahren zur Stofftrennung kennen und selbst durchgeführt haben. Diese Trennverfahren reichen vom Sandsieben in der Sandkiste über das Filtern von Kaffee, das Abgießen des Nudelwassers, Goldwaschen bis hin zum Aussortieren der ungeliebten Erbsen aus dem Mittagessen. Der Transfer vom Alltag zum Chemieunterricht soll den SuS somit erleichtert werden. Außerdem bieten die Trennverfahren die Möglichkeit, das erlernte Wissen aus vorangegangenem Unterricht über Stoffeigenschaften (Dichte, Löslichkeit, etc.) anzuwenden und somit Zusammenhänge des Lernstoffs besser zu verstehen und einzuordnen. Wissensinseln können so vermieden und die Motivation gesteigert werden. Didaktisch wurde das Thema so reduziert, dass alle Prozesse auf der makroskopischen, also phänomenologischen Ebene erklärt werden können. Ein tieferes Verständnis (mikroskopische Ebene) für die genauen Prozesse der Stofftrennung mittels der Nutzung von Stoffeigenschaften wie zum Beispiel der Löslichkeit wird in höheren Klassenstufen thematisiert. Die Reduktion auf makroskopische Ebene erleichtert den SuS ein besseres Verständnis für die ablaufenden Prozesse zu entwickeln.
6 3 Lehrerversuch - Das Salz in der Suppe 3 Lehrerversuch - Das Salz in der Suppe In diesem Versuch soll aus herkömmlicher Gemüsebrühe das Salz extrahiert werden. Hierzu werden verschiedene Trennverfahren angewandt. Der Versuch stellt einen anschaulichen Alltagsbezug her, da den SuS bereits aus dem Alltag Gemüsebrühe bekannt ist. Es werden keinerlei Gefahrstoffe verwendet. Materialien: Chemikalien: Durchführung: Becherglas (100 ml), Erlenmeyerkolben, Porzellanschale, Trichter, Filter, Bunsenbrenner, Dreifuß mit Drahtnetz, Glasstab, Handbrenner destilliertes Wasser, Gemüsebrühe 2 Spatellöffel der Gemüsebrühe werden in ein 100 ml Becherglas gegeben, mit 50 ml kaltem destilliertem Wasser versetzt und gut umgerührt. Der Becherglasinhalt wird in einen Erlenmeyerkolben filtriert, danach in die Porzellanschale gefüllt und mit dem Bunsenbrenner erhitzt bis das Wasser vollständig verdampft ist (ACHTUNG: bei starkem Erhitzen spritzt der Feststoff). Nach Abkühlen der Porzellanschale wird etwa eine Spatelspitze des braunen Feststoffs aus der Porzellanschale entnommen und auf das Drahtnetz gegeben. Der Stoff wird mit einem Handbrenner so lange von oben kräftig erhitzt bis sich ein weißer Feststoff erkennen lässt. Abbildung 1: Nach der Filtration bleiben größere Teilchen im Filter zurück, das Filtrat ist braun (links); brauner Feststoff nach dem ersten Erhitzen (Mitte); brauner Feststoff wird von oben erhitzt (rechts). Beobachtung: Im Filter bleiben größere hellgelbe und grüne Stücke zurück. Das Filtrat ist eine braune Flüssigkeit. Nach dem Eindampfen in der Porzellanschale liegt ein brauner Feststoff vor. Bei weiterem Erhitzen des Feststoffes auf dem
7 3 Lehrerversuch - Das Salz in der Suppe Drahtnetz wird dieser schwarz bis nach etwa 10 Minuten kräftigem Erhitzens ein weißer Feststoff zu erkennen ist. Abbildung 2 (von links nach rechts): Gemüsebrühe, Filterrückstände (Fett, Gemüse, ), brauner Feststoff während des 2. Erhitzens, extrahiertes Salz. Deutung: Entsorgung: Die Gemüsebrühe setzt sich aus mehreren Stoffen zusammen. Sie ist ein Gemisch aus getrockneten Gemüseteilen, Fett, Gewürzen, Aromastoffen und Kochsalz. Da sich das Kochsalz im kalten Wasser löst und fast alle anderen Bestandteile durch das Filtrieren im Filterpapier haften bleiben, kann das Kochsalz durch Eindampfen des Filtrats extrahiert werden. Die zunächst braune bzw. schwarze Färbung des Feststoffes lässt sich durch organische Reste wie beispielsweise Glutamat erklären, welches sich auch im kalten Wasser löst. Die Entsorgung erfolgt über den Hausmüll bzw. Abfluss. Literatur: In Anlehnung an H. Schmidkunz, Chemische Freihandversuche - Band 1, Aulis, 2011, S. 19. Im Anschluss an diesen Versuch kann ein Nachweis des Kochsalzes mit Silbernitrat durchgeführt werden. Es sollte hier jedoch eine didaktische Reduktion vorgenommen werden, die die genauen Vorgänge der Silberchloridfällung vereinfacht (z.b. Silbernitrat ist ein Nachweisreagenz für Kochsalz). Außerdem kann eine quantitative Bestimmung des Salzgehaltes in der Gemüsebrühe erfolgen, wenn die genauen Massen der eingesetzten Brühe und des extrahierten Salzes notiert werden. In Klassen, die im Umgang mit dem Bunsenbrenner sicher sind, kann dieser Versuch auch alternativ als Schülerversuch durchgeführt werden.
8 4 Schülerexperiment - Trennen von Sand, Salz und Eisenspänen 4 Schülerexperiment - Trennen von Sand, Salz und Eisenspänen In diesem Versuch sollen mittels verschiedener Trennverfahren die drei Stoffe Sand, Salz und Eisenspäne getrennt werden. Die SuS können ihr Vorwissen über Magnetismus und die Löslichkeit von Salz in Wasser anwenden. Es werden keinerlei Gefahrstoffe verwendet. Materialien: Chemikalien: Durchführung1: Beobachtung1: Petrischale, Magnet, Taschentuch, 2 Bechergläser, Filterpapier, Trichter, Porzellanschale, Dreifuß+ Drahtnetz, Bunsenbrenner, Glasstab Sand, Eisenspäne, Kochsalz(NaCl), destilliertes Wasser Auf einer Petrischale werden etwas Sand, 2 Spatelspitzen Salz und ein Spatel Eisenspäne vermengt. Der Magnet wird in ein Taschentuch eingewickelt und über das Gemenge gehalten. Die Eisenspäne werden von dem Magneten angezogen und bleiben am Taschentuch haften. Abbildung 3: Gemenge aus Sand, Eisenspänen und Kochsalz (links), Gemenge nach Abtrennen der Eisenspäne mittels Magneten (rechts). Deutung1: Durch die magnetischen Eigenschaften der Eisenspäne, bleiben diese am Magneten haften. Das Gemenge besteht nun nur noch aus Sand und Salz. Durchführung2: Das Sand-Salz Gemenge wird in ein Becherglas gegeben. Anschließend werden etwa 100 ml destilliertes Wasser hinzugegeben und mit einem Glasstab etwas verrührt. Das Becherglas wird kurz stehen gelassen bis sich der Feststoff abgesetzt hat. Das Wasser wird abdekantiert und durch einen Trichter mit Filter in einen Erlenmeyerkolben filtriert.
9 4 Schülerexperiment - Trennen von Sand, Salz und Eisenspänen Beobachtung2: Nach dem Abdekantieren bleibt der größte Teil des Sandes im Becherglas zurück. Das Wasser ist trüb und kleinere Schwebeteilchen sind zu sehen. Nach dem Filtrieren sind keine Schwebeteilchen mehr im Wasser zu erkennen, so dass dieses fast klar aussieht. Abbildung 4: Das Gemisch aus Sand, Salz und Wasser (links) nach dem Dekantieren (Mitte) und dem Filtrieren (rechts). Deutung2: Durchführung3: Beobachtung3: Durch die höhere Dichte von Sand im Vergleich zum Salzwasser, sinkt dieser zu Boden. Durch das Filterpapier gelangen nur sehr kleine Teilchen wie z.b. die des Salzwassers; große Sandteilchen, die durch das Abdekantieren noch nicht abgetrennt wurden, passen nicht durch das Filterpapier. Das Filtrat wird in eine Porzellanschale gegeben und einige Minuten so lange kräftig mit dem Bunsenbrenner erhitzt bis das Wasser verdampft ist. In der Porzellanschale bleibt ein weißer Feststoff zurück. Abbildung 5: Weißer Feststoff aus der Porzellanschale. Deutung3: Entsorgung: Bei dem weißen Feststoff handelt es sich um das zurück gewonnene Kochsalz. Das Salz und der Sand können über den Hausmüll oder Abfluss entsorgt werden. Die abgetrennten Eisenspäne können wiederverwendet werden. Literatur: In Anlehnung an: Dr. P. Haupt, Dr. H. Möllenkamp (zuletzt aufgerufen am )
10 Thema: Verfahren zur Stofftrennung - Klasse 5 / 6 Stoffeigenschaften ausnutzen Wir trennen ein Gemenge Jeder Stoff hat ganz bestimmte Eigenschaften, die uns dabei helfen können ihn von anderen Stoffen zu unterscheiden. Im folgenden Experiment können wir uns das Wissen über die Eigenschaften bestimmter Stoffe zu Nutze machen, um diese voneinander zu trennen. Materialien: Petrischale, Magnet, Taschentuch, 2 Bechergläser, Filterpapier, Trichter, Porzellanschale, Dreifuß+ Drahtnetz, Bunsenbrenner, Glasstab Chemikalien: Durchführung 1: Sand, Eisenspäne, Kochsalz (NaCl), destilliertes Wasser Auf einer Petrischale werden etwas Sand, 2 Spatelspitzen Salz und 1 Spatel Eisenspäne vermengt. Der Magnet wird in ein Taschentuch eingewickelt und über das Gemenge gehalten. Beobachtung 1: Durchführung 2: Das Sand-Salz Gemenge wird in ein Becherglas gegeben. Anschließend werden etwa 100 ml destilliertes Wasser hinzugegeben und mit einem Glasstab etwas verrührt. Das Becherglas wird kurz stehen gelassen bis sich der Feststoff abgesetzt hat. Das Wasser wird abdekantiert und durch einen Trichter mit Filter in einen Erlenmeyerkolben filtriert. Beobachtung 2: Durchführung 3: Das Filtrat wird in eine Abdampfschale gegeben und einige Minuten so lange kräftig mit dem Bunsenbrenner erhitzt bis das Wasser verdampft ist. Beobachtung 3: Entsorgung: Das Salz und der Sand können über den Hausmüll oder Abfluss entsorgt werden. Die abgetrennten Eisenspäne können wiederverwendet werden. Auswertung: Aufgabe 1 Nenne die Trennverfahren, die du im Experiment verwendet hast! Aufgabe 2 Erkläre aufgrund welcher Stoffeigenschaften diese Trennverfahren funktionieren!
11 Thema: Verfahren zur Stofftrennung - Klasse 5 / 6 Aufgabe 3 Stelle dir vor, du bist auf einer einsamen Insel mitten im Meer gestrandet. Auf dieser Insel gibt es kein Süßwasser, was du trinken kannst. So langsam bekommst du jedoch Durst! Zeichne in das Kästchen eine Apparatur mit deren Hilfe du das salzige Meerwasser trinkbar machen könntest. Erläutere wie deine Apparatur funktioniert! Dabei stehen dir folgende Gegenstände zur Verfügung, die in einer Kiste an den Strand gespült wurden: [1] [2] [6] [3] [4] [5] [1] (zuletzt aufgerufen am ) [2] (zuletzt aufgerufen am ) [3] (zuletzt aufgerufen am ) [4] (zuletzt aufgerufen am ) [5] (zuletzt aufgerufen am ) [6] (zuletzt aufgerufen am )
12 5 Didaktischer Kommentar zum Arbeitsblatt 5 Didaktischer Kommentar zum Arbeitsblatt Das Arbeitsblatt unterstützt die Erarbeitung des Versuches Trennen von Sand Salz und Eisenspänen. Dabei beziehen sich insbesondere Aufgabe 1 und Aufgabe 2 auf die Auswertung des durchgeführten Versuches und fördern das Verständnis der dort eingesetzten Trennverfahren. Der Versuch und das Arbeitsblatt können zum Beispiel nach dem Versuch Gemenge aus Alltagsstoffen des Kurzprotokolls durchgeführt bzw. verwendet werden. Den SuS kann mit Hilfe des Einstiegsexperiments vermittelt werden, dass sich nicht alle Stoffgemische manuell (per Hand) trennen lassen und andere Trennverfahren unabdingbar sind. Zur Bearbeitung des Arbeitsblattes ist es notwendig, dass die SuS bereits Vorwissen über gängige Stoffeigenschaften wie z. B. Dichte, Löslichkeit und Teilchengröße besitzen. Im Verlauf der Unterrichtsstunde sollen die SuS nicht nur das angeleitete Experimentieren in Kleingruppen üben, sondern auch den Versuch mithilfe des Arbeitsblattes auswerten sowie beobachtete Sachverhalte beschreiben und erklären können. In Aufgabe 3 sollen die SuS selbstständig mit ihrem Vorwissen über Stofftrennung und Stoffeigenschaften ein Trennverfahren entwickeln. Die so von den SuS entworfenen Destillationsapparatur kann im weiteren Unterrichtsverlauf als ein weiteres gängiges Trennverfahren eingeführt und besprochen werden. Insgesamt ist die Aufgabe in den Kontext einer kleinen Geschichte gebettet, die den SuS das Problem näher bringen und motivierend wirken soll. Neben den benötigten Gegenständen stehen außerdem zwei Gegenstände zur Verfügung, die nicht benötigt werden, so dass die SuS eine begründete Auswahl treffen müssen. Dies erhöht den Schwierigkeitsgrad der Aufgabe. 5.1 Erwartungshorizont (Kerncurriculum) Im Folgenden soll der Bezug der Aufgaben zum Kerncurriculum aufgezeigt werden. Fachwissen: Erkenntnisgewinnung: Die SuS erklären Trennverfahren mit Hilfe ihrer Kenntnisse über Stoffeigenschaften (Aufgabe 1+2) Die SuS entwickeln Strategien zur Trennung von Stoffgemischen (Aufgabe 3) Die SuS beobachten und beschreiben sorgfältig (Versuch) Kommunikation: Bewertung: Die SuS stellen Ergebnisse vor (Versuch) Die SuS beschreiben, dass Chemie sie in ihrer Lebenswelt umgibt (Aufgabe 3)
13 5 Didaktischer Kommentar zum Arbeitsblatt Das Lernziel von Aufgabe 1 ist das Benennen der im Versuch angewandten Trennverfahren; es muss lediglich bekanntes Wissen wiedergegeben werden. In der Aufgabe 2 verknüpfen die SuS, die in Aufgabe 1 aufgelisteten Trennverfahren mit den Stoffeigenschaften, die bei dem jeweiligen Verfahren ausgenutzt wird. Hier sollen die SuS ihr Wissen über den Zusammenhang von Stoffeigenschaften und Trennverfahren erkennen und strukturieren. Bei Aufgabe 3 handelt es sich klar um eine Transferaufgabe; das Ziel hierbei ist es ihr Wissen über Stofftrennung und Stoffeigenschaften anzuwenden und damit ein neues Problem zu lösen. 5.2 Erwartungshorizont (Inhaltlich) Aufgabe 1 Folgend sind die zu erwartenden Trennverfahrene genannt: 1. Magnetscheiden (mechanisches Trennen) 2. Dekantieren 3. Filtrieren 4. Eindampfen Aufgabe 2 Beim Magnetscheiden werden sich die magnetischen Eigenschaften der Eisenspäne zu Nutzen gemacht. Da in diesem Gemenge nur Eisen diese Eigenschaft besitzt, kann es von den anderen Stoffen getrennt werden. Sand hat eine höhere Dichte als (Salz-)Wasser, so dass das (Salz-)Wasser abdekantiert werden kann. Letzte kleine Sandkörner bleiben im Filter zurück, da die Sandteilchen größer sind als die Wasserteilchen. Wasser hat eine höhere Siedetemperatur als Salz, so dass das Kochsalz in der Porzellanschale zurückbleibt. Aufgabe 3 Im Kochtopf wird Meerwasser erhitzt. Der Kochtopfdeckel wird schräg auf den Topf gelegt und ein Glas an das tieferliegende Ende des Deckels gestellt. Das Salzwasser fängt an zu kochen und das Wasser beginnt zu sieden. Am schräg aufliegenden Deckel kondensiert der Wasserdampf und läuft aufgrund des Winkels in das Glas. Das Meersalz bleibt im Kochtopf zurück. Kompass und Zitrone werden nicht benötigt.
Aggregatzustände und deren Temperaturabhängigkeit
 Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Name: Sissy Freund Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Aggregatzustände und deren Temperaturabhängigkeit Beschreibung des Themas und zugehörige Lernziele 2 Auf einen Blick: Dieses Protokoll
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 5 & 6. Verfahren zur Stofftrennung
 Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 5 & 6 Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind
Schulversuchspraktikum Sebastian Gerke Sommersemester 2012 Klassenstufen 5 & 6 Verfahren zur Stofftrennung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll sind
3. Stoffgemische und Ihre Zerlegung
 3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
3. Stoffgemische und Ihre Zerlegung Aus Stoffgemischen lassen sich die einzelnen Bestandteile durch physikalische Trennverfahren isolieren. Wenn ein Stoff mittels physikalischen Methoden nicht weiter zerlegen
Trenne ein Gemisch aus Sand und Kochsalz sowie ein Gemisch aus Sand und Eisen.
 Naturwissenschaften - Chemie - Allgemeine Chemie - 3 Trennverfahren (P750900) 3.2 Gemischtrennungen - Filtrieren, Magnetscheidung Experiment von: Phywe Gedruckt:.0.203 2:53:30 intertess (Version 3.06 B200,
Naturwissenschaften - Chemie - Allgemeine Chemie - 3 Trennverfahren (P750900) 3.2 Gemischtrennungen - Filtrieren, Magnetscheidung Experiment von: Phywe Gedruckt:.0.203 2:53:30 intertess (Version 3.06 B200,
Reinstoffe und Stoffgemische
 Schulversuchspraktikum Dörte Hartje Sommersemester 2013 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Auf einen Blick: Dieses Versuchsprotokoll enthält zwei Lehrer- und vier SchülerInnenexperimente
Schulversuchspraktikum Dörte Hartje Sommersemester 2013 Klassenstufen 5 & 6 Reinstoffe und Stoffgemische Auf einen Blick: Dieses Versuchsprotokoll enthält zwei Lehrer- und vier SchülerInnenexperimente
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Chemische Stoffe - Eigenschaften, Reinstoffe, Gemische, Trennverfahren Das komplette Material finden Sie hier: Download
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Chemische Stoffe - Eigenschaften, Reinstoffe, Gemische, Trennverfahren Das komplette Material finden Sie hier: Download
Homogene und Heterogene Gemische
 Schulversuchspraktikum Name Nicolai ter Horst Semester SS 2013 Klassenstufen 7 & 8 Homogene und Heterogene Gemische 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Name Nicolai ter Horst Semester SS 2013 Klassenstufen 7 & 8 Homogene und Heterogene Gemische 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll
Reaktionen von Metallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Aktivierungsenergie und Katalyse
 1 Beschreibung des Themas und zugehörige Lernziele Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 7 & 8 Aktivierungsenergie und Katalyse 1 Beschreibung des Themas und zugehörige
1 Beschreibung des Themas und zugehörige Lernziele Schulversuchspraktikum Marie-Lena Gallikowski Sommersemester 2015 Klassenstufen 7 & 8 Aktivierungsenergie und Katalyse 1 Beschreibung des Themas und zugehörige
VORANSICHT. Hinweise zu den Materialien
 Hinweise zu den Materialien M 1 Heterogen oder homogen könnt ihr es unterscheiden? Das Arbeitsblatt dient zur aktiven Wiederholung von bereits Gelerntem und behandelt heterogene und homogene Stoffgemische.
Hinweise zu den Materialien M 1 Heterogen oder homogen könnt ihr es unterscheiden? Das Arbeitsblatt dient zur aktiven Wiederholung von bereits Gelerntem und behandelt heterogene und homogene Stoffgemische.
Schwimmen, Schweben, Sinken
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 beinhaltet einen Lehrer- und vier Schülerversuche.
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Schwimmen, Schweben, Sinken Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 beinhaltet einen Lehrer- und vier Schülerversuche.
Arbeitsauftrag: Destillation
 Abfalltrennung Arbeitsauftrag: Destillation Aufgabe: Baue eine Destillationsapparatur auf (Lass dir dabei von deinem Lehrer helfen) und fertige eine Skizze in deinem Laborbuch dazu an. Verfolge, wie sich
Abfalltrennung Arbeitsauftrag: Destillation Aufgabe: Baue eine Destillationsapparatur auf (Lass dir dabei von deinem Lehrer helfen) und fertige eine Skizze in deinem Laborbuch dazu an. Verfolge, wie sich
Mische einige Stoffe mit Wasser und untersuche die entstandenen Gemischarten.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Schmelz- und Siedetemperatur
 Schulversuchspraktikum Name: Bastian Engelke Semester: Sommersemester 2012 Klassenstufen 5 & 6 Schmelz- und Siedetemperatur 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Das vorgestellte
Schulversuchspraktikum Name: Bastian Engelke Semester: Sommersemester 2012 Klassenstufen 5 & 6 Schmelz- und Siedetemperatur 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Das vorgestellte
Schulversuchspraktikum. Name Thomas Polle. Sommersemester Klassenstufen 5 & 6. Feuer und Kerzen
 Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Schulversuchspraktikum Name Thomas Polle Sommersemester 2015 Klassenstufen 5 & 6 Feuer und Kerzen 2 Auf einen Blick: Es werden je ein Schüler- und Lehrerversuch zum Thema Kerzen und Feuer für den 5. und
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Schulversuchspraktikum. Name: Tobias Piotrowski. Semester: Sommersemester 2013. Klassenstufen 9 & 10. ph-wert
 Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen 9 & 10 ph-wert 1 Beschreibung des Themas und zugehörige Lernziele (Max. 1 Seite) 2 Auf einen Blick: Dieses Protokoll
Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen 9 & 10 ph-wert 1 Beschreibung des Themas und zugehörige Lernziele (Max. 1 Seite) 2 Auf einen Blick: Dieses Protokoll
Arbeitsblatt Wasserkreislauf der Erde
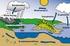 Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Arbeitsblatt Wasserkreislauf der Erde Aufgabe 1) Du hast im Unterricht bereits den Begriff des Aggregatzustands kennengelernt. Benenne die Übergänge zwischen den Aggregatzuständen, indem du die Pfeile
Vom Alkohol zum Alken
 1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
1 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufe 9 & 10 Vom Alkohol zum Alken 2 Auf einem Blick: Diese Unterrichtseinheit für die Klasse 9 & 10 enthält Lehrerversuche und 1 Schülerversuch
Haushaltsreiniger und Waschmittel
 Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Haushaltsreiniger und Waschmittel 3 Schülerversuche 2 Auf einen Blick: Dieses Protokoll befasst sich mit
Schulversuchspraktikum Name: Tobias Piotrowski Semester: Sommersemester 2013 Klassenstufen: 5 & 6 Haushaltsreiniger und Waschmittel 3 Schülerversuche 2 Auf einen Blick: Dieses Protokoll befasst sich mit
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: In diesem Protokoll
Schulversuchspraktikum. Name Lydia Reinhardt. Semester Sommersemester Klassenstufen 11 & 12. Tenside
 Schulversuchspraktikum Name Lydia Reinhardt Semester Sommersemester 2014 Klassenstufen 11 & 12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit zum
Schulversuchspraktikum Name Lydia Reinhardt Semester Sommersemester 2014 Klassenstufen 11 & 12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit zum
Wir untersuchen Mineralwasser
 Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Brenner Streichhölzer Eis
 Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Versuch 1: Wir erhitzen Eis! Reagenzglas Reagenzglasklammer Reagenzglasständer Brenner Streichhölzer Eis Fülle soviel Eis in das Reagenzglas, dass es zu einem Drittel gefüllt ist. Damit Du Dir beim Erhitzen
Aggregatszustände und deren Temperaturabhängigkeit
 Schulversuchspraktikum Name: Christoph Biesemann Semester: Sommersemester 2012 Klassenstufe 5/6 Aggregatszustände und deren Temperaturabhängigkeit 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf
Schulversuchspraktikum Name: Christoph Biesemann Semester: Sommersemester 2012 Klassenstufe 5/6 Aggregatszustände und deren Temperaturabhängigkeit 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf
Verfahren zur Stofftrennung
 Schulversuchspraktikum Denise Heckmann Sommersemester 2013 Klassenstufen 5 & 6 Verfahren zur Stofftrennung 1 Auf einen Blick: Diese Unterrichtseinheit zum Thema Verfahren zur Stofftrennung enthält 2 Lehrerversuche
Schulversuchspraktikum Denise Heckmann Sommersemester 2013 Klassenstufen 5 & 6 Verfahren zur Stofftrennung 1 Auf einen Blick: Diese Unterrichtseinheit zum Thema Verfahren zur Stofftrennung enthält 2 Lehrerversuche
und folgenden Unterricht Kooperation Vorunterrichtliche Erfahrungen,
 Schulinterner Lehrplan für das Fach Chemie in der Jahrgangsstufe 6 (Klassenunterricht) Holzkamp-Gesamtschule, Witten (aktualisiert 2/2013) Unterrichtseinheit / Thema: Stoffe im Alltag, Stoffe können gefährlich
Schulinterner Lehrplan für das Fach Chemie in der Jahrgangsstufe 6 (Klassenunterricht) Holzkamp-Gesamtschule, Witten (aktualisiert 2/2013) Unterrichtseinheit / Thema: Stoffe im Alltag, Stoffe können gefährlich
Schulversuchspraktikum. Anne Steinkuhle. Sommersemester 2013. Klassenstufen 5 & 6. Kosmetikartikel
 Schulversuchspraktikum Anne Steinkuhle Sommersemester 2013 Klassenstufen 5 & 6 Kosmetikartikel 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In dem Protokoll zum Thema Kosmetikartikel
Schulversuchspraktikum Anne Steinkuhle Sommersemester 2013 Klassenstufen 5 & 6 Kosmetikartikel 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In dem Protokoll zum Thema Kosmetikartikel
Elektrische Leitfähigkeit; magnetische Eigenschaften
 Schulversuchspraktikum Sommersemester 2013 Klassenstufen 5 & 6 Elektrische Leitfähigkeit; magnetische Eigenschaften 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch
Schulversuchspraktikum Sommersemester 2013 Klassenstufen 5 & 6 Elektrische Leitfähigkeit; magnetische Eigenschaften 1 Konzept und Lernziele 1 Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Wie wirkt sich die Zugabe von Salz auf den Schmelz- und Siedepunkt von Wasser aus?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: Klassenstufen: 5/6. Die Luft. Das unsichtbare Gasgemisch
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 5/6 Die Luft Das unsichtbare Gasgemisch 1Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. In dieser
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 5/6 Die Luft Das unsichtbare Gasgemisch 1Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. In dieser
Themengebundenes Lernen Klasse 7 SOL-Stunde zu Aktivieren und Festigen
 Themengebundenes Lernen Klasse 7 SOL-Stunde zu Aktivieren und Festigen Der Zahlen-Code eines Tresors ist zu ermitteln. Ohne den Code ist es nicht möglich, an die Schätze zu gelangen, die im Tresor verborgen
Themengebundenes Lernen Klasse 7 SOL-Stunde zu Aktivieren und Festigen Der Zahlen-Code eines Tresors ist zu ermitteln. Ohne den Code ist es nicht möglich, an die Schätze zu gelangen, die im Tresor verborgen
Schulversuchspraktikum. Sommersemester 2014 Klassenstufen 7 & 8. Reaktionen von Metallen mit Sauerstoff und mit Luft.
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:
Chemische Reaktionen ergeben neue Stoffe mit neuen Eigenschaften
 1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
Schüler und Schülerinnen im Labor in Rechtenthal. 4 weiße Stoffe
 Schüler und Schülerinnen im Labor in Rechtenthal 4 weiße Stoffe Chemische Laborgeräte (www.seilnacht.com) Chemische Stoffe unterscheiden sich durch ihre Eigenschaften 4 weiße Stoffe: Von außen sind sie
Schüler und Schülerinnen im Labor in Rechtenthal 4 weiße Stoffe Chemische Laborgeräte (www.seilnacht.com) Chemische Stoffe unterscheiden sich durch ihre Eigenschaften 4 weiße Stoffe: Von außen sind sie
Metalle und Nichtmetalle
 Schulversuchspraktium Bastian Hollemann Sommersemester 2015 Klassenstufen 9 & 10 Metalle und Nichtmetalle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Diese Unterrichtseinheit für
Schulversuchspraktium Bastian Hollemann Sommersemester 2015 Klassenstufen 9 & 10 Metalle und Nichtmetalle 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Diese Unterrichtseinheit für
Institut für Anorganische Chemie (Materialchemie)
 1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
Nussöl aus Nüssen. Trennschritt Trennverfahren Eigenschaft, in der sich die zu trennenden Stoffe unterscheiden Nüsse von Nussschalen trennen
 Nussöl aus Nüssen Aufgabe: Trennt aus Nüssen einige Tropfen Nussöl ab. Könnt ihr nachweisen, dass es sich tatsächlich um Öl handelt? Auswertung: Erstellt eine tabellarische Übersicht über euer Verfahren
Nussöl aus Nüssen Aufgabe: Trennt aus Nüssen einige Tropfen Nussöl ab. Könnt ihr nachweisen, dass es sich tatsächlich um Öl handelt? Auswertung: Erstellt eine tabellarische Übersicht über euer Verfahren
Untersuche, ob Wasser gelöste Gase enthält und wovon die Löslichkeit der Gase abhängt.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754700) 3.3 Löslichkeit von Gasen in Wasser Experiment von: Seb Gedruckt: 24.03.204 :24:34 intertess
Individualisierung im Naturwissenschaftlichen Unterricht DI Dr. mont. Monika Grasser, HTBLVA Ferlach 2. Jahrgang HTL Naturwissenschaften
 Individualisierung im Naturwissenschaftlichen Unterricht DI Dr. mont. Monika Grasser, HTBLVA Ferlach 2. Jahrgang HTL Naturwissenschaften Thema: Trennverfahren. Unterrichtsziel Anhand der vorbereiteten
Individualisierung im Naturwissenschaftlichen Unterricht DI Dr. mont. Monika Grasser, HTBLVA Ferlach 2. Jahrgang HTL Naturwissenschaften Thema: Trennverfahren. Unterrichtsziel Anhand der vorbereiteten
1 Stoffe in Alltag und Technik
 Schülerband Blickpunkt Chemie 1 Niedersachsen (978-3-507-77292-2) Basiskonzept inhaltsbezogene Kompetenzen: Fachwissen prozessbezogene Kompetenzen: Erkenntnisgewinnung, Kommunikation, Bewertung Die Schülerinnen
Schülerband Blickpunkt Chemie 1 Niedersachsen (978-3-507-77292-2) Basiskonzept inhaltsbezogene Kompetenzen: Fachwissen prozessbezogene Kompetenzen: Erkenntnisgewinnung, Kommunikation, Bewertung Die Schülerinnen
Stelle Stoffgemische aus Flüssigkeiten her und untersuche ihre Eigenschaften.
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
Teilchenmodell, Brown sche Molekularbewegung,
 Schulversuchspraktikum Axel Wuttke Sommersemester 2013 Klassenstufen 7&8 Teilchenmodell, Brown sche Molekularbewegung, Diffusion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses
Schulversuchspraktikum Axel Wuttke Sommersemester 2013 Klassenstufen 7&8 Teilchenmodell, Brown sche Molekularbewegung, Diffusion 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses
Natriumchlorid - mehr als ein Gewürz
 Schulversuchspraktikum Name: Nicolai ter Horst Semester: SS 2013 Klassenstufen: 5 & 6 Natriumchlorid - mehr als ein Gewürz 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit
Schulversuchspraktikum Name: Nicolai ter Horst Semester: SS 2013 Klassenstufen: 5 & 6 Natriumchlorid - mehr als ein Gewürz 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit
Thema: Trennverfahren I: Filtration, Eindampfen und Destillation
 Thema: Trennverfahren I: Filtration, Eindampfen und Destillation 1 Schriftliche Ausarbeitung der Unterrichtseinheit Thema: Trennverfahren I: Filtration, Eindampfen und Destillation Übergeordnete Lernziele
Thema: Trennverfahren I: Filtration, Eindampfen und Destillation 1 Schriftliche Ausarbeitung der Unterrichtseinheit Thema: Trennverfahren I: Filtration, Eindampfen und Destillation Übergeordnete Lernziele
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Kernaussagen zum Teilchenmodell
 Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Kernaussagen zum Teilchenmodell Lernbereich 2: Stoffe und ihre Eigenschaften Von beobachtbaren Stoffeigenschaften zum Teilchenmodell Kompetenzerwartung 8 (NTG) und 9 (SG): Die Schülerinnen und Schüler
Extraktion. Arbeitstechnik der Extraktion
 1 Extraktion Die heute vielfach angewandte Trennung durch Extraktion basiert auf der unterschiedlichen Löslichkeit bestimmter Verbindungen in zwei nicht (od. begrenzt) mischbaren Lösungsmittel. (Das Lösungsmittesystem
1 Extraktion Die heute vielfach angewandte Trennung durch Extraktion basiert auf der unterschiedlichen Löslichkeit bestimmter Verbindungen in zwei nicht (od. begrenzt) mischbaren Lösungsmittel. (Das Lösungsmittesystem
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: Klassenstufen: 7/8. Sauerstoff. Das Gas des Lebens
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 7/8 Sauerstoff Das Gas des Lebens 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 7/8 Sauerstoff Das Gas des Lebens 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit
Schulversuchspraktikum. Name: Jennifer Kölling. Sommersemester: 2012. Klassenstufen: 11/12. Tenside
 Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 11/12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit der Tenside in der
Schulversuchspraktikum Name: Jennifer Kölling Sommersemester: 2012 Klassenstufen: 11/12 Tenside 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick:. Die Themeneinheit der Tenside in der
Schulversuchspraktikum. Anna Hille. Sommersemester 2013. Klassenstufen 9 & 10. Salz und Salzbildung
 Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 9 & 10 Salz und Salzbildung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll enthält verschiedene
Schulversuchspraktikum Anna Hille Sommersemester 2013 Klassenstufen 9 & 10 Salz und Salzbildung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Dieses Protokoll enthält verschiedene
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen.
 Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Was macht die Chemie??? Um die Eigenschaften von Stoffen zu untersuchen, müssen diese als reine Stoffe vorliegen. Salatsosse Ein Gemisch Ich stelle eine Salatsosse her und mische dazu: -Wasser -Essig -Öl
Stoffe und ihre Eigenschaften
 Stoffe und ihre Eigenschaften 1.) Welche Stoffeigenschaften kennen Sie? Zählen Sie auf. Aussehen, Geruch, Geschmack, Verformbarkeit, elektr. LF, Magnetismus, Härte, Verhalten beim Erhitzen, Brennbarkeit;
Stoffe und ihre Eigenschaften 1.) Welche Stoffeigenschaften kennen Sie? Zählen Sie auf. Aussehen, Geruch, Geschmack, Verformbarkeit, elektr. LF, Magnetismus, Härte, Verhalten beim Erhitzen, Brennbarkeit;
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Trennverfahren auf Basis der Dichte
 Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 7 & 8 Dichte und dessen Abhängigkeit von der Temperatur; Trennverfahren auf Basis der Dichte 2 Auf einen Blick: Diese Unterrichtseinheit
Schulversuchspraktikum Olga Streck Sommersemester 2012 Klassenstufen 7 & 8 Dichte und dessen Abhängigkeit von der Temperatur; Trennverfahren auf Basis der Dichte 2 Auf einen Blick: Diese Unterrichtseinheit
Schulversuchspraktikum. Sommersemester 2014. Klassenstufen 11 & 12. Batterien und Akkus
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 11 & 12 Batterien und Akkus Auf einen Blick: In der folgenden Unterrichtseinheit Batterien und Akkus werden Schüler- und Lehrerversuche für die
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 11 & 12 Batterien und Akkus Auf einen Blick: In der folgenden Unterrichtseinheit Batterien und Akkus werden Schüler- und Lehrerversuche für die
Veranstaltung 5: Chemie macht hungrig!
 Veranstaltung 5: Chemie macht hungrig! Station 1: Kohlenhydrate E1 Gummibärchen gehen baden! E2 Ist Zucker gleich Zucker? E3 Was macht eine Kartoffel stark? Station 2: Fette E4 Können Fette verschwinden?
Veranstaltung 5: Chemie macht hungrig! Station 1: Kohlenhydrate E1 Gummibärchen gehen baden! E2 Ist Zucker gleich Zucker? E3 Was macht eine Kartoffel stark? Station 2: Fette E4 Können Fette verschwinden?
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Schulversuchspraktikum. Sommersemester 2013. Klassenstufen 7 & 8. Katalysatoren
 Schulversuchspraktikum Sommersemester 2013 Klassenstufen 7 & 8 Katalysatoren 2 Auf einen Blick: In diesem Protokoll werden sechs Versuche dargestellt, die drei inhaltliche Lernziele verfolgen: Sie zeigen,
Schulversuchspraktikum Sommersemester 2013 Klassenstufen 7 & 8 Katalysatoren 2 Auf einen Blick: In diesem Protokoll werden sechs Versuche dargestellt, die drei inhaltliche Lernziele verfolgen: Sie zeigen,
Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad
 Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele
Schulversuchspraktikum Mona-Christin Maaß Sommersemester 2013 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft; Zerteilungsgrad 1 Beschreibung des Themas und zugehörige Lernziele
N & T 3 Physikalische Verfahren 01 Name: Vorname: Datum:
 N & T 3 Physikalische Verfahren 01 Name: Vorname: Datum: Du hast nun zahlreiche Stoffeigenschaften kennengelernt, auf Grund derer sich verschiedene Stoffe unterscheiden lassen. Doch die verschiedenen Stoffeigenschaften
N & T 3 Physikalische Verfahren 01 Name: Vorname: Datum: Du hast nun zahlreiche Stoffeigenschaften kennengelernt, auf Grund derer sich verschiedene Stoffe unterscheiden lassen. Doch die verschiedenen Stoffeigenschaften
Musterlösungen zum Schülerband. 1 Stoffe und Stoffänderungen
 1 Musterlösungen zum Schülerband 1 Stoffe und Stoffänderungen Mischen und Trennen Werner Eisner Paul Gietz Axel Justus Klaus Laitenberger Hildegard Nickolay Werner Schierle Bärbel Schmidt Michael Sternberg
1 Musterlösungen zum Schülerband 1 Stoffe und Stoffänderungen Mischen und Trennen Werner Eisner Paul Gietz Axel Justus Klaus Laitenberger Hildegard Nickolay Werner Schierle Bärbel Schmidt Michael Sternberg
Extraktion. Extraktion: Unter Extrahieren versteht man das Herauslösen eines oder mehrerer Stoffe aus einem festen Gemisch oder einer Lösung.
 Extraktion Extraktion: Unter Extrahieren versteht man das Herauslösen eines oder mehrerer Stoffe aus einem festen Gemisch oder einer Lösung. a) Festkörper Zum Extrahieren gut löslicher Substanzen genügt
Extraktion Extraktion: Unter Extrahieren versteht man das Herauslösen eines oder mehrerer Stoffe aus einem festen Gemisch oder einer Lösung. a) Festkörper Zum Extrahieren gut löslicher Substanzen genügt
Energie und Energieumwandlung
 Schulversuchspraktikum Maximilian Wolf Sommersemester Klassenstufen 7 & 8 Energie und Energieumwandlung Kurzprotokoll Auf einen Blick: In Versuch 1 werden Lycopodium-Sporen (Bärlapp) in der Gasbrennerflamme
Schulversuchspraktikum Maximilian Wolf Sommersemester Klassenstufen 7 & 8 Energie und Energieumwandlung Kurzprotokoll Auf einen Blick: In Versuch 1 werden Lycopodium-Sporen (Bärlapp) in der Gasbrennerflamme
Mischen und. Trennen. Forschertagebuch von
 Mischen und Trennen Forschertagebuch von Forscherauftrag 1 Ein Stück Zucker geht baden > 2 Gläser > zwei Zuckerwürfel > warmes und kaltes Wasser > ein Thermometer > Traubenzucker 1. Fülle beide Gläser
Mischen und Trennen Forschertagebuch von Forscherauftrag 1 Ein Stück Zucker geht baden > 2 Gläser > zwei Zuckerwürfel > warmes und kaltes Wasser > ein Thermometer > Traubenzucker 1. Fülle beide Gläser
4.1 Vergleich von physikalischem Vorgang und chemischer Reaktion. Aufgabe. Woran lassen sich chemische Reaktionen erkennen? (1)
 Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
Naturwissenschaften - Chemie - Allgemeine Chemie - 4 Chemische Reaktionen (P75200) 4. Vergleich von physikalischem Vorgang und chemischer Reaktion Experiment von: Phywe Gedruckt:.0.203 2:58:37 intertess
HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser
 HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser DIE ZERDRÜCKTE ALUDOSE LEERE Alu-Getränkedose (1/2 Liter!) Tiegelzange Schüssel mit kaltem Wasser 1. Fülle die leere Getränkedose mit wenig Wasser 2. Stelle die
HTBL-PINKAFELD Arbeitsblatt A4/1 Wasser DIE ZERDRÜCKTE ALUDOSE LEERE Alu-Getränkedose (1/2 Liter!) Tiegelzange Schüssel mit kaltem Wasser 1. Fülle die leere Getränkedose mit wenig Wasser 2. Stelle die
flüssig-flüssig homogen fest-flüssig Sprudel Stoffgemisch fest-fest Weinbrand Legierung Emulsion heterogen fest-flüssig Rauch
 1. 2. dazugehörige Lies den Text Erklärung. durch. ein zweites Mal durch und unterstreiche dabei wichtige Begriffe und die Partnerpuzzle zu Reinstoffen und Mischungen 3. (Gemäßigter Vervollständigt Gruppe
1. 2. dazugehörige Lies den Text Erklärung. durch. ein zweites Mal durch und unterstreiche dabei wichtige Begriffe und die Partnerpuzzle zu Reinstoffen und Mischungen 3. (Gemäßigter Vervollständigt Gruppe
Schulversuchspraktikum. Klassenstufen 5 & 6. Licht und Farbe
 Schulversuchspraktikum Klassenstufen 5 & 6 Licht und Farbe 1 Konzept und Ziele 1 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Schüler- und 2 Lehrerversuche zum Thema Licht
Schulversuchspraktikum Klassenstufen 5 & 6 Licht und Farbe 1 Konzept und Ziele 1 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 5 & 6 enthält 2 Schüler- und 2 Lehrerversuche zum Thema Licht
Schuleigener Lehrplan Chemie, Klasse 5 und 6
 Schuleigener Lehrplan Chemie, Klasse 5 und 6 Sachkenntnis S - Physikalische und chemische Phänomene auf der Modellebene von Teilchen deuten S1 - Chemische Reaktionen als Veränderung auf der Stoff- und
Schuleigener Lehrplan Chemie, Klasse 5 und 6 Sachkenntnis S - Physikalische und chemische Phänomene auf der Modellebene von Teilchen deuten S1 - Chemische Reaktionen als Veränderung auf der Stoff- und
Destillation von Rotwein
 Destillation von Rotwein Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchen versuch
Destillation von Rotwein Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Zerlegung der Verbindung Wasser Titration Herstellung von Natronlauge Öltröpfchen versuch
Stoffeigenschafte n, Trennmethoden und Verbindungen
 Stoffeigenschafte n, Trennmethoden und Verbindungen Linus Metzler Stoffeigenschaften, Trennmethoden und Verbindungen L i m e n e t L i n u s M e t z l e r W a t t s t r a s s e 3 9 3 0 6 F r e i d o r
Stoffeigenschafte n, Trennmethoden und Verbindungen Linus Metzler Stoffeigenschaften, Trennmethoden und Verbindungen L i m e n e t L i n u s M e t z l e r W a t t s t r a s s e 3 9 3 0 6 F r e i d o r
Siede- und Schmelztemperatur
 Schulversuchspraktikum Name: Anna Elisabeth Gulyas Semester: Sommersemester 2013 Klassenstufen 5 & 6 Siede- und Schmelztemperatur Auf einen Blick: In dieser Unterrichtseinheit lernen die SuS Siede- und
Schulversuchspraktikum Name: Anna Elisabeth Gulyas Semester: Sommersemester 2013 Klassenstufen 5 & 6 Siede- und Schmelztemperatur Auf einen Blick: In dieser Unterrichtseinheit lernen die SuS Siede- und
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
N & T (R) 3 Physikalische Verfahren 01 Name: Vorname: Datum:
 N & T (R) 3 Physikalische Verfahren 01 Name: Vorname: Datum: Du hast nun zahlreiche Stoffeigenschaften kennengelernt, auf Grund derer sich verschiedene Stoffe unterscheiden lassen. Doch die verschiedenen
N & T (R) 3 Physikalische Verfahren 01 Name: Vorname: Datum: Du hast nun zahlreiche Stoffeigenschaften kennengelernt, auf Grund derer sich verschiedene Stoffe unterscheiden lassen. Doch die verschiedenen
Säuren und Laugen im Haushalt
 Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 9 & 10 Säuren und Laugen im Haushalt Auf einen Blick: Diese Unterrichtseinheit für die Klassen 9 und 10 enthält 2 Lehrerversuche,
Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 9 & 10 Säuren und Laugen im Haushalt Auf einen Blick: Diese Unterrichtseinheit für die Klassen 9 und 10 enthält 2 Lehrerversuche,
Schulversuchspraktikum. Dirk Schlemme. Sommersemester Klassenstufen 11 & 12. Alkanone
 Schulversuchspraktikum Dirk Schlemme Sommersemester 2012 Klassenstufen 11 & 12 Alkanone 1 Konzept und Ziele 1 Auf einen Blick: Die Alkanone spielen im alltäglichen Leben nur noch eine untergeordnete Rolle.
Schulversuchspraktikum Dirk Schlemme Sommersemester 2012 Klassenstufen 11 & 12 Alkanone 1 Konzept und Ziele 1 Auf einen Blick: Die Alkanone spielen im alltäglichen Leben nur noch eine untergeordnete Rolle.
Titel: Alltagsstoffe mischen und trennen
 1 Titel: Alltagsstoffe mischen und trennen Kurzbeschreibung: Anhand von Alltagsstoffen aus der Küche können Kinder einfache Erfahrungen zur Stoffeigenschaft, Löslichkeit von Stoffen und Trennverfahren
1 Titel: Alltagsstoffe mischen und trennen Kurzbeschreibung: Anhand von Alltagsstoffen aus der Küche können Kinder einfache Erfahrungen zur Stoffeigenschaft, Löslichkeit von Stoffen und Trennverfahren
Die Kleinsten unter den Kleinen. - Einführung eines Teilchenmodells
 Carl-von-Ossietzky-Universität Oldenburg Fakultät V Institut für reine und angewandte Chemie Didaktik der Chemie Arbeitsmaterialien Chemie Die Kleinsten unter den Kleinen - Einführung eines Teilchenmodells
Carl-von-Ossietzky-Universität Oldenburg Fakultät V Institut für reine und angewandte Chemie Didaktik der Chemie Arbeitsmaterialien Chemie Die Kleinsten unter den Kleinen - Einführung eines Teilchenmodells
3.3 Entparaffinierung durch Extraktion. Aufbau. Gefahren. Aufbau. Naturwissenschaften - Chemie - Organische Chemie - 3 Erdöl
 Naturwissenschaften - Chemie - Organische Chemie - 3 Erdöl (P77400) 3.3 Entparaffinierung durch Extraktion Experiment von: seb Gedruckt: 7.03.204 4:55:40 intertess (Version 3.2 B24, Export 2000) Aufbau
Naturwissenschaften - Chemie - Organische Chemie - 3 Erdöl (P77400) 3.3 Entparaffinierung durch Extraktion Experiment von: seb Gedruckt: 7.03.204 4:55:40 intertess (Version 3.2 B24, Export 2000) Aufbau
Lernzirkel WAS Station 1 Herstellung von Seife aus Kokosfett
 Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Station 1 Herstellung von Seife aus Kokosfett Zeitbedarf: 35 min. Durchführung 10 g Kokosfett und 5 ml destilliertes Wasser werden langsam in einem Becherglas erhitzt. Unter Rühren werden 10 ml Natronlauge
Schulversuchspraktikum. Sommersemester Klassenstufen 5 & 6. Wasseraufbereitung
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Wasseraufbereitung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll befinden sich verschiedene Experimente
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 5 & 6 Wasseraufbereitung 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: In diesem Protokoll befinden sich verschiedene Experimente
Der Chemielehrer wettet um eine Tafel Schokolade, dass kein Schüler länger als zwei Minuten ohne chemische Reaktion auskommen kann.
 1 Einleitung Wozu Chemie? Der Chemielehrer wettet um eine Tafel Schokolade, dass kein Schüler länger als zwei Minuten ohne chemische Reaktion auskommen kann. Überprüfung: Wer kann länger als zwei Minuten
1 Einleitung Wozu Chemie? Der Chemielehrer wettet um eine Tafel Schokolade, dass kein Schüler länger als zwei Minuten ohne chemische Reaktion auskommen kann. Überprüfung: Wer kann länger als zwei Minuten
Bundesrealgymnasium Imst. Chemie 2010-11. Klasse 4. Einführung Stoffe
 Bundesrealgymnasium Imst Chemie 2010-11 Einführung Stoffe Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 Einführung Stoffe Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Fachcurricula Chemie Jahrgangsstufe 8-10
 Planungsbüro Bettinaschule Frankfurt Tel.: (069) 21233028 Fax: (069) 21234975 Feuerbachstraße 37-47 60325 Frankfurt www.bettinaschule.de Fachcurricula Chemie Jahrgangsstufe 8-10 Beschlussfassung vom 24.03.2016
Planungsbüro Bettinaschule Frankfurt Tel.: (069) 21233028 Fax: (069) 21234975 Feuerbachstraße 37-47 60325 Frankfurt www.bettinaschule.de Fachcurricula Chemie Jahrgangsstufe 8-10 Beschlussfassung vom 24.03.2016
Experimente Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Die SuS experimentieren mit Salz und lernen es von der chemischen Seite her besser kennen. Dabei lernen sie in Modellversuchen wichtige Merkmale von Salz kennen. Ziel
Lehrerinformation 1/7 Arbeitsauftrag Die SuS experimentieren mit Salz und lernen es von der chemischen Seite her besser kennen. Dabei lernen sie in Modellversuchen wichtige Merkmale von Salz kennen. Ziel
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
"Gemische und Trennverfahren" (Chemie Sek. I, Kl. 7-9)
 Inhalt und Einsatz im Unterricht "Gemische und Trennverfahren" (Chemie Sek. I, Kl. 7-9) Diese DVD behandelt das Unterrichtsthema "Gemische und Trennverfahren" für die Sekundarstufe I (Klassenstufen 7-9).
Inhalt und Einsatz im Unterricht "Gemische und Trennverfahren" (Chemie Sek. I, Kl. 7-9) Diese DVD behandelt das Unterrichtsthema "Gemische und Trennverfahren" für die Sekundarstufe I (Klassenstufen 7-9).
Schulversuchspraktikum. Julia Müller. Klassenstufen 5/6. Feuer und Kerzen
 Schulversuchspraktikum Name Julia Müller Semester SoSe 2012 Klassenstufen 5/6 Feuer und Kerzen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit für die Klassenstufen
Schulversuchspraktikum Name Julia Müller Semester SoSe 2012 Klassenstufen 5/6 Feuer und Kerzen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Diese Unterrichtseinheit für die Klassenstufen
Textverständnis Strukturieren von Fachbegriffen Text Ggf. Demonstrationsbeispiele. Umgang mit Fachsprache Verstehendes Lesen von Fachtexten
 Methode: Aktivierung mit der Methode Partnerpuzzle Fach: Naturwissenschaften Thema des Unterrichtsbeispiels: Stoffgemisch Klassenstufe: 5-6 Kompetenzbereich: Textverarbeitung Ziele Materialien (Raum-)ausstattung
Methode: Aktivierung mit der Methode Partnerpuzzle Fach: Naturwissenschaften Thema des Unterrichtsbeispiels: Stoffgemisch Klassenstufe: 5-6 Kompetenzbereich: Textverarbeitung Ziele Materialien (Raum-)ausstattung
Dr. Schmecks Lebensmitteluntersuchungen - Eine Lernfirma zur Stofftrennung
 Dr. Schmecks Lebensmitteluntersuchungen - Eine Lernfirma zur Stofftrennung Torsten Witteck, Bielefeld, Ingo Eilks, Bremen Niveau: Sek. I (Anfangsunterricht) Dauer: 6-8 Stunden Der Beitrag enthält Materialien
Dr. Schmecks Lebensmitteluntersuchungen - Eine Lernfirma zur Stofftrennung Torsten Witteck, Bielefeld, Ingo Eilks, Bremen Niveau: Sek. I (Anfangsunterricht) Dauer: 6-8 Stunden Der Beitrag enthält Materialien
Niedersächsisches Kultusministerium. Curriculare Vorgaben. für die Oberschule. Schuljahrgänge 5/6. Chemie. Niedersachsen
 Niedersächsisches Kultusministerium Curriculare Vorgaben für die Oberschule Schuljahrgänge 5/6 Chemie Niedersachsen An der Erarbeitung der Curricularen Vorgaben für die Schuljahrgänge 5/6 der Oberschule
Niedersächsisches Kultusministerium Curriculare Vorgaben für die Oberschule Schuljahrgänge 5/6 Chemie Niedersachsen An der Erarbeitung der Curricularen Vorgaben für die Schuljahrgänge 5/6 der Oberschule
Wir untersuchen Getränke
 Umfrage: Lieblingsgetränke / Alltagsgetränke 1. Angaben zur Person: Erwachsener Mädchen Junge 2. Nenne dein nicht alkoholisches Lieblingsgetränk: 3. Nenne Alltagsgetränke, die du manchmal trinkst. Limonade
Umfrage: Lieblingsgetränke / Alltagsgetränke 1. Angaben zur Person: Erwachsener Mädchen Junge 2. Nenne dein nicht alkoholisches Lieblingsgetränk: 3. Nenne Alltagsgetränke, die du manchmal trinkst. Limonade
Stoffeigenschaften: Dichte und Löslichkeit
 Grundlagenfach Chemie 4. Kl. 1/5 Stoffeigenschaften: Dichte und Löslichkeit Einleitung Chemie ist die Lehre von Stoffen. Eine wichtige Unterscheidung ist die Einteilung in Reinstoffe und Gemische. Gemische
Grundlagenfach Chemie 4. Kl. 1/5 Stoffeigenschaften: Dichte und Löslichkeit Einleitung Chemie ist die Lehre von Stoffen. Eine wichtige Unterscheidung ist die Einteilung in Reinstoffe und Gemische. Gemische
Qualitative Nachweise von Säuren und Basen
 Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Lernaufgaben Sachunterricht
 Ministerium für Schule und Weiterbildung des Landes Nordrhein - Westfalen Lernaufgaben Sachunterricht Grundschule Natur und Leben Wie kann man Salz und Wasser trennen? I. Übersicht: Sachunterricht Bereich:
Ministerium für Schule und Weiterbildung des Landes Nordrhein - Westfalen Lernaufgaben Sachunterricht Grundschule Natur und Leben Wie kann man Salz und Wasser trennen? I. Übersicht: Sachunterricht Bereich:
Mikrokosmos Vorstellungen von der Welt des Kleinen
 II Stoffe im Alltag Beitrag 2 Mikrokosmos (Klassen 5 7) 1 von 32 Mikrokosmos Vorstellungen von der Welt des Kleinen Ariane Pieta, Leonberg Unterschiedliche Alltagsphänomene können durch einfache Experimente
II Stoffe im Alltag Beitrag 2 Mikrokosmos (Klassen 5 7) 1 von 32 Mikrokosmos Vorstellungen von der Welt des Kleinen Ariane Pieta, Leonberg Unterschiedliche Alltagsphänomene können durch einfache Experimente
Schulversuchspraktikum. SoSe 2013. Klassenstufen 7 & 8. Dichte
 Schulversuchspraktikum SoSe 2013 Klassenstufen 7 & 8 Dichte 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche und vier Schülerversuche vorgestellt, die sich mit der Dichte von Gasen und Flüssigkeiten,
Schulversuchspraktikum SoSe 2013 Klassenstufen 7 & 8 Dichte 2 Auf einen Blick: Im Folgenden werden zwei Lehrerversuche und vier Schülerversuche vorgestellt, die sich mit der Dichte von Gasen und Flüssigkeiten,
