DODATAK I SAŽETAK OPISA SVOJSTAVA LIJEKA
|
|
|
- Max Buchholz
- vor 6 Jahren
- Abrufe
Transkript
1 DODATAK I SAŽETAK OPISA SVOJSTAVA LIJEKA 1
2 1. NAZIV GOTOVOG LIJEKA AZILECT 1 mg tablete 2. KVALITATIVNI I KVANTITATIVNI SASTAV Svaka tableta sadrži 1 mg razagilina (u obliku mesilata). Za cjeloviti popis pomoćnih tvari, vidjeti dio FARMACEUTSKI OBLIK Tableta Bijele do bjelkaste, okrugle, plosnate tablete kosih rubova s utisnutom oznakom «GIL» i «1» ispod toga na jednoj strani, a bez oznake na drugoj strani. 4. KLINIČKI PODACI 4.1 Terapijske indikacije AZILECT je indiciran za liječenje idiopatske Parkinsonove bolesti (PB) kao monoterapija (bez levodope) ili kao dodatna terapija (s levodopom) u bolesnika s fluktuacijama prilikom isteka doze. 4.2 Doziranje i način primjene Doziranje Razagilin se primjenjuje peroralno, u dozi od 1 mg jednom dnevno, sa ili bez levodope. Može se uzeti sa ili bez hrane. Stariji: Nije potrebna promjena doze kod starijih bolesnika. Pedijatrijska populacija: Primjena AZILECT-a se ne preporučuje u djece i adolescenata zbog nedostatka podataka o sigurnosti i djelotvornosti. Bolesnici s oštećenjem jetre: Kontraindicirana je primjena razagilina u bolesnika s teškim oštećenjem jetre (vidjeti dio 4.3). Primjenu razagilina u bolesnika s umjerenim oštećenjem jetre nužno je izbjegavati. Pri početku liječenja razagilinom u bolesnika s blagim oštećenjem jetre nužan je oprez. U slučajevima bolesnikove progresije od blagog do umjerenog oštećenja jetre, razagilin je potrebno ukinuti (vidjeti dio 4.4). Bolesnici s oštećenjem bubrega: Kod oštećenja bubrega nije potrebna promjena doze. 4.3 Kontraindikacije Preosjetljivost na djelatnu tvar ili neku od pomoćnih tvari (vidjeti dio 6.1). Istodobno liječenje drugim inhibitorima monoaminooksidaze (MAO) (uključujući lijekove bez recepta i prirodne preparate npr. gospinu travu) ili petidinom (vidjeti dio 4.5). Mora proći najmanje 14 dana između prestanka primjene razagilina i početka liječenja MAO inhibitorima ili petidinom. 2
3 Razagilin je kontraindiciran kod bolesnika s teškim oštećenjem jetre. 4.4 Posebna upozorenja i mjere opreza pri uporabi Istodobnu primjenu razagilina i fluoksetina ili fluvoksamina potrebno je izbjegavati (vidjeti dio 4.5). Mora proći najmanje 5 tjedana između prestanka primjene fluoksetina i početka liječenja razagilinom. Mora proći najmanje 14 dana između prestanka primjene razagilina i početka liječenja fluoksetinom ili fluvoksaminom. Poremećaji kontrole impulsa se mogu pojaviti kod bolesnika liječenih agonistima dopamina i/ili dopaminergičkim lijekovima. U postmarketinškom razdoblju su zaprimljene slične prijave poremećaja kontrole impulsa sa razagilinom. Bolesnike se mora redovito nadzirati za razvoj poremećaja kontrole impulsa. Bolesnici i skrbnici moraju biti upoznati sa bihevioralnim simptomima poremećaja kontrole impulsa koji su bili primjećeni kod bolesnika liječenih razagilinom, uključujući slučajeve kompulzija, opsesivnih misli, patološkog kockanja, povećanog libida, hiperseksualnosti, impulzivnog ponašanja i kompulzivnog trošenja ili kupovanja. Budući da razagilin pojačava učinke levodope, nuspojave levodope mogu se povećati i već postojeća diskinezija pogoršati. Smanjenje doze levodope može ublažiti ovu nuspojavu. Bilo je prijava hipotenzivnih učinaka kada je razagilin uziman istodobno s levodopom. Bolesnici s Parkinsonovom bolesti su posebno osjetljivi na nepovoljne učinke hipotenzije zbog postojećih problema s hodanjem. Ne preporučuje se istodobna primjena razagilina i dekstrometorfana ili simpatomimetika poput onih sadržanih u nazalnim i oralnim dekongestivima ili lijekova za prehladu koji sadrže efedrin ili pseudoefedrin (vidjeti dio 4.5). Tijekom programa kliničkog razvoja, pojava slučajeva melanoma potaknula je razmatranja o mogućoj povezanosti s razagilinom. Prikupljeni podaci upućuju na to da je Parkinsonova bolest, a ne neki određeni lijekovi, povezana s većim rizikom od karcinoma kože (ne isključivo melanoma). Svako sumnjivo oštećenje kože mora se pregledati kod specijalista. Oprez je nužan na početku liječenja razagilinom u bolesnika s blagim oštećenjem jetre. Primjenu razagilina je nužno izbjegavati u bolesnika s umjerenim oštećenjem jetre. U slučajevima bolesnikove progresije od blagog do umjerenog oštećenja jetre razagilin je potrebno ukinuti (vidjeti dio 5.2). 4.5 Interakcije s drugim lijekovima i drugi oblici interakcija Poznate su brojne interakcije između neselektivnih MAO inhibitora i drugih lijekova. Razagilin se ne smije primjenjivati zajedno s drugim MAO inhibitorima (uključujući lijekove i prirodne preparate bez recepta npr. gospinu travu) jer je moguć rizik od neselektivne MAO inhibicije, koja može dovesti do hipertenzivnih kriza (vidjeti dio 4.3). Prijavljene su ozbiljne nuspojave pri istodobnoj primjeni petidina i MAO inhibitora, uključujući i drugi selektivni MAO-B inhibitor. Istodobna primjena razagilina i petidina je kontraindicirana (vidjeti dio 4.3). Kod MAO inhibitora su prijavljene interakcije lijekova pri istodobnoj primjeni simpatomimetskih lijekova. Stoga se, s obzirom na MAO inhibitornu aktivnost razagilina, ne preporučuje istodobna primjena razagilina i simpatomimetika poput onih sadržanih u nazalnim i oralnim dekongestivima ili lijekovima za prehladu koji sadrže efedrin ili pseudoefedrin (vidjeti dio 4.4). Prijavljene su interakcije lijekova pri istodobnoj primjeni dekstrometorfana i neselektivnih MAO inhibitora. Stoga se, s obzirom na MAO inhibitornu aktivnost razagilina, ne preporučuje istodobna primjena razagilina i dekstrometorfana (vidjeti dio 4.4). 3
4 Nužno je izbjegavati istodobnu primjenu razagilina i fluoksetina ili fluvoksamina (vidjeti dio 4.4). Za istodobnu primjenu razagilina sa selektivnim inhibitorima ponovne pohrane serotonina (engl. selective serotonin reuptake inhibitors (SSRI))/selektivnim inhibitorima ponovne pohrane serotonina i noradrenalina (engl. selective serotonin norepinephrine reuptake inhibitors (SNRI)) u kliničkim ispitivanjima, vidjeti dio 4.8. Prijavljene su ozbiljne nuspojave kod istodobne primjene SSRI-a, SNRI-a, tricikličkih/tetracikličkih antidepresiva i MAO inhibitora. Stoga se, s obzirom na MAO inhibitornu aktivnost razagilina, antidepresivi moraju primjenjivati s oprezom. U bolesnika s Parkinsonovom bolešću koji se kronično liječe levodopom kao dodatnom terapijom, nije bilo klinički značajnog učinka liječenja levodopom na klirens razagilina. Ispitivanja metabolizma in vitro su uputila na to da je citokrom P450 1A2 (CYP1A2) glavni enzim odgovoran za metabolizam razagilina. Istodobna primjena razagilina i ciprofloksacina (inhibitora CYP1A2) je povećala AUC razagilina za 83 %. Istodobna primjena razagilina i teofilina (supstrata CYP1A2) nije utjecala na farmakokinetiku nijednog od dvaju navedenih lijekova. Prema tome, potentni CYP1A2 inhibitori mogu promijeniti razine razagilina u plazmi i moraju se primjenjivati s oprezom. Kod bolesnika koji su pušači postoji rizik od smanjenja razina razagilina u plazmi zbog indukcije metabolizirajućeg enzima CYP1A2. Ispitivanja in vitro su pokazala da razagilin u koncentraciji od 1 µg/ml (istovjetno razini koja je 160 puta veća od prosječne C max ~ 5,9-8,5 ng/ml u bolesnika s Parkinsonovom bolešću nakon višekratnog doziranja 1 mg razagilina) nije inhibirao izoenzime citokroma P450, CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2El, CYP3A4 i CYP4A. Ovi rezultati indiciraju da nije vjerojatno da terapijske koncentracije razagilina prouzročuju bilo kakvu klinički značajnu interferenciju sa supstratima ovih enzima. Istodobna primjena razagilina i entakapona povećava oralni klirens razagilina za 28 %. Tiramin/razagilin interakcija: Rezultati iz pet ispitivanja izloženosti tiraminu (u dobrovoljaca i bolesnika s PB), zajedno s rezultatima kućnog nadziranja krvnog tlaka nakon obroka (464 bolesnika liječenih s 0,5 ili 1 mg/dan razagilina ili placebom kao dodatnom terapijom levodopi kroz šest mjeseci bez restrikcija tiramina) i činjenicom da nije bilo prijava tiramin/razagilin interakcija u kliničkim ispitivanjima provedenim bez restrikcije tiramina, upućuju na to da se razagilin može primijenjivati sigurno bez dijetalnih restrikcija tiramina. 4.6 Plodnost, trudnoća i dojenje Nema dostupnih kliničkih podataka o izloženosti razagilinu u trudnoći. Ispitivanja na životinjama ne ukazuju na izravne ili neizravne štetne učinke na trudnoću, embrionalni/fetalni razvoj, porod ili postnatalni razvoj (vidjeti dio 5.3). Nužan je oprez kod propisivanja trudnicama. Eksperimentalni podaci pokazuju da razagilin inhibira sekreciju prolaktina i prema tome, može inhibirati laktaciju. Nije poznato izlučuje li se razagilin u majčino mlijeko. Nužan je oprez kod primjene razagilina u dojilja. 4.7 Utjecaj na sposobnost upravljanja vozilima i rada na strojevima Nisu provedene studije utjecaja na sposobnost upravljanja vozilima i rada na strojevima. Bolesnici trebaju biti oprezni pri upravljanju opasnim strojevima, uključujući motorna vozila, dok nisu dovoljno sigurni da AZILECT na njih ne utječe štetno. 4
5 4.8 Nuspojave U kliničkom programu s razagilinom je ukupno 1361 bolesnik bio liječen razagilinom kroz 3076,4 bolesničkih godina. U dvostruko slijepim placebo kontroliranim ispitivanjima 529 bolesnika bilo je liječeno razagilinom 1 mg/dan kroz 212 bolesničkih godina, a 539 bolesnika je primalo placebo kroz 213 bolesničkih godina. Monoterapija Niže navedeni popis uključuje nuspojave koje su bile prijavljene s većom incidencijom u placebo kontroliranim ispitivanjima, kod bolesnika koji su primali 1 mg/dan razagilina (razagilin skupina n=149, placebo skupina n=151). Nuspojave s najmanje 2 % razlike u odnosu na placebo su označene kurzivom. U zagradama je navedena incidencija nuspojava (% bolesnika) kod razagilina naspram placebu. Nuspojave su poredane prema učestalosti javljanja koristeći sljedeće pravilo: vrlo često ( 1/10), često ( 1/100 i < 1/10), manje često ( 1/1000 i < 1/100), rijetko ( 1/ i < 1/1000), vrlo rijetko (< 1/10 000). Infekcije i infestacije Često: influenca (4,7 % naspram 0,7 %) Dobroćudne, zloćudne i nespecificirane novotvorine (uključujući ciste i polipe) Često: karcinom kože (1,3 % naspram 0,7 %) Poremećaji krvi i limfnog sustava Često: leukopenija (1,3 % naspram 0 %) Poremećaji imunološkog sustava Često: alergija (1,3 % naspram 0,7 %) Poremećaji metabolizma i prehrane Manje često: smanjen apetit (0,7 % naspram 0 %) Psihijatrijski poremećaji Često: depresija (5,4 % naspram 2 %), halucinacije (1,3 % naspram 0,7 %) Poremećaji živčanog sustava Vrlo često: glavobolja (14,1 % naspram 11,9 %) Manje često: cerebrovaskularni događaj (0,7 % naspram 0 %) Poremećaji oka Često: konjunktivitis (2,7 % naspram 0,7 %) Poremećaji uha i labirinta Često: vrtoglavica (2,7 % naspram 1,3 %) Srčani poremećaji Često: angina pektoris (1,3 % naspram 0 %); Manje često: infarkt miokarda (0,7 % naspram 0 %) Poremećaji dišnog sustava, prsišta i sredoprsja Često: rinitis (3,4 % naspram 0,7 %) Poremećaji probavnog sustava Često: flatulencija (1,3 % naspram 0 %) Poremećaji kože i potkožnog tkiva Često: dermatitis (2,0 % naspram 0 %) Manje često: vezikulobulozni osip (0,7 % naspram 0 %) Poremećaji mišićno-koštanog sustava i vezivnog tkiva Često: mišićno-koštana bol (6,7 % naspram 2,6 %), bol u vratu (2,7 % naspram 0 %), artritis (1,3 % naspram 0,7 %) Poremećaji bubrega i mokraćnog sustava Često: urgencija mokrenja (1,3 % naspram 0,7 %). Opći poremećaji i reakcije na mjestu primjene 5
6 Često: vrućica (2,7 % naspram 1,3 %), slabost (2 % naspram. 0 %) Dodatna terapija Niže navedeni popis uključuje nuspojave koje su bile prijavljene s većom incidencijom u placebo kontroliranim ispitivanjima u bolesnika koji su primali 1 mg/dan razagilina (razagilin skupina n=380, placebo skupina n=388). U zagradama je navedena incidencija nuspojava (% bolesnika) kod razagilina naspram placebu. Nuspojave s najmanje 2 % razlike u odnosu na placebo su označene kurzivom. Nuspojave su poredane prema učestalosti javljanja koristeći sljedeće pravilo: vrlo često ( 1/10), često ( 1/100 i < 1/10), manje često ( 1/1000 i < 1/100), rijetko ( 1/ i < 1/1000), vrlo rijetko (< 1/10 000). Dobroćudne, zloćudne i nespecificirane novotvorine (uključujući ciste i polipe) Manje često: melanom kože (0,5 % naspram 0,3 %) Poremećaji metabolizma i prehrane Često: smanjen apetit (2,4 % naspram 0,8 %) Psihijatrijski poremećaji Često: halucinacije (2,9 % naspram 2,1 %), abnormalni snovi (2,1 % naspram 0,8 %) Manje često: konfuzija (0,8 % naspram 0,5 %) Poremećaji živčanog sustava Vrlo često: diskinezija (10,5 % naspram 6,2 %) Često: distonija (2,4 % naspram 0,8 %), sindrom karpalnog tunela (1,3 % naspram 0 %), poremećaj ravnoteže (1,6 % naspram 0,3 %) Manje često: cerebrovaskularni događaj (0,5 % naspram 0,3 %) Srčani poremećaji Manje često: angina pektoris (0,5 % naspram 0 %) Krvožilni poremećaji Često: ortostatska hipotenzija (3,9 % naspram 0,8 %) Poremećaji probavnog sustava Često: abdominalna bol (4,2 % naspram 1,3 %), konstipacija (4,2 % naspram. 2,1 %), mučnina i povraćanje (8,4 % naspram 6,2 %), suha usta (3,4 % naspram 1,8 %) Poremećaji kože i potkožnog tkiva Često: osip (1,1 % naspram 0,3 %) Poremećaji mišićno-koštanog sustava i vezivnog tkiva Često: atralgija (2,4 % naspram 2,1 %), bol u vratu (1,3 % naspram 0,5 %) Pretrage Često: smanjenje tjelesne težine (4,5 % naspram 1,5 %) Ozljede, trovanja i proceduralne komplikacije Često: pad (4,7 % naspram 3,4 %) Parkinsonova bolest je povezana sa simptomima halucinacija i konfuzije. U postmarketinškom iskustvu ovi su simptomi također opaženi u bolesnika s Parkinsonovom bolešću liječenih razagilinom. Poznato je da se ozbiljne nuspojave javljaju uz istodobnu primjenu SSRI-a, SNRI-a, tricikličkih/tetracikličkih antidepresiva i MAO inhibitora. U postmarketinškom razdoblju su prijavljeni slučajevi serotoninskog sindroma povezanog s agitacijom, konfuzijom, rigidnošću, pireksijom i mioklonusom u bolesnika liječenih antidepresivima/snri-em istodobno s razagilinom. U kliničkim ispitivanjima razagilina nije bila dozvoljena istodobna upotreba fluoksetina ili fuvoksamina s razagilinom, ali sljedeći antidepresivi i doze bili su dozvoljeni u ispitivanjima razagilina: amitriptilin 50 mg/dnevno, trazodon 100 mg/dnevno, citalopram 20 mg/dnevno, sertralin 100 mg/dnevno i paroksetin 30 mg/dnevno. Nije bilo slučajeva serotoninskog sindroma u kliničkom programu s razagilinom u kojem je 115 bolesnika istodobno bilo izloženo razagilinu i 6
7 triciklicima, a 141 bolesnik bio je izložen razagilinu i SSRI-ima/SNRI-ima. U postmarketinškom razdoblju su prijavljeni slučajevi povišenog krvnog tlaka, uključujući i rijetke slučajeve hipertenzivne krize povezane s ingestijom nepoznatih količina hrane bogate tiraminom u bolesnika koji su uzimali razagilin. Uz istodobnu primjenu MAO inhibitora i simpatomimetskih lijekova prijavljene su interakcije lijekova. U postmarketinškom razdoblju bio je jedan slučaj povišenog krvnog tlaka u bolesnika koji je primijenjivao oftalmički vazokonstriktor tetrahidrozolinklorid tijekom uzimanja razagilina. Poremećaji kontrole impulsa Kod bolesnika liječenih agonistima dopamina i/ili drugim dopaminergičkim lijekovima mogu se pojaviti patološko kockanje, povećan libido, hiperseksualnost, kompulzivno trošenje ili kupovanje, prejedanje i kompulzivno jedenje. U postmarketinškom razdoblju je prijavljen sličan model poremećaja kontrole impulsa sa razagilinom, što je također uključivalo kompulzije, opsesivne misli i impulzivno ponašanje (vidjeti dio 4.4). 4.9 Predoziranje Predoziranje: Simptomi prijavljeni nakon predoziranja AZILECTOM u dozama u rasponu od 3 mg do 100 mg uključivali su disforiju, hipomaniju, hipertenzivnu krizu i serotoninski sindrom. Predoziranje može biti povezano sa značajnom inhibicijom MAO-A i MAO-B. U ispitivanju s jednokratnom primjenom lijeka zdravi dobrovoljci su primili 20 mg/dan, a u desetodnevnom ispitivanju su primali 10 mg/dan. Štetni događaji bili su blagi ili umjereni i nisu bili povezani s liječenjem razagilinom. U ispitivanju postupnog povećavanja doze kod bolesnika na kroničnoj terapiji levodopom liječenih s 10 mg/dan razagilina prijavljene su neželjene kardiovaskularne reakcije (uključujući hipertenziju i posturalnu hipotenziju) koje su se povukle po prestanku liječenja. Ovi simptomi mogu nalikovati na one opažene kod neselektivnih MAO inhibitora. Nema specifičnog antidota. U slučaju predoziranja, bolesnike se mora nadzirati te započeti odgovarajuće simptomatsko i suportivno liječenje. 5. FARMAKOLOŠKA SVOJSTVA 5.1 Farmakodinamička svojstva Farmakoterapijska skupina: Antiparkinsonici, inhibitori monoaminooksidaze B, ATK oznaka: N04BD02 Mehanizam djelovanja: Pokazalo se da je razagilin potentan, ireverzibilan MAO-B selektivni inhibitor koji može prouzročiti povećanje izvanstanične razine dopamina u strijatumu. Povišena razina dopamina i posljedična povećana dopaminergička aktivnost vjerojatno posreduju korisne učinke razagilina viđene u modelima dopaminergičke motorne disfunkcije. Aktivni glavni metabolit je 1-aminoindan koji nije MAO-B inhibitor. Klinička ispitivanja: Djelotvornost razagilina je utvrđena u tri ispitivanja: kao monoterapija u ispitivanju I i kao dodatna terapija levodopi u ispitivanjima II i III. 7
8 Monoterapija: U ispitivanju I su 404 bolesnika metodom slučajnog odabira bili raspodijeljeni da prime placebo (138 bolesnika), razagilin 1 mg/dan (134 bolesnika) ili razagilin 2 mg/dan (132 bolesnika) i bili su liječeni 26 tjedana, nije bilo aktivnog komparatora. U ovom ispitivanju je primarna mjera djelotvornosti bila promjena od početne vrijednosti u ukupnom zbroju ujedinjene ljestvice za ocjenu Parkinsonove bolesti (engl. Unified Parkinson's Disease Rating Scale (UPDRS dijelovi I-III)). Razlika između srednje promjene od početnih vrijednosti do tjedna 26/ kraja praćenja (LOCF, engl. Last Observation Carried Forward; posljednje provedeno zapažanje preneseno dalje) je bila statistički značajna (UPDRS, dijelovi I-III: za razagilin 1 mg u usporedbi s placebom -4,2, 95 % CI [-5,7, -2,7]; p< 0,0001; za razagilin 2 mg u usporedbi s placebom -3,6, 95 % CI [-5,0, -2,1]; p< 0,0001, UPDRS motorička, dio II: za razagilin 1 mg u usporedbi s placebom 2,7, 95 % CI [-3,87, -1,55], p< 0,0001; za razagilin 2 mg u usporedbi s placebom -1,68, 95 % CI [-2,85, -0,51], p=0,0050). Učinak je bio očit, unatoč tome što je njegov razmjer bio skroman u ovoj populaciji bolesnika s blagom bolešću. Učinak na kvalitetu života bio je značajan i koristan (procijenjeno PD-QUALIF ljestvicom). Dodatna terapija: U ispitivanju II su bolesnici metodom slučajnog odabira bili raspodijeljeni da prime placebo (229 bolesnika), ili razagilin 1 mg/dan (231 bolesnik) ili inhibitor katehol-o-metil transferaze (engl. COMT), entakapon, 200 mg uzet zajedno s redovitim dozama levodope (LD)/inhibitora dekarboksilaze (227 bolesnika), i bili su liječeni 18 tjedana. U ispitivanju III, bolesnici su metodom slučajnog odabira bili raspodijeljeni da prime placebo (159 bolesnika), razagilin 0,5 mg/dan (164 bolesnika) ili razagilin 1 mg/dan (149 bolesnika) i bili su liječeni 26 tjedana. U oba je ispitivanja primarna mjera djelotvornosti bila promjena u srednjem broju sati provedenih u OFF stanju tijekom dana (određivano iz 24-satnih kućnih dnevnika popunjavanih tijekom 3 dana prije svakog posjeta procjene) od početne vrijednosti do razdoblja liječenja. U ispitivanju II, srednja razlika u broju sati provedenih u OFF stanju u usporedbi s placebom je iznosila -0,78 h, 95 % CI [-1,18, -0,39], p=0,0001. Srednje ukupno dnevno smanjenje u OFF vremenu u entakapon skupini (-0,80 h, 95 % CI [-1,20, -0,41], p<0,0001) bilo je slično onom opaženom u razagilin 1 mg skupini. U ispitivanju III srednja razlika u usporedbi s placebom je iznosila 0,94 h, 95 % CI [-1,36, -0,51], p< 0,0001. Također je postojalo i statistički značajno poboljšanje u razagilin 0,5 mg skupini u usporedbi s placebom, iako je razmjer poboljšanja bio manji. Pouzdanost rezultata primarnog ishoda djelotvornosti potvrđena je cijelim skupom dodatnih statističkih modela i pokazana je u tri kohorte (populacija planirana za liječenje (engl. intention to treat, (ITT)), prema protokolu i onim bolesnicima koji su dovršili ispitivanje). Sekundarne mjere djelotvornosti su uključivale opće procjene istraživača o poboljšanju, zbrojeve podljestvice aktivnosti svakodnevnog življenja (engl. Acitivities of Daily Living (ADL)) u OFF stanju te motoričke UPDRS u ON stanju. Razagilin je pokazao statistički značajnu korist u usporedbi s placebom. 5.2 Farmakokinetička svojstva Apsorpcija: Razagilin se brzo apsorbira, dosežući vršnu koncentraciju u plazmi (C max ) za približno 0,5 sati. Apsolutna bioraspoloživost pojedinačne doze razagilina je oko 36 %. Hrana ne utječe na T max razagilina, iako je C max smanjen za približno 60 %, a izloženost (AUC) za približno 20 % kada se lijek uzima s obrokom s visokim udjelom masnoća. Budući da se AUC bitno ne mijenja, razagilin se može primijeniti s hranom ili bez nje. Distribucija: Srednji volumen distribucije nakon jedne intravenske doze razagilina je 243 l. Vezanje za proteine plazme nakon pojedinačne oralne doze 14 C-obilježenog razagilina je približno 60 do 70 %. Metabolizam: Razagilin se gotovo potpuno biotransformira u jetri prije izlučivanja. Metabolizam razagilina se odvija kroz dva glavna puta: N-dealkilacijom i/ili hidroksilacijom te nastaju: 1-aminoindan, 3-hidroksi-N-propargil-1 aminoindan i 3-hidroksi-1 aminoindan. Pokusi in vitro indiciraju na to da su oba puta metabolizma razagilina ovisna o sustavu citokroma P450, s CYP1A2 8
9 kao glavnim izoenzimom uključenim u metabolizam razagilina. Također je otkriveno da je glavni eliminacijski put konjugacija razagilina i njegovih metabolita do stvaranja glukuronida. Izlučivanje: Nakon peroralne primjene 14 C-označenog razagilina, eliminacija se primarno odvija urinom (62,6 %), a sekundarno putem fecesa (21,8 %), s potpunim izlučivanjem 84,4 % doze lijeka tijekom razdoblja od 38 dana. Manje od 1 % razagilina se izlučuje nepromijenjeno u urinu. Linearnost/nelinearnost: Farmakokinetika razagilina je linearna s dozama u rasponu od 0,5-2 mg. Njegov terminalni poluvijek je 0,6-2 sata. Osobitosti kod bolesnika Bolesnici s oštećenjem jetre: U osoba s blagim oštećenjem jetre, AUC se povećava za 80 %, a C max za 38 %. U osoba s umjerenim oštećenjem jetre, AUC se povećava za 568 %, a C max za 83 % (vidjeti dio 4.4). Bolesnici s oštećenjem bubrega: Karakteristike farmakokinetike razagilina u osoba s blagim (CLcr ml/min) i umjerenim (CLcr ml/min) oštećenjem bubrega su slične onima zdravih osoba. 5.3 Neklinički podaci o sigurnosti primjene Neklinički podaci na temelju konvencionalnih ispitivanja sigurnosne farmakologije, toksičnosti ponovljenih doza i reproduktivne toksičnosti ne ukazuju na poseban rizik za ljude. Razagilin nije pokazao genotoksični potencijal in vivo te u nekoliko in vitro sustava korištenjem bakterija ili hepatocita. Prilikom aktivacije metabolita razagilin je inducirao porast kromosomskih aberacija u koncentracijama s prekomjernom citotoksičnošću, koje se ne mogu postići u kliničkim uvjetima primjene. Razagilin nije bio kancerogen u štakora pri sistemskoj ekspoziciji puta većoj od očekivane plazmatske ekspozicije u ljudi pri dozi od 1 mg/dan. U miševa je opažena povećana incidencija kombiniranih bronhiolarnih/alveolarnih adenoma i/ili karcinoma pri sistemskim ekspozicijama puta većim od očekivane plazmatske ekspozicije u ljudi pri dozi od 1 mg/dan. 6. FARMACEUTSKI PODACI 6.1 Popis pomoćnih tvari manitol kukuruzni škrob kukuruzni škrob, prethodno geliran silicijev dioksid, koloidni, bezvodni stearatna kiselina talk 6.2 Inkompatibilnosti Nije primjenjivo 6.3 Rok valjanosti Blisteri: 3 godine Bočice: 3 godine 9
10 6.4 Posebne mjere pri čuvanju lijeka Ne čuvati na temperaturi iznad 25ºC. 6.5 Vrsta i sadržaj spremnika Blisteri: Aluminij/aluminij blister pakovanja od 7, 10, 28, 30, 100 ili 112 tableta. Aluminij/aluminij perforirani blister djeljiv na jedinične doze u pakiranju od 10 x 1, 30 x 1 i 100 x 1 tableta. Bočice: Bijele bočice od polietilena visoke gustoće sa ili bez sigurnosnog zatvarača za djecu koje sadržavaju 30 tableta. Na tržištu se ne moraju nalaziti sve veličine pakovanja. 6.6 Posebne mjere za zbrinjavanje Nema posebnih zahtjeva. 7. NOSITELJ ODOBRENJA Teva B.V. Swensweg GA Haarlem Nizozemska 8. BROJ(EVI) ODOBRENJA ZA STAVLJANJE GOTOVOG LIJEKA U PROMET EU/1/04/304/ DATUM PRVOG ODOBRENJA ZA STAVLJANJE GOTOVOG LIJEKA U PROMET/ DATUM OBNOVE ODOBRENJA ZA STAVLJANJE GOTOVOG LIJEKA U PROMET Datum prvog odobrenja: 21. veljače Datum obnove odobrenja: 21. rujna DATUM REVIZIJE TEKSTA Podrobnije informacije o ovom lijeku dostupne su na web stranicama Europske agencije za lijekove 10
11 DODATAK II A. PROIZVOĐAČ ODGOVORAN ZA PUŠTANJE SERIJE LIJEKA U PROMET B. UVJETI ODOBRENJA 11
12 A. PROIZVOĐAČ ODGOVORAN ZA PUŠTANJE SERIJE LIJEKA U PROMET Naziv i adresa proizvođača odgovornog za puštanje serije lijeka u promet Teva Pharmaceuticals Europe B.V. Swensweg GA Haarlem Nizozemska Pliva Croatia Ltd. Prilaz baruna Filipovica Zagreb Hrvatska Teva Operations Poland Sp.z o.o. ul. Mogilska 80, Krakow, Poljska Na tiskanoj uputi o lijeku mora se navesti naziv i adresa proizvođača odgovornog za puštanje navedene serije u promet. B. UVJETI ODOBRENJA UVJETI ILI OGRANIČENJA VEZANA UZ OPSKRBU I UPORABU LIJEKA ZADANI NOSITELJU ODOBRENJA Lijek se izdaje na recept. UVJETI ILI OGRANIČENJA VEZANA UZ SIGURNU I DJELOTVORNU PRIMJENU LIJEKA Nije primjenjivo. DRUGI UVJETI PSURevi Sljedeći PSUR bit će predan s 3-godišnjom učestalošću (pokrivajući razdoblje od 3. siječnja do 2. siječnja 2013.). 12
13 DODATAK III OZNČAVANJE I UPUTA O LIJEKU 13
14 A. OZNAČAVANJE 14
15 PODACI KOJI SE MORAJU NALAZITI NA VANJSKOM PAKOVANJU (KUTIJA ZA BLISTER PAKOVANJE) 1. NAZIV GOTOVOG LIJEKA AZILECT 1 mg tablete razagilin 2. KVALITATIVNI I KVANTITAVNI SASTAV DJELATNIH TVARI Svaka tableta sadrži 1 mg razagilina (u obliku mesilata). 3. POPIS POMOĆNIH TVARI 4. FARMACEUTSKI OBLIK I SADRŽAJ 7 tableta 10 tableta 28 tableta 30 tableta 100 tableta 112 tableta 10 x 1 tableta 30 x 1 tableta 100 x 1 tableta 5. NAČIN I PUT(EVI) PRIMJENE LIJEKA Za primjenu kroz usta. Prije uporabe pročitati Uputu o lijeku. 6. POSEBNO UPOZORENJE DA LIJEK TREBA ČUVATI IZVAN DOHVATA I POGLEDA DJECE Čuvati izvan dohvata i pogleda djece. 7. DRUGA POSEBNA UPOZORENJA, AKO JE POTREBNO 8. ROK VALJANOSTI Rok valjanosti {MM/GGGG} 9. POSEBNE MJERE ČUVANJA Ne čuvati na temperaturi iznad 25 C. 15
16 10. POSEBNE MJERE ZA UKLANJANJE NEISKORIŠTENOG LIJEKA ILI OTPADNIH MATERIJALA KOJI POTJEČU OD LIJEKA, KADA JE POTREBNO 11. IME I ADRESA NOSITELJA ODOBRENJA ZA STAVLJANJE LIJEKA U PROMET Teva B.V GA Haarlem Nizozemska 12. BROJ(EVI) ODOBRENJA ZA STAVLJANJE GOTOVOG LIJEKA U PROMET EU/1/04/304/001 EU/1/04/304/002 EU/1/04/304/003 EU/1/04/304/004 EU/1/04/304/005 EU/1/04/304/006 EU/1/04/304/008 EU/1/04/304/009 EU/1/04/304/ BROJ SERIJE Broj serije {broj} 14. NAČIN PROPISIVANJA LIJEKA Lijek se izdaje na recept. 15. UPUTE ZA UPORABU 16. PODACI NA BRAILLEOVOM PISMU AZILECT 16
17 PODACI KOJE MORA NAJMANJE SADRŽAVATI BLISTER ILI STRIP 1. NAZIV GOTOVOG LIJEKA AZILECT 1 mg tablete razagilin 2. IME NOSITELJA ODOBRENJA ZA STAVLJANJE LIJEKA U PROMET Teva B.V. 3. ROK VALJANOSTI Rok valjanosti {MM/GGGG} 4. BROJ SERIJE Broj serije {broj} 5. DRUGO 17
18 PODACI KOJI SE MORAJU NALAZITI NA VANJSKOM PAKOVANJU (KUTIJA ZA BOČICU I NALJEPNICA NA BOČICI) 1. NAZIV GOTOVOG LIJEKA AZILECT 1 mg tablete razagilin 2. KVALITATIVNI I KVANTITAVNI SASTAV DJELATNIH TVARI Svaka tableta sadrži 1 mg razagilina (u obliku mesilata). 3. POPIS POMOĆNIH TVARI 4. FARMACEUTSKI OBLIK I SADRŽAJ 30 tableta 5. NAČIN I PUT(EVI) PRIMJENE LIJEKA Za primjenu kroz usta. Prije uporabe pročitati Uputu o lijeku. 6. POSEBNO UPOZORENJE DA LIJEK TREBA ČUVATI IZVAN DOHVATA I POGLEDA DJECE Čuvati izvan dohvata i pogleda djece. 7. DRUGA POSEBNA UPOZORENJA, AKO JE POTREBNO 8. ROK VALJANOSTI Rok valjanosti {MM/GGGG} 9. POSEBNE MJERE ČUVANJA Ne čuvati na temperaturi iznad 25 C. 10. POSEBNE MJERE ZA UKLANJANJE NEISKORIŠTENOG LIJEKA ILI OTPADNIH MATERIJALA KOJI POTJEČU OD LIJEKA, KADA JE POTREBNO 18
19 11. IME I ADRESA NOSITELJA ODOBRENJA ZA STAVLJANJE LIJEKA U PROMET Teva B.V GA Haarlem Nizozemska 12. BROJ(EVI) ODOBRENJA ZA STAVLJANJE GOTOVOG LIJEKA U PROMET EU/1/04/304/ BROJ SERIJE Broj serije {broj} 14. NAČIN PROPISIVANJA LIJEKA Lijek se izdaje na recept. 15. UPUTE ZA UPORABU 16. PODACI NA BRAILLEOVOM PISMU AZILECT 19
20 B. UPUTA O LIJEKU 20
21 UPUTA O LIJEKU: PODACI ZA KORISNIKA AZILECT 1 mg tablete razagilin Pažljivo pročitajte cijelu uputu prije nego počnete uzimati lijek. - Sačuvajte ovu uputu. Možda ćete ju trebati ponovo pročitati. - Ako imate dodatnih pitanja, obratite se svom liječniku ili ljekarniku. - Ovaj je lijek propisan Vama. Nemojte ga davati drugima. Može im štetiti, čak i ako imaju simptome jednake Vašima. - Ako primjetite bilo koju nuspojavu, potrebno je obavijestiti liječnika ili ljekarnika. U ovoj uputi: 1. Što je AZILECT i za što se koristi 2. Prije nego počnete uzimati AZILECT 3. Kako uzimati AZILECT 4. Moguće nuspojave 5. Kako čuvati AZILECT 6. Dodatne informacije 1. ŠTO JE AZILECT I ZA ŠTO SE KORISTI AZILECT se primjenjuje za liječenje Parkinsonove bolesti. Može se primjeniti zajedno s levodopom ili bez levodope (drugi lijek koji se primjenjuje za liječenje Parkinsonove bolesti). Kod Parkinsonove bolesti postoji gubitak stanica koje proizvode dopamin u mozgu. Dopamin je kemijska tvar u mozgu koja je uključena u kontrolu pokreta. AZILECT pomaže u povećavanju i održavanju razina dopamina u mozgu. 2. PRIJE NEGO POČNETE UZIMATI AZILECT Nemojte uzimati AZILECT - ako ste alergični (preosjetljivi) na razagilin ili bilo koji drugi sastojak lijeka AZILECT. - ako imate teške probleme s jetrom. Nemojte uzimati sljedeće lijekove dok uzimate AZILECT: - inhibitore monoaminooksidaze (MAO) (npr. za liječenje depresije ili Parkinsonove bolesti ili za bilo koju drugu indikaciju), uključujući lijekove i prirodne preparate bez recepta npr. gospinu travu - petidin (snažan lijek protiv boli). Morate čekati najmanje 14 dana nakon prestanka liječenja AZILECT-om i početka liječenja MAO inhibitorima ili petidinom. Budite posebno oprezni s AZILECT-om - ako imate blage do umjerene probleme s jetrom - morali biste razgovarati sa svojim liječnikom o bilo kakvim sumnjivim promjenama na koži. Djeca Ne preporučuje se primjena AZILECT-a u djece mlađe od 18 godina. Uzimanje drugih lijekova Obavijestite svog liječnika ili ljekarnika ako uzimate ili ste nedavno uzimali bilo koje druge lijekove, uključujući i one koje ste nabavili bez recepta, ili ako pušite ili namjeravate prestati pušiti. 21
22 Posavjetujte se s liječnikom prije uzimanja bilo kojeg od sljedećih lijekova zajedno s AZILECT-om: - određenih antidepresiva (selektivnih inhibitora ponovne pohrane serotonina, selektivnih inhibitora ponovne pohrane serotonina i noradrenalina, tricikličkih ili tetracikličkih antidepresiva) - antibiotika ciprofloksacina koji se upotrebljava protiv infekcija - dekstrometorfana koji se primjenjuje protiv kašlja - simpatomimetika poput onih sadržanih u kapima za oči, nazalnim i oralnim dekongestivima i lijekovima za prehladu koji sadrže efedrin ili pseudoefedrin. Istodobna primjena AZILECT-a s antidepresivima koji sadrže fluoksetin ili fluvoksamin mora se izbjegavati. Ako započinjete liječenje AZILECT-om, morate čekati najmanje 5 tjedana nakon prekida liječenja fluoksetinom. Ako započinjete liječenje fluoksetinom ili fluvoksaminom, morate čekati najmanje 14 dana nakon prekida liječenja AZILECT-om. Obavijestite Vašeg liječnika ako Vi ili Vaša obitelj/skrbnik primijetite da razvijate neuobičajeno ponašanje u smislu da se ne možete oduprijeti nagonu, potrebi ili žudnji za obavljanjem određenih aktivnosti, škodljivih ili loših za Vas ili druge. Ovo se zove poremećaj kontrole impulsa. Kod bolesnika koji uzimaju AZILECT i/ili druge lijekove koji se koriste za liječenje Parkinsonove bolesti bila su opažena ponašanja kao što su kompulzije, opsesivne misli, ovisnost o kockanju, prekomjerno trošenje, impulzivno ponašanje i nenormalno visok seksualni nagon ili povećanje misli i osjećanja povezanih sa seksualnošću. Vaš liječnik će možda morati prilagoditi dozu ili prekinuti liječenje. Uzimanje hrane i pića s AZILECT-om AZILECT se može uzimati sa ili bez hrane. Trudnoća i dojenje Obratite se svom liječniku ili ljekarniku za savjet prije nego uzmete bilo koji lijek. Upravljanje vozilima i strojevima Nisu provedena ispitivanja o učincima na sposobnost upravljanja vozilima i strojevima. Posavjetujte se sa svojim liječnikom prije upravljanja vozilima ili strojevima. 3. KAKO UZIMATI AZILECT Uvijek uzmite AZILECT točno onako kako Vam je rekao liječnik. Provjerite s Vašim liječnikom ili ljekarnikom ako niste sigurni. Uobičajena doza AZILECT-a je 1 tableta od 1 mg uzeta na usta jedanput dnevno. AZILECT se može uzeti sa ili bez hrane. Ako uzmete više AZILECT-a nego što ste trebali Ako mislite da ste možda uzeli previše AZILECT tableta, odmah se obratite svom liječniku ili ljekarniku. Ponesite sa sobom AZILECT kutiju/bočicu da pokažete svom liječniku ili ljekarniku. Ako ste zaboravili uzeti AZILECT Nemojte uzeti dvostruku dozu kako biste nadoknadili zaboravljenu dozu. Uzmite sljedeću dozu kako je uobičajeno, kada je vrijeme da je uzmete. Ako prestanete uzimati AZILECT Nemojte prestati uzimati AZILECT prije razgovora sa svojim liječnikom. 22
23 U slučaju bilo kakvih nejasnoća ili pitanja u vezi s primjenom ovog lijeka, obratite se svom liječniku ili ljekarniku. 4. MOGUĆE NUSPOJAVE Kao i svi drugi lijekovi, AZILECT može uzrokovati nuspojave iako se neće javiti kod svakoga. Sljedeće nuspojave su prijavljene u placebo kontroliranim kliničkim ispitivanjima: Učestalost niže navedenih mogućih nuspojava definirana je koristeći sljedeće pravilo: Vrlo često (javljaju se u više od 1 na 10 korisnika) Često (javljaju se u 1 do 10 na 100 korisnika) Manje često (javljaju se u 1 do 10 na 1000 korisnika) Rijetko (javljaju se u 1 do 10 na korisnika) Vrlo rijetko (javljaju se u manje od 1 na korisnika) Nepoznato (učestalost se ne može procijeniti iz dostupnih podataka) Vrlo često - abnormalni pokreti (diskinezija) - glavobolja Često: - bol u trbuhu - pad - alergija - vrućica - gripa (influenca) - opće loše osjećanje (malaksalost) - bol u vratu - bol u prsima (angina pektoris) - nizak krvni tlak pri ustajanju u stojeći položaj sa simptomima kao što su omaglica/ošamućenost (ortostatska hipotenzija) - smanjen apetit - zatvor - suha usta - mučnina i povraćanje - nadutost - abnormalni rezultati krvnih testova (leukopenija) - bol u zglobovima (artralgija) - mišićno-koštana bol - upala zglobova (artritis) - utrnulost i slabost mišića ruke (sindrom karpalnog tunela) - smanjenje tjelesne težine - abnormalni snovi - poteškoće u mišićnoj koordinaciji (poremećaj ravnoteže) - depresija - omaglica (vrtoglavica) - produljene mišićne kontrakcije (distonija) - curenje nosa (rinitis) - nadražaj kože (dermatitis) - osip - crvenilo očiju (konjunktivitis) - hitan nagon za mokrenjem 23
24 Manje često: - moždani udar (cerebrovaskularni događaj) - srčani udar (infarkt miokarda) - osip s mjehurićima (vezikulobulozni osip) Dodatno, rak kože je bio prijavljen u oko 1 % bolesnika u placebo kontroliranim kliničkim ispitivanjima. Ipak, znanstveni dokazi upućuju na to da je Parkinsonova bolest, a ne neki lijek posebno, povezana s većim rizikom od karcinoma kože (ne isključivo melanom). Morate razgovarati sa svojim liječnikom o svakoj sumnjivoj promjeni na koži. Parkinsonova bolest se povezuje sa simptomima halucinacija i smetenosti. Ovi simptomi su opaženi i tijekom razdoblja nakon stavljanja lijeka u promet u bolesnika s Parkinsonovom bolešću liječenih AZlLECT-om. Zabilježeni su slučajevi bolesnika koji se, tijekom uzimanja jednog ili više lijekova za liječenje Parkinsonove bolesti, nisu mogli oduprijeti nagonu ili iskušenju da izvode određenu radnju koja bi mogla biti škodljiva za njih same ili za druge. Ovo se zove poremećaj kontrole impulsa. Kod bolesnika koji uzimaju AZILECT i/ili druge lijekove koji se koriste za liječenje Parkinsonove bolesti opaženo je sljedeće: - Opsesivne misli ili impulzivno ponašanje. - Jak nagon za pretjeranim kockanjem unatoč ozbiljnim posljedicama po njih ili obitelj. - Promijenjen ili povećan seksualni interes i ponašanje koje je značajno zabrinjavajuće za Vas ili druge, primjerice povećan seksualni nagon. - Nekontrolirano prekomjerno kupovanje ili trošenje. Obavijestite svog liječnika ako iskusite ovakvo ponašanje; s njim ćete razgovarati o načinima kako kontrolirati ili smanjiti simptome. Ako primjetite bilo koju nuspojavu, potrebno je obavijestiti liječnika ili ljekarnika. 5. KAKO ČUVATI AZILECT Čuvati izvan dohvata i pogleda djece. AZILECT se ne smije upotrijebiti nakon isteka roka valjanosti navedenog na kutiji, bočici ili blisteru. Rok valjanosti odnosi se na zadnji dan navedenog mjeseca. Ne čuvati na temperaturi iznad 25 o C. Lijekovi se ne smiju uklanjati putem otpadnih voda ili kućnog otpada. Pitajte svog ljekarnika kako ukloniti lijekove koje više ne trebate. Ove mjere pomoći će u zaštiti okoliša. 6. DODATNE INFORMACIJE Što AZILECT sadrži - Djelatna tvar je razagilin. Svaka tableta sadrži 1 mg razagilina (u obliku mesilata). - Pomoćne tvari su manitol, koloidni, bezvodni silicijev dioksid, kukuruzni škrob, prethodno geliran kukuruzni škrob, stearatna kiselina, talk. Kako AZILECT izgleda i sadržaj pakovanja AZILECT tablete su bijele do bjelkaste, okrugle, plosnate tablete kosih rubova, s utisnutom oznakom GIL i 1 ispod toga na jednoj strani, i bez oznake na drugoj strani. 24
25 Tablete su dostupne u blister pakovanjima od 7, 10, 28, 30, 100 i 112 tableta, u perforirnim blisterima djeljivim na jedinične doze u pakiranjima od 10 x 1, 30 x1 i 100 x 1 tableta ili u bočici koja sadrži 30 tableta. Na tržištu se ne moraju nalaziti sve veličine pakovanja. Nositelj odobrenja za stavljanje u promet gotovog lijeka i proizvođač Nositelj odobrenja Proizvođač Teva B.V. Teva Pharmaceuticals Europe B.V. Swensweg 5 Swensweg GA Haarlem 2031 GA Haarlem Nizozemska Nizozemska Pliva Croatia Ltd. Prilaz baruna Filipovica Zagreb Hrvatska Teva Operations Poland Sp.z o.o. ul. Mogilska 80, Krakow, Poljska Za sve informacije o ovom lijeku obratite se lokalnom predstavniku nositelja odobrenja za stavljanje u promet gotovog lijeka: België/Belgique/Belgien Teva Pharma Belgium N.V./S.A./AG Tél/Tel: България Тева Фармасютикълс България ЕООД Teл: Česká republika Teva Pharmaceuticals CR, s.r.o. Tel: Danmark Teva Denmark A/S Tlf: Deutschland Teva GmbH Tel: Eesti Teva Eesti esindus UAB Sicor Biotech Eesti filiaal Tel: Lietuva UAB "Sicor Biotech" Tel: Luxembourg/Luxemburg Teva Pharma Belgium N.V./S.A./AG, Belgique/Belgien Tél/Tel: Magyarország Teva Gyógyszergyár Zrt. Tel.: Malta Teva Pharmaceuticals Ireland L-Irlanda Tel: Nederland Teva Nederland B.V. Tel: +31 (0) Norge Teva Norway AS Tlf:
26 Ελλάδα Teva Ελλάς Α.Ε. Τηλ: España Teva Pharma, S.L.U. Tel: France Teva Santé Tél: Hrvatska Pliva Hrvatska d.o.o. Tel.: Österreich ratiopharm Arzneimittel Vertriebs-GmbH Tel.: +43 (0) Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel.: Portugal Teva Pharma - Produtos Farmacêuticos Lda Tel: România Teva Pharmaceuticals S.R.L Tel: Ireland Teva Pharmaceuticals Ireland Tel: Slovenija Pliva Ljubljana d.o.o. Tel: Ísland Vistor hf. Sími: Italia Teva Italia S.r.l. Tel: Κύπρος Teva Ελλάς Α.Ε., Ελλάδα Τηλ: Latvija UAB "Sicor Biotech" filiāle Latvijā Tel: Slovenská republika TEVA Pharmaceuticals Slovakia s.r.o. Tel: Suomi/Finland ratiopharm Oy Puh/Tel: Sverige Teva Sweden AB Tel: United Kingdom Teva UK Limited Tel: +44(0) Uputa je zadnji puta odobrena u 26
Aufklärung Nr. 11: Influenza Kroatisch / Hrvatski
 Na zaštitno cijepljenje protiv influence ( gripe ) Akutna oboljenja dišnih putova ubrajaju se među najčešća oboljenja ljudi. Uzrokuje ih mnoštvo raznih uzročnika, a osobito virusi. Osobitu ulogu igra virus
Na zaštitno cijepljenje protiv influence ( gripe ) Akutna oboljenja dišnih putova ubrajaju se među najčešća oboljenja ljudi. Uzrokuje ih mnoštvo raznih uzročnika, a osobito virusi. Osobitu ulogu igra virus
Gebrauchsinformation: Information für Patienten. Levetiracetam Teva 250 mg Filmtabletten Levetiracetam
 Gebrauchsinformation: Information für Patienten Levetiracetam Teva 250 mg Filmtabletten Levetiracetam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Levetiracetam Teva 250 mg Filmtabletten Levetiracetam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Mission Berlin. Deutsch lernen und unterrichten Arbeitsmaterialien. Mission Berlin 24 Sat otkucava
 24 Sat otkucava Ana pronalazi metalnu futrolu, onu istu koju je sakrila 1961. godine. Ne uspijeva da je otvori jer je zahrđala. Kad joj to konačno podje za rukom, u futroli pronalazi ključ. Da li je to
24 Sat otkucava Ana pronalazi metalnu futrolu, onu istu koju je sakrila 1961. godine. Ne uspijeva da je otvori jer je zahrđala. Kad joj to konačno podje za rukom, u futroli pronalazi ključ. Da li je to
NJEMAČKI JEZIK. osnovna razina ISPIT SLUŠANJA (Hörverstehen) NJEB.26.HR.R.K2.12 NJE B IK-2 D-S026. NJE B IK-2 D-S026.indd 1 25.3.2015.
 NJEMAČKI JEZIK osnovna razina ISPIT SLUŠANJA () NJE26.HR.R.K2.12 12 1.indd 1 25.3.2015. 10:17:09 Prazna stranica 99 2.indd 2 25.3.2015. 10:17:09 OPĆE UPUTE Pozorno pročitajte sve upute i slijedite ih.
NJEMAČKI JEZIK osnovna razina ISPIT SLUŠANJA () NJE26.HR.R.K2.12 12 1.indd 1 25.3.2015. 10:17:09 Prazna stranica 99 2.indd 2 25.3.2015. 10:17:09 OPĆE UPUTE Pozorno pročitajte sve upute i slijedite ih.
Njemački jezik. osnovna razina ISPIT SLUŠANJA (Hörverstehen) NJEB.21.HR.R.K2.12 NJE B IK-2 D-S021. NJE B IK-2 D-S021.indd 1 11.6.
 osnovna razina ISPIT SLUŠANJA () NJE21.HR.R.K2.12 6765 12 1.indd 1 11.6.2014 15:52:19 Prazna stranica 99 2.indd 2 11.6.2014 15:52:19 OPĆE UPUTE Pozorno pročitajte sve upute i slijedite ih. Ne okrećite
osnovna razina ISPIT SLUŠANJA () NJE21.HR.R.K2.12 6765 12 1.indd 1 11.6.2014 15:52:19 Prazna stranica 99 2.indd 2 11.6.2014 15:52:19 OPĆE UPUTE Pozorno pročitajte sve upute i slijedite ih. Ne okrećite
NJEMAČKI JEZIK. viša razina ISPIT SLUŠANJA (Hörverstehen) NJEA.24.HR.R.K3.12 NJE A IK-3 D-S024. NJE A IK-3 D-S024.indd 1 24.3.2015.
 NJEMČKI JEZIK viša razina ISPIT SLUŠNJ () NJE.24.HR.R.K3.12 NJE IK-3 D-S024 12 1 NJE IK-3 D-S024.indd 1 24.3.2015. 11:06:43 Prazna stranica NJE IK-3 D-S024 99 2 NJE IK-3 D-S024.indd 2 24.3.2015. 11:06:43
NJEMČKI JEZIK viša razina ISPIT SLUŠNJ () NJE.24.HR.R.K3.12 NJE IK-3 D-S024 12 1 NJE IK-3 D-S024.indd 1 24.3.2015. 11:06:43 Prazna stranica NJE IK-3 D-S024 99 2 NJE IK-3 D-S024.indd 2 24.3.2015. 11:06:43
Gebrauchsinformation: Information für Patienten. Picato 150 Mikrogramm/g Gel Ingenolmebutat
 Gebrauchsinformation: Information für Patienten Picato 150 Mikrogramm/g Gel Ingenolmebutat Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Patienten Picato 150 Mikrogramm/g Gel Ingenolmebutat Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Ovaleap 300 I.E./0,5 ml Injektionslösung Ovaleap 450 I.E./0,75 ml Injektionslösung Ovaleap 900 I.E./1,5 ml Injektionslösung Follitropin alfa Dieses Arzneimittel
Gebrauchsinformation: Information für Anwender Ovaleap 300 I.E./0,5 ml Injektionslösung Ovaleap 450 I.E./0,75 ml Injektionslösung Ovaleap 900 I.E./1,5 ml Injektionslösung Follitropin alfa Dieses Arzneimittel
Gebrauchsinformation: Information für den Anwender Karvea 150 mg Filmtabletten Irbesartan
 Gebrauchsinformation: Information für den Anwender Karvea 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für den Anwender Karvea 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Karvea 75 mg Filmtabletten Irbesartan
 Gebrauchsinformation: Information für Anwender Karvea 75 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Karvea 75 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tractocile 6,75 mg/0,9 ml Injektionslösung Atosiban
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tractocile 6,75 mg/0,9 ml Injektionslösung Atosiban Lesen Sie sich diese Packungsbeilage bitte sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tractocile 6,75 mg/0,9 ml Injektionslösung Atosiban Lesen Sie sich diese Packungsbeilage bitte sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Njemački Hrvatski Deutsch Kroatisch. Gesundheitswegweiser. Migrantinnen und Migranten im Landkreis Darmstadt-Dieburg. www.ladadi.
 Njemački Hrvatski Deutsch Kroatisch Gesundheitswegweiser Migrantinnen und Migranten im Landkreis Darmstadt-Dieburg www.ladadi.de Dieses Faltblatt wurde in verschiedene Sprachen übersetzt. Sie finden es
Njemački Hrvatski Deutsch Kroatisch Gesundheitswegweiser Migrantinnen und Migranten im Landkreis Darmstadt-Dieburg www.ladadi.de Dieses Faltblatt wurde in verschiedene Sprachen übersetzt. Sie finden es
BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH. Jahrgang 1998 Ausgegeben am 13. Oktober 1998 Teil III
 P. b. b. Erscheinungsort Wien, Verlagspostamt 1030 Wien BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 1998 Ausgegeben am 13. Oktober 1998 Teil III 162. Abkommen zwischen der Republik Österreich
P. b. b. Erscheinungsort Wien, Verlagspostamt 1030 Wien BUNDESGESETZBLATT FÜR DIE REPUBLIK ÖSTERREICH Jahrgang 1998 Ausgegeben am 13. Oktober 1998 Teil III 162. Abkommen zwischen der Republik Österreich
Gebrauchsinformation: Information für den Anwender. Thyrogen 0,9 mg Pulver zur Herstellung einer Injektionslösung Thyrotropin alfa
 Gebrauchsinformation: Information für den Anwender Thyrogen 0,9 mg Pulver zur Herstellung einer Injektionslösung Thyrotropin alfa Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für den Anwender Thyrogen 0,9 mg Pulver zur Herstellung einer Injektionslösung Thyrotropin alfa Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für Anwender. Galvus 50 mg Tabletten Vildagliptin
 Gebrauchsinformation: Information für Anwender Galvus 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Galvus 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Patienten. Aerius 5 mg Filmtabletten Desloratadin
 Gebrauchsinformation: Information für Patienten Aerius 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten Aerius 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender. Jalra 50 mg Tabletten Vildagliptin
 Gebrauchsinformation: Information für Anwender Jalra 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Jalra 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Leitfaden Gesundheit
 Leitfaden Gesundheit für Migrantinnen und und Migranten Migranten in Baden-Württemberg in Jena Allemand Tedesco Njemački Alemão Germanikå- Português - Italiano English Hrvatski Ellhnikå Français Deutsch
Leitfaden Gesundheit für Migrantinnen und und Migranten Migranten in Baden-Württemberg in Jena Allemand Tedesco Njemački Alemão Germanikå- Português - Italiano English Hrvatski Ellhnikå Français Deutsch
Gebrauchsinformation: Information für Patienten. Januvia 50 mg Filmtabletten Wirkstoff: Sitagliptin
 Gebrauchsinformation: Information für Patienten Januvia 50 mg Filmtabletten Wirkstoff: Sitagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Januvia 50 mg Filmtabletten Wirkstoff: Sitagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Leitfaden Gesundheit
 Leitfaden Gesundheit für Migrantinnen und Migranten in Aachen mit aktuellen Informationen zu: Krankenversicherung Arztbesuch Krankmeldung Medikamenten Vorsorgeuntersuchungen Verhalten im Notfall Stand
Leitfaden Gesundheit für Migrantinnen und Migranten in Aachen mit aktuellen Informationen zu: Krankenversicherung Arztbesuch Krankmeldung Medikamenten Vorsorgeuntersuchungen Verhalten im Notfall Stand
DODATAK I SAŽETAK OPISA SVOJSTAVA LIJEKA
 DODATAK I SAŽETAK OPISA SVOJSTAVA LIJEKA 1 1. NAZIV LIJEKA Helicobacter Test INFAI 75 mg prašak za oralnu otopinu 2. KVALITATIVNI I KVANTITATIVNI SASTAV Jedna posudica sadrži 75 mg praška 13 C-uree. Za
DODATAK I SAŽETAK OPISA SVOJSTAVA LIJEKA 1 1. NAZIV LIJEKA Helicobacter Test INFAI 75 mg prašak za oralnu otopinu 2. KVALITATIVNI I KVANTITATIVNI SASTAV Jedna posudica sadrži 75 mg praška 13 C-uree. Za
Profil Magazin o želji za potomstvom kod muškaraca
 www.profertil.eu ROFERTIL Od želje za potomstvom do željenog potomstva Savjeti za obiteljsku sreću Spermiji u formi za samo tri mjeseca Spermiji i njihova kvaliteta o muškoj plodnosti Broj patenta: 50.219
www.profertil.eu ROFERTIL Od želje za potomstvom do željenog potomstva Savjeti za obiteljsku sreću Spermiji u formi za samo tri mjeseca Spermiji i njihova kvaliteta o muškoj plodnosti Broj patenta: 50.219
VI PITATE, MI ODGOVARAMO: u informativnom centru pitanja i fraze sa prevodom
 VI PITATE, MI ODGOVARAMO: u informativnom centru pitanja i fraze sa prevodom oder In der Stadt zum ersten mal Wortschatz mit Tipps, häufigsten Fragen und Antworten Einleitung Stadtpark 1, Wien An der Rezeption:
VI PITATE, MI ODGOVARAMO: u informativnom centru pitanja i fraze sa prevodom oder In der Stadt zum ersten mal Wortschatz mit Tipps, häufigsten Fragen und Antworten Einleitung Stadtpark 1, Wien An der Rezeption:
Osnovna škola, 8. razred
 Osnovna škola, 8. razred TRANKSRIPTI TEKSTOVA Text 1: UČITELJI TREBAJU GLASNO PROČITATI UPUTU, A POTOM I TEKST U SKLADU S UPUTOM. Iako to neće učenicima posebno objašnjavati jer je navedeno u uputi, učitelji
Osnovna škola, 8. razred TRANKSRIPTI TEKSTOVA Text 1: UČITELJI TREBAJU GLASNO PROČITATI UPUTU, A POTOM I TEKST U SKLADU S UPUTOM. Iako to neće učenicima posebno objašnjavati jer je navedeno u uputi, učitelji
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Orgalutran 0,25 mg/0,5 ml Injektionslösung Ganirelix
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Orgalutran 0,25 mg/0,5 ml Injektionslösung Ganirelix Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Orgalutran 0,25 mg/0,5 ml Injektionslösung Ganirelix Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
NJEMAČKI JEZIK. osnovna razina ISPIT ČITANJA I PISANJA (Leseverstehen und Schreiben) NJEB.26.HR.R.K1.20 NJE B IK-1 D-S026
 NJEMČKI JEZIK osnovna razina ISPIT ČITNJ I PISNJ (Leseverstehen und Schreiben) NJ26.HR.R.K1.20 12 1.indd 1 25.3.2015. 12:51:14 Prazna stranica 99 2.indd 2 25.3.2015. 12:51:15 OPĆE UPUTE Pozorno pročitajte
NJEMČKI JEZIK osnovna razina ISPIT ČITNJ I PISNJ (Leseverstehen und Schreiben) NJ26.HR.R.K1.20 12 1.indd 1 25.3.2015. 12:51:14 Prazna stranica 99 2.indd 2 25.3.2015. 12:51:15 OPĆE UPUTE Pozorno pročitajte
Gebrauchsinformation: Information für den Anwender. Bondronat 50 mg Filmtabletten Ibandronsäure
 Gebrauchsinformation: Information für den Anwender Bondronat 50 mg Filmtabletten Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für den Anwender Bondronat 50 mg Filmtabletten Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Januvia 100 mg Filmtabletten Wirkstoff: Sitagliptin
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Januvia 100 mg Filmtabletten Wirkstoff: Sitagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Januvia 100 mg Filmtabletten Wirkstoff: Sitagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Predgovor. Drage porodice!
 Predgovor Drage porodice! Parlamentsdirektion/WILKE Ova brošura - Pravilna ishrana od samog početka! bebina prva žličica je zamišljena kao pomoć roditeljima, temeljena na najnovijim naučnim spoznajama.
Predgovor Drage porodice! Parlamentsdirektion/WILKE Ova brošura - Pravilna ishrana od samog početka! bebina prva žličica je zamišljena kao pomoć roditeljima, temeljena na najnovijim naučnim spoznajama.
B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für den Anwender ellaone 30 mg Tablette Ulipristalacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für den Anwender ellaone 30 mg Tablette Ulipristalacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender. Eucreas 50 mg/850 mg Filmtabletten Eucreas 50 mg/1000 mg Filmtabletten
 Gebrauchsinformation: Information für Anwender Eucreas 50 mg/850 mg Filmtabletten Eucreas 50 mg/1000 mg Filmtabletten Vildagliptin/Metforminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Eucreas 50 mg/850 mg Filmtabletten Eucreas 50 mg/1000 mg Filmtabletten Vildagliptin/Metforminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Bolesti prostate: dobroćudno povećanje prostate
 Bolesti prostate: dobroćudno povećanje prostate HRVATSKI 2 BOLESTI PROSTATE BOLESTI PROSTATE 3 mokraćni mjehur prostata mokraćna cijev spužvasto tkivo sjemenovod pasjemenik sjemenik sjemene vrećice debelo
Bolesti prostate: dobroćudno povećanje prostate HRVATSKI 2 BOLESTI PROSTATE BOLESTI PROSTATE 3 mokraćni mjehur prostata mokraćna cijev spužvasto tkivo sjemenovod pasjemenik sjemenik sjemene vrećice debelo
1. Was ist Synflorix und wofür wird es angewendet?
 Gebrauchsinformation: Information für Anwender Synflorix Injektionssuspension in einer Fertigspritze Pneumokokkenpolysaccharid-Konjugatimpfstoff (adsorbiert) Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Synflorix Injektionssuspension in einer Fertigspritze Pneumokokkenpolysaccharid-Konjugatimpfstoff (adsorbiert) Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Xarelto 10 mg Filmtabletten Rivaroxaban
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xarelto 10 mg Filmtabletten Rivaroxaban Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xarelto 10 mg Filmtabletten Rivaroxaban Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Efient 10 mg Filmtabletten Efient 5 mg Filmtabletten Prasugrel
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Efient 10 mg Filmtabletten Efient 5 mg Filmtabletten Prasugrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Efient 10 mg Filmtabletten Efient 5 mg Filmtabletten Prasugrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
2. WAS MÜSSEN SIE VOR DER EINNAHME VON AZILECT BEACHTEN?
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER AZILECT 1mg Tabletten Rasagilin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. - Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER AZILECT 1mg Tabletten Rasagilin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. - Heben
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Bonviva 3 mg Injektionslösung Ibandronsäure
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Bonviva 3 mg Injektionslösung Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Bonviva 3 mg Injektionslösung Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für Patienten
 Gebrauchsinformation: Information für Patienten Jakavi 5 mg Tabletten Jakavi 10 mg Tabletten Jakavi 15 mg Tabletten Jakavi 20 mg Tabletten Ruxolitinib Dieses Arzneimittel unterliegt einer zusätzlichen
Gebrauchsinformation: Information für Patienten Jakavi 5 mg Tabletten Jakavi 10 mg Tabletten Jakavi 15 mg Tabletten Jakavi 20 mg Tabletten Ruxolitinib Dieses Arzneimittel unterliegt einer zusätzlichen
Gebrauchsinformation: Information für Anwender. RotaTeq Lösung zum Einnehmen Rotavirus-Lebendimpfstoff
 Gebrauchsinformation: Information für Anwender RotaTeq Lösung zum Einnehmen Rotavirus-Lebendimpfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Ihr Kind mit diesem Impfstoff geimpft
Gebrauchsinformation: Information für Anwender RotaTeq Lösung zum Einnehmen Rotavirus-Lebendimpfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Ihr Kind mit diesem Impfstoff geimpft
Gebrauchsinformation: Information für Patienten. Cosentyx 150 mg Injektionslösung in einem Fertigpen. Secukinumab
 Gebrauchsinformation: Information für Patienten Cosentyx 150 mg Injektionslösung in einem Fertigpen Secukinumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle
Gebrauchsinformation: Information für Patienten Cosentyx 150 mg Injektionslösung in einem Fertigpen Secukinumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle
Abkommen über Soziale Sicherheit Sporazum o socijalnom osiguranju. Deutsche Versicherungsnummer Nemački broj osiguranja. Aktenzeichen: Broj predmeta:
 Abkommen über Soziale Sicherheit Sporazum o socilnom osiguranju D-SRB 203 Versicherungsträger in Nosilac osiguran u Deutschland: Nemačkoj Serbien: Srbiji: Deutsche Rentenversicherung Bayern Süd 84024 Landshut
Abkommen über Soziale Sicherheit Sporazum o socilnom osiguranju D-SRB 203 Versicherungsträger in Nosilac osiguran u Deutschland: Nemačkoj Serbien: Srbiji: Deutsche Rentenversicherung Bayern Süd 84024 Landshut
Road Safety 2014. How is your country doing? STRASSENVERKEHRSSICHERHEIT: Wie sieht es in Ihrem Land aus?
 Road Safety 2014 How is your country doing? STRASSENVERKEHRSSICHERHEIT: Wie sieht es in Ihrem Land aus? SÉCURITÉ ROUTIÈRE: Quelle est la situation dans votre pays? Transport Die EU hat das Ziel, die Anzahl
Road Safety 2014 How is your country doing? STRASSENVERKEHRSSICHERHEIT: Wie sieht es in Ihrem Land aus? SÉCURITÉ ROUTIÈRE: Quelle est la situation dans votre pays? Transport Die EU hat das Ziel, die Anzahl
B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für den Anwender ellaone 30 mg Tablette Ulipristalacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für den Anwender ellaone 30 mg Tablette Ulipristalacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Campsite management asks its dear guests to obey the following house rules: Only guests registered at the reception can be accommodated in the
 Campsite management asks its dear guests to obey the following house rules: Only guests registered at the reception can be accommodated in the campsite. The choice of space in the camping area is free,
Campsite management asks its dear guests to obey the following house rules: Only guests registered at the reception can be accommodated in the campsite. The choice of space in the camping area is free,
Basisinformationen zum Aufenthaltsrecht für Flüchtlinge. Osnovne informacije o pravu boravka za izbeglice
 Rechtshilfebroschüre Deutsch / Serbisch Basisinformationen zum Aufenthaltsrecht für Flüchtlinge - besonders aus Ex-Jugoslawien - Osnovne informacije o pravu boravka za izbeglice - naročito iz bivše Jugoslavije
Rechtshilfebroschüre Deutsch / Serbisch Basisinformationen zum Aufenthaltsrecht für Flüchtlinge - besonders aus Ex-Jugoslawien - Osnovne informacije o pravu boravka za izbeglice - naročito iz bivše Jugoslavije
Gebrauchsinformation: Information für Anwender. Xolair 150 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Omalizumab
 Gebrauchsinformation: Information für Anwender Xolair 150 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Omalizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
Gebrauchsinformation: Information für Anwender Xolair 150 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Omalizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
3. Klasse, Hausaufgaben lösen: Leitfaden für die Lehrperson
 3. Klasse, Hausaufgaben lösen: Leitfaden für die Lehrperson 3.71 Hausaufgaben Ziele E wissen, welche Rahmenbedingungen bei den Hausaufgaben wichtig sind E begleiten ihr Kind beim Überprüfen der Rahmenbedingungen
3. Klasse, Hausaufgaben lösen: Leitfaden für die Lehrperson 3.71 Hausaufgaben Ziele E wissen, welche Rahmenbedingungen bei den Hausaufgaben wichtig sind E begleiten ihr Kind beim Überprüfen der Rahmenbedingungen
Gebrauchsinformation: Information für Patienten. Atriance 5 mg/ml Infusionslösung
 Gebrauchsinformation: Information für Patienten Atriance 5 mg/ml Infusionslösung Nelarabin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Patienten Atriance 5 mg/ml Infusionslösung Nelarabin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
B. PACKUNGSBEILAGE 19
 B. PACKUNGSBEILAGE 19 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ellaone 30 mg Tablette Ulipristalacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
B. PACKUNGSBEILAGE 19 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ellaone 30 mg Tablette Ulipristalacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Levitra 10 mg Filmtabletten Vardenafil
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Levitra 10 mg Filmtabletten Vardenafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Levitra 10 mg Filmtabletten Vardenafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Kritični parametri projektiranja garaža
 UDK 625.748.28.001.1 Građevinar 6/2013 Primljen / Received: 30.12.2012. Ispravljen / Corrected: 12.5.2013. Prihvaćen / Accepted: 21.5.2013. Dostupno online / Available online: 10.7.2013. Kritični parametri
UDK 625.748.28.001.1 Građevinar 6/2013 Primljen / Received: 30.12.2012. Ispravljen / Corrected: 12.5.2013. Prihvaćen / Accepted: 21.5.2013. Dostupno online / Available online: 10.7.2013. Kritični parametri
Bolesti pluća Bez disanja nema života
 Bolesti pluća Bez disanja nema života DEUTSCH 2 BOLESTI PLUĆA BOLESTI PLUĆA 3 desno plućno krilo rebra štitnjača dušnik bronh Ova brošura za pacijente treba Vam na lagani i razumljivi način objasniti simptome,
Bolesti pluća Bez disanja nema života DEUTSCH 2 BOLESTI PLUĆA BOLESTI PLUĆA 3 desno plućno krilo rebra štitnjača dušnik bronh Ova brošura za pacijente treba Vam na lagani i razumljivi način objasniti simptome,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. VIAGRA 25 mg Filmtabletten VIAGRA 50 mg Filmtabletten VIAGRA 100 mg Filmtabletten Sildenafilcitrat
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER VIAGRA 25 mg Filmtabletten VIAGRA 50 mg Filmtabletten VIAGRA 100 mg Filmtabletten Sildenafilcitrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER VIAGRA 25 mg Filmtabletten VIAGRA 50 mg Filmtabletten VIAGRA 100 mg Filmtabletten Sildenafilcitrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
ivjeti i raditi u Hrvatskoj Leben und Arbeiten in Kroatien
 ivjeti i raditi u Hrvatskoj Leben und Arbeiten in Kroatien Mobilität und Integration Ausgabe: 2006 Inhalt: Eine gute Entscheidung treffen Mein eigener Chef sein Eine gute und sichere Arbeitsstelle Die
ivjeti i raditi u Hrvatskoj Leben und Arbeiten in Kroatien Mobilität und Integration Ausgabe: 2006 Inhalt: Eine gute Entscheidung treffen Mein eigener Chef sein Eine gute und sichere Arbeitsstelle Die
VAT after Croatia joins the EU. Umsatzsteuer nach dem EU-Beitritt Kroatiens. PDV nakon ulaska Hrvatske u EU
 VAT after Croatia joins the EU Umsatzsteuer nach dem EU-Beitritt Kroatiens PDV nakon ulaska Hrvatske u EU Success is a matter of setting the right goals. And having the right partner. 2 VAT after Croatia
VAT after Croatia joins the EU Umsatzsteuer nach dem EU-Beitritt Kroatiens PDV nakon ulaska Hrvatske u EU Success is a matter of setting the right goals. And having the right partner. 2 VAT after Croatia
IBM ISV/TP-Beitrittserklärung
 IBM ISV/TPBeitrittserklärung (Vom ISV auszufüllen und an den Distributor LIS.TEC) FIRMENNAME DES ISVs/TPs: Firmenadresse des ISVs/TPs: PLZ/Stadt: Land: Germany Telefon: +49 Fax: +49 Email: Kontaktperson
IBM ISV/TPBeitrittserklärung (Vom ISV auszufüllen und an den Distributor LIS.TEC) FIRMENNAME DES ISVs/TPs: Firmenadresse des ISVs/TPs: PLZ/Stadt: Land: Germany Telefon: +49 Fax: +49 Email: Kontaktperson
Gebrauchsinformation: Information für Anwender. Levitra 5 mg Filmtabletten Vardenafil
 Gebrauchsinformation: Information für Anwender Levitra 5 mg Filmtabletten Vardenafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Levitra 5 mg Filmtabletten Vardenafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Patienten. Onglyza 2,5 mg Filmtabletten Saxagliptin
 Gebrauchsinformation: Information für Patienten Onglyza 2,5 mg Filmtabletten Saxagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten Onglyza 2,5 mg Filmtabletten Saxagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten. Janumet 50 mg/850 mg Filmtabletten
 Gebrauchsinformation: Information für Patienten Janumet 50 mg/850 mg Filmtabletten Wirkstoffe: Sitagliptin und Metforminhydrochlorid (1 Tablette enthält 50 mg Sitagliptin und 850 mg Metforminhydrochlorid)
Gebrauchsinformation: Information für Patienten Janumet 50 mg/850 mg Filmtabletten Wirkstoffe: Sitagliptin und Metforminhydrochlorid (1 Tablette enthält 50 mg Sitagliptin und 850 mg Metforminhydrochlorid)
Elternratgeber: Ausbildung in Deutschland Savjetnik za roditelje: Strukovno obrazovanje u Njemačkoj
 KAUSA Elternratgeber: Ausbildung in Deutschland Savjetnik za roditelje: Strukovno obrazovanje u Njemačkoj Zugewanderte Eltern unterstützen ihre Kinder beim Einstieg ins Berufsleben Roditelji doseljenici
KAUSA Elternratgeber: Ausbildung in Deutschland Savjetnik za roditelje: Strukovno obrazovanje u Njemačkoj Zugewanderte Eltern unterstützen ihre Kinder beim Einstieg ins Berufsleben Roditelji doseljenici
Gebrauchsinformation: Information für Patienten. Ivabradin
 Gebrauchsinformation: Information für Patienten Procoralan 5 mg Filmtabletten Procoralan 7.5 mg Filmtabletten Ivabradin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Gebrauchsinformation: Information für Patienten Procoralan 5 mg Filmtabletten Procoralan 7.5 mg Filmtabletten Ivabradin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Einwilligungserklärung zur Datenverarbeitung
 Einwilligungserklärung zur Datenverarbeitung 1. Sie möchten sich bei Dräger online bewerben. Mit einer Registrierung auf den Dräger Karriere Seiten zeigen Sie uns Ihr Interesse an einer Beschäftigung bei
Einwilligungserklärung zur Datenverarbeitung 1. Sie möchten sich bei Dräger online bewerben. Mit einer Registrierung auf den Dräger Karriere Seiten zeigen Sie uns Ihr Interesse an einer Beschäftigung bei
Gebrauchsinformation: Information für Anwender Ketek 400 mg Filmtabletten Telithromycin
 Gebrauchsinformation: Information für Anwender Ketek 400 mg Filmtabletten Telithromycin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Ketek 400 mg Filmtabletten Telithromycin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Geschäftszeichen MI11-5781. Stand: Mai 2012. Durchführung zur zwischenstaatlichen Arbeitsvermittlung. Pflegekräfte
 Geschäftszeichen MI11-5781 Stand: Mai 2012 Durchführung zur zwischenstaatlichen Arbeitsvermittlung Pflegekräfte Durchführungsanweisungen zur zwischenstaatlichen Arbeitsvermittlung aufgrund der Vermittlungsabsprache
Geschäftszeichen MI11-5781 Stand: Mai 2012 Durchführung zur zwischenstaatlichen Arbeitsvermittlung Pflegekräfte Durchführungsanweisungen zur zwischenstaatlichen Arbeitsvermittlung aufgrund der Vermittlungsabsprache
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Xenical 120 mg Hartkapseln Orlistat
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xenical 120 mg Hartkapseln Orlistat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xenical 120 mg Hartkapseln Orlistat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Aktuelle Marktrends und Aussichten
 Aktuelle Marktrends und Aussichten Leiterplatten Michael Gasch, Data4PCB ZVEI- Forum electronica 2010, 11.11.2010, 10 11 Uhr Folie 1 Entwicklung des Wechselkurses : US$ 2005 bis 2010/09 1,60 1,58 1,56
Aktuelle Marktrends und Aussichten Leiterplatten Michael Gasch, Data4PCB ZVEI- Forum electronica 2010, 11.11.2010, 10 11 Uhr Folie 1 Entwicklung des Wechselkurses : US$ 2005 bis 2010/09 1,60 1,58 1,56
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Fasturtec 1,5 mg/ml Pulver und Lösungsmittel zur Herstellung eines Infusionslösungskonzentrats, Rasburicase Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Fasturtec 1,5 mg/ml Pulver und Lösungsmittel zur Herstellung eines Infusionslösungskonzentrats, Rasburicase Lesen Sie die gesamte Packungsbeilage sorgfältig
Tretman izdvajanja (Oustourcing-a) u pravu nadzora prema nemačkom Zakonu o nadzoru osiguranja i Direktivi o solventnosti II
 Martin LANGE Tretman izdvajanja (Oustourcing-a) u pravu nadzora prema nemačkom Zakonu o nadzoru osiguranja i Direktivi o solventnosti II ČLANCI 49 Apstrakt Nemački Zakon o nadzoru osiguranja (Versicherungsaufsichtsgesetz;
Martin LANGE Tretman izdvajanja (Oustourcing-a) u pravu nadzora prema nemačkom Zakonu o nadzoru osiguranja i Direktivi o solventnosti II ČLANCI 49 Apstrakt Nemački Zakon o nadzoru osiguranja (Versicherungsaufsichtsgesetz;
Gebrauchsinformation: Information für Anwender. Tarceva 25 mg Filmtabletten Tarceva 100 mg Filmtabletten Tarceva 150 mg Filmtabletten Erlotinib
 Gebrauchsinformation: Information für Anwender Tarceva 25 mg Filmtabletten Tarceva 100 mg Filmtabletten Tarceva 150 mg Filmtabletten Erlotinib Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender Tarceva 25 mg Filmtabletten Tarceva 100 mg Filmtabletten Tarceva 150 mg Filmtabletten Erlotinib Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
CERAN Kochflächen / CERAN Cooktop panels
 CERAN Kochflächen / CERAN Cooktop panels Approved cleaners with SCHOTT contracts Home Tech SCHOTT AG Hattenbergstrasse 10 55122 Mainz Germany E-Mail: info.ceran@schott.com www.schott-ceran.com Approved
CERAN Kochflächen / CERAN Cooktop panels Approved cleaners with SCHOTT contracts Home Tech SCHOTT AG Hattenbergstrasse 10 55122 Mainz Germany E-Mail: info.ceran@schott.com www.schott-ceran.com Approved
HRVATSKA UDRUGA ENERGETSKIH CERTIFIKATORA HUEC CROATIAN ASSOCIATION OF BUILDING ENERGY ASSESSORS
 HRVATSKA UDRUGA ENERGETSKIH CERTIFIKATORA HUEC CROATIAN ASSOCIATION OF BUILDING ENERGY ASSESSORS Überblick der Tätigkeiten im Gebäudezertifizierungsbereich, energetische Sanierungsprojekte und Bau von
HRVATSKA UDRUGA ENERGETSKIH CERTIFIKATORA HUEC CROATIAN ASSOCIATION OF BUILDING ENERGY ASSESSORS Überblick der Tätigkeiten im Gebäudezertifizierungsbereich, energetische Sanierungsprojekte und Bau von
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. FOSAVANCE 70 mg/5.600 I.E. Tabletten Wirkstoffe: Alendronsäure/Colecalciferol
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER FOSAVANCE 70 mg/5.600 I.E. Tabletten Wirkstoffe: Alendronsäure/Colecalciferol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER FOSAVANCE 70 mg/5.600 I.E. Tabletten Wirkstoffe: Alendronsäure/Colecalciferol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
Die chemische Zusammensetzung des Geflügelfleisches Ein Vergleich zwischen Broilern, Suppenhühnern, Puten, Enten und Gänsen
 tehnologija mesa UDK: 637.54 65.045:636.52/.598 Die Osnivač chemische i izdavač: Zusammensetzung Institut za higijenu des Gefl ügelfl i tehnologiju eisches... mesa, Beograd Die chemische Zusamennensetzung
tehnologija mesa UDK: 637.54 65.045:636.52/.598 Die Osnivač chemische i izdavač: Zusammensetzung Institut za higijenu des Gefl ügelfl i tehnologiju eisches... mesa, Beograd Die chemische Zusamennensetzung
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Tamiflu 75 mg Hartkapseln Oseltamivir
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tamiflu 75 mg Hartkapseln Oseltamivir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tamiflu 75 mg Hartkapseln Oseltamivir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Die Mitgliedstaaten der EU
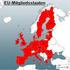 Die Mitgliedstaaten der EU Arbeitsaufträge: 1. Trage in die einzelnen EU-Mitgliedstaaten die jeweilige Abkürzung ein! 2. Schlage in deinem Atlas nach, wo die Hauptstädte der einzelnen Länder liegen und
Die Mitgliedstaaten der EU Arbeitsaufträge: 1. Trage in die einzelnen EU-Mitgliedstaaten die jeweilige Abkürzung ein! 2. Schlage in deinem Atlas nach, wo die Hauptstädte der einzelnen Länder liegen und
Gebrauchsinformation: Information für Patienten. PANTOZOL Control 20 mg magensaftresistente Tabletten Pantoprazol
 Gebrauchsinformation: Information für Patienten PANTOZOL Control 20 mg magensaftresistente Tabletten Pantoprazol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten PANTOZOL Control 20 mg magensaftresistente Tabletten Pantoprazol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
INFORMATIONEN zu den europäischen Verordnungen über soziale Sicherheit
 Deutsche Rentenversicherung Bayern Süd Am Alten Viehmarkt 2, 84028 Landshut Postanschrift: 84024 Landshut Telefon 0871 81-0, Telefax 0871 81-2150 Bürgertelefon 0800 1000 48015 service@drv-bayernsued.de
Deutsche Rentenversicherung Bayern Süd Am Alten Viehmarkt 2, 84028 Landshut Postanschrift: 84024 Landshut Telefon 0871 81-0, Telefax 0871 81-2150 Bürgertelefon 0800 1000 48015 service@drv-bayernsued.de
BOSNISCH/KROATISCH/SERBISCH
 BOSNISCH/KROATISCH/SERBISCH Impressum Das österreichische Gesundheitssystem Ein Wegweiser für Migrantinnen und Migranten Gesundheit Hand in Hand Herausgeber: Volkshilfe Wien Weinberggasse 77, 1190 Wien
BOSNISCH/KROATISCH/SERBISCH Impressum Das österreichische Gesundheitssystem Ein Wegweiser für Migrantinnen und Migranten Gesundheit Hand in Hand Herausgeber: Volkshilfe Wien Weinberggasse 77, 1190 Wien
UNIVERSITÄT ZAGREB PHILOSOPHISCHE FAKULTÄT ABTEILUNG FÜR GERMANISTIK DIPLOMARBEIT AN DER ABTEILUNG FÜR GERMANISTIK.
 UNIVERSITÄT ZAGREB PHILOSOPHISCHE FAKULTÄT ABTEILUNG FÜR GERMANISTIK DIPLOMARBEIT AN DER ABTEILUNG FÜR GERMANISTIK Martina Jelenić Die deutsche Sprache im Tourismus von Zadar sprachbiographischer Aspekt
UNIVERSITÄT ZAGREB PHILOSOPHISCHE FAKULTÄT ABTEILUNG FÜR GERMANISTIK DIPLOMARBEIT AN DER ABTEILUNG FÜR GERMANISTIK Martina Jelenić Die deutsche Sprache im Tourismus von Zadar sprachbiographischer Aspekt
NJEMAČKI JEZIK viša razina
 Nacionalni centar za vanjsko vrednovanje obrazovanja NJEMAČKI JEZIK viša razina NACIONALNI ISPIT svibanj 28. TEXTE ZUM LESEVERSTEHEN 12 UPUTE U ovoj knjižici nalaze se tekstovi na kojima se ispituje vještina
Nacionalni centar za vanjsko vrednovanje obrazovanja NJEMAČKI JEZIK viša razina NACIONALNI ISPIT svibanj 28. TEXTE ZUM LESEVERSTEHEN 12 UPUTE U ovoj knjižici nalaze se tekstovi na kojima se ispituje vještina
Trudna?! NJEMACKl. BOSANSKl HRVATSKl SRPSKl. Informacije za migrantice o savjetovanju i pomoći u trudnoći
 Trudna?! Informacije za migrantice o savjetovanju i pomoći u trudnoći ˇ NJEMACKl BOSANSKl HRVATSKl SRPSKl Informationen für Migrantinnen in Deutschland zu Beratung und Hilfen bei Schwangerschaft in Deutsch/Bosnisch/Kroatisch/
Trudna?! Informacije za migrantice o savjetovanju i pomoći u trudnoći ˇ NJEMACKl BOSANSKl HRVATSKl SRPSKl Informationen für Migrantinnen in Deutschland zu Beratung und Hilfen bei Schwangerschaft in Deutsch/Bosnisch/Kroatisch/
B. PACKUNGSBEILAGE 1
 B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Adempas 0,5 mg Filmtabletten Adempas 1 mg Filmtabletten Adempas 1,5 mg Filmtabletten Adempas 2 mg Filmtabletten Adempas 2,5 mg Filmtabletten
B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Adempas 0,5 mg Filmtabletten Adempas 1 mg Filmtabletten Adempas 1,5 mg Filmtabletten Adempas 2 mg Filmtabletten Adempas 2,5 mg Filmtabletten
Gebrauchsinformation: Information für Anwender. Bonviva 150 mg Filmtabletten Ibandronsäure
 Gebrauchsinformation: Information für Anwender Bonviva 150 mg Filmtabletten Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Bonviva 150 mg Filmtabletten Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte Packungsbeilage
Univerzitet Novi Sad Ekonomski fakultet Subotica. Aleksandra Breu WIRTSCHAFTSDEUTSCH FÜR ANFÄNGER 2/2
 Univerzitet Novi Sad Ekonomski fakultet Subotica Aleksandra Breu WIRTSCHAFTSDEUTSCH FÜR ANFÄNGER 2/2 Anja hat Geburtstag 1. Heute ist Samstag. Die Familie Meier ist zu Hause. Nach dem Frühstück gehen sie
Univerzitet Novi Sad Ekonomski fakultet Subotica Aleksandra Breu WIRTSCHAFTSDEUTSCH FÜR ANFÄNGER 2/2 Anja hat Geburtstag 1. Heute ist Samstag. Die Familie Meier ist zu Hause. Nach dem Frühstück gehen sie
Puregon wird zur Behandlung von Unfruchtbarkeit in folgenden Fällen eingesetzt:
 RA 2540 EU P10 (REF 4.0) Gebrauchsinformation: Information für den Anwender Puregon 600 IE/0,72 ml Injektionslösung Follitropin beta Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
RA 2540 EU P10 (REF 4.0) Gebrauchsinformation: Information für den Anwender Puregon 600 IE/0,72 ml Injektionslösung Follitropin beta Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Xarelto 15 mg Filmtabletten Xarelto 20 mg Filmtabletten Rivaroxaban
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xarelto 15 mg Filmtabletten Xarelto 20 mg Filmtabletten Rivaroxaban Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xarelto 15 mg Filmtabletten Xarelto 20 mg Filmtabletten Rivaroxaban Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme
WIR+ 4 Radna bilježnica njemačkog jezika za 7. razred osnovne škole 4. godina učenja
 Inhaltsverzeichnis: Modul 10 3 Modul 11 48 Modul 12 77 Lektion 1 3 Lektion 4 48 Lektion 7 77 Lektion 2 16 Lektion 5 57 Lektion 8 87 Lektion 3 29 Lektion 6 62 Lektion 9 94 Wortschatz 1-3 41 Wortschatz 4-6
Inhaltsverzeichnis: Modul 10 3 Modul 11 48 Modul 12 77 Lektion 1 3 Lektion 4 48 Lektion 7 77 Lektion 2 16 Lektion 5 57 Lektion 8 87 Lektion 3 29 Lektion 6 62 Lektion 9 94 Wortschatz 1-3 41 Wortschatz 4-6
Gebrauchsinformation: Information für Patienten. Komboglyze 2,5 mg/1000 mg Filmtabletten Saxagliptin/Metformin
 Gebrauchsinformation: Information für Patienten Komboglyze 2,5 mg/1000 mg Filmtabletten Saxagliptin/Metformin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Komboglyze 2,5 mg/1000 mg Filmtabletten Saxagliptin/Metformin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Abteilung Prävention. «Rođenje: početak veze za cijeli život» Informacije za roditelje o pripremama za porođaj, rođenju i tjednima nakon toga
 Abteilung Prävention «Rođenje: početak veze za cijeli život» Informacije za roditelje o pripremama za porođaj, rođenju i tjednima nakon toga Bilješka o izdavaču Gesundheitsdepartement Basel-Stadt 2012
Abteilung Prävention «Rođenje: početak veze za cijeli život» Informacije za roditelje o pripremama za porođaj, rođenju i tjednima nakon toga Bilješka o izdavaču Gesundheitsdepartement Basel-Stadt 2012
Vaše zadovoljstvo odmorom naša je odgovornost!
 Vaše zadovoljstvo odmorom naša je odgovornost! Želite pronaći idealno mjesto za vaš godišnji odmor? Zovite RONU! Vaš pouzdani partner u turizmu. Ili se baviti iznajmljivanjem apartmana bez obaveza poput
Vaše zadovoljstvo odmorom naša je odgovornost! Želite pronaći idealno mjesto za vaš godišnji odmor? Zovite RONU! Vaš pouzdani partner u turizmu. Ili se baviti iznajmljivanjem apartmana bez obaveza poput
Selbständig in Deutschland Fachbegriffe in zwei Sprachen
 Foto: fotogestoeber fotolia.com Selbständig in Deutschland Fachbegriffe in zwei Sprachen Förderprogramm Integration durch Qualifizierung (IQ) Deutsch Bosnisch (bosanski) Begriffe aus der Gründungsunterstützung
Foto: fotogestoeber fotolia.com Selbständig in Deutschland Fachbegriffe in zwei Sprachen Förderprogramm Integration durch Qualifizierung (IQ) Deutsch Bosnisch (bosanski) Begriffe aus der Gründungsunterstützung
INTERWIEV: Vesna Pusić Završetak pregovora je samo pitanje europske političke odluke Verhandlungsabschluss hängt ab vom politischen Entscheid Europas
 29 LIPANJ 2011. JUNI 2011 ČASOPIS HRVATSKOG KULTURNOG KLUBA U ŠVICARSKOJ ZEITSCHRIFT DES KROATISCHEN KULTURKLUBS IN DER SCHWEIZ INTERWIEV: Vesna Pusić Završetak pregovora je samo pitanje europske političke
29 LIPANJ 2011. JUNI 2011 ČASOPIS HRVATSKOG KULTURNOG KLUBA U ŠVICARSKOJ ZEITSCHRIFT DES KROATISCHEN KULTURKLUBS IN DER SCHWEIZ INTERWIEV: Vesna Pusić Završetak pregovora je samo pitanje europske političke
Sada jedem sa velikima!
 Bosnisch/Kroatisch/Serbisch Sada jedem sa velikima! Ispravno jesti za djecu od jedne do tri godine Jetzt ess ich mit den Großen! Richtig essen für Ein- bis Dreijährige 1 Vorwort Liebe Eltern! Unsere Kinder
Bosnisch/Kroatisch/Serbisch Sada jedem sa velikima! Ispravno jesti za djecu od jedne do tri godine Jetzt ess ich mit den Großen! Richtig essen für Ein- bis Dreijährige 1 Vorwort Liebe Eltern! Unsere Kinder
WIR+ 3 Udžbenik njemačkog jezika za 6. razred osnovne škole 3. godina učenja
 Giorgio Motta Mirjana Klobučar WIR+ 3 Udžbenik njemačkog jezika za 6. razred osnovne škole 3. godina učenja Udžbenik WIR+ 3 usklađen je s Nastavnim planom i programom za osnovnu školu (2006.) i Hrvatskim
Giorgio Motta Mirjana Klobučar WIR+ 3 Udžbenik njemačkog jezika za 6. razred osnovne škole 3. godina učenja Udžbenik WIR+ 3 usklađen je s Nastavnim planom i programom za osnovnu školu (2006.) i Hrvatskim
1. Was ist RoActemra und wofür wird es angewendet?
 Gebrauchsinformation: Information für Anwender RoActemra 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung Tocilizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für Anwender RoActemra 20 mg/ml Konzentrat zur Herstellung einer Infusionslösung Tocilizumab Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
