Thermodynamik (Wärmelehre) III kinetische Gastheorie
|
|
|
- Michaela Lilli Kästner
- vor 6 Jahren
- Abrufe
Transkript
1 Physik A VL6 ( ) Thermodynamik (Wärmelehre) III kinetische Gastheorie Thermische Bewegung Die kinetische Gastheorie Mikroskopische Betrachtung des Druckes Mawell sche Geschwindigkeitserteilung gdes idealen Gases 1
2 Wärme und Bewegung Wärme ist kinetische Energie kleinster Bewegungen on Molekülen Diese Bewegung g ist nicht sichtbar, aber die makroskopische Folge ist Wärme historisch: on J. Ingenhousz 1785 entdeckt, on R. Brown 188 wiederentdeckt (Pollenbewegung) kaum beachtete Entdeckung ( Störeffekt, Rauschen) G.L. Guoy (1889): Brown sche Bewegung ist Beweis der kontinuierlichen Molekülbewegung A. Einstein (1905): quantitatie Analyse: mathematische Gesetze beschreiben die Bewegung der Moleküle, auf der Basis der Prinzipen der kinetischmolekularen Theorie der Wärme J. Ingenhousz ( ) R. Brown ( ) A. Einstein ( )
3 Wärme und Bewegung Die Brown sche Molekularbewegung Thermodynamik III die in Wasser schwimmenden Polystyrolkügelchen y führen Zitterbewegungen g aus Die Bewegung on Atomen oder Molekülen wird auf größere Körper übertragen, diese ollführen ruck- artige, zitternde Wegänderungen Der Weg der Bewegung g ist zufällig Bedeutung der Brown schen Molekularbewegung - Festkörper sind starr N Atome oder Moleküle in festen Abständen nur 3 räumliche Freiheitsgrade keine Statistik notwendig - Moleküle: Bewegung, Rotation, Schwingung zusätzliche Freiheitsgrade der Bewegung - Gase: N Moleküle führen statistisch unabhängige Bewegungen aus N Bewegungsgleichungen zur Beschreibung allgemeine, statistische Beschreibung (ideales Gas!) sinnoll 3
4 Wärme und Bewegung Thermodynamik III Eigenschaften eines idealen Gases Annahmen es gelten die Gesetze der klassischen Mechanik (Newton sche Aiome) alle auftretenden Geschwindigkeiten sind klein gegen die Lichtgeschwindigkeit: 1000 m/s, ß /c die zahl ist sehr groß: N >>> 1 der mittlere e Abstand der e >> Durchmesser der die Ausdehnung der ist ernachlässigbar die Wechselwirkung (Anziehungs- und Abstossungskräfte) zwischen den Gasteilchen kann ernachlässigt werden kinetische Energie >> potentielle Energie der Gasteilchen führen im wesentlichen nur elastische Stöße mit den Wänden und untereinander aus 4
5 Wärme und Bewegung Eigenschaften eines idealen Gases mechanisches Modell des idealen Gases Druck im idealen Gas: Folge des Aufpralls on auf Fläche des Stempels im mechanischen Modell: mit zunehmender kinetischer Energie der Stahlkugeln wird der Stempel weiter nach oben geschoben! 5
6 Mikroskopische Betrachtung des Druckes Betrachtung einer Einzelsituation: ein (Masse m) trifft auf den Stempel (Masse M, M >> m) und wird dort reflektiert elastischer Stoß: Anwendung on Energie- und Impulserhaltungssatz für Komponente in -Richtung Energieerhaltung: (Annahmen nur kinetische Energien) 1 m m ' + M S y m r r Impulserhaltung: s Impulserhaltung: m m' + M S y r M 6
7 Mikroskopische Betrachtung des Druckes Geschwindigkeit aus Energieerhaltungssatz in Impulserhaltungssatz einsetzen ( Mechanik elastischer Stoß): m auf den Stempel übertragene Energie S m + M E kin m MS M ( m + M ) Berücksichtigung on: Stempelmasse M >>> m E 4m M kin E kin m M 1 + M 4 m m M E kin 1 m Es wird (näherungsweise) keine kinetische Energie auf den Stempel übertragen: S 0 ' Durch die Stöße der auf den Stempel entsteht trotzdem eine Kraft Impulsübertrag beachten 7
8 Mikroskopische Betrachtung des Druckes Impulserhaltungssatz: m m' + P aus Stoßgesetz (orehrige Betrachtung): Stempel ' Stempel. Newton sches Gesetz: P m p r F r dp dt Übertragung auf eine große -Zahl N: alle, die sich in der Schicht mit der Dicke s Δ t r F r P Δt or dem Stempel befinden, treffen innerhalb der Zeit Δt auf den Stempel. N zahl Definition der dichte n V Volumen mit V s A N n V nδta mittlere Kraft zahl N im Volumen 8
9 Mikroskopische Betrachtung des Druckes Berechnung der Kraft auf den Stempel aus dem Impulsübertrag und der Zahl der Stempel P m p 1 Stempel 1 m F P p Δt Δt Δt 1 F m N n A N N F n ΔtA Δt nm A N n A Der Druck ergibt sich daraus zu: F p nm 4nE kin A kin p 4 n E Schwächen und unrealistische Annahmen der Herleitung der Formel: 1. Die haben nicht alle dieselbe Geschwindigkeit.. Nur mit > 0 tragen zum Druck bei. 9
10 Mikroskopische Betrachtung des Druckes Verbesserung der Berechnung: bisher p 4 n E kin Das Geschwindigkeitsquadrat wird durch das mittlere Geschwindigkeitsquadrat aller ersetzt: N, i N 1 1 i Von den N im Volumen V bewegen sich nur N/6 auf die Wand zu (zur Erinnerung: Gasteilchen 3 Translationsfreiheitsgrade mit je Richtungen, nur 1 Freiheitsgrad in 1 Richtung führt zur Kollision m.d. Wand) 1 r 6 da die Geschwindigkeitserteilung gisotrop ist. nur 1/6 des Impulses wird pro Volumen an die Wand übertragen 10
11 Mikroskopische Betrachtung des Druckes Verbesserung der Berechnung: E kin bisher 1 m mittlere kinetische Energie der : p 4 n E kin r mittlerer Druck herorgerufen durch die : p n m n m 6 m r n m E kin p 3 n E kin Die dichte n N/V ist, also folgt: pv 3 N E kin E 3 kin E kin : mittlere kinetische Energie des gesamten Gases 11
12 Mikroskopische Betrachtung des Druckes Verbesserung der Berechnung: pv 3 E kin E kin : mittlere kinetische Energie des gesamten Gases da im idealen Gas keine Kräfte der untereinander wirken, ist die gesamte gemittelte potentielle Energie des Gases ernachlässigbar. Die innere Energie U des Systems ist gleich der kinetischen Gesamtenergie aller im Gas U N E kin E kin pv U 3 Zustandsgleichung des idealen Gases 1
13 Mikroskopische Betrachtung des Druckes pv 3 3 U E kin Ekin pv N kb T 3 3 jeder Translations-Freiheitsgrad hat eine Energie on 0,5 k BT Diese Gleichung gilt in guter Näherung nur für... einatomige Gase (z.b. Edelgase, wie He, Ne, Xe) mittlere Temperaturen, d.h. etwa Zimmertemperatur. In der Nähe des absoluten Nullpunktes kondensieren iele Gase, bei Temperaturen > 1000 C ionisieren sie. wenn die innere Energie bei einem idealen Gas konstant ist, dann ist auch die Temperatur T konstant Temperatur T zur mittleren kinetischen Energie der Gasmoleküle Definition der Temperatur über obige Formel! 13
14 Mawell sche Geschwindigkeitserteilung des idealen Gases (Mawell-Boltzmann-Verteilung) Eperiment: Geschwindigkeitserteilung on Kugeln Kugeln werden aus mechanischem Modell herausgeschleudert ΔN/Δ Anteil der Moleküle mit Geschwindigkeit im Interall Δ. 14
15 Mawell sche Geschwindigkeitserteilung des idealen Gases (Mawell-Boltzmann-Verteilung) ΔN/Δ dn d f (, T ) ep m k T B 15
16 Mawell sche Geschwindigkeitserteilung des idealen Gases (Mawell-Boltzmann-Verteilung) ΔN/Δ dn d f (, T ) ep m k T B 16
17 Zusammenfassung Stöße mit der Wand (z.b. Kolben) in einem idealen Gas Es wird keine kinetische Energie auf den Stempel übertragen Gasmoleküle durch die Stöße der auf den Stempel entsteht aber eine Kraft Impulsübertrag Mittelung über iele : mittleres Geschwindigkeitsquadrat F Stempel mit der Fläche A Zylinder: Volumen V() pv 3 3 U E kin Ekin pv N kbt 3 3 Temperatur T zur mittleren kinetischen Energie der Gasmoleküle Definition der Temperatur über obige Formel! Mawell sche Geschwindigkeitserteilung (Mawell-Boltzmann-Verteilung) dn d m f (, T ) ep kbt 17
Einführung in die Physik I. Wärme 2 Kinetische Gastheorie
 Einführung in die Physik I Wärme Kinetische Gastheorie O. von der Lühe und U. Landgraf Kinetische Gastheorie - Gasdruck Der Druck in einem mit einem Gas gefüllten Behälter entsteht durch Impulsübertragung
Einführung in die Physik I Wärme Kinetische Gastheorie O. von der Lühe und U. Landgraf Kinetische Gastheorie - Gasdruck Der Druck in einem mit einem Gas gefüllten Behälter entsteht durch Impulsübertragung
11. Ideale Gasgleichung
 . Ideale Gasgleichung.Ideale Gasgleichung Definition eines idealen Gases: Gasmoleküle sind harte punktförmige eilchen, die nur elastische Stöße ausführen und kein Eigenvolumen besitzen. iele Gase zeigen
. Ideale Gasgleichung.Ideale Gasgleichung Definition eines idealen Gases: Gasmoleküle sind harte punktförmige eilchen, die nur elastische Stöße ausführen und kein Eigenvolumen besitzen. iele Gase zeigen
5.1. Kinetische Gastheorie. Ziel: Der Gasdruck: Kolben ohne Reibung, Gasatome im Volumen V Wie groß ist F auf den Kolben?
 5.1. Kinetische Gastheorie z.b: He-Gas : 3 10 Atome/cm diese wechselwirken über die elektrische Kraft: Materie besteht aus sehr vielen Atomen: gehorchen den Gesetzen der Mechanik Ziel: Verständnis der
5.1. Kinetische Gastheorie z.b: He-Gas : 3 10 Atome/cm diese wechselwirken über die elektrische Kraft: Materie besteht aus sehr vielen Atomen: gehorchen den Gesetzen der Mechanik Ziel: Verständnis der
Kräfte zwischen Teilchen (Atomen) eines Gases und deren Idealisierung
 kinetische Gastheorie Zurückführung der makroskopischen Zusammenhänge: p(v,t) auf mikroskopische Ursachen. Atomistische Natur der Gase lange umstritten, Akzeptanz Ende 19. Jahrh., Boltzmann. Modell des
kinetische Gastheorie Zurückführung der makroskopischen Zusammenhänge: p(v,t) auf mikroskopische Ursachen. Atomistische Natur der Gase lange umstritten, Akzeptanz Ende 19. Jahrh., Boltzmann. Modell des
Gase, Flüssigkeiten, Feststoffe
 Gase, Flüssigkeiten, Feststoffe Charakteristische Eigenschaften der Aggregatzustände Gas: Flüssigkeit: Feststoff: Nimmt das Volumen und die Form seines Behälters an. Ist komprimierbar. Fliesst leicht.
Gase, Flüssigkeiten, Feststoffe Charakteristische Eigenschaften der Aggregatzustände Gas: Flüssigkeit: Feststoff: Nimmt das Volumen und die Form seines Behälters an. Ist komprimierbar. Fliesst leicht.
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet
 Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet Unterrichtsmaterial - schriftliche Informationen zu Gasen für Studierende - Folien Fach Schultyp: Vorkenntnisse: Bearbeitungsdauer Thermodynamik
Kreisprozesse und Wärmekraftmaschinen: Wie ein Gas Arbeit verrichtet Unterrichtsmaterial - schriftliche Informationen zu Gasen für Studierende - Folien Fach Schultyp: Vorkenntnisse: Bearbeitungsdauer Thermodynamik
Kinetische Gastheorie
 Kinetische Gastheorie Mikroskopischer Zugang zur Wärmelehre ausgehend on Gesetzen aus der Mechanik. Ziel: Beschreibung eines Gases mit ielen wechselwirkenden Atomen. Beschreibung mit Mitteln der Mechanik:
Kinetische Gastheorie Mikroskopischer Zugang zur Wärmelehre ausgehend on Gesetzen aus der Mechanik. Ziel: Beschreibung eines Gases mit ielen wechselwirkenden Atomen. Beschreibung mit Mitteln der Mechanik:
Die Avogadro-Konstante N A
 Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
5 Gase...2. 5.1 Das ideale Gasgesetz...2. 5.2 Kinetische Gastheorie...3. 5.2.1 Geschwindigkeit der Gasteilchen:...5. 5.2.2 Diffusion...
 5 Gase...2 5.1 Das ideale Gasgesetz...2 5.2 Kinetische Gastheorie...3 5.2.1 Geschwindigkeit der Gasteilchen:...5 5.2.2 Diffusion...5 5.2.3 Zusammenstöße...6 5.2.4 Geschwindigkeitsverteilung...6 5.2.5 Partialdruck...7
5 Gase...2 5.1 Das ideale Gasgesetz...2 5.2 Kinetische Gastheorie...3 5.2.1 Geschwindigkeit der Gasteilchen:...5 5.2.2 Diffusion...5 5.2.3 Zusammenstöße...6 5.2.4 Geschwindigkeitsverteilung...6 5.2.5 Partialdruck...7
Physikalische Chemie IV Statistische Thermodynamik, SS2013
 Physikalische Chemie IV Statistische Thermodynamik, SS013 Inhaltsverzeichnis mit Referenzen 1. Einführung 1.1 Vergleich makroskopische und mikroskopische Systeme: Beispiel: ideales Gas, Herleitung eines
Physikalische Chemie IV Statistische Thermodynamik, SS013 Inhaltsverzeichnis mit Referenzen 1. Einführung 1.1 Vergleich makroskopische und mikroskopische Systeme: Beispiel: ideales Gas, Herleitung eines
Physik für Studierende der Biologie und Chemie Universität Zürich, HS 2009, U. Straumann Version 9. Dezember 2009
 Physik für Studierende der Biologie und Chemie Universität Zürich, HS 2009, U. Straumann Version 9. Dezember 2009 Inhaltsverzeichnis 4.2 Zustandsgleichungen von Gasen und kinetische Gastheorie........
Physik für Studierende der Biologie und Chemie Universität Zürich, HS 2009, U. Straumann Version 9. Dezember 2009 Inhaltsverzeichnis 4.2 Zustandsgleichungen von Gasen und kinetische Gastheorie........
wegen Massenerhaltung
 3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
3.3 Bilanzgleichungen Allgemein: Änderung der Bilanzgröße im System = Eingang Ausgang + Bildung - Verbrauch. 3.3.1 Massenbilanz Integration für konstante Massenströme: 0 wegen Massenerhaltung 3.3-1 3.3.2
Grenzflächen-Phänomene
 Grenzflächen-Phänomene Oberflächenspannung Betrachtet: Grenzfläche Flüssigkeit-Gas Kräfte Fl Fl grösser als Fl Gas im Inneren der Flüssigkeit: kräftefrei an der Oberfläche: resultierende Kraft ins Innere
Grenzflächen-Phänomene Oberflächenspannung Betrachtet: Grenzfläche Flüssigkeit-Gas Kräfte Fl Fl grösser als Fl Gas im Inneren der Flüssigkeit: kräftefrei an der Oberfläche: resultierende Kraft ins Innere
8. Wärmelehre. 8.1 Temperaturskala 1 = 2. kinetische und potentielle Energie, die ein System bei Temperaturänderung aufnimmt oder abgibt
 9 8. Wärmelehre 8. emperatursala Wärmeenergie: emperatur: inetische und potentielle Energie, die ein System bei emperaturänderung aunimmt oder abgibt Maß ür mittlere inetische Energie eines Systems (im
9 8. Wärmelehre 8. emperatursala Wärmeenergie: emperatur: inetische und potentielle Energie, die ein System bei emperaturänderung aunimmt oder abgibt Maß ür mittlere inetische Energie eines Systems (im
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 010 10. 14. Mai 010 Physik für Bauingenieure Übungsblatt 4 1. Wie viele Luftmoleküle befinden sich im Hörsaal Gruppenübungen
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 010 10. 14. Mai 010 Physik für Bauingenieure Übungsblatt 4 1. Wie viele Luftmoleküle befinden sich im Hörsaal Gruppenübungen
Temperatur Wärme Thermodynamik
 Temperatur Wärme Thermodynamik Stoffwiederholung und Übungsaufgaben... 2 Lösungen... 33 Thermodynamik / 1 Einführung: Temperatur und Wärme Alle Körper haben eine innere Energie, denn sie sind aus komplizierten
Temperatur Wärme Thermodynamik Stoffwiederholung und Übungsaufgaben... 2 Lösungen... 33 Thermodynamik / 1 Einführung: Temperatur und Wärme Alle Körper haben eine innere Energie, denn sie sind aus komplizierten
Thermische Isolierung mit Hilfe von Vakuum. 9.1.2013 Thermische Isolierung 1
 Thermische Isolierung mit Hilfe von Vakuum 9.1.2013 Thermische Isolierung 1 Einleitung Wieso nutzt man Isolierkannen / Dewargefäße, wenn man ein Getränk über eine möglichst lange Zeit heiß (oder auch kalt)
Thermische Isolierung mit Hilfe von Vakuum 9.1.2013 Thermische Isolierung 1 Einleitung Wieso nutzt man Isolierkannen / Dewargefäße, wenn man ein Getränk über eine möglichst lange Zeit heiß (oder auch kalt)
Thermodynamik I. Sommersemester 2012 Kapitel 3, Teil 1. Prof. Dr.-Ing. Heinz Pitsch
 Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 1 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 1: Übersicht 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie 3.1.2 Innere Energie U 3.1.3 Energietransfer
Thermodynamik I Sommersemester 2012 Kapitel 3, Teil 1 Prof. Dr.-Ing. Heinz Pitsch Kapitel 3, Teil 1: Übersicht 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie 3.1.2 Innere Energie U 3.1.3 Energietransfer
Administratives BSL PB
 Administratives Die folgenden Seiten sind ausschliesslich als Ergänzung zum Unterricht für die Schüler der BSL gedacht (intern) und dürfen weder teilweise noch vollständig kopiert oder verbreitet werden.
Administratives Die folgenden Seiten sind ausschliesslich als Ergänzung zum Unterricht für die Schüler der BSL gedacht (intern) und dürfen weder teilweise noch vollständig kopiert oder verbreitet werden.
Temperatur. Gebräuchliche Thermometer
 Temperatur Wärme ist Form von mechanischer Energie Umwandlung Wärme mechanische Energie ist möglich! Thermometer Messung der absoluten Temperatur ist aufwendig Menschliche Sinnesorgane sind schlechte "Thermometer"!
Temperatur Wärme ist Form von mechanischer Energie Umwandlung Wärme mechanische Energie ist möglich! Thermometer Messung der absoluten Temperatur ist aufwendig Menschliche Sinnesorgane sind schlechte "Thermometer"!
grundsätzlich Mittel über große Zahl von Teilchen thermisches Gleichgewicht (Verteilungsfunktionen)
 10. Wärmelehre Temperatur aus mikroskopischer Theorie: = 3/2 kt = ½ m = 0 T = 0 quantitative Messung von T nutzbares Maß? grundsätzlich Mittel über große Zahl von Teilchen thermisches
10. Wärmelehre Temperatur aus mikroskopischer Theorie: = 3/2 kt = ½ m = 0 T = 0 quantitative Messung von T nutzbares Maß? grundsätzlich Mittel über große Zahl von Teilchen thermisches
Gase unter Druck: Die Gasgesetze
 Gase unter Druck: Die Gasgesetze In diesem Kapitel... Den Begriff»Physikalische Chemie«definieren Den Einfluss von Druck und Temperatur auf Gase beschreiben Ideales und reales Verhalten von Gasen unterscheiden
Gase unter Druck: Die Gasgesetze In diesem Kapitel... Den Begriff»Physikalische Chemie«definieren Den Einfluss von Druck und Temperatur auf Gase beschreiben Ideales und reales Verhalten von Gasen unterscheiden
Ideale und Reale Gase. Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig)
 Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Vordiplomsklausur Physik
 Institut für Physik und Physikalische Technologien der TU-Clausthal; Prof. Dr. W. Schade Vordiplomsklausur Physik 14.Februar 2006, 9:00-11:00 Uhr für den Studiengang: Maschinenbau intensiv (bitte deutlich
Institut für Physik und Physikalische Technologien der TU-Clausthal; Prof. Dr. W. Schade Vordiplomsklausur Physik 14.Februar 2006, 9:00-11:00 Uhr für den Studiengang: Maschinenbau intensiv (bitte deutlich
Physikalische Grundlagen der Hygrometrie
 Den Druck der durch die verdampfenden Teilchen entsteht, nennt man auch Dampfdru Dampfdruck einen gewissen Wert, so können keine weiteren Teilchen aus der Flüssigk Physikalische Grundlagen der Hygrometrie
Den Druck der durch die verdampfenden Teilchen entsteht, nennt man auch Dampfdru Dampfdruck einen gewissen Wert, so können keine weiteren Teilchen aus der Flüssigk Physikalische Grundlagen der Hygrometrie
Innere Reibung von Gasen
 Blatt: 1 Aufgabe Bestimmen Sie die Viskosität η von Gasen aus der Messung der Strömung durch Kapillaren. Berechnen Sie aus den Messergebnissen für jedes Gas die Sutherland-Konstante C, die effektiven Moleküldurchmesser
Blatt: 1 Aufgabe Bestimmen Sie die Viskosität η von Gasen aus der Messung der Strömung durch Kapillaren. Berechnen Sie aus den Messergebnissen für jedes Gas die Sutherland-Konstante C, die effektiven Moleküldurchmesser
Kalorimetrie (Wärmelehre)
 Thermische Molekularbewegung Phasenübergänge Reaktionswärme Kalorimetrie (Wärmelehre) Gase Flüssigkeiten/Festkörper Ideales Gasgesetz Dulong-Petit-Gesetz 1 Thermodynamik Beschreibung der Zustände und deren
Thermische Molekularbewegung Phasenübergänge Reaktionswärme Kalorimetrie (Wärmelehre) Gase Flüssigkeiten/Festkörper Ideales Gasgesetz Dulong-Petit-Gesetz 1 Thermodynamik Beschreibung der Zustände und deren
Grundwissen Physik (8. Klasse)
 Grundwissen Physik (8. Klasse) 1 Energie 1.1 Energieerhaltungssatz 1.2 Goldene egel der Mechanik Energieerhaltungssatz: n einem abgeschlossenen System ist die Gesamtenergie konstant. Goldene egel der Mechanik:
Grundwissen Physik (8. Klasse) 1 Energie 1.1 Energieerhaltungssatz 1.2 Goldene egel der Mechanik Energieerhaltungssatz: n einem abgeschlossenen System ist die Gesamtenergie konstant. Goldene egel der Mechanik:
1 Grundwissen Energie. 2 Grundwissen mechanische Energie
 1 Grundwissen Energie Die physikalische Größe Energie E ist so festgelegt, dass Energieerhaltung gilt. Energie kann weder erzeugt noch vernichtet werden. Sie kann nur von einer Form in andere Formen umgewandelt
1 Grundwissen Energie Die physikalische Größe Energie E ist so festgelegt, dass Energieerhaltung gilt. Energie kann weder erzeugt noch vernichtet werden. Sie kann nur von einer Form in andere Formen umgewandelt
Thermodynamik. Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur
 Thermodynamik Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur kann voraussagen, ob eine chemische Reaktion abläuft oder nicht kann nichts über den zeitlichen
Thermodynamik Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur kann voraussagen, ob eine chemische Reaktion abläuft oder nicht kann nichts über den zeitlichen
Seminar zur Theorie der Teilchen und Felder. Van der Waals Theorie
 Seminar zur Theorie der Teilchen und Felder Van der Waals Theorie Tobias Berheide 18.11.2009 1 Inhaltsverzeichnis 1 Einleitung 3 2 Das Van der Waals Gas 3 2.1 Das ideale Gas..............................
Seminar zur Theorie der Teilchen und Felder Van der Waals Theorie Tobias Berheide 18.11.2009 1 Inhaltsverzeichnis 1 Einleitung 3 2 Das Van der Waals Gas 3 2.1 Das ideale Gas..............................
Physikalisches Praktikum Wirtschaftsingenieurwesen Physikalische Technik und Orthopädietechnik Prof. Dr. Chlebek, MSc. M. Gilbert
 Physikalisches Praktikum Wirtschaftsingenieurwesen Physikalische Technik und Orthopädietechnik Prof. Dr. Chlebek, MSc. M. Gilbert TH 01 Wärmekapazität und Wirkungsgrad (Pr_PhI_TH01_Wärmekapazität_6, 30.8.009)
Physikalisches Praktikum Wirtschaftsingenieurwesen Physikalische Technik und Orthopädietechnik Prof. Dr. Chlebek, MSc. M. Gilbert TH 01 Wärmekapazität und Wirkungsgrad (Pr_PhI_TH01_Wärmekapazität_6, 30.8.009)
2,00 1,75. Kompressionsfaktor z 1,50 1,25 1,00 0,75 0,50 0,25. Druck in MPa. Druckabhängigkeit des Kompressionsfaktors. Chemische Verfahrenstechnik
 Kompressionsfaktor z,00 1,75 1,50 1,5 1,00 0,75 0,50 0,5 H CH 4 CO 0 0 0 40 60 80 Druck in MPa ideales Gas Nach dem idealen Gasgesetz gilt: pv nrt = pv m RT = 1 (z) Nennenswerte Abweichungen vom idealen
Kompressionsfaktor z,00 1,75 1,50 1,5 1,00 0,75 0,50 0,5 H CH 4 CO 0 0 0 40 60 80 Druck in MPa ideales Gas Nach dem idealen Gasgesetz gilt: pv nrt = pv m RT = 1 (z) Nennenswerte Abweichungen vom idealen
- potentiell E pot. Gesamtenergie: E = U + E kin + E pot. 3 Energiebilanz. 3.1 Energie. 3.1.1 Formen der Energie
 3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie Innere Energie: U - thermisch - latent Äußere Energien: E a - kinetisch E kin - potentiell E pot Gesamtenergie: E = U + E kin + E pot 3.1-1 3.1.2 Die
3 Energiebilanz 3.1 Energie 3.1.1 Formen der Energie Innere Energie: U - thermisch - latent Äußere Energien: E a - kinetisch E kin - potentiell E pot Gesamtenergie: E = U + E kin + E pot 3.1-1 3.1.2 Die
Thermodynamik. Vorlesung 1. Nicolas Thomas
 Thermodynamik Vorlesung 1 Thermodynamik ist nur ein bisschen schwerig. Geschichtlicher Hintergrund! Im 19. Jahrhundert Zunahme an Mechanisierung durch Konstruktion von Maschinen und Motoren.! Besonders
Thermodynamik Vorlesung 1 Thermodynamik ist nur ein bisschen schwerig. Geschichtlicher Hintergrund! Im 19. Jahrhundert Zunahme an Mechanisierung durch Konstruktion von Maschinen und Motoren.! Besonders
Arbeit und Leistung. 2mgs/2 = mgs. m g. m g. mgs = const. m g. 2m g. .. nmgs/n = mgs
 Arbeit und Leistung s s m g m g mgs = mgs s/2 mgs = const. s 2m g m g 2mgs/2 = mgs.. nmgs/n = mgs Arbeit und Leistung Arbeit ist Kraft mal Weg Gotthardstraße Treppe und Lift Feder Bergsteiger/Wanderer
Arbeit und Leistung s s m g m g mgs = mgs s/2 mgs = const. s 2m g m g 2mgs/2 = mgs.. nmgs/n = mgs Arbeit und Leistung Arbeit ist Kraft mal Weg Gotthardstraße Treppe und Lift Feder Bergsteiger/Wanderer
Vorlesung am 7. Juni 2010
 Materialwissenschaften, SS 2008 Ernst Bauer, Ch. Eisenmenger-Sittner und Josef Fidler 1.) Kristallstrukturen 2.) Strukturbestimmung 3.) Mehrstoffsysteme 4.) Makroskopische Eigenschaften von Festkörpern
Materialwissenschaften, SS 2008 Ernst Bauer, Ch. Eisenmenger-Sittner und Josef Fidler 1.) Kristallstrukturen 2.) Strukturbestimmung 3.) Mehrstoffsysteme 4.) Makroskopische Eigenschaften von Festkörpern
Der atmosphärische Luftdruck
 Gasdruck Der Druck in einem eingeschlossenen Gas entsteht durch Stöße der Gasteilchen (Moleküle) untereinander und gegen die Gefäßwände. In einem Gefäß ist der Gasdruck an allen Stellen gleich groß und
Gasdruck Der Druck in einem eingeschlossenen Gas entsteht durch Stöße der Gasteilchen (Moleküle) untereinander und gegen die Gefäßwände. In einem Gefäß ist der Gasdruck an allen Stellen gleich groß und
Probeklausur zur Vorlesung Physik I für Chemiker, Pharmazeuten, Geoökologen, Lebensmittelchemiker
 Technische Universität Braunschweig Institut für Geophysik und extraterrestrische Physik Prof. A. Hördt Probeklausur zur Vorlesung Physik I für Chemiker, Pharmazeuten, Geoökologen, Lebensmittelchemiker
Technische Universität Braunschweig Institut für Geophysik und extraterrestrische Physik Prof. A. Hördt Probeklausur zur Vorlesung Physik I für Chemiker, Pharmazeuten, Geoökologen, Lebensmittelchemiker
Thermische Ausdehnung
 Versuch: TA Fachrichtung Physik Physikalisches Grundpraktikum Aktualisiert: am 16. 09. 2009 Bearbeitet: M. Kreller J. Kelling F. Lemke S. Majewsky i.a. Dr. Escher Thermische Ausdehnung Inhaltsverzeichnis
Versuch: TA Fachrichtung Physik Physikalisches Grundpraktikum Aktualisiert: am 16. 09. 2009 Bearbeitet: M. Kreller J. Kelling F. Lemke S. Majewsky i.a. Dr. Escher Thermische Ausdehnung Inhaltsverzeichnis
Rückblick auf vorherige Vorlesung:
 Rückblick auf vorherige Vorlesung: Der Zustand eines Systems wird durch Zustandsgrößen beschrieben 0. Hauptsatz der Thermodynamik Stehen zwei Körper A und B sowie zwei Körper B und C im thermischen Gleichgewicht
Rückblick auf vorherige Vorlesung: Der Zustand eines Systems wird durch Zustandsgrößen beschrieben 0. Hauptsatz der Thermodynamik Stehen zwei Körper A und B sowie zwei Körper B und C im thermischen Gleichgewicht
Praktikum Physik. Protokoll zum Versuch 1: Viskosität. Durchgeführt am 26.01.2012. Gruppe X
 Praktikum Physik Protokoll zum Versuch 1: Viskosität Durchgeführt am 26.01.2012 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuerin: Wir bestätigen hiermit, dass wir das Protokoll
Praktikum Physik Protokoll zum Versuch 1: Viskosität Durchgeführt am 26.01.2012 Gruppe X Name 1 und Name 2 (abc.xyz@uni-ulm.de) (abc.xyz@uni-ulm.de) Betreuerin: Wir bestätigen hiermit, dass wir das Protokoll
Versuch A02: Thermische Ausdehnung von Metallen
 Versuch A02: Thermische Ausdehnung von Metallen 13. März 2014 I Lernziele Wechselwirkungspotential im Festkörper Gitterschwingungen Ausdehnungskoezient II Physikalische Grundlagen Die thermische Längen-
Versuch A02: Thermische Ausdehnung von Metallen 13. März 2014 I Lernziele Wechselwirkungspotential im Festkörper Gitterschwingungen Ausdehnungskoezient II Physikalische Grundlagen Die thermische Längen-
9.Vorlesung EP WS2009/10
 9.Vorlesung EP WS2009/10 I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik c) Oberflächenspannung und Kapillarität 6. Hydro- und Aerodynamik
9.Vorlesung EP WS2009/10 I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik c) Oberflächenspannung und Kapillarität 6. Hydro- und Aerodynamik
Optik. Optik. Optik. Optik. Optik
 Nenne das Brechungsgesetz! Beim Übergang von Luft in Glas (Wasser, Kunststoff) wird der Lichtstrahl zum Lot hin gebrochen. Beim Übergang von Glas (Wasser...) in Luft wird der Lichtstrahl vom Lot weg gebrochen.
Nenne das Brechungsgesetz! Beim Übergang von Luft in Glas (Wasser, Kunststoff) wird der Lichtstrahl zum Lot hin gebrochen. Beim Übergang von Glas (Wasser...) in Luft wird der Lichtstrahl vom Lot weg gebrochen.
Transportvorgänge. 1. Einleitung. 2. Wärmetransport (makroskopische Betrachtung) KAPITEL D
 3 KAPITEL D Transportvorgänge. Einleitung Bisher wurde das Hauptaugenmerk auf Gleichgewichtszustände gerichtet. Hat man in einem System an unterschiedlichen Orten unterschiedliche Temperaturen, so liegt
3 KAPITEL D Transportvorgänge. Einleitung Bisher wurde das Hauptaugenmerk auf Gleichgewichtszustände gerichtet. Hat man in einem System an unterschiedlichen Orten unterschiedliche Temperaturen, so liegt
Kapitel 2 Thermische Ausdehnung
 Kapitel 2 Thermische Ausdehnung Die Ausdehnung von Festkörpern, Flüssigkeiten und Gasen hängt von der Temperatur ab. Für Festkörper und Flüssigkeiten ist diese temperaturabhängige Ausdehnung zusätzlich
Kapitel 2 Thermische Ausdehnung Die Ausdehnung von Festkörpern, Flüssigkeiten und Gasen hängt von der Temperatur ab. Für Festkörper und Flüssigkeiten ist diese temperaturabhängige Ausdehnung zusätzlich
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #12 10/11/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Konvektion Verbunden mit Materietransport Ursache: Temperaturabhängigkeit der Dichte In Festkörpern
Physik für Mediziner im 1. Fachsemester #12 10/11/2010 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Konvektion Verbunden mit Materietransport Ursache: Temperaturabhängigkeit der Dichte In Festkörpern
Physik A VL8 (25.10.2012)
 Physik A VL8 (5.10.01) Arbeit, nergie und Leistung Arbeit und nergie nergiebilanzen Leistung Reibung Arbeit und nergie umgangssprachlich: man muss arbeiten, um etwas hochzuheben: physikalisch im alle der
Physik A VL8 (5.10.01) Arbeit, nergie und Leistung Arbeit und nergie nergiebilanzen Leistung Reibung Arbeit und nergie umgangssprachlich: man muss arbeiten, um etwas hochzuheben: physikalisch im alle der
F63 Gitterenergie von festem Argon
 1 F63 Gitteenegie von festem Agon 1. Einleitung Die Sublimationsenthalpie von festem Agon kann aus de Dampfduckkuve bestimmt weden. Dazu vewendet man die Clausius-Clapeyon-Gleichung. Wenn außedem noch
1 F63 Gitteenegie von festem Agon 1. Einleitung Die Sublimationsenthalpie von festem Agon kann aus de Dampfduckkuve bestimmt weden. Dazu vewendet man die Clausius-Clapeyon-Gleichung. Wenn außedem noch
22. Chemische Bindungen
 .05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
.05.03. Chemische Bindungen Molekül: System aus zwei oder mehr Atomen Kleinste Einheit einer Substanz, die deren chemische Eigenschaften ausweist Quantenmechanisches Vielteilchensystem: Exakte explizite
Tropfenkonturanalyse
 Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
Phasen und Grenzflächen Tropfenkonturanalyse Abstract Mit Hilfe der Tropfenkonturanalyse kann die Oberflächenspannung einer Flüssigkeit ermittelt werden. Wird die Oberflächenspannung von Tensidlösungen
4. Die Energiebilanz. 4.1. Mechanische Formen der Energie. 4.1.1 Energie und Arbeit Arbeit einer Kraft
 4. Die Energiebilanz 4.1. Mechanische Formen der Energie 4.1.1 Energie und Arbeit Arbeit einer Kraft Die auf dem Weg von 1 nach 2 geleistete Arbeit berechnet sich durch Integration entlang der Bahnkurve
4. Die Energiebilanz 4.1. Mechanische Formen der Energie 4.1.1 Energie und Arbeit Arbeit einer Kraft Die auf dem Weg von 1 nach 2 geleistete Arbeit berechnet sich durch Integration entlang der Bahnkurve
D = 10 mm δ = 5 mm a = 0, 1 m L = 1, 5 m λ i = 0, 4 W/mK ϑ 0 = 130 C ϑ L = 30 C α W = 20 W/m 2 K ɛ 0 = 0, 8 ɛ W = 0, 2
 Seminargruppe WuSt Aufgabe.: Kabelkanal (ehemalige Vordiplom-Aufgabe) In einem horizontalen hohlen Kabelkanal der Länge L mit einem quadratischen Querschnitt der Seitenlänge a verläuft in Längsrichtung
Seminargruppe WuSt Aufgabe.: Kabelkanal (ehemalige Vordiplom-Aufgabe) In einem horizontalen hohlen Kabelkanal der Länge L mit einem quadratischen Querschnitt der Seitenlänge a verläuft in Längsrichtung
Experimentalphysik I: Lösung Übungsklausur
 Experimentalphysik I: Lösung Übungsklausur 3. Januar 1 1 (5 Punkte) Eine Punktmasse, welche sich zum Zeitpunkt t = am Koordinatenursprung befindet, bewegt sich mit der Geschwindigkeit v = α cos t δ βt
Experimentalphysik I: Lösung Übungsklausur 3. Januar 1 1 (5 Punkte) Eine Punktmasse, welche sich zum Zeitpunkt t = am Koordinatenursprung befindet, bewegt sich mit der Geschwindigkeit v = α cos t δ βt
Verflüssigung von Gasen / Joule-Thomson-Effekt
 Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Sieden und Kondensation: T p T p S S 0 1 RTSp0 1 ln p p0 Dampfdrucktopf, Autoklave zur Sterilisation absolute Luftfeuchtigkeit relative Luftfeuchtigkeit a ( g/m 3 ) a pw rel S ps rel 1 Taupunkt erflüssigung
Energie, mechanische Arbeit und Leistung
 Grundwissen Physik Klasse 8 erstellt am Finsterwalder-Gymnasium Rosenheim auf Basis eines Grundwissenskatalogs des Klenze-Gymnasiums München Energie, mechanische Arbeit und Leistung Mit Energie können
Grundwissen Physik Klasse 8 erstellt am Finsterwalder-Gymnasium Rosenheim auf Basis eines Grundwissenskatalogs des Klenze-Gymnasiums München Energie, mechanische Arbeit und Leistung Mit Energie können
Wichtige Begriffe dieser Vorlesung:
 Wichtige Begiffe diese Volesung: Impuls Abeit, Enegie, kinetische Enegie Ehaltungssätze: - Impulsehaltung - Enegieehaltung Die Newtonschen Gundgesetze 1. Newtonsches Axiom (Tägheitspinzip) Ein Köpe, de
Wichtige Begiffe diese Volesung: Impuls Abeit, Enegie, kinetische Enegie Ehaltungssätze: - Impulsehaltung - Enegieehaltung Die Newtonschen Gundgesetze 1. Newtonsches Axiom (Tägheitspinzip) Ein Köpe, de
Energieumsatz bei Phasenübergang
 Energieumsatz bei Phasenübergang wenn E Vib > E Bindung schmelzen verdampfen Q Aufbrechen von Bindungen Kondensation: Bildung von Bindungen E Bindung Q E Transl. E Bindung für System A B durch Stöße auf
Energieumsatz bei Phasenübergang wenn E Vib > E Bindung schmelzen verdampfen Q Aufbrechen von Bindungen Kondensation: Bildung von Bindungen E Bindung Q E Transl. E Bindung für System A B durch Stöße auf
Physik1. Physik der Wärme. WS 15/16 1. Sem. B.Sc. Oec. und B.Sc. CH
 3 Physik1. Physik der Wärme. WS 15/16 1. Sem. B.Sc. Oec. und B.Sc. CH Physik Wärme 5 Themen Begriffsklärung Anwendungen Temperaturskalen Modellvorstellung Wärmeausdehnung Thermische Ausdehnung Phasenübergänge
3 Physik1. Physik der Wärme. WS 15/16 1. Sem. B.Sc. Oec. und B.Sc. CH Physik Wärme 5 Themen Begriffsklärung Anwendungen Temperaturskalen Modellvorstellung Wärmeausdehnung Thermische Ausdehnung Phasenübergänge
Anfänger-Praktikum I WS 11/12. Michael Seidling Timo Raab. Praktikumsbericht: Stoßgesetze
 Anfänger-Praktikum I WS 11/12 Michael Seidling Timo Raab Praktikumsbericht: Stoßgesetze 1 Inhaltsverzeichnis Inhaltsverzeichnis I. Einführung 4 II. Grundlagen 4 1. Die Zykloide 4 2. Das Trägheitsmoment
Anfänger-Praktikum I WS 11/12 Michael Seidling Timo Raab Praktikumsbericht: Stoßgesetze 1 Inhaltsverzeichnis Inhaltsverzeichnis I. Einführung 4 II. Grundlagen 4 1. Die Zykloide 4 2. Das Trägheitsmoment
Grimsehl Lehrbuch der Physik
 Grimsehl Lehrbuch der Physik BAND 1 Mechanik Akustik Wärmelehre 27., unveränderte Auflage mit 655 Abbildungen BEGRÜNDET VON PROF. E. GRIMSEHL WEITERGEFÜHRT VON PROF. DR. W. SCHALLREUTER NEU BEARBEITET
Grimsehl Lehrbuch der Physik BAND 1 Mechanik Akustik Wärmelehre 27., unveränderte Auflage mit 655 Abbildungen BEGRÜNDET VON PROF. E. GRIMSEHL WEITERGEFÜHRT VON PROF. DR. W. SCHALLREUTER NEU BEARBEITET
Sternentstehung. Von der Molekülwolke zum T-Tauri-Stern. Von Benedict Höger
 Sternentstehung Von der Molekülwolke zum T-Tauri-Stern Von Benedict Höger Inhaltsverzeichnis 1. Unterschied zwischen Stern und Planet 2. Sternentstehung 2.1 Wo entsteht ein Stern? 2.2 Unterschied HI und
Sternentstehung Von der Molekülwolke zum T-Tauri-Stern Von Benedict Höger Inhaltsverzeichnis 1. Unterschied zwischen Stern und Planet 2. Sternentstehung 2.1 Wo entsteht ein Stern? 2.2 Unterschied HI und
Physikalisches Praktikum I. PTC und NTC Widerstände. Fachbereich Physik. Energielücke. E g. Valenzband. Matrikelnummer:
 Fachbereich Physik Physikalisches Praktikum I Name: PTC und NTC Widerstände Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Dieser Fragebogen muss von
Fachbereich Physik Physikalisches Praktikum I Name: PTC und NTC Widerstände Matrikelnummer: Fachrichtung: Mitarbeiter/in: Assistent/in: Versuchsdatum: Gruppennummer: Endtestat: Dieser Fragebogen muss von
Die innere Energie eines geschlossenen Systems ist konstant
 Rückblick auf vorherige Vorlesung Grundsätzlich sind alle möglichen Formen von Arbeit denkbar hier diskutiert: Mechanische Arbeit: Arbeit, die nötig ist um einen Massepunkt von A nach B zu bewegen Konservative
Rückblick auf vorherige Vorlesung Grundsätzlich sind alle möglichen Formen von Arbeit denkbar hier diskutiert: Mechanische Arbeit: Arbeit, die nötig ist um einen Massepunkt von A nach B zu bewegen Konservative
THERMISCHE AUSDEHNUNG
 INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11 THERMISCHE AUSDEHNUNG Unter thermischer Ausdehnung versteht man
INSTITUT FÜR ANGEWANDTE PHYSIK Physikalisches Praktikum für Studierende der Ingenieurswissenschaften Universität Hamburg, Jungiusstraße 11 THERMISCHE AUSDEHNUNG Unter thermischer Ausdehnung versteht man
Spezifische Wärmekapazität
 Versuch: KA Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: L. Jahn B. Wehner J. Pöthig J. Stelzer am 01. 06. 1997 Bearbeitet: M. Kreller J. Kelling F. Lemke S. Majewsky i. A. Dr. Escher am
Versuch: KA Fachrichtung Physik Physikalisches Grundpraktikum Erstellt: L. Jahn B. Wehner J. Pöthig J. Stelzer am 01. 06. 1997 Bearbeitet: M. Kreller J. Kelling F. Lemke S. Majewsky i. A. Dr. Escher am
Allgemeine Chemie. SS 2014 Thomas Loerting. Thomas Loerting Allgemeine Chemie
 Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
Allgemeine Chemie SS 2014 Thomas Loerting 1 Inhalt 1 Der Aufbau der Materie (Teil 1) 2 Die chemische Bindung (Teil 2) 3 Die chemische Reaktion (Teil 3) 2 Definitionen von den an einer chemischen Reaktion
24. Transportprozesse
 4. Transportprozesse 4.1. Diffusion Gas- und Flüssigkeitsteilchen befinden sich in ständiger unregelmäßiger Bewegung (Gas: BROWNsche Bewegung). unwahrscheinliche Ausgangsverteilungen gleichen sich selbständig
4. Transportprozesse 4.1. Diffusion Gas- und Flüssigkeitsteilchen befinden sich in ständiger unregelmäßiger Bewegung (Gas: BROWNsche Bewegung). unwahrscheinliche Ausgangsverteilungen gleichen sich selbständig
Physik für Mediziner und Zahmediziner
 Physik für Mediziner und Zahmediziner Vorlesung 03 Prof. F. Wörgötter (nach M. Seibt) -- Physik für Mediziner und Zahnmediziner 1 Arbeit: vorläufige Definition Definition der Arbeit (vorläufig): Wird auf
Physik für Mediziner und Zahmediziner Vorlesung 03 Prof. F. Wörgötter (nach M. Seibt) -- Physik für Mediziner und Zahnmediziner 1 Arbeit: vorläufige Definition Definition der Arbeit (vorläufig): Wird auf
Physikalische Chemie: Kreisprozesse
 Physikalische Chemie: Kreisprozesse Version vom 29. Mai 2006 Inhaltsverzeichnis 1 Diesel Kreisprozess 2 1.1 Wärmemenge Q.................................. 2 1.2 Arbeit W.....................................
Physikalische Chemie: Kreisprozesse Version vom 29. Mai 2006 Inhaltsverzeichnis 1 Diesel Kreisprozess 2 1.1 Wärmemenge Q.................................. 2 1.2 Arbeit W.....................................
Thermische Ausdehnung. heißt Volumenausdehnungskoeffizient. Betrachtet man nur eine Dimension, erhält man den Längenausdehnungskoeffizienten
 W1 Thermische Ausdehnung ie Volumenausdehnung von Flüssigkeiten und die Längenänderung von festen Körpern in Abhängigkeit von der Temperatur sollen nachgewiesen. 1. Theoretische Grundlagen 1.1 Allgemeines
W1 Thermische Ausdehnung ie Volumenausdehnung von Flüssigkeiten und die Längenänderung von festen Körpern in Abhängigkeit von der Temperatur sollen nachgewiesen. 1. Theoretische Grundlagen 1.1 Allgemeines
B H 0 H definieren, die somit die Antwort des Ordnungsparameters auf eine Variation der dazu konjugierten
 In Anwesenheit eines äußeren magnetischen Felds B entsteht in der paramagnetischen Phase eine induzierte Magnetisierung M. In der ferromagnetischen Phase führt B zu einer Verschiebung der Magnetisierung
In Anwesenheit eines äußeren magnetischen Felds B entsteht in der paramagnetischen Phase eine induzierte Magnetisierung M. In der ferromagnetischen Phase führt B zu einer Verschiebung der Magnetisierung
Lehre der Energie, ihrer Erscheinungsform und Fähigkeit, Arbeit zu verrichten.
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov Raum E143, Tel. 888-5875, email: dyakonov@physik.uni-wuerzburg.de 10 Wärmelehre/Thermodynamik Lehre der Energie,
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 Vladimir Dyakonov Raum E143, Tel. 888-5875, email: dyakonov@physik.uni-wuerzburg.de 10 Wärmelehre/Thermodynamik Lehre der Energie,
Die Van der Waals Zustandsgleichung realer Gase
 deale Gase sind dadurch definiert, dass sie die Zustandsgleichung = nrt erfüllen n ist dabei gleich der Molzahl des vorhandenen Gases). n der Praxis ist dies dann der Fall, wenn die Gase bei niedrigem
deale Gase sind dadurch definiert, dass sie die Zustandsgleichung = nrt erfüllen n ist dabei gleich der Molzahl des vorhandenen Gases). n der Praxis ist dies dann der Fall, wenn die Gase bei niedrigem
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 200 24. 28. Mai 200 Physik für Bauingenieure Übungsblatt 6. Luftfeuchtigkeit Gruppenübungen In einer Finnischen Sauna
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 200 24. 28. Mai 200 Physik für Bauingenieure Übungsblatt 6. Luftfeuchtigkeit Gruppenübungen In einer Finnischen Sauna
Übungen zur Vorlesung. Energiesysteme
 Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
Übungen zur Vorlesung Energiesysteme 1. Wärme als Form der Energieübertragung 1.1 Eine Halle mit 500 m 2 Grundfläche soll mit einer Fußbodenheizung ausgestattet werden, die mit einer mittleren Temperatur
PHYSIK. HYDROMECHANIK Statik, Dynamik, Kinematik der Flüssigkeiten ANGEWANDTE HYDROMECHANIK. HYDRAULIK Rohrleitung, Gerinne Eindimensionale Strömung
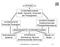 PHYSIK HYDROMECHANIK Statik, Dynamik, Kinematik der Flüssigkeiten HYDROSTATIK Ruhende Flüssigkeit HYDRODYNAMIK Dreidimensionale Flüssigkeitsbewegung ANGEWANDTE HYDROMECHANIK Hydrostatische Systeme HYDRAULIK
PHYSIK HYDROMECHANIK Statik, Dynamik, Kinematik der Flüssigkeiten HYDROSTATIK Ruhende Flüssigkeit HYDRODYNAMIK Dreidimensionale Flüssigkeitsbewegung ANGEWANDTE HYDROMECHANIK Hydrostatische Systeme HYDRAULIK
Gegenstand der letzten Vorlesung
 Thermodynamik - Kinetische Gastheorie (Wdh.) Gegenstand der letzten Vorlesung Einführung in die physikalische Chemie Kinetische Gastheorie (Einführung) Ideales Gas, Zustandsgleichung des idealen Gases
Thermodynamik - Kinetische Gastheorie (Wdh.) Gegenstand der letzten Vorlesung Einführung in die physikalische Chemie Kinetische Gastheorie (Einführung) Ideales Gas, Zustandsgleichung des idealen Gases
Übungsblatt 3 (10.06.2011)
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/hermodynamik Wintersemester 2007 ladimir Dyakonov #2 am 10.01.2007 Raum E143, el. 888-5875, email: dyakonov@hysik.uni-wuerzburg.de 10.2 emeraturmessung Wärmeausdehnung
Einführung in die Physik I Wärmelehre/hermodynamik Wintersemester 2007 ladimir Dyakonov #2 am 10.01.2007 Raum E143, el. 888-5875, email: dyakonov@hysik.uni-wuerzburg.de 10.2 emeraturmessung Wärmeausdehnung
Kapitel 4. Die Grundlagen der Kinetik
 Kapitel 4. Die Grundlagen der Kinetik Monomolekulare Reaktion erster rdnung A Produkte; v = k [A] (S N 1) bimolekulare Reaktion zweiter rdnung (S N 2) A + B Produkte; v = k [A] [B] Einfluss der Aktivierungsbarrieren
Kapitel 4. Die Grundlagen der Kinetik Monomolekulare Reaktion erster rdnung A Produkte; v = k [A] (S N 1) bimolekulare Reaktion zweiter rdnung (S N 2) A + B Produkte; v = k [A] [B] Einfluss der Aktivierungsbarrieren
Formelsammlung. Physikalische Größen. physikalische Größe = Wert Einheit Meßgröße = (Wert ± Fehler) Einheit
 Formelsammlung Physikalische Größen physikalische Größe = Wert Einheit Meßgröße = (Wert ± Fehler) Einheit Grundgrößen Zeit t s (Sekunde) Länge l m (Meter) Masse m kg (Kilogramm) elektrischer Strom I A
Formelsammlung Physikalische Größen physikalische Größe = Wert Einheit Meßgröße = (Wert ± Fehler) Einheit Grundgrößen Zeit t s (Sekunde) Länge l m (Meter) Masse m kg (Kilogramm) elektrischer Strom I A
Physikalische Formelsammlung
 Physikalische Formelsammlung Gleichförmige Bahnbewegung und Kreisbewegung Bewegungsgleichung für die gleichförmige lineare Bewegung: Winkelgeschwindigkeit bei der gleichmäßigen Kreisbewegung: Zusammenhang
Physikalische Formelsammlung Gleichförmige Bahnbewegung und Kreisbewegung Bewegungsgleichung für die gleichförmige lineare Bewegung: Winkelgeschwindigkeit bei der gleichmäßigen Kreisbewegung: Zusammenhang
Versuch 1.6: Franck-Hertz-Versuch
 Physikalisches Praktikum für Fortgeschrittene TU Darmstadt Abteilung A: Angewandte Physik Versuch 1.6: Franck-Hertz-Versuch Stefan A. Gärtner Durchgeführt mit: Christian Klose Betreut von: Dr. Rainer Spehr
Physikalisches Praktikum für Fortgeschrittene TU Darmstadt Abteilung A: Angewandte Physik Versuch 1.6: Franck-Hertz-Versuch Stefan A. Gärtner Durchgeführt mit: Christian Klose Betreut von: Dr. Rainer Spehr
Chemische Thermodynamik: Grundlagen
 Cheische herodynai: Grundlagen Marosoische Größen aros. Obserable in aros. Syste Intensie Größen (engenunabhängig): Druc eeratur Magnetfeld H r Magnetisierung M r Eletrisches Feld E r... Etensie Größen
Cheische herodynai: Grundlagen Marosoische Größen aros. Obserable in aros. Syste Intensie Größen (engenunabhängig): Druc eeratur Magnetfeld H r Magnetisierung M r Eletrisches Feld E r... Etensie Größen
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Diese Präsentation soll in kurzer Form den zweiten Teil des Kapitels thermische Eigenschaften der Phononen näher erläutern. Im Speziellen wird auf
 Diese Präsentation soll in kurzer Form den zweiten Teil des Kapitels thermische Eigenschaften der Phononen näher erläutern. Im Speziellen wird auf den Zusammenhang zwischen anharmonischen Kristallwechselwirkungen
Diese Präsentation soll in kurzer Form den zweiten Teil des Kapitels thermische Eigenschaften der Phononen näher erläutern. Im Speziellen wird auf den Zusammenhang zwischen anharmonischen Kristallwechselwirkungen
Der Dampfdruck von Wasser
 Physikalisches Grundpraktikum Versuch 8 Der Dampfdruck von Wasser Praktikant: Tobias Wegener Alexander Osterkorn E-Mail: tobias.wegener@stud.uni-goettingen.de a.osterkorn@stud.uni-goettingen.de Tutor:
Physikalisches Grundpraktikum Versuch 8 Der Dampfdruck von Wasser Praktikant: Tobias Wegener Alexander Osterkorn E-Mail: tobias.wegener@stud.uni-goettingen.de a.osterkorn@stud.uni-goettingen.de Tutor:
Projekt Standardisierte schriftliche Reifeprüfung in Mathematik. T e s t h e f t B 1. Schulbezeichnung:.. Klasse: Vorname: Datum:.
 Projekt Standardisierte schriftliche Reifeprüfung in Mathematik T e s t h e f t B Schulbezeichnung:.. Klasse: Schüler(in) Nachname:. Vorname: Datum:. B Große und kleine Zahlen In Wikipedia findet man die
Projekt Standardisierte schriftliche Reifeprüfung in Mathematik T e s t h e f t B Schulbezeichnung:.. Klasse: Schüler(in) Nachname:. Vorname: Datum:. B Große und kleine Zahlen In Wikipedia findet man die
Themengebiet: Mechanik
 Seite 1 Themengebiet: Mechanik 1 Literatur D. Meschede, Gerthsen Physik, Springer, Berlin M. Wutz, H. Adam, W. Walcher, Theorie und Praxis der technik, Vieweg 2 Grundlagen Historisch gesehen bezeichnet
Seite 1 Themengebiet: Mechanik 1 Literatur D. Meschede, Gerthsen Physik, Springer, Berlin M. Wutz, H. Adam, W. Walcher, Theorie und Praxis der technik, Vieweg 2 Grundlagen Historisch gesehen bezeichnet
Physikalische Chemie. Heinz Hug Wolfgang Reiser EHRMITTEL. EUROPA-FACHBUCHREIHE für Chemieberufe. 2. neu bearbeitete Auflage. von
 2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. EHRMITTEL EUROPA-FACHBUCHREIHE für Chemieberufe Physikalische Chemie
2008 AGI-Information Management Consultants May be used for personal purporses only or by libraries associated to dandelon.com network. EHRMITTEL EUROPA-FACHBUCHREIHE für Chemieberufe Physikalische Chemie
= 8.28 10 23 g = 50u. n = 1 a 3 = = 2.02 10 8 = 2.02Å. 2 a. k G = Die Dispersionsfunktion hat an der Brillouinzonengrenze ein Maximum; dort gilt also
 Aufgabe 1 Ein reines Material habe sc-struktur und eine Dichte von 10 g/cm ; in (1,1,1) Richtung messen Sie eine Schallgeschwindigkeit (für große Wellenlängen) von 000 m/s. Außerdem messen Sie bei nicht
Aufgabe 1 Ein reines Material habe sc-struktur und eine Dichte von 10 g/cm ; in (1,1,1) Richtung messen Sie eine Schallgeschwindigkeit (für große Wellenlängen) von 000 m/s. Außerdem messen Sie bei nicht
Bestimmung von Federkonstanten
 D. Samm 2014 1 Bestimmung von Federkonstanten 1 Der Versuch im Überblick Ohne Zweifel! Stürzt man sich - festgezurrt wie bei einem Bungee-Sprung - in die Tiefe (Abb. 1), sind Kenntnisse über die Längenänderung
D. Samm 2014 1 Bestimmung von Federkonstanten 1 Der Versuch im Überblick Ohne Zweifel! Stürzt man sich - festgezurrt wie bei einem Bungee-Sprung - in die Tiefe (Abb. 1), sind Kenntnisse über die Längenänderung
21. Wärmekraftmaschinen
 . Wärmekraftmaschinen.. Einleitung Wärmekraftmaschinen (Motoren, Gasturbinen) wandeln Wärmeenergie in mechanische Energie um. Analoge Maschinen ( Kraftwärmemaschinen ) verwandeln mechanische Energie in
. Wärmekraftmaschinen.. Einleitung Wärmekraftmaschinen (Motoren, Gasturbinen) wandeln Wärmeenergie in mechanische Energie um. Analoge Maschinen ( Kraftwärmemaschinen ) verwandeln mechanische Energie in
Thermodynamik Wärmestrom
 Folie 1/11 Werden zwei Körper mit unterschiedlichen Temperaturen in thermischen Kontakt miteinander gebracht, so strömt Wärme immer vom Körper mit der höheren Temperatur auf den Körper mit der niedrigen
Folie 1/11 Werden zwei Körper mit unterschiedlichen Temperaturen in thermischen Kontakt miteinander gebracht, so strömt Wärme immer vom Körper mit der höheren Temperatur auf den Körper mit der niedrigen
Wie man sieht ist der Luftwiderstand -abgesehen von der Fahrgeschwindigkeit- nur von Werten abhängig, die sich während der Messung nicht ändern.
 Wie hoch ist der - und Luftwiderstand eines Autos? Original s. http://www.arstechnica.de/index.html (Diese Seite bietet außer dieser Aufgabe mehr Interessantes zur Kfz-Technik) Kann man den Luftwiderstand
Wie hoch ist der - und Luftwiderstand eines Autos? Original s. http://www.arstechnica.de/index.html (Diese Seite bietet außer dieser Aufgabe mehr Interessantes zur Kfz-Technik) Kann man den Luftwiderstand
Physik 1 VNT Aufgabenblatt 8 5. Übung (50. KW)
 Physik 1 VNT Aufgabenblatt 8 5. Übung (5. KW) 5. Übung (5. KW) Aufgabe 1 (Achterbahn) Start v h 1 25 m h 2 2 m Ziel v 2? v 1 Welche Geschwindigkeit erreicht die Achterbahn in der Abbildung, wenn deren
Physik 1 VNT Aufgabenblatt 8 5. Übung (5. KW) 5. Übung (5. KW) Aufgabe 1 (Achterbahn) Start v h 1 25 m h 2 2 m Ziel v 2? v 1 Welche Geschwindigkeit erreicht die Achterbahn in der Abbildung, wenn deren
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde. Sommersemester 2007
 Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #45 am 18.07.2007 Vladimir Dyakonov Erzeugung von Interferenzen: 1) Durch Wellenfrontaufspaltung
Einführung in die Physik II für Studierende der Naturwissenschaften und Zahnheilkunde Sommersemester 2007 VL #45 am 18.07.2007 Vladimir Dyakonov Erzeugung von Interferenzen: 1) Durch Wellenfrontaufspaltung
