Prüfung von Ausgangsstoffen. Simon
|
|
|
- Irma Voss
- vor 6 Jahren
- Abrufe
Transkript
1 Prüfung von Ausgangsstoffen 1
2 Was sind Ausgangsstoffe 1a ApoBetrO: Begriffsbestimmungen (6) Ausgangsstoff ist jeder bei der Herstellung eines Arzneimittels verwendete Stoff oder jede Zubereitung aus Stoffen, ausgenommen Verpackungsmaterial 2
3 11 ApoBetrO Ausgangsstoffe (1) Zur Herstellung von Arzneimitteln dürfen nur Ausgangsstoffe verwendet werden, deren ordnungsgemäße Qualität festgestellt ist. Auf die Prüfung der Ausgangsstoffe finden die Vorschriften des 6 Abs. 1 und 3 entsprechende Anwendung. 3
4 11 ApoBetrO Ausgangsstoffe (2) Werden Ausgangsstoffe bezogen, deren Qualität durch ein Prüfzertifikat nach 6 Abs. 3 nachgewiesen ist, ist in der Apotheke mindestens die Identität festzustellen Die Verantwortung des Apothekenleiters für die ordnungsgemäße Qualität der Ausgangsstoffe bleibt unberührt. Über die in der Apotheke durchgeführten Prüfungen sind Aufzeichnungen mit Namenszeichen des Prüfenden oder die Prüfung beaufsichtigenden Apothekers zu machen. 4
5 6 ApoBetrO Allgemeine Vorschriften über die Herstellung und Prüfung (1) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen Wissenschaft erforderliche Qualität ausweisen. Sie sind nach den anerkannten pharmazeutischen Regeln herzustellen und zu prüfen; enthält das Arzneibuch entsprechende Regeln, sind die Arzneimittel nach diesen Regeln herzustellen und zu prüfen. 5
6 6 ApoBetrO Dabei können für die Prüfung auch andere Methoden angewandt und andere Geräte benutzt werden, als im Deutschen Arzneibuch beschrieben sind, unter der Voraussetzung, dass die gleichen Ergebnisse wie mit den beschriebenen Methoden und Geräten erzielt werden. Soweit erforderlich, ist die Prüfung in angemessenen Zeiträumen zu wiederholen. 6
7 6 ApoBetrO (3) Die Prüfung der Arzneimittel kann unter Verantwortung des Apothekenleiters auch außerhalb der Apotheke... erfolgen. Der für die Prüfung Verantwortliche des Betriebes.. hat unter Angabe der Charge sowie des Datums und der Ergebnisse der Prüfung zu bescheinigen, dass das Arzneimittel nach den anerkannten pharm. Regeln geprüft worden ist und die erforderliche Qualität aufweist (Prüfzertifikat). 7
8 6 ApoBetrO Die Ergebnisse aus dem Prüfzertifikat sind der Freigabe in der Apotheke zugrunde zu legen. In der Apotheke ist mindestens die Identität des Arzneimittels festzustellen; über die durchgeführten Prüfungen sind Aufzeichnungen zu machen. 8
9 Prüfung der Grundstoffe außerhalb der Apotheke Zertifikat muss vorliegen Identität muss in der Apotheke erneut geprüft werden Die Verantwortung für die Qualität trägt trotz Zertifikat der Apothekenleiter 9
10 Ausgangsstoffe, was ist in der Praxis zu beachten Arzneibuch-Qualität notwendig Bedarfsgerecht bestellen Exakte Bezeichnung (z.b. freie Base oder Salz), für Anwendung geeignet? Besondere Eigenschaften (z.b. mikronisiert) Eventuell Rezepturkonzentrate, Verreibungen bevorzugen Nur Ware mit gültigem Prüfzertifikat verwenden 10
11 Eingang von Ausgangsstoffen Vorsicht bei Ersatzlieferungen vom GH Prüfzertifikat vorhanden? Ausgangsstoff nach dem Wareneingang unverzüglich der Quarantäne zuführen, solange noch keine Identitätsprüfung durchgeführt wurde 11
12 Wer darf prüfen? Die Prüfung ist laut 1a ApoBetrO eine pharmazeutische Tätigkeit (3) Pharmazeutische Tätigkeit im Sinne dieser Verordnung ist 2. die Prüfung von Ausgangsstoffen oder Arzneimitteln 12
13 Prüfungsvorschriften DAB, PhEur, HAB, DAC USP, BP, ÖAB etc. DAC Band 3 Alternative Identifizierungen Rohdewald... Apothekengerechte Prüfvorschriften Wichtl: Teedrogen Pachaly: DC Atlas Hagers Handbuch, Stoffliste Standardzulassungen 13
14 Identätsprüfungen in der Apothekenpraxis Schmelzpunkt (Mischschmelzpunkt) Micro-DC Nass-chemische Reaktionen Brechungsindex Dichte 14
15 Beispiel Identitätsprüfung Clotrimazol PH. EUR.: 1: B 2: A,C A: Schmelztemperatur (2.2.14) 141 bis 145 C B: IR-Spektroskopie ( ) Vergleich: Clotrimazol CRS C: Dünnschichtchromatographie (2.2.27) 15
16 Beispiel Identitätsprüfung Clotrimazol DAC Alternative Identitätsprüfungen: Weißes bis blassgelbes, kristallines Pulver Schmelztemperatur (2.2.60) C ohne vorheriges Trocknen Mischschmelzpunkt (DAC-Probe 3) Die Differenz zwischen der Schmelztemperatur der Substanz und dem Mischschmelzpunkt darf höchstens 1 C betragen 16
17 Beispiel Identitätsprüfung PH. EUR.: 1: A,B 2: A,C,D Harnstoff A: Schmelztemperatur (2.2.14) 132 bis 135 C B: IR Spektroskopie C: 0,1g Substanz werden in 1 ml Salpetersäure bildet sich ein weißer, kristalliner- Niederschlag D: ebenfalls Nasschemisch 17
18 Beispiel Identitätsprüfung Harnstoff DAC Alternative Identitätsprüfungen: Weißes, kristallines Pulver Schmelztemperatur (2.2.60) C ohne vorheriges Trocknen Mischschmelzpunkt (DAC-Probe 3) Die Differenz zwischen der Schmelztemperatur der Substanz und dem Mischschmelzpunkt darf höchstens 1 C betragen 18
19 Beispiel Identitätsprüfung Natriumcitrat PH. EUR.: A: 1ml Prüflösung mit 4ml Wasser R verdünnt gibt die Identitätsreaktion auf Citrat (2.3.1) B: 1ml Prüflösung gibt die Identitätsreaktion auf Natrium (2.3.1) 19
20 Basiscreme DAC Alternative Identifizierung Stand DAC Aussehen: weiße, weiche, mit Wasser von der Haut abwaschbare Creme. Geruch: schwach. Nichtionische Emulgatoren: 50 mg Zubereitung werden in einem engen Reagenzglas mit 0,1 ml einer wässrigen Lösung von Methylenblau R (1,5 g L 1), 2 ml verdünnter Schwefelsäure R und 2 ml Dichlormethan R versetzt. Nach kräftigem Schütteln ist die obere Phase intensiver blau gefärbt als die untere. Hydrophile Creme: 0,5 g Zubereitung werden anteilsweise mit 10 ml Wasser R verrührt. Es entsteht eine gleichmäßig getrübte, milchige Mischung. 20
21 Erythromycin Alternative Identifizierung Stand DAC Erythromycin Aussehen: weißes bis schwach gelbes Pulver oder farblose bis schwach gelbe Kristalle, schwach hygroskopisch. Dünnschichtchromatographie (DAC-Probe 11) Untersuchungslösung: 5 mg Substanz werden in 5 ml Methanol R gelöst. Referenzlösung: 5 mg Erythromycin, dessen Identität bekannt ist, werden in 5 ml Methanol R gelöst. Untersuchungsbedingungen Stationäre Phase: DC-Platte mit Kieselgel R. Auftragevolumen: je 2 μl, punktförmig. Fließmittel: Mischung aus 90 Volumteilen Methanol R und 10 Volumteilen Ethylacetat R. Laufstrecke: 6 cm. Detektion und Auswertung Die Platte wird an der Luft getrocknet, mit Anisaldehyd-Reagenz R besprüht oder darin getaucht und bei 110 C unter Beobachtung bis zur deutlichen Farbentwicklung der Flecke erhitzt. Nach dem Erkalten wird im Tageslicht ausgewertet. In den Chromatogrammen der Untersuchungslösung und der Referenzlösung tritt im unteren Drittel jeweils ein brauner Fleck mit dem gleichen Rf-Wert und der gleichen Intensität auf. 21
22 Angaben auf dem Prüfzertifikat Bezeichnung des Stoffes Prüfvorschrift Chargennummer Hersteller Prüfergebnisse: maßgebliche Zahlenwerte sind aufzuführen Datum der Prüfung Name des für die Prüfung Verantwortlichen 22
23 Clotrimazol Ph. Eur.... Clotrimazol micronisiert 5 g Ch.-B Fa. Chemifix Clotrimazol, micronisiert Ch.-B Prüfvorschrift Ph.Eur. Identität entspricht Reinheit entspricht Sulfatasche < 0,1% ( 0,1%) Verwandte Substanzen entspricht Trocknungsverlust 0,2% ( 0,5 %) Gehalt 100,1 % (98,5-100,5%) Dr. Unbekannt (Kontrollleiter) 23
24 Urea pura Ph. Eur... Harnstoff 25 g Ch.-B Fa. Chemifix Urea pura Ch.-B Prüfvorschrift Ph. Eur... Identität entspricht Reinheit entspricht alkalische Substanzen entspricht Biuret < 0,1% ( 0,1%) Ammonium < 500ppm ( 500ppm) Schwermetalle < 10 ppm ( 500ppm ) Sulfatasche < 0,1% ( 0,1 %) Trockungsverlust 0,17% ( 1,0%) Gehalt 100,1 % ( 98,5 101,5 %) Dr. Unbekannt (Kontrollleiter) 24
25 Erythrmoycin Ph. Eur.... Erythromycin micronisiert 5 g Ch.-B Fa. Chemifix Erythromycin, micronisiert Ch.-B Prüfvorschrift Ph.Eur. Identität entspricht Reinheit entspricht Spez. Drehung: -75 ( ) Verwandte Substanzen entspricht ( 3,0%) Thyocyanat 0,1% ( 0,3%) Wasser 1,8% ( 6,5%) Sulfatasche < 0,1%(< 0,2%) Gehalt 97,5% (93,0-102,0%) Dr. Unbekannt (Kontrollleiter) 25
26 Korrekturfaktor Ziel: Vermeidung von Mindergehalten der Wirkund Konservierungsstoffen einer Zubereitung Berechnung der Einwaagekorrektur auf den chargenspezifischen Wirkstoffgehalt Allgemeine Hinweise: NRF I.2.11 Sehr einfach durchzuführen mit dem NRF Tool Ermittelter Korrekturfaktor im Prüfprotokoll und auf der Rezeptursubstanz vermerken 26
27 Beispiel 1: Korrekturfaktor Bsp: Erythromycin Gehalt: 97,5% Wasser: 1,8% Korrekturfaktor: 1,044 Beispiel 2: Gehalt: 97,6% Wasser: 3,7% Korrekturfaktor: 1,064 27
28 Haltbarkeit von Ausgangsstoffen Im Arzneibuch sind keine Angaben zu finden Heute geben fast alle Hersteller Haltbarkeitsdaten oder Retestdaten an, danach muss der Ausgangsstoff einer Nachprüfung unterzogen oder vernichtet werden Karsten Albert: Verwendbarkeitsfristen von Ausgangsstoffen in der Apotheke Maßgeblich ist das Prüfdatum Wichtig: am Standgefäß Haltbarkeit kenntlich machen 28
29 Prüfprotokoll Folgende Angaben sind aufzuzeichnen: Name des Ausgangsstoffes Hersteller Herstellercharge Prüfdatum Interne Charge Haltbarkeit Verwendete Prüfvorschrift Ergebnisse (Zahlenwerte etc.!!!) der durchgeführten Prüfung Namenszeichen Prüfender Datum und Unterschrift der Freigabe (Apotheker) Das Zertifikat ist Bestandteil des Prüfprotokolls Zusätzlich: Haltbarkeit, Korrekturfaktor 29
30 22 ApoBetrO Allgemeine Dokumentation Das Prüfprotokoll muss aufbewahrt werden Das Prüfzertifikat muss ebenfalls aufbewahrt werden (sinnvoll: mit Prüfprotokoll fixieren) Aufbewahrungsfrist: Mindestens 5 Jahre Mindestens 1 Jahr nach Ablauf des Verfalldatums 30
31 Kennzeichnung des Ausgangsstoffes Vorschriften der Gefahrstoffverordnung beachten Auf der Verpackung des Ausgangsstoffes oder auf dem Standgefäß sind folgende zusätzliche Angaben zu machen: Interne Charge Verfalldatum (falls nicht schon angegeben) Korrekturfaktor (falls nicht schon angegeben) 31
32 Wie sieht die Praxis aus? Beim Wareneingang darauf achten, dass es sich um Arzneibuchware handelt Mit Sachverstand arbeiten Nur das dokumentieren, was durchgeführt wurde (Täuschung!) Alle Unregelmäßigkeiten im Protokoll festhalten Sogenannte organoleptische Prüfungen sind nicht ausreichend! 32
33 Beispiele für Verwechslungen Kaliumhydroxid Natriumhydroxid Zinkpaste Weiche Zinkpaste Sennesblätter Birkenblätter Isopropanol - Isobutanol Wasserstoffperoxyd Salmiaklösung Erythromycin Clotrimazol Hammamelisblätter - Ginkgoblätter 33
34 Leitlinie zur Prüfung von Ausgansstoffen Homepage der ABDA: abda.de» Themen» Arbeit in der Apotheke» Qualitätssicherung» Leitlinien und Arbeitshilfen Leitlinie Prüfung von FAM 34
35 Durchführung der Wareneingangskontrolle Weiterleitung der ungeprüften Ware in den Quarantänebereich zur Prüfung der Ausgangsstoffe ( 16 Abs. 1 ApBetrO) Monographie oder anerkanntes Prüfverfahren für den Ausgangsstoff vorhanden? Prüfung und Lagerung der Ausgangsstoffe Stand: Nein Wareneingangskontrolle Kontrolle des Lieferscheins (Vergleich mit Bestelldaten und Angaben auf dem Gebinde) Vorhandensein des Prüfzertifikats und ggf. des Sicherheitsdatenblatts Sichtprüfung der Verpackung/Gebinde Kontrolle der Einhaltung der Transportbedingungen Bei Abweichungen Apotheker hinzuziehen Eingangsprüfung Prüfvorschrift auswählen Ph. Eur., DAB oder andere Vorschriftensammlungen Alternative Identifizierung von Ausgangsstoffen nach DAC/NRF Ggf. Prüfanweisung des Herstellers Der Ausgangsstoff kann nicht verwendet werden. Eine Ausnahme ist nur im begründeten Einzelfall (Nutzen-Risiko-Abwägung) möglich. Ja Prüfzertifikat vorhanden? Ja Kontrolle des Prüfzertifikats Prüfzertifikat valide? Ja Vorschrift für Identitätsprüfung im DAC vorhanden? Ja Prüfung nach DAC-Vorschrift Nein Nein Nein Ersatz durch vorgeprüften Ausgangsstoff oder Komplettprüfung nach Vorgaben der Monographie bzw. dem anerkannten Prüfverfahren Eingangsprüfung Kontrolle des Prüfzertifikats Erforderliche Angaben Beurteilung der Eignung/Angemessenheit der eingesetzten Methode Vergleich der Analysenwerte mit den Soll-Werten der aktuellen Arzneibuchmonographie Ggf. Bescheinigung über GMP-konforme Herstellung Der Ausgangsstoff kann nicht verwendet werden. Prüfung auf Identität gemäß Arzneibuchmonographie oder nach anderer Pharmakopöe durchführen Entnahme von Teilmengen zur Prüfung Identitätsprüfung ( 6, 11 ApBetrO) Fachgerechte Entnahme von Teilmengen aus dem Behältnis Beachtung der Arbeitsschutzmaßnahmen Beachtung der Maßnahmen zum Produktschutz Durchführung der Prüfung zur Identifizierung des Ausgangsstoffs und Erstellung des Prüfprotokolls ( 6, 11 ApBetrO) Erstellung des Prüfprotokolls in der Apotheke Interne Prüfnummer festlegen Prüfzertifikat aufkleben oder anheften Ergebnis der Prüfung des Prüfzertifikates dokumentieren Lagerungsbedingungen, Verwendbarkeitsfrist bzw. Nachprüfdatum festlegen Ggf. Faktor zur Einwaagekorrektur vermerken Prüfvorschrift, -methoden und -ergebnisse vermerken Name des Prüfenden Geeignete Kennzeichnung der geprüften Ware ( 16 Abs. 1 ApBetrO) Archivierung der Prüfprotokolle ( 22 ApBetrO) A 35
36 Fortsetzung A Qualitätsmängel bei der Prüfung? Verweis auf Leitlinie zur Qualitätssicherung - Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Ja Maßnahmen einleiten und Sperrung der Ware Dokumentation der Maßnahmen Verfahren bei Qualitätsmängeln ( 21 ApBetrO) Mitteilung an die zuständige Behörde und AMK Dokumentation/Berichterstattung der Qualitätsmängel unter Verwendung der AMK-Berichtsbögen Entscheidung über den Verbleib des Prüfmusters nach Absprache mit zuständiger Behörde und AMK Verbleib nicht einwandfreier Ware im Quarantänebereich bis zur endgültigen Entscheidung Festlegung der Verwendbarkeitsfrist oder des Nachprüfdatums Freigabe der geprüften Ausgangsstoffe Ordnungsgemäße Kennzeichnung und Lagerung der Ausgangsstoffe Entscheidung über die Ware treffen Bewertung der Ergebnisse Datum und Unterschrift des Apothekers im Prüfprotokoll Beschriftung und Kennzeichnung der Behältnisse Gut lesbar und dauerhaft Vorzugsweise in deutscher Sprache Bezeichnung des Ausgangstoffes Verfallsdatum, ggf. Verwendbarkeitsfrist oder Nachprüfdatum Soweit mgl., Normdosierung, Höchstmenge oder Richtkonzentration Verwendungshinweise Bei Wirkstoffen Einwaagekorrekturfaktor(en) Interne Prüfnummer Lieferant/PZN Lagertemperatur Gemäß GefStoffV, ggf. vereinfachte Kennzeichnung Nein, Verwendbarkeitsfrist erreicht Entnahme von Teilmengen zur Herstellung von Rezepturen und Defekturen Nachprüfung möglich? Durchführung der Nachprüfung Ja Verweis auf Leitlinie zur Qualitätssicherung Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Ordnungsgemäße Lagerung der Ausgangsstoffe ( 16 ApBetrO, 8, 11 GefStoffV) Lagerungsbedingungen (Ph. Eur., DAB) Getrennte Lagerung von Ausgangsstoffen und Chemikalien Dicht schließende Behältnisse Vor Licht geschützt Ggf. Trocknungsmittel verwenden Ggf. unter Verschluss ( 8 Abs. 7 GefStoffV) Nachprüfung Verlängerung der Nutzungsdauer der Substanz unter Berücksichtigung der Kosten/Nutzen-Relation Keine Bezugnahme auf das Prüfzertifikat des Herstellers Prüfung auf Konformität mit der Arzneibuch-Monographie Prüfung der Parameter, die nach der Herstellung veränderbar sind, wie z. B. ph-wert, Aussehen, Trocknungsverlust, Wasser, Gehalt, ggf. Identität Immer individuelle Festlegung der Parameter im Einzelfall Nein Qualitätsmängel bei der Prüfung? Vernichtung der Ausgangsstoffe Ja Vernichtung Sachgerechte/umweltgerechte Entsorgung (Entsorgungssysteme der Rezeptur und des Laboratoriums verwenden) 36
37 Prüfung von Fertigarzneimitteln in der Apotheke 37
38 PRÜFUNG VON FAM 12 ApoBetrO Prüfung der nicht in der Apotheke hergestellten Fertigarzneimittel (FAM) und apothekenpflichtigen Medizinprodukte 38
39 PRÜFUNG VON FAM 12 ApoBetrO (1) FAM, die nicht in der Apotheke hergestellt worden sind, sind stichprobenweise zu prüfen. Dabei darf von einer über die Sinnesprüfung hinausgehenden Prüfung abgesehen werden, wenn sich keine Anhaltspunkte ergeben haben, die Zweifel an der ordnungsgemäßen Qualität des Arzneimittels begründen. Die Sätze 1 und 2 gelten für apothekenpflichtige Medizinprodukte entsprechend. 39
40 Bedeutung der FAM-Prüfung Es werden in ca Apotheken in der BRD pro Tag 1 Untersuchung durchgeführt (24 pro Monat) Dies ergibt Untersuchungen pro Monat Dies entspricht 5,76 Mio Untersuchungen pro Jahr 40
41 Prüfhäufigkeit stichprobenweise, keine verbindliche Zahl vorgeschrieben Abhängig von der Größe des Warenlagers Regierungspräsidium Darmstadt verlangt in Hessen mindestens 1 FAM pro Arbeitstag 41
42 Probenentnahme Wareneingang Lagerbestand Alle Darreichungsformen und Lagerorte berücksichtigen Am besten: betriebsinternes festgelegtes System für Probenzug 42
43 Wer darf prüfen? Die Prüfung ist laut 1a ApoBetrO eine pharmazeutische Tätigkeit Nur pharmazeutisches Personal darf diese durchführen Unterstützung durch PKA möglich Abzeichnung des Protokolls nur durch einen Apotheker 43
44 Durchführung der Prüfung Prüfung der Kennzeichnung ( 10 AMG) Prüfung der Packungsbeilage ( 11 AMG) Prüfung des Primär- und Sekundärpackmittels Prüfung des AM je nach Darreichungsform 44
45 Prüfung nach 10 und 11 AMG Entsprechende Vorschrift aus dem aktuellen AMG heraussuchen 10 Kennzeichnung des FAM 11 Angaben in der Packungsbeilage 45
46 Prüfung der Packmittel Dichtigkeit der Verschlüsse Unversehrtheit (Schraubverschlüsse, Blisterfolie) Deklaration Übereinstimmung der Charge Vorhandensein der Packungsbeilage Verfalldatum 46
47 Prüfung der Arzneiform Sinnesprüfung Ohne Verdacht keine zerstörende Prüfung notwendig (Kosten!) Durch die Verpackung der FAM teilweise nur schwer durchführbar Dennoch häufig Prüfung auf Vollständigkeit der Arzneimittelmenge möglich 47
48 Umstände, die die Prüfung erschweren Umverpackung ist versiegelt Blisterfolie ist nicht durchsichtig Tube ist zugesiegelt Schraubverschluss ist versiegelt Flaschen sind nicht durchsichtig (z.b. braun, milchig, weiß) 48
49 Prüfung von FAM 12 ApoBetrO (2) Das anzufertigende Prüfprotokoll muss mindestens enthalten: 1. Den Namen oder die Firma des Pharmazeutischen Unternehmers, bei Medizinprodukten des Herstellers 2. Die Bezeichnung und Darreichungsform des Arzneimittels 3. Die Chargenbezeichnung oder das Herstellungsdatum 4. Das Datum und die Ergebnisse der Prüfung 5. Das Namenszeichen des prüfenden oder die Prüfung beaufsichtigenden Apothekers 49
50 Prüfprotokoll Es gibt keine Formvorschrift Tabellarische Auflistung der Ergebnisse möglich Empfehlenswert sind aber detaillierte Aufzeichnungen wie z.b. im Prüfprotokoll der BAK 50
51 Dokumentation Aufbewahrungsfrist nach 22 ApoBetrO: Mindestens 5 Jahre Mindestens bis 1 Jahr nach Ablauf des Verfalldatums 51
52 Verfahren bei Qualitätsmangel Arzneimittel, bei denen ein Qualitätsmangel festgestellt wurde sind nicht mehr verkehrsfähig Arzneimittel muss unverzüglich in die Quarantäne 52
53 21 ApoBetrO Arzneimittelrisiken, Behandlung nicht verkehrsfähiger AM (1) Alle Informationen über Beanstandungen bei AM sind dem Apothekenleiter unverzüglich mitzuteilen. (2) Er.. hat die erforderlichen Maßnahmen zur Gefahrenabwehr zu veranlassen. 53
54 21 (3) Ist bei Arzneimitteln oder Ausgangsstoffen, die die Apotheke bezogen hat, die Annahme gerechtfertigt, daß Qualitätsmängel vorliegen, die vom Hersteller verursacht sind, ist die zuständige Behörde unverzüglich zu benachrichtigen. 54
55 21 (4) Bei Rückruf von AM, die in der Apotheke hergestellt worden sind, ist die zuständige Behörde unter Angabe des Grundes unverzüglich zu benachrichtigen. 55
56 Risiken bei Arzneimitteln Maßnahmen in der Apotheke - Meldung pharmazeutischer Qualitätsmängel bei Arzneimitteln - Stand: Verdacht auf Qualitätsmängel Verweis auf Leitlinien zur Qualitätssicherung - Prüfung und Lagerung der Ausgangsstoffe - Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Qualitätsmängel können sichtbar werden bei: - Prüfung der Fertigarzneimittel - Prüfung des Wareneingangs - Reklamation des Patienten oder des Arztes Qualitätsmängel können sein, z. B. - Mängel der Beschaffenheit (Identität, Gehalt, Reinheit) - Mängel der Behältnisse und äußeren Umhüllung - Mängel der Kennzeichnung und der Fach- und Gebrauchsinformation - Arzneimittelfälschungen - Weitere technische Mängel Prüfung und Bewertung des Risikos durch Apotheker Erforderliche Maßnahmen einleiten Erforderliche Maßnahmen - Quarantänelagerung des Arzneimittels und der ggf. vorhandenen Restbestände der Charge in der Apotheke bis zur Klärung Meldung an die Überwachungsbehörde Meldung an die AMK Meldungen an die Überwachungsbehörde und die Arzneimittelkommission der Deutschen Apotheker (AMK) - Berichtsbogen der AMK Berichtsbogen über Verdachtsfälle auf Qualitätsmängel von Arzneimitteln (Kopie der AMK-Meldung an die zuständige Überwachungsbehörde) - Ggf. Einsendung des Produkts, der Packungsbeilage,des Umkartons Dokumentation Dokumentation - Kopie des Berichtsbogens - Mitteilung über Ergebnis der Untersuchung - Aufzeichnung über Rückrufe und durchgeführte Maßnahmen - Archivierung für mindestens ein Jahr nach Ablauf des Verfallsdatums, jedoch nicht weniger als fünf Jahre 56
57 Zuständige Behörde Die zuständige Behörde ist in Hessen das Regierungspräsidium in Darmstadt Die zuständige Behörde ist nicht die AMK der Apotheker, die aber dennoch zu benachrichtigen ist!!!!!! 57
58 Benachrichtigung der AMK der ABDA Nach 3 der Berufsordnung der Landesapothekerkammer Hessen müssen Arzneimittelrisiken auch der AMK gemeldet werden, unabhängig einer Meldung an das RP Die AMK ist die zuständige Stelle für Meldungen nach 62 AMG 58
59 Bearbeitung der Quarantäne Berichtsbogen der ABDA benutzen Auf der Homepage der ABDA online ausfüllen oder ausdrucken Auch ein Zusenden seitens der AMK ist möglich 59
60 Berichtsbogen ABDA Homepage»Themen»Arzneimittelsicherheit AMK»Berichtsbogen Formulare 60
61 Bearbeitung der Quarantäne Berichtsbogen Qualitätsmängel In der Regel müssen Meldungen sowohl an das RP als auch an die AMK geschickt werden Zeitfaktor berücksichtigen: Meldungen möglichst schnell per FAX oder an die entsprechenden Stellen senden 61
62 Berichtsbogen UAW 62 Pharmakovigilanz und 63 AMG Stufenplan und eine Verwaltungsvorschrift regeln das Vorgehen bei Arzneimittelrisiken Dabei ist die Arzneimittelkommision (AMK) der Apotheker als zuständige Stelle genannt Die AMK ist verpflichtet, Meldungen über Verdachtsfälle an die zuständige Bundesoberoder Landesbehörde weiterzuleiten 62
63 Vorkomnisse bei Medizinprodukten Ein Vorkommnis ist eine Funktionsstörung, ein Ausfall oder eine Änderung der Merkmale oder der Leistung oder eine Unsachgemäßheit der Kennzeichnung oder der Gebrauchsanweisung eines Medizinprodukts... als Funktionsstörung gilt auch ein Mangel der Gebrauchstauglichkeit, der eine Fehlanwendung verursacht. Meldungen erfolgen an das BfArM 63
64 Risiken bei Medizinprodukten Maßnahmen in der Apotheke - Meldung von Vorkommnissen bei Medizinprodukten - Stand: Vorkommnis bei einem Medizinprodukt Vorkommnis ist: - Funktionsstörung (auch Mangel der Gebrauchstauglichkeit, der eine Fehlanwendung verursacht), Ausfall, Änderung der Merkmale oder der Leistung oder - unsachgemäße Kennzeichnung oder Gebrauchsanweisung die oder der unmittelbar oder mittelbar zum Tod oder zu einer schwerwiegenden Verschlechterung des Gesundheitszustands eines Patienten, eines Anwenders oder einer anderen Person geführt hat, geführt haben könnte oder führen könnten Prüfung und Bewertung des Vorkommnisses durch Apotheker Erforderliche Maßnahmen einleiten Erforderliche Maßnahmen -Quarantänelagerung des Medizinprodukts in der Apotheke bis zur Klärung Meldung an die Überwachungsbehörde Meldungen an die Überwachungsbehörde (BfArM) - Formular des BfArM zur Meldung von Vorkommnissen bei Medizinprodukten - Medizinprodukt ggf. dem Hersteller für weitere Untersuchungen zur Verfügung stellen Dokumentation Dokumentation - Kopie des Meldebogens - Archivierung für mindestens ein Jahr nach Ablauf des Verfallsdatums, jedoch nicht weniger als fünf Jahre 64
65 Meldungen an die AMK 2016 Qualitätsmeldungen: 6251 Verpackungsfehler: 2640 Galenische Mängel 1547 Mechanische Defekte: 1060 Deklarationsmängel: 725 Minderwirkung: 170 Sonstiges: 95 Manipulation/Fälschungen: 14 65
66 AMK Chargenrückrufe 10 Chargenüberprüfungen 35 Rückrufe 66
67 Leitlinie zur Prüfung von FAM Homepage der ABDA: abda.de» Themen» Arbeit in der Apotheke» Qualitätssicherung» Leitlinien und Arbeitshilfen Leitlinie Prüfung von FAM 67
Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 23.11.2016 Inhaltsverzeichnis
Unter welchen Voraussetzungen werden Betriebe für den Bezug von Ausgangsstoffen anerkannt?
 I Hinweis zur Bearbeitung des Arbeitsbogens Führen Sie die Prüfung eines Ausgangsstoffes durch. Grundlage des Arbeitsbogens ist die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung und
I Hinweis zur Bearbeitung des Arbeitsbogens Führen Sie die Prüfung eines Ausgangsstoffes durch. Grundlage des Arbeitsbogens ist die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung und
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV Zweckbestimmung
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV Zweckbestimmung
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung der Fertigarzneimittel und apothekenpflichtigen
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Stand der Revision:16.06.2016 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Prüfung der Fertigarzneimittel und apothekenpflichtigen Medizinprodukte Stand der Revision:16.06.2016 Inhaltsverzeichnis
Wareneingang und Prüfung von Fertigarzneimitteln
 30 7 Wareneingang und Prüfung von Fertigarzneimitteln 7.1 Prüfung von Fertigarzneimitteln Wird pro Arbeitstag mindestens ein Fertigarzneimittel organoleptisch geprüft und die Prüfung dokumentiert? Es Auslegung
30 7 Wareneingang und Prüfung von Fertigarzneimitteln 7.1 Prüfung von Fertigarzneimitteln Wird pro Arbeitstag mindestens ein Fertigarzneimittel organoleptisch geprüft und die Prüfung dokumentiert? Es Auslegung
Die Prüfung der Ausgangsstoffe. Eine Hilfe zur Umsetzung
 Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung Gesetzliche Vorgaben Apothekenbetriebsordnung (ApBetrO) Arzneimittel, die in der Apotheke hergestellt werden, müssen die nach der pharmazeutischen
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Prüfung der Fertigarzneimittel
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 21.04.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
ARBEITSBOGEN 4: PRÜFUNG DER FERTIGARZNEIMITTEL UND APOTHEKENPFLICHTIGEN MEDIZIN- PRODUKTE
 I Hinweis zur Bearbeitung des Arbeitsbogens Überprüfen Sie ein Fertigarzneimittel (FAM) oder ein apothekenpflichtiges Medizinprodukt (MP) gemäß 12 Apothekenbetriebsordnung (ApBetrO). Grundlage des Arbeitsbogens
I Hinweis zur Bearbeitung des Arbeitsbogens Überprüfen Sie ein Fertigarzneimittel (FAM) oder ein apothekenpflichtiges Medizinprodukt (MP) gemäß 12 Apothekenbetriebsordnung (ApBetrO). Grundlage des Arbeitsbogens
Gesetzliche Vorgaben. Sammlung pharmazeutischer Regeln. Gesetzliche Vorgaben. Die Prüfung der Ausgangsstoffe. Eine Hilfe zur Umsetzung
 Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung 19.02.2008 Monika Paul 2 Sammlung pharmazeutischer Regeln Europäische Arzneibuch (Ph. Eur.) mit den harmonisierten Monographien Deutsche Arzneibuch
Die Prüfung der Ausgangsstoffe Eine Hilfe zur Umsetzung 19.02.2008 Monika Paul 2 Sammlung pharmazeutischer Regeln Europäische Arzneibuch (Ph. Eur.) mit den harmonisierten Monographien Deutsche Arzneibuch
Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Risiken bei Arzneimitteln und Medizinprodukten Maßnahmen in der Apotheke Stand der Revision: 13.11.2013 Inhaltsübersicht
FIT FÜR DIE ANALYTIK. Ingrid Tieke Caesar & Loretz GmbH
 FIT FÜR DIE ANALYTIK Ingrid Tieke Caesar & Loretz GmbH Interpharm 2017 Fit für die Analytik Ingrid Tieke Caesar & Loretz GmbH Interpharm, 1. April 2017 Gliederung 1. Gesetzliche Anforderungen an die Qualität
FIT FÜR DIE ANALYTIK Ingrid Tieke Caesar & Loretz GmbH Interpharm 2017 Fit für die Analytik Ingrid Tieke Caesar & Loretz GmbH Interpharm, 1. April 2017 Gliederung 1. Gesetzliche Anforderungen an die Qualität
Sommersemester 2010 Vorlesung - Spezielles Arzneimittelrecht. Teil VIII Mittwoch, 2. Juni 2010
 Ministerium für,,, und Sommersemester 2010 Vorlesung - Spezielles Arzneimittelrecht Teil VIII Mittwoch, 2. Juni 2010 Folie 1 Ministerium für,,, und 4 Beschaffenheit, Größe und Einrichtung der Apothekenbetriebsräume
Ministerium für,,, und Sommersemester 2010 Vorlesung - Spezielles Arzneimittelrecht Teil VIII Mittwoch, 2. Juni 2010 Folie 1 Ministerium für,,, und 4 Beschaffenheit, Größe und Einrichtung der Apothekenbetriebsräume
Coffein-Natriumbenzoat Coffeinum-natrii benzoas Synonym: Coffeinum-Natrium benzoicum
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 08.05.2012 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 08.05.2012 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
Coffeincitrat Coffeini citras Synonym: Coffeinum citricum
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmenf sind bis zum 15.September 2008 an folgende Adresse
KOMMENTAR ZUR LEITLINIE. Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung KOMMENTAR ZUR LEITLINIE Stand der Revision: 21.04.2009 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer Regeln.
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung KOMMENTAR ZUR LEITLINIE Stand der Revision: 21.04.2009 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer Regeln.
Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- Stand der Revision: 25.11.2008 Inhaltsübersicht
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- Stand der Revision: 25.11.2008 Inhaltsübersicht
Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel
 Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Stand der Revision: 25.11.2008 Inhaltsübersicht I II III
Leitlinie der Bundesapothekerkammer zur Herstellung und Prüfung der nicht zur parenteralen Anwendung bestimmten Rezeptur- und Defekturarzneimittel Stand der Revision: 25.11.2008 Inhaltsübersicht I II III
Plausibilitätsprüfung Wurde für das vorliegende Rezepturarzneimittel bereits die Plausibilitätsprüfung vorgenommen?
 I Hinweis zur Bearbeitung des Arbeitsbogens Erstellen Sie die Herstellungsanweisung für ein Rezepturarzneimittel. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer
I Hinweis zur Bearbeitung des Arbeitsbogens Erstellen Sie die Herstellungsanweisung für ein Rezepturarzneimittel. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Herstellung und Prüfung applikationsfertiger Parenteralia ohne toxisches Potenzial
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne toxisches Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I II III IV
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Prüfung applikationsfertiger Parenteralia ohne toxisches Potenzial Stand der Revision: 25.11.2008 Inhaltsübersicht I II III IV
ARBEITSBOGEN 1: HALTBARKEIT, LAGERUNG UND ENTSORGUNG DER FERTIGARZNEIMITTEL, MEDI- ZINPRODUKTE, APOTHEKENÜBLICHEN WAREN UND AUSGANGSSTOFFE
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
SALICYLAMID. Salicylamidum Salicylsäureamid. 2-Hydroxybenzamid Gehalt: 99,0 bis 101,0% Salicylamid (getrocknete Substanz)
 SALICYLAMID Salicylamidum Salicylsäureamid C7H7NO2 Mr = 137,1 CAS Nr. 65-45-2 Definition 2-Hydroxybenzamid Gehalt: 99,0 bis 101,0% Salicylamid (getrocknete Substanz) Eigenschaften: Aussehen: weißes bis
SALICYLAMID Salicylamidum Salicylsäureamid C7H7NO2 Mr = 137,1 CAS Nr. 65-45-2 Definition 2-Hydroxybenzamid Gehalt: 99,0 bis 101,0% Salicylamid (getrocknete Substanz) Eigenschaften: Aussehen: weißes bis
ARBEITSBOGEN 15: RISIKEN BEI ARZNEIMITTELN UND MEDIZINPRODUKTEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Bearbeiten Sie Meldungen der Arzneimittelkommission der Deutschen Apotheker (AMK), andere Risikomeldungen sowie Berichte über unerwünschte Arzneimittelwirkungen
I Hinweis zur Bearbeitung des Arbeitsbogens Bearbeiten Sie Meldungen der Arzneimittelkommission der Deutschen Apotheker (AMK), andere Risikomeldungen sowie Berichte über unerwünschte Arzneimittelwirkungen
Fischer /Schüler. Rezeptur - Qualität in 7 Schritten. Ulrike Fischer, Dresden Katrin Schüler, Dresden. Mit 55 Abbildungen und 101 Tabellen
 Fischer /Schüler Rezeptur - Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Ä Checklisten, Arbeitsblätter und Fallbeispiele unterwww.online-plusbase.de
Fischer /Schüler Rezeptur - Qualität in 7 Schritten Ulrike Fischer, Dresden Katrin Schüler, Dresden Mit 55 Abbildungen und 101 Tabellen Ä Checklisten, Arbeitsblätter und Fallbeispiele unterwww.online-plusbase.de
!!! NEUE ÖAB-MONOGRAPHIE!!!
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
Hygiene und Lagerung. 11. Juli Neue Apothekenbetriebsordnung Informationsveranstaltung von LAK und LAV
 Hygiene und Lagerung 11. Juli 2012 1 HYGIENEMAßNAHMEN 11. Juli 2012 2 Hygienemaßnahmen Neu aufgenommen in 4a ApoBetrO Der Apothekenleiter muss für das Personal und die Betriebsräume, die zur Arzneimittelherstellung
Hygiene und Lagerung 11. Juli 2012 1 HYGIENEMAßNAHMEN 11. Juli 2012 2 Hygienemaßnahmen Neu aufgenommen in 4a ApoBetrO Der Apothekenleiter muss für das Personal und die Betriebsräume, die zur Arzneimittelherstellung
ARBEITSBOGEN 15: RISIKEN BEI ARZNEIMITTELN UND MEDIZINPRODUKTEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Bearbeiten Sie Meldungen der Arzneimittelkommission der Deutschen Apotheker (AMK), andere Risikomeldungen sowie Berichte über unerwünschte Arzneimittelwirkungen
I Hinweis zur Bearbeitung des Arbeitsbogens Bearbeiten Sie Meldungen der Arzneimittelkommission der Deutschen Apotheker (AMK), andere Risikomeldungen sowie Berichte über unerwünschte Arzneimittelwirkungen
KOMMENTAR ZUR LEITLINIE. Prüfung und Lagerung der Primärpackmittel
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung KOMMENTAR ZUR LEITLINIE Stand der Revision: 09.05.2006 Dieser Kommentar ist bis zur Aktualisierung der Qualitätsstandards des Zentrallaboratoriums
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung KOMMENTAR ZUR LEITLINIE Stand der Revision: 09.05.2006 Dieser Kommentar ist bis zur Aktualisierung der Qualitätsstandards des Zentrallaboratoriums
Leitlinie Kommentar Arbeitshilfe. Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung und Lagerung der Ausgangsstoffe
 Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
ARBEITSBOGEN 5: HERSTELLUNG VON REZEPTURARZNEIMITTELN
 I Hinweis zur Bearbeitung des Arbeitsbogens Stellen Sie ein wirkstoffhaltiges Rezepturarzneimittel her. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
I Hinweis zur Bearbeitung des Arbeitsbogens Stellen Sie ein wirkstoffhaltiges Rezepturarzneimittel her. Verwenden Sie zur Bearbeitung des Arbeitsbogens die Leitlinie der Bundesapothekerkammer zur Qualitätssicherung
Fichtenfaulpech Picea abies pix putorius
 Fichtenfaulpech Picea abies pix putorius Definition Das durch Abkratzen von Stämmen von Picea abies gewonnene vom Baum selbst abgesonderte Produkt. Sammelvorschrift Picea abies kann sehr unterschiedliche
Fichtenfaulpech Picea abies pix putorius Definition Das durch Abkratzen von Stämmen von Picea abies gewonnene vom Baum selbst abgesonderte Produkt. Sammelvorschrift Picea abies kann sehr unterschiedliche
Solutio Natrii chlorati isotonica
 BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report Betreff: Monographie-Entwurf Blutisotonische Natriumchlorid-Lösung VORWORT Die Revision erfolgte in Anlehnung an ähnliche Ph.Eur. Monographien
BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report Betreff: Monographie-Entwurf Blutisotonische Natriumchlorid-Lösung VORWORT Die Revision erfolgte in Anlehnung an ähnliche Ph.Eur. Monographien
Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution Stand: 23.11.2011 Inhaltsübersicht I II III
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Herstellung und Abgabe der Betäubungsmittel zur Opiatsubstitution Stand: 23.11.2011 Inhaltsübersicht I II III
Rezepturarzneimittel und Defekturarzneimittel. (Dr. Andreas Kiefer)
 Rezepturarzneimittel und Defekturarzneimittel (Dr. Andreas Kiefer) 1 Arzneimittelherstellung im europäischen Kontext Aus der Resolution des Ministerrates des Europarates: Fertigarzneimittel genügen nicht
Rezepturarzneimittel und Defekturarzneimittel (Dr. Andreas Kiefer) 1 Arzneimittelherstellung im europäischen Kontext Aus der Resolution des Ministerrates des Europarates: Fertigarzneimittel genügen nicht
Dr. Michael Hörnig Deutsche Arzneimittel Codex Neues Rezeptur Formularium Eschborn
 21. Juni 2016, Berlin DAC Monographie Cannabisblüten Dr. Michael Hörnig Deutsche Arzneimittel Codex Neues Rezeptur Formularium Eschborn Pharmazeutische Qualität Was ist eine Monographie? Das amtliches
21. Juni 2016, Berlin DAC Monographie Cannabisblüten Dr. Michael Hörnig Deutsche Arzneimittel Codex Neues Rezeptur Formularium Eschborn Pharmazeutische Qualität Was ist eine Monographie? Das amtliches
!!! NEUE ÖAB-MONOGRAPHIE!!!
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende neue Monographie ist für die Aufnahme in das ÖAB (österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.05.2014 an folgende
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende neue Monographie ist für die Aufnahme in das ÖAB (österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.05.2014 an folgende
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement. Stand der Revision:
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 04.05.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 04.05.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische
Versand der Arzneimittel aus der Apotheke
 Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 25.11.2009 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich Regulatorische Anforderungen Zuständigkeiten
Ch.-B.: Packungsgröße: Darreichungsform: Verfallsdatum:
 I Hinweis zur Bearbeitung des Arbeitsbogens Für einige Arzneimittel gilt in der Apotheke eine Dokumentations- bzw. Anzeigepflicht. Bearbeiten Sie den Arbeitsbogen für dokumentations- bzw. anzeigepflichtige
I Hinweis zur Bearbeitung des Arbeitsbogens Für einige Arzneimittel gilt in der Apotheke eine Dokumentations- bzw. Anzeigepflicht. Bearbeiten Sie den Arbeitsbogen für dokumentations- bzw. anzeigepflichtige
!!! NEUE ÖAB-MONOGRAPHIE!!!
 !!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende neue Monographie ist für die Aufnahme in das ÖAB (österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2015 an folgende
!!! NEUE ÖAB-MONOGRAPHIE!!! Die folgende neue Monographie ist für die Aufnahme in das ÖAB (österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2015 an folgende
Wenn der Pharmazierat kommt
 Wenn der Pharmazierat kommt Überwachung der öffentlichen Apotheken in Hessen durch das Regierungspräsidium Darmstadt 1 Besichtigung erfolgt in der Regel alle 3 Jahre Besichtigungen werden nicht angemeldet
Wenn der Pharmazierat kommt Überwachung der öffentlichen Apotheken in Hessen durch das Regierungspräsidium Darmstadt 1 Besichtigung erfolgt in der Regel alle 3 Jahre Besichtigungen werden nicht angemeldet
Medizinproduktebuch. Blatt 1. Geräte-Stammdaten Funktionsprüfung Geräteeinweisung... 4
 Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Medizinproduktebuch Nach 7 MPBetreibV für Medizinprodukte 1 Für das Gerät Inhalt Blatt 1. Geräte-Stammdaten... 2 2. Funktionsprüfung... 3 3. Geräteeinweisung... 4 3.1 Einweisung der vom Betreiber beauftragten
Seite 1 von 5. Merkblatt. betreffend die
 Seite 1 von 5 Landesuntersuchungsamt Rheinland-Pfalz Institut für Lebensmittelchemie und Arzneimittelprüfung, Mainz Merkblatt betreffend die Kennzeichnung von Arzneimitteln, die in öffentlichen Apotheken
Seite 1 von 5 Landesuntersuchungsamt Rheinland-Pfalz Institut für Lebensmittelchemie und Arzneimittelprüfung, Mainz Merkblatt betreffend die Kennzeichnung von Arzneimitteln, die in öffentlichen Apotheken
Kalmustinktur Calami tinctura Tinctura Calami
 Kalmustinktur Calami tinctura Tinctura Calami ÖAB 2010/xxx Definition Kalmustinktur wird aus Kalmuswurzelstock (Calami Rhizoma, Radix Calami, ÖAB) hergestellt. Gehalt: mindestens 0,3 Prozent ätherisches
Kalmustinktur Calami tinctura Tinctura Calami ÖAB 2010/xxx Definition Kalmustinktur wird aus Kalmuswurzelstock (Calami Rhizoma, Radix Calami, ÖAB) hergestellt. Gehalt: mindestens 0,3 Prozent ätherisches
Tab. 3.1 Was muss im Einzelnen dokumentiert werden? A Ausgangsstoff/Bezeichnung. B Lieferdatum/Herstellungsdatum. C Lieferant/Hersteller
 51 3.1 Prüfung von Ausgangsstoffen und Defekturarzneimitteln Tab. 3.1 Was muss im Einzelnen dokumentiert werden? Was Wer Apothekenbetriebsordnung 6 Allgemeine Vorschriften über die Herstellung und Prüfung
51 3.1 Prüfung von Ausgangsstoffen und Defekturarzneimitteln Tab. 3.1 Was muss im Einzelnen dokumentiert werden? Was Wer Apothekenbetriebsordnung 6 Allgemeine Vorschriften über die Herstellung und Prüfung
Medizinische Gase. Arzneimittel und Medizinprodukte der Westfalen AG.
 Medizinische Gase. Arzneimittel und Medizinprodukte der Westfalen AG. Fertigarzneimittel der Westfalen AG. Sauerstoff für medizinische Zwecke (gasförmig) Hierzu nutzt die Westfalen AG die Standardzulassung
Medizinische Gase. Arzneimittel und Medizinprodukte der Westfalen AG. Fertigarzneimittel der Westfalen AG. Sauerstoff für medizinische Zwecke (gasförmig) Hierzu nutzt die Westfalen AG die Standardzulassung
Die neue Apothekenbetriebsordnung
 - Pharmazie 04. Juli 2012 Die neue Apothekenbetriebsordnung Parenteraliaherstellung Reiner Herkner Darmstadt, den 4. Juli 2012 Entscheidende Änderungen Rezepturen Plausibilitätsprüfung Herstellungsanweisung
- Pharmazie 04. Juli 2012 Die neue Apothekenbetriebsordnung Parenteraliaherstellung Reiner Herkner Darmstadt, den 4. Juli 2012 Entscheidende Änderungen Rezepturen Plausibilitätsprüfung Herstellungsanweisung
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Versand der Arzneimittel aus der Apotheke
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 28.04.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 28.04.2015 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
ETHANOL 70 Prozent Ethanolum 70 per centum. Aethanolum dilutum. Ethanol 70 Prozent ist eine Mischung von Ethanol 96 Prozent und Wasser.
 ÖAB 2008/004 ETHANOL 70 Prozent Ethanolum 70 per centum Aethanolum dilutum Definition Ethanol 70 Prozent ist eine Mischung von Ethanol 96 Prozent und Wasser. Gehalt: Ethanol 70 Prozent enthält mindestens
ÖAB 2008/004 ETHANOL 70 Prozent Ethanolum 70 per centum Aethanolum dilutum Definition Ethanol 70 Prozent ist eine Mischung von Ethanol 96 Prozent und Wasser. Gehalt: Ethanol 70 Prozent enthält mindestens
Dokumentationen nach MPBetreibV
 Dokumentationen nach MPBetreibV Das vorliegende Dokument soll eine beispielhafte Umsetzung von einigen ausgewählten Anforderungen aus der Medizinprodukte-Betreiberverordnung aufzeigen. Anmerkungen in grün
Dokumentationen nach MPBetreibV Das vorliegende Dokument soll eine beispielhafte Umsetzung von einigen ausgewählten Anforderungen aus der Medizinprodukte-Betreiberverordnung aufzeigen. Anmerkungen in grün
Dithranol. Arbeitsvorschrift
 um Anthralin, Batidrol, Cignolin 1,8-Dihydroxyanthracen-9(10H)-on Ph. Eur. C 14 H 10 3 M r 226,2 CAS r. 1143-38-0 Gelblich-bräunliches kristallines Pulver, oxidationsempfindlich Smp. 178 bis 182 C H H
um Anthralin, Batidrol, Cignolin 1,8-Dihydroxyanthracen-9(10H)-on Ph. Eur. C 14 H 10 3 M r 226,2 CAS r. 1143-38-0 Gelblich-bräunliches kristallines Pulver, oxidationsempfindlich Smp. 178 bis 182 C H H
Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr. Abnahme-, Regel-, Kurz-, Nachbesichtigung
 Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr Apothekenanschrift mit Telefon (Stempel): Abnahme-, Regel-, Kurz-, Nachbesichtigung Teilnehmer:......... Datum der letzten Besichtigung:...
Niederschrift über die Apothekenbesichtigung vom... von... bis... Uhr Apothekenanschrift mit Telefon (Stempel): Abnahme-, Regel-, Kurz-, Nachbesichtigung Teilnehmer:......... Datum der letzten Besichtigung:...
ÖAB-Monographie Sulfadiazin-Na Revision des Tests verwandte Substanzen
 BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report ÖAB-Exp.Gr. z.h. Mag. R. Macas Datum: 03.03.2014 Kontakt: Dr. Andreas Mayrhofer Telefon: +43 (0) 505 55-36910 Fax: -36909 E-Mail: andreas.mayrhofer@ages.at
BASG / AGES Institut OMCL Zimmermanngasse 3, A-1090 Wien ÖAB Report ÖAB-Exp.Gr. z.h. Mag. R. Macas Datum: 03.03.2014 Kontakt: Dr. Andreas Mayrhofer Telefon: +43 (0) 505 55-36910 Fax: -36909 E-Mail: andreas.mayrhofer@ages.at
Akkreditierte Ausbildungsapotheke der Landesapothekerkammer Hessen. Ausbildungsplan
 4.2 Ausbildungsplan Ausbildungsplan Pharmazeut/in im Praktikum Ausbilder/in Name: Vorname: Name: Vorname: : Ausbildungszeitraum: Einführungsgespräch (Monat 1) Betriebsablauf (Arbeitszeiten, Pausen, Urlaub,
4.2 Ausbildungsplan Ausbildungsplan Pharmazeut/in im Praktikum Ausbilder/in Name: Vorname: Name: Vorname: : Ausbildungszeitraum: Einführungsgespräch (Monat 1) Betriebsablauf (Arbeitszeiten, Pausen, Urlaub,
Unterweisungsmodul. Medizinprodukte
 Unterweisungsmodul Medizinprodukte Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Was ist in der Praxis wichtig? Was heißt aktives Medizinprodukt? Aufgaben Prüfpflichten Bestandsverzeichnis Medizinproduktebuch
Unterweisungsmodul Medizinprodukte Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Was ist in der Praxis wichtig? Was heißt aktives Medizinprodukt? Aufgaben Prüfpflichten Bestandsverzeichnis Medizinproduktebuch
Ablauf zur Meldung von Vorkommnissen, Rückrufen, FSCA und FSN bei DEKRA Certification GmbH
 Sehr geehrte Kunden, gemäß den Richtlinien MDD 93/42/EWG, MPG, MPSV und unseren AGB s (siehe Spezielle Bedingungen für die Durchführung einer Zertifizierung von Qualitätsmanagementsystem im Bereich Medizin
Sehr geehrte Kunden, gemäß den Richtlinien MDD 93/42/EWG, MPG, MPSV und unseren AGB s (siehe Spezielle Bedingungen für die Durchführung einer Zertifizierung von Qualitätsmanagementsystem im Bereich Medizin
Unterweisungsmodul. Hochfrequenzgeräte
 Unterweisungsmodul Hochfrequenzgeräte Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Hochfrequenzgeräte - Was ist in der Praxis wichtig? Hochfrequenzgeräte Was heißt aktives Medizinprodukt? Hochfrequenzgeräte
Unterweisungsmodul Hochfrequenzgeräte Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Hochfrequenzgeräte - Was ist in der Praxis wichtig? Hochfrequenzgeräte Was heißt aktives Medizinprodukt? Hochfrequenzgeräte
Bezirksregierung Düsseldorf. Eine arzneimittelrechtliche Erlaubnis (nach 13 AMG resp. 20b/c AMG) ist immer erforderlich bei
 Bezirksregierung Düsseldorf.. Anzeige gemäß 67 Abs. 1 u. 2 AMG für die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte und zur Ausübung der Heilkunde bei Menschen befugten Personen gemäß 13 Abs.
Bezirksregierung Düsseldorf.. Anzeige gemäß 67 Abs. 1 u. 2 AMG für die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte und zur Ausübung der Heilkunde bei Menschen befugten Personen gemäß 13 Abs.
Stellen der Arzneimittel
 Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung Stand: 14.11.2006 Kapitel VII-1.1im Flussdiagramm aktualisiert am 20.09.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich
Empfehlungen der Bundesapothekerkammer zur Qualitätssicherung Stand: 14.11.2006 Kapitel VII-1.1im Flussdiagramm aktualisiert am 20.09.2010 Inhaltsübersicht I II III IV V Zweckbestimmung und Geltungsbereich
Basis Cordes RK ist eine wirkstofffreie Basissalbe für die Rezepturkonzentrate
 Prüfanweisung Nr. A00957-5 Seite 1 von 5 Basis Cordes RK ist eine wirkstofffreie Basissalbe für die Rezepturkonzentrate 1 Aussehen Fast weiß bis weiß 2 Geruch Praktisch geruchlos 3 Konsistenz Salbenartig
Prüfanweisung Nr. A00957-5 Seite 1 von 5 Basis Cordes RK ist eine wirkstofffreie Basissalbe für die Rezepturkonzentrate 1 Aussehen Fast weiß bis weiß 2 Geruch Praktisch geruchlos 3 Konsistenz Salbenartig
Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke
 Landesamt für soziale Dienste Schleswig-Holstein - Abt. Gesundheitsschutz - Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke (ohne Versandhandel, Stellen/Verblistern, Krankenhaus-und Heimbelieferung,
Landesamt für soziale Dienste Schleswig-Holstein - Abt. Gesundheitsschutz - Checkliste zur Überprüfung des QMS in der öffentlichen Apotheke (ohne Versandhandel, Stellen/Verblistern, Krankenhaus-und Heimbelieferung,
Allgemeine und spezielle Fragen zur neuen PharmBetrV
 Allgemeine und spezielle Fragen zur neuen PharmBetrV Martin Sieling, BR-Detmold Begründung für die neue PharmBetrV Anpassung an die 14. AMG Novelle Festlegungen an die GMP-gemäße Wirkstoff- (und Hilfsstoff-)herstellung
Allgemeine und spezielle Fragen zur neuen PharmBetrV Martin Sieling, BR-Detmold Begründung für die neue PharmBetrV Anpassung an die 14. AMG Novelle Festlegungen an die GMP-gemäße Wirkstoff- (und Hilfsstoff-)herstellung
Apothekenbetriebsordnung Kommentar
 Apothekenbetriebsordnung Kommentar Bearbeitet von Begründet von Walter Cyran, herausgegeben von Christian Rotta, bearbeitet von Sabine Wesser, Dr. Heinz-Uwe Dettling, Timo Kieser, Valentin Saalfrank, und
Apothekenbetriebsordnung Kommentar Bearbeitet von Begründet von Walter Cyran, herausgegeben von Christian Rotta, bearbeitet von Sabine Wesser, Dr. Heinz-Uwe Dettling, Timo Kieser, Valentin Saalfrank, und
Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Einnahmezeitpunkte
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand: 26.11.2014 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Patientenindividuelle manuelle Neuverpackung von Fertigarzneimitteln für bestimmte Stand: 26.11.2014 Inhaltsverzeichnis
Eingestellter Ginkgotrockenextrakt
 Eingestellter Ginkgotrockenextrakt Ginkgo extractum siccum normatum Definition Eingestellter Ginkgotrockenextrakt wird hergestellt aus den getrockneten Blättern von Ginkgo biloba L. Er enthält mindestens
Eingestellter Ginkgotrockenextrakt Ginkgo extractum siccum normatum Definition Eingestellter Ginkgotrockenextrakt wird hergestellt aus den getrockneten Blättern von Ginkgo biloba L. Er enthält mindestens
Informationswege und Maßnahmen bei Qualitätsmängeln von Arzneimitteln
 Ministerium für Arbeit, Gesundheit und Soziales 1 Allgemeines Informationswege und Maßnahmen bei Qualitätsmängeln von Arzneimitteln Bek. d. Ministeriums für Arbeit, Gesundheit und Soziales v. 12. Februar
Ministerium für Arbeit, Gesundheit und Soziales 1 Allgemeines Informationswege und Maßnahmen bei Qualitätsmängeln von Arzneimitteln Bek. d. Ministeriums für Arbeit, Gesundheit und Soziales v. 12. Februar
Apothekenbetriebsordnung. RAin Daniela Pach Justitiarin der Landesapothekerkammer Hessen
 Apothekenbetriebsordnung RAin Daniela Pach Justitiarin der Landesapothekerkammer Hessen 1 Apothekenbetriebsordnung - Übersicht Erster Abschnitt: Allgemeine Bestimmung Zweiter Abschnitt: Der Betrieb von
Apothekenbetriebsordnung RAin Daniela Pach Justitiarin der Landesapothekerkammer Hessen 1 Apothekenbetriebsordnung - Übersicht Erster Abschnitt: Allgemeine Bestimmung Zweiter Abschnitt: Der Betrieb von
Anhang. E. Deutsch, Hans-Dieter Lippert, Kommentar zum Arzneimittelgesetz (AMG), DOI / , Springer-Verlag Berlin Heidelberg 2011
 E. Deutsch, Hans-Dieter Lippert, Kommentar zum Arzneimittelgesetz (AMG), DOI 10.1007/978-3-642-01455-0, Springer-Verlag Berlin Heidelberg 2011 Anhang 1. Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung
E. Deutsch, Hans-Dieter Lippert, Kommentar zum Arzneimittelgesetz (AMG), DOI 10.1007/978-3-642-01455-0, Springer-Verlag Berlin Heidelberg 2011 Anhang 1. Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung
DAC-Probe 10. Hochleistungsdünnschichtchromatographie (HPTLC) Einleitung. Allgemeine Angaben
 DAC-Probe 0 Probe_0 DAC-Probe 0 Hochleistungsdünnschichtchromatographie (HPTLC) Sofern in der Monographie nichts anderes angegeben ist, wird die Auftrennung mit den folgenden Angaben durchgeführt: es werden
DAC-Probe 0 Probe_0 DAC-Probe 0 Hochleistungsdünnschichtchromatographie (HPTLC) Sofern in der Monographie nichts anderes angegeben ist, wird die Auftrennung mit den folgenden Angaben durchgeführt: es werden
Klausur Arzneistoffanalytik unter besonderer Berücksichtigung der Arzneibücher (Qualitätskontrolle und -sicherung bei Arzneistoffen) 6.
 Klausur Arzneistoffanalytik unter besonderer Berücksichtigung der Arzneibücher (Qualitätskontrolle und -sicherung bei Arzneistoffen) 6. Fachsemester SS 2013 Datum: 22.07. 2013 NAME (in Druckbuchstaben):
Klausur Arzneistoffanalytik unter besonderer Berücksichtigung der Arzneibücher (Qualitätskontrolle und -sicherung bei Arzneistoffen) 6. Fachsemester SS 2013 Datum: 22.07. 2013 NAME (in Druckbuchstaben):
Unterweisungsmodul. Laser
 Unterweisungsmodul Laser Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Laserschutzbeauftragte/r Betriebsanweisung Prüfpflichten Persönliche Schutzausrüstung Bestandsverzeichnis Medizinproduktebuch
Unterweisungsmodul Laser Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Laserschutzbeauftragte/r Betriebsanweisung Prüfpflichten Persönliche Schutzausrüstung Bestandsverzeichnis Medizinproduktebuch
Eckpunkte 1 für die Dokumentation der Apothekenbesichtigung im Sinn der Grundsätze für die Apothekenüberwachung
 Arbeitsgruppe Arzneimittel-, Apotheken-, Transfusions- und Betäubungsmittelwesen (AATB) Stand 14. Februar 2013 Eckpunkte 1 für die Dokumentation der Apothekenbesichtigung im Sinn der Grundsätze für die
Arbeitsgruppe Arzneimittel-, Apotheken-, Transfusions- und Betäubungsmittelwesen (AATB) Stand 14. Februar 2013 Eckpunkte 1 für die Dokumentation der Apothekenbesichtigung im Sinn der Grundsätze für die
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO)
 Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO) ApBetrO Ausfertigungsdatum: 09.02.1987 Vollzitat: "Apothekenbetriebsordnung in der Fassung der Bekanntmachung vom 26. September
Verordnung über den Betrieb von Apotheken (Apothekenbetriebsordnung - ApBetrO) ApBetrO Ausfertigungsdatum: 09.02.1987 Vollzitat: "Apothekenbetriebsordnung in der Fassung der Bekanntmachung vom 26. September
Bezirksregierung Münster Dezernat 24 Domplatz Münster Fax: +49 (251)
 Bezirksregierungen Münster Anzeige gemäß 67 Abs. 1 u. 2 AMG für die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte und zur Ausübung der Heilkunde bei Menschen befugten Personen gemäß 13 Abs.
Bezirksregierungen Münster Anzeige gemäß 67 Abs. 1 u. 2 AMG für die erlaubnisfreie Herstellung von Arzneimitteln durch Ärzte und zur Ausübung der Heilkunde bei Menschen befugten Personen gemäß 13 Abs.
Unterweisungsmodul. Laser
 Unterweisungsmodul Laser Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Laserschutzbeauftragte/r Anzeigeverfahren Betriebsanweisung Prüfpflichten Persönliche Schutzausrüstung Bestandsverzeichnis
Unterweisungsmodul Laser Unterweisungsinhalte - Beispiele Rechtliche Grundlagen Laserschutzbeauftragte/r Anzeigeverfahren Betriebsanweisung Prüfpflichten Persönliche Schutzausrüstung Bestandsverzeichnis
ARBEITSBOGEN 11: ARZNEIMITTELBERATUNG ÄRZTLICHE VERORDNUNGEN
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über ein Fertigarzneimittel (FAM) bei der Abgabe im Rahmen einer ärztlichen Verordnung. Grundlage des Arbeitsbogens
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren und beraten Sie einen Patienten über ein Fertigarzneimittel (FAM) bei der Abgabe im Rahmen einer ärztlichen Verordnung. Grundlage des Arbeitsbogens
Klausur Arzneistoffanalytik unter besonderer Berücksichtigung der Arzneibücher (Qualitätskontrolle und -sicherung bei Arzneistoffen)
 Klausur Arzneistoffanalytik unter besonderer Berücksichtigung der Arzneibücher (Qualitätskontrolle und -sicherung bei Arzneistoffen) WS2014/15 6. Fachsemester 1. Wiederholungsklausur: 10.04.2015 Name (in
Klausur Arzneistoffanalytik unter besonderer Berücksichtigung der Arzneibücher (Qualitätskontrolle und -sicherung bei Arzneistoffen) WS2014/15 6. Fachsemester 1. Wiederholungsklausur: 10.04.2015 Name (in
Selbstinspektionsprotokoll gemäß 2a ApBetrO
 Mielke / Paul Selbstinspektionsprotokoll gemäß 2a ApBetrO Mitra Mielke, Köln Monika Paul, Köln Für die Durchführung der Selbstinspektion im Zeitraum (Monat/Jahr) bis (Monat/Jahr) Allgemeine Angaben zur
Mielke / Paul Selbstinspektionsprotokoll gemäß 2a ApBetrO Mitra Mielke, Köln Monika Paul, Köln Für die Durchführung der Selbstinspektion im Zeitraum (Monat/Jahr) bis (Monat/Jahr) Allgemeine Angaben zur
Leitlinie Kommentar Arbeitshilfe. Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Hygienemanagement
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 08.05.2018 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 08.05.2018 Inhaltsverzeichnis I Zweckbestimmung und Geltungsbereich... 3 II Regulatorische
Text Anlage. Heparin-Calcium
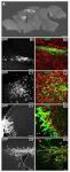 Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Kurztitel 27. Nachtrag zum Arzneibuch Kundmachungsorgan BGBl. II Nr. 307/2008 /Artikel/Anlage Anl. 1 Inkrafttretensdatum 03.09.2008 Text Anlage Heparin-Calcium Definition Heparinum calcicum Heparin-Calcium
Einführung 9. 1 Die amtliche Besichtigung der Apotheke l.i
 3 Inhaltsverzeichnis Einführung 9 1 Die amtliche Besichtigung der Apotheke l.i 1.1 Die verschiedenen Besichtigungsarten 1.1 1.1.1 Die Abnahmebesichtigung 1.2 1.1.2 Die routinemäßige Überwachung (Regelbesichtigung)
3 Inhaltsverzeichnis Einführung 9 1 Die amtliche Besichtigung der Apotheke l.i 1.1 Die verschiedenen Besichtigungsarten 1.1 1.1.1 Die Abnahmebesichtigung 1.2 1.1.2 Die routinemäßige Überwachung (Regelbesichtigung)
Unverzichtbar für ein effizientes Beobachtungs- und Meldesystem sind:
 Medizintechnologie.de Vigilanzsystem Probleme mit Medizinprodukten treten häufig erst auf, nachdem die Produkte bereits langfristig im Einsatz sind oder von einer größeren Population von Anwendern oder
Medizintechnologie.de Vigilanzsystem Probleme mit Medizinprodukten treten häufig erst auf, nachdem die Produkte bereits langfristig im Einsatz sind oder von einer größeren Population von Anwendern oder
Dokumentationshilfe Einzelhändler - Arzneimittelrecht
 Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Dokumentationshilfe Einzelhändler - Arzneimittelrecht Besichtigung des Bestandes an Arzneimitteln Fertigarzneimittel Der Einzelhändler bringt nur freiverkäufliche Arzneimittel in den Verkehr ( 43 Abs.
Als Grundlage für die Revision wird die Monographie gemäß HELV. mit folgendem Änderungsvorschlag herangezogen:
 !!! NEE ÖAB-MONOGAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
!!! NEE ÖAB-MONOGAPHIE!!! Die folgende revidierte Monographie ist für die Aufnahme in das ÖAB (Österreichisches Arzneibuch) vorgesehen. Stellungnahmen zu diesem Gesetzesentwurf sind bis zum 31.01.2008
Verordnung über Medizinprodukte - MPV (Medizinprodukte-Verordnung)
 Verordnung über Medizinprodukte - MPV (Medizinprodukte-Verordnung) Vom 20. Dezember 2001,Bundesgesetzblatt I Nr. 72, S. 3854 22. Dezember 2001, geändert durch Bundesgesetzblatt I S. 4456 vom 4. Dezember
Verordnung über Medizinprodukte - MPV (Medizinprodukte-Verordnung) Vom 20. Dezember 2001,Bundesgesetzblatt I Nr. 72, S. 3854 22. Dezember 2001, geändert durch Bundesgesetzblatt I S. 4456 vom 4. Dezember
NIR-Spektroskopie & Chemmetrie
 NIR-Spektroskopie & Chemmetrie www.hiperscan.com, 28-Feb-16, Folie 1 NIR-Spektroskopie Eignung der Methode NIR-Spektroskopie Methode für verschiedene pharmazeutische Analysen, insbesondere auch für die
NIR-Spektroskopie & Chemmetrie www.hiperscan.com, 28-Feb-16, Folie 1 NIR-Spektroskopie Eignung der Methode NIR-Spektroskopie Methode für verschiedene pharmazeutische Analysen, insbesondere auch für die
H1 Allgemeine Vorschriften
 1 H1 Allgemeine Vorschriften H1 Allgemeine Vorschriften H1.1 Allgemeines Für den Homöopathischen Teil des Arzneibuchs, Homöopathisches Arzneibuch, gelten die Allgemeinen Vorschriften, Allgemeinen Methoden,
1 H1 Allgemeine Vorschriften H1 Allgemeine Vorschriften H1.1 Allgemeines Für den Homöopathischen Teil des Arzneibuchs, Homöopathisches Arzneibuch, gelten die Allgemeinen Vorschriften, Allgemeinen Methoden,
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch
 Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch
 Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Deutscher Arzneimittel-Codex / Neues Rezeptur- Formularium (DAC/NRF) - DVD-ROM-Version: Ergänzung zum amtlichen Arzneibuch Click here if your download doesn"t start automatically Deutscher Arzneimittel-Codex
Für Sie untersucht: Stabilitätsuntersuchungen
 Für Sie untersucht: Stabilitätsuntersuchungen Die Wirk- und Hilfsstoffstabilität in Rezepturen wird durch verschiedenste Faktoren wie dem ph- Wert, der Temperatur, dem Licht, der stofflichen Zusammensetzung
Für Sie untersucht: Stabilitätsuntersuchungen Die Wirk- und Hilfsstoffstabilität in Rezepturen wird durch verschiedenste Faktoren wie dem ph- Wert, der Temperatur, dem Licht, der stofflichen Zusammensetzung
18. Symposium Herstellung in der Krankenhausapotheke 18. Januar 2019, Berlin Defekturprüfung: Plausibilität abschätzen Prüfungen reduzieren
 18. Symposium Herstellung in der Krankenhausapotheke 18. Januar 2019, Berlin Defekturprüfung: Plausibilität abschätzen Prüfungen reduzieren Dr. Michael Hörnig DAC/NRF, Eschborn Herstellung von Defekturarzneimitteln
18. Symposium Herstellung in der Krankenhausapotheke 18. Januar 2019, Berlin Defekturprüfung: Plausibilität abschätzen Prüfungen reduzieren Dr. Michael Hörnig DAC/NRF, Eschborn Herstellung von Defekturarzneimitteln
LEITFADEN FÜR DIE PRAKTISCHE AUSBILDUNG VON PHARMAZEUTEN IM PRAKTIKUM IN DER APOTHEKE
 In Zusammenarbeit mit VERABSCHIEDET VON DER MITGLIEDERVERSAMMLUNG DER BUNDESAPOTHEKERKAMMER AM XX.XX.XXXX LEITFADEN FÜR DIE PRAKTISCHE AUSBILDUNG VON PHARMAZEUTEN IM PRAKTIKUM IN DER APOTHEKE Empfehlungen
In Zusammenarbeit mit VERABSCHIEDET VON DER MITGLIEDERVERSAMMLUNG DER BUNDESAPOTHEKERKAMMER AM XX.XX.XXXX LEITFADEN FÜR DIE PRAKTISCHE AUSBILDUNG VON PHARMAZEUTEN IM PRAKTIKUM IN DER APOTHEKE Empfehlungen
Leitlinie Kommentar Arbeitshilfe. Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung. Prüfung und Lagerung der Primärpackmittel
 Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
Leitlinie Kommentar Arbeitshilfe Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Stand der Revision: 16.06.2016 Die Erläuterungen sind eine Zusammenfassung der Anforderungen pharmazeutischer
ARBEITSBOGEN 1: HALTBARKEIT, LAGERUNG UND ENTSORGUNG DER FERTIGARZNEIMITTEL, MEDI- ZINPRODUKTE, APOTHEKENÜBLICHEN WAREN UND AUSGANGSSTOFFE
 I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
I Hinweis zur Bearbeitung des Arbeitsbogens Informieren Sie sich über die Haltbarkeit, Lagerung und Entsorgung der Fertigarzneimittel (FAM), Medizinprodukte (MP), apothekenüblichen Ware und Ausgangsstoffe
Arzneimittelinformation in der Apotheke und in Informationsstellen der Apothekerschaft
 Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Arzneimittelinformation in der Apotheke und in Informationsstellen der Apothekerschaft Stand: 08.05.2018 Inhaltsverzeichnis
Leitlinie Kommentar Arbeitshilfe Leitlinie der Bundesapothekerkammer zur Qualitätssicherung Arzneimittelinformation in der Apotheke und in Informationsstellen der Apothekerschaft Stand: 08.05.2018 Inhaltsverzeichnis
