Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
|
|
|
- Sven Schenck
- vor 6 Jahren
- Abrufe
Transkript
1 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: Gruppe 5: alogenalkane Versuch: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung Zeitbedarf Vorbereitung: 5 Minuten Durchführung: 5 Minuten Nachbereitung: 5 Minuten Reaktionsgleichung 3 C AgNO 3 C 3 O (1) 3 C AgNO 3 3 C O O 3 C Ag NO 3 (2) O 3 C AgNO 3 3 C O 3 C C3 Ag NO 3 (3) Chemikalien Tab. 1: Verwendete Chemikalien. Eingesetzte Stoffe Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Ethanol F S I 1-ombutan V = 0,5 ml 11-36/37/38-51/ F, Xi, N S I
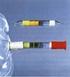
2 2-ombutan V = 0,5 ml 10-52/53 24 S I 2-om-2- V = 0,5 ml /25 F S I Methylpropan Silbernitrat 2 % in Ethanol 11-36/ Xi, F, N S I Geräte 3 Reagenzgläser Reagenzglasständer Spatel Becherglas Waage 5 ml-messpipette Aufbau Abb. 1: Niederschläge bei der Reaktion der Alkylbromide mit ethanolischer Silbernitrat-Lösung. Durchführung In drei Reagenzgläser werden je 2 ml einer 2%igen AgNO 3 -Lösung in Ethanol gegeben. Anschließend werden je 0,5 ml des entsprechenden Butylbromids in Ethanol (Butylbromid: Ethanol = 1 : 4) hinzugegeben. Im Folgenden wird beobachtet, welche Lösung am schnellsten und welche am langsamsten zu einer Trübung führt. 2
3 Beobachtung Nachdem die mit ethanolischer Silbernitratlösung versetzten Reagenzgläser nacheinander mit 1-ombutan, 2-ombutan und 2-om-2-Methylpropan gefüllt werden, bildet sich im dritten Reagenzglas, das mit 2-om-2-Methylpropan versetzt wurde, sofort ein deutlich sichtbarer weißer Niederschlag. Bei der Mischung von ethanolischer Silbernitratlösung mit 2-ombutan ist nach kurzer Zeit auch ein deutlicher weißer Niederschlag zu erkennen. Die Verbindung mit 1-ombutan zeigt zwar eine milchige Trübung, jedoch ist kein ausgefallener Feststoff zu erkennen. Entsorgung Die Lösungen werden in einem Becherglas gesammelt und mit Salzsäure versetzt in die sauren Silberabfälle entsorgt. Fachliche Auswertung der Versuchsergebnisse Bei der Reaktion von ethanolischer Silbernitratlösung mit dem jeweiligen Alkylbromid kommt es zur Bildung eines ausfallenden Feststoffes. Dieser bildet sich dadurch, dass ein Austausch von Molekülteilen stattfindet. Diese Reaktion läuft nach dem Mechanismus der nucleophilen Substitution. Grundsätzlich werden zwei besondere Typen der nucleophilen Substitution unterschieden: die bimolekulare nucleophile Substitution (S N 2) und die unimolekulare nucleophile Substitution (S N 1). Die in diesem Versuch eingesetzten alogenalkane reagieren bevorzugt mit einem ungepaarten Elektron, wie es zum Beispiel im ydroxidion oder im Ammoniak enthalten ist. Diese Reaktion ist vorteilhaft, da alogenalkane eine polare Bindung haben. Das alogenid besitzt eine größere Elektronegativität als das Kohlenstoffatom, sodass die Elektronendichte am alogenid größer ist. Durch diese Polarisierung trägt das Kohlenstoffatom, das an das alogenid gebunden ist, eine partielle positive Ladung (es ist elektrophil) und kann daher gut von elektronenreichen Verbindungen (Nucleophilen) angegriffen werden. Das alogenid wird durch das Nucleophil verdrängt und ist somit die Abgangsgruppe. Die bimolekulare Substitution (S N 2) verläuft nach einem Geschwindigkeitsgesetz zweiter Ordnung. Das bedeutet, dass die Anfangskonzentrationen beider Reaktanten zur Geschwin- 3
4 digkeit der Reaktion beitragen. Bei einer Verdopplung der Konzentration des Nucleophils verdoppelt sich auch die Reaktionsgeschwindigkeit (ebenso wie bei einer Verdoppelung des alogenalkans). Werden beide Reaktanden verdoppelt, so vervierfacht sich die Reaktionsgeschwindigkeit. Sie ist durch folgende Gleichung definiert: Da immer der langsamste Schritt geschwindigkeitsbestimmend ist und hier beide Reaktanten mit ihren Konzentrationen dazu beitragen, läuft die Reaktion konzertiert ab. Dies bedeutet, dass die neue Bindung zum Nucleophil zur gleichen Zeit ausgebildet wird, wie die Bindung zum alogenid gebrochen wird. Die allgemeine Reaktion ist in den Abbildungen 2 und 3 dargestellt. Nu - Nu - Nu - Abb. 2: Vorderseitenangriff der bimolekularen nucleophilen Substitution. Nu - Nu - 3 C Nu - Abb. 3: Rückseitenangriff der bimolekularen nucleophilen Substitution. Die Nucleophilie wird durch eine negative Ladung und von rechts nach links im Periodensystem erhöht. Die Solvatation erschwert die Nucleophilie jedoch, da sich die Solvathülle um ein Nucleophil anlagert und somit den Angriff auf das Elektrophil beeinträchtigt. Die Reaktivität der alogenalkane nimmt in der Reihe primäres alogenalkan, sekundäres alogenalkan, tertiäres alogenalkan ab. Das tertiäre reagiert gar nicht mehr nach diesem Mechanismus. Sekundäre und tertiäre alogenalkane reagieren nach dem S N 2-Mechanismus sehr langsam oder gar nicht. Sie besitzen aber im Gegensatz zum primären alogenalkan die Fähigkeit mit 4
5 dem Lösungsmittel zu reagieren. Eine solche Reaktion nennt man Solvolyse. Ist Wasser das Lösungsmittel, wird es als ydrolyse bezeichnet. Bei der Reaktion der Solvolyse ist das Lösungsmittel das Nucleophil, das an das alogenalkan angreift. In diesem Versuch diente Ethanol als Lösungsmittel. Die Solvolyse wird dann genauer als Ethanolyse bezeichnet. 3 C C 3 O O 3 C 3 C Abb. 4: Ethanolyse des sekundären Alkylbromids. 3 C C 3 O 3 C O 3 C Abb. 5: Ethanolyse des tertiären Alkylbromids. Die Ethanolyse (Solvolyse) verläuft nach dem Mechanismus der unimolekularen Substitution (S N 1). Die Kinetik verläuft dabei nach erster Ordnung und ist somit nur von der Konzentration des eingesetzten alogenalkans abhängig. Das Geschwindigkeitsgesetz erster Ordnung ist somit definiert als: Dies bedeutet, dass das alogenalkan alleine für den geschwindigkeitsbestimmenden Schritt verantwortlich ist. Erst dann findet die eigentliche Substitution statt. Daraus ergibt sich ein Mechanismus, der über die Bildung eines Carbeniumions geht. 3 C C C 3 - Abb. 6: Dissoziation zum Carbenium-Ion in der unimolekularen nucleophilen Substitution. Diese Dissoziation zum Carbenium-Ion ist geschwindigkeitsbestimmend, da dies der langsamste Reaktionsschritt ist. Daraufhin folgt der nucleophile Angriff des Lösungsmittels (Ethanol). Dieser Schritt verläuft sehr schnell, da das Carbenium-Ion sehr reaktiv ist. 5
6 3 C C 3 C O C 3 C3 O Abb. 7: Nucleophiler Angriff des Ethanols. Nach dem Nucleophilen Angriff von Ethanol folgt die Deprotonierung am Oxonium-Ion, um wieder ein neutrales Molekül zu erhalten. C 3 C3 O 2 O C 3 C3 O 3 O Abb. 8: Deprotonierung des Alkyloxonium-Ions. Zusammenfassend läuft der Mechanismus wie in Abbildung 9 und 10 dargestellt ab. Das abgespaltene omid-ion geht mit dem Silber-Ion aus dem Silbernitrat eine Bindung ein. Diese Reaktion dient dabei als Indikator, da es zu einem Niederschlag kommt, wenn ein Carbenium- Ion gebildet werden kann. Die Geschwindigkeit der Niederschlagsbildung ist folglich proportional zur Reaktivität der eingesetzten Alkylbromide. Die Trübung trat beim tertiären Alkylbromid sofort nach Zugabe der Silbernitratlösung auf, beim sekundären Alkylbromid kurze Zeit später und beim primären fast gar nicht. 3 C AgNO 3 Ag NO 3 - O C 3 C C 3 C C C O Abb. 9: Mechanismus der S N 1-Reaktion beim sekundären Alkylbromid. 6
7 3 C AgNO 3 3 C C Ag - NO 3 3 C C O 3 C O - Abb. 10: Mechanismus der S N 1-Reaktion beim tertiären Alkylbromid. Durch das polare Lösungsmittel werden die S N 1-Reaktionen bei den sekundären und tertiären Alkylbromiden beschleunigt. Das primäre Alkylbromid kann wegen der zu geringen Stabilisierung nicht über den Mechanismus der S N 1-Reaktion zum entsprechenden Ether reagieren. Daher ist auch im Versuch kaum ein Niederschlag von Ag zu sehen. Das Carbenium-Ion kann in diesem Fall nicht stabilisiert werden. Für eine S N 1-Reaktion sind gute Abgangsgruppen sehr vorteilhaft. Durch eine gute Abgangsgruppe kann schneller das Carbenium-Ion gebildet werden, das dann weiterreagiert. Weiterhin beschleunigen auch polare Lösungsmittel diesen Mechanismus. Die Stärke des Nucleophils spielt für die Reaktionsgeschwindigkeit der S N 1-Reaktion keine Rolle. Methodisch-Didaktische Analyse 1 Einordnung Das Thema alogenalkane wird im hessischen Lehrplan im zweiten albjahr der Jahrgangstufe 10 zum auptthema Einführung in die Kohlenstoffchemie angesiedelt. Allerdings ist das Grundlagenwissen der Schüler zu diesem Zeitpunkt auf die Bindungsverhältnisse beschränkt. Der Unterricht soll sich in diesem Zeitraum auch vorwiegend mit der Nomenklatur und den Eigenschaften sowie den Dipolmolekülen befassen. Der Reaktionstyp der Substitution wird jedoch erst im ersten albjahr der Jahrgangsstufe 11 eingeführt, wenn die Schüler sich mit dem Themengebiet der Alkanole beschäftigen sollen. Ein Leistungskurs könnte sich dann zusätzlich mit diesem Mechanismus bei der Etherdarstellung auseinandersetzen. 2 Aufwand Der Aufwand für diesen Versuch ist sehr gering, da kein besonderer Aufbau benötigt wird. Die Materialien sind in der Regel an jeder Schule vorhanden, sodass dies keiner weiteren Or- 7
8 ganisation bedarf. Da der Versuch sehr schnell durchzuführen ist, entstehen keine langen Wartezeiten, die durch den Lehrer überbrückt werden müssten. 3 Durchführung Da der Versuch schnell durchzuführen ist und auch mit einer ziemlich großen Wahrscheinlichkeit funktioniert, eignet er sich sehr gut als Schulversuch. Die verwendeten Chemikalien sind für den Einsatz in der Sekundarstufe I erlaubt. Somit kann der Versuch auch sehr gut als Schülerversuch durchgeführt werden. Ein großer Vorteil dieses Versuchs ist das schnelle Ergebnis, das Schüler nicht lange warten lässt. Literatur [1] ilt, Gerhard und Peter Rinze: Chemisches Praktikum für Mediziner, 6. Auflage, 6. Kurstag, 38. Aufgabe: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung, Wiesbaden, [2] Vollhardt, K. P. C. und Neil E Schore: Organische Chemie. Übersetzungs-rsg: olger Butenschön. Vierte Auflage. WILEY-VC. Weinheim S [3] Soester Liste. Version 2.7. [4] essischer Lehrplan: Chemie
Versuch: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung. keine Reaktion.
 Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Gruppe 05: Alkylchloride gegenüber AgNO 3
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Versuchsprotokoll. Reaktivität von Alkylbromiden. Gruppe 5, Typ: Pflichtversuch. AgBr + HNO 3 + H 3 C C C C. AgBr + HNO 3 +
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktivität von Alkylbromiden Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktivität von Alkylbromiden Gruppe
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Gruppe 3: Alkene, Alkine Versuch: omierung von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Gruppe 3: Alkene, Alkine Versuch: omierung von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 2: Alkane Versuch: alogenierung von Alkanen
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 2: Alkane Versuch: alogenierung von Alkanen
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether)
 Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Endersch, Jonas 17./19.06.2008 Praktikum Allgemeine Chemie 2, Saal G1, Platz 53 Versuchsprotokoll Versuch 2.1: Herstellung von Propoxybenzol (Phenylpropylether) Reaktionsgleichung: Einleitung und Theorie
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 3: Alkene, Alkine Versuch: erstellung und
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 3: Alkene, Alkine Versuch: erstellung und
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Zeitbedarf Gruppe 6: Alkohole Versuch: Mischungsexperimente
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Zeitbedarf Gruppe 6: Alkohole Versuch: Mischungsexperimente
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Versuch: Bromierung von n-hexan. Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Bemerkung
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Gruppe 5 eigener Versuch. Hydrolyse von 2-Chlor-2-methylpropan
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 27.05.09 SS 09 Gruppe 5 eigener Versuch ydrolyse von 2-Chlor-2-methylpropan
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 27.05.09 SS 09 Gruppe 5 eigener Versuch ydrolyse von 2-Chlor-2-methylpropan
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Versuch: Molischprobe mit Gelatine H 2 SO 4. O - 2 H e H 2. Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Schulversuch (Gruppe 6/Assistentenversuch): Vergleich aliphatischer Alkohole und Phenole
 Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
Philipps-Universität Marburg 26.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 6/Assistentenversuch):
+ 30,5 O 2 (g) 20 CO 2 (g) + 21 H 2 O
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Nachweis
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Nachweis
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: Die klassische Atemalkoholprobe
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: Die klassische Atemalkoholprobe
Gruppe 5 Pflichtversuch. Reaktivität von Halogenalkanen
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 27.05.09 SS 09 Gruppe 5 Pflichtversuch Reaktivität von Halogenalkanen
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 27.05.09 SS 09 Gruppe 5 Pflichtversuch Reaktivität von Halogenalkanen
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 17.12.2010 Gruppe 9: Kohlenhydrate Versuch (Nachweis):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 17.12.2010 Gruppe 9: Kohlenhydrate Versuch (Nachweis):
Versuch: Elektrophile Addition von Brom an Ethen
 Philipps-Universität Marburg 03.12.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 3, Alkene / Alkine Versuch: Elektrophile Addition von
Philipps-Universität Marburg 03.12.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 3, Alkene / Alkine Versuch: Elektrophile Addition von
+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose
![+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose + 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose](/thumbs/54/33374656.jpg) Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 17.12.2010 Gruppe 8: Ester, Fette, Seifen und
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 17.12.2010 Gruppe 8: Ester, Fette, Seifen und
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 4, 09./10.05.11 Nucleophile Substitution 1. Beschreiben Sie den Reaktionsmechanismus von a) S N 1 X = beliebige Abgangsgruppe
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuch: Hydrolyse von Stärke mit Speichel
 Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Versuch: Isolierung von Citronensäure aus Zitronen
 Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 11, Naturstoffe und Lebensmittel Versuch: Isolierung
Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 11, Naturstoffe und Lebensmittel Versuch: Isolierung
Versuch: Fäden spinnen Polymer aus Citronensäure und Glycerin
 Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff
 Vorlesung 16 Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff Bimolekulare nucleophile Substitutionen (S N 2-Reaktionen) In Vorlesung 11 hatten wir bereits die nucleophile Substitution
Vorlesung 16 Mechanismen nucleophiler Substitutionen am aliphatischen Kohlenstoff Bimolekulare nucleophile Substitutionen (S N 2-Reaktionen) In Vorlesung 11 hatten wir bereits die nucleophile Substitution
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß. Schulversuch-Protokoll Jan gr.
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 26.12.2007 Jan gr. Austing 1) Versuchsbezeichnung: Darstellung von β-aphtholorange
Schulversuch-Protokoll Jan gr. Austing
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
rganisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. ilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: xidation von Milchsäure ) Reaktionsgleichung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 4: Aromaten Versuch: Substituenteneinfluss
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 19.11.2008 Gruppe 4: Aromaten Versuch: Substituenteneinfluss
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23.11.2010 Gruppe 4: Aromaten Versuch (elektr.
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Versuch: Darstellung des Dibenzalacetons
 Philipps-Universität Marburg 02.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: Darstellung des Dibenzalacetons Zeitbedarf:
Philipps-Universität Marburg 02.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: Darstellung des Dibenzalacetons Zeitbedarf:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Jan Schäfer Name: Sarah enkel Datum: 19.12.2008 Gruppe 13: Polymere Versuch: Nylon-Seil-Trick
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Jan Schäfer Name: Sarah enkel Datum: 19.12.2008 Gruppe 13: Polymere Versuch: Nylon-Seil-Trick
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 24.11.2010 Gruppe 4: Aromaten Versuch (selbst):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 24.11.2010 Gruppe 4: Aromaten Versuch (selbst):
Versuch: Maillardreaktion
 Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Maillardreaktion
Philipps-Universität Marburg 10.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Maillardreaktion
+ R 2 OH H 2 SO 4 R 1
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Herstellung
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Herstellung
Schuleinsatz Calciumfluorid CaF 2 (s) 22-24/ S1 Schwefelsäure, (konz., w = 96 %)
 Reaktionsgleichungen F + (aq ) + H (aq ) HF (g) 4 HF (g) + SiO 2 (s) SiF 4 g + 2 H 2 O (l) Zeitbedarf Vorbereitung: 5min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Reaktionsgleichungen F + (aq ) + H (aq ) HF (g) 4 HF (g) + SiO 2 (s) SiF 4 g + 2 H 2 O (l) Zeitbedarf Vorbereitung: 5min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 03: Umsetzung von Hexan und Hexen mit Bromwasser Reaktion: Chemikalien:
Gruppe 06: pulsierende Amöben
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: pulsierende Amöben Reaktion: Chemikalien: Eingesetzte Stoffe Gefahrensymbole
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: pulsierende Amöben Reaktion: Chemikalien: Eingesetzte Stoffe Gefahrensymbole
Philipps-Universität Marburg Organisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß Assistentin: Beate Abé
 Philipps-Universität Marburg 14.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 4/Assistentenversuch):
Philipps-Universität Marburg 14.11.2008 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß WS 2008/09 Assistentin: Beate Abé Schulversuch (Gruppe 4/Assistentenversuch):
Gruppe 13 vorgegebener Versuch. Polyelektrolyte im Haargel
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Versuch: Alkoholtest mit Dichromat. Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz:
 Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: xidation der Propanole
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: xidation der Propanole
Versuch: Blitze unter Wasser
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Blitze unter Wasser
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Blitze unter Wasser
Reaktionstypen der Aliphate
 Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Einleitung Klasse 8 Reine Kohlenstoffketten, wie Alkane, Alkene und Alkine werden als Aliphate bezeichnet. Bei jeder chemischen Reaktion werden bestehende Verbindungen gebrochen und neue Bindungen erstellt.
Versuch: Emulgierende und dispergierende Wirkung von Tensiden
 Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Versuchsprotokoll. Synthese von Aromastoffen. Gruppe 7, Typ: Pflichtversuch O OH H 3 C C C C C CH 3 H H 3 C C C C C O C C OH
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese von Aromastoffen Gruppe
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose
 Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Übungen zur VL Chemie für Biologen und Humanbiologen Lösung Übung 9
 Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Übungen zur VL Chemie für Biologen und Humanbiologen 13.01.2012 Lösung Übung 9 1. Geben Sie jeweils zwei Beispiele für Konformations- und Konstitutionsisomere, d.h. insgesamt vier Paare von Molekülen.
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Chemie für Biologen, 2017
 Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Chemie für Biologen, 2017 Übung 11 Organisch chemische Reaktionen (Thema 12.1 12.6) Aufgabe 1: a) Erklären Sie folgende Begriffe: i) Übergangszustand Zustand der höchsten Energie in einer Reaktion, kann
Nucleophile Substitution
 3. Nucleophile Substitution 3.1 Nucleophile Substitution Vom alogenalkan zum Alkohol Erhitzt man eine heterogene Mischung aus Bromethan und Kalilauge, so wird das Gemisch homogen. Es entsteht das wasserlösliche
3. Nucleophile Substitution 3.1 Nucleophile Substitution Vom alogenalkan zum Alkohol Erhitzt man eine heterogene Mischung aus Bromethan und Kalilauge, so wird das Gemisch homogen. Es entsteht das wasserlösliche
CHE 102.1: Grundlagen der Chemie - Organische Chemie
 E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 8. alogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen alogenalkane sind in der organischen
E 102.1: Grundlagen der hemie - Organische hemie Prof Dr. E. Landau und Prof. Dr. J. A. Robinson 8. alogenalkane : Nucleophile Substitutions- und Eliminationsreaktionen alogenalkane sind in der organischen
a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten!
 Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Übung Nr. 9 Mi. 02.05.2012 bzw. Fr. 04.05.2012 1. Aromatensynthese a) Schlagen Sie eine Synthese für den folgenden Aromaten vor, ausgehend von den gezeigten Edukten! b) Was passiert bei der Umsetzung von
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 17.12.2010 Gruppe 8: Ester, Fette, Seifen u.
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Sarah Henkel Name: Johannes Hergt Datum: 17.12.2010 Gruppe 8: Ester, Fette, Seifen u.
Versuchsprotokoll. Züchtung von Kandiszucker-Kristallen
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Gruppe 2 vorgegebener Versuch Darstellung und Bromierung von Ethen
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 15.05.09 SS 09 Gruppe 2 vorgegebener Versuch Darstellung und omierung
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 15.05.09 SS 09 Gruppe 2 vorgegebener Versuch Darstellung und omierung
Versuchsprotokoll. Mischbarkeit von Alkoholen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Gruppe 8 eigener Versuch. Hydrolyse der Seife
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
2.Präparat: 1,2 Dibrom -1-phenylethan
 Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Marcus Wolf 04.06.3 2.Präparat: 1,2 Dibrom -1-phenylethan Literatur: Autorenkollektiv; Organikum; VEB Deutscher Verlag der Wissenschaften Berlin;7. Auflage; 1967; Seite 246 Streitwieser/eathcock ; Organische
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 2: Alkane Versuch: Gewinnung von Methan
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 2: Alkane Versuch: Gewinnung von Methan
Gruppe 6 Pflichtversuch. Abnahme der Wasserlöslichkeit der Alkanole mit zunehmender Molekülgröße
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Versuchsprotokoll. Kernbromierung und Seitenkettenbromierung von Xylol. Gruppe 4, Typ: Assiversuch KKK SSS
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Kernbromierung und Seitenkettenbromierung
KW Alkene. Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1
 KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
KW Alkene Nomenklatur. Darstellung. Reaktionen. Elektrophile Additionen. Prof. Ivo C. Ivanov 1 Alkene Alkene sind Kohlenwasserstoffe mit einer C=C-Bindung. Sie enthalten zwei -Atome weniger als die entsprechenden
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Oxidation
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Oxidation
Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in):Beate Abé Name: Johannes Hergt Datum: 16.11.2010 Gruppe 1: Einführung in die organische
Organisch-chemisches Praktikum für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in):Beate Abé Name: Johannes Hergt Datum: 16.11.2010 Gruppe 1: Einführung in die organische
SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration
 SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration Der Versuch sollte mindestens zu zweit oder in einer Gruppe durchgeführt werden, damit die Messung so genau wie möglich erfolgt. Als
SV: Abhängigkeit der Reaktionsgeschwindigkeit von der Konzentration Der Versuch sollte mindestens zu zweit oder in einer Gruppe durchgeführt werden, damit die Messung so genau wie möglich erfolgt. Als
Versuchsprotokoll: Mutarotation von Glucose
 Versuchsprotokoll: Mutarotation von Glucose Zeitaufwand: Aufbau: 10 Minuten Durchführung: 24 Stunden Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Glucose
Versuchsprotokoll: Mutarotation von Glucose Zeitaufwand: Aufbau: 10 Minuten Durchführung: 24 Stunden Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Glucose
Gruppe 6 eigener Versuch. Reaktion von Methanol mit Calciumchlorid
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.06.09 SS 09 Gruppe 6 eigener Versuch Reaktion von Methanol mit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 02.06.09 SS 09 Gruppe 6 eigener Versuch Reaktion von Methanol mit
2. Übungsblatt. Organische Chemie für Studierende mit Nebenfach Chemie
 Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
Allgemeine und Anorganische Chemie 2. Übungsblatt Organische Chemie für Studierende mit Nebenfach Chemie 1. Aufgabe: Ordnen Sie folgende Radikale nach steigender Stabilität: A B C D E F Lösung: A < C
= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]
![= Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s] = Durchschnittliche Bildungs- Geschwindigkeit [mol/s] = Durchschnittliche Verbrauchs- Geschwindigkeit [mol/s]](/thumbs/94/122358469.jpg) Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Ache2 Kapitel 14: Chemische Kinetik (Geschwindigkeit) Reaktionsgeschwindigkeit Beeinflussung: 1. Aggregatszustände der Reaktanten: Je öfters Moleküle zusammenstossen, desto schneller reagieren sie. (Oberflächenvergrösserung
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) OH H + - H 2 O. (aus H 3 PO 4 H 2 SO 4 ) - H + Stichpunkte zum E1-Mechanismus:
 Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Eliminierung nach E1 (Konkurrenzreaktion zu S N 1) + (aus 3 P 4 2 S 4 ) - 2 - + Stichpunkte zum E1-Mechanismus: 2-Schritt-eaktion über ein Carbenium-Ion (1. Schritt ist Abspaltung der Abgangsgruppe (im
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 14.12.2010 Gruppe 9: Kohlenhydrate Versuch (Assi):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 14.12.2010 Gruppe 9: Kohlenhydrate Versuch (Assi):
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 4: Aromaten Versuch: omierung von Toluol
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 4: Aromaten Versuch: omierung von Toluol
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Die elektrophile Addition
 Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Die elektrophile Addition Roland Heynkes 3.10.2005, Aachen Die elektrophile Addition als typische Reaktion der Doppelbindung in Alkenen bietet einen Einstieg in die Welt der organisch-chemischen Reaktionsmechanismen.
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
1.4 Die elektrophile aromatische Substitution
 1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
1.4 Die elektrophile aromatische Substitution Versuch: Bromierung von Toluol mit Eisen V In einem RG werden 2ml Toluol mit 0,5 g Eisenspänen gemischt. Hierzu werden 5 Tropfen Brom gegeben B Es bildet sich
Versuch: Fehling- und Biuretprobe mit Gummibärchen
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Fehling- und Biuretprobe mit
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Fehling- und Biuretprobe mit
Versuchsprotokoll: Fehling-Glucose
 Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 10 Minuten Abbau/Entsorgung: 5 Minuten (bei angesetzten Lösungen) Chemikalien: Chemikalie R-Sätze S-Sätze Gefahrensymbol Pentahydrat CuS 4 *5 2 22-36/38-50/53
Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 10 Minuten Abbau/Entsorgung: 5 Minuten (bei angesetzten Lösungen) Chemikalien: Chemikalie R-Sätze S-Sätze Gefahrensymbol Pentahydrat CuS 4 *5 2 22-36/38-50/53
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Vorlesung "Organische Chemie 1" Übungsblatt 4
 Vorlesung "Organische hemie 1" Übungsblatt 4 Ü1: Beim Steamcracken wird eine komplexe Mischung von Kohlenwasserstoffen durch kurzzeitiges Erhitzen in Gegenwart von Wasserdampf in eine Mischung von leichter
Vorlesung "Organische hemie 1" Übungsblatt 4 Ü1: Beim Steamcracken wird eine komplexe Mischung von Kohlenwasserstoffen durch kurzzeitiges Erhitzen in Gegenwart von Wasserdampf in eine Mischung von leichter
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23112010 Gruppe 4: Aromaten Assi-Versuch: Reaktion
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr Reiß Assistent(in): Jan Schäfer Name: Johannes Hergt Datum: 23112010 Gruppe 4: Aromaten Assi-Versuch: Reaktion
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Katrin Hohmann Name: Johannes Hergt Datum: 8.11.2010 Gruppe 7: Aldehyde und Carbonsäuren
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Katrin Hohmann Name: Johannes Hergt Datum: 8.11.2010 Gruppe 7: Aldehyde und Carbonsäuren
Gruppe 1 Pflichtversuch. Qualitative Analyse: Nachweis von Kohlenstoff als Kohlendioxid
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Versuch: Nachweis von Salicylsäure
 Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Schulversuchspraktikum. Moritz Pemberneck. Sommersemester Klassenstufen 7 & 8. Fällungsreaktionen. Kurzprotokoll
 Schulversuchspraktikum Moritz Pemberneck Sommersemester 2016 Klassenstufen 7 & 8 Fällungsreaktionen Kurzprotokoll Auf einen Blick: In diesem Protokoll werden weitere Schülerversuche zum Thema Fällungsreaktionen
Schulversuchspraktikum Moritz Pemberneck Sommersemester 2016 Klassenstufen 7 & 8 Fällungsreaktionen Kurzprotokoll Auf einen Blick: In diesem Protokoll werden weitere Schülerversuche zum Thema Fällungsreaktionen
Kapitel 3. Nucleophile Substitution
 Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Kapitel 3. Nucleophile Substitution Reaktionsmechanismen - S N 1-Reaktion: Reaktionskoordinate-Energie-Diagramm; Kinetik, Struktur-Reaktivitätsbeziehungen (stabiles Carbokation, schwaches Nucleophil, gute
Gruppe 2 eigener Versuch. Veränderung einer Kerzenflamme in Feuerzeuggas
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 20.05.09 SS 09 Gruppe 2 eigener Versuch Veränderung einer Kerzenflamme
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 20.05.09 SS 09 Gruppe 2 eigener Versuch Veränderung einer Kerzenflamme
Zuckernachweis mit Tollens-Reagenz
 Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
N H H. Carbanionen Lewis-Basen Olefine (Alkane) Die Stärke der Nucleophilie wird von versch. Faktoren beeinflußt z.b.
 Organische hemie Nucleophil = kernliebend Nucleophil = Teilchen oder Gruppe, die Lewis-basische Eigenschaften aufweist (also mind. ein freies Elektronenpaar besitzt), es gibt neutrale Nucleophile sowie
Organische hemie Nucleophil = kernliebend Nucleophil = Teilchen oder Gruppe, die Lewis-basische Eigenschaften aufweist (also mind. ein freies Elektronenpaar besitzt), es gibt neutrale Nucleophile sowie
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 26.11.2008 Gruppe 5: alogenalkane Versuch: Synthese von odoform
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 26.11.2008 Gruppe 5: alogenalkane Versuch: Synthese von odoform
Schulversuch-Protokoll Jan gr. Austing
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: Bromierung von Butan ) Reaktionsgleichung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: Bromierung von Butan ) Reaktionsgleichung:
