Aufgaben zur Experimentalphysik II: Thermodynamik
|
|
|
- Michael Weiss
- vor 5 Jahren
- Abrufe
Transkript
1 Aufgaben zur Experimentalphysik II: Thermodynamik Lösungen William Hefter - 5// Durchmesser der Stahlstange nach T : D s D s (1 + α Stahl T) Durchmesser der Bohrung im Ring nach T : D m D m (1 + α Messing T) D s D m T. Benötigte Wärme: Q mc w (1 C 15 C) mc w 85K Leistung durch Schütteln: P E f mgh f, wobei f, 5Hz D s D m α m D m α s D s 335 C T 5 C C 36 C t Q P c w85k gh f, s, 8 Tage 3. Es gibt drei Möglichkeiten: a) Das Eis erreicht gerade den Schmelzpunkt und schmilzt nicht. b) Ein Teil des Eis schmilzt und es stellt sich eine Temperatur von C ein c) Das ganze Eis schmizt und es stellt sich eine Temperatur oberhalb von C ein. a) Wärme, die dem Eis zugeführt wird: Q Eis m e c e (T End T Eis ) Wärme, die dem Wasser entzogen wird: Q w m w c w (T End T w ) Q Eis Q w T End m ec e T Eis + m w c w T w m e c e + m w c w 16, 6 C Liegt über dem Schmelzpunkt von Eis; also muss mindestens ein Teil vom Eis geschmolzen sein, die Rechnung berücksichtigt das nicht und ist falsch. b) Ein Teil des Eises schmilzt: m < m e Q eis m e c e ( C T eis ) + ml w, mit L w : Latente Schmelzwärme von Wasser Q w m w c w ( C T w ) m w c w T w Q eis Q w m c wm w T w + c e m e T eis L w 53g Also: Es ist genug Eis vorhanden, um das Wasser auf C runterzukühlen, aber nicht gefrieren zu lassen, da nur ein Teil des Eises schmilzt. Das ist die gesuchte Lösung. c) Dieser Fall tritt ein, wenn nur ein Eiswürfel verwendet wird: Es sind weniger als 53g Eis vorhanden, also schmilzt das ganze Eis und das Gemisch erreicht eine Temperatur oberhalb von C. Q w m w c w (T End T w ) Q eis c e m e ( T eis ) + c w m w (T eis ) + m e L w Q w Q eis T f c wm w T w + c e m e T eis m e L w c w (m w + m e ), 5 C 4. Im Gleichgewicht: D D (1 + α Cu (T f )) D (1 + α Cu T f ) d d (1 + α Al (T f 1 C)) d (1 + α Al (T f T a )) sind beide Durchmesser gleich, also: D (1 + α Cu T f ) d (1 + α Al (T f T a )) T f d D T a α Al d α Cu D α Al d 5, 38C Der Ring absorbiert also Q c m c c Cu T f und die Kugel gibt Q k m k c Al (T f T a ) ab. Q c Q k m k m cc Cu T f 8, 71g c Al (T a T f )
2 5. 1. Hauptsatz: U Q + W, wobei Q, W positiv bei Zufuhr iaf: Q ia f 5J, W ia f J U ia f 3J a) U ia f U ib f U ib f Q ib f + W ib f mit Q ib f 36J W ib f 6J b) U f i 3J U ia f Q f i U f i W f i 43J c) U f U i + 3J 4J d) U b J: Volumen konstant, also W b f Q b f U f U b 18J U ib 1J Q ib + W }{{ ib Q } ib 18J 6J 6. d() 5cm, T w C, T e 1 C. Mit der Wärmeleitungsgleichung: dq dt λa T Heiss T Kalt L λa T w T e d(t) Und der Wärmemenge, die nötig ist, um dm an Wasser gefrieren zu lassen, also dq L w dm Man stellt nach d () um und erhält: λa T d(t) L dm w dt L wρ e Ad (t) d () λ T L w ρ e d() 39, 5cm h 7. Die Wärmemenge, die das Wasser abstrahlen muss, um zu gefrieren, entspricht der Summe der abgegebenen Wärme bis zum Erreichen von C und der latenten Schmelzwärme, die es abgeben muss, um zu gefrieren, also: Q m w c w ( 6 C) + ( m w L w ) 1499J Das Wasser strahlt mit dem Emissionsgrad ɛ, 9 und der Temperatur T 6 C, der Nachthimmel wirkt als perfekter Strahler der Temperatur T h 3 C, mit dem Stefan-Boltzmann-Gesetz erhält man: P Q t σɛat4 h σɛat4 σɛa(t 4 h T4 ) t m w(l w + T w c w ) σɛa(t 4 h T4 ) 5, 9h Was weniger als einer Nacht entspricht. Diese Methode wurde in einigen Teilen der Welt vor der Erfindung von entsprechenden Maschinen tatsächlich verwendet.. 1. Wichtig: nr sowie nr p V V p ( ( a) 1 : Isothermer Prozess, also gilt U sowie W nr ln V p1 ln p ). Überdruck bedeutet Druck über Luftdruck, also ist p + 1, Pa, Pa und p ist gerade p, also: W J )
3 b) 3: Isobarer Prozess, die Arbeit entspricht gerade p V. Benötigt wird also V, was nach der Anfangsbemerkung gerade V p, also W 3 p ( V ) p ( p ) (p ) 1, J Also entspricht die Gesamtarbeit gerade W W 1 + W 3 5, 6kJ. Der Faktor nr im idealen Gasgesetz ist in beiden Fällen gleich, also folgt durch Gleichsetzen: p V T V T p (p + ρg 4m) p (73K + K) (73K + 4K) (cm3 ) 13cm 3 3. Ähnlich wie bei der Transformation der Planck schen Strahlungskurve gilt: Der Wert des Integrals muss gleich bleiben. In unseren Fall heisst das: P(E) P(v)dv. Mit folgt dv mv dv mv me P(E) P(v)dv ( ) m 3/ ( ) mv v exp dv π k b T k b T m 3/ ( E π (k b T) 3/ m exp m E k b T m ( E π (k b T) 3/ exp E ) k b T ( E π(kb T) 3/ exp E k b T ) ) me Interessant ist, dass die Geschwindigkeitsverteilung nicht mehr von der Masse abhängt, sondern tatsächlich nur von der Temperatur. Dies folgt nicht aus der Gleichung für die innere Energie, sondern ist der Grund dafür, wie die nächste Aufgabe zeigt. 4. Vgl. Vorlesung: Die mittlere Geschwindigkeit eines Systems von Teilchen, das durch die Maxwell-Verteilung beschrieben wird, ist gegeben durch Analog ist die mittlere Energie dann v vp(v)dv E EP(E) ( π(kb T) 3/ E 3/ exp E ) k B T Wir benutzen nun die Substition und erhalten E x E k b T E xk bt dx 1 k b T dxk bt ( π(kb T) 3/ x 3/ (k b T) 3/ exp E ) k k B T b Tdx
4 k b T x 3/ exp( x)dx π 3 πkb T π 4 3 k bt Das ist die mittlere kinetische Energie eines Moleküls in einem Maxwell-System. Für alle N Moleküle ergibt sich dann E N 3 k bt 3 nrt 3RT 5. Die rms-geschwindigkeit ist lt. Vorlesung v rms M. Die Fluchtgeschwindigkeit leitet sich aus der Gesamtenergie eines Teilchens auf der Erdoberfläche E mgr e + 1 mv und der Tatsache, dass diese Energie im Unendlichen gerade sein muss, her, also folgt v f gr e, wobei R e 637km ist. 3RT M die molare Masse von molekularem Wasser- a) Es muss also g gr e gelten, wobei M, stoff ist. Auflösen nach T ergibt T gr em 3R mol 1 4 K b) Analog mit Sauerstoff, wobei M 3 g mol T 1, K c) Die mittlere Temperatur des Wasserstoffs entspricht in etwa der Temperatur in den höheren Schichten, also können die schnellsten Moleküle, entsprechend dem rechten Anteil der Maxwell-Kurve, entweichen. Die neue Verteilung enthält wieder einen Anteil an Wasserstoff, der schnell genug ist und entweicht usw. Daher gibt es in der Erdatmosphäre kaum Wasserstoff. Sauerstoff dagegen ist viel zu schwer, was der Grund ist, warum unser Sauerstoff zum Atmen nicht entweicht. 6. Zweiatomiges ideales Gas: 3 translatorische + Rotationsfreiheitsgrade 5 Freiheitsgrade, also C v 5 R, C p C v + R 7 R. a) Q nc p T 4mol 7 R 6K 6, 98kJ b) U nc v T 4mol 5 T 6K 4, 99kJ c) W U Q 1, 99kJ d) Nur translatorische Energie! K 3 nr T, 99kJ 7. Analog zu 6): C v 5 R, C p 7 R γ C p C v 1, 4 (Adiabatenkoeffizient) a) Adiabatengleichung für Druck: V γ 1 p ( V1 ) γ p γ, 67bar Adiabatengleichung für Temperatur: V γ 1 1 T V γ 1 T γ 1 36K b) Hier gilt das ideale Gasgesetz, also / T V V, 38l 8. Zur Erinnerung: U nc v T gilt immer für alle Prozesse. Einatomiges ideales Gas: C v 3 R, C p 5 R a)
5 b) 1 : isochor W U Q nc v (T ) 3, 74kJ 3: adiabatisch Q W U nc v (T 3 ) 1, 81kJ 3 1: isobar Q nc p ( T 3 ) 3, kj U nc v ( T 3 ) 1, 93kJ W U Q 1, 9kJ Gesamter Prozess: Q 3, 74kJ 3, kj 5J U (Kreisprozess!) W U Q 5J c) : nr nr, 46 1 m 3 1 ist isochor, also bleibt das Volumen konstant, und p nrt 3 1 ist isobar, also p 3 und V nrt 3 3, 73 1 m 3, 1 5 Pa Entropie a) Zunächst wird die Gleichgewichtstemperatur bestimmt: T f c wm w T w + c Al m Al T Al c w m w + c Al m Al 57 C b) Allg. ist die Entropieänderung S ˆ dq T ˆ mcdt T mc ln T Für das Aluminium ergibt sich: S Al m Al c Al ln T f T Al c) Analog für das Wasser: S w 4, 9 J K, 1 J K d) Die Entropie für das Gesamtsystem ist einfach die Summe der Teilentropien, also S, 8 J K ; und die ist positiv, wie sie sein sollte.. Die Entropiezunahme für den Würfel besteht aus drei Teilen: Die Wärmeaufnahme des Eises bis C, der Schmelzvorgang bei C und der Wärmeaufnahme bis 15 C. Die Temperatur des Sees kann als annähernd konstant betrachtet werden, wenn man sich die Massenverhältnisse klarmacht. Also, für den Eiswürfel: S eis mc eis ln 73K 63K + mc w ln 88K 73K + ml w 73K 15, 7 J K Die Entropie für den See is einfach S see dq T see, wobei dq die dem Würfel übertragene Wärmemenge ist. S see mc eis( ( 1 C)) + ml w + mc w (15 C ) 88K 14, 51 J K Die gesamte Änderung der Entropie ist damit S S eis + S see, 76 J K Die Unordnung hat also im Einklang mit dem. Hauptsatz zugenommen. 3. Für den dargestellten Kreisprozess:
6 a) Wärme wird nur im Prozess ab zugeführt (isochore Expansion). Hier ist W und Q ab nc v (T b T a ). Die Temperaturen erhalten wir über das ideale Gasgesetz: T b p bv b nr, T a p av b nr, eingesetzt erhält man Q ab nc v nr V b(p b p a ) 3 V b(p b p a ) Wir benötigen noch p a. Wir erkennen, dass bc ein adiabatischer Prozess ist, also p a V γ a p b V γ b p a p b ( 1 8) γ, Pa Alle weiteren Werte für Q ab sind bekannte, es folgt Q ab 1, 47kJ b) bc ist adiabatisch, also Q bc. Wärme wird nur im Prozess ca abgegeben, gemäß Q ca nc p (T a T c ), T c erhält man wieder über das ideale Gasgesetz und Q ca 5 p a(v b 8V b ) 7 5 p av b 554J c) Für einen Umlauf ist U gerade gleich Null und die Arbeit erwartungsgemäß die Differenz zwischen aufgenommener und abgegebener Wärme, also W ( Q) ( Q ac + Q ca ) 918J. d) Die Effizienz ist ɛ bekommen gezahlt 4. Gegeben sind γ,, p 3, V, V 3 V 4 4 und. W Qab, 64 a) 1 : nr :p 3, T 3 nr 3( ) 3 :p V γ p 3V γ γ 3 p 3 3p V1 ( γ, ( 3p1 4) analog T ) γ 1 ) γ 1 4 : V γ 1 p 4V γ 4 p ( 4 γ ( 1 4), T4 1 4 b) Der Wirkungsgrad ist W ɛ W 3 + W 41 Q rein Q nc v (T 3 T + T 4 ) 1 nc v (T ) 1 4 γ Die innere Energie berechnet sich ja immer über U 3 nrt. In diesem Fall setzt sich n aus den beiden einzelnen Stoffmengen der beiden Volumina. Man berechnet also zuerst: n 1 3pV RT n pv RT Also ist n n 1 + n 7 pv RT und damit U 3 1 nrt pv Das System ist thermisch isoliert und die beiden Gase haben dieselbe Temperatur, also ändert sich die Temperatur auch nicht. Die innere Energie ändert sich auch nicht, also erhalten wir für p : U 3 nrt 3 p 3V 9 p V 1 pv p 7 3 p
7 Zur Entropie: Hier liegt ein isothermer Prozess vor, also ist U dq dw pdv nrt V dv dq T nr dv V S nr ln V Das gilt für eine Seite; die Gesamtänderung der Entropie ist folglich die Summe S n 1 R ln V + n R ln V V Überlegung: Das große Volumen hatte 6mal so viele Moleküle wie das kleine, trägt also 6mal so viel zum Volumen bei, also ist 6V. Weiter bekannt: + V 3V. Zwei Gleichungen für zwei Unbekannte: 6V 18 7 V. Zusammen: S n 1 R ln n R ln 3 7 pv T pv T (6 ln 9 6 ln 7 + ln 3 ln 7) (13 ln 3 7 ln 7), 66 pv T. Diskussion des Carnot-Zyklus a) Hier Skizze Besteht aus 1 : Isotherme Expansion, System nimmt Wärme vom Wärmebad auf und gibt Arbeit ab; dq >, dw < 3: Adiabatische Expansion, System gibt Arbeit ab; dw < 3 4: Isotherme Kompression, System gibt Wärme an das Wärmebad ab; dq <, dw > 4 1: Adiabatische Kompression, es wird Arbeit am System geleistet; dw > b) du, dq, dw für jeden Teilprozess i. Isotherm: du dq dw nr ln V ii. Adiabatisch: dq dw du nc v (T ) iii. Isotherm: du dq dw nrt ln V 3 V iv. Adiabatisch: dq dw du nc v ( T ) c) Wirkungsgrad: ɛ bekommen gezahlt dw ges T heiss T kalt 1 T T heiss dq 1
TU-München, Musterlösung. Experimentalphysik II - Ferienkurs Andreas Schindewolf
 TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
TU-München, 18.08.2009 Musterlösung Experimentalphysik II - Ferienkurs Andreas Schindewolf 1 Random Kreisprozess a Wärme wird nur im isochoren Prozess ab zugeführt. Hier ist W = 0 und Q ab = nc V t b T
Übungsblatt 2 ( )
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 01 Übungsblatt (11.05.01) 1) Geschwindigkeitsverteilung eines idealen Gases (a) Durch welche Verteilung lässt sich die Geschwindigkeitsverteilung
(b) Schritt I: freie adiabatische Expansion, also ist δw = 0, δq = 0 und damit T 2 = T 1. Folglich ist nach 1. Hauptsatz auch U = 0.
 3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
3 Lösungen Lösung zu 65. (a) Siehe Abbildung 1. (b) Schritt I: freie adiabatische Expansion, also ist δw 0, δq 0 und damit. Folglich ist nach 1. Hauptsatz auch U 0. Schritt II: isobare Kompression, also
Experimentalphysik II: Thermodynamik
 Experimentalphysik II: Thermodynamik Ferienkurs Wintersemester 08/09 William Hefter 23/02/2009 Inhaltsverzeichnis 1 Thermodynamik 2 1.1 Temperatur, Wärme und Arbeit.................................. 2
Experimentalphysik II: Thermodynamik Ferienkurs Wintersemester 08/09 William Hefter 23/02/2009 Inhaltsverzeichnis 1 Thermodynamik 2 1.1 Temperatur, Wärme und Arbeit.................................. 2
Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt
 1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
1 Aufgabe: Entropieänderung Ferienkurs Experimentalphysik 2 - Donnerstag-Übungsblatt 1 Aufgabe: Entropieänderung a) Ein Kilogramm Wasser bei = C wird in thermischen Kontakt mit einem Wärmereservoir bei
10. Thermodynamik Der erste Hauptsatz Der zweite Hauptsatz Thermodynamischer Wirkungsgrad Der Carnotsche Kreisprozess
 Inhalt 10.10 Der zweite Hauptsatz 10.10.1 Thermodynamischer Wirkungsgrad 10.10.2 Der Carnotsche Kreisprozess Für kinetische Energie der ungeordneten Bewegung gilt: Frage: Frage: Wie kann man mit U Arbeit
Inhalt 10.10 Der zweite Hauptsatz 10.10.1 Thermodynamischer Wirkungsgrad 10.10.2 Der Carnotsche Kreisprozess Für kinetische Energie der ungeordneten Bewegung gilt: Frage: Frage: Wie kann man mit U Arbeit
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 14.09.2010 Inhaltsverzeichnis Inhaltsverzeichnis 1 Thermodynamische Hauptsätze 3 1.1 Aufgabe 1:.................................... 3 1.2 Aufgabe
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen - Lösungen
 Ferienkurs Experimentalphysik II Thermodynamik Grundlagen - Lösungen Lennart Schmidt 08.09.011 Aufgabe 1: Berechnen Sie den Volumenausdehnungskoeffizienten für das ideale Gas. Zustandsgleichung des idealen
Ferienkurs Experimentalphysik II Thermodynamik Grundlagen - Lösungen Lennart Schmidt 08.09.011 Aufgabe 1: Berechnen Sie den Volumenausdehnungskoeffizienten für das ideale Gas. Zustandsgleichung des idealen
Thermodynamische Hauptsätze, Kreisprozesse Übung
 Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Thermodynamische Hauptsätze, Kreisprozesse Übung Marcus Jung 4.09.00 Inhaltsverzeichnis Inhaltsverzeichnis Thermodynamische Hauptsätze. Aufgabe :..................................... Aufgabe :.....................................
Der Zustand eines Systems ist durch Zustandsgrößen charakterisiert.
 Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Grundbegriffe der Thermodynamik Die Thermodynamik beschäftigt sich mit der Interpretation gegenseitiger Abhängigkeit von stofflichen und energetischen Phänomenen in der Natur. Die Thermodynamik kann voraussagen,
Musterlösung zur Abschlussklausur PC I Übungen (27. Juni 2018)
 1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
1. Abkühlung (100 Punkte) Ein ideales Gas (genau 3 mol) durchläuft hintereinander zwei (reversible) Zustandsänderungen: Zuerst expandiert es isobar, wobei die Temperatur von 50 K auf 500 K steigt und sich
Physik 2 (B.Sc. EIT) 2. Übungsblatt
 Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
Institut für Physik Werner-Heisenberg-Weg 9 Fakultät für Elektrotechnik 85577 München / Neubiberg Universität der Bundeswehr München / Neubiberg Prof Dr H Baumgärtner Übungen: Dr-Ing Tanja Stimpel-Lindner,
V 1. pdv mit p = = p 0 V 0 ln p 1. m = C H2 O T ln p 1. = P a 150m J 8K ln P a
 2 Lösungen Lösung zu 46. Nutze den 1. Hauptsatz du = Q + W = Q pdv. Bei einem isothermen Prozess ändert sich die innere Energie nicht: du = 0, was wir schon in mehreren Aufgaben zuvor benutzt haben. Also
2 Lösungen Lösung zu 46. Nutze den 1. Hauptsatz du = Q + W = Q pdv. Bei einem isothermen Prozess ändert sich die innere Energie nicht: du = 0, was wir schon in mehreren Aufgaben zuvor benutzt haben. Also
1 Thermodynamik allgemein
 Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Einführung in die Energietechnik Tutorium II: Thermodynamik Thermodynamik allgemein. offenes System: kann Materie und Energie mit der Umgebung austauschen. geschlossenes System: kann nur Energie mit der
Ferienkurs Experimentalphysik 2
 Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Ferienkurs Experimentalphysik 2 Vorlesung 1 Thermodynamik Andreas Brenneis, Marcus Jung, Ann-Kathrin Straub 13.09.2010 1 Allgemeines und Grundbegriffe Grundlegend für das nun folgende Kapitel Thermodynamik
Musterlösung Übung 3
 Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Musterlösung Übung 3 Aufgabe 1: Der 1. Hautsatz der Thermodynamik a) Für ein geschlossenes System folgt aus der Energieerhaltung (Gleichung (94) im Skrit) du = dw + dq, (1.1) da ausser Arbeit und Wärme
Die Carnot-Maschine SCHRITT III. Isotherme Kompression bei einer Temperatur T 2 T 2. Wärmesenke T 2 = konstant. Nicolas Thomas
 Die Carnot-Maschine SCHRITT III Isotherme Kompression bei einer Temperatur T 2 T 2 Wärmesenke T 2 = konstant Die Carnot-Maschine SCHRITT IV Man isoliert das Gas wieder thermisch und drückt den Kolben noch
Die Carnot-Maschine SCHRITT III Isotherme Kompression bei einer Temperatur T 2 T 2 Wärmesenke T 2 = konstant Die Carnot-Maschine SCHRITT IV Man isoliert das Gas wieder thermisch und drückt den Kolben noch
Physik 2 Hydrologen et al., SoSe 2013 Lösungen 3. Übung (KW 19/20) Carnot-Wärmekraftmaschine )
 3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
3. Übung KW 19/20) Aufgabe 1 T 4.5 Carnot-Wärmekraftmaschine ) Eine Carnot-Wärmekraftmaschine arbeitet zwischen den Temperaturen und. Während der isothermen Expansion vergrößert sich das Volumen von auf
Musterlösung Klausur Physikalische Chemie I: Thermodynamik
 Musterlösung Klausur Physikalische Chemie I: hermodynamik Aufgabe : Dimerisierung von Stickstoffdioxid a Nach dem Prinzip des kleinsten Zwanges von LeChatelier sollte der Druck p möglichst klein und die
Musterlösung Klausur Physikalische Chemie I: hermodynamik Aufgabe : Dimerisierung von Stickstoffdioxid a Nach dem Prinzip des kleinsten Zwanges von LeChatelier sollte der Druck p möglichst klein und die
Versuch: Sieden durch Abkühlen
 ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
ersuch: Sieden durch Abkühlen Ein Rundkolben wird zur Hälfte mit Wasser gefüllt und auf ein Dreibein mit Netz gestellt. Mit dem Bunsenbrenner bringt man das Wasser zum Sieden, nimmt dann die Flamme weg
Wärmelehre Wärme als Energie-Form
 Wärmelehre Wärme als Energie-Form Joule's Vorrichtung zur Messung des mechanischen Wärme-Äquivalents alte Einheit: 1 cal = 4.184 J 1 kcal Wärme erwärmt 1 kg H 2 O um 1 K Wird einem Körper mit der Masse
Wärmelehre Wärme als Energie-Form Joule's Vorrichtung zur Messung des mechanischen Wärme-Äquivalents alte Einheit: 1 cal = 4.184 J 1 kcal Wärme erwärmt 1 kg H 2 O um 1 K Wird einem Körper mit der Masse
Übungen zu Experimentalphysik 2 für MSE
 Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
Physik-Department LS für Funktionelle Materialien SS 208 Übungen zu Experimentalphysik 2 für MSE Prof. Dr. Peter Müller-Buschbaum, Dr. olker Körstgens, Sebastian Grott, Julian Heger, Dr. Neelima Paul,
Musterlösung zu Übung 7
 PCI Thermodynamik G. eschke FS 011 Musterlösung zu Übung 7 (8. April 011) Aufgabe 1 (a) Die Shomate-Gleichung (Script (153)) lautet: C p (gas, T ) A + BT + CT + DT 3 + E T (1) Für das Kohlenstoffmonooxid
PCI Thermodynamik G. eschke FS 011 Musterlösung zu Übung 7 (8. April 011) Aufgabe 1 (a) Die Shomate-Gleichung (Script (153)) lautet: C p (gas, T ) A + BT + CT + DT 3 + E T (1) Für das Kohlenstoffmonooxid
Formelsammlung. Experimentalphysik II. Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester Pascal Del Haye 27.
 Formelsammlung Experimentalphysik II Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester 2003 Pascal Del Haye www.delhaye.de 27. Juli 2003 Inhaltsverzeichnis Thermodynamik 3. Ideale Gasgleichung........................
Formelsammlung Experimentalphysik II Zur Vorlesung bei Prof. Dr. M. Wuttig, Sommersemester 2003 Pascal Del Haye www.delhaye.de 27. Juli 2003 Inhaltsverzeichnis Thermodynamik 3. Ideale Gasgleichung........................
3 Der 1. Hauptsatz der Thermodynamik
 3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
3 Der 1. Hauptsatz der Thermodynamik 3.1 Der Begriff der inneren Energie Wir betrachten zunächst ein isoliertes System, d. h. es können weder Teilchen noch Energie mit der Umgebung ausgetauscht werden.
Vorbemerkung. [disclaimer]
![Vorbemerkung. [disclaimer] Vorbemerkung. [disclaimer]](/thumbs/97/130802699.jpg) orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
orbemerkung Dies ist ein abgegebener Übungszettel aus dem Modul physik2. Dieser Übungszettel wurde nicht korrigiert. Es handelt sich lediglich um meine Abgabe und keine Musterlösung. Alle Übungszettel
ST Der Stirling-Motor als Wärmekraftmaschine
 ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
ST Der Stirling-Motor als Wärmekraftmaschine Blockpraktikum Herbst 2007 Gruppe 2b 24. Oktober 2007 Inhaltsverzeichnis 1 Grundlagen 2 1.1 Stirling-Kreisprozess............................. 2 1.2 Technische
O. Sternal, V. Hankele. 5. Thermodynamik
 5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
5. Thermodynamik 5. Thermodynamik 5.1 Temperatur und Wärme Systeme aus vielen Teilchen Quelle: Wikimedia Commons Datei: Translational_motion.gif Versuch: Beschreibe 1 m 3 Luft mit Newton-Mechanik Beschreibe
Klausur Wärmelehre E2/E2p SoSe 2016 Braun. Formelsammlung Thermodynamik
 Klausur Wärmelehre E2/E2p SoSe 2016 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Wärmelehre E2/E2p SoSe 2016 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Aufgaben zur Wärmelehre
 Aufgaben zur Wärmelehre 1. Ein falsch kalibriertes Quecksilberthermometer zeigt -5 C eingetaucht im schmelzenden Eis und 103 C im kochenden Wasser. Welche ist die richtige Temperatur, wenn das Thermometer
Aufgaben zur Wärmelehre 1. Ein falsch kalibriertes Quecksilberthermometer zeigt -5 C eingetaucht im schmelzenden Eis und 103 C im kochenden Wasser. Welche ist die richtige Temperatur, wenn das Thermometer
Allgemeine Gasgleichung und technische Anwendungen
 Allgemeine Gasgleichung und technische Anwendungen Ziele i.allgemeine Gasgleichung: Darstellung in Diagrammen: Begriffsdefinitionen : Iso bar chor them Adiabatische Zustandsänderung Kreisprozess prinzipiell:
Allgemeine Gasgleichung und technische Anwendungen Ziele i.allgemeine Gasgleichung: Darstellung in Diagrammen: Begriffsdefinitionen : Iso bar chor them Adiabatische Zustandsänderung Kreisprozess prinzipiell:
Musterlösung Aufgabe 1: Zweikammermesssysatem
 Klausur Thermodynamik I (08.09.2016) 1 Musterlösung Aufgabe 1: Zweikammermesssysatem Teilaufgabe a) Da die Membrane zunächst für Wärme undurchlässig ist, handelt es sich um eine adiabate Zustandsänderung
Klausur Thermodynamik I (08.09.2016) 1 Musterlösung Aufgabe 1: Zweikammermesssysatem Teilaufgabe a) Da die Membrane zunächst für Wärme undurchlässig ist, handelt es sich um eine adiabate Zustandsänderung
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C?
 A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
A 1.1 a Wie groß ist das Molvolumen von Helium, flüssigem Wasser, Kupfer, Stickstoff und Sauerstoff bei 1 bar und 25 C? (-> Tabelle p) A 1.1 b Wie groß ist der Auftrieb eines Helium (Wasserstoff) gefüllten
T4p: Thermodynamik und Statistische Physik Prof. Dr. H. Ruhl Übungsblatt 8 Lösungsvorschlag
 T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
T4p: Thermodynamik und Statistische Physik Pro Dr H Ruhl Übungsblatt 8 Lösungsvorschlag 1 Adiabatengleichung Als adiabatische Zustandssänderung bezeichnet man einen thermodynamischen organg, bei dem ein
1. Klausur zur Vorlesung Physikalische Chemie I
 1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
1. Klausur zur Vorlesung Physikalische Chemie I Sommersemester 2006 8. Juni 2006 Angaben zur Person (BITTE LESERLICH UND IN DRUCKBUCHSTABEN) Name, Vorname... Geburtsdatum und -ort... Matrikelnummer...
Physikdepartment. Ferienkurs zur Experimentalphysik 4. Daniel Jost 10/09/15
 Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Physikdepartment Ferienkurs zur Experimentalphysik 4 Daniel Jost 10/09/15 Inhaltsverzeichnis Technische Universität München 1 Kurze Einführung in die Thermodynamik 1 1.1 Hauptsätze der Thermodynamik.......................
Experimentalphysik. Vorlesungsergänzung (VE), Wintersemester 2017 Modulnummer PTI 301
 Experimentalphysik Vorlesungsergänzung (VE), Wintersemester 2017 Modulnummer PTI 301 Experimentalphysik, Inhalt VE 2.1: Temperatur und Wärmeausdehnung VE 2.2: Zustandsgleichung idealer Gase VE 2.3: Erster
Experimentalphysik Vorlesungsergänzung (VE), Wintersemester 2017 Modulnummer PTI 301 Experimentalphysik, Inhalt VE 2.1: Temperatur und Wärmeausdehnung VE 2.2: Zustandsgleichung idealer Gase VE 2.3: Erster
Übungen zur Theoretischen Physik F SS Ideales Boltzmann-Gas: ( =25 Punkte, schriftlich)
 Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zur Theoretischen Physik F SS 2016 Prof. Dr. A. Shnirman Blatt 2 Dr. B. Narozhny, Dipl.-Phys. P. Schad Lösungsvorschlag
Karlsruher Institut für Technologie Institut für Theorie der Kondensierten Materie Übungen zur Theoretischen Physik F SS 2016 Prof. Dr. A. Shnirman Blatt 2 Dr. B. Narozhny, Dipl.-Phys. P. Schad Lösungsvorschlag
Moderne Theoretische Physik III (Theorie F Statistische Mechanik) SS 17
 Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik III (heorie F Statistische Mechanik) SS 17 Prof. Dr. Alexander Mirlin Blatt 2 PD Dr. Igor Gornyi,
Karlsruher Institut für echnologie Institut für heorie der Kondensierten Materie Moderne heoretische Physik III (heorie F Statistische Mechanik) SS 17 Prof. Dr. Alexander Mirlin Blatt 2 PD Dr. Igor Gornyi,
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Prof. Dr. U. Schollwöck Sommersemester 2013
 Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Theoretische Physik 25. Juli 2013 Thermodynamik und statistische Physik (T4) Klausur Prof. Dr. U. Schollwöck Sommersemester 2013 Matrikelnummer: Aufgabe 1 2 3 4 5 6 Summe Punkte Note: WICHTIG! Schreiben
Der 1. Hauptsatz. Energieerhaltung:
 Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
Der 1. Hauptsatz Energieerhaltung: Bei einer Zustandsänderung tauscht das betrachtete System Energie ( W, Q mit seiner Umgebung aus (oft ein Wärmereservoir bei konstantem. Für die Energiebilanz gilt: U
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases. f=5 Translation + Rotation. f=7 Translation + Rotation +Vibration. Wiederholung
 1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
1. Wärmelehre 2.4. Die Freiheitsgrade eines Gases Wiederholung Speziische molare Wärmekapazität c m,v = 2 R R = N A k B = 8.315 J mol K =5 Translation + Rotation =7 Translation + Rotation +ibration 1.
Allgemeines Gasgesetz. PV = K o T
 Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Allgemeines Gasgesetz Die Kombination der beiden Gesetze von Gay-Lussac mit dem Gesetz von Boyle-Mariotte gibt den Zusammenhang der drei Zustandsgrößen Druck, Volumen, und Temperatur eines idealen Gases,
Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler
 TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
TU München Reinhard Scholz Physik Department, T33 Thomas Eissfeller, Peter Greck, Tillmann Kubis, Christoph Schindler http://www.wsi.tum.de/t33/teaching/teaching.htm Übung in Theoretischer Physik B (Thermodynamik)
Hauptsatz der Thermodynamik
 0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
0.7. Hauptsatz der Thermodynamik Die einem System von außen zugeführte Wärmemenge Q führt zu Erhöhung U der inneren Energie U und damit Erhöhung T der Temperatur T Expansion des olumens gegen den äußeren
Winter-Semester 2017/18. Moderne Theoretische Physik IIIa. Statistische Physik
 Winter-Semester 2017/18 Moderne Theoretische Physik IIIa Statistische Physik Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie Do 11:30-13:00, Lehmann Raum 022, Geb 30.22 http://www.tkm.kit.edu/lehre/
Winter-Semester 2017/18 Moderne Theoretische Physik IIIa Statistische Physik Dozent: Alexander Shnirman Institut für Theorie der Kondensierten Materie Do 11:30-13:00, Lehmann Raum 022, Geb 30.22 http://www.tkm.kit.edu/lehre/
Ferienkurs Experimentalphysik II Elektro- und Thermodynamik. Thermodynamik Teil II. 12. September 2011 Michael Mittermair
 Ferienkurs Experimentalphysik II Elektro- und Thermodynamik Thermodynamik Teil II 12. September 2011 Michael Mittermair Inhaltsverzeichnis 1 Allgemeines 3 1.1 Kategorisierung von Systemen..................
Ferienkurs Experimentalphysik II Elektro- und Thermodynamik Thermodynamik Teil II 12. September 2011 Michael Mittermair Inhaltsverzeichnis 1 Allgemeines 3 1.1 Kategorisierung von Systemen..................
T 300K,p 1,00 10 Pa, V 0, m,t 1200K, Kontrolle Physik Leistungskurs Klasse Hauptsatz, Kreisprozesse
 Kontrolle Physik Leistungskurs Klasse 2 7.3.207. Hauptsatz, Kreisprozesse. Als man früh aus dem Haus gegangen ist, hat man doch versehentlich die Kühlschranktür offen gelassen. Man merkt es erst, als man
Kontrolle Physik Leistungskurs Klasse 2 7.3.207. Hauptsatz, Kreisprozesse. Als man früh aus dem Haus gegangen ist, hat man doch versehentlich die Kühlschranktür offen gelassen. Man merkt es erst, als man
Thermodynamik. Kapitel 4. Nicolas Thomas
 Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Thermodynamik Kapitel 4 Arbeit und Wärme Länge, x F Kolben Länge, x F Der Kolben wird sehr langsam um die Distanz -dx verschoben. dx Kolben Wieviel Arbeit mussten wir leisten, um den Kolben zu bewegen?
Physikalische Chemie: Kreisprozesse
 Physikalische Chemie: Kreisprozesse Version vom 29. Mai 2006 Inhaltsverzeichnis 1 Diesel Kreisprozess 2 1.1 Wärmemenge Q.................................. 2 1.2 Arbeit W.....................................
Physikalische Chemie: Kreisprozesse Version vom 29. Mai 2006 Inhaltsverzeichnis 1 Diesel Kreisprozess 2 1.1 Wärmemenge Q.................................. 2 1.2 Arbeit W.....................................
Verbundstudium TBW Teil 1 Wärmelehre 1 3. Semester
 Verbundstudium TBW Teil 1 Wärmelehre 1 3. Semester 1. Temperaturmessung Definition der Temperaturskala durch ein reproduzierbares thermodynam. Phänomen, dem Thermometer Tripelpunkt: Eis Wasser - Dampf
Verbundstudium TBW Teil 1 Wärmelehre 1 3. Semester 1. Temperaturmessung Definition der Temperaturskala durch ein reproduzierbares thermodynam. Phänomen, dem Thermometer Tripelpunkt: Eis Wasser - Dampf
Klausur Thermodynamik E2/E2p SoSe 2019 Braun. Formelsammlung Thermodynamik
 Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Klausur Thermodynamik E2/E2p SoSe 2019 Braun Name: Matrikelnummer: O E2 O E2p (bitte ankreuzen) Die mit Stern (*) gekennzeichneten Aufgaben sind für E2-Kandidaten vorgesehen - E2p-Kandidaten dürfen diese
Kapitel IV Wärmelehre und Thermodynamik
 Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas - makroskopisch e) Das reale Gas / Phasenübergänge f) Das ideale Gas mikroskopisch g)
Kapitel IV Wärmelehre und Thermodynamik a) Definitionen b) Temperatur c) Wärme und Wärmekapazität d) Das ideale Gas - makroskopisch e) Das reale Gas / Phasenübergänge f) Das ideale Gas mikroskopisch g)
Probeklausur: Thermodynamik
 E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Probeklausur: Thermodynamik Probeklausur: Thermodynamik Vorname: Nachname: Matrikelnummer: Studiengang: Fachsemester: Studierende der E2p (6 ECTS)
E2-E2p: Experimentalphysik 2 Prof. J. Lipfert SS 2018 Probeklausur: Thermodynamik Probeklausur: Thermodynamik Vorname: Nachname: Matrikelnummer: Studiengang: Fachsemester: Studierende der E2p (6 ECTS)
II. Wärmelehre. II.2. Die Hauptsätze der Wärmelehre. Physik für Mediziner 1
 II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
II. Wärmelehre II.2. Die auptsätze der Wärmelehre Physik für Mediziner 1 1. auptsatz der Wärmelehre Formulierung des Energieerhaltungssatzes unter Einschluss der Wärmenergie: die Zunahme der Inneren Energie
Kapitel 8: Thermodynamik
 Kapitel 8: Thermodynamik 8.1 Der erste Hauptsatz der Thermodynamik 8.2 Mechanische Arbeit eines expandierenden Gases 8.3 Thermische Prozesse des idealen Gases 8.4 Wärmemaschine 8.5 Der zweite Hauptsatz
Kapitel 8: Thermodynamik 8.1 Der erste Hauptsatz der Thermodynamik 8.2 Mechanische Arbeit eines expandierenden Gases 8.3 Thermische Prozesse des idealen Gases 8.4 Wärmemaschine 8.5 Der zweite Hauptsatz
Gesetz von Boyle. Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V.
 Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Gesetz von Boyle Empirisch wurde beobachtet, dass bei konstanter Temperatur gilt: p.v = Konstant bzw V 1 / p bzw p 1 / V Isothermen Gesetz von Gay-Lussac Jacques Charles und Joseph-Louis Gay-Lussac fanden
Übung 2. Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen
 Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Ziel: Bedeutung/Umgang innere Energie U und Enthalpie H verstehen Wärmekapazitäten isochore/isobare Zustandsänderungen Standardbildungsenthalpien Heizwert/Brennwert adiabatische Flammentemperatur WS 2013/14
Klausur Wärmelehre E2/E2p, SoSe 2012 Braun. Formelsammlung Thermodynamik
 Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Name: Klausur Wärmelehre E2/E2p, SoSe 2012 Braun Matrikelnummer: Benotung für: O E2 O E2p (bitte ankreuzen, Mehrfachnennungen möglich) Mit Stern (*) gekennzeichnete Aufgaben sind für E2-Kandidaten [E2p-Kandidaten
Physikalische Chemie 0 Klausur, 22. Oktober 2011
 Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
Physikalische Chemie 0 Klausur, 22. Oktober 2011 Bitte beantworten Sie die Fragen direkt auf dem Blatt. Auf jedem Blatt bitte Name, Matrikelnummer und Platznummer angeben. Zu jeder der 25 Fragen werden
f) Ideales Gas - mikroskopisch
 f) Ideales Gas - mikroskopisch i) Annahmen Schon gehabt: Massenpunkte ohne Eigenvolumen Nur elastische Stöße, keine Wechselwirkungen Jetzt dazu: Wände vollkommen elastisch, perfekte Reflektoren Zeitliches
f) Ideales Gas - mikroskopisch i) Annahmen Schon gehabt: Massenpunkte ohne Eigenvolumen Nur elastische Stöße, keine Wechselwirkungen Jetzt dazu: Wände vollkommen elastisch, perfekte Reflektoren Zeitliches
Thermodynamik Hauptsatz
 Thermodynamik. Hauptsatz Inhalt Wärmekraftmaschinen / Kälteprozesse. Hauptsatz der Thermodynamik Reversibilität Carnot Prozess Thermodynamische Temperatur Entropie Entropiebilanzen Anergie und Exergie
Thermodynamik. Hauptsatz Inhalt Wärmekraftmaschinen / Kälteprozesse. Hauptsatz der Thermodynamik Reversibilität Carnot Prozess Thermodynamische Temperatur Entropie Entropiebilanzen Anergie und Exergie
Grundlagen der Physik 2 Schwingungen und Wärmelehre Othmar Marti.
 (c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
(c) Ulm University p. 1/1 Grundlagen der Physik 2 Schwingungen und Wärmelehre 14. 05. 2007 Othmar Marti othmar.marti@uni-ulm.de Institut für Experimentelle Physik Universität Ulm (c) Ulm University p.
Physik 2 ET, SoSe 2013 Aufgaben mit Lösung 3. Übung (KW 19/20) Temperaturen ) Dampfmaschine )
 3. Übung (KW 19/20) Aufgabe 1 (T 4.1 Temperaturen ) Zwischen den beiden Wärmespeichern einer Carnot-Maschine (Wirkungsgrad η) besteht eine Temperaturdifferenz T. Welche Temperaturen und T t haben die beiden
3. Übung (KW 19/20) Aufgabe 1 (T 4.1 Temperaturen ) Zwischen den beiden Wärmespeichern einer Carnot-Maschine (Wirkungsgrad η) besteht eine Temperaturdifferenz T. Welche Temperaturen und T t haben die beiden
Thermodynamik I Formeln
 Thermodynamik I Formeln Tobi 4. September 2006 Inhaltsverzeichnis Thermodynamische Systeme 3. Auftriebskraft........................................ 3 2 Erster Hauptsatz der Thermodynamik 3 2. Systemenergie........................................
Thermodynamik I Formeln Tobi 4. September 2006 Inhaltsverzeichnis Thermodynamische Systeme 3. Auftriebskraft........................................ 3 2 Erster Hauptsatz der Thermodynamik 3 2. Systemenergie........................................
Höhere Experimentalphysik 1
 Höhere Experimentalphysik 1 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 9. Vorlesung 20.01.2017 Was bisher geschah Thermodynamik Thermodynamische Systeme und Zustandsgrößen Gleichgewichtszustand
Höhere Experimentalphysik 1 Institut für Angewandte Physik Goethe-Universität Frankfurt am Main 9. Vorlesung 20.01.2017 Was bisher geschah Thermodynamik Thermodynamische Systeme und Zustandsgrößen Gleichgewichtszustand
4 Thermodynamik mikroskopisch: kinetische Gastheorie makroskopisch: System:
 Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Theorie der Wärme kann auf zwei verschiedene Arten behandelt werden. mikroskopisch: Bewegung von Gasatomen oder -molekülen. Vielzahl von Teilchen ( 10 23 ) im Allgemeinen nicht vollständig beschreibbar
Hochschule Düsseldorf University of Applied Sciences. 13. April 2016 HSD. Energiespeicher. Thermodynamik
 13. April 2016 Energiespeicher Thermodynamik Prof. Dr. Alexander Braun // Energiespeicher // SS 2016 26. April 2017 Thermodynamik Grundbegriffe Prof. Dr. Alexander Braun // Energiespeicher // SS 2017 26.
13. April 2016 Energiespeicher Thermodynamik Prof. Dr. Alexander Braun // Energiespeicher // SS 2016 26. April 2017 Thermodynamik Grundbegriffe Prof. Dr. Alexander Braun // Energiespeicher // SS 2017 26.
1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen
 IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
IV. Wärmelehre 1. Wärme und der 1. Hauptsatz der Thermodynamik 1.1. Grundlagen Historisch: Wärme als Stoff, der übertragen und in beliebiger Menge erzeugt werden kann. Übertragung: Wärmezufuhr Joulesche
Isotherme 3. 4 Adiabate 2 T 1. Adiabate Isotherme T 2. Arbeit nach außen = eingeschlossene Kurve
 Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
Carnotscher Kreisprozess Carnot Maschine = idealisierte Maschine, experimentell nicht gut zu realisieren. Einfacher Kreisprozess aus zwei isothermen und zwei adiabatischen Zustandsänderungen. Arbeit nach
PN 1 Einführung in die Experimentalphysik für Chemiker und Biologen
 PN 1 Einführung in die Experimentalphysik für Chemiker und Biologen 26.1.2007 Paul Koza, Nadja Regner, Thorben Cordes, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 1 Einführung in die Experimentalphysik für Chemiker und Biologen 26.1.2007 Paul Koza, Nadja Regner, Thorben Cordes, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Grundlagen der Physik 3 Lösung zu Übungsblatt 1
 Grundlagen der Physik 3 Lösung zu Übungsblatt Daniel Weiss 0. Oktober 200 Inhaltsverzeichnis Aufgabe - Anzahl von Atomen und Molekülen a) ohlensto..................................... 2 b) Helium.......................................
Grundlagen der Physik 3 Lösung zu Übungsblatt Daniel Weiss 0. Oktober 200 Inhaltsverzeichnis Aufgabe - Anzahl von Atomen und Molekülen a) ohlensto..................................... 2 b) Helium.......................................
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen!
 1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
1. Klausur ist am 5.12.! Jetzt lernen! Klausuranmeldung: Bitte heute in Listen eintragen! Aggregatzustände Fest, flüssig, gasförmig Schmelz -wärme Kondensations -wärme Die Umwandlung von Aggregatzuständen
Carnotscher Kreisprozess
 Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
Carnotscher Kreisprozess (idealisierter Kreisprozess) 2 p 1, V 1, T 1 p(v) dv > 0 p 2, V 2, T 1 Expansionsarbeit wird geleistet dq fließt aus Wärmebad zu dq > 0 p 2, V 2, T 1 p(v) dv > 0 p 3, V 3, T 2
E2: Wärmelehre und Elektromagnetismus 8. Vorlesung
 E2: Wärmelehre und Elektromagnetismus 8. Vorlesung 3.5.2018 Heute: - Boltzmann-Verteilung - Wärmekraftmaschinen - Carnot-Prozess und Wirkungsgrad - Kraftwärmemaschinen Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de
E2: Wärmelehre und Elektromagnetismus 8. Vorlesung 3.5.2018 Heute: - Boltzmann-Verteilung - Wärmekraftmaschinen - Carnot-Prozess und Wirkungsgrad - Kraftwärmemaschinen Prof. Dr. Jan Lipfert Jan.Lipfert@lmu.de
1. Wärmelehre 1.1. Temperatur Wiederholung
 1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
1. Wärmelehre 1.1. Temperatur Wiederholung a) Zur Messung der Temperatur verwendet man physikalische Effekte, die von der Temperatur abhängen. Beispiele: Volumen einer Flüssigkeit (Hg-Thermometer), aber
Ferienkurs Experimentalphysik IV
 Ferienkurs Experimentalphysik IV Michael Mittermair, Daniel Jost 04.09.14 Inhaltsverzeichnis 1 Moleküle 2 1.1 Das H + 2 Molekül-Ion....................... 2 1.2 Näherungen............................ 3
Ferienkurs Experimentalphysik IV Michael Mittermair, Daniel Jost 04.09.14 Inhaltsverzeichnis 1 Moleküle 2 1.1 Das H + 2 Molekül-Ion....................... 2 1.2 Näherungen............................ 3
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene)
 Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Das Ideale Gas Kinetische Gastheorie (auf atomarer Ebene) Wir haben gesehen, dass ein sogenanntes 'ideales Gas' durch die Zustandsgleichung pv = νr T [1] beschrieben wird; wir wollen nun verstehen, welchen
Physik 2 ET, SoSe 2013 Aufgaben mit Lösung 2. Übung (KW 17/18)
 2. Übung (KW 17/18) Aufgabe 1 (T 3.1 Sauerstoffflasche ) Eine Sauerstoffflasche, die das Volumen hat, enthält ab Werk eine Füllung O 2, die bei Atmosphärendruck p 1 das Volumen V 1 einnähme. Die bis auf
2. Übung (KW 17/18) Aufgabe 1 (T 3.1 Sauerstoffflasche ) Eine Sauerstoffflasche, die das Volumen hat, enthält ab Werk eine Füllung O 2, die bei Atmosphärendruck p 1 das Volumen V 1 einnähme. Die bis auf
Experimentalphysik II: Thermodynamik
 Exerimentalhysik II: Thermodynamik Zweitversuch-Ferienkurs Sommersemester 09 William Hefter 11/09/2009 Inhaltsverzeichnis 1 Temeratur, Wärme und Arbeit 2 1.1 Einschub zur mathematischen Schreibweise.........................
Exerimentalhysik II: Thermodynamik Zweitversuch-Ferienkurs Sommersemester 09 William Hefter 11/09/2009 Inhaltsverzeichnis 1 Temeratur, Wärme und Arbeit 2 1.1 Einschub zur mathematischen Schreibweise.........................
! #!! % & ( )! ! +, +,# # !.. +, ) + + /) # %
 ! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
! #! #!! % & ( )!! +, +,# #!.. +, ) + + /)!!.0. #+,)!## 2 +, ) + + 3 4 # )!#!! ), 5 # 6! # &!). ) # )!#! #, () # # ) #!# #. # ) 6 # ) )0 4 )) #, 7) 6!!. )0 +,!# +, 4 / 4, )!#!! ))# 0.(! & ( )!! 8 # ) #+,
11.2 Die absolute Temperatur und die Kelvin-Skala
 11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
11. Die absolute Temperatur und die Kelvin-Skala p p 0 Druck p = p(t ) bei konstantem olumen 1,0 0,5 100 50 0-50 -100-150 -00-73 T/ C Tripelpunkt des Wassers: T 3 = 73,16 K = 0,01 C T = 73,16 K p 3 p Windchill-Faktor
2 Wärmelehre. Reibungswärme Reaktionswärme Stromwärme
 2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
2 Wärmelehre Die Thermodynamik ist ein Musterbeispiel an axiomatisch aufgebauten Wissenschaft. Im Gegensatz zur klassischen Mechanik hat sie die Quantenrevolution überstanden, ohne in ihren Grundlagen
d) Das ideale Gas makroskopisch
 d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
d) Das ideale Gas makroskopisch Beschreibung mit Zustandsgrößen p, V, T Brauchen trotzdem n, R dazu Immer auch Mikroskopische Argumente dazunehmen Annahmen aus mikroskopischer Betrachtung: Moleküle sind
PC-Übung Nr.3 vom
 PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
PC-Übung Nr.3 vom 31.10.08 Sebastian Meiss 25. November 2008 1. Die Säulen der Thermodynamik Beantworten Sie folgende Fragen a) Welche Größen legen den Zustand eines Gases eindeutig fest? b) Welche physikalischen
Vorlesung Physik für Pharmazeuten PPh Wärmelehre
 Vorlesung Physik für Pharmazeuten PPh - 07 Wärmelehre Aggregatzustände der Materie im atomistischen Bild Beispiel Wasser Eis Wasser Wasserdampf Dynamik an der Wasser-Luft Grenzfläche im atomistischen Bild
Vorlesung Physik für Pharmazeuten PPh - 07 Wärmelehre Aggregatzustände der Materie im atomistischen Bild Beispiel Wasser Eis Wasser Wasserdampf Dynamik an der Wasser-Luft Grenzfläche im atomistischen Bild
PC-Übung Nr.1 vom
 PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
PC-Übung Nr.1 vom 17.10.08 Sebastian Meiss 25. November 2008 1. Allgemeine Vorbereitung a) Geben Sie die Standardbedingungen in verschiedenen Einheiten an: Druck p in Pa, bar, Torr, atm Temperatur T in
T p = T = RT. V b. ( ) 2 V p. V b. 2a(V b)2 V 3 RT. 2a(V b) V 3 (p+ a V 2 )
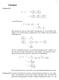 3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
3 Lösung zu 83. Lösungen ( C C = T ( = T ( ( ( 2 van-der-waals Gas: ( ( b + a 2 = T = T b a 2 Man beachte das dies nur eine andere Formulierung der van-der-waals Gleichung ist als auf dem letzten Aufgabenzettel.
4.6 Hauptsätze der Thermodynamik
 Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Thermodynamik.6 Hautsätze der Thermodynamik.6. Erster Hautsatz: Energieerhaltungssatz In einem abgeschlossenen System bleibt der gesamte Energievorrat, also die Summe aus Wärmeenergie, mechanischer Energie
Erster und Zweiter Hauptsatz
 PN 1 Einführung in die alphysik für Chemiker und Biologen 26.1.2007 Paul Koza, Nadja Regner, Thorben Cordes, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
PN 1 Einführung in die alphysik für Chemiker und Biologen 26.1.2007 Paul Koza, Nadja Regner, Thorben Cordes, Peter Gilch Lehrstuhl für BioMolekulare Optik Department für Physik Ludwig-Maximilians-Universität
Stickstoff kann als ideales Gas betrachtet werden mit einer spezifischen Gaskonstante von R N2 = 0,297 kj
 Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Aufgabe 4 Zylinder nach oben offen Der dargestellte Zylinder A und der zugehörige bis zum Ventil reichende Leitungsabschnitt enthalten Stickstoff. Dieser nimmt im Ausgangszustand ein Volumen V 5,0 dm 3
Entropie und 2. Hauptsatz der Thermodynamik
 Entropie und 2. Hauptsatz der hermodynamik Seminar Didaktik der Physik Datum: 20.11.1006 LV-Nummer: 706099 Vortragende: Markus Kaldinazzi Mathias Scherl Inhalte Reversible und Irreversible Prozesse Drei
Entropie und 2. Hauptsatz der hermodynamik Seminar Didaktik der Physik Datum: 20.11.1006 LV-Nummer: 706099 Vortragende: Markus Kaldinazzi Mathias Scherl Inhalte Reversible und Irreversible Prozesse Drei
NTB Druckdatum: DWW
 WÄRMELEHRE Der Begriff der Thermisches Gleichgewicht und - Mass für den Wärmezustand eines Körpers - Bewegung der Atome starke Schwingung schwache Schwingung gleichgewicht (Thermisches Gleichgewicht) -
WÄRMELEHRE Der Begriff der Thermisches Gleichgewicht und - Mass für den Wärmezustand eines Körpers - Bewegung der Atome starke Schwingung schwache Schwingung gleichgewicht (Thermisches Gleichgewicht) -
Physik für Biologen und Zahnmediziner
 Physik für Biologen und Zahnmediziner Kapitel 11: Wärmelehre Dr. Daniel Bick 13. Dezember 2017 Daniel Bick Physik für Biologen und Zahnmediziner 13. Dezember 2017 1 / 36 Übersicht 1 Wellen 2 Wärmelehre
Physik für Biologen und Zahnmediziner Kapitel 11: Wärmelehre Dr. Daniel Bick 13. Dezember 2017 Daniel Bick Physik für Biologen und Zahnmediziner 13. Dezember 2017 1 / 36 Übersicht 1 Wellen 2 Wärmelehre
Thermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden.
 Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Wärmemenge: hermische Energie kann nicht mehr beliebig in andere Energieformen umgewandelt werden. Sie kann aber unter gewissen oraussetzungen von einem Körer auf einen nderen übertragen werden. Dabei
Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc.
 Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc. Angaben zur Person: (bitte leserlich und in Druckbuchstaben) Name, Vorname: Geburtsdatum und ort: Matrikelnummer: Studienfach,
Musterlösung Übungsklausur zur Vorlesung PC I Chemische Thermodynamik B.Sc. Angaben zur Person: (bitte leserlich und in Druckbuchstaben) Name, Vorname: Geburtsdatum und ort: Matrikelnummer: Studienfach,
v(t) = r(t) v(t) = a(t) = Die Kraft welche das Teilchen auf der Bahn hält muss entgegen dessen Trägheit wirken F = m a(t) E kin = m 2 v(t) 2
 Aufgabe 1 Mit: und ( x r(t) = = y) ( ) A sin(ωt) B cos(ωt) v(t) = r(t) t a(t) = 2 r(t) t 2 folgt nach komponentenweisen Ableiten ( ) Aω cos(ωt) v(t) = Bω sin(ωt) a(t) = ( ) Aω2 sin(ωt) Bω 2 cos(ωt) Die
Aufgabe 1 Mit: und ( x r(t) = = y) ( ) A sin(ωt) B cos(ωt) v(t) = r(t) t a(t) = 2 r(t) t 2 folgt nach komponentenweisen Ableiten ( ) Aω cos(ωt) v(t) = Bω sin(ωt) a(t) = ( ) Aω2 sin(ωt) Bω 2 cos(ωt) Die
2 Grundbegriffe der Thermodynamik
 2 Grundbegriffe der Thermodynamik 2.1 Thermodynamische Systeme (TDS) Aufteilung zwischen System und Umgebung (= Rest der Welt) führt zu einer Klassifikation der Systeme nach Art der Aufteilung: Dazu: adiabatisch
2 Grundbegriffe der Thermodynamik 2.1 Thermodynamische Systeme (TDS) Aufteilung zwischen System und Umgebung (= Rest der Welt) führt zu einer Klassifikation der Systeme nach Art der Aufteilung: Dazu: adiabatisch
Ferienkurs Experimentalphysik IV
 Ferienkurs Experimentalphysik IV Übung 4 Michael Mittermair und Daniel Jost 03.09.14 Aufgabe 1 Ein HCl-Molekül kann sowohl zu Schwingungen als auch zu Rotationen angeregt werden. Die Energie der Schwingungs-Rotations-Zustände
Ferienkurs Experimentalphysik IV Übung 4 Michael Mittermair und Daniel Jost 03.09.14 Aufgabe 1 Ein HCl-Molekül kann sowohl zu Schwingungen als auch zu Rotationen angeregt werden. Die Energie der Schwingungs-Rotations-Zustände
