LISA I RAVIMI OMADUSTE KOKKUVÕTE
|
|
|
- Krista Haupt
- vor 6 Jahren
- Abrufe
Transkript
1 LISA I RAVIMI OMADUSTE KOKKUVÕTE 1
2 1. VETERINAARRAVIMI NIMETUS ECOPORC SHIGA süstesuspensioon sigadele 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Iga 1 ml annus sisaldab: Toimeaine: Geneetiliselt modifitseeritud rekombinantne Stx2e antigeen: 3, ELISA ühikut Adjuvant: Alumiiniumhüdroksiid max 3,5 mg Abiaine: Tiomersaal max 0,115 mg Abiainete täielik loetelu on esitatud punktis RAVIMVORM Süstesuspensioon. Välimus pärast raputamist: kollakas kuni pruunikas homogeenne suspensioon. 4. KLIINILISED ANDMED 4.1. Loomaliigid Sead Näidustused, määrates kindlaks vastavad loomaliigid Põrsaste aktiivne immuniseerimine alates 4. elupäevast, et vähendada E. coli (STEC) toodetava Stx2e toksiini põhjustatavast tursetõvest tingitud suremust ja kliinilisi sümptomeid. Immuunsuse algus: Immuunsuse kestus: 21 päeva pärast vaktsineerimist 105 päeva pärast vaktsineerimist 4.3. Vastunäidustused Mitte kasutada, kui esineb ülitundlikkust toimeaine, adjuvandi või ravimi ükskõik millise abiaine suhtes Erihoiatused iga loomaliigi kohta Vaktsineerige vaid terveid loomi. 2
3 4.5. Ettevaatusabinõud Ettevaatusabinõud kasutamisel loomadel Ei rakendata. Ettevaatusabinõud veterinaarravimit loomale manustavale isikule Juhuslikul ravimi süstimisel iseendale või allaneelamisel pöörduda viivitamatult arsti poole ja näidata pakendi infolehte või pakendi etiketti Kõrvaltoimed (sagedus ja tõsidus) Sagedasti võib täheldada väga väikeseid paikseid reaktsioone, nagu süstekoha kerge paistetus (maksimaalselt 5 mm), kuid need reaktsioonid on mööduvad ja kaovad lühikese aja jooksul (kuni seitse päeva) ravita. Kliinilisi sümptomeid, nagu ajutised kerged käitumishäired, võib ECOPORC SHIGA manustamise järgselt täheldada aeg-ajalt. Sagedasti võib pärast süstimist tekkida kehatemperatuuri kerge tõus (maksimaalselt 1,7 C). Need reaktsioonid mööduvad lühikese aja jooksul (maksimaalselt kaks päeva) ravita. Kõrvaltoimete esinemissagedus on defineeritud järgnevalt: - Väga sage (ühe ravikuuri jooksul ilmnes(id) kõrvaltoime(d) rohkem kui 1-l 10 looma hulgast) - Sage (rohkem kui 1-l, kuid vähem kui 10 loomal 100-st) - Aeg-ajalt (rohkem kui 1-l, kuid vähem kui 10-l loomal 1000-st) - Harv (rohkem kui 1-l, kuid vähem kui 10 loomal 10,000-st) - Väga harv (vähem kui 1-l loomal 10,000-st, kaasaarvatud harva esinevad üksikjuhud) Kasutamine tiinuse, laktatsiooni või munemise perioodil Veterinaarravimi ohutus tiinuse ja laktatsiooni ajal ei ole piisavalt tõestatud Koostoimed teiste ravimitega ja muud koostoimed Andmed vaktsiini ohutuse ja efektiivsuse kohta selle kasutamisel koos teiste veterinaarravimitega puuduvad. Seetõttu peab otsuse selle vaktsiini kasutamise kohta enne või pärast mistahes muud veterinaarravimit tegema vastutav veterinaararst igal erineval juhul eraldi Annustamine ja manustamisviis Intramuskulaarseks kasutuseks. Soovituslik manustamiskoht on kõrvatagune kaelalihas. Soovitatav on kasutada põrsaste vanusele vastavat nõela (soovituslik suurus 21 G ja pikkus 16 mm). Enne manustamist raputage vaktsiini ettevaatlikult. Üks intramuskulaarne süst (1- ml) sigadele alates 4. elupäevast Üleannustamine (sümptomid, esmaabi, antidoodid), vajadusel Pärast vaktsiini topeltannuse manustamist ei täheldatud mingeid muid kõrvaltoimeid peale jaotises 4.6 mainitute Keeluaeg 0 päeva. 3
4 5. IMMUNOLOOGILISED OMADUSED Farmakoterapeutiline rühm: immunoloogilised ained sigalastele, inaktiveeritud baktervaktsiinid. ATCvet kood: QI09AB02 Geneetiliselt modifitseeritud rekombinantsest Stx2e-st koosnev vaktsiin stimuleerib sigade tursetõve tekitaja toodetava Shiga toksiini 2e vastast aktiivset immuunsust. 6. FARMATSEUTILISED ANDMED 6.1. Abiainete loetelu Alumiiniumhüdroksiid (Al(OH) 3 ) Tiomersaal Süstevesi Glutaaraldehüüd 6.2. Sobimatus Mitte segada teiste veterinaarravimitega Kõlblikkusaeg Müügipakendis veterinaarravimi kõlblikkusaeg: 18 kuud Kõlblikkusaeg pärast vahetu pakendi esmast avamist: 24 tundi Kasutuskordade vahel tuleb vaktsiini hoida temperatuuril 2 C - 8 C Säilitamise eritingimused Hoida külmkapis (2 C - 8 C). Mitte külmutada. Hoida valguse eest kaitstult Vahetu pakendi iseloomustus ja koostis Bromobutüülkummist korgiga suletud ja alumiiniumist ärarebitava korgiga tihendatud 50 või 100 ml ravimit sisaldav PET-pudel. Pakendi suurused Ühte 50-annuselist (50 ml) või 100-annuselist (100 ml) PET-pudelit sisaldav pappkarp. Kõik pakendi suurused ei pruugi olla müügil Erinõuded ettevaatusabinõude osas kasutamata jäänud veterinaarravimite või nende kasutamisest tekkinud jäätmete hävitamisel Kasutamata veterinaarravim või selle jäätmed tuleb hävitada vastavalt kohalikule seadusandlusele. 4
5 7. MÜÜGILOA HOIDJA IDT Biologika GmbH Am Pharmapark Dessau-Rosslau Saksamaa 8. MÜÜGILOA NUMBER EU/2/13/149/001 EU/2/13/149/ ESMASE MÜÜGILOA VÄLJASTAMISE / MÜÜGILOA UUENDAMISE KUUPÄEV Esmase müügiloa väljastamise kuupäev: {pp/kk/aaaa} 10. TEKSTI LÄBIVAATAMISE KUUPÄEV {kk/aaaa} Üksikasjalikku teavet antud veterinaarravimi kohta leiab Euroopa Ravimiameti koduleheküljelt TOOTMISE, IMPORDI, OMAMISE, MÜÜGI, TARNIMISE JA/VÕI KASUTAMISE KEELD Ei rakendata. 5
6 LISA II A. BIOLOOGILISE TOIMEAINE TOOTJAJA RAVIMIPARTII KASUTAMISEKS VABASTAMISE EEST VASTUTAVTOOTJA B. HANKE- JA KASUTAMISTINGIMUSED VÕI PIIRANGUD C. RAVIMJÄÄKIDE PIIRNORMID 6
7 A. BIOLOOGILISE TOIMEAINE TOOTJA JA RAVIMIPARTII KASUTAMISEKS VABASTAMISE EEST VASTUTAV AD TOOTJA Bioloogilise toimeaine tootja nimi ja aadress IDT Biologika GmbH Am Pharmapark Dessau-Rosslau Saksamaa Ravimipartii kasutamiseks vabastamise eest vastutava tootja nimi ja aadress IDT Biologika GmbH Am Pharmapark Dessau-Rosslau Saksamaa B. HANKE- JA KASUTAMISTINGIMUSED VÕI PIIRANGUD Retseptiravim. C. RAVIMJÄÄKIDE PIIRNORMID Toimeaine, mis põhimõtteliselt on bioloogilist päritolu on mõeldud aktiivse immuunsuse tekitamiseks, ei kuulu määruse (EÜ) nr 470/2009 reguleerimisalasse. Abiained mis on loetletud punktis 6.1 on lubatud ained, mis vastavalt Komisjoni määruse (EL) nr 37/2010 tabelile 1 ei vaja jääkide piirnorme. 7
8 III LISA PAKENDI MÄRGISTUS JA PAKENDI INFOLEHT 8
9 A. PAKENDI MÄRGISTUS 9
10 VÄLISPAKENDIL JA SISEPAKENDIL Pappkarp (ühe 50 ml või 100 ml PET-pudeliga) 1. VETERINAARRAVIMI NIMETUS ECOPORC SHIGA süstesuspensioon sigadele 2. TOIMEAINE JA ABIAINETE SISALDUS 1 annus (1 ml) sisaldab: geneetiliselt modifitseeritud rekombinantne Stx2e antigeen: 3, ELISA ühikut 3. RAVIMVORM Süstesuspensioon 4. PAKENDI SUURUS 50 ml (50 annust) 100 ml (100 annust) 5. LOOMALIIGID Sead 6. NÄIDUSTUS 7. MANUSTAMISVIIS JA -TEE Intramuskulaarseks kasutuseks. Enne kasutamist raputada hoolikalt. Enne ravimi kasutamist lugege pakendi infolehte. 8. KEELUAEG Keeluaeg: 0 päeva 9. ERIHOIATUS(ED), KUI VAJALIK Enne ravimi kasutamist lugege pakendi infolehte. 10
11 10. KÕLBLIKKUSAEG EXP Pärast avamist kasutada 24 tunni jooksul (hoida temperatuuril 2 8 C). 11. SÄILITAMISE ERITINGIMUSED Hoida külmkapis. Mitte hoida sügavkülmas. Hoida valguse eest kaitstult. 12. ERINÕUDED ETTEVAATUSABINÕUDE OSAS KASUTAMATA JÄÄNUD PREPARAADI VÕI JÄÄTMETE HÄVITAMISEL, KUI NEED ON KEHTESTATUD Hävitamine: vt pakendi infolehte. 13. MÄRGE AINULT VETERINAARSEKS KASUTAMISEKS NING TINGIMUSED VÕI PIIRANGUD TARNIMISE JA KASUTAMISE OSAS, KUI NEED ON KOHALDATAVAD Ainult veterinaarseks kasutamiseks. Retseptiravim. 14. MÄRGE HOIDA LASTE EEST VARJATUD JA KÄTTESAAMATUS KOHAS Hoida laste eest varjatud ja kättesaamatus kohas. 15. MÜÜGILOA HOIDJA NIMI JA AADRESS IDT Biologika GmbH Am Pharmapark Dessau-Rosslau Saksamaa 16. MÜÜGILOA NUMBER (NUMBRID) EU/2/13/149/001 PET pudeli 50 ml EU/2/13/149/002 PET pudeli 100 ml 17. TOOTJAPOOLNE PARTII NUMBER Lot 11
12 KONTAKTPAKENDIL OLEVAD ÜKSIKASJAD 100 ml 1. VETERINAARRAVIMI NIMETUS ECOPORC SHIGA süstesuspensioon sigadele 2. TOIMEAINE JA ABIAINETE SISALDUS 1 annus (1 ml) sisaldab: geneetiliselt modifitseeritud rekombinantne Stx2e antigeen: 3, ELISA ühikut 3. RAVIMVORM Süstesuspensioon 4. PAKENDI SUURUS 100 annust 5. LOOMALIIGID Sead 6. NÄIDUSTUS 7. MANUSTAMISVIIS JA -TEE Intramuskulaarseks kasutuseks. Enne kasutamist raputada hoolikalt. Enne ravimi kasutamist lugege pakendi infolehte. 8. KEELUAEG Keeluaeg: 0 päeva 9. ERIHOIATUS(ED), KUI VAJALIK Enne ravimi kasutamist lugege pakendi infolehte. 12
13 10. KÕLBLIKKUSAEG EXP Pärast avamist kasutada 24 tunni jooksul (hoida temperatuuril 2 8 C). 11. SÄILITAMISE ERITINGIMUSED Hoida külmkapis. Mitte hoida sügavkülmas. Hoida valguse eest kaitstult. 12. ERINÕUDED ETTEVAATUSABINÕUDE OSAS KASUTAMATA JÄÄNUD PREPARAADI VÕI JÄÄTMETE HÄVITAMISEL, KUI NEED ON KEHTESTATUD 13. MÄRGE AINULT VETERINAARSEKS KASUTAMISEKS NING TINGIMUSED VÕI PIIRANGUD TARNIMISE JA KASUTAMISE OSAS, KUI NEED ON KOHALDATAVAD Ainult veterinaarseks kasutamiseks. Retseptiravim. 14. MÄRGE HOIDA LASTE EEST VARJATUD JA KÄTTESAAMATUS KOHAS Hoida laste eest varjatud ja kättesaamatus kohas. 15. MÜÜGILOA HOIDJA NIMI JA AADRESS IDT Biologika GmbH Am Pharmapark Dessau-Rosslau Saksamaa 16. MÜÜGILOA NUMBER (NUMBRID) EU/2/13/149/002 PET pudeli 17. TOOTJAPOOLNE PARTII NUMBER Lot: 13
14 MINIMAALSED ANDMED, MIS PEAVAD OLEMA VÄIKESEL VAHETUL SISEPAKENDIL 50 ml 1. VETERINAARRAVIMI NIMETUS ECOPORC SHIGA süstesuspensioon sigadele 2. TOIMEAINE KOGUS Geneetiliselt modifitseeritud rekombinantne Stx2e antigeen: 3, ELISA ühikut 3. PAKENDI SISU KAALU, MAHU VÕI ANNUSTE ARVU JÄRGI 50 annust 4. MANUSTAMISVIIS Intramuskulaarseks kasutuseks 5. KEELUAEG Keeluaeg: 0 päeva 6. PARTII NUMBER Lot 7. KÕLBLIKKUSAEG EXP 8. MÄRGE AINULT VETERINAARSEKS KASUTAMISEKS Ainult veterinaarseks kasutamiseks. 14
15 B. PAKENDI INFOLEHT 15
16 PAKENDI INFOLEHT ECOPORC SHIGA Süstesuspensioon sigadele 1. MÜÜGILOA HOIDJA NING, KUI NEED EI KATTU, RAVIMIPARTII VABASTAMISE EEST VASTUTAVA TOOTMISLOA HOIDJA NIMI JA AADRESS Müügiloa hoidja ja partii vabastamise eest vastutav tootja: IDT Biologika GmbH Am Pharmapark Dessau-Rosslau Saksamaa 2. VETERINAARRAVIMI NIMETUS ECOPORC SHIGA Süstesuspensioon sigadele Välimus pärast raputamist: kollakas kuni pruunikas homogeenne suspensioon 3. TOIMEAINETE JA ABIAINETE SISALDUS Iga 1 ml annus sisaldab: Toimeained: Geneetiliselt modifitseeritud rekombinantne Stx2e antigeen: 3, ELISA ühikut Adjuvant: Alumiiniumhüdroksiid Abiaine: Tiomersaal max 3,5 mg max 0,115 mg 4. NÄIDUSTUS Põrsaste aktiivne immuniseerimine alates 4. elupäevast, et vähendada E. coli (STEC) toodetava Stx2e toksiini põhjustatavast tursetõvest tingitud suremust ja kliinilisi sümptomeid. Immuunsuse algus: Immuunsuse kestus: 21 päeva pärast vaktsineerimist 105 päeva pärast vaktsineerimist 5. VASTUNÄIDUSTUSED Mitte kasutada, kui esineb ülitundlikkust toimeaine, adjuvandi või ravimi ükskõik millise abiaine suhtes. 16
17 6. KÕRVALTOIMED Sagedasti võib täheldada väga väikeseid paikseid reaktsioone, nagu süstekoha kerge paistetus (maksimaalselt 5 mm), kuid need reaktsioonid on mööduvad ja kaovad lühikese aja jooksul (kuni seitse päeva) ravita. Kliinilisi sümptomeid, nagu ajutised kerged käitumishäired, võib ECOPORC SHIGA manustamise järgselt täheldada aeg-ajalt. Sagedasti võib pärast süstimist tekkida kehatemperatuuri kerge tõus (maksimaalselt 1,7 C). Need reaktsioonid mööduvad lühikese aja jooksul (maksimaalselt kaks päeva) ravita. Kõrvaltoimete esinemissagedus on defineeritud järgnevalt: - väga sage (ühe ravikuuri jooksul ilmnes(id) kõrvaltoime(d) rohkem kui 1-l loomal 10 looma hulgast) - sage (rohkem kui 1-l, kuid vähem kui 10 loomal 100-st) - aeg-ajalt (rohkem kui 1-l, kuid vähem kui 10-l loomal 1000-st) - harv (rohkem kui 1-l, kuid vähem kui 10 loomal 10,000-st) - väga harv (vähem kui 1-l loomal 10,000-st, kaasaarvatud harva esinevad üksikjuhud). Kui täheldate tõsiseid kõrvaltoimeid või muid toimeid, mida pole käesolevas pakendi infolehes mainitud, palun teavitage sellest oma veterinaararsti. 7. LOOMALIIGID Sead 8. ANNUSTAMINE LOOMALIIGITI, MANUSTAMISVIIS JA MEETOD Enne manustamist raputage vaktsiini ettevaatlikult. Üks intramuskulaarne süst (1 ml) sigadele alates 4. elupäevast. Soovituslik manustamiskoht on kõrvatagune kaelalihas. 9. SOOVITUSED ÕIGE MANUSTAMISE OSAS Soovitatav on kasutada põrsaste vanusele vastavat nõela (soovituslik suurus 21 G ja pikkus 16 mm). 10. KEELUAEG 0 päeva. 11. SÄILITAMISE ERITINGIMUSED Hoida laste eest varjatud ja kättesaamatus kohas. Hoida külmkapis (2 C - 8 C). Mitte hoida sügavkülmas. Hoida valguse eest kaitstult. Kõlblikkusaeg pärast mahuti esmast avamist: 24 tundi (hoida temperatuuril 2-8 C). Ärge kasutage seda ravimit pärast kõlblikkusaega, mis on märgitud sildil karbil. Kõlblikkusaeg pärast pakendi esmast avamist. 17
18 12. ERIHOIATUSED Ettevaatusabinõud kasutamisel loomadel: vaktsineerige vaid terveid loomi. Ettevaatusabinõud veterinaarravimit loomale manustavale isikule: juhuslikul ravimi süstimisel iseendale või allaneelamisel pöörduda viivitamatult arsti poole ja näidata pakendi infolehte või pakendi etiketti. Kasutamine tiinuse ja laktatsiooni ajal: veterinaarravimi ohutus tiinuse või laktatsiooni ajal ei ole piisavalt tõestatud. Koostoimed teiste ravimitega ja muud koostoimed: Andmed vaktsiini ohutuse ja efektiivsuse kohta selle kasutamisel koos teiste veterinaarravimitega puuduvad. Seetõttu peab otsuse selle vaktsiini kasutamise kohta enne või pärast mis tahes muud veterinaarravimit tegema vastutav veterinaararst igal erineval juhul eraldi. Mitte segada teiste veterinaarravimitega. Üleannustamine (sümptomid, esmaabi, antidoodid): pärast vaktsiini topeltannuse manustamist ei täheldatud mingeid muid kõrvaltoimeid peale jaotises 6 mainitute. 13. ERINÕUDED ETTEVAATUSABINÕUDE OSAS KASUTAMATA JÄÄNUD PREPARAADI VÕI NENDE JÄÄTMETE, KUI NEID TEKIB, HÄVITAMISEL Küsige palun oma loomaarstilt kuidas hävitatakse ravimeid, mida enam ei vajata. Need meetmed aitavad kaitsta keskkonda. 14. PAKENDI INFOLEHE VIIMASE KOOSKÕLASTAMISE KUUPÄEV Üksikasjalikku teavet antud veterinaarravimi kohta leiab Euroopa Ravimiameti koduleheküljelt LISAINFO Bromobutüülkummist korgiga suletud ja alumiiniumist ärarebitava korgiga tihendatud 50 või 100 ml ravimit sisaldav PET-pudel. Pakendi suurused Ühte 50-annuselist (50 ml) või 100-annuselist (100 ml) PET-pudelit sisaldav pappkarp. Kõik pakendi suurused ei pruugi olla müügil. Lisaküsimuste tekkimisel selle ravimi kohta pöörduge palun müügiloa hoidja kohaliku esindaja poole. 18
19 België/Belgique/Belgien {Nom/Naam/Name} <{Adresse/Adres/Anschrift } 0000 {Localité/Stad/Stadt}> Tél/Tel: + {N de téléphone/telefoonnummer/ Telefonnummer} Република България {Наименование} <{Адрес} {Град} {Пощенски код}> Teл: {Телефонен номер} Česká republika {Název} <{Adresa} {město}> Tel: +{telefonní číslo} Danmark {Navn} <{Adresse} 0000 {by}> Tlf: + {Telefonnummer} Deutschland {Name} <{Anschrift} {Stadt}> Tel: + {Telefonnummer} Eesti (Nimi) <(Aadress) (Postiindeks) (Linn)> Tel: +(Telefoninumber) Ελλάδα {Όνομα} <{Διεύθυνση} {πόλη}> Τηλ: + {Αριθμός τηλεφώνου} España {Nombre} <{Dirección} {Ciudad}> Tel: + {Teléfono} Luxembourg/Luxemburg {Nom} <{Adresse} 0000 {Localité/Stadt}> Tél/Tel: + {N de téléphone/telefonnummer} Magyarország {Név} <{Cím} 0000 {Város}> Tel.: + {Telefonszám} Malta {Isem} <{Indirizz} 0000 {Belt/Raħal}> Tel: + {Numru tat-telefon} Nederland {Naam} <{Adres} 0000 XX {stad}> Tel: + {Telefoonnummer} Norge {Navn} <{Adresse} 0000 {poststed}> Tlf: + {Telefonnummer} Österreich {Name} <{Anschrift} {Stadt}> Tel: + {Telefonnummer} Polska {Nazwa/ Nazwisko:} <{Adres:} {Miasto:}> Tel.: + {Numer telefonu:} Portugal {Nome} <{Morada} {Cidade}> Tel: + {Número de telefone} 19
20 France {Nom} <{Adresse} {Localité}> Tél: + {Numéro de téléphone} Ireland {Name} <{Address} {Town} {Code for Dublin}> Tel: + {Telephone number} Ísland {Nafn} <{Heimilisfang} 000 {Borg/Bær}> Sími: + {Símanúmer} <{Netfang}> Italia {Nome} <{Indirizzo} {Località}> Tel: + {Numero di telefono}> Κύπρος {Όνομα} <{Διεύθυνση} {πόλη}> Τηλ: + {Αριθμός τηλεφώνου} Latvija {Nosaukums} <{Adrese} {Pilsēta}, LV{Pasta indekss }> Tel: + {Telefona numurs} România {Nume} <{Adresă} {Oraş} {Cod poştal} RO> Tel: + {Număr de telefon} Slovenija {Ime} <{Naslov} {Mesto}> Tel: + {telefonska številka} Slovenská republika {Meno} <{Adresa} {Mesto}> Tel: + {Telefónne číslo} Suomi/Finland {Nimi/Namn} <{Osoite/Adress} {Postitoimipaikka/Stad}> Puh/Tel: + {Puhelinnumero/Telefonnummer} Sverige {Namn} <{Adress} {Stad}> Tel: + {Telefonnummer} United Kingdom {Name} <{Address} {Town} {Postal code} UK> Tel: + {Telephone number} Lietuva {pavadinimas} <{adresas} {pašto indeksas} {miestas}> Tel: +370{telefono numeris} 20
LISA I RAVIMI OMADUSTE KOKKUVÕTE
 LISA I RAVIMI OMADUSTE KOKKUVÕTE 1 1. VETERINAARRAVIMI NIMETUS ERAVAC süsteemulsioon küülikutele. 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Üks 0,5 ml annus sisaldab: Toimeained: Küülikute hemorraagilise
LISA I RAVIMI OMADUSTE KOKKUVÕTE 1 1. VETERINAARRAVIMI NIMETUS ERAVAC süsteemulsioon küülikutele. 2. KVALITATIIVNE JA KVANTITATIIVNE KOOSTIS Üks 0,5 ml annus sisaldab: Toimeained: Küülikute hemorraagilise
I LISA RAVIMI OMADUSTE KOKKUVÕTE
 I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 1. RAVIMPREPARAADI NIMETUS AFLUNOV süstesuspensioon eeltäidetud süstlis. Pre-pandeemiline gripiviiruse vaktsiin (H5N1) (pinnaantigeen, inaktiveeritud, adjuveeritud).
I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 1. RAVIMPREPARAADI NIMETUS AFLUNOV süstesuspensioon eeltäidetud süstlis. Pre-pandeemiline gripiviiruse vaktsiin (H5N1) (pinnaantigeen, inaktiveeritud, adjuveeritud).
GU BKS Access. Läbipääsukontrollisüsteemid ühe- ja mitmeukselistele süsteemidele. Üheukselised süsteemid
 TOOTEINFO GU BKS Access Läbipääsukontrollisüsteemid ühe- ja mitmeukselistele süsteemidele Üheukselised süsteemid Väljumiste loenduriga kombineeritud juhtimispult Läbipääsusüsteemi juhtimispult siseruumidele
TOOTEINFO GU BKS Access Läbipääsukontrollisüsteemid ühe- ja mitmeukselistele süsteemidele Üheukselised süsteemid Väljumiste loenduriga kombineeritud juhtimispult Läbipääsusüsteemi juhtimispult siseruumidele
PACKUNGSBEILAGE 3. ARZNEILICH WIRKSAME(R) BESTANDTEIL(E) UND SONSTIGE BESTANDTEILE
 Virbagen Omega 5 ME für Hunde und Katzen Virbagen Omega 10 ME für Hunde und Katzen PACKUNGSBEILAGE 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
Virbagen Omega 5 ME für Hunde und Katzen Virbagen Omega 10 ME für Hunde und Katzen PACKUNGSBEILAGE 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
GEBRAUCHSINFORMATION FÜR. Metacam 15 mg/ ml Suspension zum Eingeben für Pferde
 GEBRAUCHSINFORMATION FÜR Metacam 15 mg/ ml Suspension zum Eingeben für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
GEBRAUCHSINFORMATION FÜR Metacam 15 mg/ ml Suspension zum Eingeben für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Riluzol Zentiva 50 mg Filmtabletten Riluzol
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Riluzol Zentiva 50 mg Filmtabletten Riluzol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Riluzol Zentiva 50 mg Filmtabletten Riluzol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION FÜR: Cerenia Tabletten für Hunde
 GEBRAUCHSINFORMATION FÜR: Cerenia Tabletten für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION FÜR: Cerenia Tabletten für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
Pakendi infoleht: teave patsiendile
 Pakendi infoleht: teave patsiendile Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Te saate sellele kaasa aidata, teavitades ravimi kõigist
Pakendi infoleht: teave patsiendile Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Te saate sellele kaasa aidata, teavitades ravimi kõigist
Gebrauchsinformation: Information für Patienten. Picato 150 Mikrogramm/g Gel Ingenolmebutat
 Gebrauchsinformation: Information für Patienten Picato 150 Mikrogramm/g Gel Ingenolmebutat Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Patienten Picato 150 Mikrogramm/g Gel Ingenolmebutat Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
LISA I RAVIMI(TE) NIMETUSTE, RAVIMVORMI(DE), TUGEVUS(T)E, MANUSTAMISVIISI(DE), TAOTLEJA(TE) LOETELU LIIKMESRIIKIDES
 LISA I RAVIMI(TE) NIMETUSTE, RAVIMVORMI(DE), TUGEVUS(T)E, MANUSTAMISVIISI(DE), TAOTLEJA(TE) LOETELU LIIKMESRIIKIDES 1 Liikmesriik EL/EMÜ Müügiloa hoidja Taotleja Ravimi väljamõeldud nimetus Tšehhi Sandoz
LISA I RAVIMI(TE) NIMETUSTE, RAVIMVORMI(DE), TUGEVUS(T)E, MANUSTAMISVIISI(DE), TAOTLEJA(TE) LOETELU LIIKMESRIIKIDES 1 Liikmesriik EL/EMÜ Müügiloa hoidja Taotleja Ravimi väljamõeldud nimetus Tšehhi Sandoz
Gebrauchsinformation: I nformation für Anwender. RILUTEK 50 mg Filmtabletten Riluzol
 Gebrauchsinformation: I nformation für Anwender RILUTEK 50 mg Filmtabletten Riluzol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: I nformation für Anwender RILUTEK 50 mg Filmtabletten Riluzol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Das politische System der EU: Entwicklung, Strukturen, Funktionen
 Anne Faber Das politische System der EU: Entwicklung, Strukturen, Funktionen Die Erweiterungspolitik der EU: Stand und Perspektiven 10.01.2011 Seminarplan Termine 18.10.- 25.10.10 Themen I Einführung 01.11.-
Anne Faber Das politische System der EU: Entwicklung, Strukturen, Funktionen Die Erweiterungspolitik der EU: Stand und Perspektiven 10.01.2011 Seminarplan Termine 18.10.- 25.10.10 Themen I Einführung 01.11.-
Gebrauchsinformation: Information für Anwender. Faslodex 250 mg Injektionslösung Fulvestrant
 Gebrauchsinformation: Information für Anwender Faslodex 250 mg Injektionslösung Fulvestrant Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Faslodex 250 mg Injektionslösung Fulvestrant Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender. Baraclude 1 mg Filmtabletten Entecavir
 Gebrauchsinformation: Information für Anwender Baraclude 1 mg Filmtabletten Entecavir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Baraclude 1 mg Filmtabletten Entecavir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Tamiflu 75 mg Hartkapseln Oseltamivir
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tamiflu 75 mg Hartkapseln Oseltamivir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tamiflu 75 mg Hartkapseln Oseltamivir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für Anwender. EMADINE 0,5 mg/ml Augentropfen Emedastin
 Gebrauchsinformation: Information für Anwender EMADINE 0,5 mg/ml Augentropfen Emedastin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender EMADINE 0,5 mg/ml Augentropfen Emedastin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Pakendi infoleht: teave kasutajale
 Pakendi infoleht: teave kasutajale Sortis, 10 mg õhukese polümeerikattega tabletid Sortis, 20 mg õhukese polümeerikattega tabletid Sortis, 40 mg õhukese polümeerikattega tabletid Sortis 80 mg, 80 mg õhukese
Pakendi infoleht: teave kasutajale Sortis, 10 mg õhukese polümeerikattega tabletid Sortis, 20 mg õhukese polümeerikattega tabletid Sortis, 40 mg õhukese polümeerikattega tabletid Sortis 80 mg, 80 mg õhukese
1. Mis ravim on YAZ ja milleks seda kasutatakse... 2
 Pakendi infoleht: teave kasutajale YAZ, 0,02 mg/3 mg õhukese polümeerikattega tabletid Etünüülöstradiool/drospirenoon Enne ravimi võtmist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet.
Pakendi infoleht: teave kasutajale YAZ, 0,02 mg/3 mg õhukese polümeerikattega tabletid Etünüülöstradiool/drospirenoon Enne ravimi võtmist lugege hoolikalt infolehte, sest siin on teile vajalikku teavet.
I LISA RAVIMI OMADUSTE KOKKUVÕTE
 I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
I LISA RAVIMI OMADUSTE KOKKUVÕTE 1 Käesoleva ravimi suhtes kohaldatakse täiendavat järelevalvet, mis võimaldab kiiresti tuvastada uut ohutusteavet. Tervishoiutöötajatel palutakse teavitada kõigist võimalikest
Gebrauchsinformation: Information für Anwender. Mozobil 20 mg/ml Injektionslösung Plerixafor
 Gebrauchsinformation: Information für Anwender Mozobil 20 mg/ml Injektionslösung Plerixafor Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Mozobil 20 mg/ml Injektionslösung Plerixafor Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
B. PACKUNGSBEILAGE 13
 B. PACKUNGSBEILAGE 13 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ACOMPLIA 20 mg Filmtabletten (Rimonabant) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
B. PACKUNGSBEILAGE 13 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER ACOMPLIA 20 mg Filmtabletten (Rimonabant) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Ferriprox 500 mg Filmtabletten Deferipron
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Ferriprox 500 mg Filmtabletten Deferipron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Ferriprox 500 mg Filmtabletten Deferipron Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender. Galvus 50 mg Tabletten Vildagliptin
 Gebrauchsinformation: Information für Anwender Galvus 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Galvus 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender. Faslodex 250 mg Injektionslösung Fulvestrant
 Gebrauchsinformation: Information für Anwender Faslodex 250 mg Injektionslösung Fulvestrant Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Faslodex 250 mg Injektionslösung Fulvestrant Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender. Galvus 50 mg Tabletten Vildagliptin
 Gebrauchsinformation: Information für Anwender Galvus 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Galvus 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr Kind mit
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr Kind mit
Road Safety 2014. How is your country doing? STRASSENVERKEHRSSICHERHEIT: Wie sieht es in Ihrem Land aus?
 Road Safety 2014 How is your country doing? STRASSENVERKEHRSSICHERHEIT: Wie sieht es in Ihrem Land aus? SÉCURITÉ ROUTIÈRE: Quelle est la situation dans votre pays? Transport Die EU hat das Ziel, die Anzahl
Road Safety 2014 How is your country doing? STRASSENVERKEHRSSICHERHEIT: Wie sieht es in Ihrem Land aus? SÉCURITÉ ROUTIÈRE: Quelle est la situation dans votre pays? Transport Die EU hat das Ziel, die Anzahl
Gebrauchsinformation: Information für Anwender. Baraclude 0,05 mg/ml Lösung zum Einnehmen Entecavir
 Gebrauchsinformation: Information für Anwender Baraclude 0,05 mg/ml Lösung zum Einnehmen Entecavir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender Baraclude 0,05 mg/ml Lösung zum Einnehmen Entecavir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. Bridion 100 mg/ml Injektionslösung Sugammadex
 Gebrauchsinformation: Information für Anwender Bridion 100 mg/ml Injektionslösung Sugammadex Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei Ihnen angewendet wird,
Gebrauchsinformation: Information für Anwender Bridion 100 mg/ml Injektionslösung Sugammadex Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei Ihnen angewendet wird,
Gebrauchsinformation: Information für Anwender. Dexdor 100 Mikrogramm/ml Konzentrat zur Herstellung einer Infusionslösung Dexmedetomidin
 Gebrauchsinformation: Information für Anwender Dexdor 100 Mikrogramm/ml Konzentrat zur Herstellung einer Infusionslösung Dexmedetomidin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor mit
Gebrauchsinformation: Information für Anwender Dexdor 100 Mikrogramm/ml Konzentrat zur Herstellung einer Infusionslösung Dexmedetomidin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor mit
Wir sind für Sie da: Bürgerfragen Heidi Heinrich. Projekte Sebastian Kramer. Leitung Barbara Sterl
 Wir sind für Sie da: Bürgerfragen Heidi Heinrich Projekte Sebastian Kramer Leitung Barbara Sterl So erreichen Sie uns: Telefon 0911/231 7676 Telefax 0911/231 7688 europe-direct@stadt.nuernberg.de Was ist
Wir sind für Sie da: Bürgerfragen Heidi Heinrich Projekte Sebastian Kramer Leitung Barbara Sterl So erreichen Sie uns: Telefon 0911/231 7676 Telefax 0911/231 7688 europe-direct@stadt.nuernberg.de Was ist
Gebrauchsinformation: Information für Anwender. Jalra 50 mg Tabletten Vildagliptin
 Gebrauchsinformation: Information für Anwender Jalra 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Jalra 50 mg Tabletten Vildagliptin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Patienten. Desloratadin Actavis 5 mg Filmtabletten Desloratadin
 Gebrauchsinformation: Information für Patienten Desloratadin Actavis 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Desloratadin Actavis 5 mg Filmtabletten Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Evista 60 mg Filmtabletten. Raloxifenhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Evista 60 mg Filmtabletten Raloxifenhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Evista 60 mg Filmtabletten Raloxifenhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. Fampyra 10 mg Retardtabletten Fampridin
 Gebrauchsinformation: Information für Anwender Fampyra 10 mg Retardtabletten Fampridin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Anwender Fampyra 10 mg Retardtabletten Fampridin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. CIALIS 20 mg Filmtabletten Tadalafil
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER CIALIS 20 mg Filmtabletten Tadalafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER CIALIS 20 mg Filmtabletten Tadalafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Evista 60 mg Filmtabletten Raloxifenhydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Evista 60 mg Filmtabletten Raloxifenhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Evista 60 mg Filmtabletten Raloxifenhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
B. PACKUNGSBEILAGE 60
 B. PACKUNGSBEILAGE 60 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tarceva 25 mg Filmtabletten Tarceva 100 mg Filmtabletten Tarceva 150 mg Filmtabletten Erlotinib Lesen Sie die gesamte Packungsbeilage
B. PACKUNGSBEILAGE 60 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Tarceva 25 mg Filmtabletten Tarceva 100 mg Filmtabletten Tarceva 150 mg Filmtabletten Erlotinib Lesen Sie die gesamte Packungsbeilage
Standardiseeritud mürtool. Sinusiidi ja bronhiidi korral
 Sinusiidi ja Bei B bronhiidi korral GeloMyrtol forte (standardiseeritud ) toimemehhanism GeloMyrtol forte (standardiseeritud ) on taimne ravim ülemiste ja alumiste hingamisteede põletike raviks. on taimne
Sinusiidi ja Bei B bronhiidi korral GeloMyrtol forte (standardiseeritud ) toimemehhanism GeloMyrtol forte (standardiseeritud ) on taimne ravim ülemiste ja alumiste hingamisteede põletike raviks. on taimne
Aktuelle Marktrends und Aussichten
 Aktuelle Marktrends und Aussichten Leiterplatten Michael Gasch, Data4PCB ZVEI- Forum electronica 2010, 11.11.2010, 10 11 Uhr Folie 1 Entwicklung des Wechselkurses : US$ 2005 bis 2010/09 1,60 1,58 1,56
Aktuelle Marktrends und Aussichten Leiterplatten Michael Gasch, Data4PCB ZVEI- Forum electronica 2010, 11.11.2010, 10 11 Uhr Folie 1 Entwicklung des Wechselkurses : US$ 2005 bis 2010/09 1,60 1,58 1,56
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Simulect 20 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung Basiliximab Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Simulect 20 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung Basiliximab Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Simulect 10 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung Basiliximab Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Simulect 10 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung Basiliximab Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender. Lixiana 15 mg Filmtabletten Lixiana 30 mg Filmtabletten Lixiana 60 mg Filmtabletten Edoxaban
 Gebrauchsinformation: Information für Anwender Lixiana 15 mg Filmtabletten Lixiana 30 mg Filmtabletten Lixiana 60 mg Filmtabletten Edoxaban Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Gebrauchsinformation: Information für Anwender Lixiana 15 mg Filmtabletten Lixiana 30 mg Filmtabletten Lixiana 60 mg Filmtabletten Edoxaban Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Gebrauchsinformation: Information für Anwender. Nucala 100 mg Pulver zur Herstellung einer Injektionslösung. Mepolizumab
 Gebrauchsinformation: Information für Anwender Nucala 100 mg Pulver zur Herstellung einer Injektionslösung Mepolizumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Gebrauchsinformation: Information für Anwender Nucala 100 mg Pulver zur Herstellung einer Injektionslösung Mepolizumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tractocile 37,5 mg/5 ml Konzentrat zur Herstellung einer Infusionslösung Atosiban
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tractocile 37,5 mg/5 ml Konzentrat zur Herstellung einer Infusionslösung Atosiban Lesen Sie sich diese Packungsbeilage bitte sorgfältig durch, bevor Sie,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tractocile 37,5 mg/5 ml Konzentrat zur Herstellung einer Infusionslösung Atosiban Lesen Sie sich diese Packungsbeilage bitte sorgfältig durch, bevor Sie,
Gebrauchsinformation: Information für Anwender. Simulect 10 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung
 Gebrauchsinformation: Information für Anwender Simulect 10 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung Basiliximab Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Simulect 10 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung oder Infusionslösung Basiliximab Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Actos 45 mg Tabletten Pioglitazon
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Actos 45 mg Tabletten Pioglitazon Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. -
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Actos 45 mg Tabletten Pioglitazon Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. -
Gebrauchsinformation: Information für Anwender. Fluenz Tetra Nasenspray, Suspension Influenza-Impfstoff (lebend-attenuiert, nasal)
 Gebrauchsinformation: Information für Anwender Fluenz Tetra Nasenspray, Suspension Influenza-Impfstoff (lebend-attenuiert, nasal) Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht
Gebrauchsinformation: Information für Anwender Fluenz Tetra Nasenspray, Suspension Influenza-Impfstoff (lebend-attenuiert, nasal) Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht
Gebrauchsinformation: Information für Anwender. Cetrotide 0,25 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Cetrorelixacetat
 Gebrauchsinformation: Information für Anwender Cetrotide 0,25 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Cetrorelixacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender Cetrotide 0,25 mg Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Cetrorelixacetat Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender. Hycamtin 1 mg. Hycamtin 4 mg. Pulver zur Herstellung eines Infusionslösungskonzentrats Topotecan
 Gebrauchsinformation: Information für Anwender Hycamtin 1 mg Hycamtin 4 mg Pulver zur Herstellung eines Infusionslösungskonzentrats Topotecan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender Hycamtin 1 mg Hycamtin 4 mg Pulver zur Herstellung eines Infusionslösungskonzentrats Topotecan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Stand der Information: /N-060 B. PACKUNGSBEILAGE
 B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST
 GEBRAUCHSINFORMATION Poulvac E. coli Lyophilisat zur Herstellung einer Suspension zur Impfung von Hühnern und Puten mittels Sprayapplikation oder über das Trinkwasser für Hühner. 1. NAME UND ANSCHRIFT
GEBRAUCHSINFORMATION Poulvac E. coli Lyophilisat zur Herstellung einer Suspension zur Impfung von Hühnern und Puten mittels Sprayapplikation oder über das Trinkwasser für Hühner. 1. NAME UND ANSCHRIFT
Gebrauchsinformation: Information für den Anwender Karvea 150 mg Filmtabletten Irbesartan
 Gebrauchsinformation: Information für den Anwender Karvea 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für den Anwender Karvea 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Irbesartan Zentiva 150 mg Filmtabletten Irbesartan
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Irbesartan Zentiva 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Irbesartan Zentiva 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für den Anwender. Resolor 1 mg Filmtabletten Resolor 2 mg Filmtabletten Prucaloprid
 Gebrauchsinformation: Information für den Anwender Resolor 1 mg Filmtabletten Resolor 2 mg Filmtabletten Prucaloprid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für den Anwender Resolor 1 mg Filmtabletten Resolor 2 mg Filmtabletten Prucaloprid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. IZBA 30 Mikrogramm/ml Augentropfen Travoprost
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IZBA 30 Mikrogramm/ml Augentropfen Travoprost Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IZBA 30 Mikrogramm/ml Augentropfen Travoprost Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Fampyra 10 mg Retardtabletten Fampridin
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Fampyra 10 mg Retardtabletten Fampridin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Fampyra 10 mg Retardtabletten Fampridin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Aprovel 150 mg Filmtabletten Irbesartan
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Aprovel 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Aprovel 150 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für den Anwender. Bondronat 50 mg Filmtabletten Ibandronsäure
 Gebrauchsinformation: Information für den Anwender Bondronat 50 mg Filmtabletten Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für den Anwender Bondronat 50 mg Filmtabletten Ibandronsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für Patienten. Mimpara 30 mg Filmtabletten Mimpara 60 mg Filmtabletten Mimpara 90 mg Filmtabletten Cinacalcet
 Gebrauchsinformation: Information für Patienten Mimpara 30 mg Filmtabletten Mimpara 60 mg Filmtabletten Mimpara 90 mg Filmtabletten Cinacalcet Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Patienten Mimpara 30 mg Filmtabletten Mimpara 60 mg Filmtabletten Mimpara 90 mg Filmtabletten Cinacalcet Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Stand der Information: / N 026 B. PACKUNGSBEILAGE
 B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Bridion 100 mg/ml Injektionslösung Sugammadex Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei Ihnen
B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Bridion 100 mg/ml Injektionslösung Sugammadex Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor dieses Arzneimittel bei Ihnen
Gebrauchsinformation: Information für Patienten. Aerius 0,5 mg/ml Lösung zum Einnehmen Desloratadin
 Gebrauchsinformation: Information für Patienten Aerius 0,5 mg/ml Lösung zum Einnehmen Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Aerius 0,5 mg/ml Lösung zum Einnehmen Desloratadin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. RotaTeq Lösung zum Einnehmen Rotavirus-Lebendimpfstoff
 Gebrauchsinformation: Information für Anwender RotaTeq Lösung zum Einnehmen Rotavirus-Lebendimpfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Ihr Kind mit diesem Impfstoff geimpft
Gebrauchsinformation: Information für Anwender RotaTeq Lösung zum Einnehmen Rotavirus-Lebendimpfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Ihr Kind mit diesem Impfstoff geimpft
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. CIALIS 5 mg Filmtabletten Tadalafil
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER CIALIS 5 mg Filmtabletten Tadalafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER CIALIS 5 mg Filmtabletten Tadalafil Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Fragebogen für Unternehmen
 Fragebogen für Unternehmen Risk & Policy Analysts Ltd (RPA) wurde zusammen mit CSES und EPRD damit beauftragt die Europäische Kommission bei einer Bewertung der Verbraucherrechte-Richtlinie (Richtlinie
Fragebogen für Unternehmen Risk & Policy Analysts Ltd (RPA) wurde zusammen mit CSES und EPRD damit beauftragt die Europäische Kommission bei einer Bewertung der Verbraucherrechte-Richtlinie (Richtlinie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Protopic 0,03% Salbe Tacrolimus-Monohydrat
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Protopic 0,03% Salbe Tacrolimus-Monohydrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Protopic 0,03% Salbe Tacrolimus-Monohydrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Patienten. IRESSA 250 mg Filmtabletten Gefitinib
 Gebrauchsinformation: Information für Patienten IRESSA 250 mg Filmtabletten Gefitinib Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Patienten IRESSA 250 mg Filmtabletten Gefitinib Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
WICHTIGE INFORMATION ZU VYNDAQEL (TAFAMIDIS) Kernbotschaften
 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Icandra 50 mg/850 mg Filmtabletten Icandra 50 mg/1000 mg Filmtabletten
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Icandra 50 mg/850 mg Filmtabletten Icandra 50 mg/1000 mg Filmtabletten Vildagliptin/Metforminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Icandra 50 mg/850 mg Filmtabletten Icandra 50 mg/1000 mg Filmtabletten Vildagliptin/Metforminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Karvea 75 mg Filmtabletten Irbesartan
 Gebrauchsinformation: Information für Anwender Karvea 75 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Anwender Karvea 75 mg Filmtabletten Irbesartan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Xeloda 500 mg Filmtabletten Capecitabin
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xeloda 500 mg Filmtabletten Capecitabin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Xeloda 500 mg Filmtabletten Capecitabin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen.
Gebrauchsinformation: Information für Anwender. Zinforo 600 mg Pulver zur Herstellung eines Konzentrats für eine Infusionslösung Ceftarolinfosamil
 Gebrauchsinformation: Information für Anwender Zinforo 600 mg Pulver zur Herstellung eines Konzentrats für eine Infusionslösung Ceftarolinfosamil Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender Zinforo 600 mg Pulver zur Herstellung eines Konzentrats für eine Infusionslösung Ceftarolinfosamil Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender. Sevelamercarbonat Zentiva 800 mg Filmtabletten Sevelamercarbonat
 Gebrauchsinformation: Information für Anwender Sevelamercarbonat Zentiva 800 mg Filmtabletten Sevelamercarbonat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Sevelamercarbonat Zentiva 800 mg Filmtabletten Sevelamercarbonat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender. NEVANAC 1 mg/ml Augentropfensuspension Nepafenac
 Gebrauchsinformation: Information für Anwender NEVANAC 1 mg/ml Augentropfensuspension Nepafenac Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender NEVANAC 1 mg/ml Augentropfensuspension Nepafenac Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. Esbriet 267 mg Hartkapseln Pirfenidon
 Gebrauchsinformation: Information für Anwender Esbriet 267 mg Hartkapseln Pirfenidon Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
Gebrauchsinformation: Information für Anwender Esbriet 267 mg Hartkapseln Pirfenidon Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
Gebrauchsinformation: Information für Anwender. Hycamtin 0,25 mg Hartkapseln Hycamtin 1 mg Hartkapseln Topotecan
 Gebrauchsinformation: Information für Anwender Hycamtin 0,25 mg Hartkapseln Hycamtin 1 mg Hartkapseln Topotecan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender Hycamtin 0,25 mg Hartkapseln Hycamtin 1 mg Hartkapseln Topotecan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten. Zeffix 100 mg Filmtabletten Lamivudin
 Gebrauchsinformation: Information für Patienten Zeffix 100 mg Filmtabletten Lamivudin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. -
Gebrauchsinformation: Information für Patienten Zeffix 100 mg Filmtabletten Lamivudin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen. -
Gebrauchsinformation: Information für Patienten. Steglatro 15 mg Filmtabletten. Ertugliflozin
 Gebrauchsinformation: Information für Patienten Steglatro 5 mg Filmtabletten Steglatro 15 mg Filmtabletten Ertugliflozin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Gebrauchsinformation: Information für Patienten Steglatro 5 mg Filmtabletten Steglatro 15 mg Filmtabletten Ertugliflozin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Protopic 0,1% Salbe Tacrolimus-Monohydrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Protopic 0,1% Salbe Tacrolimus-Monohydrat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER M-M-RvaxPro Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER M-M-RvaxPro Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die
Gebrauchsinformation: Information für Anwender. Cholestagel 625 mg Filmtabletten Colesevelam
 Gebrauchsinformation: Information für Anwender Cholestagel 625 mg Filmtabletten Colesevelam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Gebrauchsinformation: Information für Anwender Cholestagel 625 mg Filmtabletten Colesevelam Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION FÜR Convenia 80 mg/ml Pulver und Lösungsmittel zur Herstellung einer Injektionslösung für Hunde und Katzen
 GEBRAUCHSINFORMATION FÜR Convenia 80 mg/ml Pulver und Lösungsmittel zur Herstellung einer Injektionslösung für Hunde und Katzen 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES
GEBRAUCHSINFORMATION FÜR Convenia 80 mg/ml Pulver und Lösungsmittel zur Herstellung einer Injektionslösung für Hunde und Katzen 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES
Gebrauchsinformation: Information für Patienten. XGEVA 120 mg Injektionslösung Denosumab
 Gebrauchsinformation: Information für Patienten XGEVA 120 mg Injektionslösung Denosumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Patienten XGEVA 120 mg Injektionslösung Denosumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
B. PACKUNGSBEILAGE 78
 B. PACKUNGSBEILAGE 78 Gebrauchsinformation: Information für Anwender Baraclude 0,5 mg Filmtabletten Entecavir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
B. PACKUNGSBEILAGE 78 Gebrauchsinformation: Information für Anwender Baraclude 0,5 mg Filmtabletten Entecavir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Patienten. XGEVA 120 mg Injektionslösung Denosumab
 Gebrauchsinformation: Information für Patienten XGEVA 120 mg Injektionslösung Denosumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Patienten XGEVA 120 mg Injektionslösung Denosumab Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer
Gebrauchsinformation: Information für Anwender. Icandra 50 mg/850 mg Filmtabletten Icandra 50 mg/1000 mg Filmtabletten
 Gebrauchsinformation: Information für Anwender Icandra 50 mg/850 mg Filmtabletten Icandra 50 mg/1000 mg Filmtabletten Vildagliptin/Metforminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Icandra 50 mg/850 mg Filmtabletten Icandra 50 mg/1000 mg Filmtabletten Vildagliptin/Metforminhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig
INFORMATION FÜR DEN ANWENDER
 PA501GEGE00 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 2 mg Pulver und Lösungsmittel zur Herstellung einer Depot-Injektionssuspension (Exenatide) GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
PA501GEGE00 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER 2 mg Pulver und Lösungsmittel zur Herstellung einer Depot-Injektionssuspension (Exenatide) GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
Gebrauchsinformation: Information für Patienten. Orgalutran 0,25 mg/0,5 ml Injektionslösung Ganirelix
 Gebrauchsinformation: Information für Patienten Orgalutran 0,25 mg/0,5 ml Injektionslösung Ganirelix Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Patienten Orgalutran 0,25 mg/0,5 ml Injektionslösung Ganirelix Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Europäische Umweltagentur. vorstellung der Agentur ihrer Aufgabenstellung ihrer Arbeitsmethoden
 Europäische Umweltagentur Aufgaben Die EUA verfolgt das Ziel, nachhaltige Entwicklung zu fördern und zu einer erheblichen und messbaren Verbesserung der Umwelt in Europa beizutragen. Dazu stellt sie zeitgerechte,
Europäische Umweltagentur Aufgaben Die EUA verfolgt das Ziel, nachhaltige Entwicklung zu fördern und zu einer erheblichen und messbaren Verbesserung der Umwelt in Europa beizutragen. Dazu stellt sie zeitgerechte,
Gebrauchsinformation: Information für Anwender. PREVYMIS 480 mg Filmtabletten. Wirkstoff: Letermovir
 Gebrauchsinformation: Information für Anwender PREVYMIS 240 mg Filmtabletten PREVYMIS 480 mg Filmtabletten Wirkstoff: Letermovir Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht
Gebrauchsinformation: Information für Anwender PREVYMIS 240 mg Filmtabletten PREVYMIS 480 mg Filmtabletten Wirkstoff: Letermovir Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht
Forxiga 5 mg Filmtabletten
 Gebrauchsinformation: Information für Patienten Forxiga 5 mg Filmtabletten Forxiga 10 mg Filmtabletten Dapagliflozin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Gebrauchsinformation: Information für Patienten Forxiga 5 mg Filmtabletten Forxiga 10 mg Filmtabletten Dapagliflozin Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
Die Mitgliedstaaten der EU
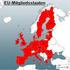 Die Mitgliedstaaten der EU Arbeitsaufträge: 1. Trage in die einzelnen EU-Mitgliedstaaten die jeweilige Abkürzung ein! 2. Schlage in deinem Atlas nach, wo die Hauptstädte der einzelnen Länder liegen und
Die Mitgliedstaaten der EU Arbeitsaufträge: 1. Trage in die einzelnen EU-Mitgliedstaaten die jeweilige Abkürzung ein! 2. Schlage in deinem Atlas nach, wo die Hauptstädte der einzelnen Länder liegen und
Gebrauchsinformation: Information für Anwender. Arixtra 1,5 mg/0,3 ml Injektionslösung Fondaparinux-Natrium
 Gebrauchsinformation: Information für Anwender Arixtra 1,5 mg/0,3 ml Injektionslösung Fondaparinux-Natrium Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender Arixtra 1,5 mg/0,3 ml Injektionslösung Fondaparinux-Natrium Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. NEVANAC 3 mg/ml Augentropfensuspension Nepafenac
 Gebrauchsinformation: Information für Anwender NEVANAC 3 mg/ml Augentropfensuspension Nepafenac Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für Anwender NEVANAC 3 mg/ml Augentropfensuspension Nepafenac Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Oluline teave, mida peab teadma enne ravimi Pioglitazone Teva (15 mg, 30 mg, 45 mg) tabletid väljakirjutamist
 Oluline teave, mida peab teadma enne ravimi Pioglitazone Teva (15 mg, 30 mg, 45 mg) tabletid väljakirjutamist Lugupeetud Tervishoiutöötaja, Käesolevaga soovime Teid teavitada olulistest ohutusnõuetest,
Oluline teave, mida peab teadma enne ravimi Pioglitazone Teva (15 mg, 30 mg, 45 mg) tabletid väljakirjutamist Lugupeetud Tervishoiutöötaja, Käesolevaga soovime Teid teavitada olulistest ohutusnõuetest,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Efient 10 mg Filmtabletten Efient 5 mg Filmtabletten Prasugrel
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Efient 10 mg Filmtabletten Efient 5 mg Filmtabletten Prasugrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Efient 10 mg Filmtabletten Efient 5 mg Filmtabletten Prasugrel Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Prevenar 13 Injektionssuspension Pneumokokkenpolysaccharid-Konjugatimpfstoff (13-valent, adsorbiert) Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Prevenar 13 Injektionssuspension Pneumokokkenpolysaccharid-Konjugatimpfstoff (13-valent, adsorbiert) Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tractocile 6,75 mg/0,9 ml Injektionslösung Atosiban
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tractocile 6,75 mg/0,9 ml Injektionslösung Atosiban Lesen Sie sich diese Packungsbeilage bitte sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tractocile 6,75 mg/0,9 ml Injektionslösung Atosiban Lesen Sie sich diese Packungsbeilage bitte sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
