Superabsorber aus der Binde!
|
|
|
- Monica Krämer
- vor 9 Jahren
- Abrufe
Transkript
1 V14 Superabsorber aus der Binde! Fach Klasse Überthema Feinthema Zeit Chemie Q2 Synthetische Makromoleküle Eigenschaften von Kunststoffen 30 Minuten Zusammenfassung Bei dem Versuch wird der Superabsorber, der in einer Binde enthalten ist, auf seine Wasserspeicherkapazität hin überprüft und der Einfluss von Säure, Base und Salz auf diese untersucht. Einordnung in den Unterricht 1 Der Versuch kann in der Qualifikationsphase Q2 zum verbindlichen Unterrichtsinhalt 2. Synthetische Makromoleküle durchgeführt werden. Die SuS sollten bereits mit den Grundbegriffen aus der Kunststoffchemie vertraut sein und die Begriffe Osmose und Diffusion kennen. Darüber hinaus sollten die grundlegenden Konzepte wie elektrostatische Anziehung und Säure-Base-Chemie angewendet werden können. Insgesamt weist der Versuch einen hohen Lebensweltbezug auf, da ein Phänomen aus dem Alltag erklärt wird. Dies sollte Interesse und Motivation auf Seiten der Schüler hervorrufen. Außerdem wird gezeigt, wie weitreichend der Einsatz von Kunststoffen ist und wie viele unterschiedliche Anwendungsbereiche sie bedienen. Ebenfalls kann an den Versuch anschließend im Unterricht am Beispiel des verwendeten Kunststoffes einer der Reaktionstypen zur Verknüpfung von Monomeren zu Makromolekülen angeführt werden. 1 Vgl. Hirt, A.: Lehrplan Chemie (2010).
2 Der Versuch Die Durchführung 2 Abbildung 1: Übersicht über die verwendeten Materialien. Eine Binde wird geöffnet und die feinen, weißen, Kügelchen über einer Schüssel abgekratzt. Nun werden die erhaltenen Kügelchen in ein großes Glas gegeben und mithilfe eines Messbechers 100 ml Wasser langsam in das Glas gegeben. Die Konsistenz und die Beschaffenheit der Substanz im Glas, werden mit der Hand überprüft. Anschließend wird ein Stück Papier so zurechtgeschnitten, dass es in das Glas gelegt werden kann und dieses leicht angedrückt. Danach wird die Beobachtung notiert. Nun werden erneut 100 ml Wasser hinzugegeben und der Papiertest durchgeführt. Die Wasserzugabe von 100 ml wird nun sooft wiederholt, bis das angedrückte Papier durchweicht wird. Daraufhin wird in drei weitere Gläser je ein Esslöffel Substanz aus dem Glas in vier Gläser gegeben. Zu einem Glas wird nun ½ Teelöffel Salz, in ein anderes ½ Teelöffel Soda und in das dritte Glas ½ Teelöffel Zitronensäure gegeben. Das vierte Glas dient als Vergleichsprobe. Die Beobachtung Wird die Binde geöffnet und die Kunststoffummantelung abgezogen, so bleibt eine mit kleinen weißen Kügelchen beschichtete Schicht übrig. 2 Vgl. Göthlich, A., Koltzenburg S., Schornick, G.: Vielseitig funktionale Polymere im Alltag. In: Chemie in unserer Zeit. Volume 39/Issue 4. Weinheim S. 272.
3 Abbildung 2: Links: Absorberkügelchen in der Binde. Rechts: Darstellung der gesamten Menge an Absorber aus einer Binde. Die Kügelchen kleben etwas an dieser Schicht und müssen abgekratzt werden. Wird zu diesen Kügelchen 100 ml Wasser gegeben kann beobachtet werden, wie die Kügelchen an Volumen zunehmen und durchsichtig werden. Es bildet sich ein Gel, in welchem das gesamte Wasser eingeschlossen wird. Abbildung 3: Aufquellen des Absorbers bei Zugabe von 100 ml Wasser. Fasst man mit den Fingern diese Oberfläche an, so ist sie nicht nass. Auch ein darauf gedrücktes Blatt Papier weicht nicht durch.
4 Abbildung 4. Das Papierstück weicht bei drücken auf den Absorber nicht durch. Abbildung 5: Aufquillen des Absorbers bei 200 ml Wasserzugabe. Erst nach der Zugabe von insgesamt 300 ml Wasser wird das Papierstück durchnässt. Abbildung 6: Bei Zugabe von 300 ml Wasser, beginnt das Papier durchzuweichen.
5 Werden Salz, Soda oder Zitronensäure zu einem Esslöffel der gelartigen Substanz gegeben, kann beobachtet werden, wie das Volumen abnimmt und Wasser abgegeben wird. Dieser Effekt ist am Stärksten bei Zugabe der Zitronensäure. Abbildung 7: Versuchsanordnung vor Zugabe der einzelnen Substanzen. Abbildung 8: Reihenfolge: Vergleichsprobe ohne Zusatz. Probe mit Salz, Probe mit Soda und Probe mit Zitronensäure. Entsorgung Der Superabsorber kann als Wasserspeicher unter Blumenerde gemischt werden. Die Windel wird in die Feststofftonne gegeben. Ansonsten wird der Absorber in den Hausmüll entsorgt.
6 Fachlicher Hintergrund Windeln, Inkontinenzartikel oder Produkte der Damenhygiene werden im Alltag als selbstverständlich hingenommen, doch wie funktionieren eigentlich diese Produkte? Allen gemeinsam ist der enthaltene Superabsorber. Was ist ein Superabsorber und wie ist er aufgebaut? Wird eine Binde oder Windel geöffnet, ist sie auf den ersten Blick hauptsächlich mit Watte gefüllt. Bei genauerer Beobachtung lassen sich jedoch kleine weiße Kügelchen darin finden. Diese Körner bestehen aus Superabsorber, SAP 3, auf den die Fähigkeit Flüssigkeiten zu speichern zurückzuführen ist. Als Superabsorber werden Polymere bezeichnet, die ein Vielfaches ihres Eigengewichts an Wasser binden können. Dabei entsteht ein festes Gel, welches pro Gramm Polymer einen Liter entmineralisiertes Wasser aufnehmen kann. So bildet sich ein Feststoff, der aus 99,9 % Wasser zusammengesetzt ist. Anwendung finden Superabsorber vor allem in Hygieneartikeln wie Babywindeln, Inkontinenzartikeln für Erwachsene und Damenhygieneprodukten. 4 Auch im Gartenbau werden Superabsorber eingesetzt, die dort als Wasserspeicher dienen. Sie geben langsam Wasser ab, ohne die gesamte Pflanze unter Wasser zu setzen. Weiterhin werden Superabsorber zum Trocknen von überschwemmten Räumen eingesetzt, oder aber zum Löschen von Großbränden. 5 Das Polymer, welches diesen nützlichen Effekt besitzt, ist eine kovalent vernetzte, teilneutralisierte Polyacrylsäure. Indem während der radikalischen Copolymerisation von Acrylsäure, mit Natriumacrylat ein Vernetzer zugegeben wird, entsteht ein dreidimensionales Netzwerk des Polymers. Dieses ist im Gegensatz zu Polyacrylat nicht wasserlöslich. Sowohl die im Grundgerüst enthaltenen Carboxy-Gruppen sind hydrophil als auch die Natrium-Gegenionen, allerdings erreichen die kovalent gebundenen Quervernetzer, dass sich das Polymer nicht mehr lösen lässt, sondern nur aufquillt. 6 3 Abkürzung für superabsorbierende Polymere. 4 Vgl. Göthlich, A., Koltzenburg S., Schornick, G.: Vielseitig funktionale Polymere im Alltag. In: Chemie in unserer Zeit. Volume 39/Issue 4. Weinheim S Vgl. Dehnicke, K. et al.: Chemie im Haushalt Was in der Babywindel steckt, von natürlichen und künstlichen Superabsorbern. In: Chemikum Marburg kurze Broschüre mit Erläuterungen zu den Experimenten. Philipps-Universität Marburg S Vgl. Hofheinz, V.: Das Babywindelprojekt Offene Forschungsaufträge und implizierter Wissenserwerb über die Natur der Naturwissenschaften. In: Naturwissenschaften im Unterricht Chemie. 21/118, S
7 Monomere: Vernetzer Acrylsäure (Probensäure) O Natriumacrylat O OH - O Na + CH 2 CH 2 Wie funktioniert ein Superabsorber? Das Natrium-Polyacrylat ist der kommerziell am häufigsten eingesetzte SAP. Dieser ist in seinem Grundzustand insgesamt betrachtet elektrisch neutral. Durch im Polymer gebundene Natriumionen wird ein osmotischer Druck erzeugt, durch den Wasser ins Innere der Vernetzungen gezogen wird. Die Hydratation dieser Ionen führt zur Abstoßung der negativ geladenen Carboxylat-Gruppen der Polyacrylsäure. Die coulombsche Anziehungskraft zwischen den Natriumionen und den Carboxylat-Gruppen sinkt bei gleichzeitiger Abstoßung der Carboxylat-Gruppen untereinander. Dieser Effekt hat das beobachtete Ausdehnen des Polymers zur Folge. Ebenfalls wird allein durch die Wasseraufnahme das zuvor fest verknäulte Polymer ausgedehnt. Durch die Ausbildung von Wasserstoffbrückenbindungen zwischen den Wassermolekülen und den Carboxylat-Gruppen des Superabsorbers wird das Wasser gebunden. Es kann jedoch nur solange Wasser einströmen, bis die elastische Rückstellkraft des Polymers genauso groß wird wie der osmotische Druck. Je nachdem, wie stark vernetzt die Polyacrylsäure ist, kann Wasser schneller oder langsamer eindringen. Die Ausbildung ausgedehnter Polyacrylfasern führt zur beobachteten ansteigenden Viskosität. Ein weiterer positiver und für die Anwendung essentieller Effekt ist, dass auch unter Druck das Wasser nicht mehr abgegeben wird. Durch die drei Aspekte: gute Aufnahme von Flüssigkeit, gleichmäßige Verteilung dieser im Superabsorber und Speicherung ohne erneute Freisetzung, ist der Superabsorber als Inhaltsstoff für Binden und Windeln geeignet. 7,8 7 Vgl. Hofheinz, V.: Das Babywindelprojekt Offene Forschungsaufträge und implizierter Wissenserwerb über die Natur der Naturwissenschaften. In: Naturwissenschaften im Unterricht Chemie. 21/118/ S Vgl. Göthlich, A., Koltzenburg S., Schornick, G.: Vielseitig funktionale Polymere im Alltag. In: Chemie in unserer Zeit. Volume 39/Issue S. 272.
8 Abbildung 9: Darstellung des Aufbaus und der Funktionsweise von Superabsorbern in der Windel. 9 Durch was kann die Wasseraufnahmekapazität eines Superabsorbers beeinflusst werden? Wird zu dem Gel aus Superabsorber und Wasser eine hohe Konzentration an Kochsalz hinzugegeben, so kann festgestellt werden, dass Wasser abgegeben wird. Dies ist darauf zurückzuführen, dass zum einen die auftretenden elektrostatischen Wechselwirkungen zwischen den ionischen Gruppen verringert werden und zum anderen der osmotische Druck des äußeren Milieus erhöht wird, wodurch Wasser unter Zurückfaltung des Polymers entweicht und nicht weiter aufgenommen werden kann. 10 Weiterhin erfolgt bei Zugabe von Säure eine Protolyse der Carboxylat-Gruppen des Polymers. Dadurch wird die elektrostatische Abstoßung geschwächt, sodass eine geringere Ausdehnung der Fasern erhalten wird. Zudem wird durch den Kationentausch ein geringerer osmotischer Druck erzeugt und eine geringere Wassermenge wird aufgenommen. Auch bei Zugabe von basischen Lösungen wird die Quellfähigkeit des Absorbers verringert. Dies hängt damit zusammen, dass hier der osmotische Druck verkleinert wird, indem die Kationenkonzentration der Lösung höher wird, als im Inneren des Polymers. 9 Göthlich, A., Koltzenburg S., Schornick, G.: Vielseitig funktionale Polymere im Alltag. In: Chemie in unserer Zeit. Volume 39/Issue S Vgl. Göthlich, A., Koltzenburg S., Schornick, G.: Vielseitig funktionale Polymere im Alltag. In: Chemie in unserer Zeit. Volume 39/Issue S
9 Prinzipiell führt ein höherer Vernetzungsgrad des Superabsorbers zu einer größeren Stabilität des Gels, gleichzeitig wird aber auch die Fähigkeit des Ausdehnens durch die vielen Quervernetzungen verringert. Dies bedeutet, dass stark vernetze Superabsorber nicht so viel Wasser aufnehmen können, es jedoch besser einschließen als weniger vernetzte. All diese Aspekte erklären auch, warum zum Beispiel eine Windel, nicht 1 L Urin hält, sondern sehr viel weniger. Zum einen enthält Urin gelöste Salze, die den ins Innere des Polymers gerichteten osmotischen Gradienten vermindern, zum anderen ist er leicht sauer, was dazu führt, das die Quellfähigkeit zusätzlich noch weiter abnimmt. All dies zeigt, dass die Quellfähigkeit von den Faktoren, ph-wert und Ionengehalt der Lösung sowie dem Vernetzungsgrad und der Neutralisation des Polymers beeinflusst wird. 11 Fällt dir ein Beispiel für einen natürlichen Superabsorber ein? Neben den aus Kunstoffen hergestellten Superabsorbern gibt es auch sogenannte natürliche (Super)absorber. Zu ihnen zählt zum Beispiel die Gelatine, die zwar nicht so effektiv Wasser einlagern kann, die aber in Wasser ein gewisses Quellvermögen aufweist. Dies ist in einem einfachen Experiment zu zeigen. Wird ein Gummibärchen in ein Glas mit Wasser gelegt, so quillt dieses mit der Zeit stark auf. Auch die dabei entstehende Konsistenz, ist der des Superabsorbers ähnlich. 12 Im Sinne einer umweltfreundlicheren Produktion, die dazu führen soll, dass der Einsatz von gesundheitlich und ökologisch unbedenklicheren Materialien gefördert wird, wird die Herstellung von SAPs aus nachwachsenden Rohstoffen erforscht. Dabei sollten Produkte auf Basis von Stärke, Pektin oder Cellulose synthetisiert werden. Diese Rohstoffe können durch Einbauen von hydrophilen Gruppen besser wasserlöslich gemacht werden und durch Vernetzung zu stabilen Gelen umgewandelt werden. Diese auf nachwachsenden 11 Vgl. Hofheinz, V.: Das Babywindelprojekt Offene Forschungsaufträge und implizierter Wissenserwerb über die Natur der Naturwissenschaften. In: Naturwissenschaften im Unterricht Chemie. 21/118, S Vgl. Dehnicke, K. et al.: Chemie im Haushalt Was in der Babywindel steckt, von natürlichen und künstlichen Superabsorbern. In: Chemikum Marburg kurze Broschüre mit Erläuterungen zu den Experimenten. Philipps-Universität Marburg S. 22.
10 Rohstoffen basierenden Absorber können durch einfaches Kompostieren unbedenklich und kostengünstig entsorgt werden Vgl. Zeuke, M.: Superabsorber aus nachwachsenden Rohstoffen Die gezielte Synthese mit nachwachsenden Rohstoffen. In: Chemkon. Volume 12/Issue S
11
Gruppe 13 vorgegebener Versuch. Polyelektrolyte im Haargel
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 17.06.09 SS 09 Gruppe 13 vorgegebener Versuch Polyelektrolyte
Projekt: Von Groß zu Klein Makromoleküle als Brücke zum molekularen Verständnis
 Wasserbindung von Polyacrylaten 1 Aufbau Polyacrylsäure ist ein synthetisch hergestelltes, hochmolekulares Polymer der Acrylsäure. Sie liegt als in der Regel als weißes Pulver vor und ist hygroskopisch
Wasserbindung von Polyacrylaten 1 Aufbau Polyacrylsäure ist ein synthetisch hergestelltes, hochmolekulares Polymer der Acrylsäure. Sie liegt als in der Regel als weißes Pulver vor und ist hygroskopisch
Herstellung von Kunsthonig
 V8 erstellung von Kunsthonig Fach Klasse Überthema Feinthema Zeit Chemie Q2 Kohlenhydrate Mono- und Disaccharide 90 Minuten Zusammenfassung Bei dem Versuch wird Saccharose durch Säurehydrolyse in seine
V8 erstellung von Kunsthonig Fach Klasse Überthema Feinthema Zeit Chemie Q2 Kohlenhydrate Mono- und Disaccharide 90 Minuten Zusammenfassung Bei dem Versuch wird Saccharose durch Säurehydrolyse in seine
Schülerlabor. Modul: Funktionale Polymere. Betreuung durch das MPI für Polymerforschung, Mainz (Gunnar Kircher und Wolfgang H.
 1 Schülerlabor Modul: Funktionale Polymere Betreuung durch das MPI für Polymerforschung, Mainz (Gunnar Kircher und Wolfgang H.Meyer) Lerninhalte: Projektschritte: Bedeutung von funktionalen Polymeren Struktur
1 Schülerlabor Modul: Funktionale Polymere Betreuung durch das MPI für Polymerforschung, Mainz (Gunnar Kircher und Wolfgang H.Meyer) Lerninhalte: Projektschritte: Bedeutung von funktionalen Polymeren Struktur
SUPERABSORBER. Eine Präsentation von Johannes Schlüter und Thomas Luckert
 SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
SUPERABSORBER Eine Präsentation von Johannes Schlüter und Thomas Luckert Inhalt: Die Windel Die Technik des Superabsorbers Anwendungsgebiete des Superabsorbers Ein kurzer Abriss aus der Geschichte der
Gerinnung von Proteinen
 V11 Gerinnung von Proteinen Fach Klasse Überthema Feinthema Zeit Chemie Q2 Aminosäuren, Peptide, Polypeptide Proteine 20 Minuten Zusammenfassung: Die Gerinnung von Eiklar wird durch Zugabe von gesättigter
V11 Gerinnung von Proteinen Fach Klasse Überthema Feinthema Zeit Chemie Q2 Aminosäuren, Peptide, Polypeptide Proteine 20 Minuten Zusammenfassung: Die Gerinnung von Eiklar wird durch Zugabe von gesättigter
Ionenaustausch & Ionenaustauscher
 Entsalzung durch Ionenaustausch LÖUNGEN eite 1 von 7 Ionenaustausch & Ionenaustauscher Lernziele Nach der Bearbeitung dieses Übungsblattes sollten ie Folgendes mitnehmen. - ie wissen, was ein Ionenaustauscher
Entsalzung durch Ionenaustausch LÖUNGEN eite 1 von 7 Ionenaustausch & Ionenaustauscher Lernziele Nach der Bearbeitung dieses Übungsblattes sollten ie Folgendes mitnehmen. - ie wissen, was ein Ionenaustauscher
Superabsorber auf Basis nachwachsender Rohstoffe
 1 Superabsorber auf Basis nachwachsender Rohstoffe Funktionsprinzip von Superabsorbern Superabsorber sind Materialien, die das 20- bis mehrere 100-fache ihrer Masse an Flüssigkeiten aufnehmen können und
1 Superabsorber auf Basis nachwachsender Rohstoffe Funktionsprinzip von Superabsorbern Superabsorber sind Materialien, die das 20- bis mehrere 100-fache ihrer Masse an Flüssigkeiten aufnehmen können und
Superabsorber Unterrichtsidee Malte Bonewitz, 2013
 Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Superabsorber Unterrichtsidee Malte Bonewitz, 2013 Technische Universität Dortmund Fakultät Rehabilitationswissenschaften
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Superabsorber Unterrichtsidee Malte Bonewitz, 2013 Technische Universität Dortmund Fakultät Rehabilitationswissenschaften
Versuch: Emulgierende und dispergierende Wirkung von Tensiden
 Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Philipps-Universität Marburg 18.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Emulgierende
Institut für Anorganische Chemie (Materialchemie)
 1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
1. Gib auf das Blatt Papier 2 Teelöffel Sand, 2 Teelöffel Kochsalz und einige kleine Nägel. 2. Vermische die drei Stoffe gut miteinander. Du hast jetzt ein so genanntes Gemenge hergestellt. 3. Zur Abtrennung
V 1 Herstellung von Natriumchlorid
 1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
1 V 1 Herstellung von Natriumchlorid In diesem Versuch wird Natriumchlorid, im Alltag als Kochsalz bekannt, aus den Edukten Natrium und Chlorgas hergestellt. Dieser Versuch ist eine Reaktion zwischen einem
Schulversuch (Gruppe 13/Assistentenversuch): Quellfähigkeit eines Superabsorbers
 Philipps-Universität Marburg 20.01.2009 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß W 2008/09 Assistent: Tobias Gerhardt chulversuch (Gruppe 13/Assistentenversuch):
Philipps-Universität Marburg 20.01.2009 rganisch-chemisches Praktikum für das Lehramt (LA) Torsten Lasse Leitung: Dr. P. Reiß W 2008/09 Assistent: Tobias Gerhardt chulversuch (Gruppe 13/Assistentenversuch):
Chemie Zusammenfassung III
 Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Konzentrationsbestimmung mit Lösungen
 Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Kapitel 5 Konzentrationsbestimmung mit Lösungen Abb. 5.1: Die Farben von Universalindikatoren sind nützlich für Konzentrationsbestimmungen. Sie lernen auf den folgenden Seiten eine sehr nützliche Methode
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Hochwasserschutz. Selbstabdichtende Türen und Fenster mit Hilfe von Superabsorber. Kilian Günthner (11)
 Hochwasserschutz Selbstabdichtende Türen und Fenster mit Hilfe von Superabsorber Kilian Günthner (11) Gliederung 1. Kurzfassung... 3 2. Idee... 3 3. Das Material... 6 3.1 Die Superabsorberkörnchen... 6
Hochwasserschutz Selbstabdichtende Türen und Fenster mit Hilfe von Superabsorber Kilian Günthner (11) Gliederung 1. Kurzfassung... 3 2. Idee... 3 3. Das Material... 6 3.1 Die Superabsorberkörnchen... 6
Versuch: Fäden spinnen Polymer aus Citronensäure und Glycerin
 Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Untersuche das Verhalten von Zitronensäure gegenüber verschiedene Stoffen in Wasser und in Aceton.
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758500).6 Brönstedt Säuren - Aciditätvergleich einer wässrigen und einer acetonischen Citronensäurel Experiment von: Phywe Gedruckt: 5.0.203
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P758500).6 Brönstedt Säuren - Aciditätvergleich einer wässrigen und einer acetonischen Citronensäurel Experiment von: Phywe Gedruckt: 5.0.203
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Diffusion und Osmose. Osmose 1
 Osmose 1 Diffusion und Osmose In flüssigen oder gasförmigen Medien sind die Moleküle in ständiger Bewegung. Sie bewegen sich gradlinig, bis sie auf ein anderes Molekül stossen. Diese Bewegung führt mit
Osmose 1 Diffusion und Osmose In flüssigen oder gasförmigen Medien sind die Moleküle in ständiger Bewegung. Sie bewegen sich gradlinig, bis sie auf ein anderes Molekül stossen. Diese Bewegung führt mit
Schulversuchspraktikum. Carl Föst. Sommersemester Klassenstufen 5 & 6. Einfache Messgeräte
 Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 5 & 6 Einfache Messgeräte 1 1 Auf einen Blick: In dieser Versuchsreihe geht es um den Bau von Messinstrumenten für Temperatur, Luftfeuchtigkeit
Schulversuchspraktikum Carl Föst Sommersemester 2015 Klassenstufen 5 & 6 Einfache Messgeräte 1 1 Auf einen Blick: In dieser Versuchsreihe geht es um den Bau von Messinstrumenten für Temperatur, Luftfeuchtigkeit
Gruppe 05: Alkylchloride gegenüber AgNO 3
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Fortbildung am Schülerlabor in Rechtenthal für die Grundschule. Ideen zu weiterführenden Versuchen in der Klasse:
 Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Reinigen mit Zitronensäure
 V4 Reinigen mit Zitronensäure Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Zitronensäure 30 Minuten Zusammenfassung: Beim dem Versuch werden zitronenhaltige Lösungen zum
V4 Reinigen mit Zitronensäure Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Zitronensäure 30 Minuten Zusammenfassung: Beim dem Versuch werden zitronenhaltige Lösungen zum
Ionisierungsenergie und Elektronenaffinität. Bindigkeit Valenzstrichformel Molekülgeometrie
 Tendenzen im Periodensystem Ionisierungsenergie und Elektronenaffinität Atombindung (Elektronenpaarbindung) Bindigkeit Valenzstrichformel Molekülgeometrie Räumlicher Bau einfacher Moleküle Polare Atombindung
Tendenzen im Periodensystem Ionisierungsenergie und Elektronenaffinität Atombindung (Elektronenpaarbindung) Bindigkeit Valenzstrichformel Molekülgeometrie Räumlicher Bau einfacher Moleküle Polare Atombindung
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Schulversuchspraktikum. Maximilian Konrad. Sommersemester Klassenstufen 11 & 12. Kunststoffe
 Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 11 & 12 Kunststoffe 1 Konzept und Ziele 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält 2 Lehrerversuche
Schulversuchspraktikum Maximilian Konrad Sommersemester 2012 Klassenstufen 11 & 12 Kunststoffe 1 Konzept und Ziele 2 Auf einen Blick: Diese Unterrichtseinheit für die Klassen 11 und 12 enthält 2 Lehrerversuche
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1. Bsp.: Grundwissen 9.Klasse NTG 2 Grundwissen 9.Klasse NTG 2
 Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1 Die Stoffmenge n = 1mol ist die Stoffportion, die 6,022 10 23 Teilchen enthält. Die Stoffmenge n n(he) = 1 mol n(h 2 ) = 1 mol enthält 6,022 10 23
Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1 Die Stoffmenge n = 1mol ist die Stoffportion, die 6,022 10 23 Teilchen enthält. Die Stoffmenge n n(he) = 1 mol n(h 2 ) = 1 mol enthält 6,022 10 23
Inhaltlicher Schwerpunkt: Organische Verbindungen und Reaktionswege
 Unterrichtvorhaben 1: Kontext: Maßgeschneiderte Produkte aus Kunststoffen Grundkurs Qualifikationsphase 2 Unterrichtsvorhaben 2: Kontext: Wenn das Erdöl zu Ende geht UF2 Auswahl UF4 Vernetzung E3 Hypothesen
Unterrichtvorhaben 1: Kontext: Maßgeschneiderte Produkte aus Kunststoffen Grundkurs Qualifikationsphase 2 Unterrichtsvorhaben 2: Kontext: Wenn das Erdöl zu Ende geht UF2 Auswahl UF4 Vernetzung E3 Hypothesen
Experimente Arbeitsblatt
 Lehrerinformation 1/6 Arbeitsauftrag Die SuS führen nacheinander verschiedene Versuche durch und protokollieren ihre Beobachtungen. Ziel Die SuS verstehen die chemischen Prozesse und die naturwissenschaftlichen
Lehrerinformation 1/6 Arbeitsauftrag Die SuS führen nacheinander verschiedene Versuche durch und protokollieren ihre Beobachtungen. Ziel Die SuS verstehen die chemischen Prozesse und die naturwissenschaftlichen
Gruppe 13: Mischpolymerisation von Styrol und Maleinsäureanhydrid
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Reaktion: Gruppe 13: Mischpolymerisation von Styrol und Maleinsäureanhydrid
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Reaktion: Gruppe 13: Mischpolymerisation von Styrol und Maleinsäureanhydrid
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1/2 Basiskonzept Struktur-Eigenschaft
 Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1/2 Basiskonzept Struktur-Eigenschaft Ch-GK Q1/IHF 4: Unterrichtsvorhaben I: Inhaltliche Schwerpunkte:
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1/2 Basiskonzept Struktur-Eigenschaft Ch-GK Q1/IHF 4: Unterrichtsvorhaben I: Inhaltliche Schwerpunkte:
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Konsequenzen der Ozeanversauerung
 Thema: Stoffkreisläufe Jahrgang 9 & 10 Konsequenzen der Ozeanversauerung Lies den Ausschnitt aus dem nachfolgenden Zeitungsartikel eines Wissenschaftsmagazins aufmerksam durch und betrachte im Diagramm
Thema: Stoffkreisläufe Jahrgang 9 & 10 Konsequenzen der Ozeanversauerung Lies den Ausschnitt aus dem nachfolgenden Zeitungsartikel eines Wissenschaftsmagazins aufmerksam durch und betrachte im Diagramm
Alltäglichen Phänomenen auf der Spur VS Tobadill
 Feuer und Luft Alltäglichen Phänomenen auf der Spur VS Tobadill 2 INHALTSVERZEICHNIS 1. EINLEITUNG 4 2. METHODEN UND VORGEHENSWEISE 4 3. BEISPIELE VON EXPERIMENTEN AUS UNSERER FORSCHUNG 5 ZWEI GUMMIBÄRCHEN
Feuer und Luft Alltäglichen Phänomenen auf der Spur VS Tobadill 2 INHALTSVERZEICHNIS 1. EINLEITUNG 4 2. METHODEN UND VORGEHENSWEISE 4 3. BEISPIELE VON EXPERIMENTEN AUS UNSERER FORSCHUNG 5 ZWEI GUMMIBÄRCHEN
Schulversuchspraktikum. Johanna Osterloh. Sommersemester Klassenstufen 9 & 10. Stoffkreisläufe. Kurzprotokoll
 Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 9 & 10 Stoffkreisläufe Kurzprotokoll Auf einen Blick: Dieses Protokoll enthält vier Schülerversuche, die zum Thema Kohlenstoffdioxidkreislauf
Schulversuchspraktikum Johanna Osterloh Sommersemester 2015 Klassenstufen 9 & 10 Stoffkreisläufe Kurzprotokoll Auf einen Blick: Dieses Protokoll enthält vier Schülerversuche, die zum Thema Kohlenstoffdioxidkreislauf
Ionenbindung Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Sozialform Zeit Die SuS erarbeiten sich chemische Informationen zu Kochsalz. Sie kennen die Bestandteile und wissen, wie Salz chemisch aufgebaut ist.
Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Sozialform Zeit Die SuS erarbeiten sich chemische Informationen zu Kochsalz. Sie kennen die Bestandteile und wissen, wie Salz chemisch aufgebaut ist.
Säuren und Basen. Biology with Vernier Versuch Nr. 3 Schülerversion LERNZIELE
 Biology with Vernier Versuch Nr. 3 Schülerversion n und n Organismen reagieren oft sehr empfindlich auf die Auswirkungen von n und n in ihrer Umgebung. Sie müssen zum Überleben einen stabilen inneren ph-wert
Biology with Vernier Versuch Nr. 3 Schülerversion n und n Organismen reagieren oft sehr empfindlich auf die Auswirkungen von n und n in ihrer Umgebung. Sie müssen zum Überleben einen stabilen inneren ph-wert
II. KRÄFTE ZWISCHEN ELEKTRISCH GELADENEN KÖRPERN
 KLASSE: DATUM: NAMEN: I. GRUNDLAGEN Schon bei den alten Griechen war bekannt, dass zwischen Bernstein und Wollfasern (oder Federn) anziehende Kräfte entstehen können, wenn der Bernstein mit einem Wolltuch
KLASSE: DATUM: NAMEN: I. GRUNDLAGEN Schon bei den alten Griechen war bekannt, dass zwischen Bernstein und Wollfasern (oder Federn) anziehende Kräfte entstehen können, wenn der Bernstein mit einem Wolltuch
Stoffeigenschaften auf der Spur
 Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Stoffeigenschaften auf der Spur Station 1 Welche Stoffe sind magnetisch? Sicherheit Entsorgung:/ Prüfe, welche Stoffe vom Magneten angezogen werden! Trage deine Beobachtungen in die Tabelle in deinem Forscherbuch
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Korrosion und Korrosionsschutz
 Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7&8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll beinhaltet drei weitere Schülerversuche
Schulversuchspraktikum Christian Köhler Sommersemester 2016 Klassenstufen 7&8 Korrosion und Korrosionsschutz Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll beinhaltet drei weitere Schülerversuche
3.5 Hydrolyse von Salzen. Aufgabe. Reagieren wässrige Salzlösungen neutral? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Lösungen, Salze, Ionen und Elektrolyte
 Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Schülerversuche mit Präsentation rund um die Osmose
 Schülerversuche mit Präsentation rund um die Osmose Mögliche Experimente: Übersicht 1 2 3 Experiment Pflanzenstängel in demineralisiertem Wasser bzw. in Salzlösung Pflanzengewebe in Salzlösungen unterschiedlicher
Schülerversuche mit Präsentation rund um die Osmose Mögliche Experimente: Übersicht 1 2 3 Experiment Pflanzenstängel in demineralisiertem Wasser bzw. in Salzlösung Pflanzengewebe in Salzlösungen unterschiedlicher
Waschmittel auf Bäumen
 Datum:.11.015 Schüler: Daniel Tetla Schule: Gymnasium Friedrich Ebert Klasse: T1 Waschmittel auf Bäumen 1a. Versuch Herstellen einer Waschlauge aus Kastanien und Untersuchung ihrer Geräte: Material: Waage
Datum:.11.015 Schüler: Daniel Tetla Schule: Gymnasium Friedrich Ebert Klasse: T1 Waschmittel auf Bäumen 1a. Versuch Herstellen einer Waschlauge aus Kastanien und Untersuchung ihrer Geräte: Material: Waage
Kernlehrpläne ab Schuljahr 2014/15 Schuleigener Lehrplan / FMG / Sekundarstufe II CHEMIE
 CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
CHEMIE QUALIFIKATIONSSPHASE 2 LEISTUNGSKURS Konkretisierung der Unterrichtsvorhaben Unterrichtsvorhaben I: Vom fossilen Rohstoff zum Anwendungsprodukt Organische Reaktionsabläufe Oxidationsreihe der Alkohole
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008
 Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: [email protected] 1. Abstract
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: [email protected] 1. Abstract
Schuljahrgänge 9 und Schwierige Geburt Chemie wird
 Schuljahrgänge 9 und 10 5.1 Schwierige Geburt Chemie wird - ordnen Elemente bestimmten Naturwissenschaft 5.2 In Reih und Glied das Periodensystem - ordnen Elemente bestimmten - verknüpfen Stoff- und Teilchenebene.
Schuljahrgänge 9 und 10 5.1 Schwierige Geburt Chemie wird - ordnen Elemente bestimmten Naturwissenschaft 5.2 In Reih und Glied das Periodensystem - ordnen Elemente bestimmten - verknüpfen Stoff- und Teilchenebene.
Titration von Aminosäuren, Lösung. 1. Aufnahme der Titrationskurve
 1. Aufnahme der Titrationskurve Beobachtung: Zu Beginn hat die Lösung einen ph-wert von etwa 2. Der ph-wert steigt nur langsam. Nach Zugabe von etwa 9 ml Natronlauge steigt der ph-wert sprunghaft an. Anschießend
1. Aufnahme der Titrationskurve Beobachtung: Zu Beginn hat die Lösung einen ph-wert von etwa 2. Der ph-wert steigt nur langsam. Nach Zugabe von etwa 9 ml Natronlauge steigt der ph-wert sprunghaft an. Anschießend
SÄUR E. BASE oder LAU GE SAUE R BASI SCH
 SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
Eigenschaften von Tensidlösungen
 V17 Eigenschaften von Tensidlösungen Fach Klasse Überthema Feinthema Zeit Chemie Q4 Grenzflächenaktive Substanzen Eigenschaften von Tenisden 30 Minuten Zusammenfassung Bei dem Versuch werden die Eigenschaften
V17 Eigenschaften von Tensidlösungen Fach Klasse Überthema Feinthema Zeit Chemie Q4 Grenzflächenaktive Substanzen Eigenschaften von Tenisden 30 Minuten Zusammenfassung Bei dem Versuch werden die Eigenschaften
Versuchsprotokoll: Stärkefolie
 Versuchsprotokoll: Stärkefolie Zeitaufwand: Aufbau: 10 Minuten Durchführung: 30 Minuten + 1 Tag trocknen Abbau: 10 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Kartoffel-
Versuchsprotokoll: Stärkefolie Zeitaufwand: Aufbau: 10 Minuten Durchführung: 30 Minuten + 1 Tag trocknen Abbau: 10 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Kartoffel-
1 Lehrerversuch Alkalimetalle in Wasser
 1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
Prime Slime. der Spielzeug-Hit der 70er Jahre. feucht, kalt und schwabbelig. für kleine und grosse Kinder. macht Kinderparties unvergesslich
 01/2017 Prime Slime der Spielzeug-Hit der 70er Jahre feucht, kalt und schwabbelig für kleine und grosse Kinder macht Kinderparties unvergesslich chemische Vernetzung am praktischen Beispiel www.magicscience.ch
01/2017 Prime Slime der Spielzeug-Hit der 70er Jahre feucht, kalt und schwabbelig für kleine und grosse Kinder macht Kinderparties unvergesslich chemische Vernetzung am praktischen Beispiel www.magicscience.ch
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Titel des Mysterys: Magic Sand
 Titel des Mysterys: Von J. Dittmar und I. Eilks Universität Bremen Titel: Übersicht: Fach: Fachinhalte:. Jahrgangsstufe(n): Dauer: Gruppengröße: Beim handelt es sich um eine besondere Art von Sand. Obwohl
Titel des Mysterys: Von J. Dittmar und I. Eilks Universität Bremen Titel: Übersicht: Fach: Fachinhalte:. Jahrgangsstufe(n): Dauer: Gruppengröße: Beim handelt es sich um eine besondere Art von Sand. Obwohl
Wasser. von. PH Vorarlberg Seite 1 Blum Gabriela. cc-gabriela Blum
 Wasser cc-gabriela Blum von PH Vorarlberg Seite 1 Blum Gabriela Forscherauftrag Nr. 1 Was schwimmt, was sinkt? Gefäß mit Wasser Gegenstände wie Styropor, Stein, Blatt Papier, Holz, und vieles mehr einfach
Wasser cc-gabriela Blum von PH Vorarlberg Seite 1 Blum Gabriela Forscherauftrag Nr. 1 Was schwimmt, was sinkt? Gefäß mit Wasser Gegenstände wie Styropor, Stein, Blatt Papier, Holz, und vieles mehr einfach
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)
 Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Kohlenstoffverbindungen und Gleichgewichtsreaktionen (EF)... interpretieren den zeitlichen Ablauf chemischer Reaktionen in Abhängigkeit von verschiedenen Parametern (u.a. Oberfläche, Konzentration, Temperatur)
Crashkurs Säure-Base
 Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Das Wasser - Kinder experimentieren. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Das Wasser - Kinder experimentieren Das komplette Material finden Sie hier: School-Scout.de Titel: Kinder experimentieren: Wasser
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Das Wasser - Kinder experimentieren Das komplette Material finden Sie hier: School-Scout.de Titel: Kinder experimentieren: Wasser
Endotherm und Exotherm
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 7 & 8 Endotherm und Exotherm Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 7 und 8 einen Lehrerversuch und einen
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Kolloidchemie. Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 5; Verfasser: Philippe Knüsel
 Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 5; 26.11.2008 Kolloidchemie Verfasser: Philippe Knüsel ([email protected]) Versuchsdurchführung: Claudio Zihlmann und Philippe Knüsel Assistenz: David
Praktikum I, Teil Werkstoffe HS 2008/09 Versuch 5; 26.11.2008 Kolloidchemie Verfasser: Philippe Knüsel ([email protected]) Versuchsdurchführung: Claudio Zihlmann und Philippe Knüsel Assistenz: David
1/51. Protolysereaktion HCl + H2O + Protonenakzeptor: Ein H2O-Molekül. Protonendonator: Ein HCl-Molekül
 Protolysereaktion HCl + H2O + 1/51 - Protonendonator: Ein HCl-Molekül Protonenakzeptor: Ein H2O-Molekül Protolyse + 2/51 - Protolyse: Ein Proton "wandert" von einem Protonendonator zu einem Protonenakzeptor.
Protolysereaktion HCl + H2O + 1/51 - Protonendonator: Ein HCl-Molekül Protonenakzeptor: Ein H2O-Molekül Protolyse + 2/51 - Protolyse: Ein Proton "wandert" von einem Protonendonator zu einem Protonenakzeptor.
Die Zelle. Membranen: Struktur und Funktion
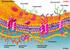 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
GYMNASIUM ISERNHAGEN. Schulinternes Curriculum 9. Jg. (epochal) Fächerverbindende. Fachspezifische. Thema Kompetenzen Methoden
 Fachbereich CHEMIE GYMNASIUM ISERNHAGEN Schulinternes Curriculum 9. Jg. (epochal) Thema Kompetenzen Methoden Chemische Reaktionen auf Teilchenebene differenziert erklären Gase sind aus Atomen oder Molekülen
Fachbereich CHEMIE GYMNASIUM ISERNHAGEN Schulinternes Curriculum 9. Jg. (epochal) Thema Kompetenzen Methoden Chemische Reaktionen auf Teilchenebene differenziert erklären Gase sind aus Atomen oder Molekülen
Experimente lösen und den Effekt nachvollziehen. Die Sch steigen einfach und spielerisch ins Thema ein.
 ARBEITSBESCHRIEB Arbeitsauftrag: Was funktioniert wieso? Die Sch sehen ein spannendes technisches Experiment. Sie müssen herausfinden, was passiert und wie der Effekt für technische Lösungen verwendet
ARBEITSBESCHRIEB Arbeitsauftrag: Was funktioniert wieso? Die Sch sehen ein spannendes technisches Experiment. Sie müssen herausfinden, was passiert und wie der Effekt für technische Lösungen verwendet
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Mische einige Stoffe mit Wasser und untersuche die entstandenen Gemischarten.
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P754800) 3.4 Lösungen, Kolloide, Suspensionen Experiment von: Seb Gedruckt: 24.03.204 :28:39 intertess
1.3 Herstellung des Sirups und des Erfrischungsgetränks
 1 Versuchsdurchführung 1.1 Herstellung der Rohemulsion 300g Rohemulsion wird aus den folgenden Komponenten hergestellt: Disperse Phase: Kontinuierliche Phase: Emulgator: 30 g Aromaöl 243 g Wasser 27 g
1 Versuchsdurchführung 1.1 Herstellung der Rohemulsion 300g Rohemulsion wird aus den folgenden Komponenten hergestellt: Disperse Phase: Kontinuierliche Phase: Emulgator: 30 g Aromaöl 243 g Wasser 27 g
Standortbestimmung / Äquivalenzprüfung. Chemie. Mittwoch, 13. April 2016, Uhr
 Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Umwelt und Recycling
 Schulversuchspraktikum Anonym_16 Sommersemester 2016 Klassenstufen 5 & 6 Umwelt und Recycling Kurzprotokoll Auf einen Blick: Versuch 1 und 2 behandeln die Problematik der Meeresverschmutzung mit Ölen.
Schulversuchspraktikum Anonym_16 Sommersemester 2016 Klassenstufen 5 & 6 Umwelt und Recycling Kurzprotokoll Auf einen Blick: Versuch 1 und 2 behandeln die Problematik der Meeresverschmutzung mit Ölen.
Wir untersuchen Mineralwasser
 Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Wir untersuchen Mineralwasser Jeder von uns kennt es: Mineralwasser. Im Geschäft wird es mit viel, wenig oder gar keiner Kohlensäure angeboten. Kohlensäure beschreibt die Form, in der das Gas Kohlenstoffdioxid
Das Salz in unserer Suppe
 Das Salz in unserer Suppe Aufgabe 1 In der Küche verwendet man oft zwei Arten von Salz. Das eine ist Steinsalz und das andere ist Meersalz. Das Meerwasser im Mittelmeer enthält 3,8 % Salz, im Toten Meer
Das Salz in unserer Suppe Aufgabe 1 In der Küche verwendet man oft zwei Arten von Salz. Das eine ist Steinsalz und das andere ist Meersalz. Das Meerwasser im Mittelmeer enthält 3,8 % Salz, im Toten Meer
Arbeitsblatt Ist groß besser als klein?
 Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
Arbeitsblatt Ist groß besser als klein? Aufgabe 1: Führe folgendes Experiment durch und notiere deine Beobachtungen. Materialien: 4 Reagenzgläser, Reagenzglasständer, Spatel Chemikalien: Gefahrenstoffe
2 Elektrische Ladung, Strom, Spannung
 2 Elektrische Ladung, Strom, Spannung In diesem Kapitel lernen Sie, ein Grundverständnis der Elektrizität zur Beschäftigung mit Elektronik, welche physikalischen Grundgrößen in der Elektronik verwendet
2 Elektrische Ladung, Strom, Spannung In diesem Kapitel lernen Sie, ein Grundverständnis der Elektrizität zur Beschäftigung mit Elektronik, welche physikalischen Grundgrößen in der Elektronik verwendet
Erftgymnasium der Stadt Bergheim. Schulinternes Curriculum für das Fach Chemie in der Sekundarstufe II
 Erftgymnasium der Stadt Bergheim Schulinternes Curriculum für das Fach Chemie in der Sekundarstufe II Als Fortführung des Unterrichts in der Sekundarstufe I wird Schülerinnen und Schülern ein anwendungs-
Erftgymnasium der Stadt Bergheim Schulinternes Curriculum für das Fach Chemie in der Sekundarstufe II Als Fortführung des Unterrichts in der Sekundarstufe I wird Schülerinnen und Schülern ein anwendungs-
Gefahrenstoffe H:
 V1 Verseifungsgeschwindigkeit eines Esters In diesem Versuch wird die Reaktionsgeschwindigkeit quantitativ ermittelt. Da dies anhand einer Verseifung eines Esters geschieht, sollten die Schülerinnen und
V1 Verseifungsgeschwindigkeit eines Esters In diesem Versuch wird die Reaktionsgeschwindigkeit quantitativ ermittelt. Da dies anhand einer Verseifung eines Esters geschieht, sollten die Schülerinnen und
Konfitüre selbst machen ist im Grunde ein Kinderspiel: Man vermischt Zucker und Früchte, kocht sie eine Weile und füllt die erhaltene Masse ab.
 Wie aus Erdbeeren Marmelade wird "Konfitüre selbst machen ist im Grunde ein Kinderspiel: Man vermischt Zucker und Früchte, kocht sie eine Weile und füllt die erhaltene Masse ab." (Quelle: Hervé This-Benckhard,
Wie aus Erdbeeren Marmelade wird "Konfitüre selbst machen ist im Grunde ein Kinderspiel: Man vermischt Zucker und Früchte, kocht sie eine Weile und füllt die erhaltene Masse ab." (Quelle: Hervé This-Benckhard,
GEFÄHRDUNGSBEURT BADEN - WÜRTTEMBERG. Chemie. Gesamtband _2CBBH_ U1+U4_SI 1
 GEFÄHRDUNGSBEURT EILUNGEN BADEN - WÜRTTEMBERG Chemie Gesamtband _2CBBH_9783060156900 U1+U4_SI 1 06.02.17 12:37 Eine Welt aus en In ruhigem Wasser Wirf mit der Pinzette einen einzigen Kristall Kaliumpermanganat
GEFÄHRDUNGSBEURT EILUNGEN BADEN - WÜRTTEMBERG Chemie Gesamtband _2CBBH_9783060156900 U1+U4_SI 1 06.02.17 12:37 Eine Welt aus en In ruhigem Wasser Wirf mit der Pinzette einen einzigen Kristall Kaliumpermanganat
Experiment Lehrerinformation
 Lehrerinformation 1/6 Arbeitsauftrag Was funktioniert wieso? Die SuS sehen ein spannendes technisches. Sie müssen herausfinden, was passiert und wie der Effekt für technische Lösungen verwendet wird. Ziel
Lehrerinformation 1/6 Arbeitsauftrag Was funktioniert wieso? Die SuS sehen ein spannendes technisches. Sie müssen herausfinden, was passiert und wie der Effekt für technische Lösungen verwendet wird. Ziel
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 2: Unterrichtsvorhaben I:
 Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 2: Unterrichtsvorhaben I: Kontext: Säuren und Basen in Alltagsprodukten Inhaltsfeld: Säuren,
Vorschlag zur Planung der Unterrichtsvorhaben unter Einbezug der Kompetenzen - Qualifikationsphase 1 Ch-GK Q1/IHF 2: Unterrichtsvorhaben I: Kontext: Säuren und Basen in Alltagsprodukten Inhaltsfeld: Säuren,
Stelle Stoffgemische aus Flüssigkeiten her und untersuche ihre Eigenschaften.
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
3.7 Osmose - Chemischer Garten. Aufgabe. Wie lösen sich Salze in Wasserglas? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P760000) 3.7 Osmose - Chemischer Garten Experiment von: Phywe Gedruckt: 5.0.203 2:25:55 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P760000) 3.7 Osmose - Chemischer Garten Experiment von: Phywe Gedruckt: 5.0.203 2:25:55 intertess (Version 3.06 B200, Export 2000) Aufgabe
Martin Raiber Chemie Protokoll Nr Gruppe 2 (Schrankseite) Untersuchung von Glycin
 Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Vorversuch: Milch, Quark und Molke
 Name: Datum: Vorversuch: Materialien: Becherglas (250 ml), Messzylinder (100 ml), 30 ml Milch, 10 ml Essig Durchführung: 1. Miss 30 ml Milch mit dem Messzylinder ab. 2. Gib die Milch in das Becherglas.
Name: Datum: Vorversuch: Materialien: Becherglas (250 ml), Messzylinder (100 ml), 30 ml Milch, 10 ml Essig Durchführung: 1. Miss 30 ml Milch mit dem Messzylinder ab. 2. Gib die Milch in das Becherglas.
Experiment Nr. 1: Wasser hat eine Haut. 1. Lege das Seidenpapier vorsichtig auf die Wasseroberfläche.
 Experiment Nr. 1: Wasser hat eine Haut Siehe Pädagogische Unterlagen, Seite 6, 1: Was ist Wasser? Wasser hat eine erhöhte Oberflächenspannung ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines
Experiment Nr. 1: Wasser hat eine Haut Siehe Pädagogische Unterlagen, Seite 6, 1: Was ist Wasser? Wasser hat eine erhöhte Oberflächenspannung ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Versuchsprotokoll. Züchtung von Kandiszucker-Kristallen
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
