ISOPROTSESSID Koostanud: Janno Puks
|
|
|
- Insa Dieter
- vor 6 Jahren
- Abrufe
Transkript
1 ISOPROTSESSID Koostanud: Janno Puks Soojusõpetus on füüsika osa, mis hõlmab molekulaarfüüsikat, termodünaamikat, aine ehituse aluseid ja faasisiirdeid. Molekulaarfüüsika kirjeldab ainete omadusi, tuginedes eeldustele, et : 1) kõik ained koosnevad molekulidest, 2) molekulid on pidevas kaootilises liikumises, 3) molekulide vahel on vastastikmõju ( tõmbe- ja tõukejõud) Soojusnähtuseid kirjeldatakse parameetrite abil. Parameeter on mingi füüsikaline suurus, mis kirjeldab aine olekut või omadusi (N: vedeliku ruumala, molekuli mass jt) Makroparameetrid on füüsikalised suurused, mida kasutatakse ainekoguse kui terviku soojusliku oleku kirjeldamisel (N: ainekoguse mass, rõhk, ruumala jt). Suurusi rõhk, ruumala ja temperatuur nimetatakse ka olekuparameetriteks. Olek on ainekoguse seisund, mis on määratud olekuparameetrite konkreetsete väärtuste kogumiga. Kui ühte olekuparameetrit muuta, siis muutub ka vähemalt üks teine olekuparameetritest. Mikroparameetrid on füüsikalised suurused, mida kasutatakse aine üksiku molekuli kirjeldamisel (N: molekuli mass, molekuli keskmine kiirus, molekuli keskmine kineetiline energia, kontsentratsioon jt). Seega on mikroparameetrid seotud molekulide ja nende liikumisega. Termodünaamika on füüsika osa, mis käsitleb soojusvahetust, soojuse muudnumist tööks ning muid soojusvahetusega soenduvaid nähtusi. Aine ehitus käsitleb erinevusi gaaside, vedelike, tahkiste struktuuris ja sellest tulenevaid erinevusi ülekande nähtustes (N. Difusioon, isehõõre, soojusjuhtivus jt) Faasisiirded käsitlevad üleminekuid ainete erinevate faaside (gaas, vedelik, tahkis) vahel. TEMPERATUUR Temperatuur on füüsikaline suurus, mis iseloomustab keha soojuslikku seisundit ja se on määratud keha molekulide soojusliikumise kineetilie energiaga. Temperatuurist olenevad paljud füüsikalised suurused (N: ruumala, rõhk, tihedus, pindpinevustegur, sisehõõrdetegur, eritakistus jt). Üheks levinumaks võtteks temperatuuri mõõtmisel on ainete soojuspaisumise kasutamine. Absoluutseks nulltemperatuuriks nimetatakse temperatuuri, kus molekulide kineetiline energia võrdub nulliga. Sel juhul molekul enam ei liigu, ei põrku vastu anuma seina, ei võngu ega avalda ka rõhku. Absoluutse nulli mõiste tõi füüsikasse sisse inglise teadlane William Thomson (lord Kelvin) ja see on null kelvinit (0 K) ehk -273,15 0 C. Absoluutsest nullist madalamat temperatuuri olla ei saa. Temperatuuri mõõtmiseks kasutatakse erinevaid skaalasid aastast alates kasutatakse Celsiuse skaalat, mille aluseks on jää sulamistemperatuuri ja vee keemistemperatuuri võrdseks sajaks osaks jaotamine. Celsiuse skaalal temperatuuri tähiseks on tavaliselt t ja Kelvini skaalal on temperatuuri tähiseks T. T = t C t = T C
2 Näiteks: 20 0 C = C = 293 K 250 K = C = C Suurbriannias ja Ameerikas kasutatakse aastal taani füüsiku Daniel Gabriel Fahrenheit poolt kasutusele võetud Fahreinheit temperatuuriskaalat. Selle skaalal on null fahrenheit kraadiks jää ja amooniumkloriidi ehk salmiaagi (NH 4 Cl) segu temperatuur ja sada fahrenheit kraadiks inimese normaalne kehatemperatuur. Jää sulamistemperatuur on Fahrenheit i skaalas 32 0 F ja vee keemistemperatuur F. Celsius Fahrenheiti kaudu: C = ( F 32) : 1,8 Fahrenheit Celsiuse kaudu: F = ( C * 1,8) + 32 Näiteks: 20 C = (20 C * 1,8) + 32 = 68 F 160 F = (160 F - 32) : 1,8 = 71,1 C RÕHK Rõhk on füüsikalne suurus, mis näitab ühikulisele (mingi kindla arvväärtusega) pinnale risti mõjuvat jõudu. p - rõhk (Pa, paskal) F pinnale risti jõud (N, njuuton) S pindala (m 2 ) Normaalrõhuks loetakse 760 mm/hg ehk 760 millimeetrit elavhõbeda sammast, mis on Pa (paskaliga). Kasutusel on ka teisi rõhuühikuid nagu näiteks atmosfäärid (atm) ja baarid (bar) jt. 1 atm = Pa 1 bar = Pa ehk 10 5 Pa. Seega normaalne (õhu)rõhk atmosfääris: 760 mm/hg = Pa = 1 atm = 1,01325 bar IDEAALSE GAASI OLEKUVÕRRAND Ideaalne gaas on tegeliku ehk reaalse gaasi mudel, kus: 1) molekulid loetakse punktmassideks, 2) molekulide põrgetel anuma seinaga nende kiiruste väärtus ei muutu, kuid muutub vaid kiiruse suund, 3) molekulidevahelist vastastikmõju ei arvestata. Ideaalse gaasi olekuvõrrand ehk Mendelejevi-Clapeyroni võrrand: p rõhk (Pa) V gaasi ruumala (m 3 ) m gaasi mass (kg) M gaasi molaarmass (kg/mol) R universaalne gaasikonstant: 8,31 (J / mol *K) T gaasi temperatuur (K) NB! Molaarmass tuleb leida keemiliste elementide perioodilisustabelist! See on seal ühikutes grammi mooli kohta, kuid füüsikas tuleb see teisendada kilogrammi mooli kohta. Näiteks süsihapegaasi ehk CO 2 molaarmass on 44 g/mol, mis võrdub 0,044 kg/mol.
3 ISOBAARILINE PROTSESS Isobaariline protsess on siis, kui gaasi rõhk ei muutu ehk jääval rõhul on gaasi ruumala ja temperatuur võrdelises sõltuvuses. Seda protsessi kutsutakse ka Gay-Lussac`i seaduseks. p = const ISOHOORILINE PROTSESS Isohooriline protsess on siis, kui gaasi ruumala ei muutu ehk jääval ruumalal on gaasi rõhk ja temperatuur võrdelises sõltuvuses. Seda protsessi kutsutakse ka Charles`i seaduseks. V = const ISOTERMILINE PROTSESS Isotermiline on protsess, kui gaasi temperatuur ei muutu ehk jääval temperatuuril on gaasi rõhk ja ruumala pöördvõrdelises sõltuvuses. Seda protsessi kutsutakse ka Boyle`i-Mariotte`i seaduseks. T = const
4 GAASI OLEKUVÕRRAND Gaasi olekuvõrrandiks nimetatakse protsessi, kus muutuvad gaasi rõhk, temperatuur ja ruumala, kuid gaasi mass ei muutu. Seda võrrandit nimetatakse ka Clapeyroni võrrandiks. ÜLESANDED 1) Sauna leiliruumi temperatuur oli 90 0 C ja rõhk 100 kpa. Leia veeauru ruumala, kui saunas olevale kerisele visati üks liiter vett. T = 90 0 C= = 293 K p = 100 kpa = Pa V (H 2 O) = 1 l (NB! See on vedelas olekus vee ruumala, mitte veeauru ruumala!) = 1 dm 3 M (H 2 O) = 18 g/mol = 0,018 kg/mol R = 8,31 J/mol * K V =? Vedela vee ruumalast leida vee mass, tiheduse valemi [ρ (roo) = m : V] kaudu, kus vee tihedus on 1 g/cm 3 ehk 1 kg/ dm 3. Massi saab leida tiheduse valemist: m = ρ * V. Seega m (vee mass) = 1 kg/dm 3 * 1 dm 3 = 1 kg Ülesande lahendamisel kasutatakse ideaalse gaasi olekuvõrrandi valemit: Siit ruumala gaasi V avaldub välja valemiga: Vastus: Saunas olevale kerisele ühe liitri vee viskamisel vabanes 1,67 m 3 veeauru. 2) Silindris olev gaas, mille rõhk oli normaalrõhk ja ruumala 40 cm 3, suruti kokku ruumalale 5 cm 3. Leia kokkusurutud gaasi rõhk megapaskalites, kui temperatuur ei muutu. (Vastus: 810,6 kpa ehk 0,81 MPa). 3) Sooja õhuga täidetud palli ruumala on 400 m 3 ja temperatuur 17 0 C. Gaasileegi mõjul õhk pallis soojenes 30 0 C võrra. Leia palli ruumala pärast soojendamist. (Vastus: 441,4 m 3 ) 4) Auto rehvis oleva õhu temperatuur oli 290 K. Sõites rehvi temperatuur tõusis 315 K-ni ja rõhk tõusis väärtuseni 2,5 * 10 5 Pa. Kui suur oli rehvi rõhk sõidu alguses, kui rehvi ruumala ei muutu? (Vastus: 2,3 * 10 5 Pa)
5 5) Anumas ruumalaga 830 liitrit on 850 grammi ammoniaaki (NH 3 ) temperatuuril 280 K Arvuta gaasi molaarmass ja rõhk anumas kilopaskalites. (Vastus: M(NH 3 ) = 0,017 kg/mol ja p= 140 kpa) 6) Leia 15 dm 3 hapnikupadjas oleva hapniku mass grammides temperatuuril 20 0 C, kui rõhk on 0,2 MPa. (Vastus: hapnikupadja mass on 39,4 g) 7) Aerostaadis ruumalaga 350 m 3 on 35 kg vesinikku rõhul 1,1 * 10 5 Pa. Leia gaasi temperatuur Celsiuse kraadides. (Vastus: vesiniku temperatuur on - 8,3 0 C) 8) Arvuta õhu mass 50 m 3 suuruses toas temperatuuril 7 0 C, kui rõhk on 10 5 Pa. Pärast ahju kütmist tõusis temperatuur 17 0 C-ni. Kui palju õhku väljus toast kütmise ajal? Õhu molaarmass on 29 g/mol. (Vastus: 2,1 kg) 9) Hermeetilises 1,2 liitrises plekkpurgis on õhk rõhuga 1 atm ja temperatuuril 300 K. Purk vajutati lössi. Arvuta rõhk purgis kilopaskalites ja atmosfäärides, kui õhk oli jahutatud temperatuurini 270 K ja purgi ruumala oli 0,9 liitrit. (Vastus: 121,6 kpa ja 1,2 atm) NB! Õppimisel võid kasutada ka teisi õppematerjale õpikutes või internetis nagu näiteks: (isoprotsessid)
GU BKS Access. Läbipääsukontrollisüsteemid ühe- ja mitmeukselistele süsteemidele. Üheukselised süsteemid
 TOOTEINFO GU BKS Access Läbipääsukontrollisüsteemid ühe- ja mitmeukselistele süsteemidele Üheukselised süsteemid Väljumiste loenduriga kombineeritud juhtimispult Läbipääsusüsteemi juhtimispult siseruumidele
TOOTEINFO GU BKS Access Läbipääsukontrollisüsteemid ühe- ja mitmeukselistele süsteemidele Üheukselised süsteemid Väljumiste loenduriga kombineeritud juhtimispult Läbipääsusüsteemi juhtimispult siseruumidele
ÜBERLEGUNGEN ZUR EFFIZIENZ GELDPOLITISCHER MASSNAHMEN DES EUROSYSTEMS IN DEPRESSIVEN KONJUNKTURPHASEN
 ÜBERLEGUNGEN ZUR EFFIZIENZ GELDPOLITISCHER MASSNAHMEN DES EUROSYSTEMS IN DEPRESSIVEN KONJUNKTURPHASEN Manfred O. E. Hennies Fachhochschule Kiel/University for Applied Sciences 1. Ziele der Geldpolitik
ÜBERLEGUNGEN ZUR EFFIZIENZ GELDPOLITISCHER MASSNAHMEN DES EUROSYSTEMS IN DEPRESSIVEN KONJUNKTURPHASEN Manfred O. E. Hennies Fachhochschule Kiel/University for Applied Sciences 1. Ziele der Geldpolitik
2,00 1,75. Kompressionsfaktor z 1,50 1,25 1,00 0,75 0,50 0,25. Druck in MPa. Druckabhängigkeit des Kompressionsfaktors. Chemische Verfahrenstechnik
 Kompressionsfaktor z,00 1,75 1,50 1,5 1,00 0,75 0,50 0,5 H CH 4 CO 0 0 0 40 60 80 Druck in MPa ideales Gas Nach dem idealen Gasgesetz gilt: pv nrt = pv m RT = 1 (z) Nennenswerte Abweichungen vom idealen
Kompressionsfaktor z,00 1,75 1,50 1,5 1,00 0,75 0,50 0,5 H CH 4 CO 0 0 0 40 60 80 Druck in MPa ideales Gas Nach dem idealen Gasgesetz gilt: pv nrt = pv m RT = 1 (z) Nennenswerte Abweichungen vom idealen
MATHEMATICA, PHYSICA" MBDICA VII TARTU
 EESTI VABARIIGI TAETU ÜLIKOOLI TOIMET«. 4 - ACTA ET CdHMTATIOKES UNIVERSITATIS DORPATENSIS A MATHEMATICA, PHYSICA" MBDICA VII TARTU 1925 EESTI VABARIIGI TARTU ÜLIKOOLI TOIMETUSED ACTA ET COMMEJfTATIOJfES
EESTI VABARIIGI TAETU ÜLIKOOLI TOIMET«. 4 - ACTA ET CdHMTATIOKES UNIVERSITATIS DORPATENSIS A MATHEMATICA, PHYSICA" MBDICA VII TARTU 1925 EESTI VABARIIGI TARTU ÜLIKOOLI TOIMETUSED ACTA ET COMMEJfTATIOJfES
Der Alltag estnischer Displaced Persons Die Sammlung Hintzer im Herder-Institut Marburg
 Der Alltag estnischer Displaced Persons Die Sammlung Hintzer im Herder-Institut Marburg Dorothee M. Goeze Die Sammlung Der Lehrer und Fotograf Karl Hintzer hat in der Zeit nach dem Zweiten Weltkrieg bis
Der Alltag estnischer Displaced Persons Die Sammlung Hintzer im Herder-Institut Marburg Dorothee M. Goeze Die Sammlung Der Lehrer und Fotograf Karl Hintzer hat in der Zeit nach dem Zweiten Weltkrieg bis
BILANZFÄLSCHUNGEN IN BÖRSENNOTIERTEN UNTERNEHMEN - URSACHEN UND EINFLUSSFAKTOREN. Toni Schulz Fachhochschule Kiel / University of Applied Sciences
 BILANZFÄLSCHUNGEN IN BÖRSENNOTIERTEN UNTERNEHMEN - URSACHEN UND EINFLUSSFAKTOREN Toni Schulz Fachhochschule Kiel / University of Applied Sciences 1. Problemgegenstand Bilanzfälschung Der Begriff "Bilanzfälschung"
BILANZFÄLSCHUNGEN IN BÖRSENNOTIERTEN UNTERNEHMEN - URSACHEN UND EINFLUSSFAKTOREN Toni Schulz Fachhochschule Kiel / University of Applied Sciences 1. Problemgegenstand Bilanzfälschung Der Begriff "Bilanzfälschung"
COROB D410x. Automatische Abtönmaschine Automaatne dosaator BEDIENUNGSANLEITUNG KASUTAMISÕPETUS 206122 V1.0 - R1 (04/2014)
 Automatische Abtönmaschine Automaatne dosaator DE BEDIENUNGSANLEITUNG ET KASUTAMISÕPETUS 206122 V1.0 - R1 (04/2014) Bedienerhandbuch Automatische Abtönmaschine Version 1.0 - R1 (04/2014) ÜBERSETZUNG DER
Automatische Abtönmaschine Automaatne dosaator DE BEDIENUNGSANLEITUNG ET KASUTAMISÕPETUS 206122 V1.0 - R1 (04/2014) Bedienerhandbuch Automatische Abtönmaschine Version 1.0 - R1 (04/2014) ÜBERSETZUNG DER
GOETHES FAUST IN ESTNISCHER ÜBERSETZUNG Magisterarbeit
 UNIVERSITÄT TARTU PHILOSOPHISCHE FAKULTÄT LEHRSTUHL FÜR DEUTSCHE PHILOLOGIE GOETHES FAUST IN ESTNISCHER ÜBERSETZUNG Magisterarbeit vorgelegt von Liina Sumberg Wissenschaftliche Betreuerin: Liina Lukas
UNIVERSITÄT TARTU PHILOSOPHISCHE FAKULTÄT LEHRSTUHL FÜR DEUTSCHE PHILOLOGIE GOETHES FAUST IN ESTNISCHER ÜBERSETZUNG Magisterarbeit vorgelegt von Liina Sumberg Wissenschaftliche Betreuerin: Liina Lukas
Physik1. Physik der Wärme. WS 15/16 1. Sem. B.Sc. Oec. und B.Sc. CH
 3 Physik1. Physik der Wärme. WS 15/16 1. Sem. B.Sc. Oec. und B.Sc. CH Physik Wärme 5 Themen Begriffsklärung Anwendungen Temperaturskalen Modellvorstellung Wärmeausdehnung Thermische Ausdehnung Phasenübergänge
3 Physik1. Physik der Wärme. WS 15/16 1. Sem. B.Sc. Oec. und B.Sc. CH Physik Wärme 5 Themen Begriffsklärung Anwendungen Temperaturskalen Modellvorstellung Wärmeausdehnung Thermische Ausdehnung Phasenübergänge
Klausur Physikalische Chemie für TUHH (Chemie III)
 07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
Probeklausur zur Vorlesung Physik I für Chemiker, Pharmazeuten, Geoökologen, Lebensmittelchemiker
 Technische Universität Braunschweig Institut für Geophysik und extraterrestrische Physik Prof. A. Hördt Probeklausur zur Vorlesung Physik I für Chemiker, Pharmazeuten, Geoökologen, Lebensmittelchemiker
Technische Universität Braunschweig Institut für Geophysik und extraterrestrische Physik Prof. A. Hördt Probeklausur zur Vorlesung Physik I für Chemiker, Pharmazeuten, Geoökologen, Lebensmittelchemiker
Übungsaufgaben Physikalische Chemie
 Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsaufgaben Physikalische Chemie A1. Welchen Druck übt gasförmiger Stickstoff mit einer Masse von 2,045 g bei 21 C in einem Gefäß mit einem Volumen von 2,00 l aus? A2. In Haushaltgeräten zur Erzeugung
Übungsblatt 3 (10.06.2011)
 Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
Experimentalphysik für Naturwissenschaftler Universität Erlangen Nürnberg SS 0 Übungsblatt (0.06.0 Wärmedämmung Ein Verbundfenster der Fläche A =.0 m besteht aus zwei Glasscheiben der Dicke d =.5 mm, zwischen
DIE ANALYSE DER SPRACHKOMPETENZ VON SPRACHMITTLERN, GERMANISTEN UND DEUTSCHSPRACHENKUNDIGEN
 Universität Tartu Philosophische Fakultät Die Abteilung für germanisch-romanische Philologie DIE ANALYSE DER SPRACHKOMPETENZ VON SPRACHMITTLERN, GERMANISTEN UND DEUTSCHSPRACHENKUNDIGEN Magisterarbeit Vorgelegt
Universität Tartu Philosophische Fakultät Die Abteilung für germanisch-romanische Philologie DIE ANALYSE DER SPRACHKOMPETENZ VON SPRACHMITTLERN, GERMANISTEN UND DEUTSCHSPRACHENKUNDIGEN Magisterarbeit Vorgelegt
Töid algkristliku mõtlemise kujunemise alalt. Studies in the Formation of the Early Christian Way of Thinking
 Publications of the EELC Institute of Theology XIX EELK Usuteaduse Instituudi toimetised XIX Studies in the Formation of the Early Christian Way of Thinking Töid algkristliku mõtlemise kujunemise alalt
Publications of the EELC Institute of Theology XIX EELK Usuteaduse Instituudi toimetised XIX Studies in the Formation of the Early Christian Way of Thinking Töid algkristliku mõtlemise kujunemise alalt
M3 SL, 20 SL, 20 DUO, 36 DUO 20 BOILER, 20 SL BOILER
 M3 SL, 20 SL, 20 DUO, 36 DUO 20 BOILER, 20 SL BOILER FI Asennusohje DE Montageanleitung SV Monteringsanvisning RU Èíñòðóêöèÿ ïî ìîíòàæó êàìåíêè EN Instructions for installation ET Paigaldusjuhend 20 DUO,
M3 SL, 20 SL, 20 DUO, 36 DUO 20 BOILER, 20 SL BOILER FI Asennusohje DE Montageanleitung SV Monteringsanvisning RU Èíñòðóêöèÿ ïî ìîíòàæó êàìåíêè EN Instructions for installation ET Paigaldusjuhend 20 DUO,
Thermodynamik. Vorlesung 1. Nicolas Thomas
 Thermodynamik Vorlesung 1 Thermodynamik ist nur ein bisschen schwerig. Geschichtlicher Hintergrund! Im 19. Jahrhundert Zunahme an Mechanisierung durch Konstruktion von Maschinen und Motoren.! Besonders
Thermodynamik Vorlesung 1 Thermodynamik ist nur ein bisschen schwerig. Geschichtlicher Hintergrund! Im 19. Jahrhundert Zunahme an Mechanisierung durch Konstruktion von Maschinen und Motoren.! Besonders
Übungsaufgaben Chemie Nr. 2
 Übungsaufgaben Chemie Nr. 2 11) Welche Elektronenkonfiguration haben Si, Cr, Gd, Au? 12) Zeichnen Sie das Orbitalschema für Sauerstoff (O 2 ) auf. 13) Zeichnen Sie die Lewis-Formeln für folgende Moleküle:
Übungsaufgaben Chemie Nr. 2 11) Welche Elektronenkonfiguration haben Si, Cr, Gd, Au? 12) Zeichnen Sie das Orbitalschema für Sauerstoff (O 2 ) auf. 13) Zeichnen Sie die Lewis-Formeln für folgende Moleküle:
Auf vielfachen Wunsch Ihrerseits gibt es bis auf weiteres die Vorlesungen und Übungen und Lösung der Testklausur im Internet:
 uf vielfachen Wunsch Ihrerseits gibt es bis auf weiteres die Vorlesungen und Übungen und Lösung der Testklausur im Internet: http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ******
uf vielfachen Wunsch Ihrerseits gibt es bis auf weiteres die Vorlesungen und Übungen und Lösung der Testklausur im Internet: http://www.physik.uni-giessen.de/dueren/ User: duerenvorlesung Password: ******
merken!!! 29,22 g NaCl abwiegen, in einem Becher mit etwa 800 ml Wasser lösen, dann im Messzylinder auf 1000 ml auffüllen.
 Das ABC der Stöchiometrie Lösungen aus Feststoffen Molare Lösungen herstellen (m = M c V) Beispiel 1: 1 L einer 500 mm NaCl-Lösung herstellen. Masse: Volumen: Stoffmenge: Dichte: m (kg) V (L) n (mol) (kg/l)
Das ABC der Stöchiometrie Lösungen aus Feststoffen Molare Lösungen herstellen (m = M c V) Beispiel 1: 1 L einer 500 mm NaCl-Lösung herstellen. Masse: Volumen: Stoffmenge: Dichte: m (kg) V (L) n (mol) (kg/l)
Elektrolyse. Zelle.. Bei der Elektrolyse handelt es sich im Prinzip um eine Umkehrung der in einer galvanischen Zelle Z ablaufenden Redox-Reaktion
 (Graphit) Cl - Abgabe von Elektronen: Oxidation Anode Diaphragma H + Elektrolyse Wird in einer elektrochemischen Zelle eine nicht-spontane Reaktion durch eine äußere Stromquelle erzwungen Elektrolyse-Zelle
(Graphit) Cl - Abgabe von Elektronen: Oxidation Anode Diaphragma H + Elektrolyse Wird in einer elektrochemischen Zelle eine nicht-spontane Reaktion durch eine äußere Stromquelle erzwungen Elektrolyse-Zelle
11. Ideale Gasgleichung
 . Ideale Gasgleichung.Ideale Gasgleichung Definition eines idealen Gases: Gasmoleküle sind harte punktförmige eilchen, die nur elastische Stöße ausführen und kein Eigenvolumen besitzen. iele Gase zeigen
. Ideale Gasgleichung.Ideale Gasgleichung Definition eines idealen Gases: Gasmoleküle sind harte punktförmige eilchen, die nur elastische Stöße ausführen und kein Eigenvolumen besitzen. iele Gase zeigen
Aufgabenblatt 10 Übungsblatt Stöchiometrie
 Name: Datum: Aufgabenblatt 10 Übungsblatt Stöchiometrie Berechnung von Stoffmengen bei chemischen Reaktionen II _ 20091005 Dr. Hagen Grossholz A1 Zusammenhang zwischen den verschiedenen Größen. Masse m
Name: Datum: Aufgabenblatt 10 Übungsblatt Stöchiometrie Berechnung von Stoffmengen bei chemischen Reaktionen II _ 20091005 Dr. Hagen Grossholz A1 Zusammenhang zwischen den verschiedenen Größen. Masse m
5 Gase...2. 5.1 Das ideale Gasgesetz...2. 5.2 Kinetische Gastheorie...3. 5.2.1 Geschwindigkeit der Gasteilchen:...5. 5.2.2 Diffusion...
 5 Gase...2 5.1 Das ideale Gasgesetz...2 5.2 Kinetische Gastheorie...3 5.2.1 Geschwindigkeit der Gasteilchen:...5 5.2.2 Diffusion...5 5.2.3 Zusammenstöße...6 5.2.4 Geschwindigkeitsverteilung...6 5.2.5 Partialdruck...7
5 Gase...2 5.1 Das ideale Gasgesetz...2 5.2 Kinetische Gastheorie...3 5.2.1 Geschwindigkeit der Gasteilchen:...5 5.2.2 Diffusion...5 5.2.3 Zusammenstöße...6 5.2.4 Geschwindigkeitsverteilung...6 5.2.5 Partialdruck...7
Physikalisch-chemische Grundlagen einiger Experimente aus Thermodynamik und Spektroskopie
 Physikalisch-chemische Grundlagen einiger Experimente aus Thermodynamik und Spektroskopie Rüdiger Wortmann Fachbereich Chemie, Physikalische Chemie, Technische Universität Kaiserslautern http://www.uni-kl.de/fb-chemie/wortmann
Physikalisch-chemische Grundlagen einiger Experimente aus Thermodynamik und Spektroskopie Rüdiger Wortmann Fachbereich Chemie, Physikalische Chemie, Technische Universität Kaiserslautern http://www.uni-kl.de/fb-chemie/wortmann
Muinaskarjala vaimuvara
 Muinaskarjala vaimuvara Abram Stoljar Die Geisterwelt ist nicht verschlossen; Dein Sinn ist zu, dein Herz ist tot! Auf! Bade, Schüler, unverdrossen Dein ird sche Brust im Morgenrot. Goethe, Faust Euroopa
Muinaskarjala vaimuvara Abram Stoljar Die Geisterwelt ist nicht verschlossen; Dein Sinn ist zu, dein Herz ist tot! Auf! Bade, Schüler, unverdrossen Dein ird sche Brust im Morgenrot. Goethe, Faust Euroopa
13.1 NORMEN, RICHTLINIEN UND MASSEINHEITEN
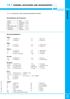 .6 EINHEITEN UND UMRECHNUNGSFAKTOREN Grundeinheiten des SI-Systems Länge Meter m Masse Kilogramm kg Zeit Sekunde s Elektrischer Strom Ampere A Temperatur Kelvin K Lichtstärke Candela cd Umrechnungsfaktoren
.6 EINHEITEN UND UMRECHNUNGSFAKTOREN Grundeinheiten des SI-Systems Länge Meter m Masse Kilogramm kg Zeit Sekunde s Elektrischer Strom Ampere A Temperatur Kelvin K Lichtstärke Candela cd Umrechnungsfaktoren
ÖAAMPJ TAD! '. v. j -, 1 * J. t*4x. V v.». -'.."j- ' "-K- : S-OüH.)LAINEN J A FiNN-UGOK j .J:
 j -, 1 * J Le. ÖAAMPJ TAD! '. v t*4x. mm m V v.». -'.."j- ' "-K- : S-OüH.)LAINEN J A FiNN-UGOK j s.j: SOOME-UGRI II. HARIDUSKONGRESS SUOMALAIS-UGRILAINEN II. KULTTUURIKOKOUS A FINN-ÜGOR II. TANÜGYIKONGRESSZUS
j -, 1 * J Le. ÖAAMPJ TAD! '. v t*4x. mm m V v.». -'.."j- ' "-K- : S-OüH.)LAINEN J A FiNN-UGOK j s.j: SOOME-UGRI II. HARIDUSKONGRESS SUOMALAIS-UGRILAINEN II. KULTTUURIKOKOUS A FINN-ÜGOR II. TANÜGYIKONGRESSZUS
Schächte Pozzetti. Schachtdeckel Coperchi
 Schächte Pozzetti Breite Larghezza Länge Lunghezza Höhe Altezza Wandstärke Spessore 60 cm 60 cm 8 cm 60 cm 120 cm 8 cm Schachtdeckel Coperchi Gussdeckel Coperchio in ghisa TELECOM Klasse D 400 beschriftet
Schächte Pozzetti Breite Larghezza Länge Lunghezza Höhe Altezza Wandstärke Spessore 60 cm 60 cm 8 cm 60 cm 120 cm 8 cm Schachtdeckel Coperchi Gussdeckel Coperchio in ghisa TELECOM Klasse D 400 beschriftet
Temperatur. Gebräuchliche Thermometer
 Temperatur Wärme ist Form von mechanischer Energie Umwandlung Wärme mechanische Energie ist möglich! Thermometer Messung der absoluten Temperatur ist aufwendig Menschliche Sinnesorgane sind schlechte "Thermometer"!
Temperatur Wärme ist Form von mechanischer Energie Umwandlung Wärme mechanische Energie ist möglich! Thermometer Messung der absoluten Temperatur ist aufwendig Menschliche Sinnesorgane sind schlechte "Thermometer"!
Glas - Chemische Eigenschaften Laugen Sa uren - konzentriert Sa uren - verdünnt
 Goodfellow GmbH Postfach 3 43 D-63 Bad Nauheim Telefon 0800 000 579 : Telefax 0800 000 580 Glas - hemische Eigenschaften Laugen Sa uren - konzentriert Sa uren - verdünnt MAOR bearbeitbare SiO 46/Al O3
Goodfellow GmbH Postfach 3 43 D-63 Bad Nauheim Telefon 0800 000 579 : Telefax 0800 000 580 Glas - hemische Eigenschaften Laugen Sa uren - konzentriert Sa uren - verdünnt MAOR bearbeitbare SiO 46/Al O3
Lösungen TM I Statik und Festigkeitslehre
 Technische Mechanik I L Lösungen TM I Statik und Festigkeitslehre Modellbildung in der Mechanik N Pa (Pascal). m.4536kg.38slug [a] m, [b] dimensionslos, [c] m, [d] m Dichte: kgm 3.94 3 slugft 3 Geschwindigkeit:
Technische Mechanik I L Lösungen TM I Statik und Festigkeitslehre Modellbildung in der Mechanik N Pa (Pascal). m.4536kg.38slug [a] m, [b] dimensionslos, [c] m, [d] m Dichte: kgm 3.94 3 slugft 3 Geschwindigkeit:
Arbeit, Energie, Leistung. 8 Arbeit, Energie, Leistung 2009 1
 Arbeit, Energie, Leistung 8 Arbeit, Energie, Leistung 2009 1 Begriffe Arbeit, Energie, Leistung von Joule, Mayer und Lord Kelvin erst im 19. Jahrhundert eingeführt! (100 Jahre nach Newton s Bewegungsgesetzen)
Arbeit, Energie, Leistung 8 Arbeit, Energie, Leistung 2009 1 Begriffe Arbeit, Energie, Leistung von Joule, Mayer und Lord Kelvin erst im 19. Jahrhundert eingeführt! (100 Jahre nach Newton s Bewegungsgesetzen)
Typ 5705 l Type 5705 KRATZBODENGETRIEBE 5705. Technische Daten l Technical Data. Einbaumaße l Dimensions HYDRAULIC SPEED REDUCERS
 Typ 5705 l Type 5705 KRTZODENGETRIEE 5705 1 : 4 1200 Nm 18 kg SE 80W-90 1 Liter -20-80 HYDRULI SPEED REDUERS 1 KRTZODENGETRIEE Typ 5700 l Type 5700 5700 1 : 8,15 1500 Nm 30 kg SE 80W-90 1,5 Liter -20-80
Typ 5705 l Type 5705 KRTZODENGETRIEE 5705 1 : 4 1200 Nm 18 kg SE 80W-90 1 Liter -20-80 HYDRULI SPEED REDUERS 1 KRTZODENGETRIEE Typ 5700 l Type 5700 5700 1 : 8,15 1500 Nm 30 kg SE 80W-90 1,5 Liter -20-80
Die Gasgesetze. Die Beziehung zwischen Volumen und Temperatur (Gesetz von J.-L. und J. Charles): Gay-Lussac
 Die Gasgesetze Die Beziehug zwische olume ud Temeratur (Gesetz vo J.-L. Gay-Lussac ud J. Charles): cost. T oder /T cost. cost.. hägt h vo ud Gasmege ab. Die extraolierte Liie scheidet die Temeratur- skala
Die Gasgesetze Die Beziehug zwische olume ud Temeratur (Gesetz vo J.-L. Gay-Lussac ud J. Charles): cost. T oder /T cost. cost.. hägt h vo ud Gasmege ab. Die extraolierte Liie scheidet die Temeratur- skala
Allgemeine Chemie. Die chemische Reaktion
 Allgemeine Chemie Die chemische Reaktion Dirk Broßke Berlin, Dezember 2005 1 3.Die chemische Reaktion In chemischen Reaktionen sind eine Vielzahl von Teilchen beteiligt. Die Gesetzmäßigkeiten chemischer
Allgemeine Chemie Die chemische Reaktion Dirk Broßke Berlin, Dezember 2005 1 3.Die chemische Reaktion In chemischen Reaktionen sind eine Vielzahl von Teilchen beteiligt. Die Gesetzmäßigkeiten chemischer
More time for living. Calendar 2015
 More time for living Calendar 205 Nordic Houses provides homes and the joy of living to many people on a daily basis. Birds returning from their spring migration to their nesting places usually bring joy
More time for living Calendar 205 Nordic Houses provides homes and the joy of living to many people on a daily basis. Birds returning from their spring migration to their nesting places usually bring joy
EXPEDITION Mathematik 3 / Übungsaufgaben
 1 Berechne das Volumen und die Oberfläche eines Prismas mit der Höhe h = 20 cm. Die Grundfläche ist ein a) Parallelogramm mit a 12 cm; b 8 cm; ha 6 cm b) gleichschenkliges Dreieck mit a b 5 cm; c 60 mm;
1 Berechne das Volumen und die Oberfläche eines Prismas mit der Höhe h = 20 cm. Die Grundfläche ist ein a) Parallelogramm mit a 12 cm; b 8 cm; ha 6 cm b) gleichschenkliges Dreieck mit a b 5 cm; c 60 mm;
TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz!
 1 Klassenarbeit Chemie 1/5 TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz! 1 Stoffe und Stoffgemische 1.1 Ordne die Begriffe Verbindung, Element, Stoff, Mischung, Reinstoff, Metall, Nichtmetall,
1 Klassenarbeit Chemie 1/5 TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz! 1 Stoffe und Stoffgemische 1.1 Ordne die Begriffe Verbindung, Element, Stoff, Mischung, Reinstoff, Metall, Nichtmetall,
Übertrittsprüfung 2011
 Departement Bildung, Kultur und Sport Abteilung Volksschule Übertrittsprüfung 2011 Aufgaben Prüfung an die 1. Klasse Sekundarschule / 1. Klasse Bezirksschule Prüfung Name und Vorname der Schülerin / des
Departement Bildung, Kultur und Sport Abteilung Volksschule Übertrittsprüfung 2011 Aufgaben Prüfung an die 1. Klasse Sekundarschule / 1. Klasse Bezirksschule Prüfung Name und Vorname der Schülerin / des
Reaktionsgleichungen und was dahinter steckt
 Reaktionsgleichungen und was dahinter steckt Prinzipien Bestehende Formeln dürfen nicht verändert werden. Bei Redoxreaktionen kann H, OH oder H 2 O ergänzt werden. Links und rechts vom Reaktionspfeil muss
Reaktionsgleichungen und was dahinter steckt Prinzipien Bestehende Formeln dürfen nicht verändert werden. Bei Redoxreaktionen kann H, OH oder H 2 O ergänzt werden. Links und rechts vom Reaktionspfeil muss
Kalorimetrie (Wärmelehre)
 Thermische Molekularbewegung Phasenübergänge Reaktionswärme Kalorimetrie (Wärmelehre) Gase Flüssigkeiten/Festkörper Ideales Gasgesetz Dulong-Petit-Gesetz 1 Thermodynamik Beschreibung der Zustände und deren
Thermische Molekularbewegung Phasenübergänge Reaktionswärme Kalorimetrie (Wärmelehre) Gase Flüssigkeiten/Festkörper Ideales Gasgesetz Dulong-Petit-Gesetz 1 Thermodynamik Beschreibung der Zustände und deren
-Homogene Gelichgewichte -Heterogene Gleichgewichte. Homogen: Die im Gleichgewicht stehenden Substanzen liegen in der gleichen Phase vor
 Heterogene Gleichgewichte Man unterscheidet: -Homogene Gelichgewichte -Heterogene Gleichgewichte Homogen: Die im Gleichgewicht stehenden Substanzen liegen in der gleichen Phase vor Heterogen: Die sich
Heterogene Gleichgewichte Man unterscheidet: -Homogene Gelichgewichte -Heterogene Gleichgewichte Homogen: Die im Gleichgewicht stehenden Substanzen liegen in der gleichen Phase vor Heterogen: Die sich
Zustandsformen der Materie Thermische Eigenschaften der Materie. Temperatur. skalare Zustandsgröße der Materie Maß für die Bewegung der Moleküle
 Zustandsformen der Materie hermische Eigenschaften der Materie Aggregatzustände: fest flüssig suprafluide gasförmig überkritisch emperatur skalare Zustandsgröße der Materie Maß für die Bewegung der Moleküle
Zustandsformen der Materie hermische Eigenschaften der Materie Aggregatzustände: fest flüssig suprafluide gasförmig überkritisch emperatur skalare Zustandsgröße der Materie Maß für die Bewegung der Moleküle
Training Reaktionsgleichungen
 Training Reaktionsgleichungen Hilfsmittel: PSE (Periodensystem der Elemente), Taschenrechner, Säure-Base-Reihe, Redox-Reihe ALLGEMEINE FORM EINER REAKTIONSGLEICHUNG Falls die Reaktion vollständig verläuft:
Training Reaktionsgleichungen Hilfsmittel: PSE (Periodensystem der Elemente), Taschenrechner, Säure-Base-Reihe, Redox-Reihe ALLGEMEINE FORM EINER REAKTIONSGLEICHUNG Falls die Reaktion vollständig verläuft:
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
Die Avogadro-Konstante N A
 Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
Aufgaben zur Vorlesung - Agrarwirtschaft / Gartenbau
 Aufgaben zur Vorlesung - Agrarwirtschaft / Gartenbau. Formen Sie die Größengleichung P = in eine Zahlenwertgleichung t /kj P /= α um und bestimmen Sie die Zahl α! t /h. Drücken Sie die Einheit V durch
Aufgaben zur Vorlesung - Agrarwirtschaft / Gartenbau. Formen Sie die Größengleichung P = in eine Zahlenwertgleichung t /kj P /= α um und bestimmen Sie die Zahl α! t /h. Drücken Sie die Einheit V durch
Ideale und Reale Gase. Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig)
 Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Ideale und Reale Gase Was ist ein ideales Gas? einatomige Moleküle mit keinerlei gegenseitiger WW keinem Eigenvolumen (punktförmig) Wann sind reale Gase ideal? Reale Gase verhalten sich wie ideale Gase
Eigenschaften von Gasen
 Eigenschaften von Gasen Die Zusammensetzung von Luft Bestandteil Prozentuale Zusammensetzung Volumen Masse Stickstoff, N 2 78.09 75.52 Sauerstoff, O 2 20.95 23.14 Argon, Ar 0.93 1.29 Kohlendioxid, CO 2
Eigenschaften von Gasen Die Zusammensetzung von Luft Bestandteil Prozentuale Zusammensetzung Volumen Masse Stickstoff, N 2 78.09 75.52 Sauerstoff, O 2 20.95 23.14 Argon, Ar 0.93 1.29 Kohlendioxid, CO 2
Übersetzungsprobleme bei Bedienungsanleitungen
 Universität Tartu Institut für germanische, romanische und slawische Philologie Abteilung für deutsche Sprache und Literatur Übersetzungsprobleme bei Bedienungsanleitungen Bakkalaureusarbeit Vorgelegt
Universität Tartu Institut für germanische, romanische und slawische Philologie Abteilung für deutsche Sprache und Literatur Übersetzungsprobleme bei Bedienungsanleitungen Bakkalaureusarbeit Vorgelegt
Syntaktische Konstruktionen im Estnischen und im Deutschen und deren lexikografische Erfassung als Teil des Fremdsprachenunterrichts
 Syntaktische Konstruktionen im Estnischen und im Deutschen und deren lexikografische Erfassung als Teil des Fremdsprachenunterrichts Anne Arold Universität Tartu Bergen 15.06.1012 Deutsch-estnisches Valenzwörterbuch
Syntaktische Konstruktionen im Estnischen und im Deutschen und deren lexikografische Erfassung als Teil des Fremdsprachenunterrichts Anne Arold Universität Tartu Bergen 15.06.1012 Deutsch-estnisches Valenzwörterbuch
Wird vom Korrektor ausgefüllt: Aufgabe 1 2 3 4 5 6 7 8 9 10 11 12 Punkte
 Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Klausur zur Vorlesung Grundlagen der Chemie für Mediziner und Biologen & Chemie-Praktikum für Molekulare Medizin und Biologie Gehalten im Wintersemester 2008/2009 Bitte diese 3 Felder ausfüllem: Name Matrikelnummer
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 17. 21. Mai 2010 Physik für Bauingenieure Übungsblatt 5 Gruppenübungen 1. Wärmepumpe Eine Wärmepumpe hat eine Leistungszahl
Lösungen zu den Übungsaufgaben zur Thematik Säure/Base (Zwei allgemeine Hinweise: aus Zeitgründen habe ich auf das Kursivsetzen bestimmter Zeichen
 Lösungen zu den Übungsaufgaben zur Thematik Säure/Base (Zwei allgemeine Hinweise: aus Zeitgründen habe ich auf das Kursivsetzen bestimmter Zeichen verzichtet; Reaktionsgleichungen sollten den üblichen
Lösungen zu den Übungsaufgaben zur Thematik Säure/Base (Zwei allgemeine Hinweise: aus Zeitgründen habe ich auf das Kursivsetzen bestimmter Zeichen verzichtet; Reaktionsgleichungen sollten den üblichen
Einführung in die Kristallographie
 Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Einführung in die Kristallographie Gerhard Heide Institut für Mineralogie Professur für Allgemeine und Angewandte Mineralogie Brennhausgasse 14 03731-39-2665 oder -2628 gerhard.heide@mineral.tu-freiberg.de
Vakuum und Vakuum- Pumpen
 und - Pumpen KNF-811 6L Schöpfl eistung 11,5 L Schöpfl eistung Was ist Bedeutung des Atmosphärendrucks KNF-18 15L Schöpfl eistung Saugleistung Uebersicht über die verschiedenen oder Druck-Erzeuger Beispiele
und - Pumpen KNF-811 6L Schöpfl eistung 11,5 L Schöpfl eistung Was ist Bedeutung des Atmosphärendrucks KNF-18 15L Schöpfl eistung Saugleistung Uebersicht über die verschiedenen oder Druck-Erzeuger Beispiele
Bachelorprüfung. Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch.
 Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch. Thienel Bachelorprüfung Prüfungsfach: Geologie, Werkstoffe und Bauchemie Prüfungsteil:
Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch. Thienel Bachelorprüfung Prüfungsfach: Geologie, Werkstoffe und Bauchemie Prüfungsteil:
Thema heute: Aufbau fester Stoffe - Kristallographie
 Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Wiederholung der letzten Vorlesungsstunde: Thema: Ionenbindung Ionenbindung, Kationen, Anionen, Coulomb-Kräfte Thema heute: Aufbau fester Stoffe - Kristallographie 244 Aufbau fester Materie Im Gegensatz
Flüssigkeiten. einige wichtige Eigenschaften
 Flüssigkeiten einige wichtige Eigenschaften Die Oberflächenspannung einer Flüssigkeit ist die zur Vergröß ößerung der Oberfläche um den Einheitsbetrag erforderliche Energie (H 2 O bei 20 C: 7.29 10-2 J/m
Flüssigkeiten einige wichtige Eigenschaften Die Oberflächenspannung einer Flüssigkeit ist die zur Vergröß ößerung der Oberfläche um den Einheitsbetrag erforderliche Energie (H 2 O bei 20 C: 7.29 10-2 J/m
Strahlenschutzverordnung
 Strahlenschutzverordnung (StSV) Änderung vom 15. November 2000 Der Schweizerische Bundesrat verordnet: I Die Strahlenschutzverordnung vom 22. Juni 1994 1 wird wie folgt geändert: Art. 9 Kommission für
Strahlenschutzverordnung (StSV) Änderung vom 15. November 2000 Der Schweizerische Bundesrat verordnet: I Die Strahlenschutzverordnung vom 22. Juni 1994 1 wird wie folgt geändert: Art. 9 Kommission für
Weiterführende Aufgaben zu chemischen Gleichgewichten
 Weiterführende Aufgaben zu hemishen Gleihgewihten Fahshule für Tehnik Suhe nah Ruhe, aber durh das Gleihgewiht, niht durh den Stillstand deiner Tätigkeiten. Friedrih Shiller Der Shlüssel zur Gelassenheit
Weiterführende Aufgaben zu hemishen Gleihgewihten Fahshule für Tehnik Suhe nah Ruhe, aber durh das Gleihgewiht, niht durh den Stillstand deiner Tätigkeiten. Friedrih Shiller Der Shlüssel zur Gelassenheit
4 Stöchiometrie. Teil II: Chemische Reaktionsgleichungen. 4.1 Chemische Reaktionsgleichungen
 35 4 Stöchiometrie Teil II: Chemische Reaktionsgleichungen Zusammenfassung Chemische Reaktionsgleichungen geben durch die Formeln der beteiligten Substanzen an, welche Reaktanden sich zu welchen Produkten
35 4 Stöchiometrie Teil II: Chemische Reaktionsgleichungen Zusammenfassung Chemische Reaktionsgleichungen geben durch die Formeln der beteiligten Substanzen an, welche Reaktanden sich zu welchen Produkten
6.3 GröSSe 2. 6.3.1 Außenzahnradpumpe
 6.3 GröSSe 2 Inhalt PGE12 Bestellschlüssel 6.3.1 ußenzahnradpumpe Technische Informationen 6.3.2 Kenngrößen 6.3.3 Hydraulikflüssigkeiten 6.3.4 Viskostiätsbereich 6.3.5 Temperaturbereich 6.3.6 Dichtungen
6.3 GröSSe 2 Inhalt PGE12 Bestellschlüssel 6.3.1 ußenzahnradpumpe Technische Informationen 6.3.2 Kenngrößen 6.3.3 Hydraulikflüssigkeiten 6.3.4 Viskostiätsbereich 6.3.5 Temperaturbereich 6.3.6 Dichtungen
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 200 24. 28. Mai 200 Physik für Bauingenieure Übungsblatt 6. Luftfeuchtigkeit Gruppenübungen In einer Finnischen Sauna
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 200 24. 28. Mai 200 Physik für Bauingenieure Übungsblatt 6. Luftfeuchtigkeit Gruppenübungen In einer Finnischen Sauna
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2
 Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Differenzdruckmeßgerät DD890-1 -
 Differenzdruckmeßgerät DD890-1 - INHALTSVERZEICHNIS TITEL SEITE 1. Einleitung... 3 2. Spezifikationen... 3 3. Tastenbeschreibung... 4 4. Displaybeschreibung... 4 5. Bedienung... 5 4.1 Einschalten... 5
Differenzdruckmeßgerät DD890-1 - INHALTSVERZEICHNIS TITEL SEITE 1. Einleitung... 3 2. Spezifikationen... 3 3. Tastenbeschreibung... 4 4. Displaybeschreibung... 4 5. Bedienung... 5 4.1 Einschalten... 5
DXRE Der Kanalkühler ist für verdampfende Kältemittel vorgesehen (DX). MONTAGEANLEITUNG WICHTIG:
 Der Kanalkühler ist für verdampfende Kältemittel vorgesehen (DX). DE MONTAGEANLEITUNG WICHTIG: Lesen Sie bitte diese Anweisung vor Montage. Ausführung/Montage Der Kanalkühler ist für verdampfende Kältemittel
Der Kanalkühler ist für verdampfende Kältemittel vorgesehen (DX). DE MONTAGEANLEITUNG WICHTIG: Lesen Sie bitte diese Anweisung vor Montage. Ausführung/Montage Der Kanalkühler ist für verdampfende Kältemittel
Preisliste Autarkic elements
 Die Innovation! Preisliste Autarkic elements Energie-Sparbausteine für Ihr unabhängiges Haus E 1 E 2 E 3 E 4 E 5 E 6 Direkt-Wärmepumpe Photovoltaik Home Manager Stromspeicherung Biomasse Klimatisierung
Die Innovation! Preisliste Autarkic elements Energie-Sparbausteine für Ihr unabhängiges Haus E 1 E 2 E 3 E 4 E 5 E 6 Direkt-Wärmepumpe Photovoltaik Home Manager Stromspeicherung Biomasse Klimatisierung
Masterlayout HB 2000. Kuratorium für Waldarbeit und Forsttechnik e.v. Beziehung Reifen - Boden. Kraftübertragung und Bodenbelastung
 Kuratorium für Waldarbeit und Forsttechnik e.v. Beziehung Reifen - Boden Kraftübertragung und Bodenbelastung Bodenfunktion und Radlast Prinzipieller Zusammenhang zwischen gewünschter Bodenfunktion, Bodenspannung,
Kuratorium für Waldarbeit und Forsttechnik e.v. Beziehung Reifen - Boden Kraftübertragung und Bodenbelastung Bodenfunktion und Radlast Prinzipieller Zusammenhang zwischen gewünschter Bodenfunktion, Bodenspannung,
Spektroskopie. im IR- und UV/VIS-Bereich. Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) http://www.analytik.ethz.
 Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
Spektroskopie im IR- und UV/VIS-Bereich Optische Rotationsdispersion (ORD) und Circulardichroismus (CD) Dr. Thomas Schmid HCI D323 schmid@org.chem.ethz.ch http://www.analytik.ethz.ch Enantiomere sind Stereoisomere,
FAVORIT55510IM0 CS Návod k použití 2 ET Kasutusjuhend 18 DE Benutzerinformation 32 SK Návod na používanie 48
 FAVORIT55510IM0 CS Návod k použití 2 ET Kasutusjuhend 18 DE Benutzerinformation 32 SK Návod na používanie 48 2 www.aeg.com OBSAH 1. BEZPEČNOSTNÍ POKYNY................................................ 3
FAVORIT55510IM0 CS Návod k použití 2 ET Kasutusjuhend 18 DE Benutzerinformation 32 SK Návod na používanie 48 2 www.aeg.com OBSAH 1. BEZPEČNOSTNÍ POKYNY................................................ 3
Einführung in die Physikalische Chemie: Inhalt
 Einführung in die Physikalische Chemie: Inhalt Woche Kapitel Dozent 1 1. Intermolecular Interactions CP 2,3 2. States of Matter SW 3,4 3. Structure of Molecules SW 5,6 4. Molecular Spectroscopy CP 6 5.
Einführung in die Physikalische Chemie: Inhalt Woche Kapitel Dozent 1 1. Intermolecular Interactions CP 2,3 2. States of Matter SW 3,4 3. Structure of Molecules SW 5,6 4. Molecular Spectroscopy CP 6 5.
DOCERAM A-101. MPa. MPa m 1/2 4 10-6 K -1 5,0-8,3 T C 250. Ω cm > 10 14. ε r 10. tanδ 0,001
 DOCERAM A-101 Al 2 O 3 95 97% weiß, elfenbein, pink, rot, lachs white, ivory, pink, red, salmon g/cm³ 3,7 MPa 300 MPa 3400 GPa 350 MPa m 1/2 4 m 10 HV 0,5 1800 10-6 K -1 5,0-8,3 W/mK 24 T C 250 C 1600
DOCERAM A-101 Al 2 O 3 95 97% weiß, elfenbein, pink, rot, lachs white, ivory, pink, red, salmon g/cm³ 3,7 MPa 300 MPa 3400 GPa 350 MPa m 1/2 4 m 10 HV 0,5 1800 10-6 K -1 5,0-8,3 W/mK 24 T C 250 C 1600
Ich bin der SirWiss. Der SWM Service
 I SW D SWM S L K K, F I a Ü ü a SWM S-. S S a B ü a W: a, ä. S a S W Z. V S a? Da I U U. E I S-. Gaa ü W, GEZ Fa a - a Laaa. U a I a, S a a U a ö. G Ea S: aü SWM. Da ä K Pa Ma R. W a ü S a: I K a C Caé
I SW D SWM S L K K, F I a Ü ü a SWM S-. S S a B ü a W: a, ä. S a S W Z. V S a? Da I U U. E I S-. Gaa ü W, GEZ Fa a - a Laaa. U a I a, S a a U a ö. G Ea S: aü SWM. Da ä K Pa Ma R. W a ü S a: I K a C Caé
VIESMANN VITOLIGNO 100-S Holzvergaserkessel 20 kw
 VIESMANN VITOLIGNO 100-S Holzvergaserkessel 20 kw Datenblatt Best.-Nr. und Preise: siehe Preisliste VITOLIGNO 100-S Typ VL1B Holzvergaserkessel für Scheitholzlänge von 45 bis 50 cm 5/2013 Vitoligno 100-S,
VIESMANN VITOLIGNO 100-S Holzvergaserkessel 20 kw Datenblatt Best.-Nr. und Preise: siehe Preisliste VITOLIGNO 100-S Typ VL1B Holzvergaserkessel für Scheitholzlänge von 45 bis 50 cm 5/2013 Vitoligno 100-S,
Gegeben sind die folgenden Werte kovalenter Bindungsenthalpien:
 Literatur: Housecroft Chemistry, Kap. 22.1011 1. Vervollständigen Sie folgende, stöchiometrisch nicht ausgeglichene Reaktions gleichungen von Sauerstoffverbindungen. Die korrekten stöchiometrischen Faktoren
Literatur: Housecroft Chemistry, Kap. 22.1011 1. Vervollständigen Sie folgende, stöchiometrisch nicht ausgeglichene Reaktions gleichungen von Sauerstoffverbindungen. Die korrekten stöchiometrischen Faktoren
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Physik für Bauingenieure
 Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 26. 30. April 2010 Physik für Bauingenieure Übungsblatt 2 Gruppenübungen 1. Springende Kugeln Die nebenstehende
Fachbereich Physik Prof. Dr. Rudolf Feile Dipl. Phys. Markus Domschke Sommersemster 2010 26. 30. April 2010 Physik für Bauingenieure Übungsblatt 2 Gruppenübungen 1. Springende Kugeln Die nebenstehende
Lektion 3. Mein erstes Date
 3 Lektion 3. Mein erstes Date GRAMMATIKTRAINING 1. Erinnerst du dich? Ordne die Präpositionen zu. Präpositionen mit... in, an, bis, um, mit, von, aus, seit, nach, auf, über, unter, vor, zwischen, für,
3 Lektion 3. Mein erstes Date GRAMMATIKTRAINING 1. Erinnerst du dich? Ordne die Präpositionen zu. Präpositionen mit... in, an, bis, um, mit, von, aus, seit, nach, auf, über, unter, vor, zwischen, für,
19-3 19-5 19-4 AUFGABEN ZU KAPITEL 19
 UFGEN ZU KPITEL 19 ntwort im Lösungshandbuch für Studenten (Student Solutions Manual) www ntwort kann abgerufen werden im World Wide Web ntwort ist in der interaktiven Lernsoftware enthalten (Interactive
UFGEN ZU KPITEL 19 ntwort im Lösungshandbuch für Studenten (Student Solutions Manual) www ntwort kann abgerufen werden im World Wide Web ntwort ist in der interaktiven Lernsoftware enthalten (Interactive
HGA 400 -, DiGas 440 -, DiGas 2200-4/5 -, MHC 218/222 - PC Mercedes-Benz AU-Daten 1.2.860
 HGA 400 -, DiGas 440 -, DiGas 2200-4/5 -, MHC 218/222 - PC Mercedes-Benz AU-Daten 1.2.860 Hersteller: Typ-Nr.: Verkaufsbezeichnung: Motorcode: HSN: TSN: Messprog.: Maybach 240.077 57S Zeppelin 285.980
HGA 400 -, DiGas 440 -, DiGas 2200-4/5 -, MHC 218/222 - PC Mercedes-Benz AU-Daten 1.2.860 Hersteller: Typ-Nr.: Verkaufsbezeichnung: Motorcode: HSN: TSN: Messprog.: Maybach 240.077 57S Zeppelin 285.980
Fällungsreaktion. Flammenfärbung. Fällungsreaktion:
 2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
Wer misst hat recht! Nanotechnik, Motor für die medizinische Diagnostik. Prof. Dr. Ing. Jörg Vienken Nephro-Solutions AG, Hamburg
 Wer misst hat recht! Nanotechnik, Motor für die medizinische Diagnostik Prof. Dr. Ing. Jörg Vienken Nephro-Solutions AG, Hamburg Wer misst hat recht! Nanotechnik, der Motor für die medizinische Diagnostik
Wer misst hat recht! Nanotechnik, Motor für die medizinische Diagnostik Prof. Dr. Ing. Jörg Vienken Nephro-Solutions AG, Hamburg Wer misst hat recht! Nanotechnik, der Motor für die medizinische Diagnostik
Tagungsplaner GÜNNEWIG. Conference planer. Hotels & Restaurants
 s & Restaurants Tagungsplaner Conference planer Preise gültig bis Ende 2015 - Änderungen vorbehalten! Prices valid until the end of 2015 - subject to change! s & Restaurants Destinationen Restaurant Bar
s & Restaurants Tagungsplaner Conference planer Preise gültig bis Ende 2015 - Änderungen vorbehalten! Prices valid until the end of 2015 - subject to change! s & Restaurants Destinationen Restaurant Bar
Project BIGGEST LOSER. Tag 0
 Project BIGGEST LOSER Wie viel Kilogramm Fett nehme ich in einer Woche ab, wenn ich mich äußerst gesund und kalorienarm ernähre und dabei sehr viel Sport treibe? - in der dritten Staffel der Serie The
Project BIGGEST LOSER Wie viel Kilogramm Fett nehme ich in einer Woche ab, wenn ich mich äußerst gesund und kalorienarm ernähre und dabei sehr viel Sport treibe? - in der dritten Staffel der Serie The
MOL - Bestimmung der Molaren Masse nach Dumas
 MOL - Bestimmung der Molaren Masse nach Dumas Anfängerpraktikum 2, 2006 Janina Fiehl Daniel Flassig Gruppe 129 Einleitung Das Mol ist, vor allem in der Chemie, als Einheit für die Basisgröße der Stoffmenge
MOL - Bestimmung der Molaren Masse nach Dumas Anfängerpraktikum 2, 2006 Janina Fiehl Daniel Flassig Gruppe 129 Einleitung Das Mol ist, vor allem in der Chemie, als Einheit für die Basisgröße der Stoffmenge
1.3. Aufgaben zu chemische Reaktionen
 1.3. Aufgaben zu chemische Reaktionen Aufgabe 1: Summenformeln Ergänze gemäß Beispiel a): a) Eine Formeleinheit Phosphorsäure H 3 PO 4 besteht aus 3 Wasserstoff-Atomen 1 H, 1 Phosphor-Atom 31 P und 4 Sauerstoff-Atomen
1.3. Aufgaben zu chemische Reaktionen Aufgabe 1: Summenformeln Ergänze gemäß Beispiel a): a) Eine Formeleinheit Phosphorsäure H 3 PO 4 besteht aus 3 Wasserstoff-Atomen 1 H, 1 Phosphor-Atom 31 P und 4 Sauerstoff-Atomen
DEU. Separett WEEKEND. Modell 7011. Separett. www.separett.com. SEPARETT AB 2007 SEPARETT is a registered trademark for Separett AB
 DEU Separett WEEKEND Modell 7011 Separett www.separett.com TECHNISCHE DATEN Folgendes befindet sich im Lieferumfang 2 m x1 x2 532 mm 450 mm Material Ober-/Unterteil: schlagfestes Polyäthylen Sitz: Hochglanz-Polypropylen
DEU Separett WEEKEND Modell 7011 Separett www.separett.com TECHNISCHE DATEN Folgendes befindet sich im Lieferumfang 2 m x1 x2 532 mm 450 mm Material Ober-/Unterteil: schlagfestes Polyäthylen Sitz: Hochglanz-Polypropylen
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/hermodynamik Wintersemester 2007 ladimir Dyakonov #2 am 10.01.2007 Raum E143, el. 888-5875, email: dyakonov@hysik.uni-wuerzburg.de 10.2 emeraturmessung Wärmeausdehnung
Einführung in die Physik I Wärmelehre/hermodynamik Wintersemester 2007 ladimir Dyakonov #2 am 10.01.2007 Raum E143, el. 888-5875, email: dyakonov@hysik.uni-wuerzburg.de 10.2 emeraturmessung Wärmeausdehnung
Messumformer Für Gasdichte, Temperatur, Druck und Feuchte von SF 6 -Gas Typ GDHT-20, mit MODBUS -Ausgang
 Instrumentierung Messumformer Für Gasdichte, Temperatur, Druck und Feuchte von SF 6 -Gas Typ GDHT-20, mit MODBUS -Ausgang WIKA Datenblatt SP 60.14 Anwendungen Permanente Überwachung der relevanten Gaszustandsparameter
Instrumentierung Messumformer Für Gasdichte, Temperatur, Druck und Feuchte von SF 6 -Gas Typ GDHT-20, mit MODBUS -Ausgang WIKA Datenblatt SP 60.14 Anwendungen Permanente Überwachung der relevanten Gaszustandsparameter
Was ist Physikalische Chemie? Die klassischen Teilgebiete der Physikalischen Chemie sind:
 Was ist Physikalische Chemie? Die klassischen eilgebiete der Physikalischen Chemie sind: 1) hermodynamik (z. B. Energetik chemischer Reaktionen, Lage von Gleichgewichten). 2) Kinetik chemischer Reaktionen
Was ist Physikalische Chemie? Die klassischen eilgebiete der Physikalischen Chemie sind: 1) hermodynamik (z. B. Energetik chemischer Reaktionen, Lage von Gleichgewichten). 2) Kinetik chemischer Reaktionen
Welche Informationen N e w s K o mpa s s G mb H s a m melt und wie wir die D aten verwenden
 Daten s chutzinformation V i el e n D a n k f ür I hr I nt e r e s s e a n u n s e r e r W e b s it e u n d u n s e r e A n g e b o t e s o w i e I hr V e rtr a u e n i n u n - s e r U n t e r n e h m
Daten s chutzinformation V i el e n D a n k f ür I hr I nt e r e s s e a n u n s e r e r W e b s it e u n d u n s e r e A n g e b o t e s o w i e I hr V e rtr a u e n i n u n - s e r U n t e r n e h m
Typische Eigenschaften von Metallen
 Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Typische Eigenschaften von Metallen hohe elektrische Leitfähigkeit (nimmt mit steigender Temperatur ab) hohe Wärmeleitfähigkeit leichte Verformbarkeit metallischer Glanz Elektronengas-Modell eines Metalls
Kapitel 2 Thermische Ausdehnung
 Kapitel 2 Thermische Ausdehnung Die Ausdehnung von Festkörpern, Flüssigkeiten und Gasen hängt von der Temperatur ab. Für Festkörper und Flüssigkeiten ist diese temperaturabhängige Ausdehnung zusätzlich
Kapitel 2 Thermische Ausdehnung Die Ausdehnung von Festkörpern, Flüssigkeiten und Gasen hängt von der Temperatur ab. Für Festkörper und Flüssigkeiten ist diese temperaturabhängige Ausdehnung zusätzlich
Grenzflächen-Phänomene
 Grenzflächen-Phänomene Oberflächenspannung Betrachtet: Grenzfläche Flüssigkeit-Gas Kräfte Fl Fl grösser als Fl Gas im Inneren der Flüssigkeit: kräftefrei an der Oberfläche: resultierende Kraft ins Innere
Grenzflächen-Phänomene Oberflächenspannung Betrachtet: Grenzfläche Flüssigkeit-Gas Kräfte Fl Fl grösser als Fl Gas im Inneren der Flüssigkeit: kräftefrei an der Oberfläche: resultierende Kraft ins Innere
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen

