Allgemeine Richtlinien zur immunhistochemischen Färbung
|
|
|
- Katarina Kalb
- vor 5 Jahren
- Abrufe
Transkript
1 Allgemeine Richtlinien zur immunhistochemischen Färbung Verwendungszweck Zur In-vitro-Diagnostik. Diese Anweisungen gelten für immunhistochemische Reagenzien von Dako. Sie gelten nicht notwendigerweise für das/die in dieser Packung enthaltene(n) Produkt(e). Antikörper von Dako werden im Labor dazu verwendet, mit Lichtmikroskopie Antigene auf oder in Zellen aus Gewebeproben bzw. Zellpräparaten qualitativ nachzuweisen. Positive oder negative Ergebnisse unterstützen die Klassifizierung normaler und abnormaler Zellen bzw. Gewebe und ergänzen die konventionelle Histopathologie. Die klinische Auswertung vorhandener oder fehlender Färbungen sollte durch morphologische und histologische Untersuchungen mit entsprechenden Kontrollen ergänzt werden. Auswertungen müssen von einem qualifizierten Pathologen unter Berücksichtigung der Krankengeschichte und anderer Diagnostiktests des Patienten vorgenommen werden. Bei allen ungewöhnlichen Färbungen den technischen Kundendienst von Dako verständigen. Verfahrensprinzip Erforderliches, aber nicht mitgeliefertes Material Antikörper von Dako können zum Nachweis von Antigenen in Gewebe- bzw. Zellproben in einer Vielzahl immunhistochemischer Verfahren als primäre Antikörper eingesetzt werden, so z. B. bei LSAB + und Dako LSAB 2 (labelled streptavidin-biotin), markierten Polymeren und erweiterten Polymeren wie EnVision, EnVision +, EnVision FLEX und FLEX+, EnVision Gl2, EnVision Gl2 Doublestain, ADVANCE, Dako Real sowie CSA (catalyzed signal amplification). IHC-Färbeverfahren ermöglichen im Allgemeinen die Demaskierung und Darstellung von Antigenen, ggf. beginnend mit einer Vorbehandlung mit proteolytischen Enzymen oder Wärme-Demaskierung, gefolgt von der sequentiellen Anwendung eines spezifischen Antikörpers gegen das Antigen (primärer Antikörper), einem sekundären Antikörper gegen den primären Antikörper (Link-Antikörper oder markiertes Polymer), eines Enzymkomplexes und eines Chromogensubstrats mit zwischengeschalteten Waschschritten. Die enzymatische Aktivierung des Chromogens führt zur Ausbildung eines sichtbaren Reaktionsprodukts an der Antigenstelle. Danach können die Proben gegengefärbt und eingedeckt werden. Die Ergebnisse werden mit einem Lichtmikroskop betrachtet und von einem qualifizierten Pathologen ausgewertet, um die Diagnostik der möglicherweise mit einem bestimmten Antigen assoziierten pathophysiologischen Prozesse zu unterstützen. (1-4) Färbereagenzien wie die mit den Dako EnVision, EnVision +, EnVision Gl2, EnVision Gl2 Doublestain, EnVision FLEX, Dako REAL, LSAB (Peroxidase- und Alkalische-Phosphatase-Detektionssystemen), Dako LSAB +, Dako LSAB 2 sowie den Artisan Staining Systems mitgelieferten, außerdem Dako Antibody Diluents und Negativkontrollen. Für bestimmte Antikörper ist ein empfindlicheres Detektionssystem wie EnVision FLEX+, ADVANCE, CSA oder CSA II erforderlich. Informationen über Produktverfügbarkeit sind von Ihrem Händler erhältlich. Weitere erforderliche, aber nicht mitgelieferte Materialien sind Geräte, Chemikalien sowie Hilfs- und Zusatzmittel. Zur Geräteausstattung gehören Lichtmikroskop, Färbeschalen oder ein automatisiertes immunhistochemisches Färbesystem von Dako, ein Zeitmesser, der Intervalle zwischen 3 und 40 Minuten anzeigen kann, sowie Waschflaschen. Benötigte Chemikalien sind beispielsweise 15 mol/l Ammoniumhydroxid, verdünnt auf 0,037 mol/l, Gegenfärbung wie Hämatoxylin, destilliertes Wasser, Ethanol (absolut und 95 %) sowie Xylol oder Xylosersatz. Zu den Hilfs- und Zusatzmitteln gehören u.a. absorbierende Tücher, (positives und negatives) Kontrollgewebe, Deckgläser, wässriges Fixiermittel bzw. nichtwässriges permanentes Fixiermittel und elektrostatisch geladene, mit Poly-L-Lysin beschichtete oder silanisierte Objektträger. Weitere Hilfsmittel wie Kontroll-Objektträger können erforderlich sein. Produkte von Dako sind unter anderem Demaskierungslösungen; Verdünnungsmittel für Antikörper; blockierende Substanzen; Gegenfärbemittel; proteolytische Enzyme; Chromogensubstrate für Peroxidase und alkalische Phosphatase; Waschpufferlösungen; PAP Pen; wässrige Fixiermittel; Silanized Slides und Kontroll-Objektträger. Informationen zu den jeweils aktuellen Produkten sind auf der Dako-Website, im Katalog von Dako oder direkt von Dako erhältlich. Aufbewahrung Antikörper für die IHC von Dako sollten unter den im jeweiligen Sicherheitsdatenblatt angegebenen Bedingungen gelagert werden. Unverdünnte (konzentrierte), unkonjugierte Antikörper können in entsprechende Aliquote aufgeteilt und bei -20 C eingefroren werd en. Bei Verwendung eingefrorener Antikörper wiederholtes Einfrieren und Auftauen vermeiden. Gefrorene Antikörper können in kleinen Aliquoten so lange aufbewahrt werden, bis die regelmäßigen Assayverifikationen durch den Anwender inakzeptable Reaktivitätsveränderungen ergeben. (Siehe Qualitätskontrolle, Abschnitt Assayverifikation ). Vor der Verwendung sollten frische Verdünnungen des Antikörpers angesetzt werden. Nicht verwendete Mengen angesetzter Antikörper sind entsprechend den örtlichen Sicherheitsvorschriften zu entsorgen. Die Stabilität der Antikörper ist vom Anwender zu validieren. Bei Aufbewahrung zwischen 2 8 C sind alle Antikörper bis z um Ablauf des auf dem Produktetikett aufgedruckten Verfalldatums verwendbar. Es gibt keine offensichtlichen Anzeichen für einen eventuellen Produktzerfall von IHC-Reagenzien. Positiv- und Negativkontrollen sollten daher zur gleichen Zeit wie die Patientenproben getestet werden. Falls es zu einer unerwarteten Färbung kommt, die sich nicht durch Unterschiede bei Laborverfahren erklären lässt und auf ein Problem mit dem Antikörper hindeutet, ist der technische Kundendienst von Dako zu verständigen. ( ) DE_001 S. 1/9
2 Produkte nach Ablauf des Verfalldatums nicht mehr verwenden. Werden die Reagenzien anders als entsprechend den in der Packungsbeilage angegebenen Bedingungen aufbewahrt, muss deren Verwendung vom Benutzer validiert werden. (5) Trübungen und/oder Ausfällungen im Reagenz können auf Zersetzung durch Verlust des Antikörpertiters oder durch Bakterienwachstum hindeuten. Zur Feststellung eventueller Titer- bzw. Empfindlichkeitsverluste sollten positive und negative Gewebekontrollproben immer parallel zu den Patientenproben getestet werden. Falls eine unerwartete Färbung auftritt, die sich nicht durch Unterschiede bei Laborverfahren erklären lässt und auf ein Problem mit dem Antikörper hindeutet, ist der technische Kundendienst von Dako zu verständigen. Vorbereitung der Probe Vor der IHC-Färbung muss das Gewebe fixiert und verarbeitet werden. Eine Fixierung schützt vor Autolyse und Zerfall des exzidierten Gewebes, erhält die Antigenität, verstärkt den Refraktionsindex der Gewebeteile und steigert die Resistenz der Zellelemente gegen Gewebeverarbeitung. Zur Gewebeverarbeitung gehört Dehydrierung, Abscheidung von Dehydrierungsmitteln, Infiltration des Einbettungsmediums, Einbetten und Schneiden des Gewebes. Die am häufigsten verwendeten Fixiermittel für IHC-Gewebepräparate werden unten erörtert. Diese Angaben sind nur Richtlinien. Optimale Verfahren müssen vom Anwender selbst ermittelt und verifiziert werden. Spezielle Angaben zur Gewebefixierung und -verarbeitung bitte den Literaturhinweisen 1 und 6 entnehmen. Örtliche Sicherheitsbestimmungen beachten. Paraffineingebettete Gewebe Allgemeine Bemerkungen Neutral phospatgepuffertes Formalin in einer Konzentration von 10 % (v/v) (in der EU im Allgemeinen als 4 %iges w/v gepuffertes Formalin bezeichnet) ist zwar das gebräuchlichste Fixiermittel, allerdings sind die Detektionssysteme von Dako (wie unter Erforderliche, aber nicht mitgelieferte Materialien aufgeführt) erfolgreich mit Geweben verwendet worden, die mit verschiedenen anderen Fixiermitteln verarbeitet wurden. Infolgedessen sollte das Fixiermittel unter Berücksichtigung der Beschränkungen des primären Antikörpers und der institutionellen bzw. labortechnischen Gegebenheiten des Anwenders gewählt werden. Art und Konzentration des Fixiermittels sowie Fixierdauer und Größe des zu fixierenden Gewebeschnitts beeinflussen die Erhaltung der Gewebeantigene für die Immunfärbung. (7) Für eine reproduzierbare Färbung ist es ist daher wichtig, möglichst immer unter optimalen standardisierten Fixierbedingungen zu arbeiten. Empfohlen werden möglichst dünne Probenschnitte und kurze Fixierzeiten. Eine zu lange Einwirkzeit von Fixiermitteln kann zur Abschwächung der Färbung durch Antigenmaskierung, -beeinträchtigung oder -zerstörung führen. Als alternative Fixiermittel zur Erhaltung der gegen eine routinemäßige Formalinfixierung (10 %iges neutral gepuffertes Formalin) empfindlichen Gewebeantigene werden oft Zenker sche Lösung, B-5 und Fixiergemisch nach Bouin empfohlen. (8,9) Weitere Informationen zur Gewebefixierung den Literaturhinweisen 1 und 6, den Packungsbeilagen des/der primären Antikörper(s) und den Protokollen der Fixiermittel entnehmen. Gewebefixierung auf Formalinbasis (Neutral gepuffertes Formalin und Fixiergemisch nach Bouin) Die meisten Fixiermittel auf Formalinbasis enthalten 10 % Formalin, ein neutrales Salz zur Tonizitätserhaltung und ein gepuffertes System zur ph-stabilisierung. Diese Fixiermittel werden von Geweben gut toleriert und zeigen eine gute histologische Penetration. Bei schlecht fixierten bzw. eingebetteten Gewebeproben kann es allerdings zu Schrumpfungen oder Verformungen kommen. Kleine Gewebeblöcke (10,0 x 10,0 x 3,0 mm) in 5 10 ml neutral gepuffertem Formalin pro Block bis zu 24 Stunden fixieren. Das Fixiergemisch nach Bouin ist ein alternatives Fixiermittel auf Formalinbasis. Es enthält Pikrinsäure und ist für alle Gewebe außer Nierengewebe geeignet. Je nach Gewebestärke können die Proben für eine Dauer von 1 bis 12 Stunden fixiert werden. Übermäßige Fixierung macht die Gewebe spröde und wirkt sich negativ auf Aussehen und Quantität von Lipiden aus. Vor den Waschschritten mit Wasser die Fixierung mit einem Bad in 70 %igem Ethanol abschließen, um lösliche Pikrate auszufällen. Quecksilberchloridhaltige Fixiermittel (B-5 und Zenker sche Lösung) Quecksilberchloridhaltige Fixiermittel wie B-5 und Zenker sche Lösung enthalten häufig ein neutrales Salz zur Tonizitätserhaltung; sie sind mit anderen Fixiermitteln mischbar. Die histologische Eindringfähigkeit von Quecksilberchlorid-Fixiermitteln ist generell schlecht, auch werden sie von Gewebeproben nicht gut toleriert. Aus diesem Grund werden kleine Gewebeblöcke (7,0 x 7,0 x 2,5 mm) und kurze Fixierzeiten (1 bis 6 Stunden für B-5 und 2 bis 15 Stunden für Zenker sche Lösung) empfohlen. Nach dem Fixieren sollten die Gewebeblöcke gründlich mit Wasser gespült und in 70 %igem Ethanol nass aufbewahrt bzw. so lange gelagert werden, bis die Gewebeverarbeitung abgeschlossen werden kann. Die Fixierung mit Gewebeverarbeitung und Paraffineinbettung abschließen (siehe Abschnitt Verarbeitung und Paraffineinbettung ). Vor der Immunfärbung Quecksilberablagerungen mit einer Jod/Ethanol/Natriumthiosulfat-Lösung entfernen. (10) Die entsprechenden Vorsichtsmaßnahmen für den Umgang mit Reagenzien beachten, die Quecksilberverbindungen enthalten. ( ) DE_001 S. 2/9
3 Gewebefixierung in Ethanol Aufgrund seiner geringen Eindringfähigkeit ist Ethanol als Fixiermittel für routinemäßige histologische Verfahren nicht weit verbreitet. Allerdings lassen sich kleine Gewebestücke schnell fixieren und zeigen eine gute zytologische Konservierung. Gewebeblöcke (5,0 x 5,0 x 2,0 mm) 48 Stunden bei Raumtemperatur (20 25 C) in absolutem Alkohol fixieren, anschließ end zweimal je eine Stunde in frisches Xylol und zweimal nacheinander je eine Stunde in flüssiges Paraffin eintauchen. Die Paraffininfiltration mit der Einbettung abschließen. Verarbeitung und Paraffineinbettung Nach der Fixierung kann die Verarbeitung mit einem automatisierten Gewebeprozessor abgeschlossen werden. Die Gewebeproben werden mit Alkohol in verschiedenen Verdünnungsstufen dehydriert, mit Xylol oder Xylolersatz gereinigt und in Paraffin getränkt. Anschließend wird das Gewebe zur Erleichterung des Schneidens in Formen oder Kassetten in Paraffin eingebettet. Um die Antigendenaturierung zu minimieren, die Gewebe während der Verarbeitung keinen Temperaturen über 60 C aussetzen. Gewebeblöcke können nach dem Einbetten gelagert oder geschnitten werden. Korrekt fixierte und einbettete Gewebe sind bei Aufbewahrung an einem kühlen Ort unbegrenzt haltbar. Objektträger mit paraffineingebetteten Geweben können bei Temperaturen zwischen 2 8 C je nach Antigen 1 bis 3 Jahre aufbewahrt werden. (11) Haftung paraffineingebetteter Gewebeschnitte an Objektträger Aus paraffineingebetteten Blöcken entnommene Gewebeschnitte auf saubere Objektträger aus Glas aufbringen. Eine Stunde lang in einem Brutschrank bei höchstens 60 C dehydrieren. Für eine bessere Ha ftung der Gewebeschnitte während des IHC-Färbeverfahrens werden FLEX IHC Slides (Code K8020), elektrostatisch geladene oder mit Poly-L-Lysin beschichtete Objektträger bzw. Silanized Slides (Code S3003) empfohlen. Bei Verwendung elektrostatisch geladener, mit Poly-L-Lysin beschichteter oder silanisierter Objektträger auf jeden Fall Haftmittel wie Gelatine, Klebstoff und/oder kommerzielle proteinhaltige Produkte in der Fixierflüssigkeit vermeiden. Für Färbeverfahren, die eine proteolytische Andauung oder wärmeinduzierte Epitopdemaskierung (Demaskierung) erfordern, werden beschichtete Objektträger ausdrücklich empfohlen. Entparaffinierung und Rehydrierung Zur Entfernung des Einbettungsmediums müssen die Gewebeschnitte vor der Färbung entparaffiniert und anschließend rehydriert werden. Eine unvollständige Entfernung von Paraffin ist zu vermeiden. Reste des Einbettungsmediums können eine unspezifische oder verminderte Färbung zur Folge haben. 1. Die Objektträger in ein Xylolbad stellen und 5 (±1) Minuten inkubieren. Den Vorgang in einem frischen Bad wiederholen. 2. Überschüssige Flüssigkeit durch Abklopfen entfernen und die Objektträger 3 (±1) Minuten in absolutes Ethanol eintauchen. Den Vorgang in einem frischen Bad wiederholen. 3. Überschüssige Flüssigkeit durch Abklopfen entfernen und die Objektträger 3 (±1) Minuten in 95 %iges Ethanol eintauchen. Den Vorgang in einem frischen Bad wiederholen. 4. Überschüssige Flüssigkeit durch Abklopfen entfernen und Objektträger mindestens 30 Sekunden in destilliertes oder entionisiertes Wasser eintauchen. Wenn weder proteolytische Andauung noch Demaskierung erforderlich sind, mit dem Färbeverfahren beginnen. Xylol und Alkohollösungen wöchentlich oder spätestens nach 200 Objektträgern auswechseln. Anstelle von Xylol kann Toluol oder ein Xylolersatz wie Histoclear verwendet werden; in diesem Fall können längere Inkubationszeiten und häufigeres Wechseln der Lösung erforderlich sein. Gegebenenfalls können die rehydrierten Gewebe bis zu 18 Stunden vor Verwendung bei 2 8 C in Pufferlösung aufbewahrt werden. Die Gewebe vor dem Färben Raumtemperatur (20 25 C) annehmen lassen. Proteolytische Andauung und Demaskierung Es ist bekannt, dass Formaldehyd durch Bildung intermolekularer Vernetzungen konformative Veränderungen an den Antigenmolekülen auslöst. Zu starke Formalinfixierung kann Antigenerkennungsstellen maskieren und die spezifische Färbung vermindern. Diese Stellen können allerdings vor der Immunfärbung durch proteolytische Gewebeandauung oder Target Retrieval der Gewebeschnitte demaskiert werden. Das jedem primären Antikörper beiliegende Sicherheitsdatenblatt enthält Informationen über die Eignung einer dieser Gewebevorbehandlungen. Vor dem Färben können entparaffinierte und rehydrierte Gewebeschnitte mit proteolytischen Enzymen vorbehandelt werden. Dazu eignen sich proteolytische Enzyme wie Dako Proteinase K, RTU (Code S3020), Pepsin (Code S3002) oder Proteolytic Enzyme, RTU (Code S3007). Die Dauer der Andauung beträgt normalerweise 6 Minuten. Die empfohlene Zeit der jeweiligen Packungsbeilage des Enzyms entnehmen. ACHTUNG: Eine zu lange Andauung kann zu unspezifischer Färbung und/oder inakzeptabler Morphologie führen. Gründlich mit destilliertem Wasser abspülen, dann das Färbeverfahren nach den Anweisungen des Detektionssystems durchführen. ( ) DE_001 S. 3/9
4 Wärmeinduzierte Epitopdemaskierung (HIER/Target Retrieval) vor IHC-Färbeverfahren verstärkt bei vielen primären Antikörpern die Färbungsintensität. Bei einigen Antikörpern ist dieses Verfahren erforderlich. Die empfohlene Demaskierungsmethode dem Sicherheitsdatenblatt des Antikörpers entnehmen. Zur wärmeinduzierten Epitopdemaskierung gehört ein Eintauchen der Gewebeschnitte in eine vorgewärmte Pufferlösung, deren Temperatur in einem PT Link, Wasser- bzw. Dampfbad (95 99 ºC), einem Dampfdrucktopf (121 C) oder einem anderen Laborgerät mit kontroll ierbarer Temperatur beibehalten wird. Für optimale Ergebnisse mit einem PT Link entweder Demaskierungslösung von EnVision FLEX und FLEX+ Kits (Codes K8000, K8002, K8010, und K8012) verwenden, oder Optional EnVision FLEX Target Retrieval Solutions (Codes K8004 und K8005). Weitere Demaskierungslösungen von Dako sind Target Retrieval Solution, ph 9 (10x), (3-in-1) a (Code S2375), Target Retrieval Solution (Code S1699 und S1700) und Target Retrieval Solution, Citrate ph 6 (Code S2369 und S2031). Die jeweiligen Bedienungsanleitungen beachten. Wird ein PT Link entweder zusammen mit Target Retrieval Solution von EnVision FLEX and FLEX+ Kits oder mit K8004, K8005, S2375, S1699 verwendet, können Entparaffinisierung, Rehydrierung und Demaskierung in einem Schritt durchgeführt werden. Nach dem PT Link-Durchlauf ein Quick Dip-Verfahren durchführen und dazu Waschpuffer von EnVision FLEX und FLEX+ Kits, Optional EnVision FLEX Waschpuffer (20x) (Code K8007), oder Dako Waschpuffer 10x (Code S3006) verwenden. Mit dem Dako EnVision + System, dem Dampfdrucktopfverfahren oder anderen Laborgeräten mit kontrollierbarer Temperatur werden stärkere Färbungen erzielt als mit der Wasserbadmethode. Die Gebrauchsanleitung der Target Retrieval Solution oder Literaturhinweis 12 beachten. Wird für die Demaskierung ein Wasserbad verwendet, kann bei manchen Antigenen vor der Erwärmung eine zusätzliche Vorbehandlung mit proteolytischen Enzymen erforderlich sein. Gewebeschnitte können 10 Minuten bei Raumtemperatur (20 25 C) mit Dako Proteinase K (Code S3004), verdünnt im Verhältnis 1:500 in Tris-HCl Puffer, ph 7,2 7,6, angedaut werden. In bestimmten Höhenlagen (oberhalb 1372 m [4500 Fuß]) kann die Demaskierungslösung kochen, noch ehe die gewünschte Optimaltemperatur erreicht ist. Unter diesen Umständen wird als Alternative die Erwärmung der Objektträger auf die höchste erreichbare Temperatur und eine längere Inkubationszeit der Objektträger in der Demaskierungslösung empfohlen, bis die gewünschte Färbungsintensität erreicht ist. (11) Wahlweise kann auch ein geschlossenes Drucksystem wie ein Dampfdrucktopf verwendet werden, um 121 C zu erzielen. Es liegt allerdings in der Zuständigkeit jedes einzelnen Labors, das beste Verfahren und die optimale Demaskierungszeit für die jeweiligen Bedingungen zu ermitteln. Gefrierschnitte Gefrierschnitte sollten von schockgefrorenen Gewebeblöcken (etwa 1,0 x 1,0 x 0,5 cm) entnommen und 2 bis 24 Stunden an der Luft getrocknet werden. Getrocknete Schnitte können 10 Minuten in raumtemperiertem (20 25 C) Azeton oder 30 Sekunden in gepuffertem F ormylazeton fixiert werden. Die Schnitte an der Luft trocknen lassen, bis sie vollständig dehydriert sind. Mit der Immunfärbung fortfahren oder die Objektträger in Aluminiumfolie einpacken und bis zu sechs Monate bei -20 C aufbewahren. Vor der Verwendung die eingewickelten Gefrierschnitte Raumtemperatur annehmen lassen. Schnitte 10 Minuten in kaltem Azeton (2 8 C) nachfixieren. Objektträger in ein TBS-Bad einlegen. Das TBS-Bad mehrmals vorsichtig wechseln, um Azetonreste zu entfernen. Sind die Schnitte zu dick (mehr als 4 6 µm), nicht korrekt fixiert oder ungleichmäßig getrocknet, können Artefakte auftreten, die die Auswertung der Färbung beeinflussen. Es kann beispielsweise zur Zerstörung der Zellmembran und zur Chromatolyse kommen. Bei einer Gegenfärbung mit Hämatoxylin können die Zellkerne ein angeschwollenes Aussehen haben und einheitlich blau gefärbt sein. Weitere Proben Dako Detektionssysteme eignen sich auch für die Antigenfärbung bei Knochenschnitten und Proben von Knochenmark, Blutausstrichen, Cytospins und Imprints. Ausstriche können 2 24 Stunden an der Luft getrocknet und dann für die sofortige Färbung verarbeitet und fixiert bzw. in Aluminiumfolie eingewickelt und bei höchstens -20 C bis zu sechs Monate aufbewahrt werden. Luftgetrocknete oder aufgetaute Ausstriche können 90 Sekunden in Azeton-Methanol (1:1) fixiert werden. Zulässig ist auch die Fixierung in Azeton oder Azeton-Methanol-Formalin (10:10:1). Knochengewebe müssen vor dem Schneiden und der Weiterverarbeitung entkalkt werden, um das Schneiden des Gewebes zu erleichtern und Schäden an den Mikrotomklingen zu vermeiden. (1) Die Entkalkung kann sich auf die IHC-Färbung auswirken. Für Fachpersonal in den USA gilt laut Clinical Laboratory Improvement Amendments of 1988 (CLIA von 1988)(42 CFR (b)), dass das Labor gefärbte Objektträger mindestens 10 Jahre und Probenblöcke mindestens zwei Jahre ab Untersuchungsdatum aufbewahren muss. Weitere Details zur Vorbereitung der Proben sind dem Dako Hochschulführer: Immunhistochemical Staining Methods (6) oder den Literaturangaben 1 und 2 zu entnehmen. a In den USA sind die Dako Target Retrieval Solution, S1699, (10x) und EnVision FLEX Target Retrieval Solution Low ph, K8005 nicht für den Verkauf als 3-in-1 -Puffer zur Verwendung bei 3-in-1 -Verfahren erhältlich. Möglicherweise ist eine Lizenzierung unter US-Patent Nr. 6,649,368 B1 erforderlich. ( ) DE_001 S. 4/9
5 Vorsichtsmaßnahmen Färbeverfahren 1. Nur für Fachpersonal bestimmt. 2. Die Produkte können Natriumazid (NaN 3) enthalten, eine in reiner Form äußerst giftige Chemikalie. NaN 3 kann auch in Konzentrationen, die nicht als gefährlich klassifiziert sind, mit Blei- und Kupferabflussrohren reagieren und hochexplosive Ansammlungen von Metallaziden bilden. Nach der Entsorgung stets mit viel Wasser nachspülen, um Ansammlungen von Metallaziden in den Leitungen vorzubeugen. (12) 3. Mit biologischen Proben, sowohl vor als auch nach der Fixierung, und allen Materialien, die damit in Berührung gekommen sind, ist so umzugehen, als könnten sie Krankheiten übertragen. Bei der Entsorgung sind angemessene Vorsichtsmaßnahmen zu beachten. (14) Reagenzien nie mit dem Mund pipettieren und Haut- bzw. Schleimhautkontakt mit Reagenzien und Proben vermeiden. Empfindliche Bereiche nach Kontakt mit den Reagenzien mit reichlich Wasser waschen. Bei der Handhabung biologischen Materials von Patienten und während des Färbevorgangs Schutzkleidung tragen. 4. Auf Anfrage sind für Fachpersonal Sicherheitsdatenblätter erhältlich. 5. Andere als die angegebenen Inkubationszeiten bzw. -temperaturen können zu fehlerhaften Ergebnissen führen. Jede derartige Abänderung ist vom Anwender zu validieren. 6. Nicht verwendete Lösung ist entsprechend örtlichen, bundesstaatlichen und staatlichen Richtlinien zu entsorgen. Für hochmoderne Färbeverfahren FLEX gebrauchsfertige Antikörper verwenden. Wenn sie mit EnVision FLEX und FLEX+ Visualisierungssystemen optimiert wurden, liefern diese Antikörper bei Anwendung auf PT Link und Autostainer Link oder Dako Autostainer-Instrumenten die gewünschten Ergebnisse. Angaben zur Verwendung konzentrierter (unverdünnter) Antikörper der jeweiligen Packungsbeilage, und Hinweise zum empfohlenen Vorgehen den Anweisungen des Detektionssystems entnehmen. Für gebrauchsfertige Antikörper der N-Serie die produktspezifischen Packungsbeilagen und den Abschnitt Färbeverfahren der Anweisungen für die Dako Detektionssysteme EnVision +, EnVision Gl2, Doublestain, LSAB 2 und LSAB + beachten. Qualitätskontrolle Unterschiede in der Gewebeverarbeitung und den technischen Verfahren im Labor des Anwenders können zu sehr unterschiedlichen Ergebnissen führen, daher sind zusätzlich zu den folgenden Verfahren regelmäßige Leistungskontrollen entsprechend den geltenden Richtlinien vorzunehmen. Für Fachpersonal in den USA sind weitere Informationen den Richtlinien zur Qualitätskontrolle des College of American Pathologists (CAP) Accreditation Program for Immunohistochemistry, NCCLS Quality Assurance for Immunocytochemistry, Approved Guideline (15), und Literaturhinweis 7 zu entnehmen. Positives Kontrollgewebe Als Kontrollen dienen frische, durch Autopsie, Biopsie oder einen operativen Eingriff gewonnene Proben, die in der gleichen Weise fixiert, verarbeitet und eingebettet werden wie die Patientenprobe(n). Positive Kontrollgewebe zeigen sachgemäß vorbereitete Gewebe und geeignete Färbetechniken an. In jedem Färbedurchlauf sollte für jedes Set von Testbedingungen ein positives Kontrollgewebe mitgeführt werden. Die als Positivkontrolle verwendeten Gewebe sollten eine schwach positive Färbung aufweisen, damit feine Veränderungen der primären Antikörpersensitivität nachweisbar sind. Im Handel erhältliche Gewebeschnitte oder Proben, die anders als die Patientenprobe(n) verarbeitet werden, validieren zwar die Leistung der Reagenzien, bestätigen jedoch nicht die Gewebevorbereitung. Angaben zu normalen Gewebeschnitten, die als positive Gewebekontrollen verwendbar sind, dem Abschnitt Leistungsmerkmale der produktspezifischen Packungsbeilage entnehmen. Bekanntermaßen positive Kontrollgewebe sollten nur zur Überprüfung der korrekten Funktionsweise der verarbeiteten Geweben und Testreagenzien verwendet werden, NICHT aber zur Unterstützung der spezifischen Diagnose anhand von Patientenproben. Weisen die positiven Kontrollgewebe keine Färbung auf, so müssen die Ergebnisse der Testprobe für ungültig erklärt werden. Negative Kontrollgewebe Um die Spezifität des primären Antikörpers zu verifizieren und Hinweise auf eine spezifische Hintergrundfärbung zu erhalten, ist bei jedem Färbedurchlauf eine bekanntermaßen gegen das getestete Antigen negative (siehe Abschnitt Leistungsmerkmale der produktspezifischen Packungsbeilage), normale Gewebeprobe, die in der gleichen Weise wie die Patientenprobe fixiert, verarbeitet und eingebettet wurde, einzusetzen. Aufgrund der in den meisten Gewebeschnitten anzutreffenden Vielzahl verschiedener Zelltypen existieren interne negative Kontrollstellen (dieses ist vom Benutzer zu verifizieren). Falls das negative Kontrollgewebe Färbungen aufweist, sollten die Ergebnisse der Patientenprobe für ungültig erklärt werden. ( ) DE_001 S. 5/9
6 Negativkontrolle Zur Beurteilung unspezifischer oder unerwünschter Färbung und im Hinblick auf eine bessere Interpretation der spezifischen Färbung an der Antigenstelle für jede Patientenprobe eine Negativkontrolle mitführen. Ein negatives Kontrollreagenz enthält im Idealfall entweder einen Antikörper, der keine spezifische Reaktivität mit menschlichen Geweben aufweist (nicht-reaktiv mit Humangewebe) in der gleichen Grundsubstanz/Lösung wie der verdünnte primäre Antikörper. Bei dem mit Humangewebe nicht-reaktiven Antikörper sollte es sich um denselben Isotyp handeln und er sollte derselben Tierart entstammen wie der primäre Antikörper. Er ist auf dieselbe Immunglobulin- oder Proteinkonzentration wie dieser zu verdünnen. Geeignet ist je nach Typ des verwendeten primären Antikörpers normales/nichtimmunes Serum desselben tierischen Ursprungs wie der primäre Antikörper in einer dem verdünnten primären Antikörper äquivalenten Proteinkonzentration in der gleichen Grundsubstanz/Lösung. Spezielle Empfehlungen der Packungsbeilage jedes primären Antikörpers und Tabelle 1 entnehmen. Das Verdünnungsmittel allein kann ebenfalls verwendet werden, ist aber eine weniger wünschenswerte Alternative als die oben beschriebenen Negativkontrollen. Die Inkubationszeit für die Negativkontrolle sollte mit der für den primären Antikörper übereinstimmen. Tabelle 1. Beispiele für Negativkontrollreagenzien für konzentrierte Antikörper Typ des primären Antikörpers Empfohlene Negativkontrolle Monoklonaler FLEX Universelle Negativkontrolle für primäre Maus-Antikörper, Code gebrauchsfertiger Maus-Antikörper. IR750 (für Autostainer Link-Instrumente) und IS750 (für Dako Autostainer-Instrumente). Polyklonaler oder monoklonaler Universelle Negativkontrolle für primäre Kaninchen-Antikörper, Code FLEX gebrauchsfertiger Kaninchen- IR600 (für Autostainer Link-Instrumente) und IS600 (für Dako Antikörper. Autostainer-Instrumente).* In Aszites erzeugter monoklonaler In Aszites erzeugter, mit Humangewebe nicht-reaktiver monoklonaler Maus-Antikörper. Antikörper. Dieser Antikörper zur Negativkontrolle sollte demselben Isotyp angehören wie der primäre Antikörper. Wahlweise kann normales/nichtimmunes Mausserum, Code X0910, verwendet werden. In Gewebekultur erzeugter In Gewebekultur erzeugter, mit Humangewebe nicht-reaktiver monoklonaler Maus-Antikörper. monoklonaler Maus-Antikörper. Dieser Antikörper zur Negativkontrolle sollte demselben Isotyp angehören wie der primäre Antikörper. Dako Codes X0931 (IgG1), X0943 (IgG2 a), X0944 (IgG2 b), X0942 (IgM). Wahlweise kann fötales Rinderserum verwendet werden.* Polyklonaler Kaninchen-Antikörper, Kaninchen-Immunglobulinfraktion (normal), Dako Code X0903. Immunglobulinfraktion. Festphasengebundener, Kaninchen-Immunglobulinfraktion (festphasengebunden), Dako Code polyklonaler Kaninchen-Antikörper, X0936. Immunglobulinfraktion. Polyklonaler Kaninchen-Antikörper, Normales/nichtimmunes Kaninchen-Serum, Vollserum, Dako Code Vollserum. X0902. * Fötales Rinderserum eignet sich, wenn es nach der Verarbeitung noch im primären Antikörper erhalten bleibt. Bei Verwendung von Antikörper-Panels an seriellen Gewebeschnitten können die Bereiche eines Objektträgers, die eine negative Färbung aufweisen, für andere Antikörper als Negativkontrolle bzw. Kontrolle einer unspezifischen Hintergrundbindung dienen, sofern sie in gleicher Verdünnung vorliegen und gleichen tierischen Ursprungs sind. Zur Unterscheidung zwischen endogener Enzymaktivität bzw. unspezifischer Enzymbindung und einer spezifischen Immunreaktivität können weitere Patientengewebe nur mit Substratchromogen oder einer Kombination aus Enzymkomplexen (Avidin-Biotion, Streptavidin, markiertes Polymer) und Substratchromogen gefärbt werden. Das genaue Vorgehen beim technischen Kundendienst von Dako erfragen. ( ) DE_001 S. 6/9
7 Tabelle 2. Zweck der täglichen Qualitätskontrolle Gewebe: Fixiert und verarbeitet wie die Patientenprobe Positivkontrollen: Das nachzuweisende Zielantigen bekanntermaßen enthaltende Gewebe oder Zellen (möglicherweise im Patientengewebe). Gewebe, das eine schwach positive Färbung aufweist, ist am empfindlichsten gegenüber Antikörperabbau bzw. Fehlern am Detektionssystem. Negativkontrolle: Vermutlich negative Gewebe oder Zellen (im Patientengewebe oder im Gewebe Spezifischer Antikörper & Detektionssystem Kontrolliert alle Analyseschritte. Validiert Reagenz und Immunfärbungsverfahren. Nachweis unbeabsichtigter Antikörper-Kreuzreaktivität mit Zellen und Zellbestandteilen. Negativkontrolle* oder Puffer mit demselben Detektionssystem wie beim spezifischen Antikörper Nachweis unspezifischer Hintergrundfärbung. Nachweis unspezifischer Hintergrundfärbung. der positiven Kontrollprobe). Patientengewebe. Nachweis spezifischer Färbung. Nachweis unspezifischer Hintergrundfärbung. * Gleiche Tierart und gleicher Isotyp wie der spezifische Antikörper, aber nicht gegen dasselbe Zielantigen gerichtet. Zum Nachweis unspezifischer Bindung, z.b. Bindung des Fc-Fragments des Antikörpers an das Gewebe. Assayverifikation Vor dem erstmaligen Gebrauch eines Antikörpers oder Immunfärbungssystems in einem diagnostischen Verfahren sollte der Anwender die Spezifität des Assays durch Tests an einer Reihe vorhandener Gewebe mit bekannten IHC-Leistungsmerkmalen, unter denen sich bekannt positive und negative Gewebe befinden, verifizieren. Siehe die zuvor in diesem Abschnitt der Allgemeinen Richtlinien erörterten Qualitätskontrollmaßnahmen und, für Anwender in den Vereinigten Staaten, die Qualitätskontrollanforderungen des CAP Certification Program for Immunohistochemistry und NCCLS Quality Assurance for Immunocytochemistry, Approved Guideline. (15) Diese Maßnahmen sind für jede neue Antikörpercharge bzw. immer dann zu wiederholen, wenn die Assayparameter verändert werden. Die in der produktspezifischen Packungsbeilage, Abschnitt Leistungsmerkmale, aufgeführten Gewebe sind für die Assayverifikation geeignet. Fehlersuche und -behebung Auswertung der Färbung Bei ungewöhnlichen Färbungen zur Mängelbeseitigung im Abschnitt Fehlersuche und -behebung im Dako Hochschulführer: Immunohistochemical Staining Methods, Fourth Edition (6) nachschlagen, den Technischen Kundendienst von Dako verständigen oder über unsere Website melden. Positives Kontrollgewebe Zuerst sollte das Positivkontrollgewebe untersucht werden, damit gewährleistet ist, dass alle Reagenzien korrekt funktionieren. Positive Reaktivität wird durch ein rotes (3-Amino-9-Ethylkarbazol, AEC), leuchtend rosafarbenes (Neu-Fuchsin oder Fast Red) oder braunes (3, 3'-Diaminobenzidin-Tetrahydrochlorid, DAB) Reaktionsprodukt an der Zielantigenstelle angezeigt. Für spezifische Färbemuster siehe die Abschnitte Auswertung der Färbung oder Leistungsmerkmale der produktspezifischen Packungsbeilagen. Weisen die positiven Kontrollgewebe nicht das erwartete Färbemuster auf, so müssen alle Ergebnisse der Testprobe für ungültig erklärt werden. HINWEIS: Die Farbe des Reaktionsprodukts kann abweichen, wenn andere Substratchromogene als angegeben verwendet werden. Die erwartete Farbreaktion der Packungsbeilage des Substrats entnehmen. Bei Abweichungen vom Färbeverfahren kann Metachromie auftreten. (16) Je nach Inkubationszeit und Stärke des Hämatoxylins ergibt die Gegenfärbung eine blaue Färbung der Zellkerne. Übermäßige oder unvollständige Gegenfärbungen können die sachgemäße Auswertung der Ergebnisse beeinträchtigen. Negative Kontrollgewebe Zur Verifizierung der spezifischen Markierung des Zielantigens durch den primären Antikörper sollte die Negativkontrolle nach dem positiven Kontrollgewebe untersucht werden. Die Abwesenheit einer spezifischen Färbung in den Negativkontrollproben bestätigt das Fehlen einer Antikörper-Kreuzreaktivität mit Zellen und Zellkomponenten. Falls das negative Kontrollgewebe andere als die vorgenannten Färbungen aufweist, sollten die Ergebnisse der Patientenproben für ungültig erklärt werden. Bei negativen Geweben sollte Hämatoxylin eine blau-violette Färbung hervorrufen. Eine eventuelle unspezifische Färbung erscheint diffus. Bei übermäßig formalinfixierten Gewebeschnitten kann es gelegentlich zur Einfärbung des Bindegewebes kommen. Für die Auswertung der Färbeergebnisse nur intakte Zellen verwenden. Nekrotische oder degenerierte Zellen können eine unspezifische Färbung aufweisen. (7) ( ) DE_001 S. 7/9
8 Aufgrund nicht-immunologischer Bindung von Proteinen oder Substrat-Reaktionsprodukten können falsch-positive Resultate auftreten. Diese können auch, insbesondere bei Gefrierschnitten bzw. in Abhängigkeit vom Typ des zur Darstellung der Reaktion verwendeten Enyzmmarkers, durch endogene Enzyme wie Myeloperoxidase, alkalische Leukozytenphosphatase und Hämoglobinpseudoperoxidase. (17) Patientengewebe Die Patientenproben sollte zuletzt untersucht werden. Die Intensität der positiven Färbung ist im Kontext einer eventuellen unspezifischen Hintergrundfärbung mit der Negativkontrolle zu bewerten. Wie bei allen IHC-Tests bedeutet ein negatives Ergebnis, dass das Antigen nicht nachgewiesen wurde, nicht aber, dass das Antigen in den getesteten Zellen/Geweben nicht vorhanden war. Gegebenenfalls ein Antikörper-Panel zum Nachweis falsch-negativer Reaktionen verwenden. Angaben zur Immunreaktivität des primären Antikörpers der produktspezifischen Packungsbeilage entnehmen. Allgemeine Beschränkungen 1. IHC ist ein diagnostisches Mehrfachschritt-Verfahren, das hinsichtlich Auswahl, Fixierung und Verarbeitung von Geweben, Auswahl der geeigneten Reagenzien sowie Vorbereitung des IHC-Objektträgers und Auswertung der Färbungsergebnisse ein Spezialtraining erfordert. 2. Gewebefärbungen hängen von der sachgemäßen Handhabung und Verarbeitung des Gewebes vor der Färbung ab. Unsachgemäßes Fixieren, Einfrieren, Auftauen, Waschen, Trocknen, Erhitzen, Schneiden oder Verunreinigung durch andere Gewebe oder Flüssigkeiten kann zu Artefakten, Antikörper-Trapping oder falsch negativen Ergebnissen führen. Widersprüchliche Ergebnisse können auf Unterschiede bei den Fixierungs- und Einbettungsmethoden oder auf Unregelmäßigkeiten innerhalb des Gewebes zurückzuführen sein. 3. Übermäßige oder unvollständige Gegenfärbung kann die sachgemäße Auswertung der Ergebnisse beeinträchtigen. 4. Die klinische Auswertung einer Färbung oder deren Ausbleiben muss durch morphologische Studien und geeignete Kontrollen sowie durch andere diagnostische Tests ergänzt werden. Für die Auswertung der gefärbten Präparate ist ein qualifizierter Pathologe zuständig, der mit Antikörpern, Reagenzien und den zur Auswertung der gefärbten Präparate angewandten Methoden vertraut ist. Die Färbung muss in einem offiziell zugelassenen, lizenzierten Labor unter Aufsicht eines Pathologen erfolgen, dessen Aufgabe es ist, die gefärbten Objektträger zu überprüfen und die Eignung der positiven und negativen Kontrollen zu gewährleisten. 5. Unerwartete negative Reaktionen bei schlecht differenzierten Neoplasien können durch Verlust oder deutliches Nachlassen der Antigenexpression bzw. durch Verluste oder Mutation(en) des Gens/der Gene, die das Antigen kodieren, hervorgerufen werden. Unerwartete positive Färbungen in Tumoren können durch die Expression eines normalerweise in morphologisch gleichen normalen Zellen nicht exprimierten Antigens, bzw. durch Persistenz oder Aneignung eines Antigens in einem Neoplasma, das mit einer unterschiedlichen Zellabstammung assoziierte morphologische und immunhistochemische Eigenschaften entwickelt (divergente Differenzierung), verursacht werden. Die histopathologische Klassifizierung von Tumoren ist keine exakte Wissenschaft, daher sind Angaben zu unerwarteten Färbungen in der Fachliteratur gelegentlich widersprüchlich. 6. Gewebe von mit dem Hepatitis-B-Virus infizierten Personen und Gewebe mit Hepatitis-B-Virus- Oberflächenantigen (HBsAg) können mit Meerrettichperoxidase eine unspezifische Färbung aufweisen. (18) 7. Reagenzien können in zuvor nicht getesteten Geweben unerwartete Reaktionen zeigen. Selbst in getesteten Gewebegruppen können unerwartete Reaktionen aufgrund biologischer Unterschiede bei der Antigen-Expression in Neoplasmen oder anderen pathologischen Geweben nicht völlig ausgeschlossen werden. (19) Bitte bei dokumentierten unerwarteten Reaktionen den technischen Kundendienst von Dako verständigen. 8. Normale/nichtimmune Sera, die von derselben Tierart stammen wie die in den Blockierungsschritten verwendeten sekundären Antiseren, können durch Auto-Antikörper oder natürliche Antikörper falschnegative oder falsch-positive Ergebnisse auslösen. 9. Aufgrund der nicht-immunologischen Bindung von Proteinen oder Substrat-Reaktionsprodukten können falschpositive Resultate auftreten. Diese können auch, insbesondere bei Gefrierschnitten bzw. in Abhängigkeit vom Typ des zur Immunfärbung verwendeten Markers, durch endogenes Biotin oder Enzyme wie Myeloperoxidase, alkalische Leukozytenphosphatase und Hämoglobinpseudoperoxidase hervorgerufen werden. (17) 10. Die wärmeinduzierte Epitopdemaskierung (Target Retrieval) kann zu HIER-Lipofuszin-Artefakten führen. Target Retrieval kann auch unerwartete oder unerwünschte Stellen demaskieren. 11. Werden primäre Antikörper mit einem bestimmten Färbesystem in zu hoher Konzentration verwendet, können falsch-negative Färbungsergebnisse mit oder ohne Hintergrund auftreten. 12. Gebrauchsfertige primäre Antikörper sind vorverdünnt und für die Verwendung mit einem speziellen Färbungssystem optimiert. Werden sie mit anderen Detektionssystemen von Dako oder anderen Herstellern verwendet, sind sie nicht gebrauchsfertig und müssen erneut optimiert und gemäß dem IHC- Protokoll des klinischen Labors validiert werden. 13. Sofern in den Anweisungen nicht spezifisch angegeben, sind die Leistungsmerkmale der zur IHC verwendeten Antikörper nicht für andere Laborverfahren vorgesehen. ( ) DE_001 S. 8/9
9 Literaturangaben 1. Kiernan JA. Histological and Histochemical Methods: Theory and Practice. New York: Pergamon Press Sheehan DC and Hrapchak BB. Theory and Practice of Histotechnology. St. Louis: C.V. Mosby Co Diamandis EP, Schwartz MK. Tumor Markers: Physiology, Pathobiology, Technology, and Clinical Applications. Washington DC: AACC Press Dabbs DJ. Diagnostic Immunohistochemistry. Philadelphia: Churchill Livingstone Elsevier Clinical Laboratory Improvement Amendments of 1988: Final Rule, 57 CFR 7163, February 28, Boenisch T, Farmilo AJ, Stead RH. Handbook: Immunochemical Staining Methods, 3rd Edition. Carpinteria: Dako Corporation Nadji M and Morales AR. Immunoperoxidase. Part I: The technique and its pitfalls. Lab Med 1983; 14: Banks PM. Diagnostic applications of an immunoperoxidase method in hematopathology. J Histochem Cytochem 1979; 27: Culling CFA, Reid PE, Sinnott NM. The effect of various fixatives and trypsin digestion upon the staining of routine paraffin-embedded sections by the peroxidase-antiperoxidase and immunofluorescent technique. J Histotech 1980; 3: Carson FL (ed.). Histotechnology: A self-instructional text. Chicago: ASCP Press 1990; Grabau DA, Nielsen O, Hansen S, Nielsen MM, Lænkholm A-V, Knoop A, Pfeiffer P. Influence of storage temperature and high-temperature antigen retrieval buffers on results of immunohistochemical staining in sections stored for long periods. Appl Immunohistochem 1998; 6(4): Shi SR, Key ME, Kalra KL. Antigen retrieval in formalin-fixed, paraffin-embedded tissues: An enhancement method for immunohistochemical staining based on microwave oven heating of tissue sections. J Histochem Cytochem 1991; 39: Koopal SA, Coma MI, Tibosch AMG, Surmeijer AJH. Low temperature heating overnight in Tris-HCI buffer ph 9 is a good alternative for antigen retrieval in formalin-fixed paraffin-embedded tissue. Appl Immunohistochem 1998; 6: National Committee for Clinical Laboratory Standards. Protection of laboratory workers from instrument biohazards and infectious disease transmitted by blood, body fluids, and tissue; approved guideline. Villanova, PA 1997: Order code M29-A 15. National Committee for Clinical Laboratory Standards. Quality assurance for immunocytochemistry; approved guideline. Villanova, PA, 1999; 19(26):Order code MM4-A 16. Koretz K, Lemain ET, Brandt I, and Moller P. Metachromasia of 3-amino-9-ethylcarbazole (AEC) and its prevention in immunoperoxidase techniques. Histochem 1987; 86: Elias JM, Gown AM, Nakamura RM, Wilbur DC, Herman GE, Jaffe ES, Battifora H, Brigati DJ. Special report: Quality control in immunohistochemistry. Amer J Clin Pathol 1989; 92: Omata M, Liew CT, Ashcavai M, Peters RL. Nonimmunologic binding of horseradish peroxidase to hepatitis B surface antigen: a possible source of error in immunohistochemistry. Amer J Clin Pathol 1980; 73: Herman GE and Elfont EA. The taming of immunohistochemistry: The new era of quality control. Biotech Histochem 1991; 66: Edition 11/09 ( ) DE_001 S. 9/9
ZytoFast human Ig-kappa Probe
 ZytoFast human Ig-kappa Probe (Digoxigenin-markiert) T-1115-400 40 (0,4 ml) Zum Nachweis von lg-kappa (κ) mrna durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß EU-Richtlinie
ZytoFast human Ig-kappa Probe (Digoxigenin-markiert) T-1115-400 40 (0,4 ml) Zum Nachweis von lg-kappa (κ) mrna durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß EU-Richtlinie
6/18 Probe (Digoxigenin-markiert)
 ZytoFast HPV type 16/1 6/18 Probe (Digoxigenin-markiert) T-1056-400 40 (0,4 ml) Zum Nachweis von Human Papilloma Virus (HPV) Typ 16/18 DNA durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum
ZytoFast HPV type 16/1 6/18 Probe (Digoxigenin-markiert) T-1056-400 40 (0,4 ml) Zum Nachweis von Human Papilloma Virus (HPV) Typ 16/18 DNA durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum
ZytoFast DNA (-) Control Probe
 ZytoFast DNA (-) Control Probe (Digoxigenin-markiert) T-1054-400 40 (0,4 ml) Zur Abschätzung der unspezifischen Hintergrundfärbung durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum
ZytoFast DNA (-) Control Probe (Digoxigenin-markiert) T-1054-400 40 (0,4 ml) Zur Abschätzung der unspezifischen Hintergrundfärbung durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum
Immunhistochemische Färbung F Immunfluoreszenz. Vortrag Immunologie am von Christopher Tollrian
 Immunhistochemische Färbung F und Immunfluoreszenz Vortrag Immunologie am 22.05.2009 von Christopher Tollrian Inhalt Grundlagen Immunhistochemische Färbung Immunfluoreszenz Proben-Vorbereitung Methoden
Immunhistochemische Färbung F und Immunfluoreszenz Vortrag Immunologie am 22.05.2009 von Christopher Tollrian Inhalt Grundlagen Immunhistochemische Färbung Immunfluoreszenz Proben-Vorbereitung Methoden
Cytokeratin Cocktail (AE1 & AE3)
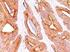 Produktidentifizierung Kat.-Nr. Beschreibung 44575 Cytokeratin Cocktail 0,1 M (AE1&AE3) 44576 Cytokeratin Cocktail 1 M (AE1&AE3) 44277 Cytokeratin Cocktail RTU M (AE1&AE3) Definition Der Symbole P C A
Produktidentifizierung Kat.-Nr. Beschreibung 44575 Cytokeratin Cocktail 0,1 M (AE1&AE3) 44576 Cytokeratin Cocktail 1 M (AE1&AE3) 44277 Cytokeratin Cocktail RTU M (AE1&AE3) Definition Der Symbole P C A
ZytoFast DNA (+) Control Probe
 ZytoFast DNA (+) Control Probe (Digoxigenin-markiert) T-1053-400 40 (0,4 ml) Zum Nachweis humaner repetitiver Alu-Sequenzen durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß
ZytoFast DNA (+) Control Probe (Digoxigenin-markiert) T-1053-400 40 (0,4 ml) Zum Nachweis humaner repetitiver Alu-Sequenzen durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44648 HHV-8 0,1 M (13B10) 44649 HHV-8 1 M (13B10) 44313 HHV-8 RTU M (13B10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44648 HHV-8 0,1 M (13B10) 44649 HHV-8 1 M (13B10) 44313 HHV-8 RTU M (13B10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
REAGENZIEN UND MATERIALIEN Positivkontrolle (1) Negativkontrolle (1) Verdünnungslösung (1) Packungsbeilage (1)
 Nur zur Verwendung in der In-vitro-Diagnostik VERWENDUNGSZWECK InflammaDry externe Kontrollen sind nur für die Verwendung mit dem InflammaDry Test. Sie dienen der Überprüfung, ob die Testreagenzien funktionieren
Nur zur Verwendung in der In-vitro-Diagnostik VERWENDUNGSZWECK InflammaDry externe Kontrollen sind nur für die Verwendung mit dem InflammaDry Test. Sie dienen der Überprüfung, ob die Testreagenzien funktionieren
ype 6/11/16/18/31/33/35 Screening Probe (Biotin-markiert
 ZytoFast HPV typ ype 6/11/16/18/31/33/35 Screening Probe (Biotin-markiert markiert) T-1044-400 40 (0,4 ml) Zum Nachweis von Human Papilloma Virus (HPV) Typ 6/11/16/18/31/33/35 DNA durch chromogene in situ
ZytoFast HPV typ ype 6/11/16/18/31/33/35 Screening Probe (Biotin-markiert markiert) T-1044-400 40 (0,4 ml) Zum Nachweis von Human Papilloma Virus (HPV) Typ 6/11/16/18/31/33/35 DNA durch chromogene in situ
Hepatitis B Virus Surface Antigen (A10F1) Mouse Monoclonal Antibody
 CMC21722000 DE Rev. 0,0v1 p. 1 Hepatitis B Virus Surface Antigen (A10F1) Mouse Monoclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung
CMC21722000 DE Rev. 0,0v1 p. 1 Hepatitis B Virus Surface Antigen (A10F1) Mouse Monoclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung
Estrogen Receptor (EP1)
 Produktidentifizierung Kat.-Nr. Beschreibung 44592 Estrogen Receptor 0,1 R (EP1) 44593 Estrogen Receptor 1 R (EP1) 44285 Estrogen Receptor RTU R (EP1) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Produktidentifizierung Kat.-Nr. Beschreibung 44592 Estrogen Receptor 0,1 R (EP1) 44593 Estrogen Receptor 1 R (EP1) 44285 Estrogen Receptor RTU R (EP1) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
ZytoFast EBV Probe (Biotin-markiert)
 ZytoFast EBV Probe (Biotin-markiert) T-1014-400 40 (0,4 ml) Zum Nachweis von Epstein-Barr-Virus (EBV) EBER RNA durch chromogene in situ Hybridisierung (CISH) Nur für Forschungszwecke bestimmt Biotin-markierte
ZytoFast EBV Probe (Biotin-markiert) T-1014-400 40 (0,4 ml) Zum Nachweis von Epstein-Barr-Virus (EBV) EBER RNA durch chromogene in situ Hybridisierung (CISH) Nur für Forschungszwecke bestimmt Biotin-markierte
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44238 CD4 RTU R (EP204) 44498 CD4 0,1 R (EP204) 44499 CD4 1 R (EP204) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44238 CD4 RTU R (EP204) 44498 CD4 0,1 R (EP204) 44499 CD4 1 R (EP204) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
ZytoFast DNA (+) Control Probe
 ZytoFast DNA (+) Control Probe (Biotin-markiert) T-1022-100 10 (0,1 ml) Zum Nachweis humaner repetitiver Alu-Sequenzen durch chromogene in situ Hybridisierung (CISH) Nur für Forschungszwecke bestimmt Biotin-markierte
ZytoFast DNA (+) Control Probe (Biotin-markiert) T-1022-100 10 (0,1 ml) Zum Nachweis humaner repetitiver Alu-Sequenzen durch chromogene in situ Hybridisierung (CISH) Nur für Forschungszwecke bestimmt Biotin-markierte
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 46922 Cathepsin K 0,1 M (3F9) 46923 Cathepsin K 1 M (3F9) 46921 Cathepsin K RTU M (3F9) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Produktidentifizierung Kat.-Nr. Beschreibung 46922 Cathepsin K 0,1 M (3F9) 46923 Cathepsin K 1 M (3F9) 46921 Cathepsin K RTU M (3F9) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
ZytoFast EBV Probe (Digoxigenin-markiert)
 ZytoFast EBV Probe (Digoxigenin-markiert) T-1114-400 40 (0,4 ml) Zum Nachweis von Epstein-Barr-Virus (EBV) EBER RNA durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß EU-Richtlinie
ZytoFast EBV Probe (Digoxigenin-markiert) T-1114-400 40 (0,4 ml) Zum Nachweis von Epstein-Barr-Virus (EBV) EBER RNA durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß EU-Richtlinie
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44439 Beta-Catenin 0,1 M (14) 44440 Beta-Catenin 1 M (14) 44207 Beta-Catenin RTU M (14) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Produktidentifizierung Kat.-Nr. Beschreibung 44439 Beta-Catenin 0,1 M (14) 44440 Beta-Catenin 1 M (14) 44207 Beta-Catenin RTU M (14) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Langerin (12D6) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG DEFINITION DER SYMBOLE PRINZIPIEN UND VERFAHREN
 DE Rev. 0.0 Langerin (12D6) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 392M-14 0,1 ml, Konzentrat 392M-15 0,5 ml, Konzentrat 392M-16 1,0 ml, Konzentrat
DE Rev. 0.0 Langerin (12D6) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 392M-14 0,1 ml, Konzentrat 392M-15 0,5 ml, Konzentrat 392M-16 1,0 ml, Konzentrat
Phosphohistone H3 (PHH3)
 Rev. 1.0 Phosphohistone H3 (PHH3) Rabbit Polyclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 369A-14 0,1 ml, Konzentrat 369A-15 0,5 ml, Konzentrat 369A-16 1,0 ml, Konzentrat 369A-17 1,0 ml,
Rev. 1.0 Phosphohistone H3 (PHH3) Rabbit Polyclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 369A-14 0,1 ml, Konzentrat 369A-15 0,5 ml, Konzentrat 369A-16 1,0 ml, Konzentrat 369A-17 1,0 ml,
Adenovirus (20/11 & 2/6)
 DE Rev. 3.0 Adenovirus (20/11 & 2/6) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 212M-14 0,1 ml, Konzentrat 212M-15 0,5 ml, Konzentrat 212M-16 1,0
DE Rev. 3.0 Adenovirus (20/11 & 2/6) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 212M-14 0,1 ml, Konzentrat 212M-15 0,5 ml, Konzentrat 212M-16 1,0
Helicobacter pylori Rabbit Polyclonal Antibody
 CMC21517040 DE Rev. 4,0 p. 1 Helicobacter pylori Rabbit Polyclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
CMC21517040 DE Rev. 4,0 p. 1 Helicobacter pylori Rabbit Polyclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
Cathepsin K (3F9) Mouse Monoclonal Antibody ZUSAMMENFASSUNG UND ERKLÄRUNG PRODUKTVERFÜGBARKEIT DEFINITION DER SYMBOLE VERWENDUNGSZWECK
 DE Rev. 0.0 Cathepsin K (3F9) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 402M-14 0,1 ml, Konzentrat 402M-15 0,5 ml, Konzentrat 402M-16 1,0 ml, Konzentrat
DE Rev. 0.0 Cathepsin K (3F9) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 402M-14 0,1 ml, Konzentrat 402M-15 0,5 ml, Konzentrat 402M-16 1,0 ml, Konzentrat
vor. Dieser Antikörper wird eingesetzt um verschiedene kutane (T-Zell) Lymphome von B-Zell-Lymphomen und Pseudolymphomen abzugrenzen.
 Produktidentifizierung Kat.-Nr. Beschreibung 44472 CD1a 0,1 R (EP3622) 44473 CD1a 1 R (EP3622) 44225 CD1a RTU R (EP3622) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44472 CD1a 0,1 R (EP3622) 44473 CD1a 1 R (EP3622) 44225 CD1a RTU R (EP3622) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44744 p57 0,1 M (Kp10) 44745 p57 1 M (Kp10) 44362 p57 RTU M (Kp10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum überstand
Produktidentifizierung Kat.-Nr. Beschreibung 44744 p57 0,1 M (Kp10) 44745 p57 1 M (Kp10) 44362 p57 RTU M (Kp10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum überstand
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44767 PNL2 0,1 M (PNL2) 44768 PNL2 1 M (PNL2) 44374 PNL2 RTU M (PNL2) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44767 PNL2 0,1 M (PNL2) 44768 PNL2 1 M (PNL2) 44374 PNL2 RTU M (PNL2) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45183 IMPATH CD43 RTU M (MT1) Definition Der Symbole Großteils der Paraffinschnitte von Lymphomen vorgenommen werden. Das Mitfärben eines lymphoiden Infiltrates
Produktidentifizierung Kat.-Nr. Beschreibung 45183 IMPATH CD43 RTU M (MT1) Definition Der Symbole Großteils der Paraffinschnitte von Lymphomen vorgenommen werden. Das Mitfärben eines lymphoiden Infiltrates
Herpes Simplex Virus I (Polyclonal)
 Produktidentifizierung Kat.-Nr. Beschreibung 45214 IMPATH Herpes Simplex Virus I RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Produktidentifizierung Kat.-Nr. Beschreibung 45214 IMPATH Herpes Simplex Virus I RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Glial Fibrillary Acidic Protein (GFAP) (SP78)
 DE Rev. 0.1 Glial Fibrillary Acidic Protein (GFAP) (SP78) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 258R-24 0,1 ml, Konzentrat 258R-25 0,5 ml, Konzentrat 258R-26 1,0 ml, Konzentrat
DE Rev. 0.1 Glial Fibrillary Acidic Protein (GFAP) (SP78) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 258R-24 0,1 ml, Konzentrat 258R-25 0,5 ml, Konzentrat 258R-26 1,0 ml, Konzentrat
SOX-2 (SP76) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG DEFINITION DER SYMBOLE VERWENDUNGSZWECK
 Rev. 0.0 SOX-2 (SP76) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 371R-14 0,1 ml, Konzentrat 371R-15 0,5 ml, Konzentrat 371R-16 1,0 ml, Konzentrat 371R-17 1,0 ml, Vorverdünnung
Rev. 0.0 SOX-2 (SP76) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 371R-14 0,1 ml, Konzentrat 371R-15 0,5 ml, Konzentrat 371R-16 1,0 ml, Konzentrat 371R-17 1,0 ml, Vorverdünnung
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44668 Kappa Light Chain 0,1 M (L1C1) 44669 Kappa Light Chain 1 M (L1C1) 44323 Kappa Light Chain RTU M (L1C1) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Produktidentifizierung Kat.-Nr. Beschreibung 44668 Kappa Light Chain 0,1 M (L1C1) 44669 Kappa Light Chain 1 M (L1C1) 44323 Kappa Light Chain RTU M (L1C1) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44488 CD31 0,1 M (JC70) 44489 CD31 1 M (JC70) 44233 CD31 RTU M (JC70) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44488 CD31 0,1 M (JC70) 44489 CD31 1 M (JC70) 44233 CD31 RTU M (JC70) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44458 CD10 0,1 M (56C6) 44459 CD10 1 M (56C6) 44217 CD10 RTU M (56C6) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44458 CD10 0,1 M (56C6) 44459 CD10 1 M (56C6) 44217 CD10 RTU M (56C6) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Calcitonin (Polyclonal)
 Produktidentifizierung Kat.-Nr. Beschreibung 45170 IMPATH Calcitonin RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45170 IMPATH Calcitonin RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45168 IMPATH CA-125 RTU M (OC125) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45168 IMPATH CA-125 RTU M (OC125) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Varicella Zoster Virus (SG1-1, SG1- SG4, NCP-1 & IE-62)
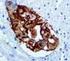 Varicella Zoster Virus (SG1-1, SG1- SG4, Produktidentifizierung Kat.-Nr. Beschreibung 44833 Varicella-zoster virus 0,1 M (Monoclonal CKT) 44834 Varicella-zoster virus 1 M (MONOCLONAL CKT) 44407 Varicella-zoster
Varicella Zoster Virus (SG1-1, SG1- SG4, Produktidentifizierung Kat.-Nr. Beschreibung 44833 Varicella-zoster virus 0,1 M (Monoclonal CKT) 44834 Varicella-zoster virus 1 M (MONOCLONAL CKT) 44407 Varicella-zoster
Treponema pallidum. Rabbit Polyclonal Antibody ZUSAMMENFASSUNG UND ERKLÄRUNG PRODUKTVERFÜGBARKEIT DEFINITION DER SYMBOLE VERWENDUNGSZWECK
 DE Rev. 0.0 Treponema pallidum Rabbit Polyclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 397A-14 0,1 ml, Konzentrat 397A-15 0,5 ml, Konzentrat 397A-16 1,0 ml,
DE Rev. 0.0 Treponema pallidum Rabbit Polyclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 397A-14 0,1 ml, Konzentrat 397A-15 0,5 ml, Konzentrat 397A-16 1,0 ml,
OptiView DAB IHC Detection Kit
 OptiView DAB IHC Detection Kit 760-700 06396500001 250 DAB Precipitate + Copper H2O2 DAB VERWENDUNGSZWECK Das OptiView DAB IHC Detection Kit (OptiView) ist ein indirektes Biotin-freies System zum Nachweis
OptiView DAB IHC Detection Kit 760-700 06396500001 250 DAB Precipitate + Copper H2O2 DAB VERWENDUNGSZWECK Das OptiView DAB IHC Detection Kit (OptiView) ist ein indirektes Biotin-freies System zum Nachweis
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44263 Cyclin D1 RTU R (EP12) 44547 Cyclin D1 0,1 R (EP12) 44548 Cyclin D1 1 R (EP12) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Produktidentifizierung Kat.-Nr. Beschreibung 44263 Cyclin D1 RTU R (EP12) 44547 Cyclin D1 0,1 R (EP12) 44548 Cyclin D1 1 R (EP12) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
IgG Rabbit Polyclonal Antibody
 CMC26911030 DE Rev. 3,0 p. 1 IgG Rabbit Polyclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik bestimmt.
CMC26911030 DE Rev. 3,0 p. 1 IgG Rabbit Polyclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik bestimmt.
Myosin, Smooth Muscle (SMMS-1)
 Produktidentifizierung Kat.-Nr. Beschreibung 45240 IMPATH Myosin Smooth Muscle RTU M (SMMS-1) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Produktidentifizierung Kat.-Nr. Beschreibung 45240 IMPATH Myosin Smooth Muscle RTU M (SMMS-1) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Hepatocyte Specific Antigen (Hep Par-1) (OCH1E5)
 Hepatocyte Specific Antigen (Hep Par-1) Produktidentifizierung Kat.-Nr. Beschreibung 44634 Hepatocyte Specific Antigen 0,1 M 44635 Hepatocyte Specific Antigen 1 M 44306 Hepatocyte Specific Antigen RTU
Hepatocyte Specific Antigen (Hep Par-1) Produktidentifizierung Kat.-Nr. Beschreibung 44634 Hepatocyte Specific Antigen 0,1 M 44635 Hepatocyte Specific Antigen 1 M 44306 Hepatocyte Specific Antigen RTU
Helicobacter pylori (Polyclonal)
 Produktidentifizierung Kat.-Nr. Beschreibung 45146 IMPATH Helicobacter pylori RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Produktidentifizierung Kat.-Nr. Beschreibung 45146 IMPATH Helicobacter pylori RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44841 Zap-70 0,1 M (2F3.2) 44842 Zap-70 1 M (2F3.2) 44411 Zap-70 RTU M (2F3.2) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44841 Zap-70 0,1 M (2F3.2) 44842 Zap-70 1 M (2F3.2) 44411 Zap-70 RTU M (2F3.2) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
GATA3 (L50-823) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG DEFINITION DER SYMBOLE VERWENDUNGSZWECK
 DE Rev. 0.0 GATA3 (L50-823) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 390M-14 0,1 ml, Konzentrat 390M-15 0,5 ml, Konzentrat 390M-16 1,0 ml, Konzentrat
DE Rev. 0.0 GATA3 (L50-823) Mouse Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 390M-14 0,1 ml, Konzentrat 390M-15 0,5 ml, Konzentrat 390M-16 1,0 ml, Konzentrat
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 47353 IMPATH GLUT3 RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 47353 IMPATH GLUT3 RTU R (Poly) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Synaptophysin (MRQ-40)
 Produktidentifizierung Kat.-Nr. Beschreibung 44803 Synaptophysin 0,1 R (MRQ-40) 44804 Synaptophysin 1 R (MRQ-40) 44392 Synaptophysin RTU R (MRQ-40) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Produktidentifizierung Kat.-Nr. Beschreibung 44803 Synaptophysin 0,1 R (MRQ-40) 44804 Synaptophysin 1 R (MRQ-40) 44392 Synaptophysin RTU R (MRQ-40) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
CD56 (MRQ-42) Rabbit Monoclonal Antibody ZUSAMMENFASSUNG UND ERKLÄRUNG PRODUKTVERFÜGBARKEIT DEFINITION DER SYMBOLE PRINZIPIEN UND VERFAHREN
 Rev. 1.1 CD56 (MRQ-42) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 156R-94 0,1 ml, Konzentrat 156R-95 0,5 ml, Konzentrat 156R-96 1,0 ml, Konzentrat 156R-97 1,0 ml, Vorverdünnung
Rev. 1.1 CD56 (MRQ-42) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 156R-94 0,1 ml, Konzentrat 156R-95 0,5 ml, Konzentrat 156R-96 1,0 ml, Konzentrat 156R-97 1,0 ml, Vorverdünnung
CD43 (SP55) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG DEFINITION DER SYMBOLE PRINZIPIEN UND VERFAHREN
 Rev. 0.1 v1 CD43 (SP55) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 143R-14 0,1 ml, Konzentrat 143R-15 0,5 ml, Konzentrat 143R-16 1,0 ml, Konzentrat 143R-17 1,0 ml, Vorverdünnung
Rev. 0.1 v1 CD43 (SP55) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT Kat.- Nr. Beschreibung 143R-14 0,1 ml, Konzentrat 143R-15 0,5 ml, Konzentrat 143R-16 1,0 ml, Konzentrat 143R-17 1,0 ml, Vorverdünnung
PAX-2 (EP235) Rabbit Monoclonal Primary Antibody
 CMC31131000 DE Rev. 0,0 p. 1 PAX-2 (EP235) Rabbit Monoclonal Primary Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
CMC31131000 DE Rev. 0,0 p. 1 PAX-2 (EP235) Rabbit Monoclonal Primary Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44734 p120 Catenin 0,1 M (MRQ-5) 44735 p120 Catenin 1 M (MRQ-5) 44357 p120 Catenin RTU M (MRQ-5) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Produktidentifizierung Kat.-Nr. Beschreibung 44734 p120 Catenin 0,1 M (MRQ-5) 44735 p120 Catenin 1 M (MRQ-5) 44357 p120 Catenin RTU M (MRQ-5) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Anti-Caldesmon wird auch zur Unterscheidung zwischen epitheloiden Mesotheliomen und serös-papillären Karzinomen der Ovarien verwendet.
 Produktidentifizierung Kat.-Nr. Beschreibung 44452 Caldesmon 0,1 R (E89) 44453 Caldesmon 1 R (E89) 44214 Caldesmon RTU R (E89) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44452 Caldesmon 0,1 R (E89) 44453 Caldesmon 1 R (E89) 44214 Caldesmon RTU R (E89) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Ep-CAM/Epithelial Specific Antigen (Ber-EP4) Mouse Monoclonal Antibody
 CMC24829031 DE Rev. 3,1 p. 1 Ep-CAM/Epithelial Specific Antigen (Ber-EP4) Mouse Monoclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung
CMC24829031 DE Rev. 3,1 p. 1 Ep-CAM/Epithelial Specific Antigen (Ber-EP4) Mouse Monoclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung
Stathmin (SP49) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG DEFINITION DER SYMBOLE VERWENDUNGSZWECK
 DE Rev. 0.0 Stathmin (SP49) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 394R-14 0,1 ml, Konzentrat 394R-15 0,5 ml, Konzentrat 394R-16 1,0 ml, Konzentrat
DE Rev. 0.0 Stathmin (SP49) Rabbit Monoclonal Antibody PRODUKTVERFÜGBARKEIT ZUSAMMENFASSUNG UND ERKLÄRUNG Kat.-Nr. Beschreibung 394R-14 0,1 ml, Konzentrat 394R-15 0,5 ml, Konzentrat 394R-16 1,0 ml, Konzentrat
Adipophilin (Polyclonal)
 Produktidentifizierung Kat.-Nr. Beschreibung 46916 Adipophilin 0,1 R ( Poly) 46917 Adipophilin 1 R ( Poly) 46915 Adipophilin RTU R ( Poly) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Produktidentifizierung Kat.-Nr. Beschreibung 46916 Adipophilin 0,1 R ( Poly) 46917 Adipophilin 1 R ( Poly) 46915 Adipophilin RTU R ( Poly) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44427 Annexin A1 0,1 M (MRQ-3) 44428 Annexin A1 1 M (MRQ-3) 44200 Annexin A1 RTU M (MRQ-3) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Produktidentifizierung Kat.-Nr. Beschreibung 44427 Annexin A1 0,1 M (MRQ-3) 44428 Annexin A1 1 M (MRQ-3) 44200 Annexin A1 RTU M (MRQ-3) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
QUANTA Chek Celiac Panel
 QUANTA Chek Celiac Panel 708113 Verwendungszweck Die QUANTA Chek TM Celiac Probereihe wird für die Qualitätskontrolle bei IFA und ELISA Autoantikörper verfahren verwendet. Jedes Serum dient sowohl als
QUANTA Chek Celiac Panel 708113 Verwendungszweck Die QUANTA Chek TM Celiac Probereihe wird für die Qualitätskontrolle bei IFA und ELISA Autoantikörper verfahren verwendet. Jedes Serum dient sowohl als
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44837 Vimentin 0,1 M (V9) 44838 Vimentin 1 M (V9) 44409 Vimentin RTU M (V9) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44837 Vimentin 0,1 M (V9) 44838 Vimentin 1 M (V9) 44409 Vimentin RTU M (V9) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44523 CD71 0,1 M (MRQ-48) 44524 CD71 1 M (MRQ-48) 44251 CD71 RTU M (MRQ-48) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44523 CD71 0,1 M (MRQ-48) 44524 CD71 1 M (MRQ-48) 44251 CD71 RTU M (MRQ-48) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44757 Perforin 0,1 M (MRQ-23) 44758 Perforin 1 M (MRQ-23) 44369 Perforin RTU M (MRQ-23) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Produktidentifizierung Kat.-Nr. Beschreibung 44757 Perforin 0,1 M (MRQ-23) 44758 Perforin 1 M (MRQ-23) 44369 Perforin RTU M (MRQ-23) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Human Placental Lactogen (hpl) (Polyclonal)
 Produktidentifizierung Kat.-Nr. Beschreibung 45312 IMPATH Hpl RTU R (Poly) Definition Der Symbole eines trophoblastischen Hodentumors berichtet, der Ähnlichkeiten mit einem trophoblastischen Plazentatumor
Produktidentifizierung Kat.-Nr. Beschreibung 45312 IMPATH Hpl RTU R (Poly) Definition Der Symbole eines trophoblastischen Hodentumors berichtet, der Ähnlichkeiten mit einem trophoblastischen Plazentatumor
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45652 IMPATH GATA3 RTU M (L50-823) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45652 IMPATH GATA3 RTU M (L50-823) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Chromogranin A (LK2H10)
 Produktidentifizierung Kat.-Nr. Beschreibung 44539 Chromogranin A 0,1 M (LK2H10) 44540 Chromogranin A 1 M (LK2H10) 44259 Chromogranin A RTU M (LK2H10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Produktidentifizierung Kat.-Nr. Beschreibung 44539 Chromogranin A 0,1 M (LK2H10) 44540 Chromogranin A 1 M (LK2H10) 44259 Chromogranin A RTU M (LK2H10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig
Hepatocyte Specific Antigen (Hep Par-1) (OCH1E5)
 Hepatocyte Specific Antigen (Hep Par-1) Produktidentifizierung Kat.-Nr. Beschreibung 45147 IMPATH Hepatocyte Specific Antigen RTU M Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum
Hepatocyte Specific Antigen (Hep Par-1) Produktidentifizierung Kat.-Nr. Beschreibung 45147 IMPATH Hepatocyte Specific Antigen RTU M Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum
Epstein-Barr Virus (MRQ-47)
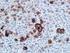 Produktidentifizierung Kat.-Nr. Beschreibung 44590 Epstein-Barr Virus 0,1 R (MRQ-47) 44591 Epstein-Barr Virus 1 R (MRQ-47) 44284 Epstein-Barr Virus RTU R (MRQ- 47) Definition Der Symbole P C A E S DIL
Produktidentifizierung Kat.-Nr. Beschreibung 44590 Epstein-Barr Virus 0,1 R (MRQ-47) 44591 Epstein-Barr Virus 1 R (MRQ-47) 44284 Epstein-Barr Virus RTU R (MRQ- 47) Definition Der Symbole P C A E S DIL
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44797 SOX-2 0,1 R (SP76) 44798 SOX-2 1 R (SP76) 44389 SOX-2 RTU R (SP76) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44797 SOX-2 0,1 R (SP76) 44798 SOX-2 1 R (SP76) 44389 SOX-2 RTU R (SP76) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45620 MyoD1 0,1 R (EP212) 45621 MyoD1 1 R (EP212) 45638 MyoD1 RTU R (EP212) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 45620 MyoD1 0,1 R (EP212) 45621 MyoD1 1 R (EP212) 45638 MyoD1 RTU R (EP212) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44537 CEA 0,1 M (CEA31) 44538 CEA 1 M (CEA31) 44258 CEA RTU M (CEA31) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44537 CEA 0,1 M (CEA31) 44538 CEA 1 M (CEA31) 44258 CEA RTU M (CEA31) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44779 PGP9.5 0,1 R (Poly) 44780 PGP9.5 1 R (Poly) 44380 PGP9.5 RTU R (Poly) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44779 PGP9.5 0,1 R (Poly) 44780 PGP9.5 1 R (Poly) 44380 PGP9.5 RTU R (Poly) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45629 SALL4 0,1 M (6E3) 45630 SALL4 1 M (6E3) 45643 SALL4 RTU M (6E3) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 45629 SALL4 0,1 M (6E3) 45630 SALL4 1 M (6E3) 45643 SALL4 RTU M (6E3) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44750 PAX-2 0,1 R (Poly) 44751 PAX-2 1 R (Poly) 44365 PAX-2 RTU R (Poly) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44750 PAX-2 0,1 R (Poly) 44751 PAX-2 1 R (Poly) 44365 PAX-2 RTU R (Poly) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
CD123 (6H6) Mouse Monoclonal Antibody. Produktidentifizierung. Definition Der Symbole. Verwendungszweck. Zusammenfassung Und Erklärung
 Produktidentifizierung Kat.-Nr. Beschreibung 47348 IMPATH CD123 RTU M (6H6) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 47348 IMPATH CD123 RTU M (6H6) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Helicobacter pylori (Polyclonal)
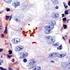 Produktidentifizierung Kat.-Nr. Beschreibung 44626 Helicobacter pylori 0,1 R (Poly) 44627 Helicobacter pylori 1 R (Poly) 44302 Helicobacter pylori RTU R (Poly) Definition Der Symbole P C A E S DIL DOC#
Produktidentifizierung Kat.-Nr. Beschreibung 44626 Helicobacter pylori 0,1 R (Poly) 44627 Helicobacter pylori 1 R (Poly) 44302 Helicobacter pylori RTU R (Poly) Definition Der Symbole P C A E S DIL DOC#
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45125 IMPATH CD10 RTU M (56C6) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45125 IMPATH CD10 RTU M (56C6) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44732 OCT-4 0,1 M (MRQ-10) 44733 OCT-4 1 M (MRQ-10) 44356 OCT-4 RTU M (MRQ-10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44732 OCT-4 0,1 M (MRQ-10) 44733 OCT-4 1 M (MRQ-10) 44356 OCT-4 RTU M (MRQ-10) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45265 IMPATH TTF-1 RTU M (8G7G3/1) Definition Der Symbole pulmonalen und nicht-pulmonalen Ursprungs bei malignen Ergüssen nützlich. 8 TTF-1- Färbung ist bei
Produktidentifizierung Kat.-Nr. Beschreibung 45265 IMPATH TTF-1 RTU M (8G7G3/1) Definition Der Symbole pulmonalen und nicht-pulmonalen Ursprungs bei malignen Ergüssen nützlich. 8 TTF-1- Färbung ist bei
p21waf1 (DCS-60.2) Mouse Monoclonal Antibody
 CMC42121030 DE Rev. 3,0 p. 1 p21waf1 (DCS-60.2) Mouse Monoclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
CMC42121030 DE Rev. 3,0 p. 1 p21waf1 (DCS-60.2) Mouse Monoclonal Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
ZytoDot CEN X Probe. Zum Nachweis der humanen alpha-satelliten von Chromosom X durch chromogene in situ Hybridisierung (CISH) In-Vitro-Diagnostikum
 ZytoDot CEN X Probe C-3025-400 40 (0,4 ml) Zum Nachweis der humanen alpha-satelliten von Chromosom X durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß EU-Richtlinie 98/79/EG
ZytoDot CEN X Probe C-3025-400 40 (0,4 ml) Zum Nachweis der humanen alpha-satelliten von Chromosom X durch chromogene in situ Hybridisierung (CISH).... In-Vitro-Diagnostikum gemäß EU-Richtlinie 98/79/EG
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45645 IMPATH Cadherin-17 RTU R (SP183) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45645 IMPATH Cadherin-17 RTU R (SP183) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
ZytoFast HPV High-Risk (HR) Types Probe (Digoxigenin
 ZytoFast HPV High-Risk (HR) Types Probe (Digoxigenin Digoxigenin-markiert markiert) T-1140-400 40 (0,4 ml) Zum Nachweis von Human Papilloma Virus (HPV) Typ 16/18/31/33/35/39/45/51/52/56/58/59/66/68/82
ZytoFast HPV High-Risk (HR) Types Probe (Digoxigenin Digoxigenin-markiert markiert) T-1140-400 40 (0,4 ml) Zum Nachweis von Human Papilloma Virus (HPV) Typ 16/18/31/33/35/39/45/51/52/56/58/59/66/68/82
QUANTA Chek ANA Panel
 QUANTA Chek ANA Panel 708111 Verwendungszweck Die QUANTA Chek TM ANA Probereihe wird für die Qualitätskontrolle bei IFA und ELISA antinukleären Antikörperverfahren verwendet. Jedes Serum dient sowohl als
QUANTA Chek ANA Panel 708111 Verwendungszweck Die QUANTA Chek TM ANA Probereihe wird für die Qualitätskontrolle bei IFA und ELISA antinukleären Antikörperverfahren verwendet. Jedes Serum dient sowohl als
Tryptase (EP259) Rabbit Monoclonal Primary Antibody
 CMC34231000 DE Rev. 0,0 p. 1 Tryptase (EP259) Rabbit Monoclonal Primary Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
CMC34231000 DE Rev. 0,0 p. 1 Tryptase (EP259) Rabbit Monoclonal Primary Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44470 CD19 0,1 M (MRQ-36) 44471 CD19 1 M (MRQ-36) 44224 CD19 RTU M (MRQ-36) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44470 CD19 0,1 M (MRQ-36) 44471 CD19 1 M (MRQ-36) 44224 CD19 RTU M (MRQ-36) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 46931 EGFR 0,1 R (SP84) 46932 EGFR 1 R (SP84) 46930 EGFR RTU R (SP84) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 46931 EGFR 0,1 R (SP84) 46932 EGFR 1 R (SP84) 46930 EGFR RTU R (SP84) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45127 IMPATH CD163 RTU M (MRQ-26) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45127 IMPATH CD163 RTU M (MRQ-26) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
IgG4 (EP138) Rabbit Monoclonal Primary Antibody
 CMC36731010 DE Rev. 1,0 p. 1 IgG4 (EP138) Rabbit Monoclonal Primary Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
CMC36731010 DE Rev. 1,0 p. 1 IgG4 (EP138) Rabbit Monoclonal Primary Antibody Zur Verwendung In Der In Vitro Diagnostik (IVD) Verwendungszweck Dieser Antikörper ist für die Verwendung in der In Vitro-Diagnostik
CD33 (PWS44) Mouse Monoclonal Antibody. Produktidentifizierung. Definition Der Symbole. Verwendungszweck. Zusammenfassung Und Erklärung
 Produktidentifizierung Kat.-Nr. Beschreibung 44490 CD33 0,1 M (PWS44) 44491 CD33 1 M (PWS44) 44234 CD33 RTU M (PWS44) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
Produktidentifizierung Kat.-Nr. Beschreibung 44490 CD33 0,1 M (PWS44) 44491 CD33 1 M (PWS44) 44234 CD33 RTU M (PWS44) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites serum
EG-Sicherheitsdatenblatt (91/155 EWG)
 Druckdatum: 14.08.2012 Seite 1/5 1. Stoff-/Zubereitungs- und Firmenbezeichnung Angaben zum Produkt Handelsname: Artikelnr: Packungsinhalt: HemosIL AcuStar 98020-12 Verwendungszweck: Automatisierter Chemilumeneszenzimmunoassay
Druckdatum: 14.08.2012 Seite 1/5 1. Stoff-/Zubereitungs- und Firmenbezeichnung Angaben zum Produkt Handelsname: Artikelnr: Packungsinhalt: HemosIL AcuStar 98020-12 Verwendungszweck: Automatisierter Chemilumeneszenzimmunoassay
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44517 CD63 0,1 M (NKI/C3) 44518 CD63 1 M (NKI/C3) 44248 CD63 RTU M (NKI/C3) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 44517 CD63 0,1 M (NKI/C3) 44518 CD63 1 M (NKI/C3) 44248 CD63 RTU M (NKI/C3) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Glutamine Synthetase (GS-6)
 Produktidentifizierung Kat.-Nr. Beschreibung 47354 IMPATH Glutamine Synthetase RTU M (GS-6) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Produktidentifizierung Kat.-Nr. Beschreibung 47354 IMPATH Glutamine Synthetase RTU M (GS-6) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45647 IMPATH CD16 RTU R (SP175) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45647 IMPATH CD16 RTU R (SP175) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45230 IMPATH MUC1 RTU M (MRQ-17) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Produktidentifizierung Kat.-Nr. Beschreibung 45230 IMPATH MUC1 RTU M (MRQ-17) Definition Der Symbole P A E S DOC# DIS gebrauchsfertig aszites serum überstand dokumentnummer vertrieben durch Verwendungszweck
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 45622 GATA3 0,1 M (L50-823) 45623 GATA3 1 M (L50-823) 45639 GATA3 RTU M (L50-823) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Produktidentifizierung Kat.-Nr. Beschreibung 45622 GATA3 0,1 M (L50-823) 45623 GATA3 1 M (L50-823) 45639 GATA3 RTU M (L50-823) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat aszites
Prinzipien Und Verfahren
 Produktidentifizierung Kat.-Nr. Beschreibung 44618 Glypican-3 0,1 M (1G12) 44619 Glypican-3 1 M (1G12) 44298 Glypican-3 RTU M (1G12) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
Produktidentifizierung Kat.-Nr. Beschreibung 44618 Glypican-3 0,1 M (1G12) 44619 Glypican-3 1 M (1G12) 44298 Glypican-3 RTU M (1G12) Definition Der Symbole P C A E S DIL DOC# DIS gebrauchsfertig konzentrat
