Alofisel (Darvadstrocel)
|
|
|
- Leander Thomas
- vor 6 Jahren
- Abrufe
Transkript
1 Alofisel (Darvadstrocel) Anleitung zur Entgegennahme und Lagerung [LEITFADEN für PHARMAZEUTEN] Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen siehe letzte Seite. Version 1, 24 April
2 Dieser Leitfaden zur Anwendung von ALOFISEL wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden über die Routinemaßnahmen hinaus, zusätzliche risikominimierende Maßnahmen mit der Zulassung des Arzneimittels beauflagt, um das Risiko des Auftretens von mikrobiellen Verunreinigungen und Nebenwirkungen zu reduzieren und das Nutzen-Risiko- Verhältnis von ALOFISEL zu erhöhen. Dieser Leitfaden ist damit verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, die ALOFISEL verschreiben und zur Anwendung bringen, die besonderen Sicherheitsanforderungen kennen und berücksichtigen. 2
3 ALOFISEL (DARVADSTROCEL) Alofisel (Darvadstrocel) ist eine Suspension expandierter humaner aus Fettgewebe gewonnener Stammzellen. Alofisel ist zur Behandlung von komplexen perianalen Fisteln bei erwachsenen Patienten mit nicht aktivem/gering aktivem luminalem Morbus Crohn indiziert, wenn die Fisteln unzureichend auf mindestens eine konventionelle oder biologische Therapie angesprochen haben. Alofisel (Darvadstrocel) wird in einem Operationsumfeld in den Bereich der Fisteln unter Allgemein- oder Regionalanästhesie lokal injiziert. Das Arzneimittel besteht aus 4 Durchstechflaschen aus Glas mit jeweils 30 Millionen Zellen (6 ml pro Durchstechflasche). Eine Einzeldosis Alofisel (Darvadstrocel) enthält daher 120 Millionen Zellen. 1 Dosis = 4 Durchstechflaschen = 120 Millionen Zellen Die 4 Glas-Durchstechflaschen sind Teil einer Packung, die für den Transport in ein Versandbehältnis gepackt wird. In dem Versandbehältnis ist ein Temperaturüberwachungsgerät integriert. ARZNEIMITTEL ENTGEGENNAHME & LAGERUNG Bewahren Sie das Arzneimittel bis zur Anwendung die gesamte Zeit in einer temperaturkontrollierten Umgebung von 15 C bis 25 C auf. Überprüfen Sie nach Ankunft des Kuriers das Versandbehältnis optisch auf etwaige übermäßige Anzeichen von Beschädigungen oder Rissen. Vermerken Sie jede Beobachtung in den begleitenden Lieferdokumenten. Setzen Sie das Versandbehältnis weder Hitze noch direkten Lichtquellen aus und lagern Sie es nicht im Kühl- oder Gefrierschrank. 3
4 Öffnen Sie den Deckel des Versandbehältnisses und nehmen Sie das Temperaturüberwachungsgerät heraus, um zu prüfen, ob das Arzneimittel während des Transports bei der geforderten Temperatur aufbewahrt wurde. Schließen Sie danach sofort den Deckel des Behältnisses, um Änderungen im Temperaturbereich zu vermeiden. Das Temperaturüberwachungsgerät wird wie folgt überprüft: 1. Stoppen Sie das Temperaturüberwachungsgerät, indem Sie die STOP- Taste für mindestens 3 Sekunden drücken. 2. Wenn es keinen Temperaturalarm und keine Abweichung aus dem Bereich (15 ºC 25 ºC) gibt, wird ein angezeigt. Das Arzneimittel wurde während des Transports im angemessenen Bereich aufbewahrt und Sie können weitergehen zu Punkt 6, d.h. das angehaltene Messgerät an den Kurier zurückgeben und das Arzneimittel verwenden. 4
5 ANLEITUNG ZUR ENTGEGENNAHME UND LAGERUNG 3. Wenn es einen Temperaturalarm gibt oder eine Abweichung aus dem Bereich (15 C - 25 C), werden ein «X» und ein Pfeil angezeigt. 4. Im Falle eines Alarms laden Sie den Bericht vom Messgerät herunter, indem Sie es mit einem PC / MAC verbinden. Es ist keine zusätzliche Software erforderlich. Klicken Sie auf die Q-tag CLm doc Datei, um diese zu öffnen. 5. Gehen Sie mit einem Doppelklick auf die PDF-Datei, um den Bericht zu öffnen. In einem Diagramm sehen Sie jegliche Temperaturabweichung außerhalb des Bereichs von 15 C 25 C. Senden Sie beides, die PDFund die TXT-Datei an [email protected] und [email protected] und kontaktieren Sie umgehend Takeda, um weitere Anweisungen zu erhalten. (Tel. Kontakt: ). 6. Geben Sie das Temperaturüberwachungsgerät an den Kurier zurück. 5
6 Öffnen Sie kurz das Versandbehältnis, um das Arzneimittel optisch auf Beschädigungen hin zu prüfen. Vergleichen Sie die Chargennummer, Verfalldatum und -uhrzeit und die Arzneimitteleigenschaften mit den Angaben in den begleitenden Lieferdokumenten und dem Konformitätszertifikat. Schließen Sie danach sofort das Behältnis, um Änderungen im Temperaturbereich zu vermeiden. Sollten sich bei irgendeinem dieser Schritte Abweichungen ergeben, kontaktieren Sie umgehend Takeda und warten Sie auf weitere Anweisungen. (Tel. Kontakt: ). Unterschreiben Sie alle Lieferpapiere ordnungsgemäß und vermerken Sie jede Beobachtung. Geben Sie die unterschriebenen Dokumente gemeinsam mit dem Temperaturüberwachungsgerät an den Kurier zurück. Bevor Sie das Versandbehältnis in den Operationssaal liefern, gleichen Sie Verfalldatum und -uhrzeit mit den Daten auf der Arzneimittelpackung und dem Lieferschein ab (Datum und Uhrzeit in mitteleuropäischer Zeit - CET). Sollten Verfalldatum und -uhrzeit bereits überschritten sein, verwenden Sie das Arzneimittel nicht. Alofisel (Darvadstrocel) ist gebrauchsfertig; es ist keine zusätzliche Zubereitung in den Gesundheitseinrichtungen erforderlich. Meldung von Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung dem Paul-Ehrlich-Institut, Paul-Ehrlich-Straße 51-59, Langen ( anzuzeigen. Dieses Informationsmaterial kann angefordert werden unter: Takeda GmbH Byk-Gulden-Straße Konstanz Telefon: Telefax: [email protected] und kann zusätzlich von folgender Homepage heruntergeladen werden: Die Fachinformation von Alofisel kann ebenfalls bei der Takeda GmbH (Deutschland) angefordert werden und/oder heruntergeladen werden von 6
7
SELBSTINJEKTIONS-TAGEBUCH Zur Unterstützung der Anwendung von Nplate zu Hause
 SELBSTINJEKTIONS-TAGEBUCH Zur Unterstützung der zu Hause Ihr Arzt soll Ihre aktuelle Dosis auf der Vorderseite dieses Selbstinjektions-ebuchs notieren. Ihr Arzt soll den Namen eines Ansprechpartners im
SELBSTINJEKTIONS-TAGEBUCH Zur Unterstützung der zu Hause Ihr Arzt soll Ihre aktuelle Dosis auf der Vorderseite dieses Selbstinjektions-ebuchs notieren. Ihr Arzt soll den Namen eines Ansprechpartners im
: Schulungsmaterial (Educational Material) für medizinisches Fachpersonal
 Kadcyla : Schulungsmaterial (Educational Material) für medizinisches Fachpersonal EU Information für medizinisches Fachpersonal Januar 2017 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Kadcyla : Schulungsmaterial (Educational Material) für medizinisches Fachpersonal EU Information für medizinisches Fachpersonal Januar 2017 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Schulungshandbuch für Angehörige der Heilberufe
 Accusol 35 Accusol 35 Kalium 2 mmol/l Accusol 35 Kalium 4 mmol/l Ersatzlösung für Hämodialyse, Hämodiafiltration und Hämofiltration Schulungshandbuch für Angehörige der Heilberufe Dieses Schulungshandbuch
Accusol 35 Accusol 35 Kalium 2 mmol/l Accusol 35 Kalium 4 mmol/l Ersatzlösung für Hämodialyse, Hämodiafiltration und Hämofiltration Schulungshandbuch für Angehörige der Heilberufe Dieses Schulungshandbuch
Hinweise zur Anwendung und Patiententagebuch
 Hinweise zur Anwendung und Dieses zur Anwendung von Rivastigmin-Pflastern wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden, über die Routinemaßnahmen hinaus,
Hinweise zur Anwendung und Dieses zur Anwendung von Rivastigmin-Pflastern wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden, über die Routinemaßnahmen hinaus,
WAS SIE ÜBER RIXATHON (RITUXIMAB) WISSEN SOLLTEN
 WAS SIE ÜBER RIXATHON (RITUXIMAB) WISSEN SOLLTEN WICHTIGE SICHERHEITSINFORMATIONEN FÜR PATIENTEN, DIE MIT RIXATHON BEHANDELT WERDEN Dieses Informationsmaterial zur Anwendung von Rixathon (Rituximab) wurde
WAS SIE ÜBER RIXATHON (RITUXIMAB) WISSEN SOLLTEN WICHTIGE SICHERHEITSINFORMATIONEN FÜR PATIENTEN, DIE MIT RIXATHON BEHANDELT WERDEN Dieses Informationsmaterial zur Anwendung von Rixathon (Rituximab) wurde
HINWEISE FÜR MEDIZINISCHES FACHPERSONAL ZUR ANWENDUNG VON TENOFOVIRDISOPROXIL BEI HIV-INFIZIERTEN JUGENDLICHEN
 HINWEISE FÜR MEDIZINISCHES FACHPERSONAL ZUR ANWENDUNG VON TENOFOVIRDISOPROXIL BEI HIV-INFIZIERTEN JUGENDLICHEN Dieses Informationsmaterial zur Anwendung von Tenofovirdisoproxil wurde als Teil der Zulassungsauflagen
HINWEISE FÜR MEDIZINISCHES FACHPERSONAL ZUR ANWENDUNG VON TENOFOVIRDISOPROXIL BEI HIV-INFIZIERTEN JUGENDLICHEN Dieses Informationsmaterial zur Anwendung von Tenofovirdisoproxil wurde als Teil der Zulassungsauflagen
Kadcyla Wichtige Informationen zur sicheren Anwendung
 Kadcyla Wichtige Informationen zur sicheren Anwendung Schulungsmaterial für Angehörige des medizinischen Fachkreises Oktober 2018 Version 6.0, Oktober 2018 ACHTUNG: Risiko der Verwechslung von KADCYLA
Kadcyla Wichtige Informationen zur sicheren Anwendung Schulungsmaterial für Angehörige des medizinischen Fachkreises Oktober 2018 Version 6.0, Oktober 2018 ACHTUNG: Risiko der Verwechslung von KADCYLA
AMYVID (FLORBETAPIR 18 F-INJEKTION) AUSWERTERSCHULUNG FÜR DIE PET-BILDGEBUNG
 AMYVID (FLORBETAPIR 18 F-INJEKTION) AUSWERTERSCHULUNG FÜR DIE PET-BILDGEBUNG Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
AMYVID (FLORBETAPIR 18 F-INJEKTION) AUSWERTERSCHULUNG FÜR DIE PET-BILDGEBUNG Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
Rekonstitution und Verabreichung von Cinryze (C1-Inhibitor [vom Menschen]) Hinweise für Ärzte und medizinisches Fachpersonal
![Rekonstitution und Verabreichung von Cinryze (C1-Inhibitor [vom Menschen]) Hinweise für Ärzte und medizinisches Fachpersonal Rekonstitution und Verabreichung von Cinryze (C1-Inhibitor [vom Menschen]) Hinweise für Ärzte und medizinisches Fachpersonal](/thumbs/67/57052806.jpg) Rekonstitution und Verabreichung von Cinryze (C1-Inhibitor [vom Menschen]) Hinweise für Ärzte und medizinisches Fachpersonal Diese Informationen werden Ihnen von der Shire Deutschland GmbH zur Verfügung
Rekonstitution und Verabreichung von Cinryze (C1-Inhibitor [vom Menschen]) Hinweise für Ärzte und medizinisches Fachpersonal Diese Informationen werden Ihnen von der Shire Deutschland GmbH zur Verfügung
MYCOPHENOLAT-MOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN. Information über die Risiken für das ungeborene Baby
 MYCOPHENOLAT-MOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN Information über die Risiken für das ungeborene Baby Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen
MYCOPHENOLAT-MOFETIL (MMF)-/ MYCOPHENOLSÄURE (MPA)-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN Information über die Risiken für das ungeborene Baby Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen
Schrittweise Anleitung zum Gebrauch des Enbrel 50 mg Fertigpens MYCLIC
 Schrittweise Anleitung zum Gebrauch des Enbrel 50 mg Fertigpens MYCLIC Diese Informationsbroschüre zur Anwendung von Etanercept wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans
Schrittweise Anleitung zum Gebrauch des Enbrel 50 mg Fertigpens MYCLIC Diese Informationsbroschüre zur Anwendung von Etanercept wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans
MYCOPHENOLAT-HALTIGE ARZNEIMITTEL LEITFADEN FÜR ANGEHÖRIGE DER GESUNDHEITSBERUFE
 MYCOPHENOLAT-HALTIGE ARZNEIMITTEL LEITFADEN FÜR ANGEHÖRIGE DER GESUNDHEITSBERUFE Teratogenes Risiko Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen Arzneimitteln wurde als Teil der Zulassungsauflagen
MYCOPHENOLAT-HALTIGE ARZNEIMITTEL LEITFADEN FÜR ANGEHÖRIGE DER GESUNDHEITSBERUFE Teratogenes Risiko Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen Arzneimitteln wurde als Teil der Zulassungsauflagen
MYCOPHENOLAT-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN
 MYCOPHENOLAT-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN Informationen über das Risiko für das ungeborene Baby Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen Arzneimitteln (Mycophenolat Mofetil
MYCOPHENOLAT-HALTIGE ARZNEIMITTEL LEITFADEN FÜR PATIENTEN Informationen über das Risiko für das ungeborene Baby Dieser Leitfaden zur Anwendung von Mycophenolat-haltigen Arzneimitteln (Mycophenolat Mofetil
Sicherheitsrelevante Hinweise für medizinische Fachkreise
 Sicherheitsrelevante Hinweise für medizinische Fachkreise für die Therapie des multiplen Myeloms mit Bortezomib in Abhängigkeit von den unterschiedlichen Indikationen im Rahmen der Indikationserweiterung
Sicherheitsrelevante Hinweise für medizinische Fachkreise für die Therapie des multiplen Myeloms mit Bortezomib in Abhängigkeit von den unterschiedlichen Indikationen im Rahmen der Indikationserweiterung
Wichtige Sicherheitshinweise in Bezug auf Schwangerschaften bei Patientinnen, die Odomzo -Kapseln (Sonidegib) einnehmen
 Wichtige Sicherheitshinweise in Bezug auf Schwangerschaften bei Patientinnen, die Odomzo -Kapseln (Sonidegib) einnehmen Diese Informationsbroschüre ist verpflichtender Teil der Zulassung von Odomzo (Sonidegib)
Wichtige Sicherheitshinweise in Bezug auf Schwangerschaften bei Patientinnen, die Odomzo -Kapseln (Sonidegib) einnehmen Diese Informationsbroschüre ist verpflichtender Teil der Zulassung von Odomzo (Sonidegib)
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Medivitan iv Fertigspritze 5mg, 1mg, 1,05mg Injektionslösung Wirkstoffe: Pyridoxinhydrochlorid / Cyanocobalamin / Folsäure Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Medivitan iv Fertigspritze 5mg, 1mg, 1,05mg Injektionslösung Wirkstoffe: Pyridoxinhydrochlorid / Cyanocobalamin / Folsäure Lesen Sie die gesamte Packungsbeilage
Anwendung von Tenofovirdisoproxil und Emtricitabin/Tenofovirdisoproxil bei Jugendlichen
 HINWEISE FÜR ANGEHÖRIGE DER HEILBERUFE ZUR ANWENDUNG VON TENOFOVIRDISOPROXIL UND TENOFOVIRDISOPROXIL-HALTIGEN ARZNEIMITTELN ZUR BEHANDLUNG HIV-1-INFIZIERTER JUGENDLICHER Diese Informationsbroschüre zur
HINWEISE FÜR ANGEHÖRIGE DER HEILBERUFE ZUR ANWENDUNG VON TENOFOVIRDISOPROXIL UND TENOFOVIRDISOPROXIL-HALTIGEN ARZNEIMITTELN ZUR BEHANDLUNG HIV-1-INFIZIERTER JUGENDLICHER Diese Informationsbroschüre zur
Multiresistente Tuberkulose Ein Leitfaden mit wichtigen Informationen über Ihre Krankheit und Ihre Behandlung mit Deltyba (Delamanid)
 Information für Patienten Multiresistente Tuberkulose Ein Leitfaden mit wichtigen Informationen über Ihre Krankheit und Ihre Behandlung mit Deltyba (Delamanid) Dieses Arzneimittel unterliegt einer zusätzlichen
Information für Patienten Multiresistente Tuberkulose Ein Leitfaden mit wichtigen Informationen über Ihre Krankheit und Ihre Behandlung mit Deltyba (Delamanid) Dieses Arzneimittel unterliegt einer zusätzlichen
ANHANG III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 ANHANG III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Die zuständigen Behörden der Mitgliedstaaten müssen die Zusammenfassung der
ANHANG III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Die zuständigen Behörden der Mitgliedstaaten müssen die Zusammenfassung der
LEITFADEN FÜR PATIENTINNEN
 LEITFADEN FÜR PATIENTINNEN Valproathaltige Arzneimittel Empfängnisverhütung und Schwangerschaft: Was Sie unbedingt wissen sollten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies er
LEITFADEN FÜR PATIENTINNEN Valproathaltige Arzneimittel Empfängnisverhütung und Schwangerschaft: Was Sie unbedingt wissen sollten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies er
DER MYCLIC-FERTIGPEN (ENBREL 50 mg INJEKTIONSLÖSUNG IM FERTIGPEN)
 Patientenschulungsmaterial für medizinische Fachkreise DER MYCLIC-FERTIGPEN (ENBREL 50 mg INJEKTIONSLÖSUNG IM FERTIGPEN) Dieses Schulungsflipchart zur Anwendung von Etanercept wurde als Teil der Zulassungsauflagen
Patientenschulungsmaterial für medizinische Fachkreise DER MYCLIC-FERTIGPEN (ENBREL 50 mg INJEKTIONSLÖSUNG IM FERTIGPEN) Dieses Schulungsflipchart zur Anwendung von Etanercept wurde als Teil der Zulassungsauflagen
'Y Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine
 'Y Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können dabei helfen, indem Sie jede auftretende
'Y Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Sie können dabei helfen, indem Sie jede auftretende
Mein Exjade (Deferasirox) Handbuch
 Mein Exjade (Deferasirox) Handbuch Name Datum Diese Patientenbroschüre zur Anwendung von Deferasirox wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden über die
Mein Exjade (Deferasirox) Handbuch Name Datum Diese Patientenbroschüre zur Anwendung von Deferasirox wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden über die
Anhang III. Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage
 Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Bewilligungsantrag Nucala (Mepolizumab) - Erstdokumentation
 Bewilligungsantrag - Erstdokumentation Sozialversicherungsnummer: Anwendungsgebiet: ist angezeigt als Zusatzbehandlung bei schwerem refraktärem eosinophilem Asthma bei erwachsenen Patienten (siehe Fachinformation
Bewilligungsantrag - Erstdokumentation Sozialversicherungsnummer: Anwendungsgebiet: ist angezeigt als Zusatzbehandlung bei schwerem refraktärem eosinophilem Asthma bei erwachsenen Patienten (siehe Fachinformation
AKTUELLE BROSCHÜRE ZU FRAGEN & ANTWORTEN FÜR MEDIZINISCHES FACHPERSONAL. VORICONAZOL-haltige Arzneimittel oral/intravenös
 AKTUELLE BROSCHÜRE ZU FRAGEN & ANTWORTEN FÜR MEDIZINISCHES FACHPERSONAL VORICONAZOL-haltige Arzneimittel oral/intravenös Diese Informationsbroschüre zur Anwendung von VORICONAZOL-haltigen Arzneimitteln
AKTUELLE BROSCHÜRE ZU FRAGEN & ANTWORTEN FÜR MEDIZINISCHES FACHPERSONAL VORICONAZOL-haltige Arzneimittel oral/intravenös Diese Informationsbroschüre zur Anwendung von VORICONAZOL-haltigen Arzneimitteln
behördlich genehmigtes Schulungsmaterial
 behördlich genehmigtes Schulungsmaterial Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige
behördlich genehmigtes Schulungsmaterial Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige
Mein Exjade (Deferasirox) Handbuch
 Mein Exjade (Deferasirox) Handbuch Name Datum Diese Patientenbroschüre zur Anwendung von Deferasirox wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden über die
Mein Exjade (Deferasirox) Handbuch Name Datum Diese Patientenbroschüre zur Anwendung von Deferasirox wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen des Risikomanagement-Plans wurden über die
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Nux vomica-homaccord -Tropfen
 1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Zusammenfassung der Merkmale des Arzneimittels
 1. Bezeichnung des Arzneimittels Eucabal -Hustensaft Zusammenfassung der Merkmale des Arzneimittels 2. Qualitative und quantitative Zusammensetzung 100 ml enthalten: 19,2 g Flüssigextrakt aus Thymian (Thymi
1. Bezeichnung des Arzneimittels Eucabal -Hustensaft Zusammenfassung der Merkmale des Arzneimittels 2. Qualitative und quantitative Zusammensetzung 100 ml enthalten: 19,2 g Flüssigextrakt aus Thymian (Thymi
Wichtige Information zu Dapoxetin (Priligy )
 Wichtige Information zu Dapoxetin (Priligy ) Diese Informationsbroschüre zur Anwendung von Dapoxetin (Priligy ) wurde als Teil der Zulassungsauflagen für das Arzneimittel erstellt und behördlich genehmigt.
Wichtige Information zu Dapoxetin (Priligy ) Diese Informationsbroschüre zur Anwendung von Dapoxetin (Priligy ) wurde als Teil der Zulassungsauflagen für das Arzneimittel erstellt und behördlich genehmigt.
Anwendungshinweise für Patienten für den Gebrauch von Abstral Sublingualtabletten
 Anwendungshinweise für Patienten für den Gebrauch von Abstral Sublingualtabletten Inhaltsverzeichnis Anwendungshinweise für Patienten für den Gebrauch von Abstral Sublingualtabletten Dieser Leitfaden zur
Anwendungshinweise für Patienten für den Gebrauch von Abstral Sublingualtabletten Inhaltsverzeichnis Anwendungshinweise für Patienten für den Gebrauch von Abstral Sublingualtabletten Dieser Leitfaden zur
INFLECTRA (INFLIXIMAB): SICHERHEITSINFORMATION FÜR VERSCHREIBENDE ÄRZTE
 INFLECTRA (INFLIXIMAB): SICHERHEITSINFORMATION FÜR VERSCHREIBENDE ÄRZTE Infliximab kann mit schwerwiegenden, potentiell lebensbedrohlichen Nebenwirkungen einhergehen, die verhindert oder identifiziert
INFLECTRA (INFLIXIMAB): SICHERHEITSINFORMATION FÜR VERSCHREIBENDE ÄRZTE Infliximab kann mit schwerwiegenden, potentiell lebensbedrohlichen Nebenwirkungen einhergehen, die verhindert oder identifiziert
Leitfaden für medizinisches Fachpersonal HEMLIBRA (Emicizumab) Subkutane Injektion
 Leitfaden für medizinisches Fachpersonal HEMLIBRA (Emicizumab) Subkutane Injektion Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
Leitfaden für medizinisches Fachpersonal HEMLIBRA (Emicizumab) Subkutane Injektion Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse
Ringer-Lösung DAB 7 Infusionslösung
 Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila Ringer-Lösung DAB 7 Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist Ringer-Lösung DAB 7
Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila Ringer-Lösung DAB 7 Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist Ringer-Lösung DAB 7
Leitfaden für Patienten zur Anwendung von KYMRIAH (Tisagenlecleucel)
 Leitfaden für Patienten zur Anwendung von KYMRIAH (Tisagenlecleucel) Wichtige Sicherheitsinformationen zur Minimierung des Risikos von KYMRIAH Der Wirkstoff von KYMRIAH heißt Tisagenlecleucel. Diese Bezeichnung
Leitfaden für Patienten zur Anwendung von KYMRIAH (Tisagenlecleucel) Wichtige Sicherheitsinformationen zur Minimierung des Risikos von KYMRIAH Der Wirkstoff von KYMRIAH heißt Tisagenlecleucel. Diese Bezeichnung
Zu den wichtigsten Nebenwirkungen gehören schwere Nierenfunktionsstörungen und Kieferosteonekrosen.
 Zoledronsäure AL (Zoledronsäure 5 mg/100 ml Infusionslösung) Leitfaden für Ärzte Dieser Leitfaden für Ärzte zur Anwendung von Zoledronsäure 5 mg wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen
Zoledronsäure AL (Zoledronsäure 5 mg/100 ml Infusionslösung) Leitfaden für Ärzte Dieser Leitfaden für Ärzte zur Anwendung von Zoledronsäure 5 mg wurde als Teil der Zulassungsauflagen erstellt. Im Rahmen
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CRIMAX Haarvitaltropfen Wirkstoffe: Acidum hydrofluoricum Dil. D12, Graphites Dil. D8, Pel talpae Dil. D8, Selenium amorphum Dil. D12 Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CRIMAX Haarvitaltropfen Wirkstoffe: Acidum hydrofluoricum Dil. D12, Graphites Dil. D8, Pel talpae Dil. D8, Selenium amorphum Dil. D12 Lesen Sie die gesamte
PATIENTEN- INFORMATIONSKARTE
 PATIENTEN- INFORMATIONSKARTE Diese Patienteninformationskarte ist ein verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, sowie Patienten die besonderen Sicherheitsanforder
PATIENTEN- INFORMATIONSKARTE Diese Patienteninformationskarte ist ein verpflichtender Teil der Zulassung, um sicherzustellen, dass Angehörige der Heilberufe, sowie Patienten die besonderen Sicherheitsanforder
Checkliste zum Empfang, zur Lagerung und zur Vorbereitung der Infusion von KYMRIAH (Tisagenlecleucel)
 Checkliste zum Empfang, zur Lagerung und zur Vorbereitung der Infusion von KYMRIAH (Tisagenlecleucel) Der Wirkstoff von KYMRIAH heißt Tisagenlecleucel. Diese Bezeichnung wird im Folgenden verwendet. Diese
Checkliste zum Empfang, zur Lagerung und zur Vorbereitung der Infusion von KYMRIAH (Tisagenlecleucel) Der Wirkstoff von KYMRIAH heißt Tisagenlecleucel. Diese Bezeichnung wird im Folgenden verwendet. Diese
Patientenpass* für Patienten zur sicheren Anwendung von Hemlibra bei der Behandlung von Hämophilie A
 PATIENTENPASS Hemlibra (Emicizumab) Subkutane Injektion Patientenpass* für Patienten zur sicheren Anwendung von Hemlibra bei der Behandlung von Hämophilie A Die risikominimierenden Informationsmaterialien
PATIENTENPASS Hemlibra (Emicizumab) Subkutane Injektion Patientenpass* für Patienten zur sicheren Anwendung von Hemlibra bei der Behandlung von Hämophilie A Die risikominimierenden Informationsmaterialien
Update-Informationen für DMR-EX80S, EX81S/71S, EX72S
 Modellnummer DMR-EX80SEG Update-Version Ver 1.15 Datei Name/Größe UPDATE_DMR-EX80SEG_V115.exe / 7.739.256 Bytes Modellnummer DMR-EX81SEG, DMR-EX71SEG Update-Version Ver 1.11 Datei Name/Größe UPDATE_DMR-EX81S_71SEG_V111.exe
Modellnummer DMR-EX80SEG Update-Version Ver 1.15 Datei Name/Größe UPDATE_DMR-EX80SEG_V115.exe / 7.739.256 Bytes Modellnummer DMR-EX81SEG, DMR-EX71SEG Update-Version Ver 1.11 Datei Name/Größe UPDATE_DMR-EX81S_71SEG_V111.exe
PARENTERAL VE Infusionslösung
 Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila PARENTERAL VE Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist PARENTERAL VE und wofür wird
Gebrauchsinformation und Fachinformation SERAG-WIESSNER GmbH & Co. KG Zum Kugelfang 8-12 95119 Naila PARENTERAL VE Infusionslösung Diese Packungsbeilage beinhaltet: 1. Was ist PARENTERAL VE und wofür wird
VPRIV (Velaglucerase alfa)
 VPRIV (Velaglucerase alfa) Schulungsmaterial für Ärzte Die hier aufgeführten Dokumente wurden von Shire im Rahmen der Verpflichtung zu Risikominimierungsmaβnahmen für VPRIV erstellt und dienen als Leitlinie
VPRIV (Velaglucerase alfa) Schulungsmaterial für Ärzte Die hier aufgeführten Dokumente wurden von Shire im Rahmen der Verpflichtung zu Risikominimierungsmaβnahmen für VPRIV erstellt und dienen als Leitlinie
WICHTIGE INFORMATIONEN FÜR PATIENTEN. denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde
 WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde 2 Version 2 (Stand: Februar 2017) Erstellt in Abstimmung mit dem
WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung des mittelschweren bis schweren aktiven Morbus Crohn verschrieben wurde 2 Version 2 (Stand: Februar 2017) Erstellt in Abstimmung mit dem
WICHTIGE INFORMATIONEN FÜR PATIENTEN
 WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung der mittelschweren bis schweren Plaque-Psoriasis bzw. aktiven psoriatischen Arthritis verschrieben wurde 2 Version 5 (Stand: Februar 2017)
WICHTIGE INFORMATIONEN FÜR PATIENTEN denen STELARA zur Behandlung der mittelschweren bis schweren Plaque-Psoriasis bzw. aktiven psoriatischen Arthritis verschrieben wurde 2 Version 5 (Stand: Februar 2017)
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Wichtiger Produkthinweis
 Wichtiger Produkthinweis Mannheim, 26.06.2017 Wichtige Information zur Accu-Chek Connect Diabetes Management App: Risiko für falsche Bolusvorschläge in verschiedenen App-Versionen für ios und Android Roche
Wichtiger Produkthinweis Mannheim, 26.06.2017 Wichtige Information zur Accu-Chek Connect Diabetes Management App: Risiko für falsche Bolusvorschläge in verschiedenen App-Versionen für ios und Android Roche
Worksheet Crafter Installationsanleitung
 Worksheet Crafter Installationsanleitung Herzlich willkommen! Mit dieser kleinen Anleitung führen wir dich Schritt für Schritt durch die Installation des Worksheet Crafter. Eigentlich ist die Installation
Worksheet Crafter Installationsanleitung Herzlich willkommen! Mit dieser kleinen Anleitung führen wir dich Schritt für Schritt durch die Installation des Worksheet Crafter. Eigentlich ist die Installation
Wichtige Informationen für medizinische Fachkräfte über die ernsten Risiken im Zusammenhang mit CAPRELSA -Tabletten
 Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert,
Wichtige sicherheitsrelevante Informationen für Apothekerinnen und Apotheker
 behördlich genehmigtes Schulungsmaterial Wichtige sicherheitsrelevante Informationen für Apothekerinnen und Apotheker REKONSTITUTION von VELCADE (Bortezomib) 3,5 mg zur subkutanen oder intravenösen Injektion
behördlich genehmigtes Schulungsmaterial Wichtige sicherheitsrelevante Informationen für Apothekerinnen und Apotheker REKONSTITUTION von VELCADE (Bortezomib) 3,5 mg zur subkutanen oder intravenösen Injektion
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER GRIPAGIL Grippetropfen mit Echinacea Wirkstoffe: Ceanothus americanus D2, Cinchona pubescens D3, Echinacea D2 Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER GRIPAGIL Grippetropfen mit Echinacea Wirkstoffe: Ceanothus americanus D2, Cinchona pubescens D3, Echinacea D2 Lesen Sie die gesamte Packungsbeilage sorgfältig
Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem Antigenhalt)
 Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
Elektronisches Vergabeinformations-System. Bedienungsanleitung für Bewerber / Bieter
 Bedienungsanleitung für Bewerber / Bieter Angebotsabgabe mit qualifizierter Signatur, fortgeschrittener Signatur und ohne Signatur - Login...Seite 2 - Angebotsabgabe mit qualifizierter Signatur...Seite
Bedienungsanleitung für Bewerber / Bieter Angebotsabgabe mit qualifizierter Signatur, fortgeschrittener Signatur und ohne Signatur - Login...Seite 2 - Angebotsabgabe mit qualifizierter Signatur...Seite
Checkliste Erstellung Educational Material / Schulungsmaterial (Printmaterialien)
 Checkliste Erstellung Educational Material / Schulungsmaterial (Printmaterialien) Version 1.0, August 2017 I. Formale Vorgaben an das Schulungsmaterial Disclaimer, z.b. Fachkreise:
Checkliste Erstellung Educational Material / Schulungsmaterial (Printmaterialien) Version 1.0, August 2017 I. Formale Vorgaben an das Schulungsmaterial Disclaimer, z.b. Fachkreise:
Anwendung von Bortezomib 3,5 mg nach Zubereitung: Subkutane oder intravenöse Injektion
 Wichtige sicherheitsrelevante Informationen zur Rekonstitution, Dosierung und Applikation/Anwendung für medizinische Fachkreise Anwendung von Bortezomib 3,5 mg nach Zubereitung: Subkutane oder intravenöse
Wichtige sicherheitsrelevante Informationen zur Rekonstitution, Dosierung und Applikation/Anwendung für medizinische Fachkreise Anwendung von Bortezomib 3,5 mg nach Zubereitung: Subkutane oder intravenöse
LEITFADEN FÜR PATIENTINNENN
 LEITFADEN FÜR PATIENTINNENN Valproathaltige Arzneimittel Empfängnisverhütung und Schwangerschaft: Was Sie unbedingt wissen sollten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies er
LEITFADEN FÜR PATIENTINNENN Valproathaltige Arzneimittel Empfängnisverhütung und Schwangerschaft: Was Sie unbedingt wissen sollten Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies er
behördlich genehmigtes Schulungsmaterial (Adalimumab) Patientenpass für Erwachsene
 behördlich genehmigtes Schulungsmaterial HUMIRA (Adalimumab) Patientenpass für Erwachsene Juli 2017 Liebe Patienten, lieber Patient, Ihr behandelnder Arzt hat Ihnen HUMIRA verordnet. Dieser Patientenpass
behördlich genehmigtes Schulungsmaterial HUMIRA (Adalimumab) Patientenpass für Erwachsene Juli 2017 Liebe Patienten, lieber Patient, Ihr behandelnder Arzt hat Ihnen HUMIRA verordnet. Dieser Patientenpass
Erforderliches Zubehör (nicht im Lieferumfang enthalten)
 T6K SOFTWARE UPDATE ANLEITUNG (Version: 2.0) Durch Software Updates bleibt Ihr Futaba T6K Fernsteuersystem stets auf dem aktuellen Stand und kann um interessante Funktionen erweitert werden. Laden Sie
T6K SOFTWARE UPDATE ANLEITUNG (Version: 2.0) Durch Software Updates bleibt Ihr Futaba T6K Fernsteuersystem stets auf dem aktuellen Stand und kann um interessante Funktionen erweitert werden. Laden Sie
Gebrauchsinformation: Information für Patienten
 Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
Spezielle Informationen bei Kinderwunsch und Schwangerschaft
 Spezielle Informationen bei Kinderwunsch und Schwangerschaft Patientenbroschüre Beauflagtes Schulungsmaterial 2 Diese Informationsbroschüre für Patienten zur Anwendung von Leflunomid medac ist eine Auflage
Spezielle Informationen bei Kinderwunsch und Schwangerschaft Patientenbroschüre Beauflagtes Schulungsmaterial 2 Diese Informationsbroschüre für Patienten zur Anwendung von Leflunomid medac ist eine Auflage
Zuerst müssen Sie prüfen, welche Anwendung für Ihre Firmware-Aktualisierung verwendet werden muss. Dies. Application to use for firmware update
 Firmware-Aktualisierung für GoGear SA4RGA Zuerst müssen Sie prüfen, welche Anwendung für Ihre Firmware-Aktualisierung verwendet werden muss. Dies hängt von der Seriennummer Ihres Players ab: Serial number
Firmware-Aktualisierung für GoGear SA4RGA Zuerst müssen Sie prüfen, welche Anwendung für Ihre Firmware-Aktualisierung verwendet werden muss. Dies hängt von der Seriennummer Ihres Players ab: Serial number
Inhaltsverzeichnis. Diese Kurzanleitung beschreibt die ersten Schritte mit dem IRIScan TM Mouse Executive 2
 Diese Kurzanleitung beschreibt die ersten Schritte mit dem IRIScan TM Mouse Executive 2 Die Beschreibungen in dieser Dokumentation beziehen sich auf die Betriebssysteme Windows 7 und Mac OS X Mountain
Diese Kurzanleitung beschreibt die ersten Schritte mit dem IRIScan TM Mouse Executive 2 Die Beschreibungen in dieser Dokumentation beziehen sich auf die Betriebssysteme Windows 7 und Mac OS X Mountain
Wie installiere ich den CFX Trader?
 Wie installiere ich den CFX Trader? Anleitung zur Installation: Die Installation des CFX Traders ist sehr einfach zu bewerkstelligen. Es reicht aus, wenn Sie die Installationsroutine des CFX Traders starten
Wie installiere ich den CFX Trader? Anleitung zur Installation: Die Installation des CFX Traders ist sehr einfach zu bewerkstelligen. Es reicht aus, wenn Sie die Installationsroutine des CFX Traders starten
RoACTEMRA (Tocilizumab) Patientenpass
 RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
HINWEIS ZUM LIEFERENGPASS UND BESONDERE HANDHABUNGSHINWEISE
 HINWEIS ZUM LIEFERENGPASS UND BESONDERE HANDHABUNGSHINWEISE ERWINASE 10.000 I.E./Durchstechflasche Pulver zur Herstellung einer Injektionslösung BEI DER ANWENDUNG DER CHARGEN 174aG116 UND 177aG116 IST
HINWEIS ZUM LIEFERENGPASS UND BESONDERE HANDHABUNGSHINWEISE ERWINASE 10.000 I.E./Durchstechflasche Pulver zur Herstellung einer Injektionslösung BEI DER ANWENDUNG DER CHARGEN 174aG116 UND 177aG116 IST
Fachinformation. Sonstige Bestandteile mit bekannter Wirkung:Enthält u.a. Macrogolglycerolhydroxystearat und Ethanol.
 Fachinformation 1. Bezeichnung des Arzneimittels Thymian Hustenlösung Flüssigkeit zum Einnehmen 2. Qualitative und quantitative Zusammensetzung 100 ml (entsprechend 97 g) Flüssigkeit enthalten: Wirkstoff:
Fachinformation 1. Bezeichnung des Arzneimittels Thymian Hustenlösung Flüssigkeit zum Einnehmen 2. Qualitative und quantitative Zusammensetzung 100 ml (entsprechend 97 g) Flüssigkeit enthalten: Wirkstoff:
Filmtabletten. Titrationsleitfaden. Beginn der Therapie mit Uptravi
 Filmtabletten Titrationsleitfaden Beginn der Therapie mit Uptravi Bitte lesen Sie vor Beginn der Therapie die beigefügte Gebrauchsinformation. Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Filmtabletten Titrationsleitfaden Beginn der Therapie mit Uptravi Bitte lesen Sie vor Beginn der Therapie die beigefügte Gebrauchsinformation. Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung.
Bedienungsanleitung für MEEM-Kabel-Desktop-App Mac
 Bedienungsanleitung für MEEM-Kabel-Desktop-App Mac Installation und Bedienungsanleitung - v0.9 Bevor Sie diese Anleitung lesen, sollten Sie bitte die Bedienungsanleitung für MEEM-Kabel und Handy-App für
Bedienungsanleitung für MEEM-Kabel-Desktop-App Mac Installation und Bedienungsanleitung - v0.9 Bevor Sie diese Anleitung lesen, sollten Sie bitte die Bedienungsanleitung für MEEM-Kabel und Handy-App für
Gebrauchsinformation: Information für Patienten. Schlaf- und Entspannungstropfen Similasan Avena sativa D1, Passiflora incarnata D1
 1/5 Gebrauchsinformation: Information für Patienten Schlaf- und Entspannungstropfen Similasan Avena sativa D1, Passiflora incarnata D1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
1/5 Gebrauchsinformation: Information für Patienten Schlaf- und Entspannungstropfen Similasan Avena sativa D1, Passiflora incarnata D1 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
INFORMATIONSBROSCHÜRE FÜR PERSONEN MIT TRUVADA ZUR PRÄ-EXPOSITIONS-PROPHYLAXE (PrEP)
 INFORMATIONSBROSCHÜRE FÜR PERSONEN MIT TRUVADA ZUR PRÄ-EXPOSITIONS-PROPHYLAXE (PrEP) Wichtige Informationen zu Truvada (Emtricitabin/ Tenofovirdisoproxilfumarat), um das Risiko einer Infektion mit dem
INFORMATIONSBROSCHÜRE FÜR PERSONEN MIT TRUVADA ZUR PRÄ-EXPOSITIONS-PROPHYLAXE (PrEP) Wichtige Informationen zu Truvada (Emtricitabin/ Tenofovirdisoproxilfumarat), um das Risiko einer Infektion mit dem
Wichtige sicherheitsrelevante Informationen für. Patienten. zur Behandlung mit Soliris bei refraktärer gmg. ( E culizumab) Patienten.
 Patienten refraktäre gmg Wichtige sicherheitsrelevante Informationen für Patienten zur Behandlung mit Soliris bei refraktärer gmg behördlich genehmigtes Schulungsmaterial ( E culizumab) Diese Informationsbroschüre
Patienten refraktäre gmg Wichtige sicherheitsrelevante Informationen für Patienten zur Behandlung mit Soliris bei refraktärer gmg behördlich genehmigtes Schulungsmaterial ( E culizumab) Diese Informationsbroschüre
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Euphorbium compositum-heel -Tropfen
 1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Euphorbium compositum-heel -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Euphorbium compositum-heel -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Nux vomica-homaccord -Tropfen
 1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
1 Dateien über das Kontextmenü in ein Archiv verschlüsseln
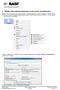 1 Dateien über das Kontextmenü in ein Archiv verschlüsseln Wählen Sie ein Dokument aus, das Sie einem verschlüsselten ZIP-Archiv hinzufügen möchten, indem Sie mit der rechten Maustaste darauf klicken;
1 Dateien über das Kontextmenü in ein Archiv verschlüsseln Wählen Sie ein Dokument aus, das Sie einem verschlüsselten ZIP-Archiv hinzufügen möchten, indem Sie mit der rechten Maustaste darauf klicken;
