Boden als Nährstoffspeicher
|
|
|
- Gerda Kurzmann
- vor 8 Jahren
- Abrufe
Transkript
1 Referentinnen: Juliana Schwarz: , Adelinde Johanna Stropahl: Boden als Nährstoffspeicher Ursachen, Vorgänge, Einflüsse des Kationen und Anionenaustausches Modul B301: Spezielle Themen der Geographie Dozent: Tilman Rost
2 Organisches & anorganisches Material Zersetzung & Aufspaltung durch Verwitterung & Mikroorganismen Stickstoff (N), Phosphor (P), Kalium (K), Schwefel (S), Calcium (Ca) und Magnesium (Mg) + Spurenelemente Nährstoffe teilweise von Pflanzenwurzeln aufgenommen Nur kurzzeitig verfügbar? Rest? Weggespühlt? Wie werden Nährstoffe im Boden gespeichert? Bindung an Sorptionskörper (Tonminerale, Si, Al & FeOxide, Huminstoffe) hohe spezifische Oberfläche elektrisch geladen
3 Prozess des Anionen und Kationenaustauschs: Austausch A/K Adsorption Sorptions körper Desorption A/K Austausch
4 1. Bedeutung des Ionenaustauschs Nährstoffe in Boden vor Auswaschung geschützt Dennoch für Pflanzen verfügbar Bodeneigenschaften (Gefüge, Wasser und Lufthaushalt, Bodenreaktion, biologische Aktivität) Bodenbewertungsmaß: KAK = Kationenaustauschkapazität
5 Gliederung Referentinnen: Juliana Schwarz, Adelinde Stropahl 1. Bedeutung des Ionenaustauschs 2. Chemische Grundlagen 3. Ursache 3.1 permanente Ladung: Isomorpher Ersatz 3.2 variable Ladung: ph 4. Prozess 4.1 Kationenaustausch 4.2 Anionenaustausch 5. Einflüsse 5.1 Ladungsstärke 5.2 Hydratation 5.3 Konzentration 6. Auswirkungen 6.1 Kationenaustauschkapazität 6.2.Basensättigung 6.3. optimaler ph Wert 5
6 3. chemische Grundlagen Ionen = elektrisch geladene Atome oder Moleküle positiv = Kationen negativ = Anionen, 8+ Kern Ladung hängt von Schalenaufbau und Anzahl der Außenelektronen ab Ionen haben je nach Ladung verschiedene Eigenschaften u.a. auf phwert: Na +, K +, Mg 2+, Ca 2+ Al 3+, Fe 3+ neben H + > basisch > sauer Bei Ladungsüberschuss/ mangel > Adsorption, Desorption von Anionen/Kationen ALTESO (2012)
7 Gliederung Referentinnen: Juliana Schwarz, Adelinde Stropahl 1. Bedeutung des Ionenaustauschs 2. Chemische Grundlagen 3. Ursache 3.1 permanente Ladung: Isomorpher Ersatz 3.2 variable Ladung: ph 4. Prozess 4.1 Kationenaustausch 4.2 Anionenaustausch 5. Einflüsse 5.1 Ladungsstärke 5.2 Hydratation 5.3 Konzentration 6. Auswirkungen 6.1 Kationenaustauschkapazität 6.2.Basensättigung 6.3. optimaler ph Wert 7
8 2.1 permanente Ladung: Isomorpher Ersatz Silikatneubildung/ umwandlung: Austausch des Zentralatoms in Tetraeder bzw. Oktaederschicht führt zu Ladungsüberschuss/mangel Tetraederschicht: Siliziumkern Si 4+ ersetzt durch Al 3+ Oktaederschicht: Aluminiumkern Al 3+ ersetzt durch Mg 2+ (DiOktaeder) Al 3+ ersetzt durch Mg 2+ oder Fe 2+ (TriOktaeder) SiO4 Tetraeder
9 = = Referentinnen: Juliana Schwarz, Adelinde Stropahl 2.2 variable Ladung: ph = amphotere Substanzen 1. Metallhydroxid Bsp: Aminocarbonsäure Metall O H Metall O + H + 2. Carbonsäure Rest O C O H O C + H + Rest O sauer alkalisch ph = 0 9
10 Gliederung Referentinnen: Juliana Schwarz, Adelinde Stropahl 1. Bedeutung des Ionenaustauschs 2. Chemische Grundlagen 3. Ursache 3.1 permanente Ladung: Isomorpher Ersatz 3.2 variable Ladung: ph 4. Prozess 4.1 Kationenaustausch 4.2 Anionenaustausch 5. Einflüsse 5.1 Ladungsstärke 5.2 Hydratation 5.3 Konzentration 6. Auswirkungen 6.1 Kationenaustauschkapazität 6.2.Basensättigung 6.3. optimaler ph Wert 10
11 4. Prozess Oberflächenladung des Austauschers Elektronenmangel Adsorption von Anionen: Chloridion Cl Nitration NO3 Sulfatanionen SO4 Elektronenüberschuss Adsorption von Kationen: Magnesiumion Mg++ Natriumion Na+ Calciumion Ca++ Ammoniumion NH4+ > Anionenaustausch > Kationenaustausch
12 4.1 Kationenaustausch = Eigenschaft Kationen austauschbar anzulagern & wieder abgeben zu können Austauschkapazität ist von Ladungsstärke des Austauschers abhängig Beispiel: Schwefeltrioxid Austauscher: SO 3 Pos. Natrumionen angelagert > neutral Ca 2+ nimmt Platz von 2Na + ein Calcium wird gespeichert, Natrium ausgewaschen Wichtigste Nährelemente in absteigender Eintauschstärke: Al > Ca + + > Mg + + > K + > Na + > H +
13 4.1 Antionenaustausch = Eigenschaft Anionen austauschbar anzulagern & wieder abgeben zu können eher nebensächlich, nur vorhanden bei pos. Geladenen Huminstoffen Beispiel: Stickstoffverbindung Austauscher: RN + NO 3 Neg. Chloridion angelagert > neutral NO 3 nimmt Platz von Cl ein Nitrat wird gespeichert, Chlorid ausgewaschen > Gewässerbelastung durch Nitrat wird verhindert Eintauschstärke absteigend: SO 4 = > NO 3 > Cl > HCO 3 > OH > F
14 5. Einflüsse Warum werden einige Kationen/ Anionen eher ausgetauscht als andere?
15 Gliederung Referentinnen: Juliana Schwarz, Adelinde Stropahl 1. Bedeutung des Ionenaustauschs 2. Chemische Grundlagen 3. Ursache 3.1 permanente Ladung: Isomorpher Ersatz 3.2 variable Ladung: ph 4. Prozess 4.1 Kationenaustausch 4.2 Anionenaustausch 5. Einflüsse 5.1 Ladungsstärke 5.2 Hydratation 5.3 Konzentration 6. Auswirkungen 6.1 Kationenaustauschkapazität 6.2.Basensättigung 6.3. optimaler ph Wert 15
16 Negativer Austauscher I I I I I I I I I I Sternschicht Diffuse Schicht + Gleichgewichtslösung Referentinnen: Juliana Schwarz, Adelinde Stropahl 5.1 Ladungsstärke Je höher die Wertigkeit eines Anions/Kations, desto stärker die Anziehung an Austauscher Bsp: Ca 2+ dominiert Na + desto näher tritt es an Austauscher heran desto fester wird es an Austauscher gebunden Schwächere Ionen treten leichter wieder in Außenlösung über
17 5.2 Hydratation Jedes Ion wird von H2OHülle umgeben Je geringermächtig die Hydrathülle, desto höher das Eintauschpotential Dicke der Hülle abhängig von Durchmesser des Ions und seiner Ladung Kleiner Durchmesser H δ+ Großes elek. Kraftfeld Starke Hydratation δ O H δ+ Daraus resultiert die Lyotrope Reihe: Al > Ca + + > Mg + + > K + > Na + > H +
18 4.3 Konzentration Je höher die Konzentration eines Ions in Bodenlösung, desto höher seine Eintauschstärke Düngung basiert auf diesem Prinzip Beispiel: SchwefeltrioxidAustauscher Ca + +, Na +, Mg + + in Lyotroper Reihe vor H + Kein Austausch Erhöhung H + Konzentration (phsenkung): chem. Gleichgewicht wird verschoben Kationenaustausch trotz geringerer Eintauschstärke
19 Gliederung Referentinnen: Juliana Schwarz, Adelinde Stropahl 1. Bedeutung des Ionenaustauschs 2. Chemische Grundlagen 3. Ursache 3.1 permanente Ladung: Isomorpher Ersatz 3.2 variable Ladung: ph 4. Prozess 4.1 Kationenaustausch 4.2 Anionenaustausch 5. Einflüsse 5.1 Ladungsstärke 5.2 Hydratation 5.3 Konzentration 6. Auswirkungen 6.1 Kationenaustauschkapazität 6.2.Basensättigung 6.3. optimaler ph Wert 19
20 Zwei wichtige Indikatoren für die Bodenfruchtbarkeit: Kationenaustauschkapazität (KAK) Basensättigung
21 Kationenaustauschkapazität (KAK) Fähigkeit des Bodens Kationen aus der Bodenlösung reversibel sorbieren zu können Abhängig von der Anzahl der wirksamen negativen Ladungen der Austauscher Vor allem aufweitbare Tonminerale und Huminstoffe haben zusätzlich zur äußeren eine innere negativ geladene Oberfläche
22 Kationenaustauschkapazität (KAK) Fähigkeit Kationen aus der Bodenlösung reversibel sorbieren zu können Abhängig von der Anzahl der wirksamen negativen Ladungen der Austauscher Vor allem aufweitbare Tonminerale und Huminstoffe haben zusätzlich zur äußeren eine innere negativ geladene Oberfläche Abb. verändert nach GEBHARDT et al (2006): Physische Geographie und Humangeographie
23 Kationenaustauschkapazität (KAK) KAK = Maß für die Menge aller negativen Ladungen an der Oberfläche des Austauschers und die Summe aller Kationen die ein Bodenkolloid absorbieren und gegen andere, in der Bodenlösung befindliche Stoffe wieder austauschen kann Aber auch abhängig vom PH Wert der Bodenlösung, nicht nur von der Größe der Oberfläche des Austauschers
24 Kationenaustauschkapazität (KAK) Effektiven Kationenaustauschkapazität (AKe) Potentielle Kationenaustauschkapazität (AKp)
25 Kationenaustauschkapazität (KAK) Effektiven Kationenaustauschkapazität (AKe) Die tatsächliche, beim aktuellen PH Wert des Bodens gemessene KAK Kationenaustausch im alkalischen Bereich am größten, im sauren Bereich am niedrigsten AKe steigt also mit ansteigendem PH Wert sauer ph = 0 alkalisch 25
26 Kationenaustauschkapazität (KAK) Potentielle Kationenaustauschkapazität (AKp) gibt die maximale Anzahl möglicher freier Kationenbindungsplätze an Alle potentiell sorbierbaren Kationen in einer Bodenlösung Nach der DIN ISO (1995) Norm liegt die AKp in Böden humider Klimate bei einem PH Wert von 8,1 (leicht alkalisch) Nach Internationalen Klassifikationen (FAO UNESCO, USSoilTaxonomy) bei ph=7 (neutral) Unter optimalen Bedingungen AKe=AKp : z. B. in carbonathaltigen Böden
27 Kationenaustauschkapazität (KAK) Insbesondere abhängig: Tongehalt des Bodens und Art der Tonminerale Humusgehalt und Qualität des Humus Oxide und Hydroxide Anteil
28 Kationenaustauschkapazität (KAK) Beispiele: Kaolinit: 315 meq/100g Illit: meq/100g Vermicullit: meq/100g Allophane <100 meq/100g Variable Ladung 2 Schicht Tonmineral Permanent negativ geladen 3 SchichtTonminerale Variable Ladung MÜCKENHAUSEN, E.(1993): Die Bodenkunde und ihre geologischen, geomorphologischen, mineralogischen und pethrologischen Grundlagen
29 Kationenaustauschkapazität (KAK) Beispiele: Organische Substanz meq/100g > Huminstoffe meq/100g Quelle: MÜCKENHAUSEN, E.(1993)
30 Kationenaustauschkapazität (KAK) Beispiele: Organische Substanz meq/100g > Huminstoffe meq/100g Hochmolekulare Stoffe des Humusbodens, bestehend aus Kernen, Brücken und reaktiven Seitengruppen Vereinfacht bestehen die Brücken meist aus Sauerstoff, Stickstoff und Kohlenstoff Seitengruppen im Wesentlichen aus Carboxy Carbonyl Hydroxy und Aminogruppen Durch lockere, dreidimensionale Struktur hohe KAK Aber flexibel, mit abfallenden PH Wert knäulen sie sich zusammen und die reaktive Oberfläche vermindert sich
31 Anionenaustauschkapazität (AAK) Umgekehrt zur KAK : Fähigkeit Anionen aus der Bodenlösung reversibel zu sorbieren Steigt mit abnehmenden PH Wert an Eintauschstärke der Anionen wie bei den Kationen von Ladung und Wertigkeit abhängig
32 Basensättigung Basen = Alkali ( Kalium, Natrium) und Erdalkali Metalle ( Calcium, Magnesium) Spielen wichtige Rolle für die Pflanzenernährung Basensättigung = prozentuale Angabe des Anteils der basischen Kationen von der gesamten Kationenaustauschkapazität des Bodens Säure Basen Verhältnis am Austauscher Entspricht etwa dem durchschnittlichen Säure Basen Verhältnis der Bodenlösung Aussagekraft der Basensättigung = deutlich genauer als die des Boden PH Wertes
33 Basensättigung Eutroph: hohe Basensättigung ( mehr als 75 %), nährstoffreich Mesotroph: mittlere Basensättigung ( zwischen % ) Oligotroph: niedrige Basensättigung (unter 25 %), karg ( nährstoffarm) Die Basensättigung sinkt mit abnehmenden PH Wert Innerhalb eines Bodenprofils kann Zusammensetzung des Kationenbelags sehr unterschiedlich sein
34 Nährstoffe und PH Wert Sauer Neutral Basisch Quelle: Fmoeckel (2010): Nutrient vs. soilph
35 Nährstoffe und PH Wert PH Wert < 3,0 saure Sulfatböden 3,0 4,0 Hochmoore 4,0 5,0 Podsol 5,0 6,0 Parabraunerden 5,0 6,0 Braunerden 6,5 7,0 Schwarzerden 7,0 Kalkmarsch 7,0 7,5 Kalkreiche Niedermoore 7,5 8,0 Neutralsalzböden 8,0 9,0 Alkaliböden 9,0 10,0 Kalkmergel BLUM (2012): Bodenkunde in Stichworten Pflanze PH Wert Bundesministerium für Land und Forstwirtschaft, Umwelt und Wasserwirtschaft (2006) : Richtlinien für die sachgerechte Düngung
36 Referentinnen: Juliana Schwarz: , Adelinde Johanna Stropahl: Danke für s Zuhören!
37 Quellen: ALTESO (2012): Atomaufbau und Periodensystem Übersicht, ( ) Blum, W. E. H.(2012): Bodenkunde in Stichpunkten. Stuttgart Bundesministerium für Land und Forstwirtschaft, 2006 S. 13; upload: IRSLINGER (2005): Bodenökologie, Rottenburg. KUNTZE, ROESCHMANN, SCHWERDTFEGER (1994): Bodenkunde, Stuttgart. MÜCKENHAUSEN, E. ( 1993 ): Die Bodenkunde und ihre geologischen, geomorphologischen, mineralogischen und pethrologischen Grundlagen. Frankfurt am Main SCHEFFER, SCHACHTSCHABEL (2010): Lehrbuch der Bodenkunde, Heidelberg.
4 Boden. 4.1 Grundlagen. Boden mit charakteristischen Bodenhorizonten Bodenprofil Bodentyp. Aufbau und Zusammensetzung
 4 Boden 4.1 Grundlagen Aufbau und Zusammensetzung Lithosphäre - feste Gesteinshülle, ca. 100 km dick (griech. lithos, Stein; lat. sphaira, Kugel) Pedosphäre - Bodenhülle, wenige Dezimeter bis einige Meter
4 Boden 4.1 Grundlagen Aufbau und Zusammensetzung Lithosphäre - feste Gesteinshülle, ca. 100 km dick (griech. lithos, Stein; lat. sphaira, Kugel) Pedosphäre - Bodenhülle, wenige Dezimeter bis einige Meter
2 Bodenentwicklung 3 Lebensraum Boden Fauna. 4 Stoffkreislauf 5 Bodeneigenschaften
 Gliederung 1 Definition iti Boden 2 3 Lebensraum Boden Fauna Flora 4 5 Bodeneigenschaften 6 Boden im Unterricht Fauna- Lebensraum -Flora 1 Definition Unter Boden versteht man die obere, lockere, belebte
Gliederung 1 Definition iti Boden 2 3 Lebensraum Boden Fauna Flora 4 5 Bodeneigenschaften 6 Boden im Unterricht Fauna- Lebensraum -Flora 1 Definition Unter Boden versteht man die obere, lockere, belebte
Das Formelpuzzle Kopiervorlage
 Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Boden Versauerung Dynamik-Gefährdung
 Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E [email protected] I www.bodenoekologie.com Boden Versauerung Dynamik-Gefährdung Univ. Lek. DI Hans
Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E [email protected] I www.bodenoekologie.com Boden Versauerung Dynamik-Gefährdung Univ. Lek. DI Hans
Sorptionskomplex, Kalkbedarf. Dr. Heinrich Holzner, LK Stmk
 Sorptionskomplex, Kalkbedarf Dr. Heinrich Holzner, LK Stmk Was ist Sorption? Sorption ist der Überbegriff für Reaktionen, die an den Oberflächen fester Bodenbestandteile ablaufen. Dabei können gasförmige
Sorptionskomplex, Kalkbedarf Dr. Heinrich Holzner, LK Stmk Was ist Sorption? Sorption ist der Überbegriff für Reaktionen, die an den Oberflächen fester Bodenbestandteile ablaufen. Dabei können gasförmige
Kalium [K] Bildung der Hydrathülle
![Kalium [K] Bildung der Hydrathülle Kalium [K] Bildung der Hydrathülle](/thumbs/53/32607333.jpg) Diffusion Kalium [K] Bildung der Hydrathülle Anzahl der an ein Ion angelagerten Wassermoleküle: Na + K + 8 Mg 2+ 4 Ca 2+ 14 10-12 Cl - 3 Kali: [K] Dünger-Effekte Dünger-K schnell verfügbar Bodenkolloide
Diffusion Kalium [K] Bildung der Hydrathülle Anzahl der an ein Ion angelagerten Wassermoleküle: Na + K + 8 Mg 2+ 4 Ca 2+ 14 10-12 Cl - 3 Kali: [K] Dünger-Effekte Dünger-K schnell verfügbar Bodenkolloide
Wirkungsweise und Einsatzmöglichkeiten von Ionenaustauschern = Weichwassergeräten gem. DIN 19633
 Wirkungsweise und Einsatzmöglichkeiten von Ionenaustauschern = Weichwassergeräten gem. DIN 19633 Auch nach der Empfehlung ResAP(2004)3 des Europarates zu Ionenaustauschern und Adsorberharzen, die bei der
Wirkungsweise und Einsatzmöglichkeiten von Ionenaustauschern = Weichwassergeräten gem. DIN 19633 Auch nach der Empfehlung ResAP(2004)3 des Europarates zu Ionenaustauschern und Adsorberharzen, die bei der
Grundlagen Chemie. Dipl.-Lab. Chem. Stephan Klotz. Freiwill ige Feuerwehr Rosenheim
 Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Klinoptilolith Zeolith Ein Überblick
 Neue Bodenhilfsstoffe zur Erhaltung und Steigerung der Bodenfruchtbarkeit im ökologischen Landbau Klinoptilolith Zeolith Ein Überblick Dipl. Ing. Nina Schulze (Hydrogeologin) 17.März 2011, Bad Düben Überblick
Neue Bodenhilfsstoffe zur Erhaltung und Steigerung der Bodenfruchtbarkeit im ökologischen Landbau Klinoptilolith Zeolith Ein Überblick Dipl. Ing. Nina Schulze (Hydrogeologin) 17.März 2011, Bad Düben Überblick
Crashkurs Säure-Base
 Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
B Chemisch Wissenwertes. Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden.
 -I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
-I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Kochsalz-Kristalle (Halit) Wichtige Stoffgruppen Atomverband Stoffgruppe Metall Metall: Metallische Stoffe Salzartige Stoffe Metall Nichtmetall:
 Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Wasserstoff. Helium. Bor. Kohlenstoff. Standort: Name: Ordnungszahl: Standort: Name: Ordnungszahl: 18. Gruppe. Standort: Ordnungszahl: Name:
 H Wasserstoff 1 1. Gruppe 1. Periode He Helium 2 18. Gruppe 1. Periode B Bor 5 13. Gruppe C Kohlenstoff 6 14. Gruppe N Stickstoff 7 15. Gruppe O Sauerstoff 8 16. Gruppe Ne Neon 10 18. Gruppe Na Natrium
H Wasserstoff 1 1. Gruppe 1. Periode He Helium 2 18. Gruppe 1. Periode B Bor 5 13. Gruppe C Kohlenstoff 6 14. Gruppe N Stickstoff 7 15. Gruppe O Sauerstoff 8 16. Gruppe Ne Neon 10 18. Gruppe Na Natrium
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
FOS: Radioaktivität und Strahlenschutz. Chemische Elemente und ihre kleinsten Teilchen
 R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
Wirkungsweise und Einsatzmöglichkeiten von Ionenaustauschern = Weichwassergeräten gem. DIN 19633
 = Weichwassergeräten gem. DIN 19633 auch nach der Empfehlung ResAP(2004)3 des Europarates zu und Adsorberharzen, die bei der Herstellung von Lebensmitteln verwendet werden. Im Gegensatz zu physikalischen
= Weichwassergeräten gem. DIN 19633 auch nach der Empfehlung ResAP(2004)3 des Europarates zu und Adsorberharzen, die bei der Herstellung von Lebensmitteln verwendet werden. Im Gegensatz zu physikalischen
1 Chemische Elemente und chemische Grundgesetze
 1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
Trennungsgang. AC-I Seminar, B.
 Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Trennungsgang http://illumina-chemie.de/mangan-chrom-t2100.html www.chemgapedia.de, www.chemische-experimente.com 1 Trennungsgang auf einen Blick Trennungsgang Reaktionen in wässriger Lösung Fällung und
Winterthurer Trinkwasser. Chemisch-physikalische Zusammensetzung des Tössgrundwassers. Mittelwerte der Jahre
 Winterthurer Trinkwasser Chemisch-physikalische Zusammensetzung des Tössgrundwassers Mittelwerte der Jahre 2008 2012 Seite 2 von 5 Chemisch-physikalische Zusammensetzung des Trinkwassers in Winterthur
Winterthurer Trinkwasser Chemisch-physikalische Zusammensetzung des Tössgrundwassers Mittelwerte der Jahre 2008 2012 Seite 2 von 5 Chemisch-physikalische Zusammensetzung des Trinkwassers in Winterthur
Einführung in die Geographie. Klimageographie
 Einführung in die Geographie Klimageographie Klimaelemente Gliederung der Vorlesung 1. Physische Geographie 2. Geologie 3. Klima, Vegetation und Wasser 4. Pedologie / Bodengeographie 5. Geomorphologie
Einführung in die Geographie Klimageographie Klimaelemente Gliederung der Vorlesung 1. Physische Geographie 2. Geologie 3. Klima, Vegetation und Wasser 4. Pedologie / Bodengeographie 5. Geomorphologie
Grundlagen des Periodensystems der Elemente
 Aus der regelmäßigen Wiederholung ähnlicher Eigenschaften der Elemente leitete Mendelejew das Gesetz der Periodizität ab. Diese Periodizität liegt im Aufbau der Atomhülle begründet. Atomradius Als Atomradius
Aus der regelmäßigen Wiederholung ähnlicher Eigenschaften der Elemente leitete Mendelejew das Gesetz der Periodizität ab. Diese Periodizität liegt im Aufbau der Atomhülle begründet. Atomradius Als Atomradius
PRÜFBERICHT 1135405-836796
 Tel.: +49 (843) 79, Fax: +49 (843) 724 [@ANALYNR_START=836796] 2 LUXEMBOURG DOC-5-322989-DE-P PRÜFBERICHT 3545-836796 Indikatorparameter der Anlage 3 / EÜV / chemisch-technische und hygienische Parameter
Tel.: +49 (843) 79, Fax: +49 (843) 724 [@ANALYNR_START=836796] 2 LUXEMBOURG DOC-5-322989-DE-P PRÜFBERICHT 3545-836796 Indikatorparameter der Anlage 3 / EÜV / chemisch-technische und hygienische Parameter
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s 2 3p 6. Geben Sie isoelektronische Ionen zu den folgenden Atomen an
 Übung 05.11.13 Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 Ne / F - / O 2- / N 3- / Na + / Mg 2+ / Al 3+. Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s
Übung 05.11.13 Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 Ne / F - / O 2- / N 3- / Na + / Mg 2+ / Al 3+. Welches Element / Ion hat die Elektronenkonfiguration 1s 2 2s 2 2p 6 3s
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Inhaltsverzeichnis. Vorwort Zur Gestaltung des Buches
 Hans Rudolf Christen Struktur Stoff Reaktion Allgemeine und anorganische Chemie Sekundarstufe I 5401 Diesterweg Salle Frankfurt am Main Berlin München Verlag Sauerländer Aarau Vorwort Zur Gestaltung des
Hans Rudolf Christen Struktur Stoff Reaktion Allgemeine und anorganische Chemie Sekundarstufe I 5401 Diesterweg Salle Frankfurt am Main Berlin München Verlag Sauerländer Aarau Vorwort Zur Gestaltung des
Physikalische. Grundlagen. L. Kölling, Fw Minden
 Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden?
 41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
41. Welches der folgenden Elemente zeigt die geringste Tendenz, Ionen zu bilden? A) Ca B) C C) F D) Na 42. Steinsalz löst sich in Wasser, A) weil beide Ionen Hydrathüllen bilden können B) es eine Säure
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
CHEMIE KAPITEL 4 SÄURE-BASE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
0.3 Formeln, Gleichungen, Reaktionen
 0.3 Formeln, Gleichungen, Reaktionen Aussage von chemischen Formeln Formeln von ionischen Verbindungen - Metallkation, ein- oder mehratomiges Anion - Formel entsteht durch Ausgleich der Ladungen - Bildung
0.3 Formeln, Gleichungen, Reaktionen Aussage von chemischen Formeln Formeln von ionischen Verbindungen - Metallkation, ein- oder mehratomiges Anion - Formel entsteht durch Ausgleich der Ladungen - Bildung
7. Tag: Säuren und Basen
 7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
Das Chemische Gleichgewicht
 II. Gleichgewichte von Säuren S und Basen 13 Puffer-Lösungen Definition: Lösungen, die einen definierten ph-wert haben, der konstant bleibt, auch wenn Säuren S oder Basen in begrenzten Mengen zugesetzt
II. Gleichgewichte von Säuren S und Basen 13 Puffer-Lösungen Definition: Lösungen, die einen definierten ph-wert haben, der konstant bleibt, auch wenn Säuren S oder Basen in begrenzten Mengen zugesetzt
Ionenaustauscher. Von Vera Hickethier
 Ionenaustauscher Von Vera Hickethier Gliederung Ionenaustauscher, was ist das? - Stoffvielfalt der Ionenaustauscher - Aufbau von Ionenaustauschern Wie funktioniert ein Ionenaustauscher? Gleichgewichtsreaktion
Ionenaustauscher Von Vera Hickethier Gliederung Ionenaustauscher, was ist das? - Stoffvielfalt der Ionenaustauscher - Aufbau von Ionenaustauschern Wie funktioniert ein Ionenaustauscher? Gleichgewichtsreaktion
Verteilungskoeffizienten
 VL Limnochemie Verteilungskoeffizienten Sorption I Inhalt Verteilungskoeffizienten K H,K d, K OW, K OC, Rd Sorption I Begriffe und Definitionen Grundlagen Sorptive Sorbentien 1 VERTEILUNGS- KOEFFIZIENTEN
VL Limnochemie Verteilungskoeffizienten Sorption I Inhalt Verteilungskoeffizienten K H,K d, K OW, K OC, Rd Sorption I Begriffe und Definitionen Grundlagen Sorptive Sorbentien 1 VERTEILUNGS- KOEFFIZIENTEN
Eine Reaktionsgleichung beschreibt die Umwandlung von Stoffen (Atomen, Molekülen, Ionen etc.), also einen chemischen Prozess.
 Chemische Reaktionen 1. Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von toffen (Atomen, Molekülen, Ionen etc.), also einen chemischen Prozess. Auf der einen eite
Chemische Reaktionen 1. Was ist eine Reaktionsgleichung? Eine Reaktionsgleichung beschreibt die Umwandlung von toffen (Atomen, Molekülen, Ionen etc.), also einen chemischen Prozess. Auf der einen eite
Einheiten und Einheitenrechnungen
 Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Chemie für Studierende der Human- und Zahnmedizin WS 2013/14 Übungsblatt 1: allgemeine Chemie, einfache Berechnungen, Periodensystem, Orbitalbesetzung, Metalle und Salze Einheiten und Einheitenrechnungen
Versauerung und Kalk-Düngung
 Versauerung und Kalk-Düngung Zuviel Kalk macht reiche Väter - arme Söhne oder: nachlässige Vornutzer, arme Flächenübernehmer Kationenaustausch ph Wert Humusabbau: Ca 2+ macht die Nährstoffe für die Pflanze
Versauerung und Kalk-Düngung Zuviel Kalk macht reiche Väter - arme Söhne oder: nachlässige Vornutzer, arme Flächenübernehmer Kationenaustausch ph Wert Humusabbau: Ca 2+ macht die Nährstoffe für die Pflanze
Ionisierungsenergie und Elektronenaffinität. Bindigkeit Valenzstrichformel Molekülgeometrie
 Tendenzen im Periodensystem Ionisierungsenergie und Elektronenaffinität Atombindung (Elektronenpaarbindung) Bindigkeit Valenzstrichformel Molekülgeometrie Räumlicher Bau einfacher Moleküle Polare Atombindung
Tendenzen im Periodensystem Ionisierungsenergie und Elektronenaffinität Atombindung (Elektronenpaarbindung) Bindigkeit Valenzstrichformel Molekülgeometrie Räumlicher Bau einfacher Moleküle Polare Atombindung
Chemie Zusammenfassung III
 Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig?
 1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
1) Welche Aussagen über die Hauptgruppenelemente im Periodensystem sind richtig? 1) Es sind alles Metalle. 2) In der äußeren Elektronenschale werden s- bzw. s- und p-orbitale aufgefüllt. 3) Sie stimmen
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 [email protected] www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 [email protected] www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Ein Puffer ist eine Mischung aus einer schwachen Säure/Base und ihrer Korrespondierenden Base/Säure.
 2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
2.8 Chemische Stoßdämpfer Puffersysteme V: ph- Messung eines Gemisches aus HAc - /AC - nach Säure- bzw Basen Zugabe; n(naac) = n(hac) > Acetat-Puffer. H2O Acetat- Puffer H2O Acetat- Puffer Die ersten beiden
Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13
 Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Periodensystem der Elemente - PSE
 Periodensystem der Elemente - PSE Historische Entwicklung Möglichkeiten der Reindarstellung seit 18. Jhdt. wissenschaftliche Beschreibung der Elemente 1817 Johann Wolfgang Döbereiner: ähnliche Elemente
Periodensystem der Elemente - PSE Historische Entwicklung Möglichkeiten der Reindarstellung seit 18. Jhdt. wissenschaftliche Beschreibung der Elemente 1817 Johann Wolfgang Döbereiner: ähnliche Elemente
Bodenfruchtbarkeit/Nährstoffdynamik im Boden Univ.Lek.DI Hans Unterfrauner
 Bodenfruchtbarkeit/Nährstoffdynamik im Boden Univ.Lek.DI Hans Unterfrauner Inhalt Bodenfruchtbarkeit Erfassen Zusammensetzung von Pflanzen und Böden Interaktionen von Nährelementen Dynamik in Böden Phosphorkreislauf
Bodenfruchtbarkeit/Nährstoffdynamik im Boden Univ.Lek.DI Hans Unterfrauner Inhalt Bodenfruchtbarkeit Erfassen Zusammensetzung von Pflanzen und Böden Interaktionen von Nährelementen Dynamik in Böden Phosphorkreislauf
Pflanz en und ihre ph-vorlieben
 Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
10. Klasse / Infoblatt 1. Grundwissen: Periodensystem
 Grundwissen: Periodensystem Metalle / Metallcharakter Nichtmetalle / Nichtmetallcharakter Elektronenaffinität Reaktivität der Halogene Reaktivität der Alkalimetalle 10. Klasse / Infoblatt 1 Eigenschaft
Grundwissen: Periodensystem Metalle / Metallcharakter Nichtmetalle / Nichtmetallcharakter Elektronenaffinität Reaktivität der Halogene Reaktivität der Alkalimetalle 10. Klasse / Infoblatt 1 Eigenschaft
Grundwasser: chemische Vorgänge bei der Infiltration. Redoxprozesse im Grundwasser Transport reaktiver Spezies
 Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Themengebiet: 1 HA + H 2 O A - + H 3 O + H 3 O + : Oxonium- oder Hydroxoniumion. Themengebiet: 2 B + H 2 O BH + + OH - OH - : Hydroxidion
 1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
Kompendium der allgemeinen und anorganischen Chemie
 Kompendium der allgemeinen und anorganischen Chemie Von Dr. rer. nat. habil. Peter Hermann Wissenschaftlicher Oberassistent am Physiologisch-Chemischen Institut der Martin-Luther-Universität Halle-Wittenberg
Kompendium der allgemeinen und anorganischen Chemie Von Dr. rer. nat. habil. Peter Hermann Wissenschaftlicher Oberassistent am Physiologisch-Chemischen Institut der Martin-Luther-Universität Halle-Wittenberg
Annette-Kolb-Gymnasium Traunstein Grundwissen der 9. Klasse für das Fach Chemie Aufgaben und Antworten
 1 Erkläre den Aufbau von Atomen und Ionen aus den Elementarteilchen: (Bsp. 23 Na, 1 H, 35 Cl - ). 2 Erläutere den Beriff Edelaskonfiuration und beschreibe, welche verschiedenen Mölichkeiten die Elemente
1 Erkläre den Aufbau von Atomen und Ionen aus den Elementarteilchen: (Bsp. 23 Na, 1 H, 35 Cl - ). 2 Erläutere den Beriff Edelaskonfiuration und beschreibe, welche verschiedenen Mölichkeiten die Elemente
Werkstoffkunde Chemische Bindungsarten
 Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
Folie 1/27 Die Elektronen auf der äußersten Schale eines Atoms (Außenelektronen oder Valenzelektronen genannt) bestimmen maßgeblich die chemischen Eigenschaften. Jedes Atom hat dabei das Bestreben die
IONENAUSTAUSCH FÜR LAIEN
 IONENAUSTAUSCH FÜR LAIEN Eine Einführung Wasser Wasser ist eine Flüssigkeit. Wasser besteht aus Wassermolekülen (Formel H 2 O). Alle natürlichen Gewässer enthalten Fremdsubstanzen, gewöhnlich in kleinen
IONENAUSTAUSCH FÜR LAIEN Eine Einführung Wasser Wasser ist eine Flüssigkeit. Wasser besteht aus Wassermolekülen (Formel H 2 O). Alle natürlichen Gewässer enthalten Fremdsubstanzen, gewöhnlich in kleinen
Bodenkunde und Meteorologie
 Modulkatalog Modulverantwortlich Prof. Dr. H.-H. Modulart Pflicht Angebotshäufigkeit Winter Regelbelegung / Empf. Semester 1. Semester Credits (ECTS) 4 Leistungsnachweis Prüfungsleistung Angeboten in der
Modulkatalog Modulverantwortlich Prof. Dr. H.-H. Modulart Pflicht Angebotshäufigkeit Winter Regelbelegung / Empf. Semester 1. Semester Credits (ECTS) 4 Leistungsnachweis Prüfungsleistung Angeboten in der
Musterprüfung Welche der Elemente Lithium, Kohlenstoff, Wasserstoff, Sauerstoff, Magnesium, Aluminium und Calcium sind Nichtmetalle?
 Module: Atombau und Periodensystem Chemische Bindungen Chemische Reaktionen 1 Musterprüfung 1. Teil: Atombau und Periodensystem 1.1. Welche Art von Teilchen befinden sich a) im Atomkern b) in der Elektronenhülle
Module: Atombau und Periodensystem Chemische Bindungen Chemische Reaktionen 1 Musterprüfung 1. Teil: Atombau und Periodensystem 1.1. Welche Art von Teilchen befinden sich a) im Atomkern b) in der Elektronenhülle
Allgemeine und anorganische Chemie. Chemie ist die Lehre von den Stoffen und den stofflichen Veränderungen.
 Allgemeine und anorganische Chemie 1. Inhalte und Aufgaben der Chemie - Chemische Grundbegriffe Chemie ist die Lehre von den Stoffen und den stofflichen Veränderungen. Chemische Verbindungen setzen sich
Allgemeine und anorganische Chemie 1. Inhalte und Aufgaben der Chemie - Chemische Grundbegriffe Chemie ist die Lehre von den Stoffen und den stofflichen Veränderungen. Chemische Verbindungen setzen sich
Bundesrealgymnasium Imst. Chemie Klasse 7. Säuren und Basen
 Bundesrealgymnasium Imst Chemie 2010-11 Klasse 7 Säuren und Basen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Bundesrealgymnasium Imst Chemie 2010-11 Klasse 7 Säuren und Basen Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff detaillierter
Wie kommen Metalle vor? CaO, MgO, Al 2 O 3, CaCO 3, CaSO 4 vs. Cu 2 S, HgS, PbS. Welche Kombinationen führen zu hohen Oxidationsstufen?
 HSAB-Prinzip Wie kommen Metalle vor? CaO, MgO, Al 2 O 3, CaCO 3, CaSO 4 vs. Cu 2 S, HgS, PbS Welche Kombinationen führen zu hohen Oxidationsstufen? XeO 6 4, ClO 4, MnO 4, MnS 4, ClS 4 Warum entsteht der
HSAB-Prinzip Wie kommen Metalle vor? CaO, MgO, Al 2 O 3, CaCO 3, CaSO 4 vs. Cu 2 S, HgS, PbS Welche Kombinationen führen zu hohen Oxidationsstufen? XeO 6 4, ClO 4, MnO 4, MnS 4, ClS 4 Warum entsteht der
-1 (außer in Verbindung mit Sauerstoff: variabel) Sauerstoff -2 (außer in Peroxiden: -1)
 1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1. Bsp.: Grundwissen 9.Klasse NTG 2 Grundwissen 9.Klasse NTG 2
 Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1 Die Stoffmenge n = 1mol ist die Stoffportion, die 6,022 10 23 Teilchen enthält. Die Stoffmenge n n(he) = 1 mol n(h 2 ) = 1 mol enthält 6,022 10 23
Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1 Die Stoffmenge n = 1mol ist die Stoffportion, die 6,022 10 23 Teilchen enthält. Die Stoffmenge n n(he) = 1 mol n(h 2 ) = 1 mol enthält 6,022 10 23
Grundwissenkarten Hans-Carossa-Gymnasium. 9. Klasse. Chemie SG
 Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa-Gymnasium 9. Klasse Chemie SG Es sind insgesamt 18 Karten für die 9. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Unterschied zwischen Physik und Chemie:
 Unterschied zwischen Physik und Chemie: Der Begriff Physik bezeichnet die Lehre über Zustände und Zustandsänderungen die Chemie hingegen beschäftigt sich mit Stoffen und stofflichen Veränderungen. Unterteilung
Unterschied zwischen Physik und Chemie: Der Begriff Physik bezeichnet die Lehre über Zustände und Zustandsänderungen die Chemie hingegen beschäftigt sich mit Stoffen und stofflichen Veränderungen. Unterteilung
1.5 Säuren und Basen und der ph-wert
 Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
n = V Lsg m n l mol Grundwissen 9. Klasse Chemie (NTG) Analytische Chemie Stoffmenge n Molare Masse M Molares Volumen V M Stoffmengenkonzentration c
 Grundwissen 9. Klasse Chemie (NTG) 1. Analytische Chemie und Stöchiometrie Analytische Chemie Untersuchung von Reinstoffen und Stoffgemischen mit dem Ziel diese eindeutig zu identifizieren (= qualitativer
Grundwissen 9. Klasse Chemie (NTG) 1. Analytische Chemie und Stöchiometrie Analytische Chemie Untersuchung von Reinstoffen und Stoffgemischen mit dem Ziel diese eindeutig zu identifizieren (= qualitativer
Trinkwasserbeschaffenheit 2015 zu den Entnahmestellen - Trinkwasser - des Auftraggebers Stadtwerke Schnaudertal - Eigenbetrieb der Stadt Meuselwitz
 colif. Keime E.-coli bakteriologische Untersuchungsparameter Entero kokken Kolonie zahl 22 C organoleptische und andere hygienisch relevante Kolonie zahl 36 C Trübung Färbung Geruch/ Geschmack Geruch (TON)
colif. Keime E.-coli bakteriologische Untersuchungsparameter Entero kokken Kolonie zahl 22 C organoleptische und andere hygienisch relevante Kolonie zahl 36 C Trübung Färbung Geruch/ Geschmack Geruch (TON)
Grundtypen der Bindung. Grundtypen chemischer Bindung. Oktettregel. A.8.1. Atombindung
 Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Grundtypen der Bindung Grundtypen chemischer Bindung Oktettregel A.8.1. Atombindung 1 A.8.1 Atombindung Valenz (Zahl der Bindungen) Atombindung auch: kovalente Bindung, ElektronenpaarBindung Zwei Atome
Säure/Base - Reaktionen. 6) Titration starker und schwacher Säuren/Basen. Elektrolytische Dissoziation. AB(aq)
 Säure/Base - Reaktionen 1) Elektrolytische Dissoziation ) Definitionen Säuren Basen ) Autoprotolyse 4) p- und po-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Säure/Base - Reaktionen 1) Elektrolytische Dissoziation ) Definitionen Säuren Basen ) Autoprotolyse 4) p- und po-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
2. Schreiben Sie für folgende Atome das Bohrsche Atommodell auf. a) Aluminium
 Übungsaufgaben 1.Seminar Atome 1. Ergänzen Sie die nachfolgende Tabelle Elementsymbol Elementname Ordnungszahl Massenzahl Bsp. H Wasserstoff 1 1 He Au 7 56 2. Schreiben Sie für folgende Atome das Bohrsche
Übungsaufgaben 1.Seminar Atome 1. Ergänzen Sie die nachfolgende Tabelle Elementsymbol Elementname Ordnungszahl Massenzahl Bsp. H Wasserstoff 1 1 He Au 7 56 2. Schreiben Sie für folgende Atome das Bohrsche
Praktikumsrelevante Themen
 Praktikumsrelevante Themen RedoxReaktionen Aufstellen von Redoxgleichungen Elektrochemie Quantitative Beschreibung von RedoxGleichgewichten Redoxtitrationen 1 Frühe Vorstellungen von Oxidation und Reduktion
Praktikumsrelevante Themen RedoxReaktionen Aufstellen von Redoxgleichungen Elektrochemie Quantitative Beschreibung von RedoxGleichgewichten Redoxtitrationen 1 Frühe Vorstellungen von Oxidation und Reduktion
Grundlagen. Maximilian Ernestus Waldorfschule Saarbrücken
 Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Elektronenpaarbindung (oder Atombindung) Nichtmetallatom + Nichtmetallatom Metallatom + Nichtmetallatom 7. Welche Bindungsart besteht jeweils?
 LÖSUNGEN Probetest 1 Kap. 03 Theorie Name: 1. C = Kohlenstoff Ag = Silber Br = Brom Schwefel = S Lithium = Li Uran = U 2. Aluminium - Finde die richtigen Zahlen mit Hilfe deines PSE: Massenzahl: 27 Ordnungszahl:
LÖSUNGEN Probetest 1 Kap. 03 Theorie Name: 1. C = Kohlenstoff Ag = Silber Br = Brom Schwefel = S Lithium = Li Uran = U 2. Aluminium - Finde die richtigen Zahlen mit Hilfe deines PSE: Massenzahl: 27 Ordnungszahl:
Biochemische Übungen
 Dr. Arnulf Hartl Biochemische Übungen Proteine Tag 1: Tag 2: Tag 3: Konzentrieren Denaturierende und native Fällungen Protein Konzentrationsbestimmung Entsalzen Gelchromatographie Dialyse Elektrophorese
Dr. Arnulf Hartl Biochemische Übungen Proteine Tag 1: Tag 2: Tag 3: Konzentrieren Denaturierende und native Fällungen Protein Konzentrationsbestimmung Entsalzen Gelchromatographie Dialyse Elektrophorese
1.3 Chemische Reaktionen des Wassers - Bildung von Säuren und Basen
 1.3 Chemische Reaktionen des Wassers Bildung von Säuren und Basen Säure und Basebegriff nach Arrhenius (1887) Wasser reagiert mit Nichtmetalloxiden (Säureanhydriden) zu Säuren. Die gebildete Säure löst
1.3 Chemische Reaktionen des Wassers Bildung von Säuren und Basen Säure und Basebegriff nach Arrhenius (1887) Wasser reagiert mit Nichtmetalloxiden (Säureanhydriden) zu Säuren. Die gebildete Säure löst
Natürliche ökologische Energie- und Stoffkreisläufe
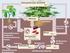 Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie
 Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Säuren und Basen Säure-Base-Konzepte Säure-Base-Gleichgewichte Säurestärke, Basenstärke ph-, poh-, pk-werte Pufferlösungen Titrationen 1 Säure-Base-Definition nach ARRHENIUS
Praktikumsrelevante Themen Säuren und Basen Säure-Base-Konzepte Säure-Base-Gleichgewichte Säurestärke, Basenstärke ph-, poh-, pk-werte Pufferlösungen Titrationen 1 Säure-Base-Definition nach ARRHENIUS
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch
 Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
Toll! Wir wissen nun eine Menge über den Bau von Atomen. Wir können Infos über Elemente aus dem PSE ablesen. Aber als Chemiker wollen wir auch Verbindungen untersuchen, ihre Zusammensetzung verstehen und
CHEMIE KAPITEL 4 SÄURE- BASE. Timm Wilke. Georg- August- Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper [email protected] Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kinetik Reaktionsgeschwindigkeit Konzentrationsabhängigkeit
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper [email protected] Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Was bislang geschah Kinetik Reaktionsgeschwindigkeit Konzentrationsabhängigkeit
Film der Einheit DA-Prinzip
 3.Teil DA-Prinzip Film der Einheit DA-Prinzip Säuren und Basen im Alltag Eigenschaften Unterschiedliche Definitionen des Säurebegriffs Säure-Base Konzept nach Brönsted DA-Prinzip bei Protolysen und Redoxreaktionen
3.Teil DA-Prinzip Film der Einheit DA-Prinzip Säuren und Basen im Alltag Eigenschaften Unterschiedliche Definitionen des Säurebegriffs Säure-Base Konzept nach Brönsted DA-Prinzip bei Protolysen und Redoxreaktionen
Alle Stoffe bestehen aus kleinen Teilchen, die sich bewegen. Je mehr Energie sie besitzen, desto mehr bewegen sie sich.
 Grundwissen 8. Klasse 1. Stoffe und Teilchen Teilchenmodell: Atome Ionen Alle Stoffe bestehen aus kleinen Teilchen, die sich bewegen. Je mehr Energie sie besitzen, desto mehr bewegen sie sich. von atomos
Grundwissen 8. Klasse 1. Stoffe und Teilchen Teilchenmodell: Atome Ionen Alle Stoffe bestehen aus kleinen Teilchen, die sich bewegen. Je mehr Energie sie besitzen, desto mehr bewegen sie sich. von atomos
Das chemische Gleichgewicht
 1 Grundlagen Viele Substanzen sind in Wasser praktisch nicht löslich, l d.h. sie sind nur sehr geringfügig gig löslich. (Tatsächlich nicht lösliche Stoffe gibt es nicht! Schwerlösliche Verbindungen In
1 Grundlagen Viele Substanzen sind in Wasser praktisch nicht löslich, l d.h. sie sind nur sehr geringfügig gig löslich. (Tatsächlich nicht lösliche Stoffe gibt es nicht! Schwerlösliche Verbindungen In
Chemische Grundbegriffe
 Chemische Grundbegriffe Arbeitsauftrag: 1. Lesen Sie sich jedes Kapitel einzeln auf dem Textblatt genau durch. 2. Lesen Sie die zu den Kapiteln die Fragen ganz genau durch. 3. Lösen Sie die Aufgaben zu
Chemische Grundbegriffe Arbeitsauftrag: 1. Lesen Sie sich jedes Kapitel einzeln auf dem Textblatt genau durch. 2. Lesen Sie die zu den Kapiteln die Fragen ganz genau durch. 3. Lösen Sie die Aufgaben zu
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Fällungsreaktion. Flammenfärbung. Fällungsreaktion:
 2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
2 Fällungsreaktion: 2 Fällungsreaktion Entsteht beim Zusammengießen zweier Salzlösungen ein Niederschlag eines schwer löslichen Salzes, so spricht man von einer Fällungsreaktion. Bsp: Na + (aq) + Cl -
Säuren, Basen, Salze
 Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Bauchemie 1. 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle?
 Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
MAGNESIUM. 1. Bei Verbrennungsreaktionen entstehen in der Regel (kreuze richtig an):
 MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
Teilchenmodell. Aggregatzustände. Diffusion. Spezifische Eigenschaften = Stoffeigenschaften
 Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser Bewegung (Brownsche Bewegung),
Teilchenmodell (1) Alle Stoffe bestehen aus kleinsten Teilchen. (2) Zwischen den Teilchen wirken Anziehungskräfte. (3) Alle Teilchen befinden sich in ständiger, regelloser Bewegung (Brownsche Bewegung),
