Phänomenologie des Schwefels
|
|
|
- Wilfried Hans Stein
- vor 6 Jahren
- Abrufe
Transkript
1 Berufsbegleitendes Ärzteseminar für Anthroposophische Medizin (BÄfAM) Phänomenologie des Schwefels Andreas Müller
2 Schwefel Schwefel Element - Bedeutung in verschiedenen Bereichen der Natur Wirkt dort dem äußeren Blick verborgen in allen dynamischen Prozessen Sondert sich manchmal aus diesen Prozessen ab und erscheint dann als helle gelbe Substanz Andreas Müller
3 nadelige Schwefelkristalle an einer Fumarole in der Nähe des Vulkans Krafla Fumarole: vulkanische Exhalation heiße Gas- u. Dampfaustrittsstelle Andreas Müller
4 dampfende Schwefel-Fumarole auf White Island in Neuseeland Solfatare: Ausscheidung von Schwefelverbindungen Andreas Müller
5 Vorkommen vor allem in der Umgebung von Vulkanen Ursprung in der Tiefe der Erde (Hitze u. große Beweglichkeit) als SO2 ( Sulfate) oder als H2S ( Sulfide) elementar aus geschmolzenem Schwefel Metallsulfide: Daraus Metall und Schwefel durch atmosphärische o. geol. Einflüsse freigesetzt Stoffwechsel der Erde AS, Peptide, Proteine, organische Thioverbindungen u. deren Zerfallsprodukte Andreas Müller
6 Schwefelkreislauf Andreas Müller
7 Tiefsee Hot spot - Black smoker
8 Pflanze: Schwefel Biochemie Schwefel (aus Sulfat) strömt rasch in die stoffwechselaktiven wachsenden Gewebe initiiert die Proteinsynthese bzw. unterhält diese ermöglicht und stabilisiert die Eiweißgestalt macht Membranlipide der Chloroplasten flüssig beweglich über funktionale SH-Gruppen in zahlreichen Enzymen an allen bedeutenden Stoffwechselvorgängen beteiligt, einschließlich der Fotosynthese Andreas Müller
9 Schwefel Biochemie Tier und Mensch: zusätzlich zu angesprochenen allgemeinen Stoffwechselwirkungen Stabilisierung und Entgiftung der Erythrozyten (Glutathion) Beteiligung an weiteren Aufbau- und Ausscheidungsvorgängen (Sulfatierung) Bildung schwefelsauerer Proteoglykane (Bindegewebsgrundsubstanz) Andreas Müller
10 Schwefel Gewinnung Abbau vulkanischer Lagerstätten Aus der Röstung von Metallsulfiden als SO 2 Aus der Rauchgas-Entschwefelung Aus Tiefen zwischen m durch überhitzten Wasserdampf an die Oberfläche pressen (Frasch-Verfahren) Tiefenschwefel aus Gips oder Anhydrit (reduktiv durch Bakterien entstanden) Andreas Müller
11 Schwefel Substanzbetrachtung Was zeigt sich von außen in der physischen Erscheinung und den physikalischen Tatsachen? Hellgelbe, durchscheinende Materie wird durch klare Formen der rhombischen Kristalle begrenzt Im Gelb wirkt die Tendenz des sich- Ausweitens und Verströmens (Geruch) Gelb hat Qualität von Wärme Andreas Müller
12 Schwefel die Bedeutung verinnerlichter Wärme Wahrnehmungen weisen auf besonderen Sachverhalt hin: Wärme durchwirkt die Substanz bis in die äußerste Erscheinung Latente Wärme zeigt sich bei chemischen Reaktionen im Freiwerden Bei äußerer Wärmezufuhr gibt der Schwefel schnell äußere Form auf Flüssiger Zustand Andreas Müller
13 Schwefel die Bedeutung verinnerlichter Wärme Smp.: 112,8 C nicht intensiv im festen kristallinen Zustand zeigt sich auch in der geringen Härte (1,5 2) Gitterenergie geringer als bei allen anderen festen Elementen Verdichtende Kräfte wenig ausgeprägt: Spezifisches Gewicht 2,07 g/cm³ Schlechter Wärmeleiter (hält Wärme fest), deswegen am leichtesten erwärmbar unter festen Substanzen Schwefel (nach P, Na und K) das feste Element mit stärkster Wärmeausdehnung Andreas Müller
14 Schwefel die Bedeutung verinnerlichter Wärme Bis 95 C: rhombische Anordnung S8: α-schwefel Zwischen 95 C und 112,8 C (S-temp.): monoklin, S8: β-schwefel Bei 160 C steigt die Viskosität des Schwefels auf das 1000fache an: Die S8-Ringe verbinden sich untereinander und es entstehen Polymere bis zu S-Atomen: μ-schwefel Zwischen 200 C und 250 C: Schwefel besitzt die größte Zähigkeit Formmetamorphose Gießt man die Flüssigkeit in kaltes Wasser: Plastischer Schwefel Ab 250 C: Abnahme der Zähigkeit: λ-s 445 C: Siedetemperatur des Schwefels: Ketten werden gespalten (S8 S2) Andreas Müller
15 Schwefel die Bedeutung verinnerlichter Wärme T e m p e r a t u r S2 - violett S3 - blau S4 - kirschrot S5 - orangerot S6 - orangegelb S7 - intensiv gelb S8 - gelb Kein Phänomen, in dem sich das Wesen des Schwefels deutlicher äußert als in der Wandelbarkeit in den Modifikationen Sn - braun n > 8 Schwefel als das Element, bei dem die Wärme wie bei keinem anderen Element bildend tätig ist Andreas Müller
16 Schwefel die Bedeutung verinnerlichter Wärme Latente innere Wärme wird bei exothermen Reaktionen frei Wärme bestimmende Kraft Haupteigenschaft: Begibt sich leicht in die Sphäre feuriger Luft Sulfur = sol-fer = Träger besonderer Kräfte, die denen der Sonne entsprechen Tria prinzipia: Sal Merkur Sulfur Sulfur ist Träger der Imponderabilien Andreas Müller
17 Schwefel Abstieg in den Sal-Zustand Verbrennung: Entzündung bei C wenig Licht, viel Wärme S + O2 SO2 + 70,9 kcal Entsteht stechend riechendes Gas, das den Schwefel verzehrt Gasförmiger Zustand SO2 = Wirksamkeit des Sauerstoffs stechender Geruch SO2 : zeigt aktiven Charakter des Schwefels und innere Hitze Andreas Müller
18 Salinischer Prozess Schwefel Abstieg in den Sal-Zustand SO2 + H2O H2SO3 (Schwefelige Säure) SO2 nur in Wasser gelöst Wärme SO2 + ½ O2 SO3 + 23,5 kcal (= weitere Verringerung der immanenten Wärme; Kräfte des Verdichtens ) führen zum SO3 SO3 + H2O H2SO4 (Schwefelsäure) + 21 kcal Schwefeltrioxid saugt das Wasser in sich auf Oleum, Vitriolöl stark hygroskopisch Verdünnen unter weiterer großer Wärmeabgabe Andreas Müller
19 Schwefel Sulfate = Vitriole Salze der Schwefelsäure Abstieg in den erstarrten mineralischen Zustand Pflanzen: Zur Schwefelaufnahme angewiesen Kristallwasserhaltige Sulfate = Rest der Wirksamkeit der Glutnatur des Schwefels saugt noch Wasser CaSO4 2 H2O Gips, Marienglas CaSO4 Anhydrit MgSO4 H2O Kieserit SrSO4 Colestin MgSO4 7 H2O Epsomit, Bittersalz BaSO4 Schwerspat Na2SO4 10H2O Mirabilit, Glaubersalz PbSO4 Anglesit FeSO4 7 H2O Melanterit CuSO 4 5 H2O Chalkantit Andreas Müller
20 Gips, Gipsspat, Calciumsulfat = Ca[SO 4 ] 2H Andreas Müller O
21 Anhydrit, Anhydritspat = CaSO4
22 Epsomit, Bittersalz, Magnesiumsulfat-Heptahydrat Mg[SO 4 ] 7H 2 O Andreas Müller 2011
23 Mirabilit; natürliches Glaubersalz Na 2 [SO 4 ] 10H 2 O
24 Melanterit, Eisenvitriol wasserhaltiges Eisen(II)-sulfat Fe[SO 4 ] 7H 2 O
25 Chalkantit Wasserhaltiges Kupfer(II)-sulfat CuSO 4 5 H 2 O
26 Schwefel Sulfate = Vitriole Vitriol Visita interiora terrae, rectificando invenies occultum lapidem Besuchst du das Innere der Erde, wirst du durch Destillation (Läuterung) einen verborgenen Stein (Schatz) finden Andreas Müller
27 Schwefel Schwefelwasserstoff = H2S Entstehung: Fäulnis, Vulkanismus, Hotspots Allgegenwärtig (Anlaufen von Silber) Eigenschaft: starke Affinität zu den Metallen Kiese, Glanze und Blenden Bleisulfid (Galenit, Bleiglanz) Silbersulfid (Akanthit, Sliberglanz) Quecksilbersulfid (Zinnober, Cinnabarit, Mercurblende) Kupfer(I)-sulfid (Chalkosin, Kupferglanz) Kupfer(II)-sulfid (Covellin, Kupferindig) Eisen(II)-sulfid (Pyrit, Schwefelkies, Markasit) Zinksulfid (Sphalerit, Zinkblende) Arsensulfid (Realgar, Rubinschwefel) Antimonsulfid (Stibnit, Grauspießglanz) Andreas Müller
28 Galenit, Bleiglanz, Blei(II)-sulfid = PbS auf Kalkspat mit Quarz
29 Akanthit, Silberglanz = Ag 2 S
30 Covellin, Kupferindig, Kupfer(II)-sulfid = CuS
31 Cinnabarit, Zinnober Merkurblende Quecksilber(II)-sulfid HgS
32 Pyrit, Schwefelkies Eisen(II)-disulfid = FeS 2
33 Stibnit; Grauspießglanz Sb 2 S 3
34 Schwefel die Bedeutung verinnerlichter Wärme Schwefelaufstieg zum H2S Aufschließen gegenüber dem kosmischen Umkreis H2 + S (fest) H2S + 4,76 kcal (gering) Die im Schwefel und im Wasserstoff verinnerlichte Wärme bleibt nahezu vollständig erhalten H2S: sulfurisches Prinzip erreicht höchste Intensität Andreas Müller
35 Schwefel die Bedeutung verinnerlichter Wärme H2S Schwefelaufstieg: R S-H Eingliederung in das Leben; ( H 2 S Sulfide) Schwefel +O2 SO2 Wärme + O2 SO3 Wärme Mikroorganismen, Verwitterung + H2O H2SO4 Wärme + H2O verdünnte H2SO4 Wärme + NaOH Na2SO4 Wärme Schwefelabstieg: SO 4 2- Aussonderung aus dem Leben und Beginn neuen Lebens Andreas Müller
36 Schwefel im Organischen Der Stickstoff hat aber, indem er wirkt im Naturwesen..vier Geschwister.. Es sind die vier Geschwister: Kohlenstoff, Sauerstoff, Wasserstoff und Schwefel. Wenn man die vollständige Bedeutung des Eiweißes kennen lernen will,.muss man den für das Eiweiß in einer tiefbedeutsamen Weise tätigen Stoff, den Schwefel mit anführen. Denn der Schwefel ist gerade dasjenige innerhalb des Eiweißes, was den Vermittler darstellt zwischen dem überall in der Welt ausgebreiteten Geistigen, zwischen der Gestaltungskraft des Geistigen und dem Physischen GA 327 Geisteswissenschaftliche Grundlagen zum Gedeihen der Landwirtschaft Dritter Vortrag: Koberwitz 11. Juni 1924 Andreas Müller
37
38 Schwefel die Bedeutung immaneter Wärme.wer in der materiellen Welt die Spuren verfolgen will, die der Geist zieht, der muss die Tätigkeit des Schwefels verfolgen GA 327 Geisteswissenschaftliche Grundlagen zum Gedeihen der Landwirtschaft; Dritter Vortrag: Koberwitz 11. Juni 1924 Andreas Müller
39 Kristalliner Schwefel Kristalliner Schwefel Blaue Schwefelflamme Amorpher Schwefel in Stangen Monokliner Schwefel aus Teidekrater
Philipps Universität Marburg Fachbereich 15: Chemie Experimentalvortrag Dozenten: Dr. Philipp Reiß Prof. Dr. Bernhard Neumüller
 Philipps Universität Marburg Fachbereich 15: Chemie Experimentalvortrag Dozenten: Dr. Philipp Reiß Prof. Dr. Bernhard Neumüller Referent: Martin Stolze Inhaltsverzeichnis 1. Zustandsformen 2. Vorkommen
Philipps Universität Marburg Fachbereich 15: Chemie Experimentalvortrag Dozenten: Dr. Philipp Reiß Prof. Dr. Bernhard Neumüller Referent: Martin Stolze Inhaltsverzeichnis 1. Zustandsformen 2. Vorkommen
Eigenschaften der Elemente der 16. Gruppe
 Eigenschaften der Elemente der 16. Gruppe Vorkommen: S_Schwefel elementar Sulfate CaSO 4, BaSO 4, Sulfide Kiese (z.b. FeS 2 ) Glanze (z.b. PbS) Blenden (z.b. ZnS) in Erdöl, Erdgas; in Steinkohle Kokereigas
Eigenschaften der Elemente der 16. Gruppe Vorkommen: S_Schwefel elementar Sulfate CaSO 4, BaSO 4, Sulfide Kiese (z.b. FeS 2 ) Glanze (z.b. PbS) Blenden (z.b. ZnS) in Erdöl, Erdgas; in Steinkohle Kokereigas
Schwefel. Abb. 1 Schwefel in Pulverform [1]
![Schwefel. Abb. 1 Schwefel in Pulverform [1] Schwefel. Abb. 1 Schwefel in Pulverform [1]](/thumbs/25/6178710.jpg) Universität Regensburg Naturwissenschaftliche Fakultät IV Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Wintersemester 2009/2010 27.11.2009 Betreuung: Dr.
Universität Regensburg Naturwissenschaftliche Fakultät IV Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvorträge im Wintersemester 2009/2010 27.11.2009 Betreuung: Dr.
Schwefel. 1. Das Element Schwefel
 Universität Regensburg Naturwissenschaftliche Fakultät IV Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2010 07.07.2010 Betreuung: Dr. M. Andratschke
Universität Regensburg Naturwissenschaftliche Fakultät IV Institut für Anorganische Chemie - Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2010 07.07.2010 Betreuung: Dr. M. Andratschke
Übungen zur Allgemeinen Geologie, Nebenfach. Erta Ale, Afrika
 Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Übungen zur Allgemeinen Geologie, Nebenfach Erta Ale, Afrika Minerale anorganisch, (natürlich) Festkörper definierte chemische Zusammensetzung homogen definiert durch chemische Formel kristallin Physikalische
Schwefelsäureherstellung
 Frederike Wolfering Anne Warrink Wolfering/Warrink 1 Inhalt Allgemeines Geschichte Herstellungsverfahren Großtechnische Herstellung Zusammenfassung Wolfering/Warrink 2 Allgemeines zur Schwefelsäure nach
Frederike Wolfering Anne Warrink Wolfering/Warrink 1 Inhalt Allgemeines Geschichte Herstellungsverfahren Großtechnische Herstellung Zusammenfassung Wolfering/Warrink 2 Allgemeines zur Schwefelsäure nach
Die Herstellung von Schwefelsäure. Vortrag Sommersemester 08
 Anorganische Chemie I Die Herstellung von Schwefelsäure Anorganische Chemie I I Vortrag Sommersemester 08 Sommersemester 08 14.04.2008 1 Überblick Einleitung Geschichte alte Herstellungsverfahren moderne
Anorganische Chemie I Die Herstellung von Schwefelsäure Anorganische Chemie I I Vortrag Sommersemester 08 Sommersemester 08 14.04.2008 1 Überblick Einleitung Geschichte alte Herstellungsverfahren moderne
Lösungen Thema: Stoffe und ihre Eigenschaften
 Lösungen Thema: Stoffe und ihre Eigenschaften zu 1: Siedetemperatur, Schmelztemperatur, Dichte (Löslichkeit) zu 2: Brennbarkeit, Härte, Löslichkeit, Farbe, Geruch zu 3: zu 4: Bei der Flüssigkeit handelt
Lösungen Thema: Stoffe und ihre Eigenschaften zu 1: Siedetemperatur, Schmelztemperatur, Dichte (Löslichkeit) zu 2: Brennbarkeit, Härte, Löslichkeit, Farbe, Geruch zu 3: zu 4: Bei der Flüssigkeit handelt
Fossile Rohstoffe. Kohlenwasserstoffe als Energieträger
 nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
nwasserstoffe als Energieträger Erdöl,, Erdgas und Torf sind im Laufe von Millionen von Jahren aus Kleinlebwesen und Pflanzen entstanden und werden deswegen als fossile Energieträger bezeichnet. Da sie
1.11 Welcher Stoff ist es?
 L *** 1.11 Welcher Stoff ist es? Didaktisch-methodische Hinweise Im Arbeitsblatt wird der Versuch des Lösens von vier verschiedenen Salzen in Wasser in einem Labor beschrieben. Aus Zahlenangaben müssen
L *** 1.11 Welcher Stoff ist es? Didaktisch-methodische Hinweise Im Arbeitsblatt wird der Versuch des Lösens von vier verschiedenen Salzen in Wasser in einem Labor beschrieben. Aus Zahlenangaben müssen
Einführung in die Geologie
 Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke International Geothermal Centre Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und
Einführung in die Geologie Teil 4: Minerale - Baustoffe der Gesteine Prof. Dr. Rolf Bracke International Geothermal Centre Lennershofstraße 140 44801 Bochum Übersicht Definition der Minerale Minerale und
Lösungen Kap. 4 Die chemische Reaktion
 Elemente Grundlagen der Chemie für Schweizer Maturitätsschulen Klett und Balmer Verlag Zug 2007 Verwendung für den Gebrauch in der eigenen Klasse gestattet Lösungen Kap. 4 Die chemische Reaktion Lösungen
Elemente Grundlagen der Chemie für Schweizer Maturitätsschulen Klett und Balmer Verlag Zug 2007 Verwendung für den Gebrauch in der eigenen Klasse gestattet Lösungen Kap. 4 Die chemische Reaktion Lösungen
Stöchiometrie. (Chemisches Rechnen)
 Ausgabe 2007-10 Stöchiometrie (Chemisches Rechnen) ist die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen sowie der Mengenverhältnisse der beteiligten Stoffe bei chemischen Reaktionen
Ausgabe 2007-10 Stöchiometrie (Chemisches Rechnen) ist die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen sowie der Mengenverhältnisse der beteiligten Stoffe bei chemischen Reaktionen
Antrieb und Wärmebilanz bei Phasenübergängen. Speyer, März 2007
 Antrieb und Wärmebilanz bei Phasenübergängen Speyer, 19-20. März 2007 Michael Pohlig, WHG-Durmersheim michael@pohlig.de Literatur: Physik in der Oberstufe; Duden-PAETEC Schmelzwärme wird auch als Schmelzenergie
Antrieb und Wärmebilanz bei Phasenübergängen Speyer, 19-20. März 2007 Michael Pohlig, WHG-Durmersheim michael@pohlig.de Literatur: Physik in der Oberstufe; Duden-PAETEC Schmelzwärme wird auch als Schmelzenergie
Bauschädigende oder bauschädliche Salze sind. wasserlösliche Verbindungen. Zunahme der Löslichkeit. Schädigende Wirkung
 Wir graben in manchem Haus, das Recht haben wir vom König aus, wir fahren zur Salpeterei, von Pflastergeld und Schranken frei, Es lebe die Saliterei, bin schranken-, zoll- und steuerfrei. Bauschädigende
Wir graben in manchem Haus, das Recht haben wir vom König aus, wir fahren zur Salpeterei, von Pflastergeld und Schranken frei, Es lebe die Saliterei, bin schranken-, zoll- und steuerfrei. Bauschädigende
Eigenschaften von H 2 S
 Eigenschaften von H 2 S sehr giftiges, brennbares, unangenehm faulig riechendes Gas Smp. -86 C, Sdp. -60,2 C mäßig wasserlöslich, gesättigte Lösung hat c = 0,1 mol/l schwache, zweiprotonige Säure H 2 S
Eigenschaften von H 2 S sehr giftiges, brennbares, unangenehm faulig riechendes Gas Smp. -86 C, Sdp. -60,2 C mäßig wasserlöslich, gesättigte Lösung hat c = 0,1 mol/l schwache, zweiprotonige Säure H 2 S
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Kochsalz-Kristalle (Halit) Wichtige Stoffgruppen Atomverband Stoffgruppe Metall Metall: Metallische Stoffe Salzartige Stoffe Metall Nichtmetall:
 Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Kochsalz-Kristalle (Halit) 1 Wichtige Stoffgruppen Atomverband Metall Metall: Metall Nichtmetall: Stoffgruppe Metallische Stoffe (Gitter) - Metalle - Legierungen (- Cluster) Salzartige Stoffe (Gitter)
Grundkenntnisse der Chemie und der Physik. Was ihr hier findet
 Grundkenntnisse der hemie und der Physik P Was ihr hier findet Wissensgebiete der hemie und der Physik Formeln Elemente Metalle Kohlenstoff Analyse Synthese Basen Laugen Salze Atome Moleküle Akustik Optik
Grundkenntnisse der hemie und der Physik P Was ihr hier findet Wissensgebiete der hemie und der Physik Formeln Elemente Metalle Kohlenstoff Analyse Synthese Basen Laugen Salze Atome Moleküle Akustik Optik
Wasserstoffbrückenbindung, H 2 O, NH 3, HF, Wasserstoff im PSE, Isotope, Vorkommen, exotherme Reaktion mit Sauerstoff zu Wasser, Energieinhalt,
 Wiederholung der letzten Vorlesungsstunde: Das Element Wasserstoff und seine Verbindungen Wasserstoffbrückenbindung, H 2 O, NH 3, HF, Wasserstoff im PSE, Isotope, Vorkommen, exotherme Reaktion mit Sauerstoff
Wiederholung der letzten Vorlesungsstunde: Das Element Wasserstoff und seine Verbindungen Wasserstoffbrückenbindung, H 2 O, NH 3, HF, Wasserstoff im PSE, Isotope, Vorkommen, exotherme Reaktion mit Sauerstoff
Chemische Evolution. Biologie-GLF von Christian Neukirchen Februar 2007
 Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Chemische Evolution Biologie-GLF von Christian Neukirchen Februar 2007 Aristoteles lehrte, aus Schlamm entstünden Würmer, und aus Würmern Aale. Omne vivum ex vivo. (Alles Leben entsteht aus Leben.) Pasteur
Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O.
 Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O. 2 Er wollte herausfinden woher die Pflanze die Stoffe bezieht wenn sie beim Wachstum
Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O. 2 Er wollte herausfinden woher die Pflanze die Stoffe bezieht wenn sie beim Wachstum
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Die Elemente der 6. Hauptgruppe: Chalkogene
 Die Elemente der 6. Hauptgruppe: Chalkogene Chalkogene = Erzbildner Sauerstoff Oxide Schwefel Schwefelverbindungen Umweltaspekte 1 Gruppeneigenschaften radioaktiv 2 Sauerstoff - Vokommen Häufigstes Element
Die Elemente der 6. Hauptgruppe: Chalkogene Chalkogene = Erzbildner Sauerstoff Oxide Schwefel Schwefelverbindungen Umweltaspekte 1 Gruppeneigenschaften radioaktiv 2 Sauerstoff - Vokommen Häufigstes Element
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Anorganische Chemie I Dr. Egbert Figgemeier. 22. Januar 2007
 Anorganische Chemie I Dr. Egbert Figgemeier 22. Januar 2007 Gruppe 16 O S Se Te Po 88 Ra 87 Fr 7. 86 Rn 85 At 84 Po 83 Bi 82 Pb 81 Tl 56 Ba 55 Cs 6. 54 Xe 53 I 52 Te 51 Sb 50 Sn 49 In 38 Sr 37 Rb 5. 36
Anorganische Chemie I Dr. Egbert Figgemeier 22. Januar 2007 Gruppe 16 O S Se Te Po 88 Ra 87 Fr 7. 86 Rn 85 At 84 Po 83 Bi 82 Pb 81 Tl 56 Ba 55 Cs 6. 54 Xe 53 I 52 Te 51 Sb 50 Sn 49 In 38 Sr 37 Rb 5. 36
Grundlagen Chemie. Dipl.-Lab. Chem. Stephan Klotz. Freiwill ige Feuerwehr Rosenheim
 Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Säuren, Basen, Salze
 Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Natürliche ökologische Energie- und Stoffkreisläufe
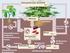 Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung der allgemeinen chemischen Grundlagen und Aspekte, die für alle Bereiche der Chemie notwendig sind; Modellvorstellungen Inhaltsübersicht:
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung der allgemeinen chemischen Grundlagen und Aspekte, die für alle Bereiche der Chemie notwendig sind; Modellvorstellungen Inhaltsübersicht:
Ammoniaksynthese nach Haber-Bosch
 Sarah Kiefer, Thomas Richter Ammoniaksynthese nach Haber-Bosch 1. Allgemeine Einführung 2. Chemisches Grundprinzip 3. Industrielle Umsetzung 4. Anwendung und Auswirkungen 1. Allgemeine Einführung Steckbrief:
Sarah Kiefer, Thomas Richter Ammoniaksynthese nach Haber-Bosch 1. Allgemeine Einführung 2. Chemisches Grundprinzip 3. Industrielle Umsetzung 4. Anwendung und Auswirkungen 1. Allgemeine Einführung Steckbrief:
Die chemische Reaktion
 Die chemische Reaktion Die Chemie beschäftigt sich mit Stoffen und ihren Eigenschaften. Die Dinge in unserer Umwelt bestehen aus vielen verschiedenen Stoffen, die häufig miteinander vermischt sind. Mit
Die chemische Reaktion Die Chemie beschäftigt sich mit Stoffen und ihren Eigenschaften. Die Dinge in unserer Umwelt bestehen aus vielen verschiedenen Stoffen, die häufig miteinander vermischt sind. Mit
Warum ist Feuer nützlich und warum sind Flammen heiß?
 Warum ist Feuer nützlich und warum sind Flammen heiß? Professor Dr.-Ing. Dieter Brüggemann KinderUniversität Bayreuth 1. Juli 2009 Wozu nutzen wir Feuer? Wir nutzen Feuer, um zu beleuchten Quelle: Wikipedia
Warum ist Feuer nützlich und warum sind Flammen heiß? Professor Dr.-Ing. Dieter Brüggemann KinderUniversität Bayreuth 1. Juli 2009 Wozu nutzen wir Feuer? Wir nutzen Feuer, um zu beleuchten Quelle: Wikipedia
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Kapitel 4: Chemische. Woher stammen die chemischen Symbole?
 Kapitel 4: Chemische Symbole Woher stammen die chemischen Symbole? Das sind die Anfangsbuchstaben (manchmal auch die ersten beiden Anfangsbuchstaben) der lateinischen oder griechischen Namen der Elemente.
Kapitel 4: Chemische Symbole Woher stammen die chemischen Symbole? Das sind die Anfangsbuchstaben (manchmal auch die ersten beiden Anfangsbuchstaben) der lateinischen oder griechischen Namen der Elemente.
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Gesteinskunde Einführung
 Gesteinskunde Einführung Christopher Giehl, Uni Tübingen 13.10.2011 Christopher Giehl (Universität Tübingen) 13.10.2011 1 / 23 1 Organisatorisches 2 Kursinhalte und -ziele 3 Grundbegriffe und Definitionen
Gesteinskunde Einführung Christopher Giehl, Uni Tübingen 13.10.2011 Christopher Giehl (Universität Tübingen) 13.10.2011 1 / 23 1 Organisatorisches 2 Kursinhalte und -ziele 3 Grundbegriffe und Definitionen
Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13
 Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
Kantonsschule Kreuzlingen, Klaus Hensler Chemiebuch Elemente Lösungen zu Aufgaben aus Kapitel 13 Grundregeln für stöchiometrische Berechnungen Wenn es um Reaktionen geht zuerst die chem. Gleichung aufstellen
LB1 Stoffe. LB1 Stoffe. LB1 Stoffe. Womit beschäftigt sich die Chemie?
 Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag
 2.1.1 Aufbau der Materie (Arbeitsaufträge) Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag 1. Beim Bearbeiten
2.1.1 Aufbau der Materie (Arbeitsaufträge) Empfohlene Hilfsmittel zum Lösen der Arbeitsaufträge: Arbeitsblätter, Theorieblätter, Fachbuch, Tabellenbuch und Ihr Wissen aus dem Praxisalltag 1. Beim Bearbeiten
2. Woche. Anorganische Analysenmethodik
 2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
2. Woche Anorganische Analysenmethodik Die analytische Chemie befasst sich mit den Methoden zur Ermittlung der stofflichen Zusammensetzung. Durch eine qualitative Analyse wird festgestellt, welche Atome
Kapitel III Salze und Salzbildungsarten
 Kapitel III Salze und Salzbildungsarten Einführung in die Grundlagen, Achtung: enthält auch die entsprechenden Übungen!!! Themen in [] müssen nicht auswendig gelernt werden! Navigation www.lernmaus.de
Kapitel III Salze und Salzbildungsarten Einführung in die Grundlagen, Achtung: enthält auch die entsprechenden Übungen!!! Themen in [] müssen nicht auswendig gelernt werden! Navigation www.lernmaus.de
Eigenschaften Reinstoffe Elemente Kugelteilchen Elementes Atom
 Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Michael Geisler Magnesium Sulfuricum - Epsomit Bittersalz
 Michael Geisler Magnesium Sulfuricum - Epsomit Bittersalz Leseprobe Magnesium Sulfuricum - Epsomit Bittersalz von Michael Geisler Herausgeber: IHHF Verlag http://www.narayana-verlag.de/b3175 Im Narayana
Michael Geisler Magnesium Sulfuricum - Epsomit Bittersalz Leseprobe Magnesium Sulfuricum - Epsomit Bittersalz von Michael Geisler Herausgeber: IHHF Verlag http://www.narayana-verlag.de/b3175 Im Narayana
by kiknet.ch 04 Gips / Radioaktivität / Arbeitsblatt
 1/7 Gips und seine Eigenschaften. Wir erstellen in der Klasse aus den Erkenntnissen aus drei Stationen ein Portrait des Baustoffes! SCENE GIPS Bautechnisch 2/7 Station 1 Bautechnisch Gips als Bindemittel
1/7 Gips und seine Eigenschaften. Wir erstellen in der Klasse aus den Erkenntnissen aus drei Stationen ein Portrait des Baustoffes! SCENE GIPS Bautechnisch 2/7 Station 1 Bautechnisch Gips als Bindemittel
Verdünnen von konzentrierter Schwefelsäure
 Verdünnen von konzentrierter Schwefelsäure Experimente, welche die Exothermizität der Reaktion von konzentrierter Schwefelsäure mit Wasser verdeutlichen sollen, sind in der Regel nicht sonderlich spektakulär,
Verdünnen von konzentrierter Schwefelsäure Experimente, welche die Exothermizität der Reaktion von konzentrierter Schwefelsäure mit Wasser verdeutlichen sollen, sind in der Regel nicht sonderlich spektakulär,
Anorganische Chemie I
 Anorganische Chemie I PRÜFUNG B. Sc. Chemieingenieurwesen 14. Juli 2014 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
Anorganische Chemie I PRÜFUNG B. Sc. Chemieingenieurwesen 14. Juli 2014 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse.
CHEMISCHE REAKTIONEN (SEKP)
 KSO CHEMISCHE REAKTIONEN (SEKP) Skript Chemische Reaktionen (SekP) V1.0 01/15 Bor 2 INHALTSVERZEICHNIS "CHEMISCHE REAKTIONEN" 1. Einleitung...03 2. Stoffe wandeln sich um... 04 2.1 Kupfer reagiert mit
KSO CHEMISCHE REAKTIONEN (SEKP) Skript Chemische Reaktionen (SekP) V1.0 01/15 Bor 2 INHALTSVERZEICHNIS "CHEMISCHE REAKTIONEN" 1. Einleitung...03 2. Stoffe wandeln sich um... 04 2.1 Kupfer reagiert mit
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
Curriculum Chemie Klasse 8 Albert-Einstein-Gymnasium Ulm Klasse 8 Themen Experimentieren im Chemieunterricht Grundregeln des Experimentierens 5. - mit Laborgeräten sachgerecht umgehen und die Sicherheitsmaßnahmen
1 Chemische Elemente und chemische Grundgesetze
 1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
Darstellung von Schwefelsäure. ein Referat von Melanie Rauhut Michael Voßkuhl
 Darstellung von Schwefelsäure ein Referat von Melanie Rauhut Michael Voßkuhl Inhaltsangabe Allgemeine Bedeutung der Schwefelsäure Geschichte der Schwefelsäuredarstellung Das Kontaktverfahren Das Bleikammerverfahren
Darstellung von Schwefelsäure ein Referat von Melanie Rauhut Michael Voßkuhl Inhaltsangabe Allgemeine Bedeutung der Schwefelsäure Geschichte der Schwefelsäuredarstellung Das Kontaktverfahren Das Bleikammerverfahren
Schwefelsäure. (Sulfat Ion)
 Schwefelsäure 1. Bau: Definition Säuren: Molekülverbindungen, deren wässrige Lösungen elektrisch positiv geladene Wasserstoff Ionen und elektrisch negativ geladene Säurerest Ionen enthalten. Baumerkmale:
Schwefelsäure 1. Bau: Definition Säuren: Molekülverbindungen, deren wässrige Lösungen elektrisch positiv geladene Wasserstoff Ionen und elektrisch negativ geladene Säurerest Ionen enthalten. Baumerkmale:
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Ein saurer Allesknner. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Ein saurer Allesknner Das komplette Material finden Sie hier: School-Scout.de 2 von 28 9. Schwefelsäure und ihre Salze (Kl. 9/10)
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Ein saurer Allesknner Das komplette Material finden Sie hier: School-Scout.de 2 von 28 9. Schwefelsäure und ihre Salze (Kl. 9/10)
Vom Atombau zum Königreich der Elemente
 Vom Atombau zum Königreich der Elemente Wiederholung: Elektronenwellenfunktionen (Orbitale) Jedes Orbital kann durch einen Satz von Quantenzahlen n, l, m charakterisiert werden Jedes Orbital kann maximal
Vom Atombau zum Königreich der Elemente Wiederholung: Elektronenwellenfunktionen (Orbitale) Jedes Orbital kann durch einen Satz von Quantenzahlen n, l, m charakterisiert werden Jedes Orbital kann maximal
ALLGEMEINE CHEMIE - GRUNDLAGEN
 ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
ALLGEMEINE CHEMIE - GRUNDLAGEN Ziel der Vorlesung: Vermittlung des Wissens allgemeiner chemischen Grundlagen und Vorstellungen, die für alle Bereiche der Naturwissenschaften notwendig sind; Modellvorstellungen
Experimentalvortrag zum Thema Schwefel
 Philipps-Universität Marburg Experimentalvortrag Dozenten: Prof. Dr. Bernhard Neumüller Dr. Philipp Reiß Wintersemester 2009/2010 Experimentalvortrag zum Thema Schwefel Autor: Martin Stolze Matrikelnummer:
Philipps-Universität Marburg Experimentalvortrag Dozenten: Prof. Dr. Bernhard Neumüller Dr. Philipp Reiß Wintersemester 2009/2010 Experimentalvortrag zum Thema Schwefel Autor: Martin Stolze Matrikelnummer:
Chemische Verbrennung
 Christopher Rank Sommerakademie Salem 2008 Gliederung Die chemische Definition Voraussetzungen sgeschwindigkeit Exotherme Reaktion Reaktionsenthalpie Heizwert Redoxreaktionen Bohrsches Atommodell s Elektrochemie:
Christopher Rank Sommerakademie Salem 2008 Gliederung Die chemische Definition Voraussetzungen sgeschwindigkeit Exotherme Reaktion Reaktionsenthalpie Heizwert Redoxreaktionen Bohrsches Atommodell s Elektrochemie:
Die 6. Hauptgruppe des Periodensystems der chemischen Elemente
 Die 6. Hauptgruppe des Periodensystems der chemischen Elemente Die 6. Hauptgruppe des Periodensystems umfaßt die Chalkogene (Erzbildner) Sauerstoff, Schwefel, Selen, Tellur und Polonium. Dieser Name leitet
Die 6. Hauptgruppe des Periodensystems der chemischen Elemente Die 6. Hauptgruppe des Periodensystems umfaßt die Chalkogene (Erzbildner) Sauerstoff, Schwefel, Selen, Tellur und Polonium. Dieser Name leitet
 www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
www.zaubervorlesung.de Institut für Anorganische Chemie Institut für Anorganische Chemie Universität Erlangen-Nürnberg Donnerstag 19. Okt. 2006 Einlass: 18:00 Uhr Beginn: 20:00 Uhr Getränke dürfen nur
Gegeben sind die folgenden Werte kovalenter Bindungsenthalpien:
 Literatur: Housecroft Chemistry, Kap. 22.1011 1. Vervollständigen Sie folgende, stöchiometrisch nicht ausgeglichene Reaktions gleichungen von Sauerstoffverbindungen. Die korrekten stöchiometrischen Faktoren
Literatur: Housecroft Chemistry, Kap. 22.1011 1. Vervollständigen Sie folgende, stöchiometrisch nicht ausgeglichene Reaktions gleichungen von Sauerstoffverbindungen. Die korrekten stöchiometrischen Faktoren
Teilnehmer/in:... Matrikel-Nr.:...
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 1 (Modul BGEO1.3.1 Anorganische und Allgemeine Chemie für Geologen, Geophysiker und Mineralogen) Teilnehmer/in:... MatrikelNr.:... 1. Sie sollen
Abschlussklausur Allgemeine und Anorganische Chemie Teil 1 (Modul BGEO1.3.1 Anorganische und Allgemeine Chemie für Geologen, Geophysiker und Mineralogen) Teilnehmer/in:... MatrikelNr.:... 1. Sie sollen
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Elemente des Periodensystems. Natürliche Häufigkeit der Elemente
 Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Akkus des menschlichen Lebens. Was ist Leben? oder: woher schöpfen die Menschen ihre Energie und wie wird sie genährt oder gestört?
 Akkus des menschlichen Lebens oder: woher schöpfen die Menschen ihre Energie und wie wird sie genährt oder gestört? Was ist Leben? Leben ist 1.: Fortpflanzung Leben ist 2.: Ernährung, Ausscheidung Leben
Akkus des menschlichen Lebens oder: woher schöpfen die Menschen ihre Energie und wie wird sie genährt oder gestört? Was ist Leben? Leben ist 1.: Fortpflanzung Leben ist 2.: Ernährung, Ausscheidung Leben
Korrosion in Biogasanlagen
 Korrosion in Biogasanlagen Dr.rer.nat. Jan Küver kuever@mpa-bremen.de Biogas Fachtagung Thüringen 24.November 2015, Bösleben 1 Mögliche Korrosionen Korrosion durch Kohlensäure (Betonkorrosion) Korrosion
Korrosion in Biogasanlagen Dr.rer.nat. Jan Küver kuever@mpa-bremen.de Biogas Fachtagung Thüringen 24.November 2015, Bösleben 1 Mögliche Korrosionen Korrosion durch Kohlensäure (Betonkorrosion) Korrosion
Die chemische Reaktion
 Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Beobachtung : Der gelbe Schwefel verbrennt mit blauer Flamme. Dabei wird Wärme frei und
Die chemische Reaktion 1. Versuch In eine mit Sauerstoff gefüllte Flasche halten wir ein Stück brennenden Schwefel. Beobachtung : Der gelbe Schwefel verbrennt mit blauer Flamme. Dabei wird Wärme frei und
Magische Kristalle Prof. Dr. R. Glaum
 Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
Magische Kristalle Prof. Dr. R. Glaum Institut für Anorganische Chemie Universität Bonn http://www.glaum.chemie.uni-bonn.de email: rglaum@uni-bonn.de Dank Herr Michael Kortmann Herr Andreas Valder Deutsche
ABFALLWIRTSCHAFT UND ABFALLENTSORGUNG
 ABFALLWIRTSCHAFT UND ABFALLENTSORGUNG Peter Lechner & Marion Huber-Humer MVA-Schlacke LVA-Nr. 813.100 & 101 Studienjahr 2011/2012 Studienjahr 2011/12 LVA 813.100 & 101 2 Stoffströme einer MVA Restabfall
ABFALLWIRTSCHAFT UND ABFALLENTSORGUNG Peter Lechner & Marion Huber-Humer MVA-Schlacke LVA-Nr. 813.100 & 101 Studienjahr 2011/2012 Studienjahr 2011/12 LVA 813.100 & 101 2 Stoffströme einer MVA Restabfall
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Der Hitzetod der Erde
 Der Hitzetod der Erde Der natürliche Treibhauseffekt In der Erdatmosphäre gibt es neben dem für uns lebenswichtigen Sauerstoff einige hoch wirksame Treibhausgase. Dies sind vor allem:! Kohlendioxid! Wasserdampf!
Der Hitzetod der Erde Der natürliche Treibhauseffekt In der Erdatmosphäre gibt es neben dem für uns lebenswichtigen Sauerstoff einige hoch wirksame Treibhausgase. Dies sind vor allem:! Kohlendioxid! Wasserdampf!
Naturwissenschaft Vermutungswissen Alles ist Chemie!!! Analyse Synthese
 SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
SPF 2 Chemie Was ist Chemie? - Chemie ist eine Naturwissenschaft Wie schafft eine Naturwissenschaft wissen? - Vermutungswissen; naturwissenschaftlicher Erkenntnisgang Womit beschäftigt sich die Chemie?
KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor
 1 KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "METALLE" 1. Einleitung...03 2. Reaktionen von Metallen... 05 3. Gewinnung von Metallen... 07 4. Domino: Eigenschaften der
1 KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "METALLE" 1. Einleitung...03 2. Reaktionen von Metallen... 05 3. Gewinnung von Metallen... 07 4. Domino: Eigenschaften der
Chemie, Kapitel 4 : Chemische Reaktionen und Luft
 Lesen Sie aufmerksam das Kapitel 4.4 und lösen Sie die folgenden Aufgaben: a) Definieren Sie die drei Begriffe in jeweils einem Satz b) Geben Sie ein Beispiel aus dem Alltag Exotherme Reaktion: Endotherme
Lesen Sie aufmerksam das Kapitel 4.4 und lösen Sie die folgenden Aufgaben: a) Definieren Sie die drei Begriffe in jeweils einem Satz b) Geben Sie ein Beispiel aus dem Alltag Exotherme Reaktion: Endotherme
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure
 Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Die Biogasanlage. GFS von Franziska Marx
 Die Biogasanlage GFS von Franziska Marx Inhalt Geschichte Die Biomasse Das Biogas Funktion der Biogasanlage Der Gärprozess Die Aufbereitung Biogasanlagen in der Umgebung Wirtschaftlichkeit Bedeutung der
Die Biogasanlage GFS von Franziska Marx Inhalt Geschichte Die Biomasse Das Biogas Funktion der Biogasanlage Der Gärprozess Die Aufbereitung Biogasanlagen in der Umgebung Wirtschaftlichkeit Bedeutung der
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Schweizerische Maturitätsprüfung Gruppe / Kandidat/in Nr:... Winter 2010, Zürich Name/Vorname:...
 Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Gruppe / Kandidat/in Nr:... Name/Vorname:... Grundlagenfach Bereich Teil: NATURWISSENSCHAFTEN Chemie Verfasser: Richtzeit: Hilfsmittel: Hinweise: R. Guenin, J. Lipscher, S. Steiner 80 Minuten (von total
Chemieepoche Klasse 11. Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen
 Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Eisengewinnung (Schülervortrag) Fortsetzung Chemische Bindungen Warum sind im Wassermolekül zwei Wasserstoffatome mit
Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Eisengewinnung (Schülervortrag) Fortsetzung Chemische Bindungen Warum sind im Wassermolekül zwei Wasserstoffatome mit
Wie sieht unsere Welt im Kleinen aus?
 Skriptum Wie sieht unsere Welt im Kleinen aus? 1 Wie sieht unsere Welt im Kleinen aus? Atom- und Quantenphysik für Kids Seminar im Rahmen der KinderUni Wien, 12. 7. 2005 Katharina Durstberger, Franz Embacher,
Skriptum Wie sieht unsere Welt im Kleinen aus? 1 Wie sieht unsere Welt im Kleinen aus? Atom- und Quantenphysik für Kids Seminar im Rahmen der KinderUni Wien, 12. 7. 2005 Katharina Durstberger, Franz Embacher,
Grundwissen Chemie 9. Klasse SG
 Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Grundwissen Chemie 9. Klasse SG Stoffe und Reaktionen - bestehen aus kleinsten Teilchen - lassen sich aufgliedern in Reinstoffe und Stoffgemische Stoffe Reinstoff Stoffe Stoffgemisch Atome Moleküle heterogen
Verschiedene feste Stoffe werden auf ihre Leitfähigkeit untersucht, z.b. Metalle, Holz, Kohle, Kunststoff, Bleistiftmine.
 R. Brinkmann http://brinkmann-du.de Seite 1 26/11/2013 Leiter und Nichtleiter Gute Leiter, schlechte Leiter, Isolatoren Prüfung der Leitfähigkeit verschiedener Stoffe Untersuchung fester Stoffe auf ihre
R. Brinkmann http://brinkmann-du.de Seite 1 26/11/2013 Leiter und Nichtleiter Gute Leiter, schlechte Leiter, Isolatoren Prüfung der Leitfähigkeit verschiedener Stoffe Untersuchung fester Stoffe auf ihre
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie. Allgemeine Chemie. Rückblick auf vorherige Übung
 Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
Planung, Bau und Betrieb von Chemieanlagen - Übung Allgemeine Chemie 1 Allgemeine Chemie Rückblick auf vorherige Übung 2 Löslichkeit Was ist eine Lösung? - Eine Lösung ist ein einphasiges (homogenes) Gemisch
9. Thermodynamik. 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala. 9.4 Wärmekapazität
 9. Thermodynamik 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala 93 9.3 Thermische h Ausdehnung 9.4 Wärmekapazität 9. Thermodynamik Aufgabe: - Temperaturverhalten von Gasen,
9. Thermodynamik 9.1 Temperatur und thermisches Gleichgewicht 9.2 Thermometer und Temperaturskala 93 9.3 Thermische h Ausdehnung 9.4 Wärmekapazität 9. Thermodynamik Aufgabe: - Temperaturverhalten von Gasen,
Chemiefragen 9.Klasse:
 Hausaufgaben bitte entweder: - auf Papier schriftlich erledigen oder - per email an Herrn Apelt senden: Reinhard.Apelt@web.de Chemiefragen 9.Klasse: A) Stoffe und ihre Erkennung B) Anwendung des Teilchenmodells
Hausaufgaben bitte entweder: - auf Papier schriftlich erledigen oder - per email an Herrn Apelt senden: Reinhard.Apelt@web.de Chemiefragen 9.Klasse: A) Stoffe und ihre Erkennung B) Anwendung des Teilchenmodells
Übung zu den Vorlesungen Organische und Anorganische Chemie
 Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 07.11.08 - Lösungen - 1. Vervollständigen Sie die Reaktionsgleichungen und benennen Sie alle Verbindungen und
Übung zu den Vorlesungen Organische und Anorganische Chemie für Biologen und Humanbiologen 07.11.08 - Lösungen - 1. Vervollständigen Sie die Reaktionsgleichungen und benennen Sie alle Verbindungen und
EINE KERZE INTERPRETATIONEN BEOBACHTUNGEN FLAMME REAKTIONEN WACHS DOCHT GASE. Reaktionsgleichungen Prozesse. Theorien
 Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Reaktionsgleichungen Prozesse INTERPRETATIONEN BEOBACHTUNGEN Theorien Licht Produkte Reaktionsgleichungen Thermodynamik Geschwindigkeit REAKTIONEN EINE KERZE FLAMME Farbe Form Bewegung Einflüsse WACHS
Tutorium zur Analytischen Chemie Übungsaufgaben 1
 Tutorium zur Analytischen Chemie Übungsaufgaben 1 1.) Berechnen Sie die folgenden Molmassen! a) [Cu(NH 3 ) 6 ]Cl 2 b) AgCl c) Ti(SO 4 ) 2 d) Na 2 [Sn(OH) 6 ] e) Na 2 CO 3 f) Ca(HCO 3 ) 2 2.) Berechnen
Tutorium zur Analytischen Chemie Übungsaufgaben 1 1.) Berechnen Sie die folgenden Molmassen! a) [Cu(NH 3 ) 6 ]Cl 2 b) AgCl c) Ti(SO 4 ) 2 d) Na 2 [Sn(OH) 6 ] e) Na 2 CO 3 f) Ca(HCO 3 ) 2 2.) Berechnen
Herstellung von Schwefelsäure
 Herstellung von Schwefelsäure Ein Referat von: Sebastian Arndt Niko Grebe Nils Wallmeyer Inhaltsverzeichnis Allgemeines Geschichte Herstellungsverfahren Wirtschaftliche Bedeutung Quellenverzeichnis Allgemeines
Herstellung von Schwefelsäure Ein Referat von: Sebastian Arndt Niko Grebe Nils Wallmeyer Inhaltsverzeichnis Allgemeines Geschichte Herstellungsverfahren Wirtschaftliche Bedeutung Quellenverzeichnis Allgemeines
Geografie, D. Langhamer. Klimarisiken. Beschreibung des Klimas eines bestimmten Ortes. Räumliche Voraussetzungen erklären Klimaverlauf.
 Klimarisiken Klimaelemente Klimafaktoren Beschreibung des Klimas eines bestimmten Ortes Räumliche Voraussetzungen erklären Klimaverlauf Definitionen Wetter Witterung Klima 1 Abb. 1 Temperaturprofil der
Klimarisiken Klimaelemente Klimafaktoren Beschreibung des Klimas eines bestimmten Ortes Räumliche Voraussetzungen erklären Klimaverlauf Definitionen Wetter Witterung Klima 1 Abb. 1 Temperaturprofil der
Rolle des S im Pflanzen- und Mikroben- Wachstum
 Rolle des S im Pflanzen- und Mikroben- Wachstum Synthese S-haltiger Aminosäuren: Cystein und Methionin, (Cystin = Disulfid) Aufbau anderer Metabolite, CoA, Biotin, Thiamine und Glutathion. Hauptfunktion:
Rolle des S im Pflanzen- und Mikroben- Wachstum Synthese S-haltiger Aminosäuren: Cystein und Methionin, (Cystin = Disulfid) Aufbau anderer Metabolite, CoA, Biotin, Thiamine und Glutathion. Hauptfunktion:
Kalk, Gips, Zement. Ein Vortrag von Björn Bahle. 12.06.2006 SS06 / Anorganische Chemie I 1 08.06.2006
 Kalk, Gips, Zement Ein Vortrag von Björn Bahle 08.06.2006 12.06.2006 SS06 / Anorganische Chemie I 1 Kalk, Gips, Zement 12.06.2006 SS06 / Anorganische Chemie I 2 Inhalt: 1.) Kalk 2.) Gips 3.) Zement 1.1.)
Kalk, Gips, Zement Ein Vortrag von Björn Bahle 08.06.2006 12.06.2006 SS06 / Anorganische Chemie I 1 Kalk, Gips, Zement 12.06.2006 SS06 / Anorganische Chemie I 2 Inhalt: 1.) Kalk 2.) Gips 3.) Zement 1.1.)
Bindungsarten und ihre Eigenschaften
 Bindungsarten und ihre Eigenschaften Atome sowohl desselben als auch verschiedener chemischer Elemente können sich miteinander verbinden. Dabei entstehen neue Stoffe, die im Allgemeinen völlig andere Eigenschaften
Bindungsarten und ihre Eigenschaften Atome sowohl desselben als auch verschiedener chemischer Elemente können sich miteinander verbinden. Dabei entstehen neue Stoffe, die im Allgemeinen völlig andere Eigenschaften
Praktikumsrelevante Themen
 Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Praktikumsrelevante Themen Lösungen Der Auflösungsprozess Beeinflussung der Löslichkeit durch Temperatur und Druck Konzentration von Lösungen Dampfdruck, Siede- und Gefrierpunkt von Lösungen Lösungen von
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Grenzflächenphänomene. Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie. J m. N m. 1. Oberflächenspannung
 Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Grenzflächenphänomene 1. Oberflächenspannung Physikalische Grundlagen der zahnärztlichen Materialkunde 3. Struktur der Materie Grenzflächenphänomene Phase/Phasendiagramm/Phasenübergang Schwerpunkte: Oberflächenspannung
Gewinnung und Reinigung der Übergangsmetalle. Von Sebastian Kreft
 Übergangsmetalle Von Sebastian Kreft Übersicht Gewinnung und Raffination von: 1. Scandium 2. Titan 3. Vanadium 4. Chrom 5. Mangan 6. Eisen 7. Cobalt 8. Nickel 9. Kupfer 10. Zink Übergangsmetalle 2 1. Scandium
Übergangsmetalle Von Sebastian Kreft Übersicht Gewinnung und Raffination von: 1. Scandium 2. Titan 3. Vanadium 4. Chrom 5. Mangan 6. Eisen 7. Cobalt 8. Nickel 9. Kupfer 10. Zink Übergangsmetalle 2 1. Scandium
