ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS NeisVac-C
|
|
|
- Dörte Martin
- vor 6 Jahren
- Abrufe
Transkript
1 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS NeisVac-C 1. BEZEICHNUNG DES ARZNEIMITTELS NeisVac-C 0,5 ml Suspension zur Injektion in einer Fertigspritze ohne Kanüle Adsorbierter Meningokokken-Gruppe C-Polysaccharid-Konjugatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5 ml) enthält: Neisseria meningitidis Gruppe C (Stamm C11) Polysaccharid (de-o-acetyliert) 10 µg gebunden an Tetanustoxoid µg adsorbiert an hydratisiertes Aluminiumhydroxid 0,5 mg Al 3+ Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Suspension zur Injektion in einer Fertigspritze ohne Kanüle. Leicht trübe, weiße bis weißliche Suspension. 4. KLINISCHE ANGABEN 4.1. Anwendungsgebiete Aktive Immunisierung von Kindern ab dem vollendeten 2. Lebensmonat, Jugendlichen und Erwachsenen zur Prävention invasiver Erkrankungen, die durch Neisseria meningitidis der Gruppe C verursacht werden. Hinsichtlich der Anwendung von NeisVac-C wird auf die aktuellen deutschen Impfempfehlungen hingewiesen Dosierung, Art und Dauer der Anwendung Dosierung Es liegen keine Daten über den Einsatz unterschiedlicher Meningokokken-C-Konjugatimpfstoffe zur Grundimmunisierung oder zur Auffrischungsimpfung vor. Wann immer möglich, sollte daher der gleiche Impfstoff verwendet werden. Grundimmunisierung Säuglinge zwischen zwei und zwölf Monaten: Es sollten zwei Dosen zu je 0,5 ml im Abstand von mindestens zwei Monaten verabreicht werden. (Zur gleichzeitigen Applikation von NeisVac-C mit anderen Impfstoffen siehe Abschnitte 4.5 und 5.1) Kinder ab dem vollendeten ersten Lebensjahr, Jugendliche und Erwachsene: Eine Einzeldosis von 0,5 ml.
2 Auffrischungsimpfung Bei Säuglingen, die eine Grundimmunisierung erhalten haben, wird eine Auffrischungsimpfung empfohlen. Der Zeitpunkt für diese Dosis sollte mit den offiziellen Impfempfehlungen übereinstimmen. Informationen zur Immunantwort nach der Auffrischungsimpfung siehe Abschnitt 5.1, sowie zur gleichzeitigen Verabreichung mit anderen Kinderimpfstoffen siehe Abschnitt 4.5 und 5.1. Die Notwendigkeit von Auffrischungsimpfungen bei Personen, die mit einer Einzeldosis (nach dem vollendeten 1. Lebensjahr) immunisiert wurden, ist noch nicht nachgewiesen (siehe Abschnitt 5.1). Art der Anwendung NeisVac-C muss intramuskulär injiziert werden, bei Säuglingen bevorzugt in den Oberschenkel (M. vastus lateralis), bei älteren Kindern, Jugendlichen und Erwachsenen in den Oberarm (M. deltoideus). Bei Kindern zwischen 12 und 24 Monaten kann der Impfstoff sowohl in den Oberarm als auch in den Oberschenkel gegeben werden. Der Impfstoff darf nicht subkutan oder intravenös verabreicht werden (siehe Abschnitt 4.4). NeisVac-C darf nicht zusammen mit anderen Impfstoffen in einer Spritze verabreicht werden. Bei gleichzeitiger Gabe mehrerer Impfstoffe sind getrennte Injektionsstellen zu wählen (siehe Abschnitt 4.5) Gegenanzeigen Überempfindlichkeit gegen Bestandteile des Impfstoffes, einschließlich Tetanustoxoid. Bei akuten schweren fieberhaften Erkrankungen muss, wie bei jeder anderen Impfung, die Gabe von NeisVac-C verschoben werden Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Für den Fall einer selten auftretenden anaphylaktischen Reaktion nach Verabreichung des Impfstoffes müssen geeignete medizinische Behandlungs- und Überwachungsmöglichkeiten zur Verfügung stehen. Auf Grund dieses Risikos muss der Patient nach der Impfung für angemessene Zeit unter ärztlicher Beobachtung bleiben. NeisVac-C DARF AUF KEINEN FALL INTRAVENÖS VERABREICHT WERDEN. Bei Patienten mit Thrombozytopenie oder Blutgerinnungsstörungen sollte der Impfstoff nur mit besonderer Vorsicht verabreicht werden. Da über die subkutane Verabreichung von NeisVac-C keine Daten vorliegen, kann eine toxische Wirkung oder eine geringere Wirksamkeit nicht ausgeschlossen werden. Das theoretische Risiko einer Apnoe und die Notwendigkeit einer respiratorischen Überwachung über Stunden sollte bei der Verabreichung der Erstimmunisierung bei sehr unreifen Frühgeborenen (geboren vor der 28. Woche) in Betracht gezogen werden, insbesondere wenn eine Vorgeschichte über eine respiratorische Unreife vorliegt. Da die Impfung für diese Gruppe einen großen Nutzen darstellt, sollte diese Impfung nicht vorenthalten oder verzögert werden. Das Arzneimittel enthält weniger als 1 mmol Natrium (23 Milligramm) pro Dosis. Es ist also praktisch natriumfrei. Bisher stehen keine Daten zur Verfügung, ob der Impfstoff zur Kontrolle einer Epidemie geeignet ist. Die Nutzen-Risiko-Abwägung einer Impfung mit NeisVac-C hängt von der Inzidenz der Infektionen mit N. meningitidis der Gruppe C in der Bevölkerung vor Einführung eines großflächigen Impfprogramms ab. Bei Personen mit geschwächter Immunabwehr (z. B. auf Grund eines genetischen Defekts oder einer immunsuppressiven Therapie) kann die Bildung schützender Antikörper eingeschränkt sein oder
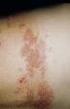
3 ausbleiben. Daher kann nicht bei allen geimpften Personen ein entsprechender Impfschutz erlangt (erreicht) werden. Es ist anzunehmen, dass Patienten mit Störungen des Komplementsystems und Patienten mit funktioneller oder anatomischer Asplenie eine Immunantwort auf Meningokokken-C-Konjugatimpfstoffe entwickeln. Das Ausmaß dieser Schutzwirkung ist allerdings unbekannt. Obwohl nach der Impfung über Meningismussymptome wie Nackenschmerzen,/-steifigkeit oder Photophobie berichtet wurde, gibt es keinen Hinweis, dass Meningokokken-C-Konjugatimpfstoffe eine Meningokokken-C-Meningitis verursachen. Die Möglichkeit einer gleichzeitig bestehenden/auftretenden Meningitis sollte daher in Betracht gezogen werden. Die Immunisierung mit diesem Impfstoff ersetzt nicht die routinemäßige Tetanus-Impfung. NeisVac-C bewirkt lediglich einen Schutz gegen Neisseria meningitidis der Gruppe C und schützt möglicherweise nicht vollständig vor Erkrankungen durch Meningokokken der Gruppe C. NeisVac-C dient nicht als Schutz vor anderen Gruppen von Neisseria meningitidis oder anderen Organismen, welche Meningitis oder Septikämie verursachen. Bei Auftreten von Petechien bzw. Purpura nach einer Impfung (siehe Abschnitt 4.8) muss deren Ursache gründlich geklärt werden. Dabei müssen sowohl infektiöse als auch nicht infektiöse Ursachen in Erwägung gezogen werden. Es liegen keine Daten über die Anwendung von NeisVac-C bei Erwachsenen über 65 Jahren vor (siehe Abschnitt 5.1) Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen NeisVac-C darf nicht zusammen mit anderen Impfstoffen in einer Spritze verabreicht werden. Bei gleichzeitiger Gabe mehrerer Impfstoffe sind getrennte Injektionsstellen zu wählen. Bei gleichzeitiger Gabe von NeisVac-C und den folgenden Impfstoffen (an separaten Injektionsstellen) im Rahmen klinischer Studien war die Immunantwort auf keines der Antigene verringert: - Diphtherie- und Tetanus-Toxoide - Ganzkeim-Pertussis-Impfstoff (wp) - azellulärer Pertussis-Impfstoff (ap) - Haemophilus influenzae-konjugat-impfstoff (Hib) - inaktivierter Polio-Impfstoff (IPV) - Masern-Mumps-Röteln-Impfstoff (MMR) In Studien, bei denen NeisVac-C an Säuglingen gleichzeitig mit einem hepta-bzw. dekavalenten Pneumokokken-Konjugatimpfstoff verabreicht wurde, konnten zufriedenstellende Immunantworten auf beide Impfstoffe beobachtet werden. Gelegentlich wurden geringfügige Schwankungen im geometrischen Mittelwert der Antikörperspiegel von gleichzeitig, gegenüber separat, verabreichten Impfungen beobachtet. Die klinische Bedeutung dieser Beobachtungen konnte jedoch nicht nachgewiesen werden. Eine gleichzeitige Verabreichung von NeisVac-C (zwei Dosen gemäß dem Impfschema für Säuglinge) und drei Dosen des hexavalenten Impfstoffes Infanrix hexa (DTaP-IPV-HBV-Hib) bei der Grundimmunisierung von Säuglingen zeigte keine klinisch relevante Interferenz mit der Immunantwort gegen eines der Antigene in diesem hexavalenten Impfstoff. Spezifische Daten zur gleichzeitigen Verabreichung von NeisVac-C mit drei Dosen des hexavalenten Impfstoffes Hexavac (DTaP-IPV-HBV-Hib) bei der Grundimmunisierung von Säuglingen zeigten, dass die Impfantwort auf die Hepatitis B-Komponente unbefriedigend war. Von einer gleichzeitigen Anwendung von NeisVac-C und Hexavac wird deshalb abgeraten. Im Rahmen mehrerer Studien zu verschiedenen Impfstoffen ergab die gleichzeitige Verabreichung von Meningokokken-C-Konjugatimpfstoffen mit Kombinationspräparaten, die azelluläre Pertussis- Komponenten enthielten (mit oder ohne inaktivierte Polio-Viren, Hepatitis B-Oberflächenantigen oder Hib- Konjugate) niedrigere SBA-GMT als die separate Verabreichung oder die gleichzeitige Verabreichung mit
4 Ganzkeim-Pertussis-Impfstoffen. Die Anzahl an Probanden, die SBA-Titer von mindestens 1:8 oder 1:128 erreichten, war unbeeinflusst. Die möglichen Auswirkungen dieser Beobachtung auf die Schutzdauer sind derzeit nicht bekannt. Bei Immunisierung mit NeisVac-C einen Monat nach Gabe eines tetanushaltigen Impfstoffes wurde eine Serokonversionsrate von 95,7 % festgestellt. Bei zeitgleicher Applikation der Impfstoffe wurde hingegen eine Serokonversionsrate von 100 % erreicht Schwangerschaft und Stillzeit Es liegen keine hinreichenden Daten über die Verwendung dieses Impfstoffs bei Schwangeren vor. Tierversuche sind in Hinblick auf die Auswirkungen auf die Schwangerschaft, die embryonale/fetale Entwicklung, die Geburt und die postnatale Entwicklung nicht aussagekräftig. Das potenzielle Risiko für den Menschen ist nicht bekannt. Trotzdem dürfen Schwangere, in Anbetracht der Schwere einer Meningokokken-C-Erkrankung, bei klar definiertem Expositionsrisiko nicht von einer Impfung ausgeschlossen werden. In der Stillzeit ist vor Verabreichung des Impfstoffs ebenfalls eine sorgfältige Risiko/Nutzen-Abwägung erforderlich Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es ist unwahrscheinlich, dass der Impfstoff die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen beeinträchtigt Nebenwirkungen Nebenwirkungen aus klinischen Prüfungen In kontrollierten klinischen Studien wurde NeisVac-C an Säuglinge oft gleichzeitig mit Impfstoffen verabreicht, die Diphtherie- und Tetanus-Toxoide (DT) wp, ap, Hib, orales Poliovirus oder Hepatitis-B- Komponenten (HBV) enthielten. Einjährige Kinder erhielten oft zeitgleich MMR-Impfstoff, 3½-6jährige Kinder DT-Impfstoff. Mit NeisVac-C geimpfte 13-17jährige erhielten oft gleichzeitig Td-Impfstoffe mit reduziertem Gehalt an Diphtherie-Toxoid (Td). NeisVac-C und die gleichzeitig verabreichten Impfstoffe wurden an verschiedenen Injektionsstellen appliziert. Die in diesen Studien am häufigsten berichteten Nebenwirkungen sind in folgender Tabelle zusammengefasst: Häufigkeit der Nebenwirkungen Sehr häufig: ( 1:10) Häufig ( 1:100 bis <1:10) Nebenwirkungen lokale Reaktionen an der Injektionsstelle: (Rötung, Spannungsgefühl/Schmerz, Schwellung) Gliederschmerzen bei älteren Kindern Kopfschmerzen Schreien und Unruhe bei Säuglingen und Kleinkindern Benommenheit/Schläfrigkeit/Schlafstörungen bei Säuglingen und Kleinkindern Erbrechen/Übelkeit/Durchfall bei Säuglingen Appetitverlust bei Säuglingen Fieber Appetitverlust bei Kindern Erbrechen/Übelkeit/Durchfall bei Kindern Muskelschmerzen bei älteren Kindern und Erwachsenen Gliederschmerzen bei Kindern Die folgenden zusätzlichen Nebenwirkungen wurden im Rahmen des Spontanmeldesystems berichtet: Erkrankungen des Blutes und des Lymphsystems: Lymphadenopathie, idiopathische thrombozytopenische Purpura
5 Erkrankungen des Immunsystems: Anaphylaxie, Überempfindlichkeitsreaktionen einschließlich Bronchospasmus, Gesichtsödem und Angioödem. Erkrankungen des Nervensystems: Schwindel, Krämpfe, einschließlich Fieberkrämpfe, Synkopen, Hypästhesie und Parästhesie sowie Hypotonie bei Säuglingen. Sehr selten wurde nach Gabe eines Gruppe-C-Meningokokken-Konjugatimpfstoffes über Krampfanfälle berichtet. Die Impflinge erholten sich meist rasch. Bei einigen der berichteten Krampfanfälle könnte es sich um Ohnmachtsanfälle gehandelt haben. Bei Kindern lag die Anzahl der berichteten Krampfanfälle unter der Anzahl von Neuerkrankungen der Epilepsie. Bei Säuglingen waren die Krampfanfälle meist mit Fieber verbunden, so dass es sich hier wahrscheinlich um Fieberkrämpfe handelte. Erkrankungen des Atemtraktes, des Brustraumes und des Mediastinums: Apnoe bei sehr unreifen Frühgeborenen (geboren vor der 28. Woche) (siehe Abschnitt 4.4.) Erkrankungen des Gastrointestinaltrakts: Übelkeit, Erbrechen Erkrankungen der Haut und des Unterhautzellgewebes: Rötung, Urtikaria, Pruritus Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen: Arthralgie Erkrankungen der Nieren und Harnwege: Es wurde über Rezidive des Nephrotischen Syndroms im Zusammenhang mit Impfstoffen gegen Meningokokken der Gruppe C berichtet. In sehr selten Fällen wurde über Petechien und/oder Purpura in Folge der Immunisierung berichtet (Siehe auch Abschnitt 4.4). Im Rahmen des Spontanmeldesystems gingen im Zusammenhang mit der Verwendung von Konjugatimpfstoffen gegen Meningokokken der Gruppe C Meldungen über das Stevens-Johnson- Syndrom und Erythema multiforme ein Überdosierung Es gibt keine Erfahrung zur Überdosierung von NeisVac-C. Da der Impfstoff durch einen Arzt in Form einer Einzeldosis verabreicht wird, ist eine Überdosierung sehr unwahrscheinlich. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1. Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Meningokokken-Impfstoff ATC-Code: J07AH Es wurden keine Studien zur klinischen Wirksamkeit durchgeführt. Für Impfstoffe gegen Meningokokken der Gruppe C wurden die serologischen Korrelate noch nicht endgültig geklärt; sie werden derzeit ermittelt. Beim unten zitierten Test für bakterizide Serumantikörper (SBA) wurde der C11-Stamm verwendet, und Kaninchenserum diente als Ausgangsprodukt für das Komplement und den C11-Stamm. In der Studie 99MCIUK (Tabelle siehe unten) erhielten fast alle Säuglinge gleichzeitig mit der NeisVac-C- Dosis (je nach Randomisierungsschema wurden eine, zwei oder drei Dosen verabreicht) einen Diphtherie-Tetanus- und Ganzkeim-Pertussis-Kombinationsimpfstoff. Unter den Säuglingen, die eine einzelne NeisVac-C-Dosis im 2. Lebensmonat erhalten hatten (n=182), erreichten 98,4 % einen SBA-Titer von mindestens 1:8, und 95,6 % wiesen einen Monat nach der zweiten Impfung einen Titer von mindestens 1:32 auf.
6 Alle Säuglinge, die zwei Dosen im Alter von zwei und vier Monaten erhalten hatten, (n=188) erreichten Antikörpertiter von 1:8, und 99,5 % wiesen einen Monat nach der zweiten Impfung einen Titer von mindestens 1:32 auf. Eine im zweiten Lebensjahr verabreichte Belastungsdosis aus unkonjugiertem Meningokokken-C- Polysaccharid-Impfstoff (verabreicht mit 1/5 der empfohlenen Dosis eines zugelassenen A/C- Impfstoffs) induzierte bei 98 % der Kleinkinder, die im Säuglingsalter entweder eine (n=166) oder zwei Dosen (n=157) NeisVac-C erhalten hatten, einen SBA-Titer von mindestens 1:32. Bei einer klinischen Studie mit Erwachsenen zwischen 18 und 64 Jahren erhielten 73 Personen, die zuvor keinen Impfstoff gegen eine Meningokokken-C-Infektion erhalten hatten und 40 Personen, denen bereits ein Impfstoff mit unkonjugiertem Meningokokken-C-Polysaccharid verabreicht worden war, eine Einzeldosis NeisVac-C. Bei den Personen, deren Titer einen Monat nach der Impfung bestimmt wurde, zeigten 65 von 68 (97,1 %) der nicht vorgeimpften und 34 von 35 (95,6 %) der vorgeimpften Personen Titer von mindestens 1:8. 65 von 68 der nicht vorgeimpften und 33 von 35 der vorgeimpften Personen wiesen Titer von mindestens 1:128 auf. Die SBA-GMT betrugen jedoch bei den beiden Gruppen 1758 bzw Somit sprachen bereits mit unkonjugiertem Polysaccharid geimpfte Erwachsene schwächer auf das konjugierte Polysaccharid in NeisVac-C an, wobei >90 % dennoch einen SBA-Titer von 1:128 erreichten. Die Immunantworten (SBA-Titer gegen Stamm C11) sind in der folgenden Tabelle - nach Altersgruppe sortiert - zusammengefasst: Studie Anzahl der Probanden, bei denen der Titer erreicht wurde / Gesamtzahl der Probanden Titer 1:8* Titer 1:32* Säuglingsstudie 99MCIUK 1 Dosis im 2. Lebensmonat 2 Dosen, davon je eine im 2. und im 4. Lebensmonat 3 Dosen, davon je eine im 2., 3. und 4. Lebensmonat 179/ / /173 (98,4 %) (100 %) (99,4 %) 174/182 (95,6 %) 187/188 (99,5 %) 170/172 (98,8 %) Säuglingsstudie 97C002 Auffrischung mit NeisVac-C (4. Dosis)** 24/24 (100 %) Kleinkinder 72/72 (100 %) 70/72 (97,2 %) 3,5-6 Jahre 72/73 (98,6 %) 72/73 (98,6 %) Jahre 28/28 (100 %) 28/28 (100 %) Erwachsene Keine frühere MenC-Impfung Vorangegangene Impfung mit unkonjugiertem MenC-Impfstoff 65/68 34/35 (95,6 %) (97,1 %) *** *** * Blutproben für serologische Tests wurden etwa vier Wochen nach der Impfung abgenommen. ** Je eine der drei Dosen im Säuglingsalter wurde im 2., 3. und 4. Lebensmonat verabreicht *** 95,6 % bzw. 94,3 % der Probanden erreichten rsba-titer von 1:128 # Alle Altersgruppen mit Ausnahme der Säuglinge erhielten nur eine Einzeldosis NeisVac-C Anwendungsbeobachtung nach einer Impfkampagne in Großbritannien Schätzungen zur Impfstoff-Wirksamkeit, die auf dem Routine-Impfplan in Großbritannien beruhen (unter Verwendung verschiedener Mengen von drei Meningokokken-C-Konjugatimpfstoffen) und den Zeitraum von der Markteinführung Ende 1999 bis zum März 2004 abdecken, belegten die Notwendigkeit einer Auffrischungsimpfung nach Abschluss der Grundimmunisierung (drei Dosen, verabreicht im 2., 3. und 4. Lebensmonat). Innerhalb eines Jahres nach vollendeter Grundimmunisierung erreichte die Wirksamkeit
7 bei der Säuglingsgruppe etwa 93 % (95 %-Vertrauensintervall %). Allerdings gab es mehr als ein Jahr nach Beendigung der Grundimmunisierung deutliche Hinweise auf eine Abnahme des Impfschutzes. Bis 2007 lagen die Abschätzungen der Wirksamkeit in den Altersgruppen von 1-18 Jahren, die während der ersten Immunisierungskampagne in Großbritannien eine Einzeldosis eines Meningokokken-C- Konjugatimpfstoffes erhalten hatten, zwischen 83 und 100 %. Die Daten zeigten während des Beobachtungszeitraums von ungefähr einem Jahr nach der Impfung keinen signifikanten Wirksamkeitsabfall innerhalb dieser Altersgruppen. Anwendungsbeobachtung nach einer Impfkampagne in den Niederlanden Im September 2002 starteten die Niederlande Routine-Meningokokken-C-Impfungen für Kleinkinder im Alter von 14 Monaten. Zusätzlich wurden zwischen Juni und November 2002 Impfkampagnen für 1-18jährige durchgeführt. Die Impfkampagne in den Niederlanden erreichte nahezu 3 Millionen Patienten (94 % Deckungsgrad). Die Durchseuchungsrate in den Niederlanden, wo ausschließlich NeisVac-C als Impfstoff benutzt wurde, sank, bezogen auf die Neuerkrankungsrate mit Meningokokken-Cerkrankungen, stark ab, bis 2008 keinerlei MenC-Erkrankungen mehr bei den mit NeisVac-C-Geimpften mehr auftraten Pharmakokinetische Eigenschaften Für Impfstoffe sind keine pharmakokinetischen Studien erforderlich Präklinische Daten zur Sicherheit Es gibt keine weiteren relevanten präklinischen Daten, die nicht bereits in anderen Abschnitten berücksichtigt wurden. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Natriumchlorid Wasser für Injektionszwecke 6.2 Inkompatibilitäten Da keine Verträglichkeitsstudien vorliegen, darf NeisVac-C nicht zusammen mit anderen Arzneimitteln in einer Spritze verabreicht werden. 6.3 Haltbarkeit 42 Monate 6.4. Besondere Vorsichtsmaßnahmen für die Aufbewahrung Im Kühlschrank bei 2 C bis 8 C lagern. Nicht einfrieren. Die Spritze im Umkarton aufbewahren Innerhalb des angegebenen Haltbarkeitszeitraums von 42 Monaten kann das Produkt einmalig bis zu 9 Monate lang bei Raumtemperatur (max. +25 C) aufbewahrt werden. Soll das Produkt bei Raumtemperatur (bis zu +25 C) gelagert werden, muss der Beginn des Lagerungszeitraums und das korrigierte Verfalldatum 9 Monate nach Beginn dieser Lagerungsart auf der Produktverpackung vermerkt werden. Das korrigierte Verfalldatum für die Lagerung bei Raumtemperatur darf die reguläre Haltbarkeitsdauer von 42 Monaten nicht überschreiten. 6.5 Art und Inhalt des Behältnisses NeisVac-C liegt als 0,5 ml Suspension in einer Fertigspritze ohne Kanüle (Glas, hydrolytische Klasse I) mit Schutzkappe (Brombutylgummi) und Kolbenstopfen (Brombutylgummi) vor und ist in Packungen mit 1, 10 oder 20 Stück erhältlich. Die Packung mit einem Stück kann zwei Nadeln unterschiedlicher Größe enthalten. Es wird empfohlen, die kleinere Nadel (0,50 x 16 mm) zur Injektion bei Kindern zu benutzen und die größere (0,60 x 25 mm) zur Impfung von Erwachsenen zu verwenden. Beide Nadeln sind steril und dienen zum einmaligen Gebrauch. Die Primärverpackung ist latexfrei.
8 Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Hinweise für die Handhabung Während der Lagerung können sich ein weißer Niederschlag und ein klarer Überstand voneinander absetzen. Um eine homogene Suspension zu erhalten, die Spritze mit dem Impfstoff vor Verabreichung gut schütteln und auf sichtbare Partikel und/oder ungewöhnliches Aussehen überprüfen. Wird eines von beiden bemerkt, die Spritze verwerfen. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den nationalen Anforderungen zu entsorgen. 7. INHABER DER ZULASSUNG UND HERSTELLER Importiert, umgepackt und vertrieben von: CC Pharma GmbH, D Densborn Mitvertrieb: Pharma Gerke GmbH, D Grevenbroich 8. ZULASSUNGSNUMMER PEI.H DATUM DER ERTEILUNG DER ZULASSUNG/ LETZTE VERLÄNGERUNG DER ZULASSUNG STAND DER INFORMATION Januar VERSCHREIBUNGSPFLICHT/APOTHEKENPFLICHT Verschreibungspflichtig
Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem Antigenhalt)
 Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS NeisVac-C 1
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS NeisVac-C 1 1. BEZEICHNUNG DES ARZNEIMITTELS NeisVac-C 0,5 ml Suspension zur Injektion in einer Fertigspritze ohne Kanüle Adsorbierter Meningokokken-Gruppe-C-Polysaccharid-Konjugatimpfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS NeisVac-C 1 1. BEZEICHNUNG DES ARZNEIMITTELS NeisVac-C 0,5 ml Suspension zur Injektion in einer Fertigspritze ohne Kanüle Adsorbierter Meningokokken-Gruppe-C-Polysaccharid-Konjugatimpfstoff
Vi-Polysaccharid von Salmonella typhi (Ty2 Stamm)
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
FACHINFORMATION. werden. Vorsichtsmaßnahmen vor der Handhabung oder Verabreichung des Arzneimittels. Der Impfstoff darf nicht subkutan oder intravenös
 1. BEZEICHNUNG DES ARZNEIMITTELS 0,5 ml Suspension zur Injektion in einer FertigspritzeohneKanüle Adsorbierter Meningokokken-Gruppe-C- Polysaccharid-Konjugatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS 0,5 ml Suspension zur Injektion in einer FertigspritzeohneKanüle Adsorbierter Meningokokken-Gruppe-C- Polysaccharid-Konjugatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Fachinformation. 32 D-Antigen²-Einheiten³. Antigenmenge im Endprodukt (Final Bulk Product), gemäß WHO (TRS 673, 1982) 3
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. Qualitative und quantitative Zusammensetzung 1 Impfdosis (0,5 ml) enthält: Wirkstoffe:
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. Qualitative und quantitative Zusammensetzung 1 Impfdosis (0,5 ml) enthält: Wirkstoffe:
1. Was ist TdaP-IMMUN und wofür wird es angewendet?
 Page 1 of 6 Gebrauchsinformation: Information für Anwender TdaP-IMMUN Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis- (azelluläre Komponente) Impfstoff (adsorbiert, reduzierter
Page 1 of 6 Gebrauchsinformation: Information für Anwender TdaP-IMMUN Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis- (azelluläre Komponente) Impfstoff (adsorbiert, reduzierter
Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert)
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Meningitec Injektionssuspension in Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert)
 1. BEZEICHNUNG DES ARZNEIMITTELS Meningitec Injektionssuspension in Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS Meningitec Injektionssuspension in Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
Fachinformation IPV Mérieux Stand: Juli 2010
 Fachinformation IPV Mérieux Stand: Juli 2010 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE
Fachinformation IPV Mérieux Stand: Juli 2010 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE
Fachinformation. Internationale Einheiten, untere Vertrauensgrenze (p=0,95) der nach der Methode der Ph.Eur. ermittelten Wirksamkeit
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) 2. Qualitative und quantitative
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) 2. Qualitative und quantitative
FACHINFORMATION IPV Mérieux 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 FACHINFORMATION IPV Mérieux 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
FACHINFORMATION IPV Mérieux 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
WOFÜR WIRD ES ANGEWENDET?
 Gebrauchsinformation: Information für die Anwenderin/den Anwender Suspension zur Injektion in einer Fertigspritze ohne Kanüle Adsorbierter Meningokokken-Gruppe C-Polysaccharid-Konjugatimpfstoff Lesen Sie
Gebrauchsinformation: Information für die Anwenderin/den Anwender Suspension zur Injektion in einer Fertigspritze ohne Kanüle Adsorbierter Meningokokken-Gruppe C-Polysaccharid-Konjugatimpfstoff Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis-Adsorbatimpfstoff für Säuglinge (ab 2 Monaten) und Kinder (bis 6 Jahre) Lesen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis-Adsorbatimpfstoff für Säuglinge (ab 2 Monaten) und Kinder (bis 6 Jahre) Lesen
Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
 Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für den Anwender. Polio-Salk Mérieux - Fertigspritze Poliomyelitis-Impfstoff (inaktiviert)
 Gebrauchsinformation: Information für den Anwender Polio-Salk Mérieux - Fertigspritze Poliomyelitis-Impfstoff (inaktiviert) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
Gebrauchsinformation: Information für den Anwender Polio-Salk Mérieux - Fertigspritze Poliomyelitis-Impfstoff (inaktiviert) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
FACHINFORMATION. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen
 FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
1. BEZEICHNUNG DES ARZNEIMITTELS 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 3. DARREICHUNGSFORM 4. KLINISCHE ANGABEN
 1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 720 Kinder Injektionssuspension Hepatitis-A-Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5ml) enthält: Hepatitis-A-Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 720 Kinder Injektionssuspension Hepatitis-A-Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5ml) enthält: Hepatitis-A-Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert)
 1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (1,0 ml) enthält: Hepatitis A Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (1,0 ml) enthält: Hepatitis A Virus
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Influenzavirus-Oberflächenantigene (Hämagglutinin und Neuraminidase), der folgenden Stämme*:
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS BEGRIPAL Injektionssuspension in Fertigspritze Influenza-Impfstoff (Oberflächenantigen, inaktiviert) (Saison 2013/2014) 2.
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS BEGRIPAL Injektionssuspension in Fertigspritze Influenza-Impfstoff (Oberflächenantigen, inaktiviert) (Saison 2013/2014) 2.
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC)
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
FACHINFORMATION 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis Adsorbatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Impfdosis
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis Adsorbatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Impfdosis
Tetravac. 1. Bezeichnung des Arzneimittels. 2. Qualitative und quantitative Zusammensetzung. 3. Darreichungsform
 1. Bezeichnung des Arzneimittels, Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis (inaktiviert)-adsorbat-impfstoff 2. Qualitative und quantitative Zusammensetzung
1. Bezeichnung des Arzneimittels, Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis (inaktiviert)-adsorbat-impfstoff 2. Qualitative und quantitative Zusammensetzung
FACHINFORMATION REVAXiS
 FACHINFORMATION REVAXiS 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt)
FACHINFORMATION REVAXiS 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt)
DARF AUF KEINEN FALL INTRAVENÖS ODER SUBKUTAN VERABREICHT WERDEN!
 NeisVacC Injektionssuspension in einer Fertigspritze 2. Qualitative und quantitative Zusammensetzung 1 Dosis (= 0,5 ml) enthält: Neisseria meningitidis Gruppe C (Stamm C11) Polysaccharid (deoacetyliert)
NeisVacC Injektionssuspension in einer Fertigspritze 2. Qualitative und quantitative Zusammensetzung 1 Dosis (= 0,5 ml) enthält: Neisseria meningitidis Gruppe C (Stamm C11) Polysaccharid (deoacetyliert)
Sanofi Pasteur MSD GmbH 1. BEZEICHNUNG DES ARZNEIMITTELS
 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis(inaktiviert)-Adsorbat-Impfstoff (reduzierter Antigengehalt) 2. QUALITATIVE UND QUANTITATIVE
1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis(inaktiviert)-Adsorbat-Impfstoff (reduzierter Antigengehalt) 2. QUALITATIVE UND QUANTITATIVE
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels)
 1 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Xanaflu Saison 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Impfstoff aus Oberflächenantigen
1 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Xanaflu Saison 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Impfstoff aus Oberflächenantigen
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS: FLUAD, Injektionssuspension in einer Fertigspritze Influenza-Impfstoff, Oberflächenantigene, inaktiviert, mit MF59C.1 als
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS: FLUAD, Injektionssuspension in einer Fertigspritze Influenza-Impfstoff, Oberflächenantigene, inaktiviert, mit MF59C.1 als
Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Einzeldosisbehältnis
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Einzeldosisbehältnis Polysaccharid-Impfstoff gegen
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Einzeldosisbehältnis Polysaccharid-Impfstoff gegen
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG. Influenzavirus Oberflächenantigene (Hämagglutinin und Neuroaminidase) der folgenden Stämme*:
 1. BEZEICHNUNG DES ARZNEIMITTELS Sandovac Injektionssuspension in einer Fertigspritze Influenzaimpfstoff (Oberflächenantigene, inaktiviert) (2014/2015) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Influenzavirus
1. BEZEICHNUNG DES ARZNEIMITTELS Sandovac Injektionssuspension in einer Fertigspritze Influenzaimpfstoff (Oberflächenantigene, inaktiviert) (2014/2015) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Influenzavirus
Sonstige Bestandteile: Eine vollständige Auflistung der sonstigen Bestandteile finden Sie unter Abschnitt 6.1.
 ZUSAMMENFASSUNG DER PRODUKTEIGENSCHAFTEN 1. BEZEICHNUNG DES TIERARZNEIMITTELS Equilis Tetanus-Vaccine Injektionssuspension für Pferde, Rinder, Schafe, Schweine und Hunde 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER PRODUKTEIGENSCHAFTEN 1. BEZEICHNUNG DES TIERARZNEIMITTELS Equilis Tetanus-Vaccine Injektionssuspension für Pferde, Rinder, Schafe, Schweine und Hunde 2. QUALITATIVE UND QUANTITATIVE
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS NeisVacC Injektionssuspension in einer Fertigspritze 0,5 ml adsorbierter Meningokokken Serogruppe C PolysaccharidKonjugatimpfstoff
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS NeisVacC Injektionssuspension in einer Fertigspritze 0,5 ml adsorbierter Meningokokken Serogruppe C PolysaccharidKonjugatimpfstoff
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Synflorix Injektionssuspension in einer Fertigspritze Pneumokokkenpolysaccharid-Konjugatimpfstoff (adsorbiert)
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Synflorix Injektionssuspension in einer Fertigspritze Pneumokokkenpolysaccharid-Konjugatimpfstoff (adsorbiert)
Meningitec 0,5 ml Injektionssuspension in einer Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2.
 Meningitec 0,5 ml Injektionssuspension in einer Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung Eine Dosis (0,5 ml)
Meningitec 0,5 ml Injektionssuspension in einer Fertigspritze Meningokokken Serogruppe C Oligosaccharid Konjugatimpfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung Eine Dosis (0,5 ml)
1 Impfdosis (0,5 ml) enthält: inaktivierte Influenza-Virus Spaltantigene* der folgenden Stämme:
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Gebrauchsinformation: Information für Patienten und Anwender
 Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
FACHINFORMATION. Wirkstoffe: Haemophilus influenzae Typ b-polysaccharide (Polyribosylribitolphosphat) konjugiert an
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Act-HIB Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Haemophilus influenzae Typ b-konjugatimpfstoff 2.
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Act-HIB Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Haemophilus influenzae Typ b-konjugatimpfstoff 2.
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Suspension zur Injektion in einer Fertigspritze Adsorbierter Meningokokken-Gruppe C-Polysaccharid-Konjugatimpfstoff Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Suspension zur Injektion in einer Fertigspritze Adsorbierter Meningokokken-Gruppe C-Polysaccharid-Konjugatimpfstoff Lesen Sie die gesamte Packungsbeilage
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC)
 1. BEZEICHNUNG DES ARZNEIMITTELS 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugat-Impfstoff gegen Meningokokken der Gruppe C 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugat-Impfstoff gegen Meningokokken der Gruppe C 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Fachinformation. mind. 30 Internationale Einheiten (I.E.) Tetanus-Toxoid 1
 1. BEZEICHNUNG DES ARZNEIMITTELS - Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie-Tetanus- (azellulärer) Pertussis-, Poliomyelitis (inaktiviert)- und Haemophilus-influenzae-Typ
1. BEZEICHNUNG DES ARZNEIMITTELS - Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie-Tetanus- (azellulärer) Pertussis-, Poliomyelitis (inaktiviert)- und Haemophilus-influenzae-Typ
FACHINFORMATION. adsorbiert an Aluminiumhydroxid 0,3 bis 0,4 mg Al 3+
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS MENJUGATE KIT 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugat-Impfstoff gegen Meningokokken der Gruppe C 2. QUALITATIVE
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS MENJUGATE KIT 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugat-Impfstoff gegen Meningokokken der Gruppe C 2. QUALITATIVE
Fachinformation. 8 D-Antigeneinheiten Typ 3 (Saukett) 2. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Boostrix Polio Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten) und Poliomyelitis (inaktivierter)-
Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Boostrix Polio Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten) und Poliomyelitis (inaktivierter)-
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Meningokokken-Impfstoff A + C Mérieux
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningokokken-Impfstoff A + C Mérieux Lyophilisat (Trockensubstanz) und Lösungsmittel zur Herstellung einer Injektionssuspension Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningokokken-Impfstoff A + C Mérieux Lyophilisat (Trockensubstanz) und Lösungsmittel zur Herstellung einer Injektionssuspension Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis-Adsorbatimpfstoff für Säuglinge (ab 2 Monaten) und Kinder (bis 6 Jahre) Lesen Sie
Gebrauchsinformation: Information für Anwender Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis-Adsorbatimpfstoff für Säuglinge (ab 2 Monaten) und Kinder (bis 6 Jahre) Lesen Sie
Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften)
 F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS Influvac - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff aus inaktivierten Oberflächenantigenen)
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS Influvac - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff aus inaktivierten Oberflächenantigenen)
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tetanol pur Injektionssuspension in einer Fertigspritze 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: Tetanus-Toxoid
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tetanol pur Injektionssuspension in einer Fertigspritze 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: Tetanus-Toxoid
Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt
 1. BEZEICHNUNG DES ARZNEIMITTELS Td-pur Injektionssuspension in Fertigspritze Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS Td-pur Injektionssuspension in Fertigspritze Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Epaxal - Suspension zur Injektion in einer Fertigspritze Hepatitis A-Impfstoff (inaktiviert, virosomal)
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Epaxal - Suspension zur Injektion in einer Fertigspritze Hepatitis A-Impfstoff (inaktiviert, virosomal)
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
Gebrauchsinformation: Information für Anwender. Inaktivierter Poliomyelitis-Impfstoff
 Gebrauchsinformation: Information für Anwender IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Act-HIB 10 Mikrogramm/0,5 ml, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Konjugatimpfstoff gegen Haemophilus influenzae Typ b Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Act-HIB 10 Mikrogramm/0,5 ml, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Konjugatimpfstoff gegen Haemophilus influenzae Typ b Lesen Sie
Fachinformation 1. Bezeichnung des Arzneimittels
 Anlage zu Zulassungsbescheid Zul.-Nr. PEI.H.04338.01.1 5/16 Fachinformation 1. Bezeichnung des Arzneimittels TETRAVAC Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis
Anlage zu Zulassungsbescheid Zul.-Nr. PEI.H.04338.01.1 5/16 Fachinformation 1. Bezeichnung des Arzneimittels TETRAVAC Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis
Meningokokken Oligosaccharid Konjugatimpfstoff der Serogruppe C (adsorbiert)
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningitec Injektionssuspension in Fertigspritze Meningokokken Oligosaccharid Konjugatimpfstoff der Serogruppe C (adsorbiert) Lesen Sie die gesamte Gebrauchsinformation
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningitec Injektionssuspension in Fertigspritze Meningokokken Oligosaccharid Konjugatimpfstoff der Serogruppe C (adsorbiert) Lesen Sie die gesamte Gebrauchsinformation
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Act-HIB 10 Mikrogramm/0,5 ml, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Konjugatimpfstoff gegen Haemophilus influenzae Typ b Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Act-HIB 10 Mikrogramm/0,5 ml, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Konjugatimpfstoff gegen Haemophilus influenzae Typ b Lesen Sie
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
Diphtherie-, Tetanus- (azellulärer) Pertussis-, Poliomyelitis (inaktiviert)- und Haemophilus-influenzae-Typ b-konjugatimpfstoff (adsorbiert)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS (Fachinformation) 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix -IPV+Hib Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie-, Tetanus-
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS (Fachinformation) 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix -IPV+Hib Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie-, Tetanus-
Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV)
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften)
 F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS FluVaccinol Subunit Impfstoff - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS FluVaccinol Subunit Impfstoff - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff
GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde
 GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
Gebrauchsinformation: Information für Anwender. Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff
 Gebrauchsinformation: Information für Anwender Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Für Kinder ab 2 Jahren und Erwachsene Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Für Kinder ab 2 Jahren und Erwachsene Lesen Sie die gesamte
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS)
 FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS) 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP Injektionssuspension in einer Fertigspritze Influenza Impfstoff (Spaltimpfstoff, inaktiviert).
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS) 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP Injektionssuspension in einer Fertigspritze Influenza Impfstoff (Spaltimpfstoff, inaktiviert).
Gebrauchsinformation: Information für Anwender. dt-reduct Mérieux Injektionssuspension in einer Fertigspritze
 Gebrauchsinformation: Information für Anwender dt-reduct Mérieux Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender dt-reduct Mérieux Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Lesen Sie die gesamte Packungsbeilage
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135
AHAG I ZUSAMMEFASSUG DER MERKMALE DES ARZEIMITTELS 1 1. BEZEICHUG DES ARZEIMITTELS - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135
Impfstoffe. Einfachimpfstoffe Mehrfachimpfstoffe
 Impfstoffe 1.1 1.2 Einfachimpfstoffe Mehrfachimpfstoffe 1.1 Einfachimpfstoffe CERVARIX. Injektionssuspension zur Prävention von prämalignen Läsionen der Zervix und von Zervixkarzinomen, die durch die Typen
Impfstoffe 1.1 1.2 Einfachimpfstoffe Mehrfachimpfstoffe 1.1 Einfachimpfstoffe CERVARIX. Injektionssuspension zur Prävention von prämalignen Läsionen der Zervix und von Zervixkarzinomen, die durch die Typen
Influenzavirus-Oberflächenantigene (Hämagglutinin und Neuraminidase), der Stämme*:
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Begripal, Injektionssuspension in Fertigspritze Influenza-Impfstoff, Oberflächenantigen, inaktiviert (Saison 2017/2018) 2.
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Begripal, Injektionssuspension in Fertigspritze Influenza-Impfstoff, Oberflächenantigen, inaktiviert (Saison 2017/2018) 2.
FACHINFORMATION. 1 Hartkapsel enthält: 6 mg lysierte immunaktive Fraktionen aus ausgewählten Escherichia-coli-Stämmen.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
- 1 - FACHINFORMATION
 - 1 - FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix -IPV+Hib Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie (D)-Tetanus (T)- (azellulärer) Pertussis (Pa)-, Poliomyelitis
- 1 - FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix -IPV+Hib Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie (D)-Tetanus (T)- (azellulärer) Pertussis (Pa)-, Poliomyelitis
40 D-Antigeneinheiten Typ 2 (MEF-1-Stamm) 2 8 D-Antigeneinheiten Typ 3 (Saukett-Stamm) 2
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS (Fachinformation) 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix -IPV+Hib Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie (D)-, Tetanus
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS (Fachinformation) 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix -IPV+Hib Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie (D)-, Tetanus
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für Kinder
Gebrauchsinformation: Information für Anwender REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für Kinder
Gebrauchsinformation: Information für den Anwender. Hepatyrix Injektionssuspension
 Gebrauchsinformation: Information für den Anwender Hepatyrix Injektionssuspension Kombinierter Hepatitis A (inaktiviert) und Typhus-Vi- Polysaccharid Impfstoff (adsorbiert) Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender Hepatyrix Injektionssuspension Kombinierter Hepatitis A (inaktiviert) und Typhus-Vi- Polysaccharid Impfstoff (adsorbiert) Lesen Sie die gesamte Packungsbeilage
2 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Page 1 of 8 FACHINFORMATION 1 BEZEICHNUNG DES ARZNEIMITTELS Tuberkulin PPD RT23 SSI 2 T.E./0,1 ml, Injektionslösung. Tuberkulin PPD RT23 SSI 10 T.E./0,1 ml, Injektionslösung. 2 QUALITATIVE UND QUANTITATIVE
Page 1 of 8 FACHINFORMATION 1 BEZEICHNUNG DES ARZNEIMITTELS Tuberkulin PPD RT23 SSI 2 T.E./0,1 ml, Injektionslösung. Tuberkulin PPD RT23 SSI 10 T.E./0,1 ml, Injektionslösung. 2 QUALITATIVE UND QUANTITATIVE
Mumpsviren, Stamm RIT , abgeleitet vom Stamm Jeryl Lynn (lebend, attenuiert) mindestens 10 3,7 ZKID 50
 1. BEZEICHNUNG DES ARZNEIMITTELS MMR-PRIORIX - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis
1. BEZEICHNUNG DES ARZNEIMITTELS MMR-PRIORIX - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis
FACHINFORMATION. Kinder und Jugendliche
 1. BEZEICHNUNG DES ARZNEIMITTELS Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
1. BEZEICHNUNG DES ARZNEIMITTELS Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
FACHINFORMATION. Kinder und Jugendliche
 1. BEZEICHNUNG DES ARZNEIMITTELS Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) 2. QUALITATIVE
1. BEZEICHNUNG DES ARZNEIMITTELS Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) 2. QUALITATIVE
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Td-Impfstoff Mérieux Injektionssuspension Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Für Kinder ab 5 Jahren und Erwachsene Lesen Sie
Gebrauchsinformation: Information für Anwender Td-Impfstoff Mérieux Injektionssuspension Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Für Kinder ab 5 Jahren und Erwachsene Lesen Sie
Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. QUALITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. QUALITATIVE
Prevenar 13 Injektionssuspension
 Gebrauchsinformation: Information für Anwender Prevenar 13 Injektionssuspension Pneumokokkenpolysaccharid-Konjugatimpfstoff (13valent, adsorbiert) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender Prevenar 13 Injektionssuspension Pneumokokkenpolysaccharid-Konjugatimpfstoff (13valent, adsorbiert) Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
720 ELISA-Einheiten Hepatitis-B-Oberflächenantigen 3,4
 Twinrix Erwachsene, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung 1 Dosis (1 ml) enthält: Hepatitis-A-Virus
Twinrix Erwachsene, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung 1 Dosis (1 ml) enthält: Hepatitis-A-Virus
GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension
 GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
Menjugate 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugatimpfstoff gegen Meningokokken der Serogruppe C
 PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Menjugate 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugatimpfstoff gegen Meningokokken der Serogruppe
PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Menjugate 10 Mikrogramm Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Konjugatimpfstoff gegen Meningokokken der Serogruppe
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Gebrauchsinformation: Information für Anwender. Typhim Vi Injektionslösung in einer Fertigspritze. Typhus-Polysaccharid-Impfstoff
 Gebrauchsinformation: Information für Anwender Typhim Vi Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr
Gebrauchsinformation: Information für Anwender Typhim Vi Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 [Version 7.3.2, 10/2011] ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Theranekron D6 Injektionslösung für Tiere 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
[Version 7.3.2, 10/2011] ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Theranekron D6 Injektionslösung für Tiere 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung. Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die Packungsbeilage sorgfältig durch, bevor Sie oder Ihr Kind
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die Packungsbeilage sorgfältig durch, bevor Sie oder Ihr Kind
GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN/DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN/DEN ANWENDER Repevax Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Poliomyelitis (inaktiviert)-impfstoff
GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN/DEN ANWENDER Repevax Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Poliomyelitis (inaktiviert)-impfstoff
Lyseen Injektionssuspension
 Gebrauchsinformation: Information für den Anwender Lyseen Injektionssuspension Wirkstoff: Inaktivierte Keime spezifizierter Lactobacillus-Stämme Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für den Anwender Lyseen Injektionssuspension Wirkstoff: Inaktivierte Keime spezifizierter Lactobacillus-Stämme Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender. HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem Impfstoff
Gebrauchsinformation: Information für Anwender HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem Impfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Menjugate 10 Mikrogramm Injektionssuspension Menjugate 10 Mikrogramm Injektionssuspension in einer Fertigspritze Adsorbierter
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Menjugate 10 Mikrogramm Injektionssuspension Menjugate 10 Mikrogramm Injektionssuspension in einer Fertigspritze Adsorbierter
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS PREFLUCEL Injektionssuspension in einer Fertigspritze Influenza-Impfstoff (Spaltimpfstoff, inaktiviert,
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS PREFLUCEL Injektionssuspension in einer Fertigspritze Influenza-Impfstoff (Spaltimpfstoff, inaktiviert,
