ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
|
|
|
- Eugen Krause
- vor 6 Jahren
- Abrufe
Transkript
1 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1
2 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Dosis (0,5 ml) enthält: Hepatitis B-Virus-Oberflächenantigen, rekombinant (HBsAg)*...5 Mikrogramm Adsorbiert an amorphes Aluminiumhydroxyphosphat-Sulfat (0,25 Milligramm Al 3+ ) * hergestellt in Saccharomyces cerevisiae (Stamm )-Hefezellen durch rekombinante DNS- Technologie Während der Herstellung werden Formaldehyd und Kaliumthiocyanat verwendet; Spuren dieser Stoffe können im Impfstoff vorhanden sein. Siehe Abschnitte 4.3, 4.4 und 4.8. Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Injektionssuspension Leicht trübe, weiße Suspension 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete HBVAXPRO ist indiziert zur aktiven Immunisierung gegen eine Infektion mit dem Hepatitis B-Virus einschließlich aller bekannten Subtypen bei Personen von der Geburt bis zu einem Alter von 15 Jahren, die besonders durch eine Infektion mit dem Hepatitis B-Virus gefährdet sind. Die Impfung von besonders gefährdeten Risikogruppen sollte entsprechend den offiziellen Impfempfehlungen durchgeführt werden. Man geht davon aus, dass eine Impfung mit HBVAXPRO auch gegen Hepatitis D schützt, da Hepatitis D (verursacht durch den Delta-Erreger) ohne eine Hepatitis B-Infektion nicht auftritt. 4.2 Dosierung und Art der Anwendung Dosierung Personen von der Geburt bis zu einem Alter von 15 Jahren: 1 Dosis (0,5 ml) pro Injektion Grundimmunisierung: Eine vollständige Grundimmunisierung besteht aus mindestens drei Injektionen. Die beiden folgenden Impfschemata werden empfohlen: 0, 1, 6 Monate: zwei Dosen im Abstand von jeweils einem Monat; eine dritte Dosis 6 Monate nach der ersten Dosis 2
3 0, 1, 2, 12 Monate: drei Dosen im Abstand von jeweils einem Monat; eine vierte Dosis 12 Monate nach der ersten Dosis Es wird empfohlen, den Impfstoff entsprechend den angegebenen Impfschemata zu verabreichen. Kinder, die entsprechend dem beschleunigten Impfschema (0, 1, 2 Monate) geimpft werden, müssen zur Bildung von höheren Antikörperkonzentrationen in Monat 12 eine Auffrischimpfung erhalten. Auffrischimpfung: Geimpfte Personen mit intaktem Immunsystem Derzeit ist nicht bekannt, ob bei gesunden geimpften Personen mit vollständiger Grundimmunisierung eine Auffrischimpfung erforderlich ist. Einige offizielle Impfprogramme empfehlen jedoch regelmäßige Auffrischimpfungen, die beachtet werden sollten. Geimpfte Personen mit geschwächtem Immunsystem (z. B. Dialysepatienten, Patienten nach Organtransplantationen, AIDS-Patienten) Bei geimpften Personen mit einem geschwächten Immunsystem muss die Verabreichung von zusätzlichen Dosen in Betracht gezogen werden, sobald die Antikörperkonzentration gegen das Hepatitis B-Virus-Oberflächenantigen (anti-hbsag) unter 10 I.E./l abfällt. Wiederholungsimpfung bei Non-Respondern Wenn Personen, die nach einer vollständigen Grundimmunisierung keine Antikörper bilden, erneut geimpft werden, kommt es bei % nach Gabe einer zusätzlichen Dosis und bei % nach Gabe von drei zusätzlichen Dosen zu einer ausreichenden Antikörperbildung. Weil es jedoch keine ausreichenden Daten über die Unbedenklichkeit von Hepatitis B-Impfstoffen gibt, wenn mehr als die empfohlene Anzahl von Dosen gegeben werden, wird eine Wiederholungsimpfung nach einer abgeschlossenen Grundimmunisierung nicht routinemäßig empfohlen. Wiederholungsimpfungen sollten bei Personen mit einem hohen Risiko durchgeführt werden; zuvor sollte der Nutzen der Impfung gegen das mögliche Risiko von erhöhten lokalen oder systemischen Nebenwirkungen abgewogen werden. Spezielle Impfschemata werden empfohlen: Folgendes Impfschema wird für Neugeborene von Müttern, die Hepatitis B-Virusträger sind, empfohlen - Eine Dosis Hepatitis B-Immunglobulin unmittelbar nach der Geburt (innerhalb der ersten 24 Stunden). - Die erste Dosis eines Hepatitis B-Impfstoffs sollte innerhalb von 7 Tagen nach der Geburt gegeben werden; der Impfstoff kann gleichzeitig mit Hepatitis B-Immunglobulin gegeben werden, die Injektionen sollten jedoch an unterschiedlichen Körperstellen erfolgen. - Weitere Impfungen sollten entsprechend den offiziellen Empfehlungen verabreicht werden. Folgendes Impfschema wird nach bekannter oder vermuteter Hepatitis B-Virus-Exposition (Verletzungen durch kontaminierte Gegenstände, wie z. B. eine Nadelstichverletzung) empfohlen - Eine Dosis Hepatitis B-Immunglobulin unmittelbar nach Exposition (innerhalb der ersten 24 Stunden). - Die erste Dosis eines Hepatitis B-Impfstoffs sollte innerhalb von 7 Tagen nach der Exposition gegeben werden; der Impfstoff kann gleichzeitig mit Hepatitis B-Immunglobulin gegeben werden, die Injektionen sollten jedoch an unterschiedlichen Körperstellen erfolgen. 3
4 - Serologische Testung wird auch bei Gabe von möglicherweise erforderlichen weiteren Impfdosen für den Kurz- bzw. Langzeitschutz empfohlen (abhängig vom Serostatus des Patienten). - Bei nicht oder unvollständig geimpften Personen sollten die erforderlichen Dosen gemäß dem empfohlenen Impfschema verabreicht werden. Das beschleunigte Impfschema, einschließlich einer Auffrischimpfung in Monat 12, kann angewendet werden. Art der Anwendung Der Impfstoff wird intramuskulär verabreicht. Bei Neugeborenen und Kleinkindern wird empfohlen, in den anterolateralen Bereich des Oberschenkels zu impfen. Bei Kindern und Jugendlichen wird empfohlen, in den Delta-Muskel zu impfen. Der Impfstoff darf nicht intravasal verabreicht werden. Bei Patienten mit Thrombozytopenie oder bei Personen mit Blutungsneigung kann der Impfstoff ausnahmsweise auch subkutan verabreicht werden. Vorsichtsmaßnahmen bei der Handhabung / vor der Anwendung des Impfstoffs, siehe Abschnitt Gegenanzeigen - Bekannte Überempfindlichkeit gegen den Wirkstoff, einen der sonstigen Bestandteile oder einen Restbestandteil aus der Herstellung (z. B. Formaldehyd und Kaliumthiocyanat), siehe Abschnitte 6.1 und 2. - Die Impfung sollte bei Personen mit einer schweren, mit Fieber einhergehenden oder akuten Erkrankung verschoben werden. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Wie bei allen Impfstoffen, die durch Injektion verabreicht werden, sollten geeignete Behandlungsmaßnahmen für den Fall von seltenen anaphylaktischen Reaktionen nach Gabe des Impfstoffs bereitstehen (siehe Abschnitt 4.8). Während der Herstellung werden Formaldehyd und Kaliumthiocyanat verwendet; Spuren dieser Stoffe können im Impfstoff vorhanden sein. Dadurch können Überempfindlichkeitsreaktionen auftreten (siehe Abschnitte 2 und 4.8). Der Gummistopfen des Fläschchens wird aus latexhaltigem, getrocknetem Naturkautschuk hergestellt und kann bei latexempfindlichen Personen allergische Reaktionen auslösen. Bezüglich der Verlaufs- oder Laborkontrolle von immunsupprimierten Personen oder Personen, bei denen bekannt ist oder vermutet wird, dass sie Kontakt mit dem Hepatitis B-Virus hatten, siehe Abschnitt 4.2. Bei der Grundimmunisierung von sehr unreifen Frühgeborenen (Geburt 28. Schwangerschaftswoche), insbesondere von solchen mit einer Lungenunreife in der Vorgeschichte, sollte das potenzielle Risiko einer Apnoe berücksichtigt und die Notwendigkeit einer Atemüberwachung über 48 bis 72 Stunden erwogen werden (siehe Abschnitt 4.8). Da der Nutzen der Impfung gerade bei dieser Säuglingsgruppe hoch ist, sollte die Impfung Frühgeborenen nicht vorenthalten und auch nicht aufgeschoben werden. Aufgrund der langen Inkubationszeit einer Hepatitis B ist es möglich, dass zum Zeitpunkt der Impfung bereits eine nicht erkannte Infektion vorliegt. Der Impfstoff kann in solchen Fällen eine Hepatitis B- Infektion nicht verhindern. 4
5 Der Impfstoff schützt nicht vor Infektionen mit anderen Erregern, wie dem Hepatitis A-, Hepatitis C- und Hepatitis E-Virus oder mit sonstigen Erregern, die zu einer Infektion der Leber führen können. Bei der Anwendung in der Schwangerschaft oder während der Stillzeit ist Vorsicht geboten (siehe Abschnitt 4.6). 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Der Impfstoff kann wie folgt verabreicht werden: - gleichzeitig mit Hepatitis B-Immunglobulin an unterschiedlichen Körperstellen - zur Vervollständigung der Grundimmunisierung oder zur Auffrischimpfung bei Personen, die zuvor mit einem anderen Hepatitis B-Impfstoff geimpft wurden - gleichzeitig mit anderen Impfstoffen. In diesem Fall sind unterschiedliche Körperstellen und Spritzen zu verwenden. Die gleichzeitige Verabreichung eines konjugierten Pneumokokken-Impfstoffs (PREVENAR) mit Hepatitis B-Impfstoff gemäß dem 0, 1 und 6 Monats- bzw. dem 0, 1, 2 und 12 Monats-Impfschema wurde nicht ausreichend untersucht. 4.6 Fertilität, Schwangerschaft und Stillzeit Fertilität: HBVAXPRO wurde nicht in Fertilitätsstudien untersucht. Schwangerschaft: Es liegen keine klinischen Daten über die Anwendung von HBVAXPRO während der Schwangerschaft vor. Der Impfstoff sollte während der Schwangerschaft nur nach sorgfältiger Nutzen-Risiko-Abwägung verabreicht werden. Stillzeit: Es liegen keine klinischen Daten über die Anwendung von HBVAXPRO während der Stillzeit vor. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Jedoch ist davon auszugehen, dass HBVAXPRO keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen hat. 4.8 Nebenwirkungen a. Zusammenfassung des Verträglichkeitsprofils Die häufigsten Nebenwirkungen traten an der Injektionsstelle auf: vorübergehende Schmerzhaftigkeit, Erythem, Verhärtung. b. Tabellarische Zusammenfassung der Nebenwirkungen Die im Folgenden genannten Nebenwirkungen wurden nach der breiten Anwendung des Impfstoffs gemeldet. Wie bei anderen Hepatitis B-Impfstoffen auch konnte jedoch in vielen Fällen kein kausaler Zusammenhang zwischen der Impfung und dem Auftreten der Nebenwirkung hergestellt werden. 5
6 Nebenwirkungen Häufigkeit Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Lokalreaktionen (Injektionsstelle): vorübergehende Schmerzhaftigkeit, Häufig Rötung, Verhärtung (> 1/100, < 1/10) Müdigkeit, Fieber, Unwohlsein, grippeähnliche Symptome Sehr selten (< 1/10.000) Erkrankungen des Blutes und des Lymphsystems Thrombozytopenie, Lymphadenopathie Sehr selten (< 1/10.000) Erkrankungen des Immunsystems Serumkrankheit, anaphylaktische Reaktionen, Panarteriitis nodosa Sehr selten (< 1/10.000) Erkrankungen des Nervensystems Parästhesien, Lähmungserscheinungen (einschließlich Bell'sche Parese, Fazialisparese), periphere Neuropathien (Polyradikuloneuritis, Guillain-Barré-Syndrom), Neuritis (einschließlich Optikusneuritis), Myelitis (einschließlich transverser Myelitis), Enzephalitis, Sehr selten (< 1/10.000) demyelinisierende Erkrankungen des zentralen Nervensystems, Verschlechterung einer bestehenden Multiplen Sklerose, Multiple Sklerose, Krampfanfälle, Kopfschmerzen, Benommenheit, Synkopen Augenerkrankungen Uveitis Sehr selten (< 1/10.000) Gefäßerkrankungen Blutdruckabfall, Vaskulitis Sehr selten (< 1/10.000) Erkrankungen der Atemwege, des Brustraums und Mediastinums Bronchospasmus-ähnliche Symptome Sehr selten (< 1/10.000) Erkrankungen des Gastrointestinaltrakts Erbrechen, Übelkeit, Durchfall, Bauchschmerzen Sehr selten (< 1/10.000) Erkrankungen der Haut und des Unterhautzellgewebes Ausschlag, Alopezie, Pruritus, Urtikaria, Erythema multiforme, Sehr selten (< 1/10.000) Angioödem, Ekzem Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Arthralgien, Arthritis, Myalgien, Schmerzen in der Extremität, in die Sehr selten (< 1/10.000) geimpft wurde Untersuchungen Anstieg der Leberenzyme Sehr selten (< 1/10.000) c. Weitere spezielle Personenkreise Apnoe bei sehr unreifen Frühgeborenen (Geburt 28. Schwangerschaftswoche) (siehe Abschnitt 4.4) Meldung des Verdachts auf Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das in Anhang V aufgeführte nationale Meldesystem anzuzeigen. 4.9 Überdosierung Es wurde berichtet, dass HBVAXPRO in höherer Dosierung als empfohlen verabreicht wurde. Im Allgemeinen war das Nebenwirkungsprofil von HBVAXPRO bei Überdosierung vergleichbar mit dem bei empfohlener Dosierung. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Anti-Infektivum, ATC-Code: J07BC01 6
7 Der Impfstoff löst die Bildung von spezifischen humoralen Antikörpern gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) aus. Eine Antikörperkonzentration gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) von mindestens 10 I.E./l, gemessen ein bis zwei Monate nach der letzten Impfdosis, korreliert mit der Schutzwirkung vor Infektionen mit dem Hepatitis B-Virus. In klinischen Studien konnten bei 96 % von gesunden Kleinkindern, Kindern, Jugendlichen und Erwachsenen nach der Gabe von 3 Dosen einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck schützende Antikörper gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) nachgewiesen werden ( 10 I.E./l). In zwei Studien mit Kleinkindern, die nach unterschiedlichen Impfschemata und gleichzeitig mit anderen Impfstoffen geimpft wurden, entwickelten jeweils 97,5 % bzw. 97,2 % der Kinder schützende Antikörperkonzentrationen; die geometrischen Mittelwerte lagen jeweils bei 214 bzw. 297 I.E./l. Die Schutzwirkung einer Dosis Hepatitis B-Immunglobulin bei Geburt und der anschließenden Gabe von 3 Dosen einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck wurde für Neugeborene von Müttern nachgewiesen, die sowohl auf das Oberflächen- (HBsAg) als auch auf das e-antigen (HBeAg) des Hepatitis B-Virus positiv sind. Im Vergleich zu Infektionsraten mit unbehandelten historischen Kontrollen betrug die geschätzte Effektivität gegen eine chronische Hepatitis B-Infektion bei 130 geimpften Kleinkindern 95 %. Es ist nicht bekannt, wie lange die Schutzwirkung einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck bei gesunden geimpften Personen anhält; jedoch zeigten Untersuchungen an einer Gruppe von Risikopersonen, die mit einem ähnlichen, aus Plasma hergestellten Impfstoff geimpft waren, dass keine dieser Personen im Beobachtungszeitraum von 5 bis 9 Jahren an einer klinisch manifesten Hepatitis B-Infektion erkrankte. Das Vorhandensein eines durch die Impfung ausgelösten immunologischen Gedächtnisses für das Oberflächenantigen des Hepatitis B-Virus (HBsAg) wurde außerdem durch eine anamnestische Antikörperantwort auf eine Auffrischimpfung mit einer früheren Hepatitis B-Impfstoff-Formulierung nachgewiesen. Wie bei anderen Hepatitis B-Impfstoffen auch ist derzeit nicht bekannt, wie lange die Schutzwirkung bei gesunden Geimpften andauert. Außer der 12-Monats-Auffrischimpfung des beschleunigten Impfschemas (0, 1, 2 Monate) ist die Notwendigkeit weiterer Auffrischimpfungen noch nicht geklärt. Reduzierung des Risikos, an einem Leberzellkarzinom zu erkranken Die Erkrankung an einem Leberzellkarzinom ist eine schwere Komplikation einer Hepatitis B- Infektion. In Studien konnte der Zusammenhang zwischen einer chronischen Hepatitis B-Infektion und dem Auftreten eines Leberzellkarzinoms nachgewiesen werden; 80 % der Leberzellkarzinome werden durch eine Hepatitis B-Infektion hervorgerufen. Somit ist der Hepatitis B-Impfstoff der erste Impfstoff, der eine Krebserkrankung verhindert, da die Impfung vor dem Auftreten eines primären Leberzellkarzinoms schützen kann. 5.2 Pharmakokinetische Eigenschaften Nicht zutreffend 5.3 Präklinische Daten zur Sicherheit Tierversuche zu Embryotoxizität und Teratogenität wurden nicht durchgeführt. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Natriumchlorid Natriumtetraborat 7
8 Wasser für Injektionszwecke 6.2 Inkompatibilitäten Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden. 6.3 Dauer der Haltbarkeit 3 Jahre 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Im Kühlschrank lagern (2 C 8 C). Nicht einfrieren. 6.5 Art und Inhalt des Behältnisses 0,5 ml Suspension in einem Fläschchen (Glas) mit einem Stopfen (graues Butylgummi) und Aluminiumsiegel mit Plastik-Flip-off-Verschluss. Packungsgrößen: 1x1 und 10x1 Dosis 0,5 ml Suspension in einem Fläschchen (Glas) mit einem Stopfen (graues Butylgummi) und Aluminiumsiegel mit Plastik-Flip-off-Verschluss zusammen mit einer leeren sterilen Injektionsspritze mit Kanüle. Packungsgröße: 1x1 Dosis Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung Der Impfstoff sollte vor Verabreichung visuell auf Ausfällungen oder Verfärbungen untersucht werden. Gegebenenfalls sollte der Impfstoff nicht verabreicht werden. Vor Gebrauch sollte das Fläschchen gut geschüttelt werden. Nach Durchstechen des Fläschchens den Impfstoff in die Fertigspritze aufziehen und umgehend anwenden; das Fläschchen muss sachgerecht entsorgt werden. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den lokalen Anforderungen zu entsorgen. 7. INHABER DER ZULASSUNG MSD VACCINS 162 avenue Jean Jaurès Lyon Frankreich 8. ZULASSUNGSNUMMER(N) EU/1/01/183/001 EU/1/01/183/018 EU/1/01/183/019 8
9 9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG Datum der Erteilung der Zulassung: Datum der letzten Verlängerung der Zulassung: STAND DER INFORMATION Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur verfügbar. 9
10 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Dosis (0,5 ml) enthält: Hepatitis B-Virus-Oberflächenantigen, rekombinant (HBsAg)*...5 Mikrogramm Adsorbiert an amorphes Aluminiumhydroxyphosphat-Sulfat (0,25 Milligramm Al 3+ ) * hergestellt in Saccharomyces cerevisiae (Stamm )-Hefezellen durch rekombinante DNS- Technologie Während der Herstellung werden Formaldehyd und Kaliumthiocyanat verwendet; Spuren dieser Stoffe können im Impfstoff vorhanden sein. Siehe Abschnitte 4.3, 4.4 und 4.8. Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Injektionssuspension in einer Fertigspritze Leicht trübe, weiße Suspension 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete HBVAXPRO ist indiziert zur aktiven Immunisierung gegen eine Infektion mit dem Hepatitis B-Virus einschließlich aller bekannten Subtypen bei Personen von der Geburt bis zu einem Alter von 15 Jahren, die besonders durch eine Infektion mit dem Hepatitis B-Virus gefährdet sind. Die Impfung von besonders gefährdeten Risikogruppen sollte entsprechend den offiziellen Impfempfehlungen durchgeführt werden. Man geht davon aus, dass eine Impfung mit HBVAXPRO auch gegen Hepatitis D schützt, da Hepatitis D (verursacht durch den Delta-Erreger) ohne eine Hepatitis B-Infektion nicht auftritt. 4.2 Dosierung und Art der Anwendung Dosierung Personen von der Geburt bis zu einem Alter von 15 Jahren: 1 Dosis (0,5 ml) pro Injektion Grundimmunisierung: Eine vollständige Grundimmunisierung besteht aus mindestens drei Injektionen. Die beiden folgenden Impfschemata werden empfohlen: 0, 1, 6 Monate: zwei Dosen im Abstand von jeweils einem Monat; eine dritte Dosis 6 Monate nach der ersten Dosis 10
11 0, 1, 2, 12 Monate: drei Dosen im Abstand von jeweils einem Monat; eine vierte Dosis 12 Monate nach der ersten Dosis Es wird empfohlen, den Impfstoff entsprechend den angegebenen Impfschemata zu verabreichen. Kinder, die entsprechend dem beschleunigten Impfschema (0, 1, 2 Monate) geimpft werden, müssen zur Bildung von höheren Antikörperkonzentrationen in Monat 12 eine Auffrischimpfung erhalten. Auffrischimpfung: Geimpfte Personen mit intaktem Immunsystem Derzeit ist nicht bekannt, ob bei gesunden geimpften Personen mit vollständiger Grundimmunisierung eine Auffrischimpfung erforderlich ist. Einige offizielle Impfprogramme empfehlen jedoch regelmäßige Auffrischimpfungen, die beachtet werden sollten. Geimpfte Personen mit geschwächtem Immunsystem (z. B. Dialysepatienten, Patienten nach Organtransplantationen, AIDS-Patienten) Bei geimpften Personen mit einem geschwächten Immunsystem muss die Verabreichung von zusätzlichen Dosen in Betracht gezogen werden, sobald die Antikörperkonzentration gegen das Hepatitis B-Virus-Oberflächenantigen (anti-hbsag) unter 10 I.E./l abfällt. Wiederholungsimpfung bei Non-Respondern Wenn Personen, die nach einer vollständigen Grundimmunisierung keine Antikörper bilden, erneut geimpft werden, kommt es bei % nach Gabe einer zusätzlichen Dosis und bei % nach Gabe von drei zusätzlichen Dosen zu einer ausreichenden Antikörperbildung. Weil es jedoch keine ausreichenden Daten über die Unbedenklichkeit von Hepatitis B-Impfstoffen gibt, wenn mehr als die empfohlene Anzahl von Dosen gegeben werden, wird eine Wiederholungsimpfung nach einer abgeschlossenen Grundimmunisierung nicht routinemäßig empfohlen. Wiederholungsimpfungen sollten bei Personen mit einem hohen Risiko durchgeführt werden; zuvor sollte der Nutzen der Impfung gegen das mögliche Risiko von erhöhten lokalen oder systemischen Nebenwirkungen abgewogen werden. Spezielle Impfschemata werden empfohlen: Folgendes Impfschema wird für Neugeborene von Müttern, die Hepatitis B-Virusträger sind, empfohlen - Eine Dosis Hepatitis B-Immunglobulin unmittelbar nach der Geburt (innerhalb der ersten 24 Stunden). - Die erste Dosis eines Hepatitis B-Impfstoffs sollte innerhalb von 7 Tagen nach der Geburt gegeben werden; der Impfstoff kann gleichzeitig mit Hepatitis B-Immunglobulin gegeben werden, die Injektionen sollten jedoch an unterschiedlichen Körperstellen erfolgen. - Weitere Impfungen sollten entsprechend den offiziellen Empfehlungen verabreicht werden. Folgendes Impfschema wird nach bekannter oder vermuteter Hepatitis B-Virus-Exposition (Verletzungen durch kontaminierte Gegenstände, wie z. B. eine Nadelstichverletzung) empfohlen - Eine Dosis Hepatitis B-Immunglobulin unmittelbar nach Exposition (innerhalb der ersten 24 Stunden). - Die erste Dosis eines Hepatitis B-Impfstoffs sollte innerhalb von 7 Tagen nach der Exposition gegeben werden; der Impfstoff kann gleichzeitig mit Hepatitis B-Immunglobulin gegeben werden, die Injektionen sollten jedoch an unterschiedlichen Körperstellen erfolgen. 11
12 - Serologische Testung wird auch bei Gabe von möglicherweise erforderlichen weiteren Impfdosen für den Kurz- bzw. Langzeitschutz empfohlen (abhängig vom Serostatus des Patienten). - Bei nicht oder unvollständig geimpften Personen sollten die erforderlichen Dosen gemäß dem empfohlenen Impfschema verabreicht werden. Das beschleunigte Impfschema, einschließlich einer Auffrischimpfung in Monat 12, kann angewendet werden. Art der Anwendung Der Impfstoff wird intramuskulär verabreicht. Bei Neugeborenen und Kleinkindern wird empfohlen, in den anterolateralen Bereich des Oberschenkels zu impfen. Bei Kindern und Jugendlichen wird empfohlen, in den Delta-Muskel zu impfen. Der Impfstoff darf nicht intravasal verabreicht werden. Bei Patienten mit Thrombozytopenie oder bei Personen mit Blutungsneigung kann der Impfstoff ausnahmsweise auch subkutan verabreicht werden. Vorsichtsmaßnahmen bei der Handhabung / vor der Anwendung des Impfstoffs, siehe Abschnitt Gegenanzeigen - Bekannte Überempfindlichkeit gegen den Wirkstoff, einen der sonstigen Bestandteile oder einen Restbestandteil aus der Herstellung (z. B. Formaldehyd und Kaliumthiocyanat), siehe Abschnitte 6.1 und 2. - Die Impfung sollte bei Personen mit einer schweren, mit Fieber einhergehenden oder akuten Erkrankung verschoben werden. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Wie bei allen Impfstoffen, die durch Injektion verabreicht werden, sollten geeignete Behandlungsmaßnahmen für den Fall von seltenen anaphylaktischen Reaktionen nach Gabe des Impfstoffs bereitstehen (siehe Abschnitt 4.8). Während der Herstellung werden Formaldehyd und Kaliumthiocyanat verwendet; Spuren dieser Stoffe können im Impfstoff vorhanden sein. Dadurch können Überempfindlichkeitsreaktionen auftreten (siehe Abschnitte 2 und 4.8). Der Kolbenstopfen und die Verschlusskappe der Fertigspritze werden aus latexhaltigem, getrocknetem Naturkautschuk hergestellt und können bei latexempfindlichen Personen allergische Reaktionen auslösen. Bezüglich der Verlaufs- oder Laborkontrolle von immunsupprimierten Personen oder Personen, bei denen bekannt ist oder vermutet wird, dass sie Kontakt mit dem Hepatitis B-Virus hatten, siehe Abschnitt 4.2. Bei der Grundimmunisierung von sehr unreifen Frühgeborenen (Geburt 28. Schwangerschaftswoche), insbesondere von solchen mit einer Lungenunreife in der Vorgeschichte, sollte das potenzielle Risiko einer Apnoe berücksichtigt und die Notwendigkeit einer Atemüberwachung über 48 bis 72 Stunden erwogen werden (siehe Abschnitt 4.8). Da der Nutzen der Impfung gerade bei dieser Säuglingsgruppe hoch ist, sollte die Impfung Frühgeborenen nicht vorenthalten und auch nicht aufgeschoben werden. 12
13 Aufgrund der langen Inkubationszeit einer Hepatitis B ist es möglich, dass zum Zeitpunkt der Impfung bereits eine nicht erkannte Infektion vorliegt. Der Impfstoff kann in solchen Fällen eine Hepatitis B- Infektion nicht verhindern. Der Impfstoff schützt nicht vor Infektionen mit anderen Erregern, wie dem Hepatitis A-, Hepatitis C- und Hepatitis E-Virus oder mit sonstigen Erregern, die zu einer Infektion der Leber führen können. Bei der Anwendung in der Schwangerschaft oder während der Stillzeit ist Vorsicht geboten (siehe Abschnitt 4.6). 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Der Impfstoff kann wie folgt verabreicht werden: - gleichzeitig mit Hepatitis B-Immunglobulin an unterschiedlichen Körperstellen - zur Vervollständigung der Grundimmunisierung oder zur Auffrischimpfung bei Personen, die zuvor mit einem anderen Hepatitis B-Impfstoff geimpft wurden - gleichzeitig mit anderen Impfstoffen. In diesem Fall sind unterschiedliche Körperstellen und Spritzen zu verwenden. Die gleichzeitige Verabreichung eines konjugierten Pneumokokken-Impfstoffs (PREVENAR) mit Hepatitis B-Impfstoff gemäß dem 0, 1 und 6 Monats- bzw. dem 0, 1, 2 und 12 Monats-Impfschema wurde nicht ausreichend untersucht. 4.6 Fertilität, Schwangerschaft und Stillzeit Fertilität: HBVAXPRO wurde nicht in Fertilitätsstudien untersucht. Schwangerschaft: Es liegen keine klinischen Daten über die Anwendung von HBVAXPRO während der Schwangerschaft vor. Der Impfstoff sollte während der Schwangerschaft nur nach sorgfältiger Nutzen-Risiko-Abwägung verabreicht werden. Stillzeit: Es liegen keine klinischen Daten über die Anwendung von HBVAXPRO während der Stillzeit vor. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Jedoch ist davon auszugehen, dass HBVAXPRO keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen hat. 4.8 Nebenwirkungen a. Zusammenfassung des Verträglichkeitsprofils Die häufigsten Nebenwirkungen traten an der Injektionsstelle auf: vorübergehende Schmerzhaftigkeit, Erythem, Verhärtung. b. Tabellarische Zusammenfassung der Nebenwirkungen 13
14 Die im Folgenden genannten Nebenwirkungen wurden nach der breiten Anwendung des Impfstoffs gemeldet. Wie bei anderen Hepatitis B-Impfstoffen auch konnte jedoch in vielen Fällen kein kausaler Zusammenhang zwischen der Impfung und dem Auftreten der Nebenwirkung hergestellt werden. Nebenwirkungen Häufigkeit Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Lokalreaktionen (Injektionsstelle): vorübergehende Schmerzhaftigkeit, Häufig Rötung, Verhärtung (> 1/100, < 1/10) Müdigkeit, Fieber, Unwohlsein, grippeähnliche Symptome Sehr selten (< 1/10.000) Erkrankungen des Blutes und des Lymphsystems Thrombozytopenie, Lymphadenopathie Sehr selten (< 1/10.000) Erkrankungen des Immunsystems Serumkrankheit, anaphylaktische Reaktionen, Panarteriitis nodosa Sehr selten (< 1/10.000) Erkrankungen des Nervensystems Parästhesien, Lähmungserscheinungen (einschließlich Bell'sche Parese, Fazialisparese), periphere Neuropathien (Polyradikuloneuritis, Guillain-Barré-Syndrom), Neuritis (einschließlich Optikusneuritis), Myelitis (einschließlich transverser Myelitis), Enzephalitis, Sehr selten (< 1/10.000) demyelinisierende Erkrankungen des zentralen Nervensystems, Verschlechterung einer bestehenden Multiplen Sklerose, Multiple Sklerose, Krampfanfälle, Kopfschmerzen, Benommenheit, Synkopen Augenerkrankungen Uveitis Sehr selten (< 1/10.000) Gefäßerkrankungen Blutdruckabfall, Vaskulitis Sehr selten (< 1/10.000) Erkrankungen der Atemwege, des Brustraums und Mediastinums Bronchospasmus-ähnliche Symptome Sehr selten (< 1/10.000) Erkrankungen des Gastrointestinaltrakts Erbrechen, Übelkeit, Durchfall, Bauchschmerzen Sehr selten (< 1/10.000) Erkrankungen der Haut und des Unterhautzellgewebes Ausschlag, Alopezie, Pruritus, Urtikaria, Erythema multiforme, Sehr selten (< 1/10.000) Angioödem, Ekzem Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Arthralgien, Arthritis, Myalgien, Schmerzen in der Extremität, in die Sehr selten (< 1/10.000) geimpft wurde Untersuchungen Anstieg der Leberenzyme Sehr selten (< 1/10.000) c. Weitere spezielle Personenkreise Apnoe bei sehr unreifen Frühgeborenen (Geburt 28. Schwangerschaftswoche) (siehe Abschnitt 4.4) Meldung des Verdachts auf Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das in Anhang V aufgeführte nationale Meldesystem anzuzeigen. 4.9 Überdosierung Es wurde berichtet, dass HBVAXPRO in höherer Dosierung als empfohlen verabreicht wurde. 14
15 Im Allgemeinen war das Nebenwirkungsprofil von HBVAXPRO bei Überdosierung vergleichbar mit dem bei empfohlener Dosierung. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Anti-Infektivum, ATC-Code: J07BC01 Der Impfstoff löst die Bildung von spezifischen humoralen Antikörpern gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) aus. Eine Antikörperkonzentration gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) von mindestens 10 I.E./l, gemessen ein bis zwei Monate nach der letzten Impfdosis, korreliert mit der Schutzwirkung vor Infektionen mit dem Hepatitis B-Virus. In klinischen Studien konnten bei 96 % von gesunden Kleinkindern, Kindern, Jugendlichen und Erwachsenen nach der Gabe von 3 Dosen einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck schützende Antikörper gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) nachgewiesen werden ( 10 I.E./l). In zwei Studien mit Kleinkindern, die nach unterschiedlichen Impfschemata und gleichzeitig mit anderen Impfstoffen geimpft wurden, entwickelten jeweils 97,5 % bzw. 97,2 % der Kinder schützende Antikörperkonzentrationen; die geometrischen Mittelwerte lagen jeweils bei 214 bzw. 297 I.E./l. Die Schutzwirkung einer Dosis Hepatitis B-Immunglobulin bei Geburt und der anschließenden Gabe von 3 Dosen einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck wurde für Neugeborene von Müttern nachgewiesen, die sowohl auf das Oberflächen- (HBsAg) als auch auf das e-antigen (HBeAg) des Hepatitis B-Virus positiv sind. Im Vergleich zu Infektionsraten mit unbehandelten historischen Kontrollen betrug die geschätzte Effektivität gegen eine chronische Hepatitis B-Infektion bei 130 geimpften Kleinkindern 95 %. Es ist nicht bekannt, wie lange die Schutzwirkung einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck bei gesunden geimpften Personen anhält; jedoch zeigten Untersuchungen an einer Gruppe von Risikopersonen, die mit einem ähnlichen, aus Plasma hergestellten Impfstoff geimpft waren, dass keine dieser Personen im Beobachtungszeitraum von 5 bis 9 Jahren an einer klinisch manifesten Hepatitis B-Infektion erkrankte. Das Vorhandensein eines durch die Impfung ausgelösten immunologischen Gedächtnisses für das Oberflächenantigen des Hepatitis B-Virus (HBsAg) wurde außerdem durch eine anamnestische Antikörperantwort auf eine Auffrischimpfung mit einer früheren Hepatitis B-Impfstoff-Formulierung nachgewiesen. Wie bei anderen Hepatitis B-Impfstoffen auch ist derzeit nicht bekannt, wie lange die Schutzwirkung bei gesunden Geimpften andauert. Außer der 12-Monats-Auffrischimpfung des beschleunigten Impfschemas (0, 1, 2 Monate) ist die Notwendigkeit weiterer Auffrischimpfungen noch nicht geklärt. Reduzierung des Risikos, an einem Leberzellkarzinom zu erkranken Die Erkrankung an einem Leberzellkarzinom ist eine schwere Komplikation einer Hepatitis B- Infektion. In Studien konnte der Zusammenhang zwischen einer chronischen Hepatitis B-Infektion und dem Auftreten eines Leberzellkarzinoms nachgewiesen werden; 80 % der Leberzellkarzinome werden durch eine Hepatitis B-Infektion hervorgerufen. Somit ist der Hepatitis B-Impfstoff der erste Impfstoff, der eine Krebserkrankung verhindert, da die Impfung vor dem Auftreten eines primären Leberzellkarzinoms schützen kann. 5.2 Pharmakokinetische Eigenschaften Nicht zutreffend 5.3 Präklinische Daten zur Sicherheit 15
16 Tierversuche zu Embryotoxizität und Teratogenität wurden nicht durchgeführt. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Natriumchlorid Natriumtetraborat Wasser für Injektionszwecke 6.2 Inkompatibilitäten Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden. 6.3 Dauer der Haltbarkeit 3 Jahre 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Im Kühlschrank lagern (2 C 8 C). Nicht einfrieren. 6.5 Art und Inhalt des Behältnisses 0,5 ml Suspension in einer Fertigspritze (Glas) ohne Kanüle und mit einem Stopfen (graues Chlorobutyl). Packungsgrößen: 1x1, 10x1, 20x1 und 50x1 Dosis 0,5 ml Suspension in einer Fertigspritze (Glas) mit einer beigepackten Kanüle und mit einem Stopfen (graues Chlorobutyl). Packungsgrößen: 1x1 und 10x1 Dosis 0,5 ml Suspension in einer Fertigspritze (Glas) mit zwei beigepackten Kanülen und mit einem Stopfen (graues Chlorobutyl). Packungsgrößen: 1x1, 10x1, 20x1 und 50x1 Dosis Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung und sonstige Hinweise zur Handhabung Der Impfstoff sollte vor Verabreichung visuell auf Ausfällungen oder Verfärbungen untersucht werden. Gegebenenfalls sollte der Impfstoff nicht verabreicht werden. Vor Gebrauch sollte die Spritze gut geschüttelt werden. Die Spritze in einer Hand halten, mit der anderen die Kanüle im Uhrzeigersinn aufdrehen, bis sie fest mit der Spritze verbunden ist. Nicht verwendetes Arzneimittel oder Abfallmaterial ist entsprechend den lokalen Anforderungen zu entsorgen. 7. INHABER DER ZULASSUNG MSD VACCINS 162 avenue Jean Jaurès Lyon Frankreich 16
17 8. ZULASSUNGSNUMMER(N) EU/1/01/183/004 EU/1/01/183/005 EU/1/01/183/020 EU/1/01/183/021 EU/1/01/183/022 EU/1/01/183/023 EU/1/01/183/024 EU/1/01/183/025 EU/1/01/183/030 EU/1/01/183/ DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG Datum der Erteilung der Zulassung: Datum der letzten Verlängerung der Zulassung: STAND DER INFORMATION Ausführliche Informationen zu diesem Arzneimittel sind auf den Internetseiten der Europäischen Arzneimittel-Agentur verfügbar. 17
18 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 10 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Dosis (1 ml) enthält: Hepatitis B-Virus-Oberflächenantigen, rekombinant (HBsAg)* Mikrogramm Adsorbiert an amorphes Aluminiumhydroxyphosphat-Sulfat (0,50 Milligramm Al 3+ ) * hergestellt in Saccharomyces cerevisiae (Stamm )-Hefezellen durch rekombinante DNS- Technologie Während der Herstellung werden Formaldehyd und Kaliumthiocyanat verwendet; Spuren dieser Stoffe können im Impfstoff vorhanden sein. Siehe Abschnitte 4.3, 4.4 und 4.8. Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Injektionssuspension Leicht trübe, weiße Suspension 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete HBVAXPRO ist indiziert zur aktiven Immunisierung gegen eine Infektion mit dem Hepatitis B-Virus einschließlich aller bekannten Subtypen bei Personen ab 16 Jahren, die besonders durch eine Infektion mit dem Hepatitis B-Virus gefährdet sind. Die Impfung von besonders gefährdeten Risikogruppen sollte entsprechend den offiziellen Impfempfehlungen durchgeführt werden. Man geht davon aus, dass eine Impfung mit HBVAXPRO auch gegen Hepatitis D schützt, da Hepatitis D (verursacht durch den Delta-Erreger) ohne eine Hepatitis B-Infektion nicht auftritt. 4.2 Dosierung und Art der Anwendung Dosierung Personen ab 16 Jahren: 1 Dosis (1 ml) pro Injektion Grundimmunisierung: Eine vollständige Grundimmunisierung besteht aus mindestens drei Injektionen. Die beiden folgenden Impfschemata werden empfohlen: 0, 1, 6 Monate: zwei Dosen im Abstand von jeweils einem Monat; eine dritte Dosis 6 Monate nach der ersten Dosis 18
19 0, 1, 2, 12 Monate: drei Dosen im Abstand von jeweils einem Monat; eine vierte Dosis 12 Monate nach der ersten Dosis Es wird empfohlen, den Impfstoff entsprechend den angegebenen Impfschemata zu verabreichen. Geimpfte Personen, die entsprechend dem beschleunigten Impfschema (0, 1, 2 Monate) geimpft werden, müssen zur Bildung von höheren Antikörperkonzentrationen in Monat 12 eine Auffrischimpfung erhalten. Auffrischimpfung: Geimpfte Personen mit intaktem Immunsystem Derzeit ist nicht bekannt, ob bei gesunden geimpften Personen mit vollständiger Grundimmunisierung eine Auffrischimpfung erforderlich ist. Einige offizielle Impfprogramme empfehlen jedoch regelmäßige Auffrischimpfungen, die beachtet werden sollten. Geimpfte Personen mit geschwächtem Immunsystem (z. B. Dialysepatienten, Patienten nach Organtransplantationen, AIDS-Patienten) Bei geimpften Personen mit einem geschwächten Immunsystem muss die Verabreichung von zusätzlichen Dosen in Betracht gezogen werden, sobald die Antikörperkonzentration gegen das Hepatitis B-Virus-Oberflächenantigen (anti-hbsag) unter 10 I.E./l abfällt. Wiederholungsimpfung bei Non-Respondern Wenn Personen, die nach einer vollständigen Grundimmunisierung keine Antikörper bilden, erneut geimpft werden, kommt es bei % nach Gabe einer zusätzlichen Dosis und bei % nach Gabe von drei zusätzlichen Dosen zu einer ausreichenden Antikörperbildung. Weil es jedoch keine ausreichenden Daten über die Unbedenklichkeit von Hepatitis B-Impfstoffen gibt, wenn mehr als die empfohlene Anzahl von Dosen gegeben werden, wird eine Wiederholungsimpfung nach einer abgeschlossenen Grundimmunisierung nicht routinemäßig empfohlen. Wiederholungsimpfungen sollten bei Personen mit einem hohen Risiko durchgeführt werden; zuvor sollte der Nutzen der Impfung gegen das mögliche Risiko von erhöhten lokalen oder systemischen Nebenwirkungen abgewogen werden. Folgendes Impfschema wird nach bekannter oder vermuteter Hepatitis B-Virus-Exposition (Verletzungen durch kontaminierte Gegenstände, wie z. B. eine Nadelstichverletzung) empfohlen: - Eine Dosis Hepatitis B-Immunglobulin unmittelbar nach Exposition (innerhalb der ersten 24 Stunden). - Die erste Dosis eines Hepatitis B-Impfstoffs sollte innerhalb von 7 Tagen nach der Exposition gegeben werden; der Impfstoff kann gleichzeitig mit Hepatitis B-Immunglobulin gegeben werden, die Injektionen sollten jedoch an unterschiedlichen Körperstellen erfolgen. - Serologische Testung wird auch bei Gabe von möglicherweise erforderlichen weiteren Impfdosen für den Kurz- bzw. Langzeitschutz empfohlen (abhängig vom Serostatus des Patienten). - Bei nicht oder unvollständig geimpften Personen sollten die erforderlichen Dosen gemäß dem empfohlenen Impfschema verabreicht werden. Das beschleunigte Impfschema, einschließlich einer Auffrischimpfung in Monat 12, kann angewendet werden. Anwendung bei Personen unter 16 Jahren HBVAXPRO 10 Mikrogramm ist für diese pädiatrische Altersgruppe nicht indiziert. Für die Verabreichung an Personen von der Geburt bis zu einem Alter von 15 Jahren ist HBVAXPRO 5 Mikrogramm die geeignete Stärke. Art der Anwendung 19
20 Der Impfstoff wird intramuskulär verabreicht. Bei Erwachsenen und Jugendlichen wird empfohlen, in den Delta-Muskel zu impfen. Der Impfstoff darf nicht intravasal verabreicht werden. Bei Patienten mit Thrombozytopenie oder bei Personen mit Blutungsneigung kann der Impfstoff ausnahmsweise auch subkutan verabreicht werden. Vorsichtsmaßnahmen bei der Handhabung / vor der Anwendung des Impfstoffs, siehe Abschnitt Gegenanzeigen - Bekannte Überempfindlichkeit gegen den Wirkstoff, einen der sonstigen Bestandteile oder einen Restbestandteil aus der Herstellung (z. B. Formaldehyd und Kaliumthiocyanat), siehe Abschnitte 6.1 und 2. - Die Impfung sollte bei Personen mit einer schweren, mit Fieber einhergehenden oder akuten Erkrankung verschoben werden. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Wie bei allen Impfstoffen, die durch Injektion verabreicht werden, sollten geeignete Behandlungsmaßnahmen für den Fall von seltenen anaphylaktischen Reaktionen nach Gabe des Impfstoffs bereitstehen (siehe Abschnitt 4.8). Während der Herstellung werden Formaldehyd und Kaliumthiocyanat verwendet; Spuren dieser Stoffe können im Impfstoff vorhanden sein. Dadurch können Überempfindlichkeitsreaktionen auftreten (siehe Abschnitte 2 und 4.8). Der Gummistopfen des Fläschchens wird aus latexhaltigem, getrocknetem Naturkautschuk hergestellt und kann bei latexempfindlichen Personen allergische Reaktionen auslösen. Bezüglich der Verlaufs- oder Laborkontrolle von immunsupprimierten Personen oder Personen, bei denen bekannt ist oder vermutet wird, dass sie Kontakt mit dem Hepatitis B-Virus hatten, siehe Abschnitt 4.2. Eine Reihe von Faktoren kann zu einer abgeschwächten Immunantwort auf Hepatitis B-Impfstoffe führen. Zu diesen Faktoren gehören ein höheres Lebensalter, männliches Geschlecht, Übergewicht, Rauchen, Art der Anwendung und einige chronische Grunderkrankungen. Eine serologische Bestimmung der Antikörper sollte bei Personen in Erwägung gezogen werden, die möglicherweise nach einer abgeschlossenen Grundimmunisierung mit HBVAXPRO keine schützenden Antikörper bilden. Die Verabreichung von weiteren Dosen muss möglicherweise für Personen, die keine oder nur eine unzureichende Immunantwort nach einer abgeschlossenen Grundimmunisierung besitzen, in Erwägung gezogen werden. Aufgrund der langen Inkubationszeit einer Hepatitis B ist es möglich, dass zum Zeitpunkt der Impfung bereits eine nicht erkannte Infektion vorliegt. Der Impfstoff kann in solchen Fällen eine Hepatitis B- Infektion nicht verhindern. Der Impfstoff schützt nicht vor Infektionen mit anderen Erregern, wie dem Hepatitis A-, Hepatitis C- und Hepatitis E-Virus oder mit sonstigen Erregern, die zu einer Infektion der Leber führen können. Bei der Anwendung in der Schwangerschaft oder während der Stillzeit ist Vorsicht geboten (siehe Abschnitt 4.6). 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen 20
21 Der Impfstoff kann wie folgt verabreicht werden: - gleichzeitig mit Hepatitis B-Immunglobulin an unterschiedlichen Körperstellen - zur Vervollständigung der Grundimmunisierung oder zur Auffrischimpfung bei Personen, die zuvor mit einem anderen Hepatitis B-Impfstoff geimpft wurden - gleichzeitig mit anderen Impfstoffen. In diesem Fall sind unterschiedliche Körperstellen und Spritzen zu verwenden. 4.6 Fertilität, Schwangerschaft und Stillzeit Fertilität: HBVAXPRO wurde nicht in Fertilitätsstudien untersucht. Schwangerschaft: Es liegen keine klinischen Daten über die Anwendung von HBVAXPRO während der Schwangerschaft vor. Der Impfstoff sollte während der Schwangerschaft nur nach sorgfältiger Nutzen-Risiko-Abwägung verabreicht werden. Stillzeit: Es liegen keine klinischen Daten über die Anwendung von HBVAXPRO während der Stillzeit vor. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. Jedoch ist davon auszugehen, dass HBVAXPRO keinen oder einen zu vernachlässigenden Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen hat. 4.8 Nebenwirkungen a. Zusammenfassung des Verträglichkeitsprofils Die häufigsten Nebenwirkungen traten an der Injektionsstelle auf: vorübergehende Schmerzhaftigkeit, Erythem, Verhärtung. b. Tabellarische Zusammenfassung der Nebenwirkungen Die im Folgenden genannten Nebenwirkungen wurden nach der breiten Anwendung des Impfstoffs gemeldet. Wie bei anderen Hepatitis B-Impfstoffen auch konnte jedoch in vielen Fällen kein kausaler Zusammenhang zwischen der Impfung und dem Auftreten der Nebenwirkung hergestellt werden. Nebenwirkungen Häufigkeit Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Lokalreaktionen (Injektionsstelle): vorübergehende Schmerzhaftigkeit, Häufig Rötung, Verhärtung (> 1/100, < 1/10) Müdigkeit, Fieber, Unwohlsein, grippeähnliche Symptome Sehr selten (< 1/10.000) Erkrankungen des Blutes und des Lymphsystems Thrombozytopenie, Lymphadenopathie Sehr selten (< 1/10.000) Erkrankungen des Immunsystems Serumkrankheit, anaphylaktische Reaktionen, Panarteriitis nodosa Sehr selten (< 1/10.000) Erkrankungen des Nervensystems Parästhesien, Lähmungserscheinungen (einschließlich Bell'sche Parese, Fazialisparese), periphere Neuropathien (Polyradikuloneuritis, Sehr selten (< 1/10.000) Guillain-Barré-Syndrom), Neuritis (einschließlich Optikusneuritis), 21
22 Myelitis (einschließlich transverser Myelitis), Enzephalitis, demyelinisierende Erkrankungen des zentralen Nervensystems, Verschlechterung einer bestehenden Multiplen Sklerose, Multiple Sklerose, Krampfanfälle, Kopfschmerzen, Benommenheit, Synkopen Augenerkrankungen Uveitis Sehr selten (< 1/10.000) Gefäßerkrankungen Blutdruckabfall, Vaskulitis Sehr selten (< 1/10.000) Erkrankungen der Atemwege, des Brustraums und Mediastinums Bronchospasmus-ähnliche Symptome Sehr selten (< 1/10.000) Erkrankungen des Gastrointestinaltrakts Erbrechen, Übelkeit, Durchfall, Bauchschmerzen Sehr selten (< 1/10.000) Erkrankungen der Haut und des Unterhautzellgewebes Ausschlag, Alopezie, Pruritus, Urtikaria, Erythema multiforme, Sehr selten (< 1/10.000) Angioödem, Ekzem Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Arthralgien, Arthritis, Myalgien, Schmerzen in der Extremität, in die Sehr selten (< 1/10.000) geimpft wurde Untersuchungen Anstieg der Leberenzyme Sehr selten (< 1/10.000) Meldung des Verdachts auf Nebenwirkungen Die Meldung des Verdachts auf Nebenwirkungen nach der Zulassung ist von großer Wichtigkeit. Sie ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung über das in Anhang V aufgeführte nationale Meldesystem anzuzeigen. 4.9 Überdosierung Es wurde berichtet, dass HBVAXPRO in höherer Dosierung als empfohlen verabreicht wurde. Im Allgemeinen war das Nebenwirkungsprofil von HBVAXPRO bei Überdosierung vergleichbar mit dem bei empfohlener Dosierung. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Anti-Infektivum, ATC-Code: J07BC01 Der Impfstoff löst die Bildung von spezifischen humoralen Antikörpern gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) aus. Eine Antikörperkonzentration gegen das Oberflächenantigen des Hepatitis B-Virus (anti-hbsag) von mindestens 10 I.E./l, gemessen ein bis zwei Monate nach der letzten Impfdosis, korreliert mit der Schutzwirkung vor Infektionen mit dem Hepatitis B-Virus. In klinischen Studien konnten bei 96 % von gesunden Kleinkindern, Kindern, Jugendlichen und Erwachsenen nach der Gabe von 3 Dosen einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck schützende Antikörper gegen das Oberflächenantigen des Hepatitis B-Virus nachgewiesen werden ( 10 I.E./l). In zwei Studien mit älteren Jugendlichen und Erwachsenen entwickelten 95,6 bis 97,5 % der Geimpften schützende Antikörperkonzentrationen; die geometrischen Mittelwerte lagen zwischen 535 und 793 I.E./l. Es ist nicht bekannt, wie lange die Schutzwirkung einer früheren Formulierung des rekombinanten Hepatitis B-Impfstoffs von Merck bei gesunden geimpften Personen anhält; jedoch zeigten Untersuchungen an einer Gruppe von Risikopersonen, die mit einem ähnlichen, aus Plasma 22
23 hergestellten Impfstoff geimpft waren, dass keine dieser Personen im Beobachtungszeitraum von 5 bis 9 Jahren an einer klinisch manifesten Hepatitis B-Infektion erkrankte. Das Vorhandensein eines durch die Impfung ausgelösten immunologischen Gedächtnisses für das Oberflächenantigen des Hepatitis B-Virus (HBsAg) wurde außerdem durch eine anamnestische Antikörperantwort auf eine Auffrischimpfung mit einer früheren Hepatitis B-Impfstoff-Formulierung bei gesunden Erwachsenen nachgewiesen. Wie bei anderen Hepatitis B-Impfstoffen auch ist derzeit nicht bekannt, wie lange die Schutzwirkung bei gesunden Geimpften andauert. Außer der 12-Monats- Auffrischimpfung des beschleunigten Impfschemas (0, 1, 2 Monate) ist die Notwendigkeit weiterer Auffrischimpfungen noch nicht geklärt. Reduzierung des Risikos, an einem Leberzellkarzinom zu erkranken Die Erkrankung an einem Leberzellkarzinom ist eine schwere Komplikation einer Hepatitis B- Infektion. In Studien konnte der Zusammenhang zwischen einer chronischen Hepatitis B-Infektion und dem Auftreten eines Leberzellkarzinoms nachgewiesen werden; 80 % der Leberzellkarzinome werden durch eine Hepatitis B-Infektion hervorgerufen. Somit ist der Hepatitis B-Impfstoff der erste Impfstoff, der eine Krebserkrankung verhindert, da die Impfung vor dem Auftreten eines primären Leberzellkarzinoms schützen kann. 5.2 Pharmakokinetische Eigenschaften Nicht zutreffend 5.3 Präklinische Daten zur Sicherheit Tierversuche zu Embryotoxizität und Teratogenität wurden nicht durchgeführt. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Natriumchlorid Natriumtetraborat Wasser für Injektionszwecke 6.2 Inkompatibilitäten Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieses Arzneimittel nicht mit anderen Arzneimitteln gemischt werden. 6.3 Dauer der Haltbarkeit 3 Jahre 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Im Kühlschrank lagern (2 C 8 C). Nicht einfrieren. 6.5 Art und Inhalt des Behältnisses 1 ml Suspension in einem Fläschchen (Glas) mit einem Stopfen (graues Butylgummi) und Aluminiumsiegel mit Plastik-Flip-off-Verschluss. Packungsgrößen: 1x1 und 10x1 Dosis. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 23
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Gebrauchsinformation: Information für Anwender. HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem Impfstoff
Gebrauchsinformation: Information für Anwender HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem Impfstoff
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender. HBVAXPRO 10 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 10 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender HBVAXPRO 10 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Vi-Polysaccharid von Salmonella typhi (Ty2 Stamm)
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV)
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften)
 F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS Influvac - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff aus inaktivierten Oberflächenantigenen)
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS Influvac - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff aus inaktivierten Oberflächenantigenen)
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr Kind mit
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr Kind mit
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
FACHINFORMATION IPV Mérieux 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 FACHINFORMATION IPV Mérieux 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
FACHINFORMATION IPV Mérieux 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert)
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. QUALITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. QUALITATIVE
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG. Influenzavirus Oberflächenantigene (Hämagglutinin und Neuroaminidase) der folgenden Stämme*:
 1. BEZEICHNUNG DES ARZNEIMITTELS Sandovac Injektionssuspension in einer Fertigspritze Influenzaimpfstoff (Oberflächenantigene, inaktiviert) (2014/2015) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Influenzavirus
1. BEZEICHNUNG DES ARZNEIMITTELS Sandovac Injektionssuspension in einer Fertigspritze Influenzaimpfstoff (Oberflächenantigene, inaktiviert) (2014/2015) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Influenzavirus
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS: FLUAD, Injektionssuspension in einer Fertigspritze Influenza-Impfstoff, Oberflächenantigene, inaktiviert, mit MF59C.1 als
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS: FLUAD, Injektionssuspension in einer Fertigspritze Influenza-Impfstoff, Oberflächenantigene, inaktiviert, mit MF59C.1 als
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert)
 1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (1,0 ml) enthält: Hepatitis A Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (1,0 ml) enthält: Hepatitis A Virus
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels)
 1 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Xanaflu Saison 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Impfstoff aus Oberflächenantigen
1 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Xanaflu Saison 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Impfstoff aus Oberflächenantigen
Fachinformation. 32 D-Antigen²-Einheiten³. Antigenmenge im Endprodukt (Final Bulk Product), gemäß WHO (TRS 673, 1982) 3
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. Qualitative und quantitative Zusammensetzung 1 Impfdosis (0,5 ml) enthält: Wirkstoffe:
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. Qualitative und quantitative Zusammensetzung 1 Impfdosis (0,5 ml) enthält: Wirkstoffe:
10 Mikrogramm. Adsorbiert an hydratisiertes Aluminiumhydroxid Gesamt: 0,25 Milligramm Al 3+ 2
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Kinder Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Kinder Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 3. DARREICHUNGSFORM 4. KLINISCHE ANGABEN
 1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 720 Kinder Injektionssuspension Hepatitis-A-Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5ml) enthält: Hepatitis-A-Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 720 Kinder Injektionssuspension Hepatitis-A-Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5ml) enthält: Hepatitis-A-Virus
Fachinformation IPV Mérieux Stand: Juli 2010
 Fachinformation IPV Mérieux Stand: Juli 2010 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE
Fachinformation IPV Mérieux Stand: Juli 2010 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
720 ELISA-Einheiten Hepatitis-B-Oberflächenantigen 3,4
 Twinrix Erwachsene, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung 1 Dosis (1 ml) enthält: Hepatitis-A-Virus
Twinrix Erwachsene, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung 1 Dosis (1 ml) enthält: Hepatitis-A-Virus
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften)
 F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS FluVaccinol Subunit Impfstoff - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS FluVaccinol Subunit Impfstoff - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff
Fachinformation. Internationale Einheiten, untere Vertrauensgrenze (p=0,95) der nach der Methode der Ph.Eur. ermittelten Wirksamkeit
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) 2. Qualitative und quantitative
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) 2. Qualitative und quantitative
Sanofi Pasteur MSD GmbH 1. BEZEICHNUNG DES ARZNEIMITTELS
 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis(inaktiviert)-Adsorbat-Impfstoff (reduzierter Antigengehalt) 2. QUALITATIVE UND QUANTITATIVE
1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis(inaktiviert)-Adsorbat-Impfstoff (reduzierter Antigengehalt) 2. QUALITATIVE UND QUANTITATIVE
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS)
 FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS) 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP Injektionssuspension in einer Fertigspritze Influenza Impfstoff (Spaltimpfstoff, inaktiviert).
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS) 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP Injektionssuspension in einer Fertigspritze Influenza Impfstoff (Spaltimpfstoff, inaktiviert).
FACHINFORMATION REVAXiS
 FACHINFORMATION REVAXiS 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt)
FACHINFORMATION REVAXiS 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt)
Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt
 1. BEZEICHNUNG DES ARZNEIMITTELS Td-pur Injektionssuspension in Fertigspritze Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS Td-pur Injektionssuspension in Fertigspritze Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 Impfdosis (0,5 ml) enthält: inaktivierte Influenza-Virus Spaltantigene* der folgenden Stämme:
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Sonstige Bestandteile: Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP 2013/2014 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml)
1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP 2013/2014 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml)
Vollständige Auflistung der sonstigen Bestandteile siehe, Abschnitt 6.1.
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix-B 10 Mikrogramm/0,5 ml Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna) Impfstoff (adsorbiert) (HBV)
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix-B 10 Mikrogramm/0,5 ml Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna) Impfstoff (adsorbiert) (HBV)
Gebrauchsinformation: Information für den Anwender. Polio-Salk Mérieux - Fertigspritze Poliomyelitis-Impfstoff (inaktiviert)
 Gebrauchsinformation: Information für den Anwender Polio-Salk Mérieux - Fertigspritze Poliomyelitis-Impfstoff (inaktiviert) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
Gebrauchsinformation: Information für den Anwender Polio-Salk Mérieux - Fertigspritze Poliomyelitis-Impfstoff (inaktiviert) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS AFLUBIN- Grippetropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 ml enthalten: 1 ml Gentiana lutea D1, 10 ml Aconitum
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS AFLUBIN- Grippetropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 ml enthalten: 1 ml Gentiana lutea D1, 10 ml Aconitum
Zulassungsbescheid Zul.-Nr. PEI.H /16
 Zulassungsbescheid Zul.-Nr. PEI.H.11453.02.1 5/16 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Engerix-B Kinder, Injektionssuspension Hepatitis-B (rdna)-impfstoff (adsorbiert) Lesen Sie die gesamte
Zulassungsbescheid Zul.-Nr. PEI.H.11453.02.1 5/16 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Engerix-B Kinder, Injektionssuspension Hepatitis-B (rdna)-impfstoff (adsorbiert) Lesen Sie die gesamte
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tetanol pur Injektionssuspension in einer Fertigspritze 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: Tetanus-Toxoid
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tetanol pur Injektionssuspension in einer Fertigspritze 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: Tetanus-Toxoid
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Td-Impfstoff Mérieux Injektionssuspension Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Für Kinder ab 5 Jahren und Erwachsene Lesen Sie
Gebrauchsinformation: Information für Anwender Td-Impfstoff Mérieux Injektionssuspension Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Für Kinder ab 5 Jahren und Erwachsene Lesen Sie
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender. Typhim Vi Injektionslösung in einer Fertigspritze. Typhus-Polysaccharid-Impfstoff
 Gebrauchsinformation: Information für Anwender Typhim Vi Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr
Gebrauchsinformation: Information für Anwender Typhim Vi Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Tetanus-Impfstoff Mérieux, mind. 40 I.E. Injektionssuspension in einer Fertigspritze Injektionssuspension Tetanus-Adsorbat-Impfstoff Für Säuglinge, Kinder
Gebrauchsinformation: Information für Anwender Tetanus-Impfstoff Mérieux, mind. 40 I.E. Injektionssuspension in einer Fertigspritze Injektionssuspension Tetanus-Adsorbat-Impfstoff Für Säuglinge, Kinder
20 Mikrogramm. Adsorbiert an hydratisiertes Aluminiumhydroxid Gesamt: 0,50 Milligramm Al 3+ 2
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix -B Erwachsene Injektionssuspension in einer Durchstechflasche oder in einer Fertigspritze Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) 2. QUALITATIVE
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für Kinder
Gebrauchsinformation: Information für Anwender REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für Kinder
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Epaxal - Suspension zur Injektion in einer Fertigspritze Hepatitis A-Impfstoff (inaktiviert, virosomal)
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Epaxal - Suspension zur Injektion in einer Fertigspritze Hepatitis A-Impfstoff (inaktiviert, virosomal)
Gebrauchsinformation: Information für Anwender. Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff
 Gebrauchsinformation: Information für Anwender Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Für Kinder ab 2 Jahren und Erwachsene Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Für Kinder ab 2 Jahren und Erwachsene Lesen Sie die gesamte
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Erwachsene, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert)
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Erwachsene, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert)
Zulassungsbescheid Zul.-Nr. PEI.H /18
 Zulassungsbescheid Zul.-Nr. PEI.H.11453.01.1 5/18 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Engerix-B Erwachsene, Injektionssuspension Hepatitis-B (rdna)-impfstoff (adsorbiert) Lesen Sie die gesamte
Zulassungsbescheid Zul.-Nr. PEI.H.11453.01.1 5/18 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Engerix-B Erwachsene, Injektionssuspension Hepatitis-B (rdna)-impfstoff (adsorbiert) Lesen Sie die gesamte
FACHINFORMATION. PHARMA WESTEN Ges.m.b.H. 1. BEZEICHNUNG DES ARZNEIMITTELS PNEUMOVAX 23 Injektionslösung Pneumokokken-Polysaccharid-Impfstoff
 1. BEZEICHNUNG DES ARZNEIMITTELS PNEUMOVAX 23 Injektionslösung Pneumokokken-Polysaccharid-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml) enthält jeweils 25 Mikrogramm der
1. BEZEICHNUNG DES ARZNEIMITTELS PNEUMOVAX 23 Injektionslösung Pneumokokken-Polysaccharid-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml) enthält jeweils 25 Mikrogramm der
Stand der Information: /N-060 B. PACKUNGSBEILAGE
 B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
B. PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
360 ELISA-Einheiten Hepatitis-B-Oberflächenantigen 3,4
 Twinrix Kinder-Injektionssuspension in einer Fertigspritze Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung 1 Dosis (0,5 ml)
Twinrix Kinder-Injektionssuspension in einer Fertigspritze Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. Qualitative und quantitative Zusammensetzung 1 Dosis (0,5 ml)
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels/SPC)
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
Gewonnen aus Hefezellen (Saccharomyces cerevisiae) mittels rekombinanter DNA-Technologie
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix-B 20 Mikrogramm /1 ml Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna) Impfstoff (adsorbiert) (HBV)
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix-B 20 Mikrogramm /1 ml Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna) Impfstoff (adsorbiert) (HBV)
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Daflon 500 mg Filmtabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Filmtablette enthält 500 mg gereinigte, mikronisierte
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Daflon 500 mg Filmtabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Filmtablette enthält 500 mg gereinigte, mikronisierte
Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
Gebrauchsinformation: Information für Anwender. Inaktivierter Poliomyelitis-Impfstoff
 Gebrauchsinformation: Information für Anwender IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
FACHINFORMATION. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen
 FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
FACHINFORMATION 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis Adsorbatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Impfdosis
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis Adsorbatimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Impfdosis
5 bis 10 Jahre: 0,5 ml Td-pur
 Td-pur für Erwachsene und Heranwachsende Tetanus-Diphtherie-Impfstoff (inaktiviert, adsorbiert, reduzierter Antigengehalt) Injektionssuspension in Fertigspritze 2. Qualitative und quantitative Zusammensetzung
Td-pur für Erwachsene und Heranwachsende Tetanus-Diphtherie-Impfstoff (inaktiviert, adsorbiert, reduzierter Antigengehalt) Injektionssuspension in Fertigspritze 2. Qualitative und quantitative Zusammensetzung
Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
1. Was ist TdaP-IMMUN und wofür wird es angewendet?
 Page 1 of 6 Gebrauchsinformation: Information für Anwender TdaP-IMMUN Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis- (azelluläre Komponente) Impfstoff (adsorbiert, reduzierter
Page 1 of 6 Gebrauchsinformation: Information für Anwender TdaP-IMMUN Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis- (azelluläre Komponente) Impfstoff (adsorbiert, reduzierter
Mumpsviren, Stamm RIT , abgeleitet vom Stamm Jeryl Lynn (lebend, attenuiert) mindestens 10 3,7 ZKID 50
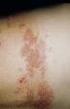 1. BEZEICHNUNG DES ARZNEIMITTELS MMR-PRIORIX - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis
1. BEZEICHNUNG DES ARZNEIMITTELS MMR-PRIORIX - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis
Anhang III. Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage
 Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
GEBRAUCHSINFORMATION FÜR. Eurican LR Injektionssuspension
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION FÜR Eurican LR Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION FÜR Eurican LR Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
FACHINFORMATION. Kinder und Jugendliche
 1. BEZEICHNUNG DES ARZNEIMITTELS Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
1. BEZEICHNUNG DES ARZNEIMITTELS Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten)-Adsorbatimpfstoff (mit reduziertem Antigengehalt) ab dem vollendeten
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Condrosulf 800 mg-tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Tablette enthält 800 mg Natriumchondroitinsulfat
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Condrosulf 800 mg-tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Tablette enthält 800 mg Natriumchondroitinsulfat
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Meningokokken-Impfstoff A + C Mérieux
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningokokken-Impfstoff A + C Mérieux Lyophilisat (Trockensubstanz) und Lösungsmittel zur Herstellung einer Injektionssuspension Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningokokken-Impfstoff A + C Mérieux Lyophilisat (Trockensubstanz) und Lösungsmittel zur Herstellung einer Injektionssuspension Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung. Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die Packungsbeilage sorgfältig durch, bevor Sie oder Ihr Kind
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die Packungsbeilage sorgfältig durch, bevor Sie oder Ihr Kind
Fachinformation. 8 D-Antigeneinheiten Typ 3 (Saukett) 2. Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Boostrix Polio Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten) und Poliomyelitis (inaktivierter)-
Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Boostrix Polio Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis (azellulär, aus Komponenten) und Poliomyelitis (inaktivierter)-
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET
 1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 100 mg Brausetabletten
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 100 mg Brausetabletten
Tetravac. 1. Bezeichnung des Arzneimittels. 2. Qualitative und quantitative Zusammensetzung. 3. Darreichungsform
 1. Bezeichnung des Arzneimittels, Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis (inaktiviert)-adsorbat-impfstoff 2. Qualitative und quantitative Zusammensetzung
1. Bezeichnung des Arzneimittels, Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis (inaktiviert)-adsorbat-impfstoff 2. Qualitative und quantitative Zusammensetzung
GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN/DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN/DEN ANWENDER Repevax Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Poliomyelitis (inaktiviert)-impfstoff
GEBRAUCHSINFORMATION: INFORMATION FÜR DIE ANWENDERIN/DEN ANWENDER Repevax Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär, aus Komponenten)-Poliomyelitis (inaktiviert)-impfstoff
FACHINFORMATION. 1 Hartkapsel enthält: 6 mg lysierte immunaktive Fraktionen aus ausgewählten Escherichia-coli-Stämmen.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
B/Brisbane/60/2008 ähnlicher Stamm (B/Brisbane/60/2008, Wildtyp) Mikrogramm HA 2
 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml)
1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml)
GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
 GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Fovepta 200 I.E. Injektionslösung in einer Fertigspritze Hepatitis-B-Immunglobulin vom Menschen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Fovepta 200 I.E. Injektionslösung in einer Fertigspritze Hepatitis-B-Immunglobulin vom Menschen Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Fovepta 200 I.E. Injektionslösung in einer Fertigspritze Hepatitis-B-Immunglobulin vom Menschen Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Sonstige Bestandteile: Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP Kinder 2014/2015 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis
1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP Kinder 2014/2015 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis
GEBRAUCHSINFORMATION UND FACHINFORMATION 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG. Wirkstoff: Hepatitis B Immunglobulin vom Menschen
 GEBRAUCHSINFORMATION UND FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Injektionslösung zur intramuskulären Anwendung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: Hepatitis B Immunglobulin
GEBRAUCHSINFORMATION UND FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Injektionslösung zur intramuskulären Anwendung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: Hepatitis B Immunglobulin
Gebrauchsinformation: Information für Anwender. dt-reduct Mérieux Injektionssuspension in einer Fertigspritze
 Gebrauchsinformation: Information für Anwender dt-reduct Mérieux Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender dt-reduct Mérieux Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender. Hepatyrix Injektionssuspension
 Gebrauchsinformation: Information für den Anwender Hepatyrix Injektionssuspension Kombinierter Hepatitis A (inaktiviert) und Typhus-Vi- Polysaccharid Impfstoff (adsorbiert) Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender Hepatyrix Injektionssuspension Kombinierter Hepatitis A (inaktiviert) und Typhus-Vi- Polysaccharid Impfstoff (adsorbiert) Lesen Sie die gesamte Packungsbeilage
Zusammenfassung der Merkmale des Arzneimittels
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Stieprox 1,5%-Shampoo 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 g Shampoo enthalten 1,5 g Ciclopirox-Olamin (1,5
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Stieprox 1,5%-Shampoo 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 g Shampoo enthalten 1,5 g Ciclopirox-Olamin (1,5
Gewonnen aus Hefezellen (Saccharomyces cerevisiae) mittels rekombinanter DNA-Technologie
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix-B 10 Mikrogramm/0,5 ml Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna) Impfstoff (adsorbiert) (HBV)
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Engerix-B 10 Mikrogramm/0,5 ml Injektionssuspension in einer Fertigspritze Hepatitis-B (rdna) Impfstoff (adsorbiert) (HBV)
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis-Adsorbatimpfstoff für Säuglinge (ab 2 Monaten) und Kinder (bis 6 Jahre) Lesen
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Infanrix, Injektionssuspension Diphtherie-Tetanus-(azellulärer) Pertussis-Adsorbatimpfstoff für Säuglinge (ab 2 Monaten) und Kinder (bis 6 Jahre) Lesen
Gebrauchsinformation: Information für Patienten. Tetanol pur Injektionssuspension in einer Fertigspritze Tetanus-Toxoid
 Gebrauchsinformation: Information für Patienten Tetanol pur Injektionssuspension in einer Fertigspritze Tetanus-Toxoid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Patienten Tetanol pur Injektionssuspension in einer Fertigspritze Tetanus-Toxoid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Patienten. Tetanol pur Injektionssuspension in einer Fertigspritze Tetanus-Toxoid
 Gebrauchsinformation: Information für Patienten Tetanol pur Injektionssuspension in einer Fertigspritze Tetanus-Toxoid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Patienten Tetanol pur Injektionssuspension in einer Fertigspritze Tetanus-Toxoid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
1. Was ist Engerix-B Kinder und wofür wird es angewendet?
 1 Gebrauchsinformation: Information für Anwender Engerix -B Kinder, Injektionssuspension Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
1 Gebrauchsinformation: Information für Anwender Engerix -B Kinder, Injektionssuspension Hepatitis-B (rdna)-impfstoff (adsorbiert) (HBV) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
2 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Page 1 of 8 FACHINFORMATION 1 BEZEICHNUNG DES ARZNEIMITTELS Tuberkulin PPD RT23 SSI 2 T.E./0,1 ml, Injektionslösung. Tuberkulin PPD RT23 SSI 10 T.E./0,1 ml, Injektionslösung. 2 QUALITATIVE UND QUANTITATIVE
Page 1 of 8 FACHINFORMATION 1 BEZEICHNUNG DES ARZNEIMITTELS Tuberkulin PPD RT23 SSI 2 T.E./0,1 ml, Injektionslösung. Tuberkulin PPD RT23 SSI 10 T.E./0,1 ml, Injektionslösung. 2 QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. RIKA-VACC Duo Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Kaninchen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. RIKA-VACC Duo Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Kaninchen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für
Boehringer Ingelheim Vetmedica GmbH
 PACKUNGSBEILAGE FÜR Insol Dermatophyton, Injektionssuspension für Pferde, Hunde und Katzen 1. NAME/FIRMA UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
PACKUNGSBEILAGE FÜR Insol Dermatophyton, Injektionssuspension für Pferde, Hunde und Katzen 1. NAME/FIRMA UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
GEBRAUCHSINFORMATION Eurican SHPPi2LT Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Hunde
 GEBRAUCHSINFORMATION Eurican SHPPi2LT Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
GEBRAUCHSINFORMATION Eurican SHPPi2LT Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
Fachinformation. mind. 30 Internationale Einheiten (I.E.) Tetanus-Toxoid 1
 1. BEZEICHNUNG DES ARZNEIMITTELS - Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie-Tetanus- (azellulärer) Pertussis-, Poliomyelitis (inaktiviert)- und Haemophilus-influenzae-Typ
1. BEZEICHNUNG DES ARZNEIMITTELS - Pulver und Suspension zur Herstellung einer Injektionssuspension Diphtherie-Tetanus- (azellulärer) Pertussis-, Poliomyelitis (inaktiviert)- und Haemophilus-influenzae-Typ
GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension
 GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
FACHINFORMATION. Wirkstoffe: Haemophilus influenzae Typ b-polysaccharide (Polyribosylribitolphosphat) konjugiert an
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Act-HIB Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Haemophilus influenzae Typ b-konjugatimpfstoff 2.
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Act-HIB Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Haemophilus influenzae Typ b-konjugatimpfstoff 2.
Vollständige Auflistung der sonstigen Bestandteile siehe, Abschnitt 6.1.
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Baldriparan für die Nacht überzogene Tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede überzogene Tablette enthält
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Baldriparan für die Nacht überzogene Tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede überzogene Tablette enthält
GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde
 GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
Gebrauchsinformation REPEVAXPP. Stand:
 Gebrauchsinformation REPEVAXPP Stand: 1/8 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER REPEVAXPP PP Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus-, Pertussis(azellulär, aus Komponenten)-Poliomyelitis(inaktiviert)-Impfstoff
Gebrauchsinformation REPEVAXPP Stand: 1/8 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER REPEVAXPP PP Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus-, Pertussis(azellulär, aus Komponenten)-Poliomyelitis(inaktiviert)-Impfstoff
GEBRAUCHSINFORMATION Bovalto Respi 3 Injektionssuspension für Rinder
 GEBRAUCHSINFORMATION Bovalto Respi 3 Injektionssuspension für Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
GEBRAUCHSINFORMATION Bovalto Respi 3 Injektionssuspension für Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
