THEORETISCHER TEST 8. Dezember Aufgabe I und II. (Die erreichbare Punktzahl für beide Aufgaben ist 20) H 2 2H + + 2e.
|
|
|
- Gerhardt Kerner
- vor 5 Jahren
- Abrufe
Transkript
1 THEORETISCHER TEST 8. Dezember 2005 Aufgabe I und II. (Die erreichbare Punktzahl für beide Aufgaben ist 20) Wenn wir das elektrische Potenzial einer besonderen Elektrode (Halbzelle) beliebig auf Null setzen, können wir sie verwenden, um die relativen Potenziale anderer Elektroden zu bestimmen. Die Wasserstoffelektrode, die in Abbildung 1 gezeigt wird, dient zu diesem Zweck als Referenzelektrode. Wasserstoffgas wird in eine Salzsäurelösung bei 25 C eingeleitet. Die Platinelektrode hat zwei Aufgaben. Erstens stellt sie eine Oberfläche zur Verfügung, an der die Dissoziation von Wasserstoffmolekülen stattfinden kann: H 2 2H + + 2e. Zweitens dient sie als elektrischer Leiter für den äußeren Stromkreis. Unter Standard-Zustandsbedingungen Abbildung 1. (wenn der Druck des Wasserstoffs Unter Standard-Bedingungen (wenn der Druck von H 2 1 atm und die Konzentration der Salzsäurelösung 1 mol/l betragen) wird das Potenzial für eine Reduktions-Reaktion von H + bei 25 C als exakt Null vorausgesetzt: T-1/12
2 V (ev) 2H + (1 mol/l) + 2e H 2 (1 atm) E 0 = 0 V Somit wird das Standard-Reduktions-Potenzial der Wasserstoffelektrode als Null definiert. Die Wasserstoffelektrode wird Standard-Wasserstoff-Elektrode genannt. Aufgabe I. Physik (Die erreichbare Punktzahl für die Aufgaben ist 10) 1. Ein Wasserstoffbläschen mit 8,00 mm 3 Volumen befindet sich nahe der Platinelektrode in einer Tiefe von 15,00 cm, wo die Temperatur 25 C beträgt. Das Bläschen steigt bis zur Oberfläche der Salzsäurelösung, die die Temperatur 27 C hat. Nimm an, dass die Temperatur des Bläschens die selbe wie die der umgebenden Flüssigkeit und dass die Dichte der Flüssigkeit einheitlich gleich der von Wasser (1, kg/m 3 ) ist. Die Erdbeschleunigung ist 9,80 m/s 2 und H 2 wird als ideales zweiatomiges Gas betrachtet. Bestimme das Volumen des Bläschens unmittelbar bevor es die Oberfläche der Lösung erreicht (1 atm = 1, Pa)! (3 Punkte) 2. Bestimme die Änderung der resultierenden Kraft, die auf das Wasserstoffbläschen wirkt, wenn es von einem Punkt außerhalb des unteren Endes der Platinelektrode, aber auf der selben Höhe, auf der sich das untere Ende der Elektrode befindet, bis zur Oberfläche der Lösung aufsteigt! (2 Punkte) 3. Sei r der Abstand zwischen den beiden Wasserstoffatomen des H 2 - Moleküls. Die beiden Wasserstoffatome des H 2 -Moleküls sind entsprechend der effektiven potentiellen Energie V(r), wie sie in Abbildung 2 dargestellt ist, aneinander gebunden V H r (Å) Abbildung 2. Die effektive potentielle Energie des H 2 -Moleküls in Abhängigkeit vom Abstand der beiden Atome (1 Ǻ = m) T-2/12
3 (a) Bestimme den Gleichgewichtsabstand der beiden Atome des H 2 - Moleküls! (1 Punkt) (b) Ist die Kraft zwischen den beiden Atomen abstoßend ( ) oder anziehend ( ) wenn ihr Abstand ein wenig kleiner als der Gleichgewichtsabstand wird? (1 Punkt) (c) Ist die Kraft zwischen den beiden Atomen abstoßend ( ) oder anziehend ( ) wenn ihr Abstand ein wenig größer als der Gleichgewichtsabstand wird? (1 Punkt) 4. Nimm an, dass ein H 2 -Molekül sich anfangs im Gleichgewichtsabstand befindet. Wie man im Diagramm in Abbildung 2 erkennt, können die beiden Wasserstoffatome sich entweder einander nähern oder sich voneinander entfernen, sobald das Molekül zusätzlich Energie aufnimmt. (a) Wie viel Energie muss von dem Molekül aufgenommen werden, um die beiden Wasserstoffatome völlig voneinander zu trennen? (1 Punkt) (b) Bestimme den kleinsten und den größten Abstand zwischen den beiden Atomen, wenn die vom Molekül aufgenommene Energie 2,8 ev beträgt? (1 Punkt) T-3/12
4 Aufgabe II. Chemie (Die erreichbare Punktzahl für die Aufgaben ist 10) (In den Teilaufgabe 1, 2 und 3 geht es um denselben Prozess wie in Aufgabe I) 1. Welche chemischen Bindungen oder Kräfte wirken zwischen (a) Wasserstoffatomen innerhalb des Wasserstoffmoleküls? (b) mehreren Wasserstoffmolekülen im flüssigen Zustand? (1 Punkt) (1 Punkt) 2. Das Wasserstoffgas muss in einer Wasserstoffelektrode kontinuierlich in die Elektrolytlösung eingeleitet werden. Dadurch wird eine der folgenden Bedingungen erfüllt: (2 Punkte) A. kontinuierliche Sättigung der Lösung mit Wasserstoffgas B. Säuberung der Platinelektrode C. Steuerung des höchsten Elektrodenpotenzials D. Minimierung des Spannungsverlustes E. Beschleunigung des Prozesses F. Minimierung der Kosten 2. Eine Redoxreaktion (Reduktion-Oxidation) beruht auf einem Elektronenübergang vom Reduktionsmittel zum Oxidationsmittel. Üblicherweise wird eine Standard-Wasserstoff-Elektrode eingesetzt, um Stärke des Oxidationsmittels zu messen. Tabelle 1. Standardpotenziale der Reduktionsreaktionen Reaktion in einer Halbzelle Standardpotenzial in Volt Ag + + e Ag(s) H + + 2e H 2 (g) Cd e Cd(s) Zn e Zn(s) Unter Verwendung der aufgelisteten Daten aus Tabelle 1, (a) ordne die relative Stärke der vier Ionensorten als Oxidationsmittel in absteigender Reihenfolge! (1 Punkt) (b) stelle die Reaktionsgleichung der folgenden Reaktion auf: Ein Cadmium- Stab (Cd) wird in eine wässrige Lösung von Silbernitrat (AgNO 3 ) gestellt. (2 Punkte) T-4/12
5 4. Luft-Batterien nutzen O 2 (g) aus der Luft als Oxidationsmittel. Dabei ist das Reduktionsmittel üblicherweise ein Metall, beispielsweise Zink oder Aluminium. Bei Aluminium-Luft-Batterien finden die Oxidation an einer Aluminiumelektrode und die Reduktion an einer Kohlenstoffelektrode statt. Die Elektrolytlösung innerhalb der Batterie besteht aus NaOH(aq). Aluminium wird zu Al 3+ oxidiert, aber aufgrund der hohen Konzentration an OH bildet sich der anionische Komplex Al(OH) 4. Stelle die Gesamtgleichung der Reaktion auf! (3 Punkte) 3. Die Standardelektrodenpotentiale für die vier halben Zellen werden in aufgelistet T-5/12
6 Problem III. Biologie (Die erreichbare Punktzahl für diese Aufgabe ist 10) 1. Jeder Organismus besteht aus Zellen. Ordne dem jeweiligen Zell-Schema aus der unteren Tabelle 2 die richtige Gruppe von Organismen zu, indem du die richtigen Buchstaben im Antwortbogen für Abbildung 2a und 2b einträgst! (0,5 Punkte) Tabelle 2. Abbildung 2a Abbildung 2b A. Bakterien B. Archaebacterien C. Tiere D. Pflanzen E. Pilze a b Abbildung Die Existenz einiger der unten aufgeführten Merkmale lässt darauf schließen, ob es sich um Pflanzen- oder Tierzellen handelt. Bitte trage die entsprechenden vier Buchstaben (aus A bis I) in das Antwortblatt (1,0 Punkte) A. Zellwand, B. Vakuole, C. Chloroplast, D. Ribosom, E. Zellkern (Nucleus), F. Centriole, G. endoplasmatisches Retikulum, H. Golgi-Apparat, I. Mitocbondrium T-6/12
7 2. Parathormon (Parathyroidhormon, PTH), das in der Nebenschilddrüse gebildet wird, hat ihre regulierende Funktion hauptsächlich in... (Trage den richtigen Buchstaben im Antwortbogen ein, 0,5 Punkte). A. der Erhöhung des Kalziumniveaus im Blut. B. dem Absenken des Glucoseniveaus im Blut. C. der Kontrolle des Kohlehydratstoffwechsel. D. der Kontrolle der Eiweißsynthese. E. der Anregung des Abbaus von Glykogen zu Glucose. 3. Bei den meisten Säugetierarten einschließlich dem Menschen entwickeln sich männliche und weibliche Fortpflanzungsorgane entsprechend ihrem Alter. Teile der weiblichen Fortpflanzungsorgane sind bei der Entwicklung des Eierstocks wichtig. Bei den männlichen Fortpflanzungsorganen spielen einige eine wichtige Rolle bei der Bildung von Spermien (Spermatogenese). Betrachte in Abbildung 3 die Schemata weiblicher und männlicher Fortpflanzungsorgane. T-7/12
8 A B Prostate gland Cervix Vagina C D Scrotum Abbildung Ordne im Antwortbogen den Teilen der Fortpflanzungsorgane, die mit Buchstaben gekennzeichnet sind (A, B, C und D) in der linken Spalte die Ziffern der entsprechenden Organe in der rechten Spalte der Tabelle 3 zu. (1,0 Punkte) Tabelle 3. A... B... C... D Testis (Hoden) 2. Eierstock 3. Samenleiter 4. Epididymis (Nebenhoden) 5. Eileiter 6. Gebärmutter 7. große Schamlippen 8. Bartholinische Drüse T-8/12
9 3.2. Bei der Frau sind mehrere Hormone an der Gesamtheit eines Zyklus der Menstruation beteiligt. Wähle die vier Hormone (aus A bis G) aus der untenstehenden Liste aus, die mit dem Zyklus verbunden sind: (1)..., (2)..., und (3)..., (4)... Trage die richtigen Buchstaben im Antwortbogen ein. (1 Punkt) A. FSH (Follikel stimuliendes Hormon) B. LH (Luteinbildendes Gelbkörperhormon) C. Östrogen D. Testosteron E. Progesteron F. Hypothalamus G. Androgen 3.3. Im männlichen Fortpflanzungssystem gibt es mehrere Hormone, die bestimmte Funktionen haben. Wähle aus der folgenden Tabelle 4 zu der angegebenen Funktion eines Hormons in der linken Spalte das dazu passende Hormon in der rechten Spalte aus! (1 Punkt) Tabelle Stimuliert frühe Stadien der Bildung von Spermien 2. Stimuliert die Sekretion des Testosterons von Leydig-Zellen 3. Stimuliert die Entwicklung und Aufrechterhaltung männlicher sekundärer Sexualmerkmale A. FSH B. Testosteron C. LH D. Progesteron E. Östrogen 4. Die Blutzirkulation hängt bei Säugetieren von der Anatomie des Herzens sowie seines Kreislaufes ab. Der strukturelle Unterschied der Arterien, Venen und Kapillaren steht mit deren Funktionen in Beziehung. Abbildung 4 zeigt das menschliche Herz mit seinen Blutgefäßen. Abbildung 4 (rechts ist dort immer links!) zeigt den Blutfluss durch das Herz. Fülle die Leerstellen der Ziffern (4.1) bis (4.5) im folgenden Absatz mit den dazugehörigen Buchstaben (A bis J) der Tabelle 5 aus und trage die Antworten im Antwortbogen ein. (2,5 Punkte) Die (4.1)... pumpt das Blut zu den Lungen durch die (4.2).... In den Lungen geben Blutzellen Kohlenstoffdioxid ab und nehmen Sauerstoff auf. Sauerstoffreiches Blut geht von den Lungen durch die (4.3)... zum Herzen zurück, dann wird es von der (4.4)... zu den gesamten Körperkreisläufen durch die (4.5)... gepumpt. T-9/12
10 Obere Körper vene Kapillaren des Kopfes und der Arme Kapillaren des rechten Lungenflügels Kapillaren der Verdauungsorgane und der Beine Abbildung 4 Table 5 A. Lungenarterie B. Lungenvene C. Linker Vorhof (Atrium) D. Rechter Vorhof (Atrium) E. Linke Kammer F. Rechte Kammer G. Aorta H. Vene I. Semilunar-Valvus J. Atrioventicular- Valvus T-10/12
11 5. Vogelgrippe ist eine ansteckende Tierkrankheit, die von Viren verursacht wird. Diese infizieren normalerweise nur Vögel und weit weniger Schweine. Vogelgrippeviren sind hoch artspezifisch, aber sie haben in seltenen Fällen die Artschranke überwunden, um Menschen zu infizieren. Vogelgrippeviren haben 16 H (H1 - H16) Untertypen und 9 N (N1 - N9) Unterformen. Unter diesen sind einige der erstgenannten Untertypen bekannt, die hoch pathogene Krankheitsformen verursachen können. Jedoch sind nicht alle Viren dieser Untertypen hoch pathogen und verursachen folglich auch nicht alle schwerwiegende Krankheiten unter Vögeln. 5.1.Im gegenwärtigen Verständnis sind Viren in Geflügelbeständen in ihrer niedrig pathogenen Form weit verbreitet. Vorausgesetzt, dass diese in Geflügelpopulation innerhalb von wenigen Monaten zirkulieren, können die Viren in eine hoch pathogene Form mutieren. Diese beiden Virusuntertypen, die bei uns Menschen am ehesten auftreten können, sind (5.1)... und (5.2)... (je 0,5 Punkte) 5.2.Wird das Vogelgrippevirus leicht von Vögeln auf Menschen übertragen? (0,5 zeigt) A. Ja, das Virus wird leicht vom Vogel auf den Menschen übertragen, insbesondere in Hühnerfarmen. B. Ja, das Virus wird leicht auf den Menschen übertragen, weil Mensch und Hühner dieselben Virusrezeptoren besitzen. C. Nein, weil Menschen keinen besonderen Rezeptor für Vogelviren besitzen. D. Nein, weil im Vergleich zu infizierten Vögeln erst eine relativ geringe Anzahl von Menschen angesteckt wurde. T-11/12
12 6. DNA-Technik ermöglicht Molekularbiologen, die Gene direkt zu studieren, ohne vom Phänotyp auf den Genotyp schließen zu müssen, wie in der klassischen Genetik. Der DNA-Fingerabdruck kann für eine gerichtsmedizinische Analyse verwendet werden, z.b. in einem Strafverfahren. Wähle die richtige Aussage aus der unteren Liste aus, die in erster Linie heute den DNA-Fingerabdruck definiert (0,5 Punkte) A. DNA unterschiedlicher Personen hat praktisch nie genau dasselbe DNA-Muster, PCR-Technik wird verwendet B. DNA unterschiedlicher Personen hat dasselbe Muster C. Um Vorgänger und Vorfahren zu unterscheiden, lässt sich mit DNA Blutgruppenvererbung verfolgen D. Unterschiedliche DNA-Stränge haben unterschiedliche Restriktionsenzym-Schnittstellen. E. Eine Kombination von A und D kann gleichzeitig verwendet werden T-12/12
Zellen. Biologie. Kennzeichen des Lebens. Das Skelett des Menschen. Zellen sind die kleinste Einheit aller Lebewesen.
 1. 3. Biologie Zellen Zellen sind die kleinste Einheit aller Lebewesen. Ist die Naturwissenschaft, die sich mit dem Bau und Funktion der Lebewesen beschäftigt. Dazu zählen Bakterien, Pflanzen, Pilze und
1. 3. Biologie Zellen Zellen sind die kleinste Einheit aller Lebewesen. Ist die Naturwissenschaft, die sich mit dem Bau und Funktion der Lebewesen beschäftigt. Dazu zählen Bakterien, Pflanzen, Pilze und
Herz & Blutgefäße des Menschen sowie Blutdruck
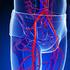 Blut Themen- & Lernzettel (5) Datum: 19.11.16 1 Das Herz: Herz & Blutgefäße des Menschen sowie Blutdruck Das Herz ist ein Muskel und zwar ein Hohlmuskel. Es pumpt das Blut (gerichtet!*) durch den Körper.
Blut Themen- & Lernzettel (5) Datum: 19.11.16 1 Das Herz: Herz & Blutgefäße des Menschen sowie Blutdruck Das Herz ist ein Muskel und zwar ein Hohlmuskel. Es pumpt das Blut (gerichtet!*) durch den Körper.
Die roten Fäden durch die Biologie Natur und Technik/ Biologie Grundwissen: 8. Klasse
 Die roten Fäden durch die Biologie Natur und Technik/ Biologie Grundwissen: 8. Klasse Steuerung und Regelung Struktur und Funktion Variabilität und Angepasstheit Stoff- und Energieumwandlung Steuerung
Die roten Fäden durch die Biologie Natur und Technik/ Biologie Grundwissen: 8. Klasse Steuerung und Regelung Struktur und Funktion Variabilität und Angepasstheit Stoff- und Energieumwandlung Steuerung
Das Blut fließt nicht wie beim geschlossenen Blutkreislauf in Gefäßen (Adern) zu den Organen, sondern umspült diese frei.
 Grundwissen Biologie 8. Klasse 6 Eucyte Zelle: kleinste lebensfähige Einheit der Lebewesen abgeschlossene spezialisierte Reaktionsräume Procyte Vakuole Zellwand pflanzliche Zelle Zellkern tierische Zelle
Grundwissen Biologie 8. Klasse 6 Eucyte Zelle: kleinste lebensfähige Einheit der Lebewesen abgeschlossene spezialisierte Reaktionsräume Procyte Vakuole Zellwand pflanzliche Zelle Zellkern tierische Zelle
Was ist Elektrochemie? Elektrochemie. Elektrochemie ist die Lehre von der Beziehung
 Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Was ist Elektrochemie? Elektrochemie Elektrochemie ist die Lehre von der Beziehung zwischen elektrischen und chemischen Prozessen. 131 Stromleitung in einem Metall Wir haben gelernt, dass die Stromleitung
Hoden Eierstöcke FSH (Follikel- stimulierendes Hormon) LH (Luteinisierendes Hormon). Testosteron
 Geschlechtshormone Wie ihr schon gelernt habt, bildet die Nebennierenrinde Geschlechtshormone, welche aber eher schwach wirken oder als Vorläufer dienen. Die wichtigeren Hormondrüsen für die Entwicklung
Geschlechtshormone Wie ihr schon gelernt habt, bildet die Nebennierenrinde Geschlechtshormone, welche aber eher schwach wirken oder als Vorläufer dienen. Die wichtigeren Hormondrüsen für die Entwicklung
Grundlagen: Galvanische Zellen:
 E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
E1 : Ionenprodukt des Wassers Grundlagen: Galvanische Zellen: Die Galvanische Zelle ist eine elektrochemische Zelle. In ihr laufen spontan elektrochemische Reaktionen unter Erzeugung von elektrischer Energie
Allgemeines - Die biologischen Kennzeichen der Lebewesen: 1.) Stoffwechsel und Energiewandlung. 5.) Aufbau aus Zellen 2.) Information + Reizbarkeit
 Allgemeines - Die biologischen Kennzeichen der Lebewesen: 1.) Stoffwechsel und Energiewandlung 5.) Aufbau aus Zellen 2.) Information + Reizbarkeit 3.) Aktive Bewegung 4.) Fortpflanzung und Entwicklung
Allgemeines - Die biologischen Kennzeichen der Lebewesen: 1.) Stoffwechsel und Energiewandlung 5.) Aufbau aus Zellen 2.) Information + Reizbarkeit 3.) Aktive Bewegung 4.) Fortpflanzung und Entwicklung
Funktionsmodell des Blutkreislaufes
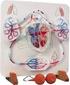 Funktionsmodell des Blutkreislaufes 1. Benutzung Füllen des Blutkreislaufmodells 1. Legen Sie das Modell flach auf den Tisch. 2. Koppeln Sie die blauen Röhrchen vom Blutkreislauf ab, die Verbindungen befinden
Funktionsmodell des Blutkreislaufes 1. Benutzung Füllen des Blutkreislaufmodells 1. Legen Sie das Modell flach auf den Tisch. 2. Koppeln Sie die blauen Röhrchen vom Blutkreislauf ab, die Verbindungen befinden
Übung 10 (Redox-Gleichgewichte und Elektrochemie)
 Übung 10 (Redox-Gleichgewichte und Elektrochemie) Verwenden Sie neben den in der Aufgabenstellung gegebenen Potenzialen auch die Werte aus der Potenzial-Tabelle im Mortimer. 1. Ammoniak kann als Oxidationsmittel
Übung 10 (Redox-Gleichgewichte und Elektrochemie) Verwenden Sie neben den in der Aufgabenstellung gegebenen Potenzialen auch die Werte aus der Potenzial-Tabelle im Mortimer. 1. Ammoniak kann als Oxidationsmittel
EinFaCh 1. Studienvorbereitung Chemie. Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie.
 Studienvorbereitung Chemie EinFaCh 1 Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie www.tu-freiberg.de http://tu-freiberg.de/fakultaet2/einfach Was ist eine
Studienvorbereitung Chemie EinFaCh 1 Einstieg in Freibergs anschauliches Chemiewissen Teil 1: Redoxreaktionen und Elektrochemie www.tu-freiberg.de http://tu-freiberg.de/fakultaet2/einfach Was ist eine
GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN
 10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
10. Einheit: GALVANISCHE ELEMENTE, BATTERIEN UND BRENNSTOFFZELLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 17 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Galvanische Elemente, Batterien und
Redoxgleichungen: Massenerhaltung Elektronenaufnahme/ -abgabe Halbreaktion: Getrennter Prozess (Reduktion, Oxidation getrennt anschauen)
 AChe 2 Kapitel 20: Elektrochemie Oxidationszahlen: Ladung des Atomes wenn es als Ion vorliegen würde. Oxidation: OX-Zahl steigt, Reduktion: OX-Zahl sinkt. Redoxgleichungen: Massenerhaltung Elektronenaufnahme/
AChe 2 Kapitel 20: Elektrochemie Oxidationszahlen: Ladung des Atomes wenn es als Ion vorliegen würde. Oxidation: OX-Zahl steigt, Reduktion: OX-Zahl sinkt. Redoxgleichungen: Massenerhaltung Elektronenaufnahme/
6.1 Elektrodenpotenzial und elektromotorische Kraft
 6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
6.1 Elektrodenpotenzial und elektromotorische Kraft Zinkstab Kupferstab Cu 2+ Lösung Cu 2+ Lösung Zn + 2e Cu Cu 2+ + 2e Cu 2+ Eine Elektrode ist ein metallisch leitender Gegenstand, der zur Zu oder Ableitung
Das Herz. 02a / Das Herz
 Das Herz 02a / Das Herz Das Herz Das Herz liegt leicht links vorne im Brustkorb Die Grösse des Herzens entspricht ungefähr deiner Faust Das Herz wiegt bei einem Erwachsenen ungefähr 300 350 g (Die Herze
Das Herz 02a / Das Herz Das Herz Das Herz liegt leicht links vorne im Brustkorb Die Grösse des Herzens entspricht ungefähr deiner Faust Das Herz wiegt bei einem Erwachsenen ungefähr 300 350 g (Die Herze
Redoxreaktionen. Mg + ½ O 2. MgO. 3 Mg + N 2 Mg 3 N 2. Mg ½ O + 2 e O 2. 3 Mg 3 Mg e
 Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 2 Mg ½ O + 2 e 2+ Mg + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N + 6 e 2 N 3 2 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 2 Mg ½ O + 2 e 2+ Mg + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N + 6 e 2 N 3 2 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Physiologie des Herz- PDF created with pdffactory trial version
 Physiologie des Herz- Kreislaufsystems Fakten über das Herz ca. 3 Milliarden Schläge im Leben pumpt ca. 250 Millionen Liter Blut durch den Körper wiegt in etwa 300 g das Herz bildet zusammen mit den Blutgefäßen
Physiologie des Herz- Kreislaufsystems Fakten über das Herz ca. 3 Milliarden Schläge im Leben pumpt ca. 250 Millionen Liter Blut durch den Körper wiegt in etwa 300 g das Herz bildet zusammen mit den Blutgefäßen
Kennzeichen des Lebens. Zelle. Evolution. Skelett (5B1) (5B2) (5B3) (5B4)
 Kennzeichen des Lebens (5B1) 1. Informationsaufnahme, Informationsverarbeitung und Reaktion 2. aktive Bewegung 3. Stoffwechsel 4. Energieumwandlung 5. Fortpflanzung 6. Wachstum 7. Aufbau aus Zellen Zelle
Kennzeichen des Lebens (5B1) 1. Informationsaufnahme, Informationsverarbeitung und Reaktion 2. aktive Bewegung 3. Stoffwechsel 4. Energieumwandlung 5. Fortpflanzung 6. Wachstum 7. Aufbau aus Zellen Zelle
Das Potenzial einer Halbzelle lässt sich mittels der Nernstschen Gleichung berechnen. oder
 Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Allgemeine Chemie I (AC) HS 2011 Übungen Serie 9
 Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 9 Redox-Reaktionen C 1. Aus den Angaben in den Latimer-Diagrammen für Vanadium in saurer bw. basischer konstruieren Sie
Prof. A. Togni, D-CHAB, HCI H 239 Allgemeine Chemie I (AC) HS 2011 Übungen Serie 9 Redox-Reaktionen C 1. Aus den Angaben in den Latimer-Diagrammen für Vanadium in saurer bw. basischer konstruieren Sie
Universität des Saarlandes - Fachrichtung Anorganische Chemie C h e m i s c h e s E i n f ü h r u n g s p r a k t i k u m.
 Universität des Saarlandes - Fachrichtung Anorganische Chemie C h e m i s c h e s E i n f ü h r u n g s p r a k t i k u m Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb
Universität des Saarlandes - Fachrichtung Anorganische Chemie C h e m i s c h e s E i n f ü h r u n g s p r a k t i k u m Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb
Aufnahme der Nährstoffbausteine vom Darm in die Blutbahn durch Diffusion und aktiven Transport
 Nährstoffe 10 1 10 1 Organische Stoffe, die von heterotrophen Organismen zur Energiegewinnung bzw. zum Aufbau des Organismus aufgenommen werden müssen. Kohlenhydrate (Zucker und Stärke) Fette (ein Fettmolekül
Nährstoffe 10 1 10 1 Organische Stoffe, die von heterotrophen Organismen zur Energiegewinnung bzw. zum Aufbau des Organismus aufgenommen werden müssen. Kohlenhydrate (Zucker und Stärke) Fette (ein Fettmolekül
Das Potenzial einer Halbzelle lässt sich mittels der Nernstschen Gleichung berechnen. oder
 Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Zusammenfassung Redoxreaktionen Oxidation entspricht einer Elektronenabgabe Reduktion entspricht einer Elektronenaufnahme Oxidation und Reduktion treten immer gemeinsam auf Oxidationszahlen sind ein Hilfsmittel
Suprijono Suharjoto - Fotolia.com. Alles neu? 10w. Alles anders! 7s 8w. 4s 6s. 2s 5s. 1s 9w. Lösung: 1w 7w 8s. 3s 11w. Arbeitsblatt 7 1 Seite 38
 6w 5w Alles anders! 4s 6s 1s 9w 1w 7w 8s 9 6 2 13 10w 2w 5 9s 2s 5s 7 3s 11w 10 14 3w 7s 8w 1 11 15 4w 12 3 8 4 Lösung: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Arbeitsblatt 7 1 Seite 38 Alles anders! waagrecht
6w 5w Alles anders! 4s 6s 1s 9w 1w 7w 8s 9 6 2 13 10w 2w 5 9s 2s 5s 7 3s 11w 10 14 3w 7s 8w 1 11 15 4w 12 3 8 4 Lösung: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Arbeitsblatt 7 1 Seite 38 Alles anders! waagrecht
Die roten Fäden durch die Biologie
 Die roten Fäden durch die Biologie LPG-Grundwissen: 5. Klasse Energie ebene Energie Oberfläche Oberfläche...... Organisations- Fortpflanzung Fortpflanzung Stoffwechsel Stoffwechsel 5. Jgst. 1 5. Jgst.
Die roten Fäden durch die Biologie LPG-Grundwissen: 5. Klasse Energie ebene Energie Oberfläche Oberfläche...... Organisations- Fortpflanzung Fortpflanzung Stoffwechsel Stoffwechsel 5. Jgst. 1 5. Jgst.
Universität des Saarlandes - Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum. Elektrochemie
 Universität des Saarlandes Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb der Chemie. Sie ist zum einen
Universität des Saarlandes Fachrichtung Anorganische Chemie Chemisches Einführungspraktikum Elektrochemie Elektrochemie bezeichnet mehrere verschiedene Teilgebiete innerhalb der Chemie. Sie ist zum einen
Übungen zur VL Chemie für Biologen und Humanbiologen Was wird gebildet, wenn Natrium oxidiert wird und Chlor reduziert wird?
 Übungen zur VL Chemie für Biologen und Humanbiologen 12. 11.2010 1. Was wird gebildet, wenn Natrium oxidiert wird und Chlor reduziert wird? Natrium gibt bei der Oxidation ein Elektron ab und bildet damit
Übungen zur VL Chemie für Biologen und Humanbiologen 12. 11.2010 1. Was wird gebildet, wenn Natrium oxidiert wird und Chlor reduziert wird? Natrium gibt bei der Oxidation ein Elektron ab und bildet damit
Beispiele zur Anwendung der Nernst-Gleichung (II)
 Chemie-Arbeitsblatt Klasse _ Name: Datum:.. Beispiele zur Anwendung der Nernst-Gleichung (II) 3 Aufgabe I: Gegeben sind die Standard-Elektrodenpotenziale für Cu/Cu : 0,35V, Au/Au : 1,4 V und Cl /Cl : 1,36
Chemie-Arbeitsblatt Klasse _ Name: Datum:.. Beispiele zur Anwendung der Nernst-Gleichung (II) 3 Aufgabe I: Gegeben sind die Standard-Elektrodenpotenziale für Cu/Cu : 0,35V, Au/Au : 1,4 V und Cl /Cl : 1,36
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
M 1.1: Checkup beim Taucharzt Die Blutdruckmessung
 M 1.1: Checkup beim Taucharzt Die Blutdruckmessung Der Tauchsport verlangt geistige Wachsamkeit und körperliche Fitness. Der Arzt untersucht bei der Tauchtauglichkeitsuntersuchung neben dem Allgemeinzustand
M 1.1: Checkup beim Taucharzt Die Blutdruckmessung Der Tauchsport verlangt geistige Wachsamkeit und körperliche Fitness. Der Arzt untersucht bei der Tauchtauglichkeitsuntersuchung neben dem Allgemeinzustand
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R , Tel /Sekretariat Frau Endrias Tel.
 Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Grundlagen der Molekularen Biophysik WS 2011/12 (Bachelor) Dozent: Prof Dr. Ulrike Alexiev (R.1.2.34, Tel. 55157/Sekretariat Frau Endrias Tel. 53337) Tutoren: Dr. Kristina Kirchberg, Alex Boreham 6-stündig
Glossar. gesamte Schülerinformation. Bezug
 Stufe 1 06 / Das Blut Lehrerinformation 1/5 Bezug gesamte Schülerinformation Arbeitsauftrag Die Schüler suchen zu den nummerierten Begriffen den zugehörigen Erklärungstext und notieren die richtige Ziffer
Stufe 1 06 / Das Blut Lehrerinformation 1/5 Bezug gesamte Schülerinformation Arbeitsauftrag Die Schüler suchen zu den nummerierten Begriffen den zugehörigen Erklärungstext und notieren die richtige Ziffer
Procyte Eucyte Organell Aufgabe Zellorganell Autotrophe Stellen Nährstoffe selbst her Organismen Pflanzen Fotosynthese Bakterien Chemosynthese
 Procyte (die) Eucyte (die) Zellorganell (das; -organellen) Organell Zellkern Ribosomen Mitochondrien Chloroplasten Endoplasmatisches Retikulum (ER) Golgiapparat (Dictyosom) Membran Zellwand Vakuole Aufgabe
Procyte (die) Eucyte (die) Zellorganell (das; -organellen) Organell Zellkern Ribosomen Mitochondrien Chloroplasten Endoplasmatisches Retikulum (ER) Golgiapparat (Dictyosom) Membran Zellwand Vakuole Aufgabe
vegetatives Nervensystem Zentrales Nervensystem ZNS Nervenzelle Synapse unwillkürlicher Teil des Nervensystems mit Sympathicus und Parasympathicus;
 vegetatives Nervensystem ( 9. Klasse 1 / 32 ) unwillkürlicher Teil des Nervensystems mit Sympathicus und Parasympathicus; innerviert innere Organe, Blutgefäße und Drüsen bestehend aus Zentrales Nervensystem
vegetatives Nervensystem ( 9. Klasse 1 / 32 ) unwillkürlicher Teil des Nervensystems mit Sympathicus und Parasympathicus; innerviert innere Organe, Blutgefäße und Drüsen bestehend aus Zentrales Nervensystem
In der Jahrgangsstufe 8 erwerben die Schüler folgendes Grundwissen:
 In der Jahrgangsstufe 8 erwerben die Schüler folgendes Grundwissen: Sie kennen die Bedeutung der Bakterien und grundlegende Unterschiede zwischen Pro- und Eucyte. Sie können einfache Objekte mikroskopisch
In der Jahrgangsstufe 8 erwerben die Schüler folgendes Grundwissen: Sie kennen die Bedeutung der Bakterien und grundlegende Unterschiede zwischen Pro- und Eucyte. Sie können einfache Objekte mikroskopisch
Reduktion und Oxidation. Oxidationszahlen (OZ)
 Redox-Reaktionen Reduktion und Oxidation Oxidationszahlen (OZ) REDOX Reaktionen / - Gleichungen Das elektrochemische Potential Die Spannungsreihe der Chemischen Elemente Die Nernstsche Gleichung Definitionen
Redox-Reaktionen Reduktion und Oxidation Oxidationszahlen (OZ) REDOX Reaktionen / - Gleichungen Das elektrochemische Potential Die Spannungsreihe der Chemischen Elemente Die Nernstsche Gleichung Definitionen
Merkmale des Lebens. - Aufbau aus Zellen - Wachstum - Vermehrung - Reaktion auf Reize - Bewegung aus eigener Kraft - Stoffwechsel
 Merkmale des Lebens - Aufbau aus Zellen - Wachstum - Vermehrung - Reaktion auf Reize - Bewegung aus eigener Kraft - Stoffwechsel Alle Lebewesen bestehen aus Zellen Fragen zum Text: - Was sah Hooke genau?
Merkmale des Lebens - Aufbau aus Zellen - Wachstum - Vermehrung - Reaktion auf Reize - Bewegung aus eigener Kraft - Stoffwechsel Alle Lebewesen bestehen aus Zellen Fragen zum Text: - Was sah Hooke genau?
SS Thomas Schrader. der Universität Duisburg-Essen. (Teil 8: Redoxprozesse, Elektrochemie)
 Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Chemie für Biologen SS 2010 Thomas Schrader Institut t für Organische Chemie der Universität Duisburg-Essen (Teil 8: Redoxprozesse, Elektrochemie) Oxidation und Reduktion Redoxreaktionen: Ein Atom oder
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
2. Vergleiche die Werte, die bei Methode A bzw. B herauskommen, miteinander!
 Chemie-Arbeitsblatt Klasse _ Name: Datum:.. Beispiele zur Anwendung der Nernst-Gleichung (II) Aufgabe I: Gegeben sind die Standard-Elektrodenpotenziale für Cu/Cu 2+ : +0,35V, Au/Au 3+ : +1,42 V und 2ClG/Cl
Chemie-Arbeitsblatt Klasse _ Name: Datum:.. Beispiele zur Anwendung der Nernst-Gleichung (II) Aufgabe I: Gegeben sind die Standard-Elektrodenpotenziale für Cu/Cu 2+ : +0,35V, Au/Au 3+ : +1,42 V und 2ClG/Cl
Kennzeichen des Lebens. Zelle. Stoffebene und Teilchenebene. Teilchenmodell. Allen Lebewesen sind folgende Merkmale gemeinsam:
 Allen Lebewesen sind folgende Merkmale gemeinsam: Kennzeichen des Lebens Zelle Grundbaustein der Lebewesen. Ist aus verschiedenen Zellorganellen, die spezielle Aufgaben besitzen, aufgebaut. Pflanzenzelle
Allen Lebewesen sind folgende Merkmale gemeinsam: Kennzeichen des Lebens Zelle Grundbaustein der Lebewesen. Ist aus verschiedenen Zellorganellen, die spezielle Aufgaben besitzen, aufgebaut. Pflanzenzelle
3 Mg 3 Mg e N e 2 N 3
 Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Redoxreaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 1 Redoxreaktionen 2 Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust
Was macht eigentlich das Herz? Lehrerinformation
 Was macht eigentlich das Herz? Lehrerinformation 1/6 Arbeitsauftrag Ziel Die SuS erfahren durch ein Referat, welche wichtige Arbeit das Herz verrichtet und was dabei im Körper vorgeht. Sie erfahren zudem,
Was macht eigentlich das Herz? Lehrerinformation 1/6 Arbeitsauftrag Ziel Die SuS erfahren durch ein Referat, welche wichtige Arbeit das Herz verrichtet und was dabei im Körper vorgeht. Sie erfahren zudem,
Elektrizität. = C J m. Das Coulomb Potential φ ist dabei:
 Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Elektrizität Die Coulombsche potentielle Energie V einer Ladung q im Abstand r von einer anderen Ladung q ist die Arbeit, die aufgewendet werden muss um die zwei Ladungen aus dem Unendlichen auf den Abstand
Nr. Aussage In der Nase wird die Luft erwärmt, gefiltert und getrocknet.
 Diagnosebogen Der Weg der Atemluft - Die Bestandteile des Atemapparates nennen und ihre Funktion angeben. - Den Weg der Atemluft beschreiben. Häkchen in Spalte 1 ein. 1 In der Nase wird die Luft erwärmt,
Diagnosebogen Der Weg der Atemluft - Die Bestandteile des Atemapparates nennen und ihre Funktion angeben. - Den Weg der Atemluft beschreiben. Häkchen in Spalte 1 ein. 1 In der Nase wird die Luft erwärmt,
Kapitel 2 Repetitionen Chemie und Werkstoffkunde. Thema 6 Oxidation und Reduktion
 BEARBEITUNGSTECHNIK REPETITONEN LÖSUNGSSATZ Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 6 Oxidation und Reduktion Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772
BEARBEITUNGSTECHNIK REPETITONEN LÖSUNGSSATZ Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 6 Oxidation und Reduktion Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772
DOWNLOAD. Last Minute: Der Körperkreislauf. Materialien für die schnelle Unterrichtsvorbereitung. Biologie 6. Klasse. Last Minute: Biologie 6.
 DOWNLOAD Rebecca Dziomba Tina Konz Michaela Seim Last Minute: Körperkreislauf Materialien für die schnelle Unterrichtsvorbereitung Rebecca Dziomba, Tina Konz, Michaela Seim Biologie 6. Klasse Bergedorfer
DOWNLOAD Rebecca Dziomba Tina Konz Michaela Seim Last Minute: Körperkreislauf Materialien für die schnelle Unterrichtsvorbereitung Rebecca Dziomba, Tina Konz, Michaela Seim Biologie 6. Klasse Bergedorfer
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Elektrochemie Stefan Wuttke # 2 Aus den Anfängen
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2016 Elektrochemie Stefan Wuttke # 2 Aus den Anfängen
Der Blutkreislauf Veränderung von Wissen über die Zeit
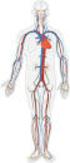 Der Blutkreislauf Veränderung von Wissen über die Zeit Jahrgangsstufen 5 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Natur und Technik (Schwerpunkt Biologie) --- 40 min Benötigtes
Der Blutkreislauf Veränderung von Wissen über die Zeit Jahrgangsstufen 5 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Natur und Technik (Schwerpunkt Biologie) --- 40 min Benötigtes
Mein Buch des Lebens: Ein Mensch entsteht. Wörtersalat:
 Arbeitsblatt 1 zur Sendung 40 Wochen Von der Keimzelle zum Kind im SWR Fernsehen Stammnummer 4685036 MEIN BUCH DES LEBENS EIN MENSCH ENTSTEHT (1): DECKBLATT UND WÖRTERSALAT Aus einer weiblichen Eizelle
Arbeitsblatt 1 zur Sendung 40 Wochen Von der Keimzelle zum Kind im SWR Fernsehen Stammnummer 4685036 MEIN BUCH DES LEBENS EIN MENSCH ENTSTEHT (1): DECKBLATT UND WÖRTERSALAT Aus einer weiblichen Eizelle
Grundaufbau. Das menschliche Herz setzt sich aus 2 Teilen zusammen.
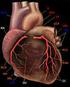 Das Herz und EKG Grundaufbau Das menschliche Herz setzt sich aus 2 Teilen zusammen. Rechte Herzhälfte: Blut kommt vom Körper und geht zur Lunge. Linke Herzhälfte: Blut kommt von der Lunge und geht zum
Das Herz und EKG Grundaufbau Das menschliche Herz setzt sich aus 2 Teilen zusammen. Rechte Herzhälfte: Blut kommt vom Körper und geht zur Lunge. Linke Herzhälfte: Blut kommt von der Lunge und geht zum
THEORETISCHE KLAUSUR 9. Dezember 2004
 THEORETISCHE KLAUSUR 9. Dezember 2004 Aufgabe I. (10 Punkte) I.A Das menschliche Verdauungssystem. (6 Punkte) Verwende die folgende Abbildung und die Tabelle, um die Fragen auf der nächsten Seite zu beantworten
THEORETISCHE KLAUSUR 9. Dezember 2004 Aufgabe I. (10 Punkte) I.A Das menschliche Verdauungssystem. (6 Punkte) Verwende die folgende Abbildung und die Tabelle, um die Fragen auf der nächsten Seite zu beantworten
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 3, /
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 3, 02.05.11/03.05.11 1. Sie haben Silberbesteck geerbt. Um Ihren neuen Reichtum ordentlich zur Schau zu stellen, haben
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 3, 02.05.11/03.05.11 1. Sie haben Silberbesteck geerbt. Um Ihren neuen Reichtum ordentlich zur Schau zu stellen, haben
Sexualität. und bewerten. Kombination aus reproduzierendem und selbstständigem Handeln. B4.1 Organe von Pflanzen und ihre Aufgaben
 Sexualität Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung B3.7 Fortpflanzung bei Menschen, Tieren und Pflanzen in Grundzügen W1 Ich kann Vorgänge und Phänomene in Natur, Umwelt und Technik
Sexualität Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung B3.7 Fortpflanzung bei Menschen, Tieren und Pflanzen in Grundzügen W1 Ich kann Vorgänge und Phänomene in Natur, Umwelt und Technik
Diagnose Vorhofflimmern. Das Risiko eines Schlaganfalls
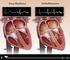 Diagnose Vorhofflimmern Das Risiko eines Schlaganfalls Inhalt Einleitung... 4 Das Herz... 4 Herz-Kreislauf-System... 5 Was versteht man unter Vorhofflimmern?... 6 Was können Ursachen des Vorhofflimmerns
Diagnose Vorhofflimmern Das Risiko eines Schlaganfalls Inhalt Einleitung... 4 Das Herz... 4 Herz-Kreislauf-System... 5 Was versteht man unter Vorhofflimmern?... 6 Was können Ursachen des Vorhofflimmerns
EKG und periphere Zirkulation - Hintergrund
 EKG und periphere Zirkulation - Hintergrund Das Herz ist eine Doppelpumpe, die Blut durch den Körper und die Lunge pumpt. Das Blut tritt mit einem niedrigen Druck in die Vorhofkammern des Herzens ein und
EKG und periphere Zirkulation - Hintergrund Das Herz ist eine Doppelpumpe, die Blut durch den Körper und die Lunge pumpt. Das Blut tritt mit einem niedrigen Druck in die Vorhofkammern des Herzens ein und
Übungsaufgaben zum Lernprogramm Stoffwechsler
 1 Energiebindung und Stoffaufbau durch Photosynthese 1.1 Ergänze mit Hilfe des Programms die folgende Tabelle: Ort in der Zelle: Lichtreaktion Calvin-Zyklus der Edukte: der Produkte: Energieträger: Bildung:
1 Energiebindung und Stoffaufbau durch Photosynthese 1.1 Ergänze mit Hilfe des Programms die folgende Tabelle: Ort in der Zelle: Lichtreaktion Calvin-Zyklus der Edukte: der Produkte: Energieträger: Bildung:
2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom 01.02.2012 A1 A2 A3 R4 F5 E6 Σ Note 8 11 6 10 10 5 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben
2. Teilklausur zum Chemischen Grundpraktikum im WS 2011/12 vom 01.02.2012 A1 A2 A3 R4 F5 E6 Σ Note 8 11 6 10 10 5 50 NAME/VORNAME:... Matrikelnummer:... Pseudonym für Ergebnisveröffentlichung Schreiben
Lernzielkontrolle Sekunda
 Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (15) Richtzeit: 25 Minuten 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) Manche
Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (15) Richtzeit: 25 Minuten 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) Manche
MacGyver Batterie. Wer ist MacGyver?
 MacGyver Batterie Wer ist MacGyver? Angus Mac Gyvers auffälligste Fähigkeit ist die praktische Anwendung der Naturwissenschaften und die damit verbundene erfinderische Nutzung alltäglicher Gegenstände.
MacGyver Batterie Wer ist MacGyver? Angus Mac Gyvers auffälligste Fähigkeit ist die praktische Anwendung der Naturwissenschaften und die damit verbundene erfinderische Nutzung alltäglicher Gegenstände.
Zellen brauchen Sauerstoff Information
 Zellen brauchen Sauerstoff Information Tauchregel: Suche mit deiner schweren Tauchausrüstung einen direkten Weg zum Einstieg ins Wasser. Tauchen ist wie jede andere Sportart geprägt von körperlicher Anstrengung.
Zellen brauchen Sauerstoff Information Tauchregel: Suche mit deiner schweren Tauchausrüstung einen direkten Weg zum Einstieg ins Wasser. Tauchen ist wie jede andere Sportart geprägt von körperlicher Anstrengung.
(a) [4] Um welches Element handelt es sich? (Lösungsweg angeben)
![(a) [4] Um welches Element handelt es sich? (Lösungsweg angeben) (a) [4] Um welches Element handelt es sich? (Lösungsweg angeben)](/thumbs/88/117474080.jpg) Klausur zur Vorlesung LV 18000, AC1 (Anorganische Experimentalchemie) am 03.09.2007 1 1 2 3 4 5 6 7 8 9 10 Σ Note: Vorname: Matr.-Nr.: Nachname: Chemie und Biochemie Lehramt Chemie vertieft Lehramt Chemie
Klausur zur Vorlesung LV 18000, AC1 (Anorganische Experimentalchemie) am 03.09.2007 1 1 2 3 4 5 6 7 8 9 10 Σ Note: Vorname: Matr.-Nr.: Nachname: Chemie und Biochemie Lehramt Chemie vertieft Lehramt Chemie
Protokoll für die Gewässergütebestimmung mit Zeigerarten. Bestimme alle gefangenen Arten. Zähle sie aus und trage sie in das Protokoll ein.
 Protokoll Protokoll für die Gewässergütebestimmung mit Zeigerarten Bestimme alle gefangenen Arten. Zähle sie aus und trage sie in das Protokoll ein. Bioindikator Anzahl Index Produkt Steinfliegenlarve
Protokoll Protokoll für die Gewässergütebestimmung mit Zeigerarten Bestimme alle gefangenen Arten. Zähle sie aus und trage sie in das Protokoll ein. Bioindikator Anzahl Index Produkt Steinfliegenlarve
Kennzeichen des Lebens. Zelle. Skelett. Muskeln
 Kennzeichen des Lebens aktive Bewegung Stoffwechsel (Stoff- und Energieumwandlung) Fortpflanzung Wachstum und Entwicklung Reizbarkeit (Informationsaufnahme, -verarbeitung, Reaktion) Aufbau aus Zellen Grundbaustein
Kennzeichen des Lebens aktive Bewegung Stoffwechsel (Stoff- und Energieumwandlung) Fortpflanzung Wachstum und Entwicklung Reizbarkeit (Informationsaufnahme, -verarbeitung, Reaktion) Aufbau aus Zellen Grundbaustein
-1 (außer in Verbindung mit Sauerstoff: variabel) Sauerstoff -2 (außer in Peroxiden: -1)
 1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
1) DEFINITIONEN DIE REDOXREAKTION Eine Redoxreaktion = Reaktion mit Elektronenübertragung sie teilt sich in Oxidation = Elektronenabgabe Reduktion = Elektronenaufnahme z.b.: Mg Mg 2 + 2 e z.b.: Cl 2 +
MgO. Mg Mg e ½ O e O 2. 3 Mg 3 Mg e N e 2 N 3
 Redox-Reaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 Redox-Reaktionen Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust Na
Redox-Reaktionen Mg + ½ O 2 MgO 3 Mg + N 2 Mg 3 N 2 Mg Mg 2+ + 2 e ½ O 2 + 2 e O 2 3 Mg 3 Mg 2+ + 6 e N 2 + 6 e 2 N 3 Redox-Reaktionen Oxidation und Reduktion Eine Oxidation ist ein Elektronenverlust Na
KORROSION UND KORROSIONSSCHUTZ VON METALLEN
 11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
5.1 Merkmale der Lebewesen. 5.2 Bau der Zelle. 5.3 Reiz-Reaktions-Schema
 5.1 Merkmale der Lebewesen GW 5.Klasse NuT Wachstum und Individualentwicklung Fortpflanzung Stoffwechsel (Stoff- und Energieumwandlung) Aufbau aus Zellen Aktive Bewegung Reizbarkeit : Informationsaufnahme,
5.1 Merkmale der Lebewesen GW 5.Klasse NuT Wachstum und Individualentwicklung Fortpflanzung Stoffwechsel (Stoff- und Energieumwandlung) Aufbau aus Zellen Aktive Bewegung Reizbarkeit : Informationsaufnahme,
Was macht eigentlich das Herz? Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel Die SuS erfahren durch ein Referat, welche wichtige Arbeit das Herz verrichtet und was dabei im Körper vorgeht. Sie erfahren zudem, wie das Herz aufgebaut ist.
Lehrerinformation 1/5 Arbeitsauftrag Ziel Die SuS erfahren durch ein Referat, welche wichtige Arbeit das Herz verrichtet und was dabei im Körper vorgeht. Sie erfahren zudem, wie das Herz aufgebaut ist.
Herz un Blutkreislauf
 1 Herz un Blutkreislauf Name... WORTSCHATZ Blutdruck Blutkreislauf Herzbeutel Herzzyklus Körperkreislauf Lungenkreislauf Muskel Vorhof presión sanguínea circulación sanguínea pericardio ciclo cardíaco
1 Herz un Blutkreislauf Name... WORTSCHATZ Blutdruck Blutkreislauf Herzbeutel Herzzyklus Körperkreislauf Lungenkreislauf Muskel Vorhof presión sanguínea circulación sanguínea pericardio ciclo cardíaco
1 Chemische Elemente und chemische Grundgesetze
 1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1. Biologie die Wissenschaft von den Lebewesen. 2. Der Mensch als Lebewesen. Grundwissen NuT 5. Klasse (LehrplanPlus) Kennzeichen des Lebens
 (zusammengestellt von E. Fischer, A. Grenzinger, A. Hutschenreuther, B. Müller, G. Stadler) 1. Biologie die Wissenschaft von den Lebewesen Kennzeichen des Lebens Stoffwechsel Bewegung aus eigener Kraft
(zusammengestellt von E. Fischer, A. Grenzinger, A. Hutschenreuther, B. Müller, G. Stadler) 1. Biologie die Wissenschaft von den Lebewesen Kennzeichen des Lebens Stoffwechsel Bewegung aus eigener Kraft
Das passiert im Körper des Mannes Im Körper des Mannes sind die Vorgänge nicht weniger
 Die Gelbkörperphase, also die zweite Zyklushälfte, dauert normalerweise 12 bis 14 Tage. Schwankt die Zykluslänge, betrifft dies meist die erste Zyklushälfte, also die Follikelphase. Wie Sie die Länge der
Die Gelbkörperphase, also die zweite Zyklushälfte, dauert normalerweise 12 bis 14 Tage. Schwankt die Zykluslänge, betrifft dies meist die erste Zyklushälfte, also die Follikelphase. Wie Sie die Länge der
1 Was ist Leben? Kennzeichen der Lebewesen
 1 In diesem Kapitel versuche ich, ein großes Geheimnis zu lüften. Ob es mir gelingt? Wir werden sehen! Leben scheint so selbstverständlich zu sein, so einfach. Du wirst die wichtigsten Kennzeichen der
1 In diesem Kapitel versuche ich, ein großes Geheimnis zu lüften. Ob es mir gelingt? Wir werden sehen! Leben scheint so selbstverständlich zu sein, so einfach. Du wirst die wichtigsten Kennzeichen der
Elektrochemie Chemie der Metalle
 Elektrochemie Chemie der Metalle Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Bauchemische Grundlagen Elektrochemie Redoxreaktionen Oxidation Reduktion
Elektrochemie Chemie der Metalle Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Bauchemische Grundlagen Elektrochemie Redoxreaktionen Oxidation Reduktion
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 6 Oxidation und Reduktion Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772 Nidfurn 055-654
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 6 Oxidation und Reduktion Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL Vordergut 1, 8772 Nidfurn 055-654
Praktikumsrelevante Themen
 Praktikumsrelevante Themen RedoxReaktionen Aufstellen von Redoxgleichungen Elektrochemie Quantitative Beschreibung von RedoxGleichgewichten Redoxtitrationen 1 Frühe Vorstellungen von Oxidation und Reduktion
Praktikumsrelevante Themen RedoxReaktionen Aufstellen von Redoxgleichungen Elektrochemie Quantitative Beschreibung von RedoxGleichgewichten Redoxtitrationen 1 Frühe Vorstellungen von Oxidation und Reduktion
4. Redox- und Elektrochemie
 4. Redox und Elektrochemie 4. Redox und Elektrochemie 4.1 Oxidationszahlen Eine Oxidation ist ein Vorgang, wo ein Teilchen Elektronen abgibt. Eine Reduktion ist ein Vorgang, wo ein Teilchen ein Elektron
4. Redox und Elektrochemie 4. Redox und Elektrochemie 4.1 Oxidationszahlen Eine Oxidation ist ein Vorgang, wo ein Teilchen Elektronen abgibt. Eine Reduktion ist ein Vorgang, wo ein Teilchen ein Elektron
Curriculum Naturwissenschaft (NW) Jahrgang 5/6
 Curriculum Naturwissenschaft (NW) Jahrgang 5/6 Themenfeld: Leben mit Pflanzen und Tieren Bauplan der Blütenpflanzen Nutzpflanzen Bewegungssystem Unterscheidung zwischen Wirbeltieren und Wirbellosen Entwicklung
Curriculum Naturwissenschaft (NW) Jahrgang 5/6 Themenfeld: Leben mit Pflanzen und Tieren Bauplan der Blütenpflanzen Nutzpflanzen Bewegungssystem Unterscheidung zwischen Wirbeltieren und Wirbellosen Entwicklung
Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse
 Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Wasserelektrolyse Peter Bützer Inhalt Eine Brennstoffzelle, die Umkehr der Wasserelektrolyse 1 Einleitung/Theorie... 1 2 Datenbasis... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen...
Aufgabe 5 1 (L) Die folgende Redox-Reaktion läuft in der angegebenen Richtung spontan ab: Cr 2
 Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 2015/2016 Prof. Dr. Eckhard Bartsch / Marcel Werner M.Sc. Aufgabenblatt 5 vom 27.11.15 Aufgabe 5 1
Institut für Physikalische Chemie Lösungen zu den Übungen zur Vorlesung Physikalische Chemie II im WS 2015/2016 Prof. Dr. Eckhard Bartsch / Marcel Werner M.Sc. Aufgabenblatt 5 vom 27.11.15 Aufgabe 5 1
Teilchenmodell. Reinstoffe. Stoffgemische. Luft ist ein Gasgemisch. Gasnachweise. Naturwissenschaftliches Arbeiten. Reinstoffe.
 1 1 Teilchenmodell Alle Stoffe bestehen aus kleinsten Teilchen, die sich in Größe und Masse unterscheiden. Sie sind selbst unter dem Mikroskop noch nicht sichtbar. Zwischen den kleinsten Teilchen ist nichts.
1 1 Teilchenmodell Alle Stoffe bestehen aus kleinsten Teilchen, die sich in Größe und Masse unterscheiden. Sie sind selbst unter dem Mikroskop noch nicht sichtbar. Zwischen den kleinsten Teilchen ist nichts.
Was ist wichtig für die siebte Kursarbeit?
 Was ist wichtig für die siebte Kursarbeit? Redoxreaktion: Oxidation (Elektronen-Donator) und Reduktion (Elektronen-Akzeptor) korrespondierende Redoxpaare. Prinzip der Lösungstension, Betrachtung der Halbzellenreaktion
Was ist wichtig für die siebte Kursarbeit? Redoxreaktion: Oxidation (Elektronen-Donator) und Reduktion (Elektronen-Akzeptor) korrespondierende Redoxpaare. Prinzip der Lösungstension, Betrachtung der Halbzellenreaktion
Atmung und Energie. Biologie und Umweltkunde. Zuordnung zum Kompetenzmodell (KM)
 Atmung und Energie Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung B3.2 Charakteristische Merkmale von Tiergruppen W3 Ich kann Vorgänge und Phänomene in Natur, Umwelt und Technik in verschiedenen
Atmung und Energie Zuordnung zum Kompetenzmodell (KM) Aufgabe(n) KM Beschreibung B3.2 Charakteristische Merkmale von Tiergruppen W3 Ich kann Vorgänge und Phänomene in Natur, Umwelt und Technik in verschiedenen
Wie ist das gesunde Herz aufgebaut? (vereinfachte Darstellung)
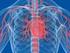 Trikuspidaldysplasie Was ist das? Wie ist das gesunde Herz aufgebaut? (vereinfachte Darstellung) (http://www.transplantation-verstehen.de/dotasset/25070.jpg) Das Herz wird in eine linke und eine rechte
Trikuspidaldysplasie Was ist das? Wie ist das gesunde Herz aufgebaut? (vereinfachte Darstellung) (http://www.transplantation-verstehen.de/dotasset/25070.jpg) Das Herz wird in eine linke und eine rechte
Masse, Volumen und Dichte
 Masse, Volumen und Dichte Ziel: Uns umgeben zahlreiche Gegenstände, die in der Physik als Körper bezeichnet werden. Diese Körper haben eine Reihe von grundlegenden Eigenschaften: Sie nehmen einen Raum
Masse, Volumen und Dichte Ziel: Uns umgeben zahlreiche Gegenstände, die in der Physik als Körper bezeichnet werden. Diese Körper haben eine Reihe von grundlegenden Eigenschaften: Sie nehmen einen Raum
Die Standard Reduktions-Halbzellenpotentiale. Die Standard Reduktions. Wird die Halbzellenreaktion Zn 2+ /Zn gegen die Standard-Wassersoffelektrode
 Die Standard Reduktions Die Standard Reduktions-Halbzellenpotentiale Wird die Halbzellenreaktion Zn 2+ /Zn gegen die Standard-Wassersoffelektrode in einer galvanischen Zelle geschaltet, ergibt sich eine
Die Standard Reduktions Die Standard Reduktions-Halbzellenpotentiale Wird die Halbzellenreaktion Zn 2+ /Zn gegen die Standard-Wassersoffelektrode in einer galvanischen Zelle geschaltet, ergibt sich eine
Biologie. Was ist das? Was tut man da? Womit beschäftigt man sich?
 Biologie Was ist das? Was tut man da? Womit beschäftigt man sich? Wiederholung Merkmal des Lebens Aufbau aus Zellen Alle Lebewesen bestehen aus Zellen. Man kann grob drei verschiedene Zelltypen unterscheiden?
Biologie Was ist das? Was tut man da? Womit beschäftigt man sich? Wiederholung Merkmal des Lebens Aufbau aus Zellen Alle Lebewesen bestehen aus Zellen. Man kann grob drei verschiedene Zelltypen unterscheiden?
Lerneinheit für 5. Klasse AHS
 Lerneinheit für 5. Klasse AHS Zelllehre (Cytologie) Bau und Funktion pflanzlicher und tierischer Zellen Mag. Josef Wöckinger Präge dir mittels folgender Folie die wichtigsten Zellorganellen einer Pflanzenzelle
Lerneinheit für 5. Klasse AHS Zelllehre (Cytologie) Bau und Funktion pflanzlicher und tierischer Zellen Mag. Josef Wöckinger Präge dir mittels folgender Folie die wichtigsten Zellorganellen einer Pflanzenzelle
Chemie. Elektrochemie, Alkane und Alkene
 Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
Zinkhalbzelle Mehr Zusammenfassungen von Malte Jakob findest du hier: hemie Elektrochemie, Alkane und Alkene Elektrochemie Galvanische Zelle: Anode Oxidation - e - e- e U - e - + Kathode Reduktion Zinkelektrode
LICHTENERGIE SOLARZELLE BASIEREND AUF KÜNSTLICHER FOTOSYNTHESE
 LICHTENERGIE SOLARZELLE BASIEREND AUF KÜNSTLICHER FOTOSYNTHESE 15. MAI 2008 - ANTWORTBOGEN 1-1. Land und Team:.. Name: Name:. Name:. Page 1 of 13 EXPERIMENT 1: Vorgehensweise zur Herstellung nanokristalliner
LICHTENERGIE SOLARZELLE BASIEREND AUF KÜNSTLICHER FOTOSYNTHESE 15. MAI 2008 - ANTWORTBOGEN 1-1. Land und Team:.. Name: Name:. Name:. Page 1 of 13 EXPERIMENT 1: Vorgehensweise zur Herstellung nanokristalliner
Natur und Technik. Lernstandserhebung zu den Schwerpunkten Biologie, Naturwissenschaftliches Arbeiten, Informatik. Datum:
 Name: Natur und Technik Lernstandserhebung zu den Schwerpunkten Biologie, Naturwissenschaftliches Arbeiten, Informatik Datum: Klasse: 1 In einem Becherglas befindet sich flüssiges Wasser. Dies lässt sich
Name: Natur und Technik Lernstandserhebung zu den Schwerpunkten Biologie, Naturwissenschaftliches Arbeiten, Informatik Datum: Klasse: 1 In einem Becherglas befindet sich flüssiges Wasser. Dies lässt sich
Stoffwechsel. Die Chemie des Lebens ist in Stoffwechselwegen organisiert
 Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
Die Chemie des Lebens ist in Stoffwechselwegen organisiert Der Stoffwechsel ist die Summe aller chemischen Reaktionen, die in den Zellen eines Organismus auftreten. Unter Mithilfe von Enzymen verläuft
