Vom Handy bis zum Mountainbike Metalle in unserem Alltag im Fokus
|
|
|
- Erna Lorentz
- vor 7 Jahren
- Abrufe
Transkript
1 1 von 42 m Handy bis zum Mountainbike Metalle in uerem Alltag im Fokus t h c i s n a r o V In uerem Alltag kommen wir bewusst und unbewusst mit den unterschiedlhsten Metallen und Metallverbindungen in Kontakt sei es beim Gebuch von Besteck, bei der Benutzung ueres Fahrdes, beim Bezahlen mit Münzgeld oder ganz einfach bei der Verwendung eines Nagels zum Bildaufhängen. Selten machen wir u jedoch Gedanken darüber, wo die Metalle für uere Alltagsgegetände herkommen, wie sie gewonnen und verbeitet werden und welche Eigechaften sie haben. Ihre Schüler führen in Kleingruppen selbstständig Versuche durch, erstellen Versuchsprotokolle und prüfen ihr Wissen anhand von Fgestellungen mit Alltagsbezug und eines abschließenden Kreuzworträtsels. Die Stahlschienen bei der Acerbahn halten enorme Belastungen aus. Auch viele andere Gegetände, die wir im Alltag nutzen, sind aus Metallen gefertigt. Taugt ein : e b a g f u a als Forscher sgetränk g n u h c is Erfr rner? Rostentfe Das Wigste auf einen Blk Klassen: ab Klasse 8 Aus dem Inhalt: Dauer: Stunden Wie wird aus einem Klumpen Erz das gewüce Metall? Kompetenzen: Die Schüler sind in der Lage, rkommen, Gewinnung und Verwendung wiger Metalle zu beschreiben. führen selbstständig Versuche durch, erstellen Versuchsprotokolle und tauschen ihre Erfahrungen aus. Was bedeutet verrosten chemisch betcet? Welche Eigechaften haben Metalle? Welches Metall ist in Handy, Laptop und Co. unerlässlh? erkennen, dass viele chemische rgänge im Zusammenhang mit Metallen und Materialien sie in ihrem Alltag ständig begleiten. Beteiligte Fächer: Chemie Physik Anteil hoch mittel gering Foto: Thinkstockphotos.com Günther Lohmer, Leverkusen
2 10 von 42 M1 Metalle Meister der Vielseitigkeit! Hättet ihr gewusst, welche Metalle u in uerem Alltag begegnen und welche heute für u im Grunde unverzbar geworden sind? In welchen Berehen nutzen wir Metalle? Schaut euch die Abbildungen an. Fotos: Thinkstockphotos.com, istockphoto, G. Lohmer 1. Um welche Metalle könnte es sh in den Abbildungen jeweils handeln bzw. welche Metalle sind in den einzelnen Gegetänden enthalten? Was glaubt ihr? 2. Schreibt eure Vermutungen zu den verwendeten Metallen auf und besprec eure Ergebnisse achließend in der Klasse.
3 11 von 42 Eisen woher kommt es und wie wird es gewonnen? M2 Wusstest du, dass über 90 Prozent des weltweit genutzten Metalls Eisen sind? Eisen bzw. sein Verbeitungsprodukt Stahl dient u in mannigfaltiger Weise. Hier erfährst du mehr über dieses Element, sein rkommen, seine Gewinnung und seine Nutzung. Eisen altbekannt und noch immer heiß begehrt! Eisen gehört zu den am längsten bekannten Metallen. Nach ihm ist eine Periode der Ur- und Frühgesche benannt, die sogenannte Eisenzeit. Die Eisenzeit dauerte in Mitteleuropa von 800 vor Christi bis 100 vor Christi. Gegetände aus Eisen und Stahl kommen vielfach in uerem Schon in der Frühgesche Alltag vor, sei es in Form von Nägeln, Schuben, Maschinen, wurde Eisen für Werkzeuge Brücken oder Schiffen. Selbst in uerem Körper spielt es eine und Waffen verwendet. entscheidende Rolle, da der rote Blutfarbstoff das Hämoglobin Eisen enthält, an das sh der Sauerstoff bindet und dieser dann im Körper tportiert werden kann. Eisen ist wie zahlrehe andere Metalle sehr reaktiofreudig und ge mit anderen Elementen zahlrehe Verbindungen ein. rkommen in der Natur In der Erdkruste ist Eisen mit 4,7 % das vierthäuigste Element und nach Aluminium das zweithäuigste Metall. Eisen kommt aufgrund seiner Reaktiofreudigkeit in der Natur aber fast nur in gebundener Form vor. Gewinnung Eisen ist nach Aluminium das zweit häufigste Metall in der Erdkruste. Die wigsten eisenhaltigen Gesteine (Erze) sind die Erze Magnetit Fe3O4 (bis 72 % Eisengehalt) und Hämatit Fe2O3 (bis 70 % Eisengehalt). Hämatit gehört zu der am häuigsten natürlh auftretenden Modiikation des Eisen-(I)-oxids. Es hat eine rote bis rötlhe Farbe. Neben diesen Erzen sind sowohl das Eisenerz Siderit FeCO3 als auch das Eisenerz Pyrit FeS2 als Ausgangsmaterial für den Hochofenprozess von Bedeutung. Fotos: Thinkstockphotos.com Das chemische Symbol für Eisen lautet Fe. Eisenerz kann sowohl im Untertagebau als auch oberirdisch im Tagebau abgebaut werden. Die Hauptlagerstätten für den oberirdischen Abbau von Eisenerz beinden sh in Bsilien, China, Ost-Europa (u. a. Ukine), Kanada und im Westen von Austlien. Das abgebaute Eisenerz (Eisengehalt mehr als 60 %) wird direkt am Abbauort von unerwücen Beimengungen der sogenannten Gangart getrennt. Die groben Gesteibrocken werden mithilfe von Brechern und Mühlen zerkleinert. Das feine Eisenerz wird unter hohen Tempeturen zu kleineren Brocken verbacken. Diesen Prozess nennt man sintern. 1. Lest euch die Infotexte aufmerksam durch. Erstellt zusammen eine Mindmap auf einem Plakat rund um das Thema Eisen. Ihr könnt auch eigene, passende Bilder oder Skizzen dazu zehnen. 2. Präsentiert in einem kurzen rtg eure Ergebnisse euren Mitschülern. Helft euch gegeeitig, eventuell fehlende Informationen zu ergänzen.
4 13 von 42 Hier ge es ganz schön heiß her Gewinnung von Roheisen M3 Mit dem gewonnenen Eisenerz kann der Mech zunächst noch n viel anfangen. Die Erzeugung von Roheisen in einem Hochofen ist sehr aufwendig und benötigt sehr viel Energie. Findet nun heus, wie Roheisen hergestellt wird und warum es zur weiteren Verbeitung zu Stahl veredelt wird. Der Hochofenprozess Der Hochofen einer Eisenhütte (also der eisenproduzierenden Anlage) ist eine Kotruktion eines bis zu 75 m hohen Turmes, der einem Schortein oder Kamin ähnelt. Unten ist er etwas breiter als oben. Die chemischen Reaktionen im Hochofen Im Hochofenprozess ge es darum, dem oxidischen Eisenerz (Magnetit, Hämatit) den Sauerstoff zu entziehen. Diesen Entzug von Sauerstoff bezehnet man als Reduktion. Der Hochofen wird abwechselnd mit dem abgebauten Eisenerz und Koks (kohletoffhaltiger Brentoff) befüllt. Je nachdem, welche Erzbeimengungen mit dem Eisenerz in den Hochofen gelangen, setzt man Kalkstein, Dolomit, Feldspat oder Schsilate zu (auch als Zuschlag bezehnet). Dieser Zuschlag bildet mit den Erzbeimengungen (auch Gangart genannt) le schmelzbare Verbindungen, die Schlacke. Dieses Gemisch (auch Möller genannt) wird achließend stark erhitzt. Dazu wird von unten mithilfe von sogenannten Winderhitzern heiße Luft mit ca C eingeblasen. Dabei verbrennt der Kohletoff aus dem Koks an der Einblasöffnung mit dem eitrömenden Sauerstoff zunächst zu CO2. Dabei entstehen Tempeturen bis zu C. Das CO2 reagiert sofort mit dem heißen Koks weiter zu Kohlenmonoxid CO. 1. Kohletoff Sauerstoff Kohletoffdioxid C O2 CO2 2. Kohletoffdioxid Kohletoff CO2 C HR = 393 kj/mol Kohletoffmonoxid 2 CO HR = 173 kj/mol Da diese zweite Reaktion Energie verbuc ( HR = 173 kj/mol), kühlt sh das Gas ganz le ab. Die Tempeturen im unteren Teil des Hochofe liegen nun bei ca C. Dieses steigt im Hochofen auf und reduziert dabei stufenweise die darüberliegenden Erzschen zu Eisen und CO2. Im unteren Teil des Hochofe ist das Eisen bereits teilreduziert und liegt in Form von Eisen-()oxid FeO (Wüstit genannt) vor. Dieses wird zu Fe und CO2 reduziert. 3. Eisenoxid Kohletoffmonoxid Eisen FeO CO Fe Kohletoffdioxid CO2 HR = 17 kj/mol
5 15 von 42 Was geschie im Hochofen? m Eisenerz zum Roheisen M3
6 23 von 42 Was hilft gegen Rost? Spürnasen aufgepasst! Ihr habt heusgefunden, dass Eisen, wenn es n durch spezielle Beschungen oder Verfahren geschützt wird, relativ schnell rostet. Aber was tun, wenn der Rost nun einmal da ist? Gibt es vielle ganz einfache Mittel, um ihn wieder loszuwerden? Aufgabe Führt zu zweit den folgenden Versuch durch. Notiert euch dabei sorgfältig eure Beobacungen! Das benötigt ihr 2 rostige Stücke Eisen (Nägel oder Blech) 2 Bechergläser à 100 ml Gummihandschuhe Messzylinder 50 ml 10 %ige Phosphorsäure 50 ml Cola Schutzbrille Laborkittel So ge ihr vor 1. Füllt ein Becherglas zur Hälfte mit 10%iger Phosphorsäure, ein weiteres mit 50 ml handelsüblher Cola. 2. Legt vorsig ein rostiges Stück Eisen in das Becherglas mit Phosphorsäure und eines in das zweite Becherglas mit der Cola. Acung: Phosphorsäure ist ätzend! Arbeitet vorsig und mit Schutzbrille, Laborkittel und Handschuhen! 3. Wartet circa 30 Minuten und holt dann die Teile vorsig mit einer Zange wieder heus. Spült die Teile mit Wasser ab. Schreibt eure Beobacungen auf! rostiges Stück Eisen in Cola rostiges Stück Eisen in Phosphorsäure 1. Informiert euch in eurem Chemiebuch über folgende Begriffe und schreibt euch kurze Deinitionen dazu auf: Oxidation; Reduktion; Redoxreaktion; Oxidatiozahl 2. Vervollständige die Reaktioglehung bei der Umwandlung von Rost, also Eisen-(I)-oxidhydroxid, bzw. FeO(OH), mithilfe von Phosphorsäure H3PO4 zu Eisenphosphat und Wasser. Schreibt die zugehörigen Oxidatiozahlen über die Glehung. FeO(OH) H3PO4 M8
7 30 von 42 M 12 Töpfe, Pfannen und Co. Metallen wird s oft ganz schön heiß! Metalle haben viele nützlhe Eigechaften. Eine davon nutzen wir beinahe täglh. Schon die alten Römer haben Kessel aus ganz bestimmten Metallen zum Kochen und Schmoren verwendet. Warum waren hierfür einige aber besser geeignet als andere? Führt folgenden Versuch in Vierergruppen durch. Das benötigt ihr 1 Stövchen Strehhölzer Wachsplättchen, Teel Stoppuhr So ge ihr vor Metallstreifen aus Eisen, Kupfer, Aluminium, Zink, Bronze Tiegelzange bzw. Wärmeschutzhandschuhe Feuerfeste Unterlage, beispielsweise Porzellanteller 1. Nehmt die Metallstreifen und klebt jeweils am Ende eines jeden Metallstreife ein Wachsplättchen dauf. Stövchen 2. Haltet eine Stoppuhr bereit. Zündet das Teel im Stövchen an und legt vorsig den ersten Metallstreifen über die Teellamme. Acet dabei dauf, dass sh das Wachsplättchen am Ende des Metallstreife beindet. Sobald der Metallstreifen über dem Teel liegt, startet eure Stoppuhr. Metallstreifen Zeit Eisen Kupfer Teel Wachsplättchen Aluminium Metallstreifen Zink Bronze 3. Ermittelt mithilfe eurer Stoppuhr, wie lange das Wachsplättchen benötigt, um vollständig zu schmelzen. Notiert die Zeit. 4. Entfernt den Metallstreifen vorsig mithilfe der Tiegelzange vom Stövchen und legt ihn auf die feuerfeste Unterlage. Hinweis: Acet dabei dauf, dass kein lüssiges Wachs verläuft. Sherheitshalber könnt ihr das Teel ausblasen und warten, bis der Streifen abgekühlt und das Wachs fest geworden ist! 1. Teste mithilfe der unterschiedlhen Metallstreifen, beispielsweise Eisen, Kupfer, Aluminium, Zink und Bronze, welches Material am besten die Wärme leitet. Ordne deine Metallproben entsprechend. Das Material mit der besten Wärmeleitfähigkeit ste an erster Stelle usw. 2. Überlege anhand deiner Beobacungen, welches Material du für die Herstellung von Heizspilen verwenden würdest. Begründe deine Antwort.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Vom Handy bis zum Mountainbike - Metalle in unserem Alltag im Fokus
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Vom Handy bis zum Mountainbike - Metalle in unserem Alltag im Fokus Das komplette Material finden Sie hier: School-Scout.de 1 von
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Vom Handy bis zum Mountainbike - Metalle in unserem Alltag im Fokus Das komplette Material finden Sie hier: School-Scout.de 1 von
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung Chemische Bindungen in Metallen, Elektronengasmodell, elektronische Bänder, Bandstrukturmodell, Metalle, Halbleiter, Isolatoren, Bandlücke,
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung Chemische Bindungen in Metallen, Elektronengasmodell, elektronische Bänder, Bandstrukturmodell, Metalle, Halbleiter, Isolatoren, Bandlücke,
Luftdruck und Wind Wetterelemente experimentell erkunden
 1 von 34 Luftdruck und Wind Wetterelemente experimentell erkunden Dr. Norma Kreuzberger, Lohmar Das Wetter begegnet den Schülern jeden Tag vor der eigenen Haustüre, aber auch bei Wettervorhersagen und
1 von 34 Luftdruck und Wind Wetterelemente experimentell erkunden Dr. Norma Kreuzberger, Lohmar Das Wetter begegnet den Schülern jeden Tag vor der eigenen Haustüre, aber auch bei Wettervorhersagen und
Wiederholungsfragen Metall 9
 Wiederholungsfragen Metall 9 Die richtige Beantwortung der Wiederholungsfragen aus dem Stoff der 9. Jahrgangsstufe ist Voraussetzung für die Vorbereitung auf die Abschlussprüfung. Dazu muss auch das Arbeitsheft
Wiederholungsfragen Metall 9 Die richtige Beantwortung der Wiederholungsfragen aus dem Stoff der 9. Jahrgangsstufe ist Voraussetzung für die Vorbereitung auf die Abschlussprüfung. Dazu muss auch das Arbeitsheft
Vom Erz zum Stahl. Von Andre Hähnel & Tobias Bomkamp
 Vom Erz zum Stahl Von Andre Hähnel & Tobias Bomkamp Inhaltsverzeichnis Das Element Eisen Was ist eigentlich Erz? Herstellung von Roheisen Hochofenprozess Herstellung von Stahl Veredelung zum Stahl Eigenschaften
Vom Erz zum Stahl Von Andre Hähnel & Tobias Bomkamp Inhaltsverzeichnis Das Element Eisen Was ist eigentlich Erz? Herstellung von Roheisen Hochofenprozess Herstellung von Stahl Veredelung zum Stahl Eigenschaften
Stoffe und ihre Eigenschaften 14. Metalle in unserem Alltag (Kl. 8/9) Vom Handy bis zum Mountainbike Metalle in unserem Alltag
 Stoffe und ihre Eigenschaften 14. Metalle in unserem Alltag (Kl. 8/9) 1 von 26 Vom Handy bis zum Mountainbike Metalle in unserem Alltag Ein Beitrag von Günther Lohmer, Leverkusen In unserem Alltag kommen
Stoffe und ihre Eigenschaften 14. Metalle in unserem Alltag (Kl. 8/9) 1 von 26 Vom Handy bis zum Mountainbike Metalle in unserem Alltag Ein Beitrag von Günther Lohmer, Leverkusen In unserem Alltag kommen
KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor
 1 KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "METALLE" 1. Einleitung...03 2. Reaktionen von Metallen... 05 3. Gewinnung von Metallen... 07 4. Domino: Eigenschaften der
1 KSO METALLE (SEKP) Skript Metalle (SekP) V1.0 04/15 Bor 2 INHALTSVERZEICHNIS "METALLE" 1. Einleitung...03 2. Reaktionen von Metallen... 05 3. Gewinnung von Metallen... 07 4. Domino: Eigenschaften der
Ohne Licht geht nichts! Wir erforschen die Vorgänge der Fotosynthese
 1 von 6 Ohne L ge! Wir erforschen die rgänge der Fotosynthese t h c i s n a r o V Planzen buchen wie wir Mechen Energie, um zum Beispiel zu wachsen. Den Schülern ist in der Regel bekannt, dass die Planzen
1 von 6 Ohne L ge! Wir erforschen die rgänge der Fotosynthese t h c i s n a r o V Planzen buchen wie wir Mechen Energie, um zum Beispiel zu wachsen. Den Schülern ist in der Regel bekannt, dass die Planzen
Stoffe und ihre Eigenschaften 12. Vom Erz zum Stahl (Kl. 8/9) Vom Erz zum Stahl ein Lernbuffet zum Hochofenprozess
 Stoffe und ihre Eigenschaften 12. Vom Erz zum Stahl (Kl. 8/9) 1 von 26 Vom Erz zum Stahl ein Lernbuffet zum Hochofenprozess Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Wolfgang Zettlmeier,
Stoffe und ihre Eigenschaften 12. Vom Erz zum Stahl (Kl. 8/9) 1 von 26 Vom Erz zum Stahl ein Lernbuffet zum Hochofenprozess Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Wolfgang Zettlmeier,
Wer spannt wem den Sauerstoff aus? Metalloxide
 1 von 24 Wer spannt wem den Sauerstoff aus? Metalloxide Ein Beitrag von Petra Frank, Tobias Frank und Dr. Hans-Peter Haseloff, Esslingen Mit Illustrationen von Julia Lenzmann, Stuttgart Foto: Colourbox
1 von 24 Wer spannt wem den Sauerstoff aus? Metalloxide Ein Beitrag von Petra Frank, Tobias Frank und Dr. Hans-Peter Haseloff, Esslingen Mit Illustrationen von Julia Lenzmann, Stuttgart Foto: Colourbox
Kupfersteckbrief 06 AB1 MS
 Um einen Stoff und seine Eigenschaften genauer beschreiben zu können, ist es wichtig verschiedene Versuche durchzuführen und genau zu beobachten. Aufgabe: Erstelle einen Steckbrief für, indem du verschiedene
Um einen Stoff und seine Eigenschaften genauer beschreiben zu können, ist es wichtig verschiedene Versuche durchzuführen und genau zu beobachten. Aufgabe: Erstelle einen Steckbrief für, indem du verschiedene
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie)
 Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Abschlussklausur Allgemeine und Anorganische Chemie Teil 2 (Geologie, Geophysik und Mineralogie) Teilnehmer/in:... Matrikel-Nr.:... - 1. Sie sollen aus NaCl und Wasser 500 ml einer Lösung herstellen, die
Vom Eisenerz zum Stahl
 Jens Wolters, Maxim Zarske Vom Eisenerz zum Stahl Was ist das Eisen? Geschichtliches Zahlen Physikalischen Eigenschaften Erze und Vorkommen Gewinnung von Roheisen Verfahren zur Stahlerzeugung 1. Definition:
Jens Wolters, Maxim Zarske Vom Eisenerz zum Stahl Was ist das Eisen? Geschichtliches Zahlen Physikalischen Eigenschaften Erze und Vorkommen Gewinnung von Roheisen Verfahren zur Stahlerzeugung 1. Definition:
Rost und Rostschutz. Definitionen [1, 2] Versuch 1: Rostvorgang [3, 4]
![Rost und Rostschutz. Definitionen [1, 2] Versuch 1: Rostvorgang [3, 4] Rost und Rostschutz. Definitionen [1, 2] Versuch 1: Rostvorgang [3, 4]](/thumbs/55/37862002.jpg) Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2011 29.06.2011 Dozentin: Dr. M. Andratschke Referenten: Graßold, Birgit
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Sommersemester 2011 29.06.2011 Dozentin: Dr. M. Andratschke Referenten: Graßold, Birgit
Eisenerz Kokskohle Flüssiges Roheisen C Hochofen
 Stahl Ist Stahl ein junger Werkstoff? Das zur Herstellung von Stahl erforderliche Eisen wird in Europa seit 1.700 vor J.C. hergestellt. Von Anfang an wurden auch kleine Mengen Stahl hergestellt, d.h. mit
Stahl Ist Stahl ein junger Werkstoff? Das zur Herstellung von Stahl erforderliche Eisen wird in Europa seit 1.700 vor J.C. hergestellt. Von Anfang an wurden auch kleine Mengen Stahl hergestellt, d.h. mit
Chemie Fragenkatalog Jahrgang 8
 Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Chemie Fragenkatalog Jahrgang 8 - Stoffe und ihre Eigenschaften - Stoffgemische und Trennverfahren - Vom Aufbau der Stoffe - Die chemische Reaktion - Luft und Verbrennung - Gewinnung von Metallen Redoxreaktionen
Schulversuchspraktikum. Sommersemester Klassenstufen 7 & 8. Vom Erz zum Metall. (oxidische und sulfidische Erze)
 Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Vom Erz zum Metall (oxidische und sulfidische Erze) Auf einen Blick: In der 7./8. Klasse wird noch statt von Redoxreaktionen von Sauerstoffübertragungsreaktionen
Schulversuchspraktikum Sommersemester 2014 Klassenstufen 7 & 8 Vom Erz zum Metall (oxidische und sulfidische Erze) Auf einen Blick: In der 7./8. Klasse wird noch statt von Redoxreaktionen von Sauerstoffübertragungsreaktionen
Mikrokosmos Vorstellungen von der Welt des Kleinen
 II Stoffe im Alltag Beitrag 2 Mikrokosmos (Klassen 5 7) 1 von 32 Mikrokosmos Vorstellungen von der Welt des Kleinen Ariane Pieta, Leonberg Unterschiedliche Alltagsphänomene können durch einfache Experimente
II Stoffe im Alltag Beitrag 2 Mikrokosmos (Klassen 5 7) 1 von 32 Mikrokosmos Vorstellungen von der Welt des Kleinen Ariane Pieta, Leonberg Unterschiedliche Alltagsphänomene können durch einfache Experimente
Eine saubere Sache welche Inhaltsstoffe Waschmittel enthalten und wie sie funktionieren
 1 von 40 Eine saubere Sache welche Inhaltsstoffe Waschmittel enthalten und wie sie funktionieren t h c i s n a r o V Jeden Tag stehen wir vor uerem Kleiderschnk und überlegen, was wir anziehen sollen.
1 von 40 Eine saubere Sache welche Inhaltsstoffe Waschmittel enthalten und wie sie funktionieren t h c i s n a r o V Jeden Tag stehen wir vor uerem Kleiderschnk und überlegen, was wir anziehen sollen.
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Vom Handy bis zum Mountainbike (PDF-Datei)
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Vom Handy bis zum Mountainbike (PDF-Datei) Das komplette Material finden Sie hier: School-Scout.de 2 von 26 14. Metalle in unserem
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Vom Handy bis zum Mountainbike (PDF-Datei) Das komplette Material finden Sie hier: School-Scout.de 2 von 26 14. Metalle in unserem
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Wer spannt wem den Sauerstoff aus? Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Wer spannt wem den Sauerstoff aus? Das komplette Material finden Sie hier: School-Scout.de 2 von 24 17. Metalloxide (Kl. 8/9) Stoffe
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Wer spannt wem den Sauerstoff aus? Das komplette Material finden Sie hier: School-Scout.de 2 von 24 17. Metalloxide (Kl. 8/9) Stoffe
Herstellen von Stählen
 Herstellen von Stählen 1. Historische Verfahren 2. Roheisenerzeugung 3. Rohstahlerzeugung 4. 1 Stahlerzeugung Ziel: Herstellen von Stahl bestimmter chemischer Zusammensetzung, möglichst homogen und weitestgehend
Herstellen von Stählen 1. Historische Verfahren 2. Roheisenerzeugung 3. Rohstahlerzeugung 4. 1 Stahlerzeugung Ziel: Herstellen von Stahl bestimmter chemischer Zusammensetzung, möglichst homogen und weitestgehend
Name, Vorname: Klasse: Schule: Seite 1 von 7
 Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Chemische Reaktionen zur Metallherstellung Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Chemische Reaktionen zur Metallherstellung Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Kopiervorlage 1: Eisen und Aluminium
 Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmenge
Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmenge
2. Roheisenerzeugung. 2.1. Rohstoffe und Erzaufbereitung. 2.1.1. Eisenerze und Erzvorkommen. Eisenerz. 2.1.2. Erzaufbereitung
 2. Roheisenerzeugung 2.1. Rohstoffe und Erzaufbereitung 2.1.1. Eisenerze und Erzvorkommen Eisen kommt in der Erdrinde nicht als reines Element vor, sondern nur in chemischen Verbindungen, meist als Oxid,
2. Roheisenerzeugung 2.1. Rohstoffe und Erzaufbereitung 2.1.1. Eisenerze und Erzvorkommen Eisen kommt in der Erdrinde nicht als reines Element vor, sondern nur in chemischen Verbindungen, meist als Oxid,
Teil der Erdkruste die Erdalkalimetalle. Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von Katja Rau, Berglen VORANSICHT
 1 von 26 Teil der Erdkruste die Erdalkalimetalle Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von Katja Rau, Berglen Ob im Blitzlicht, im Feuerwerk, als Kreide oder als Mörtel Erdalkalimetalle
1 von 26 Teil der Erdkruste die Erdalkalimetalle Ein Beitrag von Günther Lohmer, Leverkusen Mit Illustrationen von Katja Rau, Berglen Ob im Blitzlicht, im Feuerwerk, als Kreide oder als Mörtel Erdalkalimetalle
Standortbestimmung / Äquivalenzprüfung. Chemie. Mittwoch, 13. April 2016, Uhr
 Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Name, Vorname: Klasse: Schule: Seite 1 von 7
 Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Roheisenherstellung im Hochofen Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Name, Vorname: Klasse: Schule: Seite 1 von 7 Aufgabe 1: Roheisenherstellung im Hochofen Für die Herstellung von Roheisen im Hochofen werden die Ausgangsstoffe Eisenerz (Fe 2 O 3 ), Kohle (Kohlenstoff)
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Aufgabe 1 * Mischung von Flüssigkeiten 3 Gruppen mischen Spiritus mit Wasser. 3 Gruppen mischen jeweils Erbsen mit Grieß. Füllt
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Aufgabe 1 * Mischung von Flüssigkeiten 3 Gruppen mischen Spiritus mit Wasser. 3 Gruppen mischen jeweils Erbsen mit Grieß. Füllt
Kohlenstoffdioxid (Teil2)
 Kohlenstoffdioxid (Teil2) Wo Schornsteine qualmen, ist meist auch Kohlenstoffdioxid im Spiel. Jedes Jahr werden unglaubliche Mengen des farblosen Gases ausgestoßen mit Konsequenzen für uns alle! Wie entsteht
Kohlenstoffdioxid (Teil2) Wo Schornsteine qualmen, ist meist auch Kohlenstoffdioxid im Spiel. Jedes Jahr werden unglaubliche Mengen des farblosen Gases ausgestoßen mit Konsequenzen für uns alle! Wie entsteht
VORANSICHT. Kakao, Kartoffel & Co. die wichtigsten Nutzpflanzen im Fokus. Das Wichtigste auf einen Blick
 II Planzen Beitrag 7 Nutzplanzen im Fokus (Klasse 5/6) 1 von 24 Kakao, Kartoffel & Co. die wichtigsten Nutzpflanzen im Fokus Ein Beitrag von Günther Lohmer, Leverkusen Pflanzen waren und sind ständige
II Planzen Beitrag 7 Nutzplanzen im Fokus (Klasse 5/6) 1 von 24 Kakao, Kartoffel & Co. die wichtigsten Nutzpflanzen im Fokus Ein Beitrag von Günther Lohmer, Leverkusen Pflanzen waren und sind ständige
Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann.
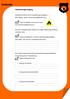 Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Verbrennungsvorgang Überlege dir welche drei Voraussetzungen gegeben sein müssen, damit Verbrennung stattfinden kann. Trage die Begriffe in die leeren Felder des Verbrennungsdreiecks ein. Die drei Voraussetzungen
Kohlensäure ohne sie wäre unser Alltag
 1 von 26 Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Dr. Wolfgang Zettlmeier, Barbing Foto: Thinkstock/Stockbyte
1 von 26 Von Soda-Streamern, Backpulver und Kalk Kohlensäure und ihre Salze Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Dr. Wolfgang Zettlmeier, Barbing Foto: Thinkstock/Stockbyte
Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus:
 Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmasse
Kopiervorlage 1: Eisen und Aluminium 1. Suche aus dem Schulbuch folgende Eigenschaften der beiden Metalle heraus: Eisen Aluminium Dichte Härte Schmelzpunkt Magnetisierbarkeit 2. a) Berechne die Eisenmasse
von Miriam Richter, Marc Sören Homeyer, Brigitte Duvinage
 Experimentiervorschriften zum Beitrag Wärmepflaster, im Chemieunterricht nachgebaut von Miriam Richter, Marc Sören Homeyer, Brigitte Duvinage 1 Experimente zur Identifizierung der Inhaltsstoffe Aus didaktisch-methodischen
Experimentiervorschriften zum Beitrag Wärmepflaster, im Chemieunterricht nachgebaut von Miriam Richter, Marc Sören Homeyer, Brigitte Duvinage 1 Experimente zur Identifizierung der Inhaltsstoffe Aus didaktisch-methodischen
Wie Metalle reagieren ein Mystery. Vanessa Engelhard, LIS Bremen, und Silvija Markic, Universität Bremen
 II 1 von 32 Wie Metalle reagieren ein Mystery Vanessa Engelhard, LIS Bremen, und Silvija Markic, Universität Bremen Foto: Thinkstock/iStock Reduktion und Oxidation sind zwei der Reaktionen, ohne die man
II 1 von 32 Wie Metalle reagieren ein Mystery Vanessa Engelhard, LIS Bremen, und Silvija Markic, Universität Bremen Foto: Thinkstock/iStock Reduktion und Oxidation sind zwei der Reaktionen, ohne die man
Grundkenntnisse der Chemie und der Physik. Was ihr hier findet
 Grundkenntnisse der hemie und der Physik P Was ihr hier findet Wissensgebiete der hemie und der Physik Formeln Elemente Metalle Kohlenstoff Analyse Synthese Basen Laugen Salze Atome Moleküle Akustik Optik
Grundkenntnisse der hemie und der Physik P Was ihr hier findet Wissensgebiete der hemie und der Physik Formeln Elemente Metalle Kohlenstoff Analyse Synthese Basen Laugen Salze Atome Moleküle Akustik Optik
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
CHEMIE WIEDERHOLUNG: KAPITEL 5 REAKTIONEN DER ANORGANISCHEN CHEMIE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Einführung Brennendes Magnesiumband reagiert mit Sauerstoff
Erwartete Kompetenzen. Kompetenzbereich Erkenntnisgewinnung Die Schülerinnen und Schüler E1 E2 E3 E4 E5 E6 E7 E8 E9 E10 E11 E12 E13 E14 E15 E16 E17
 Stoffverteilungsplan Kerncurriculum für die Oberschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1 Lehrer:
Stoffverteilungsplan Kerncurriculum für die Oberschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1 Lehrer:
Geheimnisvolle Kräfte der Magnetismus
 1 von 36 Geheimnisvolle Kräfte der Magnetismus Claudia Drescher, Waibstadt Schüler kennen sherlh schon einiges aus ihrem alltäglhen Umgang mit Magneten (Spielzeug, Magnetpinnwand, Kompass etc.). Allerdings
1 von 36 Geheimnisvolle Kräfte der Magnetismus Claudia Drescher, Waibstadt Schüler kennen sherlh schon einiges aus ihrem alltäglhen Umgang mit Magneten (Spielzeug, Magnetpinnwand, Kompass etc.). Allerdings
Eisen. Vorkommen. Eisen Stahl
 88 XXII. Eisen Stahl Eisen Vorkommen. Das Eisen ist am Aufbau der Erdrinde zu 4,7 % beteiligt. Aus der Dichte der Erde schließt man auf einen hohen Eisengehalt des Erdkerns (Ni-Fe-Kern). Gediegenes (reines)
88 XXII. Eisen Stahl Eisen Vorkommen. Das Eisen ist am Aufbau der Erdrinde zu 4,7 % beteiligt. Aus der Dichte der Erde schließt man auf einen hohen Eisengehalt des Erdkerns (Ni-Fe-Kern). Gediegenes (reines)
Film der Einheit Metalle
 Film der Einheit Metalle Edle und unedle Metalle Produktionszahlen Metalle im Periodensystem der Elemente Herstellung einiger Metalle (Eisen, Aluminium, Kupfer) Kristallgitter und Bindungen in Metallen
Film der Einheit Metalle Edle und unedle Metalle Produktionszahlen Metalle im Periodensystem der Elemente Herstellung einiger Metalle (Eisen, Aluminium, Kupfer) Kristallgitter und Bindungen in Metallen
Mögliche Punktzahl: 100 Gesamtpunkte aus Teil 1 und 2: Erreichte Punktzahl: Prozentsatz aus Teil 1 und 2:
 Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch. Thienel Bachelorprüfung Prüfungsfach: Geologie, Werkstoffe und Bauchemie am: 28.03.2014
Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch. Thienel Bachelorprüfung Prüfungsfach: Geologie, Werkstoffe und Bauchemie am: 28.03.2014
Redoxreaktionen. chemische Reaktion von Kupfer(II)-oxid mit Kohlenstoff es entstehen Kupfer und Kohlenstoffdioxid [exotherm]
![Redoxreaktionen. chemische Reaktion von Kupfer(II)-oxid mit Kohlenstoff es entstehen Kupfer und Kohlenstoffdioxid [exotherm] Redoxreaktionen. chemische Reaktion von Kupfer(II)-oxid mit Kohlenstoff es entstehen Kupfer und Kohlenstoffdioxid [exotherm]](/thumbs/33/16107015.jpg) eqiooki.de Redoxreaktionen [Realschule] Seite 1 von 9 Redoxreaktionen Ob bei der Herstellung von Roheisen und Stahl, bei der Erzeugung von Aluminium und anderer Metalle aus entsprechenden Erzen, bei elektrochemischen
eqiooki.de Redoxreaktionen [Realschule] Seite 1 von 9 Redoxreaktionen Ob bei der Herstellung von Roheisen und Stahl, bei der Erzeugung von Aluminium und anderer Metalle aus entsprechenden Erzen, bei elektrochemischen
Manchmal muss man etwas nachhelfen Energieumsatz bei chemischen Reaktionen
 1 von 26 Manchmal muss man etwas nachhelfen Energieumsatz bei chemischen Reaktionen Ein Beitrag von Dr. Leena Bröll, Gundelingen Mit Illustrationen von Dr. Leena Bröll, Gundelingen, und Katja Rau, Berglen
1 von 26 Manchmal muss man etwas nachhelfen Energieumsatz bei chemischen Reaktionen Ein Beitrag von Dr. Leena Bröll, Gundelingen Mit Illustrationen von Dr. Leena Bröll, Gundelingen, und Katja Rau, Berglen
Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte Packung, Raumausfüllung, Ionenstrukturen - abgeleitet von Ionendichtestpackungen,
 Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Wiederholung der letzten Vorlesungsstunde: Thema: Metallbindung / Salzstrukturen Der metallische Zustand, Dichtestpackung von Kugeln, hexagonal-, kubischdichte Packung, Oktaeder-, Tetraederlücken, kubisch-innenzentrierte
Kohlenstoffdioxid (Teil2): LÖSUNGEN
 Kohlenstoffdioxid (Teil2): LÖSUNGEN Wo Schornsteine qualmen, ist meist auch Kohlenstoffdioxid im Spiel. Jedes Jahr werden unglaubliche Mengen des farblosen Gases ausgestoßen mit Konsequenzen für uns alle!
Kohlenstoffdioxid (Teil2): LÖSUNGEN Wo Schornsteine qualmen, ist meist auch Kohlenstoffdioxid im Spiel. Jedes Jahr werden unglaubliche Mengen des farblosen Gases ausgestoßen mit Konsequenzen für uns alle!
Kapitel 2 Repetitionen Chemie und Werkstoffkunde. Thema 3 Gewinnung und Verarbeitung der Stoffe Eisenwerkstoffe
 BEARBEITUNGSTECHNIK REPETITONEN LÖSUNGSSATZ Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 3 Gewinnung und Verarbeitung der Stoffe Eisenwerkstoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur
BEARBEITUNGSTECHNIK REPETITONEN LÖSUNGSSATZ Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 3 Gewinnung und Verarbeitung der Stoffe Eisenwerkstoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur
Das Periodensystem der Elemente eine Einführung
 1 von 24 Das Periodensystem der Elemente eine Einführung Ein Beitrag von Dr. Nicole Kunze, Kirchzarten, und Dr. Leena Bröll, Gundelingen Mit Illustrationen von Julia Lenzmann, Stuttgart Foto: Thinkstock/iStock
1 von 24 Das Periodensystem der Elemente eine Einführung Ein Beitrag von Dr. Nicole Kunze, Kirchzarten, und Dr. Leena Bröll, Gundelingen Mit Illustrationen von Julia Lenzmann, Stuttgart Foto: Thinkstock/iStock
Löschversuche mit Wasser sowie Feuchtigkeit führen zur Spaltung von Wasser und erzeugen Knallgas
 Thermit / Blatt 1 Einleitung Gegen Ende des 19. Jahrhunderts entdeckte Hans Goldschmidt in Essen die technische Gewinnung von Schwermetallen aus ihren Oxiden durch die Oxidation von Aluminium. Thermit
Thermit / Blatt 1 Einleitung Gegen Ende des 19. Jahrhunderts entdeckte Hans Goldschmidt in Essen die technische Gewinnung von Schwermetallen aus ihren Oxiden durch die Oxidation von Aluminium. Thermit
Versuch 1. Baue ein Thermometer. Nun erwärme das Wasser im Erlenmeyerkolben auf einem Stövchen. Was geschieht?
 Versuch 1 Nun erwärme das Wasser im Erlenmeyerkolben auf einem Stövchen. Was geschieht? Baue ein Thermometer Fülle den Erlenmeyerkolben mit Wasser und verschließe ihn mit dem Stopfen. Im Stopfen befindet
Versuch 1 Nun erwärme das Wasser im Erlenmeyerkolben auf einem Stövchen. Was geschieht? Baue ein Thermometer Fülle den Erlenmeyerkolben mit Wasser und verschließe ihn mit dem Stopfen. Im Stopfen befindet
350³ Material Ausgangstemperatur in o C Temperatur nach 3 min in o C
 350³ - 1 - Löffel in heißem Wasser Achtung! Sei an dieser Station besonders vorsichtig, damit du dich bzw. deine Mitschüler mit dem heißen Wasser nicht verbrühst! 1. Benenne die Materialien der verwendeten
350³ - 1 - Löffel in heißem Wasser Achtung! Sei an dieser Station besonders vorsichtig, damit du dich bzw. deine Mitschüler mit dem heißen Wasser nicht verbrühst! 1. Benenne die Materialien der verwendeten
Elektrochemie Chemie der Metalle
 Elektrochemie Chemie der Metalle Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Bauchemische Grundlagen Elektrochemie Redoxreaktionen Oxidation Reduktion
Elektrochemie Chemie der Metalle Thomas A. BIER Institut für Keramik, Glas- und Baustofftechnik, Leipziger Straße 28, 09596 Freiberg, Bauchemische Grundlagen Elektrochemie Redoxreaktionen Oxidation Reduktion
FWU Schule und Unterricht. FWU-Klassiker Moderne Eisen- und Stahlgewinnung. FWU das Medieninstitut der Länder
 FWU Schule und Unterricht DVD 46 10382 15 min, Farbe FWU-Klassiker Moderne Eisen- und Stahlgewinnung FWU das Medieninstitut der Länder 00 Lernziele nach Lehrplänen und Schulbüchern Einblick erhalten in
FWU Schule und Unterricht DVD 46 10382 15 min, Farbe FWU-Klassiker Moderne Eisen- und Stahlgewinnung FWU das Medieninstitut der Länder 00 Lernziele nach Lehrplänen und Schulbüchern Einblick erhalten in
Vergleich von Chemie heute Teilband 1 zu den Basiskonzepten des Kerncurriculums in Niedersachsen
 934.280 Vergleich von Chemie heute zu den Basiskonzepten des Kerncurriculums in Niedersachsen Kennzeichen chem. 61 Chemie eine Naturwissenschaft 7 Was ist Chemie? 10 Methode: Sicher experimentieren 11
934.280 Vergleich von Chemie heute zu den Basiskonzepten des Kerncurriculums in Niedersachsen Kennzeichen chem. 61 Chemie eine Naturwissenschaft 7 Was ist Chemie? 10 Methode: Sicher experimentieren 11
Redoxreaktionen mit Metallen
 Redoxreaktionen mit Metallen Redoxreaktionen mit Metallen Seite 2 1. Versuch Ein chemisches Rätsel Geräte: Stativ, Muffe, Klemme, dünner Draht, fester Draht Chemikalien: Stahlwolle/Eisenwolle, Alkohol
Redoxreaktionen mit Metallen Redoxreaktionen mit Metallen Seite 2 1. Versuch Ein chemisches Rätsel Geräte: Stativ, Muffe, Klemme, dünner Draht, fester Draht Chemikalien: Stahlwolle/Eisenwolle, Alkohol
Posten 1a. Was gilt immer. bei einer Oxidation?
 Posten 1a Was gilt immer bei einer Oxidation? a) Es werden Elektronen aufgenommen. (=> Posten 3c) b) Es wird mit Sauerstoff reagiert. (=> Posten 6b) c) Sie kann alleine in einer Reaktions- 9k) gleichungg
Posten 1a Was gilt immer bei einer Oxidation? a) Es werden Elektronen aufgenommen. (=> Posten 3c) b) Es wird mit Sauerstoff reagiert. (=> Posten 6b) c) Sie kann alleine in einer Reaktions- 9k) gleichungg
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Stoffe im Alltag: Heavy Metals & Co. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stoffe im Alltag: Heavy Metals & Co. Das komplette finden Sie hier: School-Scout.de 1 von 36 Heavy Metal & Co. Metalle im Anfangsunterricht
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Stoffe im Alltag: Heavy Metals & Co. Das komplette finden Sie hier: School-Scout.de 1 von 36 Heavy Metal & Co. Metalle im Anfangsunterricht
Klausur Vertiefungsfach 1: Master
 I E H K Institut für Eisenhüttenkunde Rheinisch-Westfälische Technische Hochschule Aachen Klausur Vertiefungsfach 1: Master Eisen- und Stahlmetallurgie Univ.-Prof. Dr.-Ing. Dr. h.c. D. Senk 02.04.2013
I E H K Institut für Eisenhüttenkunde Rheinisch-Westfälische Technische Hochschule Aachen Klausur Vertiefungsfach 1: Master Eisen- und Stahlmetallurgie Univ.-Prof. Dr.-Ing. Dr. h.c. D. Senk 02.04.2013
Redoxreaktionen mit Metallen
 Redoxreaktionen mit Metallen Redoxreaktionen mit Metallen Seite 2 Vorbereitung für den 6. Versuch ( Wir lassen rosten ), da die Reaktion sehr langsam abläuft (=> Langzeitversuch)! 1. Ein chemisches Rätsel
Redoxreaktionen mit Metallen Redoxreaktionen mit Metallen Seite 2 Vorbereitung für den 6. Versuch ( Wir lassen rosten ), da die Reaktion sehr langsam abläuft (=> Langzeitversuch)! 1. Ein chemisches Rätsel
Berufssprache Deutsch für Jugendliche in Ausbildung
 Berufssprache Deutsch für Jugendliche in Ausbildung Grundlegende Informationen zur Unterrichtseinheit Beruf Industriemechanikerin/ Industriemechaniker Jahrgangsstufe 10 Lernfeld Thema Fertigen von Bauelementen
Berufssprache Deutsch für Jugendliche in Ausbildung Grundlegende Informationen zur Unterrichtseinheit Beruf Industriemechanikerin/ Industriemechaniker Jahrgangsstufe 10 Lernfeld Thema Fertigen von Bauelementen
Gefahrenstoffe. P: Zinknitrat-Hexahydrat-Lösung H: P:
 Redoxreihe Der Versuch führt den SuS vor Augen, dass sich nicht jedes Metall von jeder Metallsalz-Lösung oxidieren lässt, sondern dass es viel mehr eine experimentell zu ermittelnde Gesetzmäßigkeit dahintersteckt.
Redoxreihe Der Versuch führt den SuS vor Augen, dass sich nicht jedes Metall von jeder Metallsalz-Lösung oxidieren lässt, sondern dass es viel mehr eine experimentell zu ermittelnde Gesetzmäßigkeit dahintersteckt.
Rezepte: 1. Brause herstellen
 1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
1D Rezepte: 1. Brause herstellen zutaten ½ TL Natron 2 TL Zucker 1 TL Zitronensäure 200 ml Wasser zubereitung Natron, Zucker und Zitronensäure in das Glas geben. Das Wasser hinzufügen. aufgaben Vergleiche
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2000/2001 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2000/2001 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
1.) bei elektrochem. Reaktionen findet ein Ladungsaustausch zwischen metallischen Leitern und Elektrolytlösungen statt.
 1.) bei elektrochem. Reaktionen findet ein Ladungsaustausch zwischen metallischen Leitern und Elektrolytlösungen statt. - elektr. Leitungsvorgang ist an 2 Bedingungen geknüpft: [1] Vorhandensein frei beweglicher
1.) bei elektrochem. Reaktionen findet ein Ladungsaustausch zwischen metallischen Leitern und Elektrolytlösungen statt. - elektr. Leitungsvorgang ist an 2 Bedingungen geknüpft: [1] Vorhandensein frei beweglicher
Reaktionen von Metallen mit Sauerstoff und mit Luft
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 7 & 8 Reaktionen von Metallen mit Sauerstoff und mit Luft 1 Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Die
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie
 Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Aufgabe 1 * Mischung von Flüssigkeiten Eine Gruppe mischt Spiritus mit Wasser. Füllt dazu zunächst zwei Messzylinder mit je exakt
Physik-Übung * Jahrgangsstufe 8 * Modellvorstellung vom Aufbau der Materie Aufgabe 1 * Mischung von Flüssigkeiten Eine Gruppe mischt Spiritus mit Wasser. Füllt dazu zunächst zwei Messzylinder mit je exakt
Schulversuchspraktikum. Dörte Hartje. Sommersemester 2013. Klassenstufen 7 & 8. Vom Erz zum Metall
 Schulversuchspraktikum Dörte Hartje Sommersemester 2013 Klassenstufen 7 & 8 Vom Erz zum Metall Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Dieses Protokoll enthält drei Lehrer- und
Schulversuchspraktikum Dörte Hartje Sommersemester 2013 Klassenstufen 7 & 8 Vom Erz zum Metall Beschreibung des Themas und zugehörige Lernziele Auf einen Blick: Dieses Protokoll enthält drei Lehrer- und
DK Recycling und Roheisen GmbH, Werthauser Str. 182, Duisburg
 DK Recycling und Roheisen GmbH, Werthauser Str. 182, 47053 Duisburg Dr.-Ing. R.Deike, DEIKE iron metal services GmbH Dipl.-Ing. J.Dings, DK Recycling und Roheisen GmbH Der DK Prozess Das Recycling eisenhaltiger
DK Recycling und Roheisen GmbH, Werthauser Str. 182, 47053 Duisburg Dr.-Ing. R.Deike, DEIKE iron metal services GmbH Dipl.-Ing. J.Dings, DK Recycling und Roheisen GmbH Der DK Prozess Das Recycling eisenhaltiger
Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt VORANSICHT
 V Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) 1 von 30 Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt Tobias Dunst, Kißlegg Welche Verbindung besteht zwischen dem mysteriösen
V Chemische Reaktionen 4. Redoxreaktionen Schritt für Schritt (Kl. 8/9) 1 von 30 Ein Geben und Nehmen Redoxreaktionen Schritt für Schritt Tobias Dunst, Kißlegg Welche Verbindung besteht zwischen dem mysteriösen
9. Schwefelsäure und ihre Salze (Kl. 9/10) Ein saurer Alleskönner Eigenschaften und Verwendung von Schwefelsäure und ihren Salzen
 1 von 28 Ein saurer Alleskönner Eigenschaften und Verwendung von und ihren Salzen Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Wolfgang Zettlmeier, Barbing Mit einer Jahresproduktion
1 von 28 Ein saurer Alleskönner Eigenschaften und Verwendung von und ihren Salzen Ein Beitrag von Sabine Stoermer, Oldenburg Mit Illustrationen von Wolfgang Zettlmeier, Barbing Mit einer Jahresproduktion
Didaktische FWU-DVD. Eisen und Stahl
 55 11145 Didaktische FWU-DVD Zur Bedienung Mit den Pfeiltasten der Fernbedienung (DVD-Player) oder der Maus (Computer) können Sie Menüpunkte und Buttons ansteuern und mit der OK-Taste bzw. Mausklick starten.
55 11145 Didaktische FWU-DVD Zur Bedienung Mit den Pfeiltasten der Fernbedienung (DVD-Player) oder der Maus (Computer) können Sie Menüpunkte und Buttons ansteuern und mit der OK-Taste bzw. Mausklick starten.
Warum korrodiert Eisen?
 Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Warum korrodiert Eisen? Korrodiertes Eisen bzw. Rost findet sich überall. An Brücken, Autos, an unseren Fahrrädern und an altem Werkzeug. Es richtet in Deutschland jährlich Schäden im Wert von 100 Millionen
Wir bauen ein Bimetallthermometer
 Unterrichtsfach/ Lehrplanbezug Physik Schulstufe 6 Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Bimetallstreifen, Bimetallthermometer Kompetenzen laut Kompetenzmodell Naturwissenschaften
Unterrichtsfach/ Lehrplanbezug Physik Schulstufe 6 Thema Fachliche Vorkenntnisse Fachliche Kompetenzen Sprachliche Kompetenzen Bimetallstreifen, Bimetallthermometer Kompetenzen laut Kompetenzmodell Naturwissenschaften
Weil die Werkzeug der Menschen aus Stein waren. Urgeschichte. Weshalb nennt man die Steinzeit, Steinzeit?
 Weshalb nennt man die Steinzeit, Steinzeit? Weil die Werkzeug der Menschen aus Stein waren. In welche Zeiten wird die eingeteilt? Die wird eingeteilt in...... die Altsteinzeit,... die Jungsteinzeit,...
Weshalb nennt man die Steinzeit, Steinzeit? Weil die Werkzeug der Menschen aus Stein waren. In welche Zeiten wird die eingeteilt? Die wird eingeteilt in...... die Altsteinzeit,... die Jungsteinzeit,...
Erwartete Kompetenzen
 Stoffverteilungsplan Kerncurriculum für die Oberschule/Realschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1
Stoffverteilungsplan Kerncurriculum für die Oberschule/Realschule in Niedersachsen (Schuljahrgänge 7/8) PRISMA Chemie Niedersachsen Differenzierende Ausgabe Band 7/8 Schule: Klettbuch ISBN 978-3-12-068537-1
Modulbeschreibung. Eisen- und Stahlerzeugung. Schularten: Fächer: Zielgruppen: Autor: Zeitumfang: Ca. sechs Stunden
 Modulbeschreibung Schularten: Fächer: Zielgruppen: Autor: Zeitumfang: Werkrealschule; Fächerverbund Welt-Zeit-Gesellschaft (WRS/HS); 9 (WRS/HS), Guido Hennrich Ca. sechs Stunden Stahl ist seit Beginn der
Modulbeschreibung Schularten: Fächer: Zielgruppen: Autor: Zeitumfang: Werkrealschule; Fächerverbund Welt-Zeit-Gesellschaft (WRS/HS); 9 (WRS/HS), Guido Hennrich Ca. sechs Stunden Stahl ist seit Beginn der
Repetitionen Chemie und Werkstoffkunde
 BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 3 Gewinnung und Verarbeitung der Stoffe Eisenwerkstoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL
BEARBEITUNGSTECHNIK REPETITONEN Kapitel 2 Repetitionen Chemie und Werkstoffkunde Thema 3 Gewinnung und Verarbeitung der Stoffe Eisenwerkstoffe Verfasser: Hans-Rudolf Niederberger Elektroingenieur FH/HTL
Wer spannt wem den Sauerstoff aus? Metalloxide
 II Stoffe und ihre Eigenschaften 17. Metalloxide (Kl. 8/9) 1 von 24 Wer spannt wem den Sauerstoff aus? Metalloxide Ein Beitrag von Petra Frank, Tobias Frank und Dr. Hans-Peter Haseloff, Esslingen Mit Illustrationen
II Stoffe und ihre Eigenschaften 17. Metalloxide (Kl. 8/9) 1 von 24 Wer spannt wem den Sauerstoff aus? Metalloxide Ein Beitrag von Petra Frank, Tobias Frank und Dr. Hans-Peter Haseloff, Esslingen Mit Illustrationen
1.1 Oxidation von Metallen. Aufgabe. Wie verändern sich Metalle beim Erhitzen? Naturwissenschaften - Chemie - Anorganische Chemie - 1 Metalle
 Naturwissenschaften - Chemie - Anorganische Chemie - Metalle (P753000). Oxidation von Metallen Experiment von: Phywe Gedruckt:.0.203 5:6:40 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe Wie
Naturwissenschaften - Chemie - Anorganische Chemie - Metalle (P753000). Oxidation von Metallen Experiment von: Phywe Gedruckt:.0.203 5:6:40 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe Wie
Die Brandbekämpfung (Gruppenversuche)
 Die Brandbekämpfung (Gruppenversuche) Führt die folgenden Versuche nacheinander durch. Lest die Versuchsbeschreibungen (Kopie) genau durch und klebt sie sofort in eure Haushefte ein. Notiert mit Bleistift
Die Brandbekämpfung (Gruppenversuche) Führt die folgenden Versuche nacheinander durch. Lest die Versuchsbeschreibungen (Kopie) genau durch und klebt sie sofort in eure Haushefte ein. Notiert mit Bleistift
Reduktion und Oxidation Redoxreaktionen
 Reduktion und Oxidation Redoxreaktionen Stahlkonstruktionen die weltberühmt wurden: Eiffelturm Blaues Wunder in Dresden (die grüne Farbe der Brücke wandelte sich durch das Sonnenlicht in Blau um) OXIDATION
Reduktion und Oxidation Redoxreaktionen Stahlkonstruktionen die weltberühmt wurden: Eiffelturm Blaues Wunder in Dresden (die grüne Farbe der Brücke wandelte sich durch das Sonnenlicht in Blau um) OXIDATION
Rost und Rostschutz. Beobachtung: Nach wenigen Momenten steigt das Wasser im Glasröhrchen an.
 Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Wintersemester 2010/2011 26.11.2010 Dozentin: Dr. M. Andratschke Referenten: Forster, Robert
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsvortrag im Wintersemester 2010/2011 26.11.2010 Dozentin: Dr. M. Andratschke Referenten: Forster, Robert
Gewinnung und Reinigung der Übergangsmetalle. Von Sebastian Kreft
 Übergangsmetalle Von Sebastian Kreft Übersicht Gewinnung und Raffination von: 1. Scandium 2. Titan 3. Vanadium 4. Chrom 5. Mangan 6. Eisen 7. Cobalt 8. Nickel 9. Kupfer 10. Zink Übergangsmetalle 2 1. Scandium
Übergangsmetalle Von Sebastian Kreft Übersicht Gewinnung und Raffination von: 1. Scandium 2. Titan 3. Vanadium 4. Chrom 5. Mangan 6. Eisen 7. Cobalt 8. Nickel 9. Kupfer 10. Zink Übergangsmetalle 2 1. Scandium
Verbrennung einer Kerze
 Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Verbrennung einer Kerze Schauen wir uns zunächst die Kerze genauer an. Aus welchen Bestandteilen besteht sie? Und wozu dienen diese? Bestandteil Stoff Funktion Der Stoff ist das Material, woraus ein Körper
Inhaltliche Kompetenzen Prozessbezogene Kompetenzen Methoden/Medien Die Schülerinnen und Schüler...
 Fach: Chemie Schuljahrgang: R7 Stundentafel: ein Schuljahr /2 Std. Woche Stand von: August 2018 Leistungsbewertung: eine Klassenarbeit pro Halbjahr, gem. Fachkonferenzbeschluss Gewichtung ca. 1/3 schriftliche
Fach: Chemie Schuljahrgang: R7 Stundentafel: ein Schuljahr /2 Std. Woche Stand von: August 2018 Leistungsbewertung: eine Klassenarbeit pro Halbjahr, gem. Fachkonferenzbeschluss Gewichtung ca. 1/3 schriftliche
Physik 7 Lernbuffet Teilchenmodell und thermisches Verhalten von Körpern Damköhler
 Physik 7 Lernbuffet Teilchenmodell und thermisches Verhalten von Körpern Damköhler Aufgabe 1 (Aggregatzustände nennen und Aufbau und Bewegung beschreiben) N1: Betrachte aufmerksam die Bilder und benenne
Physik 7 Lernbuffet Teilchenmodell und thermisches Verhalten von Körpern Damköhler Aufgabe 1 (Aggregatzustände nennen und Aufbau und Bewegung beschreiben) N1: Betrachte aufmerksam die Bilder und benenne
Online Ergänzung zu der RAABits Unterrichtseinheit. Wie Metalle reagieren - ein Mystery. Vanessa Engelhard Silvija Markic
 Online Ergänzung zu der RAABits Unterrichtseinheit Wie Metalle reagieren - ein Mystery Vanessa Engelhard Silvija Markic Einleitung: An den folgenden Seiten finden Sie Detektiv-Lupenkarten, die eine Ergänzung
Online Ergänzung zu der RAABits Unterrichtseinheit Wie Metalle reagieren - ein Mystery Vanessa Engelhard Silvija Markic Einleitung: An den folgenden Seiten finden Sie Detektiv-Lupenkarten, die eine Ergänzung
KORROSION UND KORROSIONSSCHUTZ VON METALLEN
 11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
11. Einheit: KORROSION UND KORROSIONSSCHUTZ VON METALLEN Sebastian Spinnen, Ingrid Reisewitz-Swertz 1 von 16 ZIELE DER HEUTIGEN EINHEIT Am Ende der Einheit Korrosion und Korrosionsschutz von Metallen..
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften
 Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Aufgabe: Unterscheidung von Stoffen anhand von Eigenschaften Vorbereitungen: Benötigte Materialien sind entsprechend der Anzahl an Gruppen für die Teams bereitzustellen. -Aufgabenstellung und Hinweise
Aufgabe Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter. Abschlußklausur zur Vorlesung. Chemie der Metalle
 Aufgabe 1 2 3 4 5 6 7 8 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Abschlußklausur zur Vorlesung Chemie der Metalle
Aufgabe 1 2 3 4 5 6 7 8 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Abschlußklausur zur Vorlesung Chemie der Metalle
Schulinternes Curriculum für Chemie 8.Schuljahr (Anfangsunterricht)
 Schulinternes Curriculum für Chemie 8.Schuljahr (Anfangsunterricht) Stoffe und ihre Eigenschaften kennen die Sicherheitsregeln im Chemieunterricht und beachten sie beim Experimentieren untersuchen Stoffe
Schulinternes Curriculum für Chemie 8.Schuljahr (Anfangsunterricht) Stoffe und ihre Eigenschaften kennen die Sicherheitsregeln im Chemieunterricht und beachten sie beim Experimentieren untersuchen Stoffe
Planungsbeispiel Chemie am Beispiel des Kompetenzschwerpunktes
 Vom Lehrplan zur individuellen Unterrichtsplanung Planungsbeispiel Chemie am Beispiel des Kompetenzschwerpunktes Chemischen Prozess der Metallgewinnung darstellen Im Folgenden wird analog dem Planungsbeispiel
Vom Lehrplan zur individuellen Unterrichtsplanung Planungsbeispiel Chemie am Beispiel des Kompetenzschwerpunktes Chemischen Prozess der Metallgewinnung darstellen Im Folgenden wird analog dem Planungsbeispiel
Chemie der Metalle (Nachklausur)
 Aufgabe 1 2 3 4 5 6 7 8 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Abschlußklausur zur Vorlesung Chemie der Metalle
Aufgabe 1 2 3 4 5 6 7 8 Punkte (je 10) Ich bin damit einverstanden, dass mein Klausurergebnis unter Angabe der Matrikelnummer im Web bekanntgegeben wird: Abschlußklausur zur Vorlesung Chemie der Metalle
Geht dir ein Licht auf?
 Geht dir ein Licht auf? Im folgenden Experiment wirst du erfahren, wie du mit einfachen Mitteln ein Lämpchen zum Leuchten bringst. Materialien - Glühlämpchen - Flachbatterie Auftrag Die folgenden Abbildungen
Geht dir ein Licht auf? Im folgenden Experiment wirst du erfahren, wie du mit einfachen Mitteln ein Lämpchen zum Leuchten bringst. Materialien - Glühlämpchen - Flachbatterie Auftrag Die folgenden Abbildungen
Stoffe im Alltag Beitrag 9 Reinstoffe und Stoffgemische (Klassen 7 9) Reinstoffe und Stoffgemische in unserem Alltag ein Stationenlernen VORANSICHT
 Stoffe im Alltag Beitrag 9 Reinstoffe und Stoffgemische (Klassen 7 9) 1 von 28 Reinstoffe und Stoffgemische in unserem Alltag ein Stationenlernen Ein Beitrag von Sabine Stoermer, Oldenburg Der Frühstückstisch
Stoffe im Alltag Beitrag 9 Reinstoffe und Stoffgemische (Klassen 7 9) 1 von 28 Reinstoffe und Stoffgemische in unserem Alltag ein Stationenlernen Ein Beitrag von Sabine Stoermer, Oldenburg Der Frühstückstisch
