Atemgastransport im Blut
|
|
|
- Edith Brauer
- vor 9 Jahren
- Abrufe
Transkript
1 Atemgastransport im Blut Institut für MTA-Ausbildung am Klinikum Osnabrück Fachgebiet Anatomie/Physiologie/Krankheitslehre - Dr. U. Krämer 1. Physikalische Löslichkeit der Atemgase Sauerstoff und Kohlendioxid sind wichtige Atemgase. Sie werden im Blut sowohl in physikalisch gelöster Form (also als "Mikrobläschen") als auch in chemisch gebundener Form transportiert. Stickstoff und andere Gase finden sich im Blut ausschließlich in physikalisch gelöster Form vor. (Übrigens: Mineralwasser mit Kohlensäure enthält CO2 wesentlich in physikalisch gelöster Form. Beim Schütteln kann man die kleinen Bläschen sehen.) Wenn man eine Flüssigkeit (Wasser, Blut) mit einem Gas (Sauerstoff, Kohlendioxid, Stickstoff o.ä.) in Kontakt bringt, dringt ein kleiner Teil des Gases in die Flüssigkeit ein und verbleibt dort in physikalischer Lösung in Form von winzigen nicht sichtbaren Mikrobläschen. Je höher der Druck des Gases über der Flüssigkeit ist, desto mehr Moleküle dieses Gases dringen in die Flüssigkeit ein. Es gilt also: Gaskonzentration in der Flüssigkeit ist proportional dem Gasdruck über der Flüssigkeit Der Gasdruck kann mit einem Barometer gemessen werden. Wir benutzen in der Physiologie [mm Hg] traditionsgemäß als Einheit für den Druck. Zimmerluft, die Oberflächenkontakt mit dem Blut hat, enthält unter anderem etwa 21 Vol% -Sauerstoff. Messe ich also mit einem Barometer z.b. einen Luftdruck von 760 mm Hg, dann ist der Luftsauerstoff zu 21% am Gesamtluftdruck beteiligt. 21% von 760 mm Hg sind etwa 160 mm Hg. Dieser Druck heißt und wird mit po2 abgekürzt. "Sauerstoffpartialdruck" Analog gibt es einen Stickstoffpartialdruck pn2 und einen CO2-Partialdruck pco2. Bitte merken: Gase diffundieren in Flüssigkeiten. Die Menge übertretender Gasmoleküle hängt ab von der Partialdruckdifferenz des Gases zwischen der Flüssigkeit und der Luft oberhalb der Flüssigkeit. Damit hängt die Sauerstoffkonzentration im Blut vom po2 der Luft ab, mit der das Blut in Kontakt tritt.
2 -2- Mathematisch ausgedrückt gilt folgende allgemeine Gleichung: Gaskonzentration im Blut = Partialdruck des Gases x Faktor Der Faktor ist der Bunsen-Löslichkeitskoeffizient, die Gleichung in dieser Form ist das Henry-Dalton-Gesetz. Praktische Bedeutung: Atmet man Zimmerluft, beträgt der po2 der Einatemluft ca. 160 mm Hg. Atmet man reinen Sauerstoff, liegt der po2 der Einatemluft erheblich höher, nämlich bei mm Hg. Somit kann physikalisch viel mehr Sauerstoff ins Blut übertreten. Die Sauerstoffversorgung des Körpers wird besser! Wenn wir aber Luft mit einem po2 von 160 mm Hg einatmen, kommen in der Lunge nicht 160 mm Hg an. Die Einatemluft mischt sich nämlich mit der sauerstoffarmen Luft, die sich in der Lunge befindet und zu Ausatmung ansteht. Diese Luftmischung in der Alveole weist einen po2 von 100 mm Hg (MTAL bitte merken!) auf. Somit ist in der Alveole die Sauerstoffkonzentration viel niedriger als in der eingeatmeten Zimmerluft. Wir haben heute die Möglichkeit, den po2-wert in einer Lösung (z.b. im Blut) mit einer Sauerstoffelektrode direkt zu messen. Der gemessene po2-wert in einer Lösung ist genauso groß, wie der po2-wert in dem Gasgemisch, das mit der Lösung Kontakt hat. Merke: Der po2-wert im alveolären Kapillarblut ist genauso groß wie der po2-wert in der Alveole also 100 mm Hg. Auf dem Weg von der Lunge in den Arterienkreislauf wird kaum Sauerstoff verbraucht. Also beträgt auch der arterielle po2-wert ungefähr 100 mm Hg. Analog findet sich im Blut auch ein messbarer CO2-Anteil. CO2 wird von den Zellen als Stoffwechselprodukt gebildet und an das Blut abgegeben. Dieses CO2 kann mit einer CO2-Elektrode als pco2 gemessen werden. Merke: Der pco2-wert im arteriellen Blut liegt zwischen 35 und 45 mm Hg. Im Venenblut, das mehr CO2 enthält, liegt er deutlich höher.
3 -3- Ein paar Zahlen: 1 Liter Arterienblut enthält 3 ml Sauerstoff in physikalisch gelöster Form. Das ist recht wenig. 1 Liter Arterienblut enthält 26 ml Kohlendioxid (CO2) in gelöster Form. Das ist ziemlich viel. Der Grund liegt darin, dass der Bunsen-Löslichkeitskoeffizient für Sauerstoff viel niedriger ist als der für CO2. Wir haben also das Problem, dass Arterienblut nur 3 ml physikalisch gelösten Sauerstoff enthält. Das reicht niemals, um den Körper mit ausreichend Sauerstoff zu versorgen. Wie ist dieses Problem gelöst? Bitte lesen Sie weiter! 2. Hämoglobin-Sauerstoff-Bindung Der weitaus größte Teil des im Blut transportierten Sauerstoffs (98,5%) ist nämlich an Hämoglobin gebunden. Wussten Sie: Anders ausgedrückt: Oder noch anders: 1 Molekül Hämoglobin kann 4 Moleküle Sauerstoff binden. 1 g Hämoglobin bindet 1,39 ml Sauerstoff (Hüfner-Zahl) 1 ml Arterienblut enthält (bei normalem Hb-Wert) 0,2 ml O2 Wir haben also im Körper unter normalen Bedingungen immer reichlich Sauerstoff zur Verfügung. Das sieht schon besser aus. Es werden übrigens vom Sauerstoff im Arterienblut im Mittel nur 25% ausgenutzt. Bei schwerer körperlicher Arbeit können es auch einmal 50% sein. Dennoch: Der physikalisch gelöste Sauerstoffanteil im Blut ist biologisch sehr wichtig. Hämoglobin kann nämlich nur den Sauerstoff binden, der in physikalisch gelöster Form das Molekül erreicht. Man darf übrigens nicht davon ausgehen, dass alle Hb-Moleküle im Arterienblut mit Sauerstoff gesättigt sind. Der Sättigungsgrad hängt nämlich vom po2-wert ab. Man kann folgendes sagen: Liegt der po2-wert im Arterienblut zwischen 70 und 100 mm Hg, führt das zu einer Hämoglobinsättigung mit Sauerstoff von 95 bis 99%.
4 -4- Hämoglobin bindet übrigens den Sauerstoff schlechter bei - hohen pco2-werten (also, wenn viel zuviel CO2 im Blut ist) - Fieber - zuviel H+ Ionen im Blut ("Azidose") Hinweis: Kohlenmonoxid (CO), das bei unvollständiger Verbrennung organischen Materials entsteht, blockiert das Hb-Molekül für den Sauerstofftransport. Beim Rauchen entstehen größere Mengen inhalierbaren Kohlenmonoxids. So haben starke Raucher durch CO-Blockade des Hämoglobins (dieses nennt man HbCO) bis zu 20% weniger Hb-Moleküle für den Sauerstofftransport zur Verfügung. Damit Hb Sauerstoff binden kann, muss das Hb-Molekül 2-wertiges Eisen (Fe++) enthalten. Enthält Hb 3-wertiges Eisen (Fe+++), wird es biologisch funktionsuntüchtig. Man bezeichnet solche Hb als Methämoglobin. 3. Kohlendioxidtransport im Blut CO2 entsteht als Endprodukt des oxidativen Stoffwechsels in den Körperzellen. Es wird zu lediglich 5% in physikalisch gelöster Form transportiert. Dieser Anteil ist als pco2 messbar. Der pco2 im Arterienblut liegt normalerweise um 40 mm Hg (35-45 mm Hg). Der pco2 im venösen Blut liegt höher, nämlich bei etwa 46 mm Hg. Der größte Anteil des CO2 (90%) liegt nach folgender Reaktionsgleichung als Bikarbonat (HCO3-) vor: CO2 + H2O > H2CO > HCO3- + H+ Diese Reaktion erfolgt im Plasma recht langsam. CO2 kann aber in die Erythrocyten diffundieren. Hier befindet sich das Enzym Carboanhydratase (= Carboanhydrase), welche die Reaktion um den Faktor beschleunigt. Somit gelangt CO2 aus den Zellen in das Blut und von dort in die Erythrocyten, wo in großem Umfang dann HCO- entsteht. Dieses HCO3- diffundiert entlang eines Konzentrationsgefälles zum Plasmaraum wieder in Richtung Plasma. Für jedes HCO3- Ion, das aus dem Ery in das Plasma überwechselt, tritt ein Chlorid-Ion (Cl-) aus dem Plasma in den Erythrocyten ("Chloridverschiebung"), um das Ladungsgleichgewicht zu erhalten. Auf diese Weise werden 90% aller CO2-Moleküle, die im Körper entstehen, zu HCO3- umgewandelt. 30% bleiben in den Erys, 60% wandern in das Plasma. 5% des im Körper gebildeten CO2 lagerts sich an freie Aminogruppen des Hämoglobins an, wodurch "Carbamino-Hämoglobin" ensteht.
5 -5- In der Lunge entsteht aus HCO3- wieder CO2, und zwar auf folgendem Wege: HCO3- + H+ (immer im Blut vorhanden) > H2CO > H2O + CO2 Das CO2 wird ausgeatmet, das H2O wird gleichfalls abgeatmet oder über die Nieren oder über die Schweißdrüsen ausgeschieden. Zusammenfassung: (1) O2 und CO2 werden im Blut sowohl physikalisch gelöst als auch in chemisch gebundener Form transportiert. (2) Die Konzentration eines physikalisch gelösten Gases in einer Lösung ist im Henry-Dalton-Gesetz beschrieben. (3) 98,5% des Sauerstoffs im Blut ist an Hb gebunden. Der Rest ist physikalisch gelöst. (4) 1 g Hb bindet maximal 1,39 ml Sauerstoff (Hüfner sche Zahl) (5) Die Anlagerung von Sauerstoff an Hämoglobin bezeichnet man als Oxygenierung. Das Produkt heißt dann Oxyhämoglobin HbO2 Hämoglobin ohne Sauerstoff heißt "reduziertes Hämoglobin" oder "Desoxy-Hämoglobin". Übrigens: Hat man mehr als 5 g/dl reduziertes Hämoglobin im Blut, verfärbt sich die Haut blau ("Cyanose") (6) Die "Sauerstoffsättigung" (Kürzel: so2) ist der Prozentsatz von HbO2 am Gesamt-Hb. So bedeutet ein so2 von 90%, dass 90% aller Hb-Moleküle mit Sauerstoff beladen sind. (7) Kohlenmonoxid blockiert Hämoglobin für den Sauerstofftransport (8) Methämoglobin (MetHb) ist biologisch funktionsuntüchtig. (9) CO2 wird transportiert in physikalisch gelöster Form, als HCO3- und als Carbamino- Hämoglobin. Kontrollfragen: (1) Ein Patient wird mit 50% Sauerstoff beatmet. Der aktuell Luftdruck beträgt 750 mm Hg. Wie hoch ist der po2 in der Einatmungsluft? (2) Mit welchem Hilfsmittel können wir po2 und pco2 im Blut oder in Flüssigkeiten messen? (3) Was bedeutet der Begriff "physikalische Lösung" eines Gases? (4) Wie hoch liegt normalerweise der alveoläre po2-wert? Warum ist er nicht 160 mm Hg? (5) Wie wird Sauerstoff im Blut transportiert? (6) Wie wird CO2 im Blut transportiert? (7) Warum ist Kohlenmonoxid giftig? (8) Was ist eine Cyanose? Wann tritt sie auf? (9) Was ist Methämoglobin?
Die Welt des Trimix vom Helium im Körper bis zum Sauerstoff-Fenster. Dr. med. Jochen Steinbrenner Vorsitzender der Spitalleitung
 Die Welt des Trimix vom Helium im Körper bis zum Sauerstoff-Fenster Dr. med. Jochen Steinbrenner Vorsitzender der Spitalleitung Programm Helium Trimix Gasgemische Isobare Gegendiffusion Sauerstoff-Fenster
Die Welt des Trimix vom Helium im Körper bis zum Sauerstoff-Fenster Dr. med. Jochen Steinbrenner Vorsitzender der Spitalleitung Programm Helium Trimix Gasgemische Isobare Gegendiffusion Sauerstoff-Fenster
Blutgase. 3.1 Sauerstoff 55. 3.2 Kohlendioxid 64. Literatur 68
 Blutgase.1 Sauerstoff 55.1.1 O 2 -Kaskade 55.1.2 Transport von Sauerstoff im Blut 57.1. O 2 -Sättigung des Hämoglobins und O 2 -Bindungskurve 58.1.4 O 2 -Gehalt und O 2 -Status des Blutes 62.1.5 O 2 -Angebot
Blutgase.1 Sauerstoff 55.1.1 O 2 -Kaskade 55.1.2 Transport von Sauerstoff im Blut 57.1. O 2 -Sättigung des Hämoglobins und O 2 -Bindungskurve 58.1.4 O 2 -Gehalt und O 2 -Status des Blutes 62.1.5 O 2 -Angebot
Abb. 1: Hai; Abb. 2: Pfeilgiftfrosch
 www.schullv.de Basiswissen > Physiologie > Die Atmung Die Atmung Skript PLUS Einführung Abb. 1: Hai; Abb. 2: Pfeilgiftfrosch Die Lebewesen auf der Erde sind alle unterschiedlich. Sie unterscheiden sich
www.schullv.de Basiswissen > Physiologie > Die Atmung Die Atmung Skript PLUS Einführung Abb. 1: Hai; Abb. 2: Pfeilgiftfrosch Die Lebewesen auf der Erde sind alle unterschiedlich. Sie unterscheiden sich
Experiment Isolierung, Aktivität und Hemmung der Carboanhydrase
 Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Experiment Isolierung, Aktivität und emmung der Carboanhydrase 1 Aufgabe: Partnerarbeit Bilden ie selbständig Zweiergruppen. tudieren ie zuerst die Einleitung. Legen ie das Material bereit. Bereiten ie
Saurer Regen, was ist das?
 Saurer Regen, was ist das? 1. SO x (x=2,3) => SO 2 und SO 3 SO 2 + H 2 O H 2 SO 3 (schwefelige Säure) SO 3 + H 2 O H 2 SO 4 (Schwefelsäure) 2. NO x (x=1,2) 2 NO + H 2 O + ½O 2 2 H NO 2 (salpetrige Säure)
Saurer Regen, was ist das? 1. SO x (x=2,3) => SO 2 und SO 3 SO 2 + H 2 O H 2 SO 3 (schwefelige Säure) SO 3 + H 2 O H 2 SO 4 (Schwefelsäure) 2. NO x (x=1,2) 2 NO + H 2 O + ½O 2 2 H NO 2 (salpetrige Säure)
Atemschutzgeräteträger der Feuerwehr Kapitel 2 Atmung
 2 Kapitel 2 Atmung 3 1 Grundlagen der Atmung Die Atmung ist einer der lebensnotwendigen Vorgänge des Menschen. Beim Einatmen wird dem Organismus der lebenswichtige Sauerstoff zugeführt. Den benötigt der
2 Kapitel 2 Atmung 3 1 Grundlagen der Atmung Die Atmung ist einer der lebensnotwendigen Vorgänge des Menschen. Beim Einatmen wird dem Organismus der lebenswichtige Sauerstoff zugeführt. Den benötigt der
Oxidation und Reduktion Redoxreaktionen Blatt 1/5
 Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Oxidation und Reduktion Redoxreaktionen Blatt 1/5 1 Elektronenübertragung, Oxidation und Reduktion Gibt Natrium sein einziges Außenelektron an ein Chloratom (7 Außenelektronen) ab, so entsteht durch diese
Lunge - Aufbau und Funktion. Zahlen und Daten. Aufbau der Atemwege. Dr. med. Manfred Werner, Facharzt für Innere Medizin und Lungenheilkunde
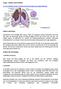 Lunge - Aufbau und Funktion Dr. med. Manfred Werner, Facharzt für Innere Medizin und Lungenheilkunde Zahlen und Daten NetDoktor.de Sauerstoff ist die Grundlage allen Lebens. Kaum ein Vorgang im Körper
Lunge - Aufbau und Funktion Dr. med. Manfred Werner, Facharzt für Innere Medizin und Lungenheilkunde Zahlen und Daten NetDoktor.de Sauerstoff ist die Grundlage allen Lebens. Kaum ein Vorgang im Körper
Das Sauerstoff-Transportsystem
 Das Sauerstoff-Transportsystem Physiologische Grundlagen Der Organismus hat praktisch keine Sauerstoffvorräte. Von der mit dem arteriellen Blutstrom an die Gewebe gelieferten Sauerstoffmenge werden in
Das Sauerstoff-Transportsystem Physiologische Grundlagen Der Organismus hat praktisch keine Sauerstoffvorräte. Von der mit dem arteriellen Blutstrom an die Gewebe gelieferten Sauerstoffmenge werden in
1.6 ph-werte. Einführung Chemie Seite 19
 Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011
 Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme
Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme
Proteinbestimmung. Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der Proteinbestimmung mit den folgenden Lehrzielen:
 Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Diese Lerneinheit befasst sich mit der Beschreibung von verschiedenen Methoden der mit den folgenden Lehrzielen: Verständnis der Prinzipien der sowie deren praktischer Durchführung Unterscheidung zwischen
Multiple-Choice Test. Alle Fragen können mit Hilfe der Versuchsanleitung richtig gelöst werden.
 PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
PCG-Grundpraktikum Versuch 8- Reale Gas Multiple-Choice Test Zu jedem Versuch im PCG wird ein Vorgespräch durchgeführt. Für den Versuch Reale Gas wird dieses Vorgespräch durch einen Multiple-Choice Test
Crashkurs Säure-Base
 Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Atmung, Stoffwechsel und Blutkreislauf
 Atmung, Stoffwechsel und Blutkreislauf Rainer Müller Lehrstuhl für Didaktik der Physik, Universität München Schellingstr. 4, 80799 München 1. Allgemeine Zusammenhänge Ein Thema, das bei Schülerinnen und
Atmung, Stoffwechsel und Blutkreislauf Rainer Müller Lehrstuhl für Didaktik der Physik, Universität München Schellingstr. 4, 80799 München 1. Allgemeine Zusammenhänge Ein Thema, das bei Schülerinnen und
Probleme sind Gelegenheiten zu zeigen, was man kann. Duke Ellington, amerikanischer Jazz-Musiker (1899-1974)
 1 H 2 -Atemtest (Lactose-Toleranztest) Inhalt Probleme sind Gelegenheiten zu zeigen, was man kann. Duke Ellington, amerikanischer Jazz-Musiker (1899-1974) 1 Lactose-Intoleranz: Einführung... 1 2 Wasserstoff...
1 H 2 -Atemtest (Lactose-Toleranztest) Inhalt Probleme sind Gelegenheiten zu zeigen, was man kann. Duke Ellington, amerikanischer Jazz-Musiker (1899-1974) 1 Lactose-Intoleranz: Einführung... 1 2 Wasserstoff...
Kohlendioxidfreisetzung aus Champagner. 1 Einleitung/Theorie. Peter Bützer. Inhalt
 Kohlendioxidfreisetzung aus Champagner Inhalt 1 Einleitung/Theorie... 1 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 2 2.4 Reaktionsgleichungen/Berechnungen...
Kohlendioxidfreisetzung aus Champagner Inhalt 1 Einleitung/Theorie... 1 2 Experiment... 2 2.1 Aufgabenstellung... 2 2.2 Durchführung... 2 2.3 Beobachtungen/Messungen... 2 2.4 Reaktionsgleichungen/Berechnungen...
Chemische Reaktionen ergeben neue Stoffe mit neuen Eigenschaften
 1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
1 Grundbegriffe 1.1 Die Entwicklung der Chemie Im Vergleich zu anderen Naturwissenschaften wie der Physik oder der Biologie ist die Chemie eine junge Wissenschaft. Denn erst vor etwa 200 Jahren gelangten
6 Lunge und Atmung. 6.1 Luft. 6.1.1 Zusammensetzung. 6.1.2 Löslichkeit von Gasen in Flüssigkeiten
 Literatur zu diesem Kaitel: Der Körer des Menschen, A. Faller, M. Schünke; Thieme Physics of the Body, J.R. Cameron, J.G. Skofronick, R.M. Grant, Ka. 7: Physics of the Lung and Breathing Biohysik, Hoe,
Literatur zu diesem Kaitel: Der Körer des Menschen, A. Faller, M. Schünke; Thieme Physics of the Body, J.R. Cameron, J.G. Skofronick, R.M. Grant, Ka. 7: Physics of the Lung and Breathing Biohysik, Hoe,
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Wortschema Reaktionsschema Beispiel 1: Kupfer und Schwefel Vorzahlen
 6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
6. Reaktionsgleichungen 6.1 Chemisches Reaktionsschema Das Wortschema benennt die Ausgangsstoffe und die Reaktionsprodukte einer chemischen Reaktion. Das Reaktionsschema sagt zusätzlich etwas über das
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 3, 02.05.11/03.05.11
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 3, 02.05.11/03.05.11 1. Sie haben Silberbesteck geerbt. Um Ihren neuen Reichtum ordentlich zur Schau zu stellen, haben
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 3, 02.05.11/03.05.11 1. Sie haben Silberbesteck geerbt. Um Ihren neuen Reichtum ordentlich zur Schau zu stellen, haben
12 Säure-Basen-Haushalt
 12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
12.1 Der ph-wert in Körperflüssigkeiten 281 Gotthold Gäbel Der ph-wert der extrazellulären Flüssigkeit wird in einem sehr engen Bereich zwischen 7,36 und 7,44 gehalten. Dies geschieht über Puffersysteme,
Reaktionsgleichungen und was dahinter steckt
 Reaktionsgleichungen und was dahinter steckt Prinzipien Bestehende Formeln dürfen nicht verändert werden. Bei Redoxreaktionen kann H, OH oder H 2 O ergänzt werden. Links und rechts vom Reaktionspfeil muss
Reaktionsgleichungen und was dahinter steckt Prinzipien Bestehende Formeln dürfen nicht verändert werden. Bei Redoxreaktionen kann H, OH oder H 2 O ergänzt werden. Links und rechts vom Reaktionspfeil muss
ph Werte im Organismus Alle im Organismus gebildeten Flüssigkeiten haben einen bestimmten ph-wert. Am wichtigsten ist der ph - Wert des Blutes.
 Jede Sekunde finden im menschlichen Körper Millionen von chemischen Prozessen statt: Stoffe werden aufgenommen, aufgebaut, umgebaut, abgebaut und ausgeschieden. Bei diesen hochkomplexen Abläufen spielen
Jede Sekunde finden im menschlichen Körper Millionen von chemischen Prozessen statt: Stoffe werden aufgenommen, aufgebaut, umgebaut, abgebaut und ausgeschieden. Bei diesen hochkomplexen Abläufen spielen
PBM Patientenorientiertes Blut Management 3 Säulen Modell. Arno Schiferer HTG Anästhesie & Intensivmedizin AKH / Medizinische Universität Wien
 PBM Patientenorientiertes Blut Management 3 Säulen Modell Arno Schiferer HTG Anästhesie & Intensivmedizin AKH / Medizinische Universität Wien Wo stehen wir 2013? Klinische Hämotherapie Patientenperspektive
PBM Patientenorientiertes Blut Management 3 Säulen Modell Arno Schiferer HTG Anästhesie & Intensivmedizin AKH / Medizinische Universität Wien Wo stehen wir 2013? Klinische Hämotherapie Patientenperspektive
Atome - Chemische Symbole
 Atome - Chemische Symbole Um zu erklären, dass die Grundstoffe nicht weiter zerlegbar sind, nahm der englische Wissenschaftler John Dalton um 1800 an, dass die chemischen Elemente aus unteilbaren Teilchen
Atome - Chemische Symbole Um zu erklären, dass die Grundstoffe nicht weiter zerlegbar sind, nahm der englische Wissenschaftler John Dalton um 1800 an, dass die chemischen Elemente aus unteilbaren Teilchen
Hinweise für den Schüler. Von den 2 Prüfungsblöcken A und B ist einer auszuwählen.
 Abitur 2001 Chemie Gk Seite 1 Hinweise für den Schüler Aufgabenauswahl: Von den 2 Prüfungsblöcken A und B ist einer auszuwählen. Bearbeitungszeit: Die Arbeitszeit beträgt 210 Minuten, zusätzlich stehen
Abitur 2001 Chemie Gk Seite 1 Hinweise für den Schüler Aufgabenauswahl: Von den 2 Prüfungsblöcken A und B ist einer auszuwählen. Bearbeitungszeit: Die Arbeitszeit beträgt 210 Minuten, zusätzlich stehen
Musterprüfung. 1.3. Wie nennt man einen elektrisch ungeladenen Körper mit einer Ansammlung von positiver und einer Ansammlung von negativer Ladung?
 1 Musterprüfung 1. Modul: Wasser 1.1. In Wassermolekülen gibt es Ansammlungen von Ladungen. Wo befinden sich in einem Wassermolekül Ansammlungen von positiven und negativen Ladungen? 1.2. Wie nennt man
1 Musterprüfung 1. Modul: Wasser 1.1. In Wassermolekülen gibt es Ansammlungen von Ladungen. Wo befinden sich in einem Wassermolekül Ansammlungen von positiven und negativen Ladungen? 1.2. Wie nennt man
Kapitel 4: Chemische. Woher stammen die chemischen Symbole?
 Kapitel 4: Chemische Symbole Woher stammen die chemischen Symbole? Das sind die Anfangsbuchstaben (manchmal auch die ersten beiden Anfangsbuchstaben) der lateinischen oder griechischen Namen der Elemente.
Kapitel 4: Chemische Symbole Woher stammen die chemischen Symbole? Das sind die Anfangsbuchstaben (manchmal auch die ersten beiden Anfangsbuchstaben) der lateinischen oder griechischen Namen der Elemente.
11. Klasse Heft 1. Maximilian Ernestus September/Oktober 2007. Chemie 11. Klasse Heft 1 1
 1 GRUNDLAGEN 11. Klasse Heft 1 Maximilian Ernestus September/Oktober 2007 Chemie 11. Klasse Heft 1 1 1. Chemische Elemente Elemente haben allgemein folgende Eigenschaften: sie sind nicht weiter zerlegbar
1 GRUNDLAGEN 11. Klasse Heft 1 Maximilian Ernestus September/Oktober 2007 Chemie 11. Klasse Heft 1 1 1. Chemische Elemente Elemente haben allgemein folgende Eigenschaften: sie sind nicht weiter zerlegbar
DRUCK ATMUNG BLUTKREISLAUF
 Physik und Medizin DRUCK ATMUNG BLUTKREISLAUF Teil 2 Umgebungsdruck und Atmungsstörungen Lehrstuhl für Didaktik der Physik Ludwig-Maximilians-Universität München Giuseppe Colicchia, Andrea Künzl und Hartmut
Physik und Medizin DRUCK ATMUNG BLUTKREISLAUF Teil 2 Umgebungsdruck und Atmungsstörungen Lehrstuhl für Didaktik der Physik Ludwig-Maximilians-Universität München Giuseppe Colicchia, Andrea Künzl und Hartmut
PRAKTIKUM SIMULATIONSTECHNIK
 FACHHOCHSCHULE LANDSHUT Fachbereich Elektrotechnik Prof. Dr. G. Dorn PRAKTIKUM SIMULATIONSTECHNIK 1 Versuch1: Atmungsregulation 1.1 Einleitung Bei Säugetieren gewinnt jede Zelle ihre Energie hauptsächlich
FACHHOCHSCHULE LANDSHUT Fachbereich Elektrotechnik Prof. Dr. G. Dorn PRAKTIKUM SIMULATIONSTECHNIK 1 Versuch1: Atmungsregulation 1.1 Einleitung Bei Säugetieren gewinnt jede Zelle ihre Energie hauptsächlich
Chem. Grundlagen. ure-base Begriff. Das Protonen-Donator-Akzeptor-Konzept. Wasserstoff, Proton und Säure-Basen. Basen-Definition nach Brønsted
 Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Der SäureS ure-base Begriff Chem. Grundlagen Das Protonen-Donator-Akzeptor-Konzept Wasserstoff, Proton und Säure-Basen Basen-Definition nach Brønsted Wasserstoff (H 2 ) Proton H + Anion (-) H + = Säure
Martin Raiber 21.02.07 Elektrolyse: Strom - Spannungskurven
 Martin Raiber 21.02.07 Elektrolyse: Strom - Spannungskurven Geräte: U-Rohr, verschiedene Platin-Elektroden (blank, platiniert), Graphit-Elektroden, spannungsstabilisierte Gleichspannungsquelle, CASSY-Spannungs/Stromstärkemessgerät
Martin Raiber 21.02.07 Elektrolyse: Strom - Spannungskurven Geräte: U-Rohr, verschiedene Platin-Elektroden (blank, platiniert), Graphit-Elektroden, spannungsstabilisierte Gleichspannungsquelle, CASSY-Spannungs/Stromstärkemessgerät
Rost und Rostschutz. Chemikalien: Rost, verdünnte Salzsäure HCl, Kaliumhexacyanoferrat(II)-Lösung K 4 [Fe(CN) 6 ]
![Rost und Rostschutz. Chemikalien: Rost, verdünnte Salzsäure HCl, Kaliumhexacyanoferrat(II)-Lösung K 4 [Fe(CN) 6 ] Rost und Rostschutz. Chemikalien: Rost, verdünnte Salzsäure HCl, Kaliumhexacyanoferrat(II)-Lösung K 4 [Fe(CN) 6 ]](/thumbs/28/13018795.jpg) Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsversuche im Sommersemester 2009 24.06.2009 Dozentin: Dr. M. Andratschke Referenten: Mühlbauer, Manuel
Universität Regensburg Institut für Anorganische Chemie Lehrstuhl Prof. Dr. A. Pfitzner Demonstrationsversuche im Sommersemester 2009 24.06.2009 Dozentin: Dr. M. Andratschke Referenten: Mühlbauer, Manuel
Katalysatoren - Chemische Partnervermittlung im virtuellen Labor
 Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
Seite 1 von 6 Katalysatoren - Chemische Partnervermittlung im virtuellen Labor Katalysatoren Der Katalysator in der Großindustrie Was passiert im Inneren? Das virtuelle Labor. Katalysatoren Katalysatoren
GEMEINDEWERKE KIEFERSFELDEN
 GEMEINDEWERKE KIEFERSFELDEN Strom - Gas - Wasser Allgemeine Informationen zum Trinkwasser Ernährungsphysiologische Bedeutung Funktionen von Wasser im Körper Jede chemische Reaktion und jeder Vorgang im
GEMEINDEWERKE KIEFERSFELDEN Strom - Gas - Wasser Allgemeine Informationen zum Trinkwasser Ernährungsphysiologische Bedeutung Funktionen von Wasser im Körper Jede chemische Reaktion und jeder Vorgang im
Redox- Titrationen PAC I - QUANTITATIVE ANALYSE ANALYTIK I IAAC, TU-BS, 2004. Manganometrie. Bestimmung von Eisen(III) in salzsaurer Lösung
 Redox Titrationen ANALYTK AAC, TUBS, 2004 Dr. Andreas Martens [email protected] nstitut f. Anorg.u. Analyt. Chemie, Technische Universität Braunschweig, Braunschweig, Germany PAC QUANTTATVE ANALYSE Manganometrie
Redox Titrationen ANALYTK AAC, TUBS, 2004 Dr. Andreas Martens [email protected] nstitut f. Anorg.u. Analyt. Chemie, Technische Universität Braunschweig, Braunschweig, Germany PAC QUANTTATVE ANALYSE Manganometrie
Stöchiometrie. (Chemisches Rechnen)
 Ausgabe 2007-10 Stöchiometrie (Chemisches Rechnen) ist die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen sowie der Mengenverhältnisse der beteiligten Stoffe bei chemischen Reaktionen
Ausgabe 2007-10 Stöchiometrie (Chemisches Rechnen) ist die Lehre von der mengenmäßigen Zusammensetzung chemischer Verbindungen sowie der Mengenverhältnisse der beteiligten Stoffe bei chemischen Reaktionen
+ O. Die Valenzelektronen der Natriumatome werden an das Sauerstoffatom abgegeben.
 A Oxidation und Reduktion UrsprÄngliche Bedeutung der Begriffe UrsprÅnglich wurden Reaktionen, bei denen sich Stoffe mit Sauerstoff verbinden, als Oxidationen bezeichnet. Entsprechend waren Reaktionen,
A Oxidation und Reduktion UrsprÄngliche Bedeutung der Begriffe UrsprÅnglich wurden Reaktionen, bei denen sich Stoffe mit Sauerstoff verbinden, als Oxidationen bezeichnet. Entsprechend waren Reaktionen,
Die Avogadro-Konstante N A
 Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
Die Avogadro-Konstante N A Das Ziel der folgenden Seiten ist es, festzustellen, wie viele Atome pro cm³ oder pro g in einem Stoff enthalten sind. Chemische Reaktionen zwischen Gasen (z.b. 2H 2 + O 2 2
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik
 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1 6. Tag: Chemisches Gleichgewicht und Reaktionskinetik 1. Das chemische Gleichgewicht Eine chemische Reaktion läuft in beiden Richtungen ab. Wenn
Was Sie über Gicht wissen sollten
 Was Sie über Gicht wissen sollten Wichtige Aspekte zusammengefasst diese Seite bitte herausklappen. Die mit dem Regenbogen Patienteninformation Wichtig Was ist Gicht? Vieles können Sie selber tun, um Komplikationen
Was Sie über Gicht wissen sollten Wichtige Aspekte zusammengefasst diese Seite bitte herausklappen. Die mit dem Regenbogen Patienteninformation Wichtig Was ist Gicht? Vieles können Sie selber tun, um Komplikationen
Wie kommen die Löcher in den Emmentaler AOC?
 Wie kommen die Löcher in den Emmentaler AOC? Weder Mäuse aus dem Emmental noch patentierte Bohrmaschinen sind für die typischen Löcher im berühmten Emmentalerkäse verantwortlich. Diese entstehen auf natürliche
Wie kommen die Löcher in den Emmentaler AOC? Weder Mäuse aus dem Emmental noch patentierte Bohrmaschinen sind für die typischen Löcher im berühmten Emmentalerkäse verantwortlich. Diese entstehen auf natürliche
4 Stöchiometrie. Teil II: Chemische Reaktionsgleichungen. 4.1 Chemische Reaktionsgleichungen
 35 4 Stöchiometrie Teil II: Chemische Reaktionsgleichungen Zusammenfassung Chemische Reaktionsgleichungen geben durch die Formeln der beteiligten Substanzen an, welche Reaktanden sich zu welchen Produkten
35 4 Stöchiometrie Teil II: Chemische Reaktionsgleichungen Zusammenfassung Chemische Reaktionsgleichungen geben durch die Formeln der beteiligten Substanzen an, welche Reaktanden sich zu welchen Produkten
Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse
 Trennen von Farben Was Du brauchst: schwarzfarbige Filzstifte Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse Wie Du vorgehst: Schneide einen Kreis aus dem Kaffeefilter. Steche mit
Trennen von Farben Was Du brauchst: schwarzfarbige Filzstifte Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse Wie Du vorgehst: Schneide einen Kreis aus dem Kaffeefilter. Steche mit
INSTITUT FÜR PHYSIOLOGIE
 INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
INSTITUT FÜR PHYSIOLOGIE Anleitung zum Physiologie - Praktikum P - 1. Pufferung und Säure-Basen Analyse WS 2010/11 3. Semester 2 Inhalt I. VORBEMERKUNGEN... 3 II. THEORETISCHE GRUNDLAGEN... 4 1. Säuren
Bauchemie 1. 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle?
 Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Bauchemie 1 1. Welche elementaren Teilchen enthält a) der Atomkern und b) die Atomhülle? a) Der Atomkern besteht aus Neutronen und Protonen, die zusammen auch Nukleonen genannt werden. Er befindet sich
Klausur Physikalische Chemie für TUHH (Chemie III)
 07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
07.03.2012 14.00 Uhr 17.00 Uhr Moritz / Pauer Klausur Physikalische Chemie für TUHH (Chemie III) Die folgende Tabelle dient Korrekturzwecken und darf vom Studenten nicht ausgefüllt werden. 1 2 3 4 5 6
MAGNESIUM. 1. Bei Verbrennungsreaktionen entstehen in der Regel (kreuze richtig an):
 MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
MAGNESIUM benötigte Arbeitszeit: 20 min Magnesium (Mg) ist sowohl in Wunderkerzen (Sternspritzern) als auch in Brandsätzen und in Leuchtmunition enthalten. Früher wurde es auch in (Foto-)Blitzlampen verwendet.
Grundwissen Chemie 8I
 1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
1) Stoffe, Experimente Chemie ist die Lehre von den Stoffen, ihren Eigenschaften, ihrem Aufbau, ihren Veränderungen und ihrer Herstellung. Einfache Möglichkeiten der Stofferkennung (Farbe, Glanz, Kristallform,
des Arbeitskreises Schankanlagen im DBB über den Ausschank von deutschem Bier mit Mischgas Gründe gegen den Einsatz von vorgemischtem Mischgas
 Grundsatzpapier des Arbeitskreises Schankanlagen im DBB über den Ausschank von deutschem Bier mit Mischgas Vorwort Durch die Verwendung von konfektioniertem Mischgas in Gasflaschen wird beim Ausschank
Grundsatzpapier des Arbeitskreises Schankanlagen im DBB über den Ausschank von deutschem Bier mit Mischgas Vorwort Durch die Verwendung von konfektioniertem Mischgas in Gasflaschen wird beim Ausschank
Methode: Aktivierung mit der Methode Lerntempoduett Fach: Naturwissenschaften. Thema des Unterrichtsbeispiels: Blutkreislauf Klassenstufe: 6
 Methode: Aktivierung mit der Methode Lerntempoduett Fach: Naturwissenschaften Thema des Unterrichtsbeispiels: Blutkreislauf Klassenstufe: 6 Kompetenzbereich: Textverarbeitung (K) Ziele Materialien (Raum-)ausstattung
Methode: Aktivierung mit der Methode Lerntempoduett Fach: Naturwissenschaften Thema des Unterrichtsbeispiels: Blutkreislauf Klassenstufe: 6 Kompetenzbereich: Textverarbeitung (K) Ziele Materialien (Raum-)ausstattung
Grundlagen der Chemie Elektrolyt- und Nichtelektrolytlösungen
 Elektrolyt- und Nichtelektrolytlösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektrolyt- und Nichtelektrolytlösungen
Elektrolyt- und Nichtelektrolytlösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Elektrolyt- und Nichtelektrolytlösungen
Säure-Base Titrationen. (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen)
 Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Säure-Base Titrationen (Seminar zu den Übungen zur quantitativen Bestimmung von Arznei-, Hilfs- und Schadstoffen) 1. Gehaltsbestimmung von Salzsäure HCl ist eine starke Säure (fast zu 100% dissoziiert)
Wissenswertes über die Atemwege und Therapie
 Wissenswertes über die Atemwege und Therapie Wie funktioniert unsere Atmung? Jede Zelle unseres Körpers benötigt Sauerstoff. Beim Einatmen gelangt die Luft durch die oberen Atemwege hierzu gehört der Nasenraum
Wissenswertes über die Atemwege und Therapie Wie funktioniert unsere Atmung? Jede Zelle unseres Körpers benötigt Sauerstoff. Beim Einatmen gelangt die Luft durch die oberen Atemwege hierzu gehört der Nasenraum
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie
 Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Musterklausur 1 zur Allgemeinen und Anorganischen Chemie Achtung: Taschenrechner ist nicht zugelassen. Aufgaben sind so, dass sie ohne Rechner lösbar sind. Weitere Hilfsmittel: Periodensystem der Elemente
Gefahrstoffe. Welchen Belastungen und Schadstoffen ist der Mensch bei der Arbeit ausgesetzt?
 ? Welchen Belastungen und Schadstoffen ist der Mensch bei der Arbeit ausgesetzt? Welche Auswirkungen haben mögliche Belastungen und Schadstoffe? auf den menschlichen Organismus? 2 10 Was sind potentielle
? Welchen Belastungen und Schadstoffen ist der Mensch bei der Arbeit ausgesetzt? Welche Auswirkungen haben mögliche Belastungen und Schadstoffe? auf den menschlichen Organismus? 2 10 Was sind potentielle
Der Gesamtdruck eines Gasgemisches ist gleich der Summe der Partialdrücke. p [mbar, hpa] = p N2 + p O2 + p Ar +...
![Der Gesamtdruck eines Gasgemisches ist gleich der Summe der Partialdrücke. p [mbar, hpa] = p N2 + p O2 + p Ar +... Der Gesamtdruck eines Gasgemisches ist gleich der Summe der Partialdrücke. p [mbar, hpa] = p N2 + p O2 + p Ar +...](/thumbs/25/5798672.jpg) Theorie FeucF euchtemessung Das Gesetz von v Dalton Luft ist ein Gemisch aus verschiedenen Gasen. Bei normalen Umgebungsbedingungen verhalten sich die Gase ideal, das heißt die Gasmoleküle stehen in keiner
Theorie FeucF euchtemessung Das Gesetz von v Dalton Luft ist ein Gemisch aus verschiedenen Gasen. Bei normalen Umgebungsbedingungen verhalten sich die Gase ideal, das heißt die Gasmoleküle stehen in keiner
Chemie für Studierende der Biologie I
 SäureBaseGleichgewichte Es gibt verschiedene Definitionen für SäureBaseReaktionen, an dieser Stelle ist die Definition nach BrønstedLowry, die Übertragung eines H + Ions ( Proton ), gemeint. Nach BrønstedLowry
SäureBaseGleichgewichte Es gibt verschiedene Definitionen für SäureBaseReaktionen, an dieser Stelle ist die Definition nach BrønstedLowry, die Übertragung eines H + Ions ( Proton ), gemeint. Nach BrønstedLowry
Membran- und Donnanpotentiale. (Zusammenfassung)
 Membranund Donnanpotentiale (Zusammenfassung) Inhaltsverzeichnis 1. Elektrochemische Membranen...Seite 2 2. Diffusionspotentiale...Seite 2 3. Donnanpotentiale...Seite 3 4. Zusammenhang der dargestellten
Membranund Donnanpotentiale (Zusammenfassung) Inhaltsverzeichnis 1. Elektrochemische Membranen...Seite 2 2. Diffusionspotentiale...Seite 2 3. Donnanpotentiale...Seite 3 4. Zusammenhang der dargestellten
Thema: Zusammensetzung der Luft
 Staatliches Seminar für Didaktik und Lehrerbildung (RS) Reutlingen Fach: NWA (Biologie) NWA Tag 2008: Die vier Elemente Thema: Zusammensetzung der Luft erarbeitet von: Helen Dünser und Marion Merz Inhaltsverzeichnis
Staatliches Seminar für Didaktik und Lehrerbildung (RS) Reutlingen Fach: NWA (Biologie) NWA Tag 2008: Die vier Elemente Thema: Zusammensetzung der Luft erarbeitet von: Helen Dünser und Marion Merz Inhaltsverzeichnis
Referat : Aufbau v. Proteinen u. ihre Raumstruktur
 Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Referat : Aufbau v. Proteinen u. ihre Raumstruktur 1. Einleitung Unsere Körperzellen enthalten einige Tausend verschiedene Proteine wobei man schätzt, das insgesamt über 50 000 verschiedene Eiweißstoffe
Blutspende Ihre Gesundheit - Unser Thema ist ein Service Ihrer niedergelassenen Ärzte und Psychotherapeuten in Bayern
 Patienteninformation Blutspende Ihre Gesundheit - Unser Thema ist ein Service Ihrer niedergelassenen Ärzte und Psychotherapeuten in Bayern Blut ist ein ganz besondrer Saft!, antwortet Mephisto auf die
Patienteninformation Blutspende Ihre Gesundheit - Unser Thema ist ein Service Ihrer niedergelassenen Ärzte und Psychotherapeuten in Bayern Blut ist ein ganz besondrer Saft!, antwortet Mephisto auf die
Chemische Bindung. Chemische Bindung
 Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
Chemische Bindung Atome verbinden sich zu Molekülen oder Gittern, um eine Edelgaskonfiguration zu erreichen. Es gibt drei verschiedene Arten der chemischen Bindung: Atombindung Chemische Bindung Gesetz
WAS IST DIABETES? 1. Zucker - Kraftstoff des Menschen
 WAS IST DIABETES? 1. Zucker - Kraftstoff des Menschen Traubenzucker liefert Energie Bei jedem Menschen ist ständig eine geringe Menge Traubenzucker (Glukose) im Blut gelöst. Dieser Blutzucker ist der Kraftstoff
WAS IST DIABETES? 1. Zucker - Kraftstoff des Menschen Traubenzucker liefert Energie Bei jedem Menschen ist ständig eine geringe Menge Traubenzucker (Glukose) im Blut gelöst. Dieser Blutzucker ist der Kraftstoff
Ratgeber für Patienten mit metabolischer Azidose. Metabolische Azidose. Informationen, Hintergründe und praktische Tipps TIPPS.
 Ratgeber für Patienten mit metabolischer Azidose Metabolische Azidose Informationen, Hintergründe und praktische Tipps TIPPS Ein Service von a 4 6 8 10 12 14 Inhalt Inhalt Was ist eine metabolische Azidose?
Ratgeber für Patienten mit metabolischer Azidose Metabolische Azidose Informationen, Hintergründe und praktische Tipps TIPPS Ein Service von a 4 6 8 10 12 14 Inhalt Inhalt Was ist eine metabolische Azidose?
4.1. Atmung und Lunge. Sauerstofftransport. Gasaustausch in den Lungenbläschen (Alveolen)
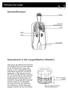 4.1 Sauerstofftransport GEHIRN LUNGE MIT LUNGENBLÄSCHEN HERZ LEBER NIERE SCHLAGADER Gasaustausch in den Lungenbläschen (Alveolen) Jedes Organ, jede Zelle braucht Sauerstoff zur Energiegewinnung. Der Sauerstoff
4.1 Sauerstofftransport GEHIRN LUNGE MIT LUNGENBLÄSCHEN HERZ LEBER NIERE SCHLAGADER Gasaustausch in den Lungenbläschen (Alveolen) Jedes Organ, jede Zelle braucht Sauerstoff zur Energiegewinnung. Der Sauerstoff
1. Luft ist mehr als nichts
 1. Luft ist mehr als nichts 1.1 Concept Cartoon - Luft Luft Als Luft bezeichnet man das der Erdatmosphäre. Sie besteht hauptsächlich aus den beiden Gasen (ca. 78%) und (ca. 21%). Die Luft ist im natürlichen
1. Luft ist mehr als nichts 1.1 Concept Cartoon - Luft Luft Als Luft bezeichnet man das der Erdatmosphäre. Sie besteht hauptsächlich aus den beiden Gasen (ca. 78%) und (ca. 21%). Die Luft ist im natürlichen
Che1 P / CheU P Praktikum Allgemeine und Anorganische Chemie. Gasmessung. 15. September 2008
 15. September 2008 1 1 Aufgabe und Lernziele... 3 2 Vorbereitung... 3 3 Einführung... 4 3.1 Grundlagen... 4 3.1.1Kohlenstoffdioxid... 4 3.2.2 Luftuntersuchungen mit Prüfröhrchen... 4 4 Praxis... 5 4.1
15. September 2008 1 1 Aufgabe und Lernziele... 3 2 Vorbereitung... 3 3 Einführung... 4 3.1 Grundlagen... 4 3.1.1Kohlenstoffdioxid... 4 3.2.2 Luftuntersuchungen mit Prüfröhrchen... 4 4 Praxis... 5 4.1
10.1 Was bedeutet Stoffwechsel? 10.2 Was sind Enzyme? 10.3 Welche Aufgabe erfüllen die Organe des Verdauungsapparats?
 10.1 Was bedeutet Stoffwechsel? Stoffwechsel Gesamtheit der Vorgänge der Stoffaufnahme, Stoffumwandlung und Stoffabgabe in lebenden Zellen (immer auch mit Energiewechsel verbunden) Energiestoffwechsel:
10.1 Was bedeutet Stoffwechsel? Stoffwechsel Gesamtheit der Vorgänge der Stoffaufnahme, Stoffumwandlung und Stoffabgabe in lebenden Zellen (immer auch mit Energiewechsel verbunden) Energiestoffwechsel:
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
2.9 Reaktion von Laugen mit Aluminium - Laugenstärke. Aufgabe. Gibt es verschieden starke Laugen?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7159300) 2.9 Reaktion von Laugen mit Aluminium - Laugenstärke Experiment von: Phywe Gedruckt: 15.10.2013 12:17:12 intertess (Version 13.06
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7159300) 2.9 Reaktion von Laugen mit Aluminium - Laugenstärke Experiment von: Phywe Gedruckt: 15.10.2013 12:17:12 intertess (Version 13.06
Dichtung und Wahrheit beim Säure-Basen-Haushalt
 Dichtung und Wahrheit beim Säure-Basen-Haushalt Diplombiologe Dr. er. nat. Martin Diefenbach Medizinische Information DRELUSO-Pharmazeutika Dr. Elten & Sohn GmbH Markt 5 31840 Hess. Oldendorf Mai 2008
Dichtung und Wahrheit beim Säure-Basen-Haushalt Diplombiologe Dr. er. nat. Martin Diefenbach Medizinische Information DRELUSO-Pharmazeutika Dr. Elten & Sohn GmbH Markt 5 31840 Hess. Oldendorf Mai 2008
Untersuchung der Absorption von Schwermetallen und Ammonium durch MAC
 Wolferner Analytik GmbH Untersuchung der Absorption von Schwermetallen und Ammonium durch MAC 1 Veröffentlichung 15.12.2004, Studie Zusammenfassung: Im Auftrag der ASTRA GmbH, einer Vorgesellschaft der
Wolferner Analytik GmbH Untersuchung der Absorption von Schwermetallen und Ammonium durch MAC 1 Veröffentlichung 15.12.2004, Studie Zusammenfassung: Im Auftrag der ASTRA GmbH, einer Vorgesellschaft der
Western Blot. Zuerst wird ein Proteingemisch mit Hilfe einer Gel-Elektrophorese aufgetrennt.
 Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
Western Blot Der Western Blot ist eine analytische Methode zum Nachweis bestimmter Proteine in einer Probe. Der Nachweis erfolgt mit spezifischen Antikörpern, die das gesuchte Protein erkennen und daran
ÜBUNGSBEISPIELE Beispiel 1.
 ÜBUNGSBEISPIELE Beispiel 1. Wieviele Ladungen sind für das Ruhepotentialpotential von -70 mv nötig?? Zusatzinfo: Membrankondensator 0.01F/m 2 a) Wieviele K + Ionen sind dies pro m 2?? Eine typische Zelle
ÜBUNGSBEISPIELE Beispiel 1. Wieviele Ladungen sind für das Ruhepotentialpotential von -70 mv nötig?? Zusatzinfo: Membrankondensator 0.01F/m 2 a) Wieviele K + Ionen sind dies pro m 2?? Eine typische Zelle
Quelle: Natur und Technik, PCB 7, 1997. ATMUNG bis
 Quelle: Natur und Technik, PCB 7, 1997 ATMUNG bis Aufgabe 1 Finde eine passende Überschrift für den gesamten Text. Aufgabe 2 Welche der folgenden Überschriften passt am besten zu den einzelnen Teilabschnitten
Quelle: Natur und Technik, PCB 7, 1997 ATMUNG bis Aufgabe 1 Finde eine passende Überschrift für den gesamten Text. Aufgabe 2 Welche der folgenden Überschriften passt am besten zu den einzelnen Teilabschnitten
Welches Mischverhältnis wird beim Schweissen am Brenner eingestellt? Begründe.
 Wie nennt man das Gasschmelzschweissen auch noch? Welches Mischverhältnis wird beim Schweissen am Brenner eingestellt? Begründe. Wie wird Acetylen in der Flasche gespeichert, damit es nicht bei 2bar explodiert?
Wie nennt man das Gasschmelzschweissen auch noch? Welches Mischverhältnis wird beim Schweissen am Brenner eingestellt? Begründe. Wie wird Acetylen in der Flasche gespeichert, damit es nicht bei 2bar explodiert?
Für Patientinnen und Patienten. Blutdruckpass. Die mit dem Regenbogen
 Für Patientinnen und Patienten Blutdruckpass Die mit dem Regenbogen Patientendaten Vorname Name Geburtsdatum Adresse Strasse Hausnummer PLZ Stadt Tel. Nr. Allergien Medikamentenunverträglichkeit Andere
Für Patientinnen und Patienten Blutdruckpass Die mit dem Regenbogen Patientendaten Vorname Name Geburtsdatum Adresse Strasse Hausnummer PLZ Stadt Tel. Nr. Allergien Medikamentenunverträglichkeit Andere
Wasser löst fast alles
 1 Wasser löst fast alles In manchen Regionen ist das Wasser ganz schön hart. Nicht, dass Steine aus der Dusche fallen, wie in diesem Cartoon; aber durch Verdunsten oder Verdampfen von Wasser können Ablagerungen
1 Wasser löst fast alles In manchen Regionen ist das Wasser ganz schön hart. Nicht, dass Steine aus der Dusche fallen, wie in diesem Cartoon; aber durch Verdunsten oder Verdampfen von Wasser können Ablagerungen
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2
 Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Übungen zur VL Chemie für Biologen und Humanbiologen 04.11.2011 Lösung Übung 2 1. Wie viel mol Eisen sind in 12 x 10 23 Molekülen enthalten? ca. 2 Mol 2. Welches Volumen Litern ergibt sich wenn ich 3 mol
Wasserchemie und Wasseranalytik SS 2015
 Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
Wasserchemie und Wasseranalytik SS 015 Übung zum Vorlesungsblock II Wasserchemie Dr.-Ing. Katrin Bauerfeld 5,5 6,5 7,5 8,5 9,5 10,5 11,5 1,5 13,5 Anteile [%] Übungsaufgaben zu Block II Wasserchemie 1.
1/6. Welche Antwort ist richtig: Wie entsteht aus organischen Kohlenstoffverbindungen das gasförmige Kohlendioxid?
 1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
Stickstoff plus Sauerstoff = Nitrox?
 Inhalt Stickstoff plus Sauerstoff = Nitrox? Diese Präsentation wurde bei der TSVÖ Tauchlehrertagung 2015 in Traunkirchen vorgetragen. Markus A. Schafheutle ([email protected]) Unsere Atemluft,
Inhalt Stickstoff plus Sauerstoff = Nitrox? Diese Präsentation wurde bei der TSVÖ Tauchlehrertagung 2015 in Traunkirchen vorgetragen. Markus A. Schafheutle ([email protected]) Unsere Atemluft,
Fachforum Radon in Wohngebäuden 27.06.2012
 Fachforum Radon in Wohngebäuden 27.06.2012 Dr. Simone Körner Woher kommt das Radon? 2 Ursprung der natürlichen Strahlung Sternenexplosion vor 6 7 Milliarden Jahren kosmische Strahlung Bildung aller Elemente
Fachforum Radon in Wohngebäuden 27.06.2012 Dr. Simone Körner Woher kommt das Radon? 2 Ursprung der natürlichen Strahlung Sternenexplosion vor 6 7 Milliarden Jahren kosmische Strahlung Bildung aller Elemente
7. Woche. Gesamtanalyse (Vollanalyse) einfacher Salze. Qualitative Analyse anorganischer Verbindungen
 7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
7. Woche Gesamtanalyse (Vollanalyse) einfacher Salze Qualitative Analyse anorganischer Verbindungen Die qualitative Analyse ist ein Teil der analytischen Chemie, der sich mit der qualitativen Zusammensetzung
Aufgaben aus der Chemie und Lösungsstrategien
 Aufgaben aus der Chemie und Lösungsstrategien Einfache Reproduktion Abfrage von gelerntem Wissen, also wird die Wiedergabe von Definitionen, Aussagen oder Tatsachen gefordert. Kennzeichen: Keine Einleitung
Aufgaben aus der Chemie und Lösungsstrategien Einfache Reproduktion Abfrage von gelerntem Wissen, also wird die Wiedergabe von Definitionen, Aussagen oder Tatsachen gefordert. Kennzeichen: Keine Einleitung
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Abwehrender Brandschutz Folien Online
 Abwehrender Brandschutz Folien Online Abwehrenden Brandschutz einfach und mühelos unterweisen 1. Auflage WEKA 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 8111 4421 7 schnell und portofrei
Abwehrender Brandschutz Folien Online Abwehrenden Brandschutz einfach und mühelos unterweisen 1. Auflage WEKA 2007 Verlag C.H. Beck im Internet: www.beck.de ISBN 978 3 8111 4421 7 schnell und portofrei
Bilanzgleichung der i-ten Komponente eines Systems mit r Reaktionen
 3.5 Die chemische Produktionsdichte Bilanzgleichung der i-ten Komponente eines Systems mit r Reaktionen und mit folgt Die rechte Seite der Gleichung wird als chemische Produktionsdichte bezeichnet: Sie
3.5 Die chemische Produktionsdichte Bilanzgleichung der i-ten Komponente eines Systems mit r Reaktionen und mit folgt Die rechte Seite der Gleichung wird als chemische Produktionsdichte bezeichnet: Sie
Der Stoff, der Leben möglich macht.
 Der Stoff, der Leben möglich macht. Eine Information über die Sauerstoff-Langzeittherapie 3 Alles über Sauerstoff... 4 Was ist Sauerstoff?...5 Woher kommt der Sauerstoff?...6 Woher kommt der Sauerstoff,
Der Stoff, der Leben möglich macht. Eine Information über die Sauerstoff-Langzeittherapie 3 Alles über Sauerstoff... 4 Was ist Sauerstoff?...5 Woher kommt der Sauerstoff?...6 Woher kommt der Sauerstoff,
Münze auf Wasser: Resultierende F gegen Münze: Wegrdrängen der. der Moleküle aus Oberfl. analog zu Gummihaut.
 5.3 Oberflächenspannung mewae/aktscr/kap5_3_oberflsp/kap5_3_s4.tex 20031214 Anziehende Molekularkräfte (ànm) zwischen Molekülen des gleichen Stoffes: Kohäsionskräfte,...verschiedene Stoffe: Adhäsionskräfte
5.3 Oberflächenspannung mewae/aktscr/kap5_3_oberflsp/kap5_3_s4.tex 20031214 Anziehende Molekularkräfte (ànm) zwischen Molekülen des gleichen Stoffes: Kohäsionskräfte,...verschiedene Stoffe: Adhäsionskräfte
