RePneuTM Coil-System (zur Lungenvolumenreduktion)
|
|
|
- Johann Bieber
- vor 6 Jahren
- Abrufe
Transkript
1 RePneuTM Coil-System (zur Lungenvolumenreduktion) GEBRAUCHSANWEISUNG 1 MPS Medical Product Service GmbH Borngasse Braunfels Deutschland Tel.: (+49) Fax: (+49) PneumRx, Inc Burton Drive Santa Clara, CA USA Tel.: (+1) Fax: (+1)
2 Inhaltsverzeichnis 1.0 Produktbeschreibung Indikationen Kontraindikationen Warnhinweise Warnhinweise zum klinischen Einsatz Allgemeine Warnhinweise Warnhinweise zur REPNEU Coil und zum Einführsystem Vorsichtsmaßnahmen Allgemeine Vorsichtsmaßnahmen Verfahrensspezifische Vorsichtsmaßnahmen Individuelle Anpassung der Behandlung Einsatz bei besonderen Patientengruppen Mögliche unerwünschte Ereignisse Informationen zum klinischen Einsatz Erforderliche Materialien Periprozedurale Betreuung Informationen für Patienten Implantatausweis für den Patienten und Patientenbroschüre Sicherheitsrelevante Informationen zur magnetresonanztomografischen Bildgebung (MRT) Lieferform und Aufbewahrung Einführsystem Coil Aufbewahrung Gebrauchsanweisungen Umpositionierung von Coils nach der Freisetzung Bronchoskopische Coil-Entfernung nach der Implantation Garantieausschluss Handelsmarken Erläuterung der Produktkennzeichnungssymbole... 21
3 1.0 Produktbeschreibung Das endobronchiale PneumRx RePneu Coil-System (auch REPNEU System genannt) besteht aus zwei Hauptkomponenten: sterilen endobronchialen REPNEU Coils (auch REPNEU Coil oder Coils genannt) und einem zur einmaligen Anwendung vorgesehenen, sterilen endobronchialen REPNEU Einführsystem (auch Einführsystem genannt). Die implantierbaren Coils aus Nitinol mit Formgedächtnis sind dazu ausgelegt, die Lungenfunktion bei Patienten mit einem fortgeschrittenen homogenen und/oder heterogenen Lungenemphysem durch die Wiederherstellung der Atemwegsdurchgängigkeit und die Reduzierung des Kollabierens (Zusammenfallens) der Atemwege beim Ausatmen sowie bei körperlicher Betätigung zu verbessern. Das REPNEU System wird zusammen mit einem therapeutischen Bronchoskop mit einem 2,8-mm-Arbeitskanal unter Fluoroskopie verwendet, um mithilfe eines minimalinvasiven Ansatzes, bei dem keine Inzision erforderlich ist, mehrere Coils in die Lunge einzubringen. Jede Nitinol-Coil ist so ausgelegt, dass sie nach der Implantation in die subsegmentalen Atemwege der Lunge geschädigtes Lungengewebe rafft und komprimiert und so dem Atemwegssystem wieder Spannung verleiht, um die Rückstellkraft der emphysematös veränderten Lunge auf mechanische Art und Weise zu steigern. So können das Kollabieren der Atemwege und Lufteinschlüsse verringert und gleichzeitig Luft in gesündere Lungenbereiche umgeleitet werden. Um unterschiedlichen Atemwegslängen gerecht zu werden, sind die Coils in mehreren Größen erhältlich. Das REPNEU Einführsystem umfasst einen Führungsdraht, eine Einführhülse, einen Katheter und eine Fasszange. Der Führungsdraht leitet den Katheter zum Atemweg und erleichtert die Auswahl der geeigneten Coil-Länge. Die Einführhülse stellt die Verbindung zum Katheter her und begradigt die Coil vorübergehend, wodurch das Vorschieben der Coil in den Katheter erleichtert wird. Mit dem Katheter wird die begradigte Coil durch das Bronchoskop in den zu behandelnden Atemweg eingebracht. Mit der Fasszange wird das proximale Ende der Coil gefasst, um sie durch den Katheter in den zu behandelnden Atemweg einzubringen, wo die Coil bei der Freisetzung am zu behandelnden Gewebesitus wieder ihre vorbestimmte Form annimmt. Bei Bedarf können der Katheter und die Fasszange auch beim Entfernen und/ oder Umpositionieren der Coil eingesetzt werden. Die Einbringung mehrerer Coils in einen Patienten im Rahmen einer Behandlung erfolgt unter Verwendung eines einzigen Einführsystems. Die REPNEU Coils sind in drei Größen verfügbar: Nr. 1 (100 mm Länge), Nr. 2 (125 mm Länge) und Nr. 3 (150 mm Länge). Jede Coil ist einzeln in einem Kunststoffschutzgehäuse verpackt, das in einen Beutel und dann einen Karton gelegt wird, und ist per Elektronenstrahl (E-Strahl) sterilisiert. Die Komponenten des Einführsystems werden zusammen in einem Beutel und dann in einem Karton verpackt und mittels Ethylenoxidgas (EtO) sterilisiert. 3
4 distale Kugel proximale Kugel Coil Luer-Lock- Ende Einführhülse proximales Ende proximales Ende Führungsdraht Spitze Luer-Lock- Ansatz Katheter Spitze am distalen Ende Backen Fasszange Abbildung 1: Komponenten des REPNEU Systems 2.0 Indikationen Das endobronchiale REPNEU Coil-System ist zur Verwendung bei Patienten mit einem fortgeschrittenen homogenen und/oder heterogenen Lungenemphysem zur Verbesserung der Lebensqualität, Lungenfunktion und körperlichen Belastbarkeit indiziert. 3.0 Kontraindikationen Für das endobronchiale REPNEU Coil-System gelten folgende Kontraindikationen: Patienten mit einer bekannten Empfindlichkeit gegenüber Medikamenten, die für die Durchführung einer Bronchoskopie erforderlich sind, oder Patienten, bei denen Bronchoskopien kontraindiziert sind Patienten mit Anzeichen einer aktiven Lungeninfektion Patienten mit einer Überempfindlichkeit oder Allergie gegen Nitinol (Nickel-Titan) oder gegen seine metallenen Bestandteile Patienten mit klinisch signifikanten Gerinnungsstörungen Patienten mit klinisch signifikanter Lungenfibrose Patienten mit Riesenbullae > 1/3 des Lungenvolumens Patienten mit klinisch signifikanten generalisierten Bronchiektasen Patienten mit schwerer pulmonaler Hypertonie, charakterisiert durch einen rechtsventrikulären systolischen Druck von > 50 mmhg (bevorzugte Bestimmung durch Rechtsherzkatheterisierung) Patienten mit Gefäßen, die bei visueller Begutachtung die Größe benachbarter Luftwege überschreiten (Potenzial für eine schwere pulmonale Hypertonie) Patienten unter Immunsuppression zur Behandlung von Krebs, rheumatoider Arthritis, Autoimmunerkrankungen oder zur Verhinderung einer Gewebe- oder Organabstoßung Patienten, die täglich > 20 mg Prednison (oder eine äquivalente Dosis eines vergleichbaren Steroids) einnehmen 4
5 4.0 Warnhinweise 4.1 Warnhinweise zum klinischen Einsatz Das REPNEU System darf nur von Ärzten verwendet werden, die im Umgang mit therapeutischen Bronchoskopen versiert und entsprechend darin geschult sind. Benutzer müssen mit den Prinzipien, klinischen Anwendungen, Komplikationen, Nebenwirkungen und Gefahren, die gewöhnlich mit interventionellen Pneumologie- Verfahren sowie mit dem endobronchialen REPNEU Coil-Verfahren einhergehen, vertraut sein Allgemeine Warnhinweise Die Hämoptyse ist eine bekannte Komplikation der Coil-Therapie sowie diagnostischer und interventioneller Bronchoskopien generell. In seltenen Fällen kam es bei Patienten, die sich einer Coil-Therapie unterzogen haben, zu einer tödlichen Hämoptyse. Aus diesem Grund ist die Anwendung von Antikoagulanzien bei Patienten, die sich einer Coil-Therapie unterziehen, sorgsam abzuwägen, da sie eventuell mit einem erhöhten Blutungsrisiko einhergeht. o Zur Verringerung des Risikos von schwerwiegenden pulmonalen Blutungsereignissen ist eine Antithrombozytentherapie (z. B. Aspirin, Clopidogrel) bzw. eine Antikoagulanzientherapie (z. B. Warfarin, NOAC) für den Zeitraum von sieben (7) Tagen vor und sieben (7) Tagen nach der Coil-Implantation bzw. entsprechend der Empfehlung des Pharmaherstellers auszusetzen. o Die Vorteile und Risiken der Einleitung oder der fortgesetzten Anwendung von Thrombozytenaggregationshemmern bzw. Antikoagulanzien bei Patienten, die sich einer Coil-Therapie unterzogen haben, sind mit Bedacht abzuwägen. Die REPNEU Coils dürfen nicht in Lungenbereichen implantiert werden, die Bronchiektasen oder eine signifikante Atelektase aufweisen. Um das Risiko von schwerwiegenden pulmonalen Blutungsereignissen zu verringern, ist eine Coil-Implantation bei Patienten mit Bronchiektasen nur nach sorgsamer Überlegung durchzuführen. Dabei sind alle verdächtigen Lungenbereiche zu vermeiden. Es ist besonders umsichtig vorzugehen, wenn in Erwägung gezogen wird, REPNEU Coils bei Patienten mit einem DLCO-Wert < 20 % des Sollwerts zu implantieren, da die Sicherheit und Wirksamkeit der Therapie mit dem REPNEU System in diesen Patientenpopulationen nicht untersucht wurde. Es ist besonders umsichtig vorzugehen, wenn die Behandlung von Patienten mit verdächtigen oder gesicherten kanzerösen Lungenknötchen oder nachweislichem Vorliegen anderer schwerer Erkrankungen oder Lungenleiden in Erwägung gezogen wird, die das Überleben des Patienten nach der Behandlung oder die Wahrscheinlichkeit des Patienten, von der REPNEU Coil-Therapie zu profitieren, gefährden könnten. 4.3 Warnhinweise zur REPNEU Coil und zum Einführsystem Den Katheter nicht ohne Abstützung durch den Führungsdraht vorschieben. Beim Vorschieben des Katheters stets den Führungsdraht verwenden. Die Komponenten des REPNEU Systems nur unter Fluoroskopie aus dem Sichtbereich des Bronchoskops herausschieben. Das Fluoroskop einschalten, wenn der schwarze proximale Markierungsstreifen der Fasszange in die Einführhülse eintritt. Um eine Punktion der Pleura oder ein Atemwegstrauma zu vermeiden, den Führungsdraht, den Katheter oder alle anderen Komponenten des REPNEU Systems auf keinen Fall gegen Widerstand vorschieben. Wird auf Widerstand gestoßen, die Ursache hierfür bestimmen und entsprechende Abhilfemaßnahmen ergreifen, bevor ein Vorschieben der REPNEU Systemkomponente erneut versucht wird. Die bronchoskopische Coil-Entfernung muss medizinisch angezeigt sein. Der mögliche Nutzen einer Coil-Entfernung muss gegen den möglichen Schaden, einschließlich der bekannten Risiken der Bronchoskopie, abgewogen werden. Die bronchoskopische Coil-Entfernung kann sich 2 oder mehr Monate nach der Implantation je nach Umfang des vorhandenen Granulationsgewebes zunehmend schwierig gestalten. Siehe Abschnitt 13.0 Bronchoskopische Coil-Entfernung nach der Implantation für weitere Informationen zur Behandlung.
6 Ist eine Coil-Entfernung notwendig, darf nicht versucht werden, die Coil auf irgendeine Art und Weise zu durchtrennen, zu verbiegen oder zu brechen. Ein unsachgemäßer Umgang mit der Coil auf eine solche Art und Weise kann dazu führen, dass das Produkt korrodiert und scharfe Oberflächen entstehen, die eine Gesundheitsschädigung, Erkrankung oder den Tod des Patienten zur Folge haben können. Die Komponenten des REPNEU Systems auf keine Art und Weise wiederverwenden, aufbereiten, reinigen oder erneut sterilisieren. Eine Wiederverwendung, Aufbereitung oder erneute Sterilisation mittels Bestrahlung, Dampf, Ethylenoxid oder anderen chemischen Sterilisationsmitteln kann die strukturelle Integrität des Produkts beeinträchtigen und/oder zu einem Produktversagen führen sowie die Gefahr einer Kontamination des Produkts nach sich ziehen und/oder eine Infektion bzw. Kreuzinfektion des Patienten verursachen, darunter u. a. die Übertragung von Infektionskrankheiten von einem Patienten auf den anderen. Eine Kontamination des Produkts kann eine Verletzung, Erkrankung oder den Tod des Patienten nach sich ziehen. Die Komponenten des REPNEU Systems nicht verwenden, wenn der Karton bei Erhalt beschädigt ist. Vor dem Öffnen des Beutels stets die Beutelversiegelungen inspizieren. Die Komponenten des REPNEU Systems nicht verwenden, wenn der Beutel geöffnet oder beschädigt ist, da in einem solchen Fall die Funktionalität und/oder Sterilität des Produkts beeinträchtigt sein können. Die Verwendung nicht steriler oder beschädigter Produkte kann beim Patienten zu Gesundheitsschädigungen führen. Die Komponenten des REPNEU Systems nicht verwenden, wenn die manipulationssichere Versiegelung geöffnet wurde, das auf der Verpackung angegebene Verfallsdatum ( Verwendbar bis ) abgelaufen ist oder das Produkt heruntergefallen ist oder beschädigt wurde. Ein beschädigtes Produkt auf keinen Fall reparieren. Wird ein Schaden festgestellt, das Produkt entsorgen und den PneumRx-Ansprechpartner anrufen, um ein Ersatzprodukt anzufordern. Das REPNEU System nicht verwenden, wenn das Etikett unvollständig oder nicht lesbar ist. Informationen zur geltenden Zweckbestimmung, zu Kontraindikationen, Warn- und Vorsichtshinweisen und möglichen Komplikationen sind der Gebrauchsanweisung, die den mit dem REPNEU System zu verwendenden Zubehörteilen beiliegt, zu entnehmen. Nach der Verwendung das Produkt und die Verpackung gemäß den Krankenhaus-, Verwaltungs- und/oder örtlichen Behördenvorschriften entsorgen. 5.0 Vorsichtsmaßnahmen Allgemeine Vorsichtsmaßnahmen Vor dem Gebrauch des REPNEU Systems alle Anweisungen sorgfältig durchlesen. Alle in dieser Gebrauchsanweisung enthaltenen Kontraindikationen, Warnhinweise und Vorsichtsmaßnahmen beachten. Ein Missachten der Gebrauchsanweisung kann zu einem erhöhten Risiko von nachteiligen gesundheitlichen Auswirkungen für den Patienten, verfahrensbezogenen Problemen, Komplikationen oder Schäden am Produkt führen. Bei der endobronchialen REPNEU Coil-Behandlung handelt es sich um eine bilaterale Therapie, die in separaten Sitzungen durchzuführen ist. Das Einführsystem darf nicht mit organischen Lösemitteln (Alkohol) in Kontakt kommen, da dadurch die strukturelle Integrität und/oder die Funktionsfähigkeit des Produkts beeinträchtigt werden könnten. 5.2 Verfahrensspezifische Vorsichtsmaßnahmen Die Behandlung stets mit einem Bronchoskop durchführen. Das REPNEU System ist zur Verwendung mit einem therapeutischen Bronchoskop mit einem Arbeitskanal mit einem Innendurchmesser von 2,8 mm und einer Nutzlänge von maximal 65 cm bestimmt. Eine Verwendung des REPNEU Systems mit Bronchoskopen, die diesen Kriterien nicht entsprechen, kann zu Geräte- oder Produktschäden führen. Coils dürfen nur unter Fluoroskopie eingebracht werden. Wenn die Komponenten des Einführsystems außerhalb des Sichtbereichs des Bronchoskops liegen, dürfen sie nur unter Fluoroskopie bewegt werden.
7 Coils so platzieren, dass sie sich nicht berühren und sich nicht gegenseitig überlappen. Große Sorgfalt walten lassen, damit nicht zwei Coils in denselben Atemweg platziert werden. Geknickte Einführsysteme oder geknickte Coils nicht verwenden. Wenn sich der Führungsdraht außerhalb des Sichtbereichs des Bronchoskops befindet, den Führungsdraht unter Fluoroskopie visualisieren. Bei Eintreten des Fluoroskopie- Markierungsstreifens des Führungsdrahts in den Katheteransatz das Fluoroskop einschalten. Den Führungsdraht nicht gegen Widerstand vorschieben. Wird der Führungsdraht bei erhöhtem Widerstand über eine plötzlich auftretende Krümmung in einem distalen Atemweg hinaus vorgeschoben, kann dies dazu führen, dass im gekrümmten Abschnitt des Führungsdrahts Gewebe hängenbleibt. Das Fluoroskop muss eingeschaltet bleiben, um sicherzustellen, dass sich der Führungsdraht während des Kathetervorschubs nicht bewegt. Den Katheter nicht über den Führungsdraht schieben, wenn der Führungsdraht einen spitzen Winkel einnimmt. Lässt sich der Katheter nicht zum distalen Ende des Führungsdrahts vorschieben, den Führungsdraht zurückziehen, bis er mit der Katheterspitze ausgerichtet ist. Bei erhöhtem Widerstand den Katheter nicht über den Draht schieben. Beim Laden einer Coil die Backen der Fasszange oder die Coil nicht aus dem proximalen Ende der Einführhülse ziehen. Ein Zurückschieben der Coil in die Einführhülse kann zu Schäden an der Coil führen. In einem solchen Fall die Coil nicht verwenden. Die Coil nicht verwenden, wenn sie heruntergefallen ist oder sich aus irgendeinem Grund außerhalb des Kunststoffschutzgehäuses befindet. Die Fasszange in maximal 5 cm Entfernung vom proximalen Ende der Einführhülse fassen, um ein Abknicken beim Vorschieben zu vermeiden. Die Bronchoskop-Position während der Freisetzung nicht verändern. Die Backen der Fasszange lassen sich nicht öffnen, wenn sie sich im Katheter befinden. Sie müssen mindestens 1 cm über die distale Spitze des Katheters und des Bronchoskops hinausragen, um die Coil freizusetzen. Die Coil nicht wiederverwenden, wenn ihre Entfernung als separates Verfahren und nicht im Rahmen der Coil-Platzierung vorgenommen wurde. Die Coil kann wiederverwendet werden, wenn sie während der ursprünglichen Bronchoskopie zum Zweck der Coil-Platzierung entfernt und erneut freigesetzt wurde. 6.0 Individuelle Anpassung der Behandlung Vor dem Gebrauch des REPNEU Systems sind die Risiken und Nutzen für jeden einzelnen Patienten abzuwägen. Faktoren in Bezug auf die Patientenwahl, wie z. B. Komorbiditäten des Patienten sowie wichtige Risikofaktoren, darunter Antithrombozyten- oder Antikoagulationstherapie, sind abzuwägen. Bei der Abwägung einer Behandlung von Patienten mit einem homogenen Lungenemphysem in Kombination mit weniger schweren Lufteinschlüssen besondere Sorgfalt walten lassen. Eine Post-hoc-Analyse dieser Untergruppe in der RENEW Studie hat eine Verschlechterung des medianen Werts bei dem 6-Minuten-Gehtest ergeben, obwohl diese Veränderung nicht statistisch signifikant war. 1 7 Das REPNEU System ist mit Vorsicht und nur nach sorgsamer Überlegung anzuwenden, besonders bei Patienten mit folgenden Gegebenheiten: - häufig auftretenden, wiederholten, klinisch signifikanten Atemwegsinfekten in der Vorgeschichte - Hyperkapnie - nicht kontrollierter oder schwerer Herzinsuffizienz oder kürzlich erlittenem Myokardinfarkt - niedriger FEV 1 1 Sciurba FC et al. JAMA 2016; 315:
8 6.1 Einsatz bei besonderen Patientengruppen Die Sicherheit und Wirksamkeit der Behandlung mit dem REPNEU System wurden bei den folgenden Patientengruppen nicht untersucht: schwangere oder stillende Frauen Patienten, die das Rauchen nicht aufgegeben haben Patienten mit FEV 1 > 45 % des Sollwerts Patienten mit früherer Lungenvolumenreduktions-OP oder Lobektomie Patienten mit Alpha-1-Antitrypsin-Mangel Patienten mit Residualvolumen (RV) < 175 %/Soll Patienten mit wenig sichtbarer Parenchymstruktur auf dem CT Patienten mit schweren Gasaustauschstörungen, definiert als PaCO 2 > 55 mmhg oder PaO 2 < 45 mmhg unter Raumluft (Höhenlagekriterium: PaO 2 < 30 mmhg) 7.0 Mögliche unerwünschte Ereignisse Zu den unerwünschten Ereignissen, die eventuell bei endobronchialen Produkten, Systemen zur Platzierung dieser Produkte und damit verbundenen Verfahren (einschließlich diagnostischer und bronchoskopischer Verfahren) sowie bei der Verwendung des REPNEU Systems auftreten, gehören u. a. die nachstehend aufgeführten Ereignisse. Diese Ereignisse können sich in Bezug auf Häufigkeit und Schweregrad unterscheiden. allergische Reaktion Aspiration Blutung oder Hemorrhagie Blutgerinnsel in den Bronchien Ulzeration der Bronchien Bronchospasmus Herzrhythmusstörungen COPD-Exazerbation Husten Ableben Verlagerung des Produkts Dyspnoe Emphysem, subkutan Hämoptyse, einschließlich schwerer Hämoptyse Heiserkeit Hypertonie Hypotonie Infektion Entzündung Schmerzen Schmerzhafte Atmung Pleuraerguss Pleurafistel Pneumonie* Pneumothorax mit dem Verfahren in Verbindung stehende Komplikationen (z. B. Fieber, Krämpfe) Lungenembolie Atemnot respiratorische Insuffizienz Infektion der Atemwege mit der Sedierung in Verbindung stehende Komplikationen (z. B. Übelkeit, Erbrechen, Kopfschmerzen) Sepsis Gewebereaktion, lokalisiert (auch bekannt als Coil Associated Opacity* [Spannungsinduzierte Gewebsverdichtung]) Gewebetrauma, prozedural (z. B. Gewebeperforation, -dissektion) Hinweis: Eventuell sind weitere interventionelle Verfahren notwendig, wenn bei Patienten einige dieser möglichen unerwünschten Ereignisse nach der REPNEU Coil-Therapie auftreten. * Es sind Fälle einer nicht infektiösen, lokalisierten Gewebereaktion, auch Coil Associated Opacity (CAO) genannt, im Bereich der implantierten REPNEU Coils dokumentiert. Hierbei handelt es sich vermutlich um eine entzündliche Reaktion, die mit pneumonie-ähnlichen Symptomen, u. a. mit Thorax- oder Pleuraschmerzen/-beschwerden, verstärkter Dyspnoe, Erschöpfung und/oder sichtbaren Verschattungen oder Infiltraten in Thorax-Röntgenaufnahmen auftreten kann und sich nur schwer von einer Pneumonie abgrenzen lässt. Daher sind Patienten bei der Entlassung anzuweisen, sich an den implantierenden Arzt zu wenden, falls sich bei ihnen Symptome einstellen, die eventuell auf eine Pneumonie oder CAO hindeuten können. 8
9 8.0 Informationen zum klinischen Einsatz Die folgenden Anweisungen sind als allgemeiner informativer Leitfaden für die sichere, wirksame Anwendung des REPNEU Systems gedacht. Bei Verwendung des REPNEU Systems muss sich das ärztliche Personal, auch hinsichtlich der aktuellen Vorschriften zur sterilen Arbeitsweise und zu interventionellen Techniken, stets auf seine klinische Erfahrung und sein Ermessen stützen. 8.1 Erforderliche Materialien Die folgenden zusätzlichen Materialien sind zur Durchführung der endobronchialen REPNEU Coil-Behandlung erforderlich: therapeutisches Bronchoskop mit einem Arbeitskanal mit einem Innendurchmesser von 2,8 mm und einer Nutzlänge von maximal 65 cm Fluoroskop sterile Kochsalzlösung hochrandige Wanne oder großer Tisch mit Kante zur sicheren Ablage des aufgerollten Führungsdrahts und der Fasszange, wenn sich diese nicht in Gebrauch befinden ausreichend Platz zur Handhabung der Komponenten des REPNEU Systems, darunter Platz für das Produkt und zum Laden der Coil in die Einführhülse 8.2 Periprozedurale Betreuung Nach sorgfältiger Untersuchung und Abwägung, um sicherzustellen, dass der Patient ein geeigneter Kandidat für das REPNEU System ist, ist die Behandlung anzuberaumen. Während der Behandlungsplanung können Computertomografie (CT) oder andere entsprechende Methoden zur Untersuchung von emphysematös verändertem Lungengewebe herangezogen werden, um die für die Therapie am besten geeigneten Lungenlappen zu bestimmen. Antibiotika sollten am Tag der Behandlung und mindestens sieben (7) Tage lang nach der Behandlung prophylaktisch eingenommen werden. Die Einnahme von Steroiden zwei (2) Tage vor und mindestens (7) Tage nach der Behandlung wird empfohlen. Röntgendurchleuchtungen vornehmen und den Patienten gemäß krankenhausüblicher Praxis auf die Bronchoskopie vorbereiten. Nach der Behandlung den Patienten von der Narkose aufwachen lassen und ihn gemäß krankenhausüblicher Praxis überwachen. Nach dem Verfahren anhand einer Röntgenaufnahme des Brustkorbs die Coil-Platzierung bestätigen und sicherstellen, dass kein Pneumothorax vorliegt. Mindestens 4 Stunden nach der ersten Röntgenaufnahme des Brustkorbs eine zweite Röntgenaufnahme durchführen. Dem Patienten sind detaillierte Informationen zu den zu erwartenden Nebenwirkungen der Coil-Behandlung zu geben, insbesondere die in Abschnitt 7.0 Mögliche unerwünschte Ereignisse aufgeführten möglichen unerwünschten Ereignisse. Er ist anzuweisen, unverzüglich mit dem behandelnden Arzt in Verbindung zu treten, falls eine oder mehrere der möglichen unerwünschten Ereignisse auftreten. Es ist besonders wichtig, den Patienten bei der Entlassung anzuweisen, sich an den implantierenden Arzt zu wenden, falls sich Symptome einstellen, die auf eine Pneumonie oder CAO hindeuten können, damit sichergestellt wird, dass er korrekt behandelt wird. Nach der Rekonvaleszenz sollte der Patient zur Folgebehandlung des kontralateralen Lungenflügels im Normalfall 1 bis 3 Monate nach der ersten Behandlung ein weiteres Mal in die Klinik kommen. 9
10 9.0 Informationen für Patienten 9.1 Implantatausweis für den Patienten und Patientenbroschüre Ein Implantatausweis für den Patienten, der konkrete Informationen zu den REPNEU Coils enthält, wird von PneumRx, Inc. zur Verfügung gestellt. Nach der Implantation wird die Anzahl und der Implantationsort der implantierten REPNEU Coils im Abschnitt mit der Überschrift Implantationsort und Anzahl der Coils notiert. Im Abschnitt mit der Überschrift Kontaktdaten der behandelnden Einrichtung werden Angaben zur behandelnden Einrichtung und zum Arzt eingetragen. Der Ausweis wird dem Patienten vor der Entlassung ausgehändigt. Alle Patienten sollten diesen Ausweis, auf dem die Behandlung und der jeweilige Implantationsort der Coils angegeben ist, jederzeit bei sich tragen. PneumRx hat eine Patientenbroschüre erstellt, die speziell an Patienten gerichtete Informationen über die Funktionsweise der REPNEU Coils und Informationen zur Behandlung, einschließlich zu möglichen Risiken und Nutzen, enthält. Exemplare der Broschüre sind per von PneumRx unter oder telefonisch unter +49 (0) erhältlich. Alle Patienten müssen die Patientenbroschüre vor der Behandlung erhalten und gelesen haben. 9.2 Sicherheitsrelevante Informationen zur magnetresonanztomografischen Bildgebung (MRT) Bedingt MR-tauglich Die REPNEU Coil ist bedingt MR-tauglich. Diese Angabe gilt für die gesamte REPNEU Coil-Produktfamilie (d. h. für alle Coil-Größen). Es wurden nicht klinische Prüfungen und MR-Simulationen durchgeführt, um die Worst-Case-Bedingungen zu bestimmen, anhand derer nachgewiesen wurde, dass die REPNEU Coil bedingt MR-tauglich ist. Ein Patient mit diesem Produkt kann unmittelbar oder jederzeit im Anschluss an die Implantation ohne Gefährdung gescannt werden, wenn folgende Bedingungen gegeben sind: nur bei einem statischen Magnetfeld von 1,5 oder 3 Tesla maximales räumliches Gradienten-Magnetfeld von maximal 5000 Gauss/cm (extrapoliert) vom MR-System gemeldete maximale durchschnittliche Ganzkörper-SAR (spezifische Absorptionsrate) von 2 W/kg bei einer Scandauer von 15 Minuten (d. h. pro Pulssequenz) im normalen Betriebsmodus des MR-Systems MR-bedingte Erwärmung Bei nicht klinischen Prüfungen bewirkte die REPNEU Coil bei einer Scandauer von 15 Minuten (d. h. pro Pulssequenz) die folgenden Temperaturanstiege bei den folgenden MR-Systemen: (1,5 Tesla/64 MHz, Magnetom, Siemens Medical Solutions, Malvern, PA. Software Numaris/4, Version Syngo MR 2002B DHHS, aktiv abgeschirmt, Scanner mit horizontalem Feld) und 3 Tesla (3 Tesla/128 MHz, Excite, HDx, Software 14X.M5, General Electric Healthcare, Milwaukee, WI): 10 1,5 Tesla 3 Tesla Vom MR-System gemeldete maximale durchschnittliche Ganzkörper-SAR 2,9 W/kg 2,9 W/kg Kalorimetrisch gemessene Werte, durchschnittliche Ganzkörper-SAR 2,1 W/kg 2,7 W/kg Maximale Temperaturänderung 5,4 C 3,2 C Temperaturskalierung auf die durchschnittliche Ganzkörper-SAR von 2 W/kg 3,7 C 2,2 C Artefaktinformationen Die maximale Artefaktgröße bei der Gradienten-Echo-Pulssequenz erstreckt sich bei einem Kernspinverfahren mit 3 Tesla ungefähr 10 mm relativ zur Größe der Form der REPNEU Coil.
11 10.0 Lieferform und Aufbewahrung 10.1 Einführsystem Das Einführsystem (Führungsdraht, Katheter, Einführhülse und Fasszange) ist auf einer Trägerkarte montiert, welche in einen Beutel abgepackt und dann in einem Karton verpackt wird. Das Einführsystem wird STERIL zur Anwendung bei einem einzelnen Patienten bereitgestellt Coil Jede einzelne Coil ist von einem Kunststoffschutzgehäuse umschlossen, welches in einem Beutel in einem Karton mit insgesamt entweder einer (1) Coil oder fünf (5) Coils verpackt wird. Jede Coil wird STERIL nur für den einmaligen Gebrauch bereitgestellt Aufbewahrung Die Komponenten des REPNEU Systems stets trocken lagern Gebrauchsanweisungen PRODUKTE FÜR DEN EINSATZ VORBEREITEN 1. Den Führungsdraht und den Katheter gemeinsam aus dem Verpackungsring entnehmen. 2. Die Fasszange und die Einführhülse aus der Verpackung entnehmen. 3. Die Einführhülse mit steriler Kochsalzlösung spülen (nur vor dem Freisetzen der ersten Coil). EINFÜHRSYSTEM POSITIONIEREN 4. Die zum erkrankten Parenchym führenden Atemwege identifizieren. a. Die Behandlung sollte auf den am stärksten geschädigten Lappen (Ober- oder Unterlappen) in den einzelnen Lungenflügeln abzielen, welcher vor der Behandlung mittels einer Untersuchung identifiziert wurde. b. In dem Segment, das am schwierigsten zugänglich ist, mit dem Freisetzen der Coils beginnen, und dann weniger schwierige Segmente behandeln. c. Als Behandlungsstrategie wird empfohlen, Coils in den Oberlappen bzw Coils in den Unterlappen freizusetzen. Wenn sich die Anzahl der implantierten Coils der Obergrenze nähert, das Freisetzen weiterer Coils unterlassen, wenn beim Vorschieben des proximalen Endes der Coil in den Lungenflügel erhöhter Widerstand zu spüren ist. d. Um eine optimale Platzierung der Coil zu erzielen, die Coils in den Bereich zwischen dem Hilum und der Pleura positionieren. Dabei ist eine Coil-freie Zone von etwa 4 cm neben der Pleura einzuhalten. Eine solche Platzierung ergibt eine fächerartige Verteilung der Coils in den subsegmentalen Atemwegen über den behandelten Lappen hinweg (siehe Abbildung 2). 11 Abbildung 2: Optimale Coil-Platzierung
12 5. Das Bronchoskop in den ausgewählten Atemweg (am Ostium der subsegmentalen Atemwege) vorschieben und dort fest positionieren. 6. Die Spitzen des Führungsdrahts und des Katheters aufeinander ausrichten. 7. Den Katheter und den Führungsdraht in den Arbeitskanal des Bronchoskops einführen. 8. Den Katheter und den Führungsdraht bis zur Spitze des Bronchoskops vorschieben. 9. Den Führungsdraht bis zum Ende des zu behandelnden Atemwegs vorschieben (siehe Abbildung 3). Achtung: Wenn sich der Führungsdraht außerhalb des Sichtbereichs des Bronchoskops befindet, den Führungsdraht unter Fluoroskopie visualisieren. Bei Eintreten des Fluoroskopie-Markierungsstreifens des Führungsdrahts in den Katheteransatz das Fluoroskop einschalten. Vorschieben des Führungsdrahts röntgendichte Katheterspitze Bronchoskop röntgendichte Führungsdrahtspitze Abbildung 3: Vorschieben des Führungsdrahts in die zu behandelnden Atemwege a. Den Führungsdraht unter fluoroskopischer Kontrolle behutsam in die distalen Atemwege vorschieben, bis die Spitze die Pleura erreicht oder plötzlich von einem geraden Einführweg abbiegt. Achtung: Den Führungsdraht nicht gegen Widerstand vorschieben. Achtung: Wird der Führungsdraht bei erhöhtem Widerstand über eine plötzlich auftretende Krümmung in einem distalen Atemweg hinaus vorgeschoben, könnte dies dazu führen, dass Gewebe im gekrümmten Abschnitt des Führungsdrahts eingeklemmt wird. 10. Die Spitze des Führungsdrahts zurückziehen; dazu das proximale Ende des Führungsdrahts neben dem Katheteransatz fassen und ihn bis auf 4 5 cm (anhand einer im Voraus festgelegten Messreferenz) vor dem Ansatz zurückziehen. 11. Den Führungsdraht stets in gleicher Ausrichtung zum Bronchoskop halten, und dabei gleichzeitig den Katheter nach distal vorschieben, bis er auf gleicher Höhe mit der Spitze des Führungsdrahts ist (siehe Abbildung 4). Achtung: Das Fluoroskop sollte eingeschaltet bleiben, um sicherzustellen, dass sich der Führungsdraht während des Kathetervorschubs nicht bewegt. Achtung: Den Katheter nicht über den Führungsdraht schieben, wenn der Führungsdraht einen spitzen Winkel einnimmt. Achtung: Lässt sich der Katheter nicht zum distalen Ende des Führungsdrahts vorschieben, den Führungsdraht zurückziehen, bis er mit der Katheterspitze ausgerichtet ist. Bei erhöhtem Widerstand den Katheter nicht über den Draht schieben. 12
13 Bronchoskop miteinander ausgerichtete röntgendichte Spitzen von Führungsdraht u. Katheter Abbildung 4: Mit der Führungsdrahtspitze ausgerichtete Katheterspitze COIL AUSWÄHLEN 12. Die geeignete Coil-Größe auswählen. Dazu die Anzahl der röntgendichten Markierungen auf dem Führungsdraht abzählen, die außerhalb des Bronchoskops sichtbar sind (siehe Abbildung 5 und Tabelle 1). a. Die Markierungen zeigen die empfohlene Mindestgröße der zu verwendenden Coils an. b. Die Führungsdrahtspitze bei der Coil-Auswahl nicht als Markierung mitzählen. Führungsdrahtund Katheterspitze (NICHT MITZÄHLEN) Markierung Nr. 1 Markierung Nr. 2 Abbildung 5: Röntgendichte Markierung des Führungsdrahts unter Fluoroskopie 13
14 Tabelle 1: Auswahl der Coil-Größe Anzahl der röntgendichten Markierungen, die außerhalb des Bronchoskops sichtbar sind Geeignete Coil-Größe Möglichkeit für Coil Nr. 1 bestimmen. Die Katheterposition beibehalten und gleichzeitig den Führungsdraht bis zum Ende des Atemwegs vorschieben. 0 Wenn eine Markierung außerhalb des Bronchoskops sichtbar ist: Coil Nr. 1 auswählen Wenn KEINE Markierung außerhalb des Bronchoskops sichtbar ist: KEINE Coil freisetzen 1 Coil Nr. 1 oder Coil Nr. 2 2 Coil Nr. 2 oder Coil Nr. 3 3 Coil Nr. 3 Hinweis: Coil Nr.1 = 100 mm Länge; Coil Nr. 2 = 125 mm Länge; Coil Nr. 3 = 150 mm Länge 13. Den Führungsdraht unter Beibehaltung der Katheterposition aus dem Katheter entfernen und das Fluoroskop ausschalten. COIL LADEN 14. Das Kunststoffschutzgehäuse mit der ausgewählten Coil aus dem Karton und dem Beutel entnehmen. 15. Die Fasszange in die Einführhülse und durch diese hindurch einführen; dabei darauf achten, dass die Fasszange am Luer-Lock-Ende der Einführhülse austritt (siehe Abbildung 6). Luer-Lock Einführhülse Röntgendichte Markierungsstreifen (95,5 cm) Arretierung Daumenring Fingergriff Abbildung 6: Vorschieben der Fasszange durch die Einführhülse Die Fasszange entsperren; dazu die Backen unter Kraftausübung schließen und die Arretierung hochdrücken (das Schließen der Backen wird bewerkstelligt, indem der Fingergriff und der Daumenring stärker zusammengedrückt werden). 17. Die Backen der Fasszange öffnen; dazu die Entfernung zwischen dem Fingergriff und dem Daumenring vergrößern.
15 18. Die Coil durch Schließen der Backen der Fasszange um die proximale Kugel fassen. 19. Die Backen der Fasszange schließen und im geschlossenen Zustand arretieren (die blaue Arretierungslasche zum Griff drücken, bis ein Klicken vernommen wird), um eine Freigabe der Coil zu verhindern. 20. Die Einführhülse in die Öffnung des Kunststoffschutzgehäuses einsetzen (siehe Abbildung 7). 21. Die Fasszange langsam ziehen, bis die Coil aus dem Kunststoffschutzgehäuse entfernt worden ist und sich vollständig in der Einführhülse befindet. Achtung: Beim Laden einer Coil die Backen der Fasszange oder die Coil nicht aus dem proximalen Ende der Einführhülse ziehen. Ein Zurückschieben der Coil in die Einführhülse kann zu Schäden an der Coil führen. In einem solchen Fall die Coil nicht verwenden. Achtung: Die Coil nicht verwenden, wenn sie heruntergefallen ist oder sich aus irgendeinem Grund außerhalb des Kunststoffschutzgehäuses befindet. Vollständig in das Kunststoffschutzgehäuse vorgeschobene Einführhülse Abbildung 7: Einziehen der Coil in die Einführhülse 22. Die Einführhülse an den Luer-Lock-Ansatz des Katheters anschließen und arretieren. 23. Die Coil in den Katheter einbringen; dazu die Fasszange gemeinsam mit der Coil vorschieben. Achtung: Die Fasszange in maximal 5 cm Entfernung vom proximalen Ende der Einführhülse fassen, um ein Abknicken beim Vorschieben zu vermeiden. 24. Bei Eintreten des Fluoroskopie-Markierungsstreifens (am Schaft der Fasszange) in die Einführhülse das Fluoroskop einschalten. 25. Die distale Kugel der Coil bis zum distalen Ende des Katheters vorschieben und die Position der Coil mittels Fluoroskopie bestätigen. 26. Den Assistenten anweisen, die Position des Bronchoskops in Relation zum Patienten zu wahren. Achtung: Die Bronchoskop-Position während der Freisetzung nicht verändern. COIL FREISETZEN 27. Die Coil durch Vorschieben der Fasszange nach distal freisetzen. Die Coil aus dem distalen Ende des Katheters vorschieben, bis die erste Hälfte der Kurve im zu behandelnden Atemweg positioniert ist (siehe Abbildung 8). Hinweis: Wenn die Ansicht der Coil blockiert ist, das Fluoroskop so justieren, dass eine ausreichende Visualisierung möglich ist. 15
16 freigesetzte halbe Kurve distale Kugel Katheter Bronchoskop Abbildung 8: Beobachten der teilweise freigesetzten Coil 28. Den Katheter unter leichter konstanter Druckausübung zurückziehen, um die Fasszange vorzuschieben, bis die Backen der Fasszange etwa 2 cm distal vom Ende des Bronchoskops sichtbar sind. Die Fasszangenposition beibehalten und den Katheter weiter in das Bronchoskop zurückziehen (siehe Abbildung 9). vollständig freigesetzte Coil Backen der Fasszange Bronchoskop Abbildung 9: Beobachten der vollständig freigesetzten Coil 29. Die Coil-Position vor dem Entsperren der Fasszange und dem Freigeben der Coil überprüfen. a. Im Idealfall befindet sich das proximale Ende der Coil im segmentalen Atemweg oder mehr distal dazu. b. Wenn die Coil-Position nicht optimal ist, siehe Abschnitt 12 Umpositionierung von Coils nach der Freisetzung. 16 EINFÜHRSYSTEM LÖSEN UND ENTFERNEN 30. Die Fasszange behutsam etwa 1 cm zurückziehen, um eine leichte Spannung zwischen der Fasszange und der Coil zu erzeugen. Die Spannung aufrechterhalten. 31. Die Backen der Fasszange entsperren und öffnen. Achtung: Die Backen der Fasszange lassen sich nicht öffnen, wenn sie sich im Katheter befinden. Die Backen der Fasszange müssen mindestens 1 cm über das distale Ende des Katheters und des Bronchoskops hinausragen, um die Coil freizusetzen. 32. Die Backen der Fasszange schließen und arretieren. 33. Vor dem Ausschalten des Fluoroskops bestätigen, dass die proximale Kugel freigesetzt wurde.
17 34. Die Einführhülse vom Katheter trennen (Luer-Lock) und zusammen mit der Fasszange als eine Einheit entfernen. 35. Die distale Spitze des Katheters in das Bronchoskop zurückziehen. Hinweis: Es ist möglich, dass der Katheter während der Positionierung in den nächsten zu behandelnden Atemweg im Bronchoskop verbleibt. Zum Freisetzen weiterer Coils die Schritte 7 bis 35 wiederholen Umpositionierung von Coils nach der Freisetzung Hinweis: Wenn die Coil von der Fasszange bereits freigegeben wurde, die proximale Kugel sich jedoch nicht im segmentalen Atemweg bzw. weiter distal dazu befindet, wird empfohlen, alle weiteren Coils freizusetzen, bevor der Versuch einer Umpositionierung unternommen wird. Befindet sich eine Coil am Ende der Behandlung weiterhin nicht in optimaler Position, die proximale Kugel mit der Fasszange wiedereinholen und die Coil wie nachstehend beschrieben umpositionieren. Kann die proximale Kugel mit der Fasszange nicht gefasst werden, den Draht fassen und das proximale Ende der Coil umpositionieren, bis die proximale Kugel gefasst werden kann. Die proximale Kugel muss 0 1 cm vorgeschoben werden 1. Den Katheter 2 cm über die Backen der Fasszange hinaus vorschieben, dann den Katheter gemeinsam mit der Fasszange behutsam vorschieben. 2. Schritt 28 und 29 wiederholen (siehe Abschnitt 11.0 Gebrauchsanweisungen). Die proximale Kugel muss 1 2 cm vorgeschoben werden 1. Die Position der Fasszange und der Coil in Relation zum Bronchoskop wahren und den Katheter nach distal vorschieben, um die Coil bis zu maximal der Hälfte der Länge wieder zu umhüllen. 2. Den Katheter zurückziehen und dabei gleichzeitig die Fasszange weiter nach distal bewegen als bei der vorherigen Freisetzung. Die proximale Kugel muss mehr als 2 cm vorgeschoben werden Die Coil wiedereinholen und erneut freisetzen: 1. Die Coil wieder umhüllen, bis sie sich vollständig im Katheter befindet. 2. Die Coil zurückziehen, indem die Fasszange nach proximal zurückgezogen wird, bis sich die Coil in der Einführhülse befindet. 3. Den Luer-Lock öffnen und die Einführhülse, die Coil und die Fasszange als eine Einheit entfernen, wobei der Katheter an Ort und Stelle verbleibt. 4. Den Führungsdraht in den Katheter einführen und den Katheter neu positionieren, damit die Coil erneut freigesetzt werden kann. 17
18 13.0 Bronchoskopische Coil- Entfernung nach der Implantation WARNUNG: Die bronchoskopische Coil-Entfernung muss medizinisch indiziert sein. Der mögliche Nutzen einer Coil-Entfernung muss gegen den möglichen Schaden, einschließlich der bekannten Risiken der Bronchoskopie, abgewogen werden. Die bronchoskopische Coil-Entfernung kann sich 2 oder mehr Monate nach der Implantation je nach Umfang des vorhandenen Granulationsgewebes zunehmend schwierig gestalten. WARNUNG: Ist eine Coil- Entfernung notwendig, darf nicht versucht werden, die Coil auf irgendeine Art und Weise zu durchtrennen, zu verbiegen oder zu brechen. Ein unsachgemäßer Umgang mit der Coil auf eine solche Art und Weise kann dazu führen, dass das Produkt korrodiert und scharfe Oberflächen entstehen, die eine Gesundheitsschädigung, Erkrankung oder den Tod des Patienten zur Folge haben können. Hinweis: Nach Möglichkeit stets versuchen, die Coil mittels bronchoskopischer Technik zu entfernen, bevor andere Methoden in Erwägung gezogen werden. Hinweis: Die Coil-Entfernung ist stets unter Fluoroskopie durchzuführen. 1. Für die Coil-Entfernung ist ein Bronchoskop mit einem 2,0-mm-Arbeitskanal und einer maximalen Nutzlänge von 65 cm erforderlich. 2. Die Position der zu entfernenden Coil unter Fluoroskopie bestimmen. 3. Das Bronchoskop zur Coil vorschieben. 4. Die Fasszange durch den Bronchoskopkanal einführen. 5. Die proximale Kugel mit der Fasszange fassen. Kann die proximale Kugel nicht gefasst werden, den Draht fassen und das proximale Ende der Coil umpositionieren, bis die proximale Kugel gefasst werden kann. 6. Die Fasszange arretieren. 7. Das Bronchoskop vorschieben (Wedge-Position) und die Coil in den Arbeitskanal des Bronchoskops zurückziehen. Achtung: Die Coil nicht wiederverwenden, wenn ihre Entfernung als separates Verfahren und nicht im Rahmen der Coil-Platzierung vorgenommen wurde. Die Coil kann wiederverwendet werden, wenn sie während der ursprünglichen Bronchoskopie zum Zweck der Coil-Platzierung entfernt und erneut freigesetzt wurde. 18
19 14.0 Garantieausschluss DAS REPNEU SYSTEM WURDE UNTER KONTROLLIERTEN BEDINGUNGEN HERGESTELLT, JEDOCH LIEGEN DIE EINSATZBEDINGUNGEN DES PRODUKTS AUSSERHALB DES EINFLUSSBEREICHS DER PNEUMRX, INC. UND IHREN VERBUNDENEN UNTERNEHMEN (ZUSAMMENGEFASST PNEUMRX ). PNEUMRX SCHLIESST DAHER ALLE AUSDRÜCKLICHEN UND STILLSCHWEIGENDEN GARANTIEN IN BEZUG AUF DAS REPNEU SYSTEM AUS, UNTER ANDEREM JEGLICHE GARANTIEN DER MARKTGÄNGIGKEIT ODER EIGNUNG FÜR EINEN BESTIMMTEN ZWECK. PNEUMRX ÜBERNIMMT KEINE HAFTUNG FÜR JEDWEDE DIREKTE, NEBEN- ODER FOLGESCHÄDEN, DIE DURCH EINE VERWENDUNG DES REPNEU SYSTEMS ENTSTEHEN BZW. DAMIT IM ZUSAMMENHANG STEHEN, UNABHÄNGIG DAVON, OB EIN ENTSPRECHENDER SCHADENSERSATZANSPRUCH AUF GEWÄHRLEISTUNG, VERTRAG, UNERLAUBTER HANDLUNG ODER SONSTIGEM RECHTSGRUND BERUHT. KEINE PERSON ODER INSTITUTION HAT DIE BEFUGNIS, PNEUMRX AN EINE DARSTELLUNG ODER GARANTIE IN BEZUG AUF DAS REPNEU SYSTEM ZU BINDEN. Die in diesem GARANTIEAUSSCHLUSS dargelegten Ausschlüsse und Beschränkungen stellen keine Widersprüche zu den zwingenden Bestimmungen des geltenden Rechts dar und sind auch nicht demgemäß auszulegen. Sollte ein Teil oder eine Bedingung dieses GARANTIEAUSSCHLUSSES von einem Gericht mit der entsprechenden juristischen Zuständigkeit für gesetzwidrig, nicht einklagbar oder widersprüchlich zum anwendbaren Gesetz befunden werden, wird davon die Wirksamkeit der restlichen Teile dieses GARANTIEAUSSCHLUSSES nicht berührt, und alle Rechte und Verpflichtungen werden so ausgelegt und durchgesetzt, als sei der jeweilige für ungültig befundene Teil bzw. die für ungültig befundene Bedingung nicht in diesem GARANTIEAUSSCHLUSS enthalten. 19
20 15.0 Handelsmarken Dieses Dokument ist vorbehaltlich aller Rechte urheberrechtlich geschützt. Nach den Bestimmungen des Urheberrechts darf es ohne die ausdrückliche schriftliche Zustimmung von PneumRx weder vollständig noch auszugsweise kopiert oder auf sonstige Weise reproduziert werden. Genehmigte Kopien müssen dieselben Eigentums- und Urheberrechtsvermerke aufweisen wie das Original. Nach dem Urheberrecht fällt unter das Kopieren auch die Übersetzung in eine andere Sprache. Zur Beachtung: Es wurden alle Anstrengungen unternommen, um die Korrektheit der in diesem Dokument enthaltenen Daten zu gewährleisten. Die Angaben, Abbildungen, Illustrationen, Tabellen, technischen Daten und Skizzen in diesem Dokument können jedoch ohne Ankündigung geändert werden. REPNEU ist eine Handelsmarke von PneumRx, Inc., einem Unternehmen der BTG International- Gruppe. PneumRx und das PneumRx-Logo sind eingetragene Handelsmarken von PneumRx, Inc. BTG und das BTG-Rundlogo sind eingetragene Handelsmarken von BTG International Ltd. Die REPNEU Coil ist außerdem unter US- sowie internationalen Patenten sowie Patentanmeldungen patentrechtlich geschützt. Hergestellt von: PneumRx, Inc Burton Drive Santa Clara, CA USA PneumRx, Inc. ist ein Unternehmen der BTG International-Gruppe. KUNDENDIENST TEL.: +49 (0) FAX: +49 (0) CS@btgplc.com 20
21 16.0 Erläuterung der Produktkennzeichnungssymbole Chargenbezeichnung Bestellnummer Verfallsdatum (Verwendbar bis) Sterilisation mit Ethylenoxid Sterilisation durch Bestrahlung Bedingt MR-tauglich Nicht zur Wiederverwendung Bei beschädigter Verpackung nicht verwenden Trocken aufbewahren Hersteller Gebrauchsanweisung beachten Inhalt Bevollmächtigter in der Europäischen Gemeinschaft Achtung Latexfreies Produkt PneumRx, Inc.
WICHTIGE RISIKOINFORMATIONEN
 WICHTIGE RISIKOINFORMATIONEN EM-PxC-2017-0598 Allgemeine Informationen Wie jedes medizinische Verfahren ist auch die Behandlung mit dem endobronchialen RePneu Coil-System von PneumRx mit Risiken und Komplikationen
WICHTIGE RISIKOINFORMATIONEN EM-PxC-2017-0598 Allgemeine Informationen Wie jedes medizinische Verfahren ist auch die Behandlung mit dem endobronchialen RePneu Coil-System von PneumRx mit Risiken und Komplikationen
RePneu Coil- Lungenvolumenreduktionssystem Bedienungsanleitung
 RePneu Coil- Lungenvolumenreduktionssystem Bedienungsanleitung 1 MPS Medical Product Service GmbH Borngasse 20 35619 Braunfels Deutschland Tel.: (+49) 6442 962073 Fax: (+49) 6442 962074 PneumRx, ein Unternehmen
RePneu Coil- Lungenvolumenreduktionssystem Bedienungsanleitung 1 MPS Medical Product Service GmbH Borngasse 20 35619 Braunfels Deutschland Tel.: (+49) 6442 962073 Fax: (+49) 6442 962074 PneumRx, ein Unternehmen
RePneu Coil-System Bedienungsanleitung
 RePneu Coil-System Bedienungsanleitung 0086 MPS Medical Product Service GmbH Borngasse 20 35619 Braunfels Deutschland Tel (+49) 6442.962073 Fax (+49) 6442.962074 PneumRx, Inc. 530 Logue Avenue Mountain
RePneu Coil-System Bedienungsanleitung 0086 MPS Medical Product Service GmbH Borngasse 20 35619 Braunfels Deutschland Tel (+49) 6442.962073 Fax (+49) 6442.962074 PneumRx, Inc. 530 Logue Avenue Mountain
Sehr geehrte ärztliche Anwender des RePneu Coil-Systems von PneumRx,
 30. April 2018 Sehr geehrte ärztliche Anwender des RePneu Coil-Systems von PneumRx, Mit diesem Rundschreiben möchten wir Sie über Aktualisierungen der Gebrauchsanweisung (LBL0139, aktualisiert von Rev.
30. April 2018 Sehr geehrte ärztliche Anwender des RePneu Coil-Systems von PneumRx, Mit diesem Rundschreiben möchten wir Sie über Aktualisierungen der Gebrauchsanweisung (LBL0139, aktualisiert von Rev.
fortgeschrittenem Lungenemphysem
 PneumRx Coils: Neue randomisierte klinische Studien bestätigen wiederholt positive Ergebnisse bei Pa PneumRx Coils Neue randomisierte klinische Studien bestätigen wiederholt positive Ergebnisse bei Patienten
PneumRx Coils: Neue randomisierte klinische Studien bestätigen wiederholt positive Ergebnisse bei Pa PneumRx Coils Neue randomisierte klinische Studien bestätigen wiederholt positive Ergebnisse bei Patienten
RePneu Coil-System (zur Lungenvolumenreduktion) Bedienungsanleitung
 RePneu Coil-System (zur Lungenvolumenreduktion) Bedienungsanleitung 1 MPS Medical Product Service GmbH Borngasse 20 35619 Braunfels Deutschland Tel.: (+49) 6442 962073 Fax: (+49) 6442 962074 PneumRx, Inc.
RePneu Coil-System (zur Lungenvolumenreduktion) Bedienungsanleitung 1 MPS Medical Product Service GmbH Borngasse 20 35619 Braunfels Deutschland Tel.: (+49) 6442 962073 Fax: (+49) 6442 962074 PneumRx, Inc.
Lungenvolumen- Reduktion mit RePneu Coils
 Lungenvolumen- Reduktion mit RePneu Coils Eine neue Behandlung für das Emphysem Revive. Rebound. Renew. Der Atem des Lebens Beim Atmen nimmt Ihre Lunge Sauerstoff auf und gibt Kohlendioxid aus dem Körper
Lungenvolumen- Reduktion mit RePneu Coils Eine neue Behandlung für das Emphysem Revive. Rebound. Renew. Der Atem des Lebens Beim Atmen nimmt Ihre Lunge Sauerstoff auf und gibt Kohlendioxid aus dem Körper
Endoskopische Lungenvolumenreduktion mit Ventilen für Patienten mit. Lungenemphysem. Patientenratgeber
 Endoskopische Lungenvolumenreduktion mit Ventilen für Patienten mit Lungenemphysem Patientenratgeber Emphysem Das Emphysem gehört zu einer Gruppe von Krankheiten, die als chronisch obstruktive Lungenerkrankung
Endoskopische Lungenvolumenreduktion mit Ventilen für Patienten mit Lungenemphysem Patientenratgeber Emphysem Das Emphysem gehört zu einer Gruppe von Krankheiten, die als chronisch obstruktive Lungenerkrankung
System zur Stimulation des unteren Ösophagussphinkters. MRT Leitlinien mit EndoStim LES-Stimulator Modell 1002
 System zur Stimulation des unteren Ösophagussphinkters MRT Leitlinien mit EndoStim LES-Stimulator Modell 1002 EndoStim ist eine eingetragene Handelsmarke von EndoStim B.V. Vor der Verwendung des Geräts
System zur Stimulation des unteren Ösophagussphinkters MRT Leitlinien mit EndoStim LES-Stimulator Modell 1002 EndoStim ist eine eingetragene Handelsmarke von EndoStim B.V. Vor der Verwendung des Geräts
Patientenleitfaden. Ventiltherapie für Patienten mit Emphysem
 Patientenleitfaden Ventiltherapie für Patienten mit Emphysem Das Emphysem gehört zu einer Gruppe von Erkrankungen, die chronisch-obstruktive Lungenerkrankung genannt wird, kurz COPD (abgeleitet vom engl.
Patientenleitfaden Ventiltherapie für Patienten mit Emphysem Das Emphysem gehört zu einer Gruppe von Erkrankungen, die chronisch-obstruktive Lungenerkrankung genannt wird, kurz COPD (abgeleitet vom engl.
Lungenvolumenreduktion mit Ventilen für Patienten mit Lungenemphysem
 Lungenvolumenreduktion mit Ventilen für Patienten mit Lungenemphysem Patientenratgeber Emphysem Das Emphysem gehört zu einer Gruppe von Krankheiten, die als chronisch - obstruktive Lungenerkrankung (COPD)
Lungenvolumenreduktion mit Ventilen für Patienten mit Lungenemphysem Patientenratgeber Emphysem Das Emphysem gehört zu einer Gruppe von Krankheiten, die als chronisch - obstruktive Lungenerkrankung (COPD)
RePneu Coils Hilfe beim Lungenemphysem
 RePneu Coils Hilfe beim Lungenemphysem Revive. Rebound. Renew. Die Lunge Die Lunge ist für die Sauerstoffversorgung des menschlichen Körpers zuständig. Sie besteht aus zwei von einander unabhängigen Lungenflügeln
RePneu Coils Hilfe beim Lungenemphysem Revive. Rebound. Renew. Die Lunge Die Lunge ist für die Sauerstoffversorgung des menschlichen Körpers zuständig. Sie besteht aus zwei von einander unabhängigen Lungenflügeln
RePneu Coils Hilfe beim Lungenemphysem
 RePneu Coils Hilfe beim Lungenemphysem Revive. Rebound. Renew. Die Lunge Die Lunge ist für die Sauerstoffversorgung des menschlichen Körpers zuständig. Sie besteht aus zwei von einander unabhängigen Lungenflügeln
RePneu Coils Hilfe beim Lungenemphysem Revive. Rebound. Renew. Die Lunge Die Lunge ist für die Sauerstoffversorgung des menschlichen Körpers zuständig. Sie besteht aus zwei von einander unabhängigen Lungenflügeln
Zenith Alpha T HORACIC ENDOVASCULAR GRAFT
 Entfaltungssequenz Zenith Alpha T HORACIC ENDOVASCULAR GRAFT www.cookmedical.com Vorbereitung und Spülung Proximale und distale Komponenten Das Innenstilett mit dem gelben Ansatz aus der Dilatatorspitze
Entfaltungssequenz Zenith Alpha T HORACIC ENDOVASCULAR GRAFT www.cookmedical.com Vorbereitung und Spülung Proximale und distale Komponenten Das Innenstilett mit dem gelben Ansatz aus der Dilatatorspitze
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli bei sekretreichem Husten Ipecacuanha D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei sekretreichem Husten Ipecacuanha D4/D6/D12 Wirkstoff: Psychotria ipecacuanha D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei sekretreichem Husten Ipecacuanha D4/D6/D12 Wirkstoff: Psychotria ipecacuanha D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei trockenem Krampf- und Reizhusten Drosera D3/D4/D6
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei trockenem Krampf- und Reizhusten Drosera D3/D4/D6 Wirkstoff: Drosera D3/D4/D6 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei trockenem Krampf- und Reizhusten Drosera D3/D4/D6 Wirkstoff: Drosera D3/D4/D6 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Patienten. Osanit Hustenkügelchen Wirkstoff: Drosera D6
 Osanit Hustenkügelchen Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Hustenkügelchen Wirkstoff: Drosera D6 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Osanit Hustenkügelchen Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Hustenkügelchen Wirkstoff: Drosera D6 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION
 ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
ANHANG III ERGÄNZUNGEN ZUR ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS UND DER GEBRAUCHSINFORMATION Diese Änderungen von SPC und Packungsbeilage treten zum Zeitpunkt der Kommissionsentscheidung in Kraft.
Wichtige Information zu Dapoxetin (Priligy )
 Wichtige Information zu Dapoxetin (Priligy ) Diese Informationsbroschüre zur Anwendung von Dapoxetin (Priligy ) wurde als Teil der Zulassungsauflagen für das Arzneimittel erstellt und behördlich genehmigt.
Wichtige Information zu Dapoxetin (Priligy ) Diese Informationsbroschüre zur Anwendung von Dapoxetin (Priligy ) wurde als Teil der Zulassungsauflagen für das Arzneimittel erstellt und behördlich genehmigt.
REVEAL LINQ LNQ11. Insertable Cardiac Monitor Informationen zu MRT-Untersuchungen. MRT-Gebrauchsanweisung
 REVEAL LINQ LNQ11 Insertable Cardiac Monitor Informationen zu MRT-Untersuchungen MRT-Gebrauchsanweisung 0123 2013 Die folgende Liste beinhaltet Marken oder eingetragene Marken von Medtronic in den USA
REVEAL LINQ LNQ11 Insertable Cardiac Monitor Informationen zu MRT-Untersuchungen MRT-Gebrauchsanweisung 0123 2013 Die folgende Liste beinhaltet Marken oder eingetragene Marken von Medtronic in den USA
Geplante Änderungen an den relevanten Abschnitten der Packungsbeilage
 Geplante Änderungen an den relevanten Abschnitten der Packungsbeilage 1 B. Packungsbeilage 1. Was ist und wofür wird es angewendet? [Dieser Abschnitt soll wie folgt gefasst werden:]
Geplante Änderungen an den relevanten Abschnitten der Packungsbeilage 1 B. Packungsbeilage 1. Was ist und wofür wird es angewendet? [Dieser Abschnitt soll wie folgt gefasst werden:]
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12 Wirkstoff: Atropa bella-donna D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei akuten Hals- und Rachenschmerzen Belladonna D4/D6/D12 Wirkstoff: Atropa bella-donna D4/D6/D12 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli bei beginnenden grippalen Infekten Aconitum sind eine D12/D18/D30
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei beginnenden grippalen Infekten Aconitum D12/D18/D30 Wirkstoff: Aconitum napellus D12/D18/D30 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei beginnenden grippalen Infekten Aconitum D12/D18/D30 Wirkstoff: Aconitum napellus D12/D18/D30 Lesen Sie die gesamte Packungsbeilage
Akute venösen Thromboembolien (VTE) oder VTE in der Vorgeschichte, einschließlich tiefer Venenthrombose und Lungenembolie.
 Aktualisierte Indikation Behandlung der schweren Osteoporose: bei postmenopausalen Frauen, bei erwachsenen Männern, mit hohem Frakturrisiko, für die eine Behandlung mit anderen für die Osteoporosetherapie
Aktualisierte Indikation Behandlung der schweren Osteoporose: bei postmenopausalen Frauen, bei erwachsenen Männern, mit hohem Frakturrisiko, für die eine Behandlung mit anderen für die Osteoporosetherapie
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Heiserkeit und Reizhusten Phosphorus D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Heiserkeit und Reizhusten Phosphorus D4/D6/D12 Wirkstoff: Phosphorus D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Heiserkeit und Reizhusten Phosphorus D4/D6/D12 Wirkstoff: Phosphorus D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsanweisung Ösophagus-Stent Danis Seal (Danis Seal) Nicht-aktive implantierbare Vorrichtung
 Hergestellt von: ELLA CS, s.r.o. Milady Horakove 504 500 06 Hradec Kralove 6 Tschechische Republik Telefon: +420 49 527 91 11 Fax: +420 49 526 56 55 E-Mail: volenec@ellacs.eu Lieferumfang: Gebrauchsanweisung
Hergestellt von: ELLA CS, s.r.o. Milady Horakove 504 500 06 Hradec Kralove 6 Tschechische Republik Telefon: +420 49 527 91 11 Fax: +420 49 526 56 55 E-Mail: volenec@ellacs.eu Lieferumfang: Gebrauchsanweisung
RipTide. Braupumpe. Montage, Betrieb und Instandhaltung
 RipTide Braupumpe Montage, Betrieb und Instandhaltung BITTE LESEN SIE DIESES HANDBUCH VOR GEBRAUCH, UM WICHTIGE SICHERHEITSHINWEISE ZU VERSTEHEN! Über diese Anleitung: Achtung: Vorsicht: Wichtig: Eine
RipTide Braupumpe Montage, Betrieb und Instandhaltung BITTE LESEN SIE DIESES HANDBUCH VOR GEBRAUCH, UM WICHTIGE SICHERHEITSHINWEISE ZU VERSTEHEN! Über diese Anleitung: Achtung: Vorsicht: Wichtig: Eine
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli zur Steigerung der Abwehrkräfte Echinacea purpurea D4/D6/D12
 Gebrauchsinformation: Information für Anwender D4/D6/D12 Wirkstoff: Echinacea purpurea D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender D4/D6/D12 Wirkstoff: Echinacea purpurea D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli zur Aktivierung nach grippalen Infekten Sulfur D12/D18/D30
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli zur Aktivierung nach grippalen Infekten Sulfur D12/D18/D30 Wirkstoff: Sulfur D12/D18/D30 Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli zur Aktivierung nach grippalen Infekten Sulfur D12/D18/D30 Wirkstoff: Sulfur D12/D18/D30 Lesen Sie die gesamte Packungsbeilage sorgfältig
RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass
 RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass Dieser Patientenpass enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/ Erziehungsberechtigte Bescheid wissen müssen, bevor,
RoACTEMRA (Tocilizumab) i.v. und s.c. Patientenpass Dieser Patientenpass enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/ Erziehungsberechtigte Bescheid wissen müssen, bevor,
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli bei Fließschnupfen Allium cepa D2/D4/D6. Wirkstoff: Allium cepa D2/D4/D6
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Fließschnupfen Allium cepa D2/D4/D6 Wirkstoff: Allium cepa D2/D4/D6 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Fließschnupfen Allium cepa D2/D4/D6 Wirkstoff: Allium cepa D2/D4/D6 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Was Sie über MabThera wissen sollten
 Die Gesundheitsbehörden der Europäischen Union haben die Markteinführung des Medikaments MabThera an bestimmte Bedingungen gebunden. Der vorgeschriebene Plan zur Risikominimierung in Belgien und im Großherzogtum
Die Gesundheitsbehörden der Europäischen Union haben die Markteinführung des Medikaments MabThera an bestimmte Bedingungen gebunden. Der vorgeschriebene Plan zur Risikominimierung in Belgien und im Großherzogtum
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept
 PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
PATIENTENAUFKLÄRUNG UND EINVERSTÄNDNISERKLÄRUNG zur Basistherapie mit Abatacept Sehr geehrte Patientin! Sehr geehrter Patient! Sie leiden an einer chronischen Polyarthritis (Rheumatoiden Arthritis). Ihr
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli bei Hals- und Rachenschmerzen Phytolacca D3/D4/D6
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Hals- und Rachenschmerzen Phytolacca D3/D4/D6 Wirkstoff: Phytolacca americana D3/D4/D6 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Hals- und Rachenschmerzen Phytolacca D3/D4/D6 Wirkstoff: Phytolacca americana D3/D4/D6 Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Patienten. Osanit Blähungskügelchen Wirkstoff: Matricaria recutita (Chamomilla) D12
 Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Blähungskügelchen Wirkstoff: Matricaria recutita (Chamomilla) D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
Seite 1 von 5 Gebrauchsinformation: Information für Patienten Osanit Blähungskügelchen Wirkstoff: Matricaria recutita (Chamomilla) D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
TIELLE NICHTHAFTEND. Nichthaftender Hydropolymerverband. Technologie
 TIELLE NICHTHAFTEND Nichthaftender Hydropolymerverband Mit Technologie DE Produktbeschreibung Der nichthaftende TIELLE Hydropolymerverband absorbiert Exsudat, hält bei wenig bis stark exsudierenden Wunden
TIELLE NICHTHAFTEND Nichthaftender Hydropolymerverband Mit Technologie DE Produktbeschreibung Der nichthaftende TIELLE Hydropolymerverband absorbiert Exsudat, hält bei wenig bis stark exsudierenden Wunden
Gebrauchsinformation: Information für Anwender. Apozema Dreiklang Globuli bei Stockschnupfen Luffa D4/D6/D12. Wirkstoff: Luffa operculata D4/D6/D12
 Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Stockschnupfen Luffa D4/D6/D12 Wirkstoff: Luffa operculata D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Anwender Apozema Dreiklang Globuli bei Stockschnupfen Luffa D4/D6/D12 Wirkstoff: Luffa operculata D4/D6/D12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für Patienten. Hedelix s. a. Tropfen zum Einnehmen. Wirkstoff: Efeublätter-Auszug
 Gebrauchsinformation: Information für Patienten Hedelix s. a. Tropfen zum Einnehmen Wirkstoff: Efeublätter-Auszug Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Patienten Hedelix s. a. Tropfen zum Einnehmen Wirkstoff: Efeublätter-Auszug Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
RoACTEMRA (Tocilizumab) Patientenpass
 RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
RoACTEMRA (Tocilizumab) Patientenpass Dieser Patientenpass ist eine Auflage im Rahmen der Zulassung von RoACTEMRA und enthält wichtige Sicherheitsinformationen, über die Patienten bzw. deren Eltern/gesetzliche
Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen
 Gebrauchsanweisung 1st Inject P2.2 Instrument Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen Gebrauchsanweisungen werden auf unserer Webseite bereitgestellt: www.1stq.de Inhalt:
Gebrauchsanweisung 1st Inject P2.2 Instrument Injektor zur Implantation von hydrophilen preloaded 1stQ Intraokularlinsen Gebrauchsanweisungen werden auf unserer Webseite bereitgestellt: www.1stq.de Inhalt:
Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahre
 Gebrauchsinformation: Information für den Anwender Aspecton Eukaps 200 mg Weichkapseln Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahre Wirkstoff: Eucalyptusöl Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender Aspecton Eukaps 200 mg Weichkapseln Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahre Wirkstoff: Eucalyptusöl Lesen Sie die gesamte Packungsbeilage
Anhang III. Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage
 Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
Anhang III Änderungen der Entsprechenden Abschnitte der Zusammenfassung der Merkmale des arzneimittels und der Packungsbeilage Hinweis: Diese Zusammenfassung der Merkmale, Etikettierung und Packungsbeilage
INSTALLATIONSANLEITUNG
 8-2016 INSTALLATIONSANLEITUNG 2 DEUTSCH ENGLISH SICHERHEIT UND KORREKTER GEBRAUCH Um eine sichere und dauerhaft korrekte Funktion des Produktes gewährleisten zu können, sind die beigefügten Hinweise strikt
8-2016 INSTALLATIONSANLEITUNG 2 DEUTSCH ENGLISH SICHERHEIT UND KORREKTER GEBRAUCH Um eine sichere und dauerhaft korrekte Funktion des Produktes gewährleisten zu können, sind die beigefügten Hinweise strikt
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Zovirax 3%-Augensalbe Wirkstoff: Aciclovir
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Zovirax 3%-Augensalbe Wirkstoff: Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Zovirax 3%-Augensalbe Wirkstoff: Aciclovir Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels beginnen,
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome
 Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Lang wirksame Beta-Mimetika Long Acting Beta Agonists (LABAs) erhöhtes Risiko einer Exazerbation der Asthmasymptome Basisinformation FACHINFORMATION Lang wirksame Beta-Mimetika - Long Acting Beta Agonists
Gebrauchsinformation: Information für Anwender. RheumaCare Tabletten
 Gebrauchsinformation: Information für Anwender RheumaCare Tabletten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie enthält wichtige
Gebrauchsinformation: Information für Anwender RheumaCare Tabletten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Wirkstoffe: Dequaliniumchlorid und Dexpanthenol
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER dexalgin Dequadex Halspastillen Wirkstoffe: Dequaliniumchlorid und Dexpanthenol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER dexalgin Dequadex Halspastillen Wirkstoffe: Dequaliniumchlorid und Dexpanthenol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Nux vomica-homaccord -Tropfen
 1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
Gebrauchsinformation: Information für Patienten. Tabletten gegen Magen-Darm-Beschwerden Similasan
 1 Gebrauchsinformation: Information für Patienten Tabletten gegen Magen-Darm-Beschwerden Similasan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
1 Gebrauchsinformation: Information für Patienten Tabletten gegen Magen-Darm-Beschwerden Similasan Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 6 Heuschnupfentropfen Mag. Doskar Gelsemium sempervirens D6, Euphorbium D6, Echinacea D1, Kalium chromosulfuricum (Alumen chromicum) D4 Lesen Sie die
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 6 Heuschnupfentropfen Mag. Doskar Gelsemium sempervirens D6, Euphorbium D6, Echinacea D1, Kalium chromosulfuricum (Alumen chromicum) D4 Lesen Sie die
Gebrauchsinformation: Information für den Anwender
 Gebrauchsinformation: Information für den Anwender 0,9 g Auszug aus Bärentraubenblättern und 0,6 g Auszug aus Echtem Goldrutenkraut Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält
Gebrauchsinformation: Information für den Anwender 0,9 g Auszug aus Bärentraubenblättern und 0,6 g Auszug aus Echtem Goldrutenkraut Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält
Gebrauchsinformation: Information für den Anwender
 Gebrauchsinformation: Information für den Anwender Cystinol N Lösung 0,9 g Auszug aus Bärentraubenblättern und 0,6 g Auszug aus Echtem Goldrutenkraut Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Gebrauchsinformation: Information für den Anwender Cystinol N Lösung 0,9 g Auszug aus Bärentraubenblättern und 0,6 g Auszug aus Echtem Goldrutenkraut Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
Kanülierungsschulung
 Kanülierungsschulung Beachten Sie alle Kontraindikationen, Warn- und Vorsichtshinweise, möglichen unerwünschten Ereignisse sowie alle anderen Hinweise in der Gebrauchsanweisung. 00274 DE Rev F 12Sep2014
Kanülierungsschulung Beachten Sie alle Kontraindikationen, Warn- und Vorsichtshinweise, möglichen unerwünschten Ereignisse sowie alle anderen Hinweise in der Gebrauchsanweisung. 00274 DE Rev F 12Sep2014
1. Teil: Grundlegendes über Atemwegserkrankungen, ihre Symptome, ihre Ursachen und ihren Verlauf
 Inhaltsverzeichnis 1. Teil: Grundlegendes über Atemwegserkrankungen, ihre Symptome, ihre Ursachen und ihren Verlauf 0. Warum eine chronische Erkrankung der Atemwege dauerhafte Beachtung finden muß 16 1.
Inhaltsverzeichnis 1. Teil: Grundlegendes über Atemwegserkrankungen, ihre Symptome, ihre Ursachen und ihren Verlauf 0. Warum eine chronische Erkrankung der Atemwege dauerhafte Beachtung finden muß 16 1.
Gebrauchsanweisung. für den Mann. VaPro / VaPro F-Style VaPro Plus / VaPro Plus F-Style. Kontinenzversorgung People First
 VaPro / VaPro F-Style VaPro Plus / VaPro Plus F-Style Einmalkatheter zur Intermittierenden Katheterisierung Gebrauchsanweisung für den Mann Kontinenzversorgung People First VaPro / VaPro F-Style Berührungsfreier
VaPro / VaPro F-Style VaPro Plus / VaPro Plus F-Style Einmalkatheter zur Intermittierenden Katheterisierung Gebrauchsanweisung für den Mann Kontinenzversorgung People First VaPro / VaPro F-Style Berührungsfreier
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 33 Entwöhnungstropfen Mag. Doskar Nicotiana tabacum D30, Strychnos nux-vomica D30, Magnesium phosphoricum D12, Acidum phosphoricum D3, Ambra grisea D3
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 33 Entwöhnungstropfen Mag. Doskar Nicotiana tabacum D30, Strychnos nux-vomica D30, Magnesium phosphoricum D12, Acidum phosphoricum D3, Ambra grisea D3
Bitte lesen Sie die gesamte Gebrauchsinformation sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
 Gebrauchsinformation RECESSAN Lauromacrogol 400 (Polidocanol) 30 mg/g Schmerzbetäubende Salbe für die Mundschleimhaut Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte Gebrauchsinformation sorgfältig
Gebrauchsinformation RECESSAN Lauromacrogol 400 (Polidocanol) 30 mg/g Schmerzbetäubende Salbe für die Mundschleimhaut Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte Gebrauchsinformation sorgfältig
Gebrauchsinformation: Information für Anwender. Monuril 3 g Granulat zum Herstellung einer Lösung zum Einnehmen Fosfomycin-Trometamol
 Gebrauchsinformation: Information für Anwender Monuril 3 g Granulat zum Herstellung einer Lösung zum Einnehmen Fosfomycin-Trometamol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Gebrauchsinformation: Information für Anwender Monuril 3 g Granulat zum Herstellung einer Lösung zum Einnehmen Fosfomycin-Trometamol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Gebrauchsinformation: Information für Patienten
 1 Gebrauchsinformation: Information für Patienten Globuli gegen stockenden Schnupfen Similasan Wirkstoffe: Hydrargyrum sulfuratum rubrum D10, Kalium bichromicum D8, Luffa operculata D8 Lesen Sie die gesamte
1 Gebrauchsinformation: Information für Patienten Globuli gegen stockenden Schnupfen Similasan Wirkstoffe: Hydrargyrum sulfuratum rubrum D10, Kalium bichromicum D8, Luffa operculata D8 Lesen Sie die gesamte
Bedienungsanleitung. MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008
 Bedienungsanleitung MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008 PMT GmbH Im Gewerbegebiet 11 D 66709 Weiskirchen Telefon: +49 (0)6876 9100-0 PD_IFU_MICROPERC-Set-D_A 1 1 Sicherheit 1.1 Vorgesehener
Bedienungsanleitung MICROPERC -Set steril, zur Einmalverwendung PD-PN-1008 PMT GmbH Im Gewerbegebiet 11 D 66709 Weiskirchen Telefon: +49 (0)6876 9100-0 PD_IFU_MICROPERC-Set-D_A 1 1 Sicherheit 1.1 Vorgesehener
PATIENTENINFORMATION
 Die belgischen Gesundheitsbehörden haben bestimmte Voraussetzungen für das Inverkehrbringen des Arzneimittels BOCOUTURE erlassen. Der in Belgien vorgeschriebene Plan zur Risikominimierung, zu dem diese
Die belgischen Gesundheitsbehörden haben bestimmte Voraussetzungen für das Inverkehrbringen des Arzneimittels BOCOUTURE erlassen. Der in Belgien vorgeschriebene Plan zur Risikominimierung, zu dem diese
AMGEVITA (Adalimumab)
 AMGEVITA (Adalimumab) Patientenpass für Ihr Kind behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an der medizinischen Versorgung
AMGEVITA (Adalimumab) Patientenpass für Ihr Kind behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an der medizinischen Versorgung
Die Periduralkatheter-Therapie nach SALIM. Eine neue Methode der minimalinvasiven Behandlung von Bandscheibenvorfällen
 Seite1 Die Periduralkatheter-Therapie nach SALIM Eine neue Methode der minimalinvasiven Behandlung von Bandscheibenvorfällen Rückenschmerzen aufgrund von Wirbelsäulenerkrankungen gehören zu den häufigsten
Seite1 Die Periduralkatheter-Therapie nach SALIM Eine neue Methode der minimalinvasiven Behandlung von Bandscheibenvorfällen Rückenschmerzen aufgrund von Wirbelsäulenerkrankungen gehören zu den häufigsten
Wirkstoff: Eschenrinde-Auszug, Zitterpappelrinde und -blätter-auszug, Goldrutenkraut-Auszug Pflanzliches Arzneimittel Zur Anwendung bei Erwachsenen
 Gebrauchsinformation: Bitte aufmerksam lesen! Wirkstoff: Eschenrinde-Auszug, Zitterpappelrinde und -blätter-auszug, Goldrutenkraut-Auszug Pflanzliches Arzneimittel Zur Anwendung bei Erwachsenen Was in
Gebrauchsinformation: Bitte aufmerksam lesen! Wirkstoff: Eschenrinde-Auszug, Zitterpappelrinde und -blätter-auszug, Goldrutenkraut-Auszug Pflanzliches Arzneimittel Zur Anwendung bei Erwachsenen Was in
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Nr. 19 Aknetropfen Mag. Doskar Kalium iodatum D3, Juglans regia D2, Berberis vulgaris D3
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 19 Aknetropfen Mag. Doskar Kalium iodatum D3, Juglans regia D2, Berberis vulgaris D3 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 19 Aknetropfen Mag. Doskar Kalium iodatum D3, Juglans regia D2, Berberis vulgaris D3 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
Gebrauchsinformation: Information für Anwender. Euphrasia D3 Augentropfen Weleda
 1/5 Gebrauchsinformation: Information für Anwender Euphrasia D3 Augentropfen Weleda Wirkstoff: Euphrasia D3 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
1/5 Gebrauchsinformation: Information für Anwender Euphrasia D3 Augentropfen Weleda Wirkstoff: Euphrasia D3 Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 29 Neuralgietropfen Mag. Doskar Aconitum napellus D6, Verbascum densiflorum D2, Citrullus colocynthis (Colocynthis) D4, Magnesium phosphoricum D12, Plantago
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 29 Neuralgietropfen Mag. Doskar Aconitum napellus D6, Verbascum densiflorum D2, Citrullus colocynthis (Colocynthis) D4, Magnesium phosphoricum D12, Plantago
Gebrauchsinformation: Information für Patienten. Aesculus hippocastanum D 8, Lycopodium clavatum D 12, Graphites D 10, Lachesis D 12
 Tropfen gegen Krampfadern und Hämorrhoiden Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Krampfadern und Hämorrhoiden Similasan Aesculus hippocastanum D 8, Lycopodium clavatum
Tropfen gegen Krampfadern und Hämorrhoiden Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Krampfadern und Hämorrhoiden Similasan Aesculus hippocastanum D 8, Lycopodium clavatum
AMGEVITA (Adalimumab)
 AMGEVITA (Adalimumab) Patientenpass behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an Ihrer medizinischen Versorgung beteiligt sind,
AMGEVITA (Adalimumab) Patientenpass behördlich genehmigtes Schulungsmaterial Dieser Pass enthält wichtige Sicherheitsinformationen über AMGEVITA. Alle, die an Ihrer medizinischen Versorgung beteiligt sind,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Furacine Soluble Dressing 2 mg/g Salbe Furacine 2 mg/ml Lösung zur Anwendung auf der Haut Nitrofural Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Furacine Soluble Dressing 2 mg/g Salbe Furacine 2 mg/ml Lösung zur Anwendung auf der Haut Nitrofural Lesen Sie die gesamte Packungsbeilage sorgfältig
Arbeitsspeicher. Hinweis: Online-Anweisungen finden Sie unter der Adresse
 Deutsch Arbeitsspeicher Austausch Anleitung Bitte folgen Sie diesen Anweisungen gewissenhaft. Geschieht dies nicht, können die Geräte beschädigt werden, und Ihr Garantieanspruch kann verlorengehen. Hinweis:
Deutsch Arbeitsspeicher Austausch Anleitung Bitte folgen Sie diesen Anweisungen gewissenhaft. Geschieht dies nicht, können die Geräte beschädigt werden, und Ihr Garantieanspruch kann verlorengehen. Hinweis:
Gebrauchsinformation: Information für Patienten
 Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
Tropfen gegen Akne Similasan 1 Gebrauchsinformation: Information für Patienten Tropfen gegen Akne Similasan Acidum arsenicosum D 12, Clematis recta D 8, Graphites D 12 Lesen Sie die gesamte Packungsbeilage
LEBEN MIT AML: MEINE PERSÖNLICHE CHECKLISTE
 LEBEN MIT AML: MEINE PERSÖNLICHE CHECKLISTE Leitfaden für Ihr Gespräch mit dem Arzt und praktische Informationen rund um die Erkrankung und ihre Behandlung Was Sie fragen sollten, was Sie wissen sollten
LEBEN MIT AML: MEINE PERSÖNLICHE CHECKLISTE Leitfaden für Ihr Gespräch mit dem Arzt und praktische Informationen rund um die Erkrankung und ihre Behandlung Was Sie fragen sollten, was Sie wissen sollten
Gebrauchsinformation: Information für Patienten. Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt
 Gebrauchsinformation: Information für Patienten Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt Für Erwachsene und Kinder ab 2 Jahren Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Patienten Aspecton Hustentropfen Flüssigkeit zum Einnehmen Thymiankraut-Dickextrakt Für Erwachsene und Kinder ab 2 Jahren Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 31 Schwindeltropfen Mag. Doskar Conium maculatum D4, Veratrum album D4, Anamirta cocculus D4, Secale cornutum D4, Cinchona pubescens D3. Lesen Sie die
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 31 Schwindeltropfen Mag. Doskar Conium maculatum D4, Veratrum album D4, Anamirta cocculus D4, Secale cornutum D4, Cinchona pubescens D3. Lesen Sie die
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 22 Stärkungstropfen für Kinder Mag. Doskar Ferrum phosphoricum D12, Calcium phosphoricum D12, Cinchona pubescens D4 Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 22 Stärkungstropfen für Kinder Mag. Doskar Ferrum phosphoricum D12, Calcium phosphoricum D12, Cinchona pubescens D4 Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 40 Gelenksentzündungstropfen Mag. Doskar Bryonia D4, Colchicum autumnale D4, Rhus toxicodendron (Toxicodendron quercifolium) D4, Echinacea angustifolia
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 40 Gelenksentzündungstropfen Mag. Doskar Bryonia D4, Colchicum autumnale D4, Rhus toxicodendron (Toxicodendron quercifolium) D4, Echinacea angustifolia
FORMULAR FÜR DEN START DER BEHANDLUNG MIT TYSABRI
 Die europäischen Gesundheitsbehörden haben für die Markteinführung von TYSABRI Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information gehört - ist
Die europäischen Gesundheitsbehörden haben für die Markteinführung von TYSABRI Bedingungen auferlegt. Dieser verpflichtende Plan zur Risikoeinschränkung in Belgien - zu dem diese Information gehört - ist
Wichtige Informationen zu Ihrem neuen Arzneimittel
 Wichtige Informationen zu Ihrem neuen Arzneimittel Wichtige Hinweise zur Behandlung Priligy wird zur Behandlung von vorzeitigem Samenerguss (vorzeitiger Ejakulation, Ejaculatio praecox, EP) bei Männern
Wichtige Informationen zu Ihrem neuen Arzneimittel Wichtige Hinweise zur Behandlung Priligy wird zur Behandlung von vorzeitigem Samenerguss (vorzeitiger Ejakulation, Ejaculatio praecox, EP) bei Männern
GEBRAUCHSINFORMATION
 GEBRAUCHSINFORMATION Gebrauchsanweisung Sulgan - Hämorrhoidalsalbe Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte Gebrauchsanweisung sorgfältig durch. Wenden Sie sich an Ihren Arzt oder Apotheker,
GEBRAUCHSINFORMATION Gebrauchsanweisung Sulgan - Hämorrhoidalsalbe Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte Gebrauchsanweisung sorgfältig durch. Wenden Sie sich an Ihren Arzt oder Apotheker,
1 Patienteninformation
 Patienteninformation 1 2 3 4 Verbesserung der Bewegungsfähigkeit Das Gerät GONDOLA wurde entwickelt, um eine AMPS- Behandlung (Automatisierte Mechanische Periphere Stimulation) zu bieten. Die AMPS-Behandlung
Patienteninformation 1 2 3 4 Verbesserung der Bewegungsfähigkeit Das Gerät GONDOLA wurde entwickelt, um eine AMPS- Behandlung (Automatisierte Mechanische Periphere Stimulation) zu bieten. Die AMPS-Behandlung
Anhang III. Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage
 Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des
Anhang III Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des Arzneimittels und der Packungsbeilage Hinweis: Diese Änderungen relevanter Abschnitte der Zusammenfassung der Merkmale des
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER CORASAN Tropfen Wirkstoffe: Crataegus D1, Selenicereus grandiflorus (Cactus) D2, Digitalis purpurea D6, Strophanthus gratus D6. Lesen Sie die
Über die Mitralinsuffizienz und die Mitralklappen-Clip-Therapie
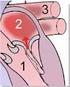 Über die Mitralinsuffizienz und die Mitralklappen-Clip-Therapie Hilfsmittel für Ärzte für die Patienteninformation. Über Mitralinsuffizienz Mitralinsuffizienz oder auch MI - ist eine Erkrankung, die eine
Über die Mitralinsuffizienz und die Mitralklappen-Clip-Therapie Hilfsmittel für Ärzte für die Patienteninformation. Über Mitralinsuffizienz Mitralinsuffizienz oder auch MI - ist eine Erkrankung, die eine
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Tonsipret Tropfen. Wirkstoffe: Capsicum annuum, Guaiacum, Phytolacca americana
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tonsipret Tropfen Wirkstoffe: Capsicum annuum, Guaiacum, Phytolacca americana Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Tonsipret Tropfen Wirkstoffe: Capsicum annuum, Guaiacum, Phytolacca americana Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER VENODRIL Tropfen Wirkstoffe: Aesculus hippocastanum Dil. D6, Hamamelis virginiana Dil. D4, Melilotus officinalis Dil. D6, Silybum marianum Dil. D4 Lesen Sie
Medikationsleitfaden für Patienten
 Mitoxantron Mitoxantron Medikationsleitfaden für Patienten Wichtige obligatorische Informationen zur Risikominimierung für Patienten, die eine Therapie mit RALENOVA /NOVANTRON (Wirkstoff: Mitoxantron)
Mitoxantron Mitoxantron Medikationsleitfaden für Patienten Wichtige obligatorische Informationen zur Risikominimierung für Patienten, die eine Therapie mit RALENOVA /NOVANTRON (Wirkstoff: Mitoxantron)
Forschungsthema: Hypertone Kochsalzlösung Von Peter Bye, MD
 Forschungsthema: Hypertone Kochsalzlösung Von Peter Bye, MD Über hypertone Kochsalzlösung Hypertone Kochsalzlösung (HS) ist einfach eine starke Salzwasserlösung. Die Konzentration beträgt normalerweise
Forschungsthema: Hypertone Kochsalzlösung Von Peter Bye, MD Über hypertone Kochsalzlösung Hypertone Kochsalzlösung (HS) ist einfach eine starke Salzwasserlösung. Die Konzentration beträgt normalerweise
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Nr. 17 Schultropfen für Jugendliche Mag. Doskar Strophanthus gratus D4, Ambra grisea D3.
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 17 Schultropfen für Jugendliche Mag. Doskar Strophanthus gratus D4, Ambra grisea D3. Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 17 Schultropfen für Jugendliche Mag. Doskar Strophanthus gratus D4, Ambra grisea D3. Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DOLPRONE 500 MG TABLETTE. Paracetamol
 Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DOLPRONE 500 MG TABLETTE Paracetamol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für
Seite 1 von 5 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER DOLPRONE 500 MG TABLETTE Paracetamol Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für
Wenn Atemnot das Leben bestimmt
 Linz, 31. Juli 2013 Wenn Atemnot das Leben bestimmt Einmalig für Oberösterreich führt die Lungenabteilung im KH der Elisabethinen eine neue Methode durch, die der Lunge von Patienten mit einem schweren
Linz, 31. Juli 2013 Wenn Atemnot das Leben bestimmt Einmalig für Oberösterreich führt die Lungenabteilung im KH der Elisabethinen eine neue Methode durch, die der Lunge von Patienten mit einem schweren
HUSTEN UND ATEMNOT. Prof. Michael Tamm Chefarzt Klinik für Pneumologie Universitätsspital Basel Leiter Lungenzentrum
 HUSTEN UND ATEMNOT Prof. Michael Tamm Chefarzt Klinik für Pneumologie Universitätsspital Basel Leiter Lungenzentrum Epidemiologie Husten jede zweite Person leidet manchmal jede sechste Person leidet ständig
HUSTEN UND ATEMNOT Prof. Michael Tamm Chefarzt Klinik für Pneumologie Universitätsspital Basel Leiter Lungenzentrum Epidemiologie Husten jede zweite Person leidet manchmal jede sechste Person leidet ständig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Prospan Hustenliquid Flüssigkeit zum Einnehmen Wirkstoff: Efeublättertrockenextrakt
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Prospan Hustenliquid Flüssigkeit zum Einnehmen Wirkstoff: Efeublättertrockenextrakt Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Prospan Hustenliquid Flüssigkeit zum Einnehmen Wirkstoff: Efeublättertrockenextrakt Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 35 Reizblasentropfen Mag. Doskar Petroselinum crispum convar. crispum D1, Causticum Hahnemanni D6, Solanum dulcamara D3, Lytta vesicatoria D6 Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Nr. 35 Reizblasentropfen Mag. Doskar Petroselinum crispum convar. crispum D1, Causticum Hahnemanni D6, Solanum dulcamara D3, Lytta vesicatoria D6 Lesen Sie
Bedienungsanleitung 5 AX 100
 Bedienungsanleitung 5 AX 100 SCHENKE 5.1 CLAMPING SYSTEM Stand: 25.01.2007 Inhaltsverzeichnis: 1. EINLEITUNG 2. SICHERHEITS- UND WARNHINWEISE 3.1 BESCHREIBUNG DES SPANNERS 3.2 TECHNISCHE DATEN 3.3 ZUSAMMENBAU
Bedienungsanleitung 5 AX 100 SCHENKE 5.1 CLAMPING SYSTEM Stand: 25.01.2007 Inhaltsverzeichnis: 1. EINLEITUNG 2. SICHERHEITS- UND WARNHINWEISE 3.1 BESCHREIBUNG DES SPANNERS 3.2 TECHNISCHE DATEN 3.3 ZUSAMMENBAU
