Kapitel 2. März Stefanie Hellbach 1
|
|
|
- Anke Böhmer
- vor 6 Jahren
- Abrufe
Transkript
1 Kapitel 2 Auswirkungen der industriellen Nutzung von Wasser, Säuren, Basen und Salzen auf Menschen und Umwelt Behandlung von Materialien Schutzmaßnahmen für Mensch und Umwelt Stefanie Hellbach 1
2 Säuren Sauerstoffhaltige Säuren Sauerstofffreie Säuren Dissoziation: Wasserstoffionen H + und Säurerestionen Elektrolyt: Lösung ist elektrisch leitend Stefanie Hellbach 2
3 Basen/Laugen Entstehung bei Reaktion von Metalloxid mit Wasser Alkalimetall mit Wasser Hydroxide: feste Stoffe Dissoziation: Metallion und Hydroxidion OH - Stefanie Hellbach 3
4 Nachweis von Säuren und Basen Farbindikatoren, z. B. Lackmuspapier Stefanie Hellbach; Quelle Bild: Dreamstime.de 4
5 Konzentration von Säuren und Basen Maß für die Stärke einer Säure/Lauge = ü.. ü Starke Säuren: Salzsäure, Schwefelsäure Starke Laugen: Natronlauge, Kalilauge Stefanie Hellbach 5
6 ph-wert ph-wert: Maßzahl zwischen 0 und 14 Er gibt an, wie viele H + bzw. OH - -Ionen in einer Lösung enthalten sind ph < 7 als saurewässrige Lösung ph = 7 als neutralewässrige Lösung ph > 7 als basische(alkalische) wässrige Lösung Anwendung: Lebensmittelherstellung, Medizin, Bodenbeschaffenheit Stefanie Hellbach; Quelle Bild: laborfachhandel-opel.de 6
7 Umgang mit Säuren und Basen Ätzend, giftig S/B als Feststoff reagieren mit Schweiß der Haut oder Feuchtigkeit der Schleimhäute sowie Luftfeuchtigkeit Schutzmaßnahmen: Schutzausrüstung (Brille, Kleidung) Nur vorgesehene Behälter nutzen, wegschließen Dämpfe nicht direkt einatmen Stefanie Hellbach 7
8 Technische Anwendung von Säuren und Basen Säuren: Laugen: Düngemittel, Farben, Herstellung von Lacke, Heilmittel, Seifen, Natriumsalz, Elektrolyt in Batterien, Farbmittel, Farbstoffe, zum Reinigen oder Kalkmörtel, Pflanzen- Aufrauen von schutzmittel, Oberflächen Wasserenthärtung Stefanie Hellbach 8
9 Salzbildung und Neutralisation Positiv geladene Metallionen und negativ geladene Säurerestionen Kristallgitter Säuren und Basen neutralisieren sich, es entsteht ein gelöstes Salz und Wasser Beispiel: Natronlauge und Salzsäure ergibt Kochsalz und Wasser Ableitung des Namens von der beteiligten Säure Stefanie Hellbach 9
10 Wasser (1/4) Wasserart Trinkwasser (Lebensmittel) Brauchwasser Destilliertes Wasser Schwebstoffe herausfiltern, destillieren Vollentsalztes Wasser Schwebstoffe herausfiltern, vollständiges Entsalzen im Ionentauscher Stefanie Hellbach 10
11 Wasser (2/4) Regenwasser Reinstes natürliches Wasser, saurer Regen Oberflächenwasser Regen/Schnee, versickert oder direkt in Gewässer Grundwasser Wasserundurchl. Bodenschicht Brunnen-/Quellwasser Stefanie Hellbach ; Quelle Bild: historischer Verein Durlach 11
12 Wasser (3/4) Fluss-, Seewasser Grund-/Oberflächenwasser, Abwasser Meerwasser Salzwasser, kann ohne Aufbereitung (Entsalzung) nicht genutzt werden Wasserkreislauf: verdunstet Wasser, bilden sich Wasserdampf/Wolken, es entstehen Niederschläge Wasseraufbereitung wird aufwendiger Grundwasserspiegel sinken Stefanie Hellbach 12
13 Wasser (4/4) Brauchwasser und Trinkwasser Trinkwasser ist das wichtigste Lebensmittel Hohe Qualitätsansprüche Brauchwasser: keine Rückstände oder Korrosion Möglichst geschlossene Kreisläufe Anwendung vielfältig: Kühlen, Energieträger, Reinigung, Werkzeug, Elektrolyt, Prozessdampf Stefanie Hellbach 13
14 Wasserhärte (1/2) Kesselstein: Carbonate oder Sulfate Bildung bei mehr als 60 C Problem: Kesselexplosion, Energieverbrauch Legionellenausbreitung bei weniger als 60 C Hartes Wasser erhöht den Seifenverbrauch Stefanie Hellbach 14
15 Wasserhärte (2/2) Permanente Härte, Nicht-Carbonhärte, z. B. Calciumsulfat Temporäre Härte: Carbonathärte-> Kesselstein 1 dh entspricht 0,178 mmol/liter Calcium-/Magnesiumoxid Vier Härtebereiche Ionentauscher zur Wasserenthärtung Stefanie Hellbach; Quelle Tabelle: Wikipedia.de 15
16 Wasseraufbereitung Verunreinigungen herausfiltern Desinfektion mit Chlor/Ozonisierung Entkeimen durch UV-Bestrahlung Entsalzung durch Ionentauscher Physikalische Wasseraufbereitung Härtestabilisierung Chemische Wasseraufbereitung Ionentauscher Stefanie Hellbach 16
17 Reinigung Säuren und Basen reinigen Metalle Konzentrierte Salzsäure: Oxidschutzschicht Königswasser löst auch Gold auf Stefanie Hellbach 17
18 Umweltschutz Gesetze und Verordnungen Chemikaliengesetz Gefahrstoffverordnung Wasserhaushaltsgesetz Bundesimmissionsschutzgesetz Technische Anleitung (TA) Luft Primärmaßnahmen: vermeiden, recyceln Sekundärmaßnahmen: reinigen, aufbereiten Stefanie Hellbach 18
19 Back Up Stefanie Hellbach 19
20 Saurer Regen Hauptverantwortlich für sauren Regen ist die Luftverschmutzung durch Abgase. Insbesondere durch Einsatz schwefelhaltiger fossiler Brennstoffe wie Kohle und Heizöl entstehen Schwefeloxide (SO x ) die mit Wasser Schwefelsäure (H 2 SO 4 ) bilden Weiterhin entstehen bei jeder Verbrennung Stickoxide (NO x ) durch Umwandlung des im Brennstoff und in der Luft enthaltenen Stickstoffes. Diese bilden mit Wasser und Sauerstoff Salpetersäure (HNO 3 ). Die Schwefelsäure ist zu etwa 2/3, die Salpetersäure zu etwa 1/3 für die Versauerung der Niederschläge verantwortlich. Global wirkt sich auch das bei der Verbrennung der o.g. fossilen Brennstoffe freiwerdende Kohlendioxid (CO 2 ) aus. Zwar ist CO 2 ein Hauptbestandteil der Atmosphäre, aber durch die Verbrennung fossiler Brennstoffe steigt der CO 2 Gehalt der Atmosphäre. Dies führt neben dem Treibhauseffekt auch zu einer weiteren Absenkung des eingangs genannten natürlichen ph-wertes des Regens, da dadurch mehr Kohlensäure gebildet werden kann. Kohlendioxid (CO 2 ) löst sich in Wasser und reagiert zu ca. 0,2% mit Wasser unter Bildung von Kohlensäure. In tropischen Gebieten können auch organische Säuren, z. B. Ameisensäure (HCOOH), einen wesentlichen Anteil an der Absenkung des ph-wertes von Niederschlägen haben. Stefanie Hellbach 20
21 Auswirkungen auf Pflanzen und Gewässer Saurer Regen kann durch die Versauerung des Bodens Pflanzen schädigen und wurde ursächlich mit Baumschädigungen ("Waldsterben") in Verbindung gebracht. Die im Wesentlichen betroffenen Wälder liegen in Regionen mit häufigen und ergiebigen Niederschlägen, die zudem relativ niedrige Jahresdurchschnittstemperaturen aufweisen. Dies trifft in Deutschland insbesondereauf Wälder in höheren Lagen der Mittelgebirge und der Alpen zu. Da die aufgetretenen Krankheitsbilder sehr unterschiedlich sind (neben gesunden Beständen kommen in vergleichbarer Lage auch stark geschädigte vor), werden neben den sauren Niederschlägen heute auch noch andere Ursachen für die Baumschädigungen vermutet (natürliche Schwankungen der Anfälligkeit gegenüber Bodenversauerung, Änderungen des Klimas) bzw. nachgewiesen (Mineralienmangel, Schädigung geschwächter Bäume durch Pilze, Bakterien, waldbauliche Fehler). Durch die Übersäuerung des Bodens wird die natürliche Zusammensetzung des Bodens gestört. Es werden giftige Schwermetallionen freigesetzt, die die Feinwurzeln der Bäume absterben lassen. Dadurch entstehen Störungen im Wasser-und Nährstoffhaushalt des Baumes, und seine Widerstandskraft nimmt stark ab. Diese Bäume sind nun anfälliger was Krankheiten und natürliche Belastungen betrifft. Selbst Bodenfrost oder ein Schädlingsbefall können jetzt erhebliche Schäden anrichten. Durch den sauren Regen werden also nicht nur die Jungbäume am Wachstum behindert, sondern auch die ausgewachsenen Bäume werden stark geschädigt. Zunächst wirkt sich der Befall auf die Blatt-oder Nadelkronen der Bäume aus, die Blätter oder Nadeln werden abgeworfen. Dies führt zu einer Kronenverlichtung. Außerdem kann Wipfeldürreentstehen und der Baum schließlich absterben. Damit ist saurer Regen eine der Ursachen für das Waldsterben. Gewässer werden zunehmend durch Säureeintrag belastet. Dabei erfolgt der Säureeintrag weniger direkt über die sauren Niederschläge als eher indirekt über die Zuflüsse. Durch den Bodenabfluss und als Folge des Säureeintrags reichern sich im Wasser Metall-Kationen, z.b. Al 3+, an, die als Zellgifte wirken und zu einer Artenverarmung führen können. Die Geologie der Einzugsgebiete von Flüssen und Seen hat weiterhin einen großen Einfluss auf die Versauerung. Stehen im Einzugsgebiet vor allem Gesteine an, die kaum neutralisierend auf den sauren Regen wirken (z.b. Granit, Gneis, Sandstein), sind diese Gewässer von der Versauerung besonders betroffen. Umgekehrt haben Gewässer, die im Einzugsgebiet große Kalksteinvorkommen haben, kaum Probleme mit der Versauerung. Der Anstieg der CO 2 -Konzentration in der Atmosphäre kann darüber hinaus zu einer Versauerung der Ozeane führen und könnte so eine Bedrohung für das Fortbestehen der ozeanischen Biosphäre darstellen, da sich beispielsweise ab einem bestimmten ph-wert die Kalkschalen von Muscheln und Schnecken auflösen. Stefanie Hellbach 21
22 Auswirkungen auf Gebäude Der saure Regen greift insbesondere Sand-und Kalkstein an, aber auch Betonkonstruktionen. Dadurch schreitet die Verwitterung von Gebäuden wesentlich schneller voran und zahlreiche Gebäude und Kulturdenkmäler werden so stark beschädigt oder zerstört. Marmor löst sich in Säuren, da er aus Calciumcarbonat besteht. Wenn saurer Regen auf Marmor trifft, entstehen vielfältige Schäden. Dazu gehören angeraute Oberflächen, Abtragung von Material und Verlust von gemeißelten Feinstrukturen. Die Zerstörung kann die gesamte Fläche betreffen oder punktuell an reaktiven Stellen auftreten. Das Calciumcarbonat reagiert mit den gelösten Wasserstoffionen im sauren Regen. Dann reagieren die Sulfationender Schwefelsäure mit den Calciumionenund überziehen den Marmor oder Kalkstein mit einer weißen Schicht von Gips. Ca 2+ +SO H 2 O CaSO 4 + 2H 2 O Der Regen trägt mit der Zeit einen Teil der Gipskruste ab. Dies führt zu kleinen Rissen und zunehmender Erosion. Die Wiederherstellung von beschädigtem Kulturgut und Gebäuden ist sehr kostspielig. Allein für die WestminsterAbbey in London wurden bis zum Jahr 1990 bis zu 10 Mio. Pfund ausgelegt, um vom sauren Regen verursachte Schäden zu beseitigen. In Geld nicht aufzuwiegen sind jedoch die Schäden an den Kulturschätzen der Erde. TajMahalin Indien und die Akropolis in Athen hatten ebenso unter der Säureeinwirkung zu leiden wie das kanadische Parlamentsgebäude oder das US Capitol. Stefanie Hellbach 22
23 Gegenmaßnahmen Als Gegenmaßnahme versucht man in vielen Gegenden Europas (in der Schweiz verboten), mit Kalk die Übersäuerung zu neutralisieren. Vielerorts werden hierzu große Mengen Kalk per Hubschrauber verstreut. In der Nähe von Kalk-oder Zementwerken mit schlechter Entstaubung kann die unbeabsichtigte Emission von Kalkstaub im Extremfall sogar zur Umkehrung des Phänomens führen und es entsteht basischer Regen. Ein solcher Effekt kann auch eintreten, wenn große Mengen Asche oder andere basische Stäube in die Luft geraten, etwa als Folge großflächiger Waldbrände oder eines Vulkanausbruches. Man ist seit den 80er-Jahren dazu übergegangen, Rauchgase zu entschwefeln. Dabei wird das SO 2 aus dem Abgas entfernt und meist zu CaSO 4 (Gips) umgesetzt, welches sich nutzen oder deponieren lässt. Dies ist bei Transportmitteln wie Automobilen, Flugzeugen etc. jedoch nicht möglich. Daher wird aus Kraftstoffen wie Benzin, Diesel, Kerosin und Erdgas der Schwefel mittels spezieller Verfahren entfernt, wodurch zumindest in den Industrieländern der Eintrag von SO 2 in die Atmosphäre erheblich verringert werden konnte. Das Entfernen der Stickstoffoxide gestaltet sich dagegen erheblich schwieriger. Diese entstehen ab einer bestimmten Temperatur bei allen Verbrennungsprozessen, sofern nicht in stickstofffreier Atmosphäre gearbeitet wird. Dies ist kaum bzw. nur mit großem Aufwand möglich, da unsere Atmosphäre zu 78,09 % aus Stickstoff besteht. Deshalb müssten die Stickstoffoxide aus dem Abgas entfernt werden, was in Autokatalysatoren geschieht, jedoch nicht zu 100 % (siehe Lambda- Fenster). Stickstoffoxide zusammen mit der UV-Strahlung der Sonne sind auch die Hauptursache für das Entstehen von bodennahem Ozon. Somit bräuchte man entweder andere Katalysatoren, oder man müsste den Verbrennungsmotor z.b. durch einen Elektromotor ersetzen. Stefanie Hellbach 23
Wiederholung und Aufgaben zur Vorlesung NTG -Chemie (Kapitel 2) November 2014 Stefanie Hellbach
 Wiederholung und Aufgaben zur Vorlesung NTG -Chemie (Kapitel 2) 1 Aufgaben (1) Nennen Sie Beispiele für sauerstoffhaltige Säuren Schwefelsäure H 2 SO 4 Kohlensäure H 2 CO 3 Salpetersäure HNO Nennen Sie
Wiederholung und Aufgaben zur Vorlesung NTG -Chemie (Kapitel 2) 1 Aufgaben (1) Nennen Sie Beispiele für sauerstoffhaltige Säuren Schwefelsäure H 2 SO 4 Kohlensäure H 2 CO 3 Salpetersäure HNO Nennen Sie
Biologie-Projekt. Saurer Regen ATHENE SAKELLARIOU HEIMBERGER HOLGER INA. -Team LANGLOTZ DANIEL VOLLBRECHT
 Biologie-Projekt Saurer Regen AT INA HO VO -Team ATHENE SAKELLARIOU INA HEIMBERGER HOLGER LANGLOTZ DANIEL VOLLBRECHT Präsentationsgliederung Vorversuch Hauptversuch Auswertung Recherche Ina Daniel Daniel
Biologie-Projekt Saurer Regen AT INA HO VO -Team ATHENE SAKELLARIOU INA HEIMBERGER HOLGER LANGLOTZ DANIEL VOLLBRECHT Präsentationsgliederung Vorversuch Hauptversuch Auswertung Recherche Ina Daniel Daniel
Säuren, Basen, Salze
 Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
Säuren, Basen, Salze Namensgebung (=Nomenklatur) Es gibt für chemische Verbindungen grundsätzlich zwei Arten von Namen: Trivialname der alltäglich bzw. umgangssprachlich benutzte Name z. B.: Wasser, Salzsäure,
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
B Chemisch Wissenwertes. Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden.
 -I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
-I B.1- B C H E M I S C H W ISSENWERTES 1 Säuren, Laugen und Salze 1.1 Definitionen von Arrhénius Arrhénius gab 1887 Definitionen für Säuren und Laugen an, die seither öfter erneuert wurden. Eine Säure
Natürliche ökologische Energie- und Stoffkreisläufe
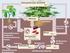 Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Schwefeldioxid. Schwefel (S) verbindet sich bei der Verbrennung mit Sauerstoff (O 2 ). Das Ergebnis ist Schwefeldioxid: SO 2.
 Standzylinder Verbrennungslöffel Deckglas Schwefel Brenner Gib etwas Schwefel auf den Verbrennungslöffel und entzünde ihn mit der rauschenden Brennerflamme. Baue den Versuch nach der Abbildung auf und
Standzylinder Verbrennungslöffel Deckglas Schwefel Brenner Gib etwas Schwefel auf den Verbrennungslöffel und entzünde ihn mit der rauschenden Brennerflamme. Baue den Versuch nach der Abbildung auf und
Der ph-wert. Warum ist der so wichtig?
 Der ph-wert Warum ist der so wichtig? Den Hinweis dafür, daß Ihr Schwimmbadwasser und alles drumherum. nur dann in Ordnung sein kann wenn der ph-wert stimmt, den bekommen Sie täglich aus Broschüren, Büchern
Der ph-wert Warum ist der so wichtig? Den Hinweis dafür, daß Ihr Schwimmbadwasser und alles drumherum. nur dann in Ordnung sein kann wenn der ph-wert stimmt, den bekommen Sie täglich aus Broschüren, Büchern
Eigenschaften von H 2 S
 Eigenschaften von H 2 S sehr giftiges, brennbares, unangenehm faulig riechendes Gas Smp. -86 C, Sdp. -60,2 C mäßig wasserlöslich, gesättigte Lösung hat c = 0,1 mol/l schwache, zweiprotonige Säure H 2 S
Eigenschaften von H 2 S sehr giftiges, brennbares, unangenehm faulig riechendes Gas Smp. -86 C, Sdp. -60,2 C mäßig wasserlöslich, gesättigte Lösung hat c = 0,1 mol/l schwache, zweiprotonige Säure H 2 S
Der Einfluss des Wassers auf die Qualität der Kühlschmierstoff-Emulsion
 Der Einfluss des Wassers auf die Qualität der KühlschmierstoffEmulsion Markus Kühni, Leiter Kundendienst Blaser Swisslube AG Winterseistrasse 3415 HasleRüegsau Tel: 034 460 01 01 email: contact@blaser.com
Der Einfluss des Wassers auf die Qualität der KühlschmierstoffEmulsion Markus Kühni, Leiter Kundendienst Blaser Swisslube AG Winterseistrasse 3415 HasleRüegsau Tel: 034 460 01 01 email: contact@blaser.com
Was verschmutzt die Luft?
 6A Lehrerkommentar MST Ziele Arbeitsauftrag Material Sozialform Zeit Die Kinder wissen, dass die Verbrennung von Energieträgern in vielen Fällen zu Luftverschmutzung führt. Sie kennen zudem einige Abgasverursacher
6A Lehrerkommentar MST Ziele Arbeitsauftrag Material Sozialform Zeit Die Kinder wissen, dass die Verbrennung von Energieträgern in vielen Fällen zu Luftverschmutzung führt. Sie kennen zudem einige Abgasverursacher
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer. Brennstoffe. Wir Unterscheiden grundsätzlich Brennstoffe in:
 Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
Lehrabschlussprüfungs Vorbereitungskurs Rauchfangkehrer Wir Unterscheiden grundsätzlich in: Feste Flüssige Gasförmige Biomasse Feste Torf Holz Kohle Brikett Koks Anthrazit Holz: Anwendung: Kachelofen,
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
1.3 Chemische Reaktionen des Wassers - Bildung von Säuren und Basen
 1.3 Chemische Reaktionen des Wassers Bildung von Säuren und Basen Säure und Basebegriff nach Arrhenius (1887) Wasser reagiert mit Nichtmetalloxiden (Säureanhydriden) zu Säuren. Die gebildete Säure löst
1.3 Chemische Reaktionen des Wassers Bildung von Säuren und Basen Säure und Basebegriff nach Arrhenius (1887) Wasser reagiert mit Nichtmetalloxiden (Säureanhydriden) zu Säuren. Die gebildete Säure löst
Wasser und Abwasser. 1.Kapitel: Die Bedeutung des Wassers
 Wasser und Abwasser 1.Kapitel: Die Bedeutung des Wassers Wer Durst hat, muss trinken. Wasser ist unser wichtigstes Lebensmittel und ohne Zufuhr von Süßwasser stirbt ein Mensch nach wenigen Tagen. Nicht
Wasser und Abwasser 1.Kapitel: Die Bedeutung des Wassers Wer Durst hat, muss trinken. Wasser ist unser wichtigstes Lebensmittel und ohne Zufuhr von Süßwasser stirbt ein Mensch nach wenigen Tagen. Nicht
Pflanz en und ihre ph-vorlieben
 Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Grundlagen Chemie. Dipl.-Lab. Chem. Stephan Klotz. Freiwill ige Feuerwehr Rosenheim
 Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
Grundlagen Dipl.-Lab. Chem. Stephan Klotz Freiwill ige Feuerwehr Rosenheim Einführung Lernziele Einfache chemische Vorgänge, die Bedeutung für die Feuerwehrpraxis haben, erklären. Chemische Grundlagen
1.5 Säuren und Basen und der ph-wert
 Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
Seite 14 1.5 Säuren und Basen und der ph-wert 1.5.1 Säuren Geschichtlich bedingte Definition: Eine Säure ist ein Stoff, dessen wässrige Lösung sauer schmeckt oder ätzend wirkt, bzw. andere Stoffe angreift.
Inhalt. Methode Methode Aktion. Aktion Fakten Projekt Projekt Projekt Projekt. Ausblick Aktion Fakten Ausblick Methode Ausblick Wissen & Training
 Stoffe im Alltag 8 Experimentieren in der Chemie 10 Wärmequellen im Unterricht 12 Sicherheit in der Chemie Lernen an Stationen 14 Stoffe und ihren Eigenschaften 16 Den Stoffen auf der Spur 16 Körper und
Stoffe im Alltag 8 Experimentieren in der Chemie 10 Wärmequellen im Unterricht 12 Sicherheit in der Chemie Lernen an Stationen 14 Stoffe und ihren Eigenschaften 16 Den Stoffen auf der Spur 16 Körper und
Dissoziation, ph-wert und Puffer
 Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
Dissoziation, ph-wert und Puffer Die Stoffmengenkonzentration (molare Konzentration) c einer Substanz wird in diesem Text in eckigen Klammern dargestellt, z. B. [CH 3 COOH] anstelle von c CH3COOH oder
CHEMIE KAPITEL 4 SÄURE- BASE. Timm Wilke. Georg- August- Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
CHEMIE KAPITEL 4 SÄURE- BASE Timm Wilke Georg- August- Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Historisches Im 17. Jahrhundert wurden von Robert Boyle Gemeinsamkeiten verschiedener Verbindungen
Zusammenfassung: Säure Base Konzept
 Zusammenfassung: Säure Base Konzept 1. Grundlegende Eigenschaften von Säuren und Laugen Säure und Laugen ätzen sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator.
Zusammenfassung: Säure Base Konzept 1. Grundlegende Eigenschaften von Säuren und Laugen Säure und Laugen ätzen sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator.
1/6. Welche Antwort ist richtig: Wie entsteht aus organischen Kohlenstoffverbindungen das gasförmige Kohlendioxid?
 1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
1/6 Der Kohlenstoffkreislauf Arbeitsblatt B Material: Inhalte des Factsheets Grundlagen zum Klimawandel Der Wasserkreislauf (siehe Arbeitsblatt A) ist leicht erklärt: Wasser verdunstet, in höheren Schichten
Inhaltsverzeichnis. Vorwort Zur Gestaltung des Buches
 Hans Rudolf Christen Struktur Stoff Reaktion Allgemeine und anorganische Chemie Sekundarstufe I 5401 Diesterweg Salle Frankfurt am Main Berlin München Verlag Sauerländer Aarau Vorwort Zur Gestaltung des
Hans Rudolf Christen Struktur Stoff Reaktion Allgemeine und anorganische Chemie Sekundarstufe I 5401 Diesterweg Salle Frankfurt am Main Berlin München Verlag Sauerländer Aarau Vorwort Zur Gestaltung des
Gliederung: 1. Einführung. 2. Schadstoffe. 3. Entstehung. 4. Hauptverursacher. 5. Folgen. 6. Gegenmaßnahmen beim Verkehr
 Gliederung: 1. Einführung 2. Schadstoffe 3. Entstehung 4. Hauptverursacher 5. Folgen 6. Gegenmaßnahmen beim Verkehr Luftverunreinigungen: Sämtliche feste, flüssige und gasförmige Substanzen, die in der
Gliederung: 1. Einführung 2. Schadstoffe 3. Entstehung 4. Hauptverursacher 5. Folgen 6. Gegenmaßnahmen beim Verkehr Luftverunreinigungen: Sämtliche feste, flüssige und gasförmige Substanzen, die in der
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Eigenschaften Reinstoffe Elemente Kugelteilchen Elementes Atom
 Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Einstieg: Atom Der Chemiker will alles genau untersuchen, um die Eigenschaften von Stoffen heraus zu finden. Er trennt Gemische in Reinstoffe. Er analysiert Reinstoffe, so dass sie in ihre Elemente zerfallen.
Chemisches Grundpraktikum
 Chemisches Grundpraktikum Lehrerhandbuch für die Sekundarstufe I Von Prof. Dr. Hermann Raaf und Prof. Martin Radau A Bibliothek Band 1 Anorganische Chemie d. Fachbereichs 3 der Technischen Hochschule Darmsfadt
Chemisches Grundpraktikum Lehrerhandbuch für die Sekundarstufe I Von Prof. Dr. Hermann Raaf und Prof. Martin Radau A Bibliothek Band 1 Anorganische Chemie d. Fachbereichs 3 der Technischen Hochschule Darmsfadt
Crashkurs Säure-Base
 Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
Crashkurs Säure-Base Was sind Säuren und Basen? Welche Eigenschaften haben sie?` Wie reagieren sie mit Wasser? Wie reagieren sie miteinander? Wie sind die Unterschiede in der Stärke definiert? Was ist
die WASSER WERKSTATT
 die WASSER WERKSTATT Inhalt: Die Mehrheit der Organismen auf unserer Erde lebt in Gewässern. Und alle egal, ob Mensch, Tier oder Pflanze sind abhängig vom Wasser. Die meisten Lebewesen bestehen sogar zu
die WASSER WERKSTATT Inhalt: Die Mehrheit der Organismen auf unserer Erde lebt in Gewässern. Und alle egal, ob Mensch, Tier oder Pflanze sind abhängig vom Wasser. Die meisten Lebewesen bestehen sogar zu
Biologie Referat für Felix
 Biologie Referat für Felix Sehr geehrter Herr Professor, liebe Mitschüler. Wir möchten euch mit unserem heutigen Referat das Wasser ein bißchen näher vorstellen. Wir haben unser Referat in 3 Abschnitte
Biologie Referat für Felix Sehr geehrter Herr Professor, liebe Mitschüler. Wir möchten euch mit unserem heutigen Referat das Wasser ein bißchen näher vorstellen. Wir haben unser Referat in 3 Abschnitte
Inhalt. Was ist Chemie? 11
 Inhalt Was ist Chemie? 11 Überall Chemie 12 Chemie Chancen und Gefahren* 14 Umgang mit Chemikalien 16 Typische Tätigkeiten in der Chemie 18 Methode Regeln beim Experimentieren 19 Methode Umgang mit dem
Inhalt Was ist Chemie? 11 Überall Chemie 12 Chemie Chancen und Gefahren* 14 Umgang mit Chemikalien 16 Typische Tätigkeiten in der Chemie 18 Methode Regeln beim Experimentieren 19 Methode Umgang mit dem
Expertenwissen: DARSTELLUNG VON POTTASCHE (historischer Text)
 HTBL-PINKAFELD Arbeitsblatt A4/1 Carbonate: POTTASCHE Expertenwissen: DARSTELLUNG VON POTTASCHE (historischer Text) QUELLE: KRÄTZ, O.: Historische chemische Versuche, Aulis Verlag Deubner & Co KG Köln,
HTBL-PINKAFELD Arbeitsblatt A4/1 Carbonate: POTTASCHE Expertenwissen: DARSTELLUNG VON POTTASCHE (historischer Text) QUELLE: KRÄTZ, O.: Historische chemische Versuche, Aulis Verlag Deubner & Co KG Köln,
Regenwasseranalyse. Fachspezifische Themenstellung. Verena Burgstaller und Lisa Lienbacher
 Regenwasseranalyse Fachspezifische Themenstellung Verena Burgstaller und Lisa Lienbacher Inhaltsverzeichnis Einleitung Das wichtigste und zugleich auch schwerste bei diesem Projekt ist es, zu regelmäßigen
Regenwasseranalyse Fachspezifische Themenstellung Verena Burgstaller und Lisa Lienbacher Inhaltsverzeichnis Einleitung Das wichtigste und zugleich auch schwerste bei diesem Projekt ist es, zu regelmäßigen
Das Formelpuzzle Kopiervorlage
 Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
Das Formelpuzzle Kopiervorlage Die Vorlage wird foliert, die einzelnen Bausteine werden ausgeschnitten. Durch einfaches Aneinanderlegen von Kationen und Anionen können die Formeln von Säuren, Basen und
1.6 ph-werte. Einführung Chemie Seite 19
 Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
Seite 19 1.6 ph-werte Säuren und Basen werden stets als Lösungen in verschiedenen Konzentrationen gebraucht. Die Stärke einer Säure wird durch ihren ph Wert festgelegt, während die Stärke einer Base durch
C Säure-Base-Reaktionen
 -V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
-V.C1- C Säure-Base-Reaktionen 1 Autoprotolyse des Wassers und ph-wert 1.1 Stoffmengenkonzentration Die Stoffmengenkonzentration eines gelösten Stoffes ist der Quotient aus der Stoffmenge und dem Volumen
Posten 3: Umwelt und Erdgas
 Anleitung Schüler Posten 3: Umwelt und Erdgas Ziel: Du kennst die unterschiedlichen Umweltbelastungen von verschiedenen Energiequellen und kennst die ökologischen und wirtschaftlichen Vorteile von Erdgas.
Anleitung Schüler Posten 3: Umwelt und Erdgas Ziel: Du kennst die unterschiedlichen Umweltbelastungen von verschiedenen Energiequellen und kennst die ökologischen und wirtschaftlichen Vorteile von Erdgas.
Bestimmung des ph-wertes des Bodens
 Bestimmung des ph-wertes des Bodens Durch den ph-wert erhältst du eine Angabe zum Säuregehalt. Er wird im Bereich zwischen 1 (sehr sauer!!!) und 14 (sehr basisch!) angegeben. Bei einem ph-wert von 7 spricht
Bestimmung des ph-wertes des Bodens Durch den ph-wert erhältst du eine Angabe zum Säuregehalt. Er wird im Bereich zwischen 1 (sehr sauer!!!) und 14 (sehr basisch!) angegeben. Bei einem ph-wert von 7 spricht
Zusatzstation: Klimalexikon Anleitung
 Anleitung Die Lexikonkarten liegen verdeckt vor euch. Mischt die Karten. Jeder Spieler zieht zwei Karten. Lest die Begriffe auf den Karten. Erklärt die Begriffe euren Mitspielern mit Hilfe des Bildes.
Anleitung Die Lexikonkarten liegen verdeckt vor euch. Mischt die Karten. Jeder Spieler zieht zwei Karten. Lest die Begriffe auf den Karten. Erklärt die Begriffe euren Mitspielern mit Hilfe des Bildes.
GYMNASIUM HARKSHEIDE. Schulinternes Fachcurriculum Chemie Sek I (G 9; Beginn des Chemieunterrichts: Klasse 8)
 GYMNASIUM HARKSHEIDE Schulinternes Fachcurriculum Chemie Sek I (G 9; Beginn des Chemieunterrichts: Klasse 8) Klassenstufe 8 Erstellt auf Beschluss der Fachkonferenz, März 2009 0. Einführung: Sicheres Arbeiten
GYMNASIUM HARKSHEIDE Schulinternes Fachcurriculum Chemie Sek I (G 9; Beginn des Chemieunterrichts: Klasse 8) Klassenstufe 8 Erstellt auf Beschluss der Fachkonferenz, März 2009 0. Einführung: Sicheres Arbeiten
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Säure-Base-Reaktion. Versuch 5.1 5.2. Neutralisation, Gehaltsbestimmungen und Titrationskurven
 Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Klimasystem. Das Klima der Erde und wie es entsteht: Definition Klima
 Das Klima der Erde und wie es entsteht: Definition Klima Unter dem Begriff Klima verstehen wir die Gesamtheit der typischen Witterungsabläufe an einem bestimmten Ort oder in einer bestimmten Region über
Das Klima der Erde und wie es entsteht: Definition Klima Unter dem Begriff Klima verstehen wir die Gesamtheit der typischen Witterungsabläufe an einem bestimmten Ort oder in einer bestimmten Region über
Themengebiet: 1 HA + H 2 O A - + H 3 O + H 3 O + : Oxonium- oder Hydroxoniumion. Themengebiet: 2 B + H 2 O BH + + OH - OH - : Hydroxidion
 1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
1 1 Säuren sind Protonendonatoren, d.h. Stoffe, die an einen Reaktionspartner ein oder mehrere Protonen abgeben können; Säuredefinition nach Brönsted Im Falle von Wasser: HA + H 2 O A - + H 3 O + H 3 O
Wasserstoff/Hydrogen-Forum für Einsteiger
 Wasserstoff/Hydrogen-Forum für Einsteiger Energie? Wofür brauchen wir die eigentlich? Auch wenn es uns kaum bewußt ist, unser aller Leben ist stark mit dem Begriff "Energie" verknüpft. Ohne Energie funktioniert
Wasserstoff/Hydrogen-Forum für Einsteiger Energie? Wofür brauchen wir die eigentlich? Auch wenn es uns kaum bewußt ist, unser aller Leben ist stark mit dem Begriff "Energie" verknüpft. Ohne Energie funktioniert
Professur Radiochemie Sommersemester 2009
 Professur Radiochemie Sommersemester 2009 Vorlesung: Umweltchemie Gliederung: 0 Einleitung 0.1 Vorbemerkungen 0.2 Definition Umweltchemie 1 Entstehung der Umwelt 1.1 Bildung der Elemente 1.2 Aufbau der
Professur Radiochemie Sommersemester 2009 Vorlesung: Umweltchemie Gliederung: 0 Einleitung 0.1 Vorbemerkungen 0.2 Definition Umweltchemie 1 Entstehung der Umwelt 1.1 Bildung der Elemente 1.2 Aufbau der
LEHRPLANÜBERSICHT: CHEMIE, KLASSE 7-10 (STAND: JANUAR 2010)
 LEHRPLANÜBERSICHT: CHEMIE, KLASSE 7-10 (STAND: JANUAR 2010) Regelschule Förderschule/Lernen Förderschule/Geistige Entwicklung Anmerkungen Regelschule Klasse 7 1. Stoffe und ihre Eigenschaften 9. Gegenstand
LEHRPLANÜBERSICHT: CHEMIE, KLASSE 7-10 (STAND: JANUAR 2010) Regelschule Förderschule/Lernen Förderschule/Geistige Entwicklung Anmerkungen Regelschule Klasse 7 1. Stoffe und ihre Eigenschaften 9. Gegenstand
Sicherheitsdatenblatt nach EU Richtlinien
 LIPCOAT 100 Staubbindemittel Seite 1 von 6 Sicherheitsdatenblatt nach EU Richtlinien Druckdatum: 16.03.2015 geändert am: 19.01.2015 1. Stoff-/Zubereitungs- und Firmenbezeichnung Handelsname: Lieferant:
LIPCOAT 100 Staubbindemittel Seite 1 von 6 Sicherheitsdatenblatt nach EU Richtlinien Druckdatum: 16.03.2015 geändert am: 19.01.2015 1. Stoff-/Zubereitungs- und Firmenbezeichnung Handelsname: Lieferant:
P1 Säuren und Laugen aus Erde, Feuer, Luft und Wasser (ca. 25 Stunden)
 SLZB Fachbereich Naturwissenschaften Schulinternes Curriculum für das Fach Chemie Klasse 9 P1 Säuren und Laugen aus Erde, Feuer, Luft und Wasser (ca. 25 ) Sicherheitsbelehrung Wdh. PSE Atombau Säuren und
SLZB Fachbereich Naturwissenschaften Schulinternes Curriculum für das Fach Chemie Klasse 9 P1 Säuren und Laugen aus Erde, Feuer, Luft und Wasser (ca. 25 ) Sicherheitsbelehrung Wdh. PSE Atombau Säuren und
Biomasse/Biomüll. Biogas/Biogasanlage. Blockheizkraftwerk. Müllheizkraftwerk. Pelletheizung
 Biomasse/Biomüll Biogas/Biogasanlage Blockheizkraftwerk Müllheizkraftwerk Pelletheizung Christoph Hennemann 10 a 09.03.2010 Biomasse: Als Biomasse wird die gesamte organische Substanz bezeichnet. Basis
Biomasse/Biomüll Biogas/Biogasanlage Blockheizkraftwerk Müllheizkraftwerk Pelletheizung Christoph Hennemann 10 a 09.03.2010 Biomasse: Als Biomasse wird die gesamte organische Substanz bezeichnet. Basis
Chemie für Biologen WS 2005/6 Arne Lützen Institut für Organische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte)
 Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte) Lösungen, Konzentration Viele chemische Reaktionen werden
Chemie für Biologen WS 2005/6 Arne Lützen Institut für rganische Chemie der Universität Duisburg-Essen (Teil 8: Säuren und Basen, Elektrolyte) Lösungen, Konzentration Viele chemische Reaktionen werden
Chemieepoche Klasse 11. Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen
 Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Die wichtigsten anorganischen Säuren Schwefelsäure H 2 SO 4 ihre Salze heißen Sulfate Salpetersäure HNO 3 ihre Salze
Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Die wichtigsten anorganischen Säuren Schwefelsäure H 2 SO 4 ihre Salze heißen Sulfate Salpetersäure HNO 3 ihre Salze
3.2. Aufgaben zu Säure-Base-Gleichgewichten
 .. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
.. Aufgaben zu Säure-Base-Gleichgewichten Aufgabe : Herstellung saurer und basischer Lösungen Gib die Reaktionsgleichungen für die Herstellung der folgenden Lösungen durch Reaktion der entsprechenden Oxide
Chemikalien: Salzsäure (Schwefelsäure) Magnesiumspäne, Eisen-, Zink-, Kupfer-Späne, Silberstreifen
 I) Verhalten von Säuren gegenüber Metallen II) Der Saure Regen in Modellversuchen III) Neutralisation a) Neutralisation ( Salzsäure mit Natronlauge) b) Eindampfen der Salzlösung c) Elektrische Leitfähigkeitsmessung
I) Verhalten von Säuren gegenüber Metallen II) Der Saure Regen in Modellversuchen III) Neutralisation a) Neutralisation ( Salzsäure mit Natronlauge) b) Eindampfen der Salzlösung c) Elektrische Leitfähigkeitsmessung
Bäume - mehr als ein Stück Holz
 Bäume - mehr als ein Stück Holz Unser Wald ist Rohstofflieferant und Devisenbringer, ein wichtiger Schutz im Gebirge vor Erdrutschen und Lawinen. Er reguliert das Klima, speichert und filtert unser Wasser.
Bäume - mehr als ein Stück Holz Unser Wald ist Rohstofflieferant und Devisenbringer, ein wichtiger Schutz im Gebirge vor Erdrutschen und Lawinen. Er reguliert das Klima, speichert und filtert unser Wasser.
Seite 1 von Standortbestimmung / Äquivalenzprüfung. Chemie. Freitag, 23. Mai 2014, Uhr
 Seite 1 von 8 2. Standortbestimmung / Äquivalenzprüfung Chemie Freitag, 23. Mai 2014, 16.45-18.45 Uhr Dauer der Prüfung: 120 Minuten Erlaubte Hilfsmittel: Eine vom Dozenten visierte Formelsammlung, Ein
Seite 1 von 8 2. Standortbestimmung / Äquivalenzprüfung Chemie Freitag, 23. Mai 2014, 16.45-18.45 Uhr Dauer der Prüfung: 120 Minuten Erlaubte Hilfsmittel: Eine vom Dozenten visierte Formelsammlung, Ein
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2004/2005 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2004/2005 Geltungsbereich: für Klassen 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Herbst Hygiene, Reinigung und Desinfektion. Quellen: LGL Würzburg Firma Wigol. Kellerwirtschaftskurs 2014, J. Burkert.
 Herbst 2014 Hygiene, Reinigung und Desinfektion Quellen: LGL Würzburg Firma Wigol Folie 1 Hygiene Reintönigkeit kommt von Reinigen Zur Erzeugung qualitativ hochwertiger und v.a. reintöniger Weine ist die
Herbst 2014 Hygiene, Reinigung und Desinfektion Quellen: LGL Würzburg Firma Wigol Folie 1 Hygiene Reintönigkeit kommt von Reinigen Zur Erzeugung qualitativ hochwertiger und v.a. reintöniger Weine ist die
Experimente mit Brausetabletten
 Experimente mit Brausetabletten Beim Auflösen von Brausetabletten reagiert Natriumhydrogencarbonat NaHCO 3 mit der ebenfalls in der Tablette enthaltener Säure (meist Wein- oder Citronensäure; allgemein
Experimente mit Brausetabletten Beim Auflösen von Brausetabletten reagiert Natriumhydrogencarbonat NaHCO 3 mit der ebenfalls in der Tablette enthaltener Säure (meist Wein- oder Citronensäure; allgemein
Wasservorräte auf der Erde Arbeitsblatt 1
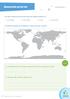 Wasservorräte auf der Erde Arbeitsblatt 1 1. Wo gibt es Süßwasser auf der Erde? Kreuze die richtigen Antworten an. In den Wolken In der Erdkruste Im Meer Im Gletschereis 2. Schraffiere die Gebiete auf
Wasservorräte auf der Erde Arbeitsblatt 1 1. Wo gibt es Süßwasser auf der Erde? Kreuze die richtigen Antworten an. In den Wolken In der Erdkruste Im Meer Im Gletschereis 2. Schraffiere die Gebiete auf
Handout Säure, Base, ph-wert
 Säure und Base Säuren sind im engeren Sinne alle Verbindungen, die in der Lage sind, Protonen (H + ) an einen Reaktionspartner zu übertragen - sie können als Protonendonator fungieren. In wässriger Lösung
Säure und Base Säuren sind im engeren Sinne alle Verbindungen, die in der Lage sind, Protonen (H + ) an einen Reaktionspartner zu übertragen - sie können als Protonendonator fungieren. In wässriger Lösung
Umwelt. Umwelt. Kein Leben ohne Wasser 1/18. Kein Leben ohne Wasser 2/18
 Kein Leben ohne Wasser 1/18 Stell dir vor, du sitzt auf dem Mond und siehst mit dem Fernrohr auf die Erde. Was siehst du? Eine nahezu blaue Scheibe. Das kommt daher, dass weit mehr als die Hälfte der Oberfläche
Kein Leben ohne Wasser 1/18 Stell dir vor, du sitzt auf dem Mond und siehst mit dem Fernrohr auf die Erde. Was siehst du? Eine nahezu blaue Scheibe. Das kommt daher, dass weit mehr als die Hälfte der Oberfläche
2.9 Reaktion von Laugen mit Aluminium - Laugenstärke. Aufgabe. Gibt es verschieden starke Laugen?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7159300) 2.9 Reaktion von Laugen mit Aluminium - Laugenstärke Experiment von: Phywe Gedruckt: 15.10.2013 12:17:12 intertess (Version 13.06
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P7159300) 2.9 Reaktion von Laugen mit Aluminium - Laugenstärke Experiment von: Phywe Gedruckt: 15.10.2013 12:17:12 intertess (Version 13.06
Elemente des Periodensystems. Natürliche Häufigkeit der Elemente
 Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Elemente des Periodensystems Natürliche Häufigkeit der Elemente 1 Der Wasserstoff Vorkommen Eigenschaften Gewinnung Verwendung Verbindungen 2 Vorkommen Interstellare Wasserstoffwolken Orion-Nebel und auf
Abgestufte Lernhilfen
 Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Abgestufte Lernhilfen Checkliste für die Beobachtungen: o o o o o Farbe des Indikators bei bei Zugabe zu Natronlauge Temperatur vor Zugabe der Salzsäure Farbveränderungen bei Zugabe der Salzsäure Temperaturveränderungen
Sicherheitsdatenblatt
 Sicherheitsdatenblatt Diaphragmareiniger (9892) 1. Stoff- / Zubereitungs- und Firmenbezeichnung Verwendung des Stoffes/ der Zubereitung Chemische Charakterisierung Reinigung/Wartung von ph-elektroden.
Sicherheitsdatenblatt Diaphragmareiniger (9892) 1. Stoff- / Zubereitungs- und Firmenbezeichnung Verwendung des Stoffes/ der Zubereitung Chemische Charakterisierung Reinigung/Wartung von ph-elektroden.
Schulinterner Lehrplan im Fach Chemie Klassenstufe 7-8
 Schulinterner Lehrplan im Fach Chemie Klassenstufe 7-8 1. Sicherheit im Chemieunterricht Angemessenes Verhalten im Fachraum Chemie Schgemäßer Umgang mit dem Gasbrenner 2. Umgang und Entsorgung von Chemikalien
Schulinterner Lehrplan im Fach Chemie Klassenstufe 7-8 1. Sicherheit im Chemieunterricht Angemessenes Verhalten im Fachraum Chemie Schgemäßer Umgang mit dem Gasbrenner 2. Umgang und Entsorgung von Chemikalien
Warum ist Feuer nützlich und warum sind Flammen heiß?
 Warum ist Feuer nützlich und warum sind Flammen heiß? Professor Dr.-Ing. Dieter Brüggemann KinderUniversität Bayreuth 1. Juli 2009 Wozu nutzen wir Feuer? Wir nutzen Feuer, um zu beleuchten Quelle: Wikipedia
Warum ist Feuer nützlich und warum sind Flammen heiß? Professor Dr.-Ing. Dieter Brüggemann KinderUniversität Bayreuth 1. Juli 2009 Wozu nutzen wir Feuer? Wir nutzen Feuer, um zu beleuchten Quelle: Wikipedia
Standortbestimmung / Äquivalenzprüfung. Chemie. Mittwoch, 13. April 2016, Uhr
 Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Inhalt. 1 Mein neues Fach - Chemie! 10. 2 Stoffe und Stoffeigenschaften
 Inhalt 1 Mein neues Fach - Chemie! 10 Ohne Chemie geht nichts 12 Methode Sicher arbeiten Exkurs Berufe aus dem Bereich mit dem Gasbrenner 20 der Chemie 13 Praktikum Arbeiten mit dem Gasbrenner _ 21 Exkurs
Inhalt 1 Mein neues Fach - Chemie! 10 Ohne Chemie geht nichts 12 Methode Sicher arbeiten Exkurs Berufe aus dem Bereich mit dem Gasbrenner 20 der Chemie 13 Praktikum Arbeiten mit dem Gasbrenner _ 21 Exkurs
Weniger CO 2 dem Klima zuliebe Lehrerinformation
 Lehrerinformation 1/8 Arbeitsauftrag Der CO 2- Kreislauf wird behandelt und die Beeinflussung des Menschen erarbeitet. Die Schülerberichte (Aufgabe 3) dienen als Grundlage zur Diskussion im Plenum. Ziel
Lehrerinformation 1/8 Arbeitsauftrag Der CO 2- Kreislauf wird behandelt und die Beeinflussung des Menschen erarbeitet. Die Schülerberichte (Aufgabe 3) dienen als Grundlage zur Diskussion im Plenum. Ziel
Waldboden. Sucht unter einem Laubbaum Blätter in unterschiedlichem Zersetzungsgrad und klebt sie nacheinander auf ein großes Blatt Papier!
 1 Sucht unter einem Laubbaum Blätter in unterschiedlichem Zersetzungsgrad und klebt sie nacheinander auf ein großes Blatt Papier! Findet heraus, welche Tiere dies bewirken! Schaut euch im Gelände um: Zersetzen
1 Sucht unter einem Laubbaum Blätter in unterschiedlichem Zersetzungsgrad und klebt sie nacheinander auf ein großes Blatt Papier! Findet heraus, welche Tiere dies bewirken! Schaut euch im Gelände um: Zersetzen
Wasserkreislauf: Arbeitsblatt
 Wasserkreislauf: Arbeitsblatt Der Wasserkreislauf beschreibt die horizontale und vertikale Zirkulation von Wasser. Dabei kommt Wasser in verschiedenen Aggregatszuständen vor. Die vier wichtigsten Vorgänge
Wasserkreislauf: Arbeitsblatt Der Wasserkreislauf beschreibt die horizontale und vertikale Zirkulation von Wasser. Dabei kommt Wasser in verschiedenen Aggregatszuständen vor. Die vier wichtigsten Vorgänge
D E. Inhaltsverzeichnis. Inhalt. Wasserschule Oberbayern A/1. Inhaltsverzeichnis... A
 Oberbayern A/1 A.................................................................. A B C D E 1 Unterrichtsgestaltung............................................................... B Gestaltungsvorschläge
Oberbayern A/1 A.................................................................. A B C D E 1 Unterrichtsgestaltung............................................................... B Gestaltungsvorschläge
Die Herstellung von Schwefelsäure. Vortrag Sommersemester 08
 Anorganische Chemie I Die Herstellung von Schwefelsäure Anorganische Chemie I I Vortrag Sommersemester 08 Sommersemester 08 14.04.2008 1 Überblick Einleitung Geschichte alte Herstellungsverfahren moderne
Anorganische Chemie I Die Herstellung von Schwefelsäure Anorganische Chemie I I Vortrag Sommersemester 08 Sommersemester 08 14.04.2008 1 Überblick Einleitung Geschichte alte Herstellungsverfahren moderne
Welt der Chemie Feuerwerk 178 Selbst untersucht Eigenschaften von Alkali- und Erdalkalimetallen 179 Natrium 180
 Inhalt Alkali- und Erdalkalimetalle 177 Welt der Chemie Feuerwerk 178 Selbst untersucht Eigenschaften von Alkali- und Erdalkalimetallen 179 Natrium 180 Die Elemente der I. Hauptgruppe 182 Magnesium und
Inhalt Alkali- und Erdalkalimetalle 177 Welt der Chemie Feuerwerk 178 Selbst untersucht Eigenschaften von Alkali- und Erdalkalimetallen 179 Natrium 180 Die Elemente der I. Hauptgruppe 182 Magnesium und
1) Typische Eigenschaften
 1) Typische Eigenschaften Saure Lösungen und Laugen sind durch bestimmte Eigenschaften gekennzeichnet. Lies dir dazu den Infotext durch und notiere typische Eigenschaften. Formuliere die im Text erwähnte
1) Typische Eigenschaften Saure Lösungen und Laugen sind durch bestimmte Eigenschaften gekennzeichnet. Lies dir dazu den Infotext durch und notiere typische Eigenschaften. Formuliere die im Text erwähnte
Kapitel 02: Erdgas und Erdöl
 Kapitel 02: Erdgas und Erdöl 1 Kapitel 02: Erdgas und Erdöl Kapitel 02: Erdgas und Erdöl 2 Inhalt Kapitel 02: Erdgas und Erdöl...1 Inhalt... 2 Einige Produkte aus Erdöl...3 Erdöl ist nicht gleich Erdöl...3
Kapitel 02: Erdgas und Erdöl 1 Kapitel 02: Erdgas und Erdöl Kapitel 02: Erdgas und Erdöl 2 Inhalt Kapitel 02: Erdgas und Erdöl...1 Inhalt... 2 Einige Produkte aus Erdöl...3 Erdöl ist nicht gleich Erdöl...3
Salpetersäure. von Anja Kalweit und Daniel Jost
 Salpetersäure von Anja Kalweit und Daniel Jost Inhaltsangabe Geschichte Technische Darstellung Eigenschaften der Salpetersäure Auswirkung auf die Umwelt Verwendung Bilder Herstellung Weltweit Daten und
Salpetersäure von Anja Kalweit und Daniel Jost Inhaltsangabe Geschichte Technische Darstellung Eigenschaften der Salpetersäure Auswirkung auf die Umwelt Verwendung Bilder Herstellung Weltweit Daten und
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010
 1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
1 Musterprüfung Chemie Klassen: MPL 09 Datum: 14. 16. April 2010 Themen: Metallische Bindungen (Skript S. 51 53, inkl. Arbeitsblatt) Reaktionsverlauf (Skript S. 54 59, inkl. Arbeitsblatt, Merke, Fig. 7.2.1
Säure/Base - Reaktionen. 6) Titration starker und schwacher Säuren/Basen. Elektrolytische Dissoziation. AB(aq)
 Säure/Base - Reaktionen 1) Elektrolytische Dissoziation ) Definitionen Säuren Basen ) Autoprotolyse 4) p- und po-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Säure/Base - Reaktionen 1) Elektrolytische Dissoziation ) Definitionen Säuren Basen ) Autoprotolyse 4) p- und po-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Kapitel II Säuren und Basen
 Kapitel II Säuren und Basen Björn Schulz, Berlin 2004, www.lernmaus.de Inhalt: Säuren Beispiele für Säuren: Herstellung von Säuren Laugen / Basen Herstellung von Säuren und Basen Säuren und Basen in chemischen
Kapitel II Säuren und Basen Björn Schulz, Berlin 2004, www.lernmaus.de Inhalt: Säuren Beispiele für Säuren: Herstellung von Säuren Laugen / Basen Herstellung von Säuren und Basen Säuren und Basen in chemischen
Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O.
 Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O. 2 Er wollte herausfinden woher die Pflanze die Stoffe bezieht wenn sie beim Wachstum
Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O. 2 Er wollte herausfinden woher die Pflanze die Stoffe bezieht wenn sie beim Wachstum
Schwefelsäure. (Sulfat Ion)
 Schwefelsäure 1. Bau: Definition Säuren: Molekülverbindungen, deren wässrige Lösungen elektrisch positiv geladene Wasserstoff Ionen und elektrisch negativ geladene Säurerest Ionen enthalten. Baumerkmale:
Schwefelsäure 1. Bau: Definition Säuren: Molekülverbindungen, deren wässrige Lösungen elektrisch positiv geladene Wasserstoff Ionen und elektrisch negativ geladene Säurerest Ionen enthalten. Baumerkmale:
Schriftliche Abschlussprüfung Chemie
 Sächsisches Staatsministerium für Kultus Schuljahr 2005/2006 Geltungsbereich: für Klassenstufe 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Sächsisches Staatsministerium für Kultus Schuljahr 2005/2006 Geltungsbereich: für Klassenstufe 10 an - Mittelschulen - Förderschulen - Abendmittelschulen Schriftliche Abschlussprüfung Chemie Realschulabschluss
Inhalt. Was ist Chemie? 7
 Inhalt Was ist Chemie? 7 Überall Chemie 8 Chemie Chancen und Gefahren 10 Umgang mit Chemikalien 12 Typische Tätigkeiten in der Chemie 14 Methode Regeln beim Experimentieren 15 Methode Umgang mit dem Brenner
Inhalt Was ist Chemie? 7 Überall Chemie 8 Chemie Chancen und Gefahren 10 Umgang mit Chemikalien 12 Typische Tätigkeiten in der Chemie 14 Methode Regeln beim Experimentieren 15 Methode Umgang mit dem Brenner
Das Thema Luft im naturwissenschaftlichen Unterricht Luftverschmutzung
 Seminar für Didaktik und Lehrerbildung (Realschule) Reutlingen NWA Tag 2010 17. November 2010 Das Thema Luft im naturwissenschaftlichen Unterricht Luftverschmutzung Anika Rieker, Nina Rückert, Stefanie
Seminar für Didaktik und Lehrerbildung (Realschule) Reutlingen NWA Tag 2010 17. November 2010 Das Thema Luft im naturwissenschaftlichen Unterricht Luftverschmutzung Anika Rieker, Nina Rückert, Stefanie
Inhalt. Was ist Chemie? 7
 Inhalt Was ist Chemie? 7 Überall Chemie 8 Chemie Chancen und Gefahren 10 Umgang mit Chemikalien 12 Typische Tätigkeiten in der Chemie 14 Methode Regeln beim Experimentieren 15 Methode Umgang mit dem Brenner
Inhalt Was ist Chemie? 7 Überall Chemie 8 Chemie Chancen und Gefahren 10 Umgang mit Chemikalien 12 Typische Tätigkeiten in der Chemie 14 Methode Regeln beim Experimentieren 15 Methode Umgang mit dem Brenner
Wasser- und Elektrolythaushalt
 Wasser- und Elektrolythaushalt Der Säure-Basenhaushalt Historie: Säuren: Die älteste bekannte Säure (lat. acidum) ist Essig (lat. acetum), eine 5% wässrige Lösung der Verbindung Essigsäure. Säuren waren
Wasser- und Elektrolythaushalt Der Säure-Basenhaushalt Historie: Säuren: Die älteste bekannte Säure (lat. acidum) ist Essig (lat. acetum), eine 5% wässrige Lösung der Verbindung Essigsäure. Säuren waren
Lösungen (ohne Aufgabenstellungen)
 Lösungen (ohne Aufgabenstellungen) Aufgaben A 1 Einerseits reflektieren die Eiswolken die von der Erde abgehende Infrarotstrahlung; dadurch erhöht sich der Treibhauseffekt. Andererseits reflektieren die
Lösungen (ohne Aufgabenstellungen) Aufgaben A 1 Einerseits reflektieren die Eiswolken die von der Erde abgehende Infrarotstrahlung; dadurch erhöht sich der Treibhauseffekt. Andererseits reflektieren die
Viele Prozesse in Natur und Technik verlaufen in Kreisläufen. Wir stellen Dir hier einige davon in Kurzform vor.
 eqiooki.de Kreisläufe Seite 1 von 7 Stoffkreisläufe Viele Prozesse in Natur und Technik verlaufen in Kreisläufen. Wir stellen Dir hier einige davon in Kurzform vor. Kohlenstoffkreislauf 1 Fotosynthese
eqiooki.de Kreisläufe Seite 1 von 7 Stoffkreisläufe Viele Prozesse in Natur und Technik verlaufen in Kreisläufen. Wir stellen Dir hier einige davon in Kurzform vor. Kohlenstoffkreislauf 1 Fotosynthese
Jahrgangsstufe 7. Lehrplan. Inhaltsfelder. Bemerkungen Schwerpunkt/Kompetenzen. Zeit. Speisen u. Getränke. Stoffe und Stoffverändungen
 Jahrgangsstufe 7 Speisen u. Getränke Stoffe und Stoffverändungen Was ist Chemie? Wir untersuchen Lebensmittel auf Bestandteile. Wir gewinnen Stoffe aus Lebensmitteln. Wir verändern Nahrungsmittel durch
Jahrgangsstufe 7 Speisen u. Getränke Stoffe und Stoffverändungen Was ist Chemie? Wir untersuchen Lebensmittel auf Bestandteile. Wir gewinnen Stoffe aus Lebensmitteln. Wir verändern Nahrungsmittel durch
Sicherheitsdatenblatt für Batteriesäure (verdünnte Schwefelsäure) gemäß EU-Richtlinien 91/155/EWG
 Stand: 1.07.2014 Sicherheitsdatenblatt für Batteriesäure (verdünnte Schwefelsäure) gemäß EU-Richtlinien 91/155/EWG 1 Stoff / Zubereitungs- und Firmenbezeichnung Angaben zum Produkt Batteriesäure - verdünnte
Stand: 1.07.2014 Sicherheitsdatenblatt für Batteriesäure (verdünnte Schwefelsäure) gemäß EU-Richtlinien 91/155/EWG 1 Stoff / Zubereitungs- und Firmenbezeichnung Angaben zum Produkt Batteriesäure - verdünnte
Biologische und chemische Vorgänge in stehenden Gewässern. Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer
 Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer Der ph-wert Das Karbonathärte-Puffersystem Algen verstehen und bekämpfen Phosphatfrachten Der Teich Symbiose aller Lebewesen In einem
Eine zusammenfassende Betrachtung der Zusammenhänge in einem Gewässer Der ph-wert Das Karbonathärte-Puffersystem Algen verstehen und bekämpfen Phosphatfrachten Der Teich Symbiose aller Lebewesen In einem
Kurzvortrag: Treibhauseffekt
 Kurzvortrag: Treibhauseffekt Von Anne- Katrin Wudi und Nicole Scherließ Gliederung 1. Wie funktioniert der Treibhauseffekt? 1.2 Natürlicher Treibhauseffekt 1.3 Anthropogener (zusätzlicher) Treibhauseffekt
Kurzvortrag: Treibhauseffekt Von Anne- Katrin Wudi und Nicole Scherließ Gliederung 1. Wie funktioniert der Treibhauseffekt? 1.2 Natürlicher Treibhauseffekt 1.3 Anthropogener (zusätzlicher) Treibhauseffekt
2.8 Laugenbildung durch Reaktion von Metalloxiden mit Wasser. Aufgabe. Woraus lassen sich Laugen herstellen? (2)
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759200) 2.8 Laugenbildung durch Reaktion von Metalloxiden mit Wasser Experiment von: Phywe Gedruckt: 5.0.203 2:6:25 intertess (Version 3.06
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 2 Basen (P759200) 2.8 Laugenbildung durch Reaktion von Metalloxiden mit Wasser Experiment von: Phywe Gedruckt: 5.0.203 2:6:25 intertess (Version 3.06
Säure/Base - Reaktionen. 6) Titration starker und schwacher Säuren/Basen
 Säure/Base - Reaktionen 1) Elektrolytische Dissoziation 2) Definitionen Säuren Basen 3) Autoprotolyse 4) ph- und poh-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Säure/Base - Reaktionen 1) Elektrolytische Dissoziation 2) Definitionen Säuren Basen 3) Autoprotolyse 4) ph- und poh-wert 5) Stärke von Säure/Basen 6) Titration starker und schwacher Säuren/Basen 7) Puffersysteme
Boden Versauerung Dynamik-Gefährdung
 Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E office@bodenoekologie.com I www.bodenoekologie.com Boden Versauerung Dynamik-Gefährdung Univ. Lek. DI Hans
Rochuspark I Erdbergstraße 10/33 I 1020 Wien T (+43 1) 236 10 30 33 I M (+43 0) 676 364 10 30 E office@bodenoekologie.com I www.bodenoekologie.com Boden Versauerung Dynamik-Gefährdung Univ. Lek. DI Hans
