Fachinformation. 4.2 Dosierung, Art und Dauer der Anwendung
|
|
|
- Joseph Schräder
- vor 5 Jahren
- Abrufe
Transkript
1 1. BEZEICHNUNG DER ARZNEIMITTEL 1,0 g Pulver zur Herstellung einer Injektionslösung 2,0 g Pulver zur Herstellung einer Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1,0 g Jede Durchstechflasche enthält Cefotaxim- Natrium 1,048 g, entsprechend 1 g Cefotaxim. Der Natriumgehalt ist annähernd 48 mg (2,18 mmol) pro Durchstechflasche. 2,0 g Jede Durchstechflasche enthält Cefotaxim- Natrium 2,096 g, entsprechend 2 g Cefotaxim. Der Natriumgehalt ist annähernd 96 mg (4,36 mmol) pro Flasche. 3. DARREICHNUNGSFORM Pulver zur Herstellung einer Injektionslösung, Pulver zur Herstellung einer Infusionslösung. Das Pulver ist gebrochen weiß bis leicht gelblich. 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete Zur Behandlung der folgenden schweren Infektionen, wenn bekannt oder höchstwahrscheinlich ist, dass diese durch Cefotaximempfindliche Erreger verursacht sind (siehe Abschnitt 5.1) Infektionen der unteren Atemwege Infektionen der Niere und ableitenden Harnwege Infektionen der Haut und des Weichteilgewebes Gonorrhoe, wenn Penicillin versagt hat oder nicht verträglich ist Infektionen des Bauchraumes, einschl. Peritonitis Akute Meningitis Lyme-Borreliose (insbesondere Stadien II und III) Sepsis (bei gramnegativen Erregern in Kombination mit weiteren geeigneten Antibiotika ) Endokarditis (bei gramnegativen Erregern in Kombination mit weiteren geeigneten Antibiotika) Perioperative Prophylaxe bei kolorektalen, gastrointestinalen, urogenitalen, geburtshilflichen und gynäkologischen Operationen, Operationen an der Prostata, bei Patienten mit eindeutigem Risiko postoperativer Infektionen Bei der Behandlung von intraabdominalen Infektionen sollte Cefotaxim in Kombination mit einem anderen Antibiotikum angewendet werden, das gegen ier wirksam ist. Bei der Behandlung von Pseudomonas- Infektionen sollte Cefotaxim mit einem Aminoglykosid kombiniert Die derzeit gültigen Richtlinien für die angemessene Anwendung von Antibiotika sollten berücksichtigt A n Art der Infektion Einzeldosis Cefotaxim typische Infektionen, bei denen ein empfindlicher Erreger nachgewiesen oder vermutet wird Infektionen, bei denen Erreger mit hoher bis mäßiger Empfindlichkeit nachgewiesen oder vermutet werden unklare bakterielle Erkrankungen, die nicht lokalisiert werden können, und bei denen der Patient in kritischem Zustand ist 4.2 Dosierung, Art und Dauer der Anwendung 1,0 g Pulver zur Herstellung einer Injektionslösung wird intravenös durch eine Bolus-Injektion oder intramuskulär verabreicht. 2,0 g Pulver zur Herstellung einer Infusionslösung wird infundiert. Dosierung und Art der Anwendung richten sich nach der Schwere der Infektion, der Empfindlichkeit des Erregers und dem Krankheitszustand des Patienten. Die intramuskuläre Verabreichung ist besonderen klinischen Situationen vorbehalten und sollte einer Risiko-Nutzen Abwägung unterzogen werden! Spezielle Hinweise für die intramuskuläre Injektion müssen beachtet werden (siehe auch Abschnitte 4.3 und 4.4). Dosierung Erwachsene und Jugendliche (über 12 Jahre) Normaldosis: 1 g Cefotaxim alle 12 Stunden. In schweren Fällen kann die Tagesdosis bis auf 12 g erhöht Tagesdosen bis zu 6 g können auf mindestens zwei Einzelgaben im Abstand von 12 Stunden verteilt Höhere Tagesdosen müssen auf mindestens 3 bis 4 Einzelgaben im Abstand von 8 bzw. 6 Stunden verteilt Oben stehende Tabelle kann als Dosierungsrichtlinie gelten. Säuglinge und Kleinkinder (28 Tage bis 24 Monate alt) sowie Kinder (2 bis 11 Jahre alt, 50 kg Körpergewicht): Normaldosis: 50 bis 150 mg/kg/tag, aufgeteilt in 2 bis 4 Einzeldosen. Bei sehr schweren Infektionen: bis zu 200 mg/kg/tag in mehreren Einzeldosen. Bei Kindern 50 kg Körpergewicht sollte die übliche Dosis für Erwachsene verabreicht werden, ohne die maximale Tagesdosis von 12 g zu überschreiten. Neugeborene (0 bis 27 Tage alt): Die empfohlene Dosis beträgt 50 mg/kg/ Tag, aufgeteilt in 2 bis 4 Einzeldosen (alle 12 6 Stunden). In lebensbedrohlichen Situationen kann die Dosis unter Berücksichtigung des Reifegrades der Ausscheidungsfunktion der Nieren auf mg/kg/tag erhöht Dosierungsintervall 1 g 12 Std. 2 g 2 g 12 Std. 4 g 2 3g 8Std. bis zu 6 Std. bis zu 6 Std Tagesdosis Cefotaxim 6g bis zu 8 g bis zu 12 g Frühgeborene: Die empfohlene Dosis beträgt 50 mg/kg/ Tag, aufgeteilt in 2 bis 4 Einzeldosen (alle 12 bis 6 Stunden). Diese maximale Tagesdosis sollte mit Rücksicht auf die noch nicht ausgereifte Ausscheidungsfunktion der Nieren nicht überschritten Spezielle Dosierungsempfehlungen: Gonorrhoe Zur Behandlung der Gonorrhoe bei Erwachsenen werden einmalig 0,5 g Cefotaxim intramuskulär verabreicht. Bei weniger empfindlichen Keimen kann eine Erhöhung der Dosis erforderlich sein, z. B. auf 1 g Cefotaxim. Vor Beginn der Behandlung muss eine Untersuchung auf Syphilis erfolgen. Perioperative Prophylaxe Zur perioperativen Infektionsprophylaxe wird die Gabe von 1 bis 2g Cefotaxim 30 bis 60 Minuten vor der Operation empfohlen. Zur Erfassung anaerober Erreger ist die Kombination mit einem weiteren Antibiotikum erforderlich. Wenn die Operation länger als 90 Minuten dauert, muss die gleiche Dosis erneut verabreicht Zur Infektionsprophylaxe (perioperative Prophylaxe bei chirurgischen Maßnahmen wie kolorektalen und gastrointestinalen Operationen, Operationen an der Prostata sowie urogenitalen, geburtshilflichen und gynäkologischen Eingriffen) bei immungeschwächten Patienten kann die Kombination mit weiteren, geeigneten Antibiotika indiziert sein. Lyme-Borreliose Zur Behandlung der Lyme-Borreliose wird eine Tagesdosis von 6 g Cefotaxim (für 14 bis 21 Tage) empfohlen. Die Tagesdosis wird im Allgemeinen auf 3 Einzeldosen verteilt (2 g Cefotaxim 3-mal täglich). Kombinationstherapie Bei schweren lebensbedrohlichen Infektionen, bei denen kein Antibiogramm vorliegt, ist eine Kombination mit Aminoglykosiden indiziert. Bei der Kombinationstherapie mit Aminoglykosiden muss die Nierenfunktion überwacht Bei Infektionen mit Pseudomonas aeruginosa kann eine Kombination mit weiteren, gegen Pseudomonas wirksamen Antibiotika angezeigt sein. Eingeschränkte Nierenfunktion Bei Patienten mit einer Einschränkung der Kreatinin-Clearance auf 20 ml/minute oder weniger muss die Erhaltungsdosis auf die Hälfte der Normaldosis reduziert 1
2 Bei Patienten mit einer Einschränkung der Kreatinin-Clearance auf 5 ml/minute oder weniger ist eine Verringerung der Erhaltungsdosis auf 1 g Cefotaxim (aufgeteilt auf 2 Einzelgaben im Abstand von 12 Stunden) angemessen. Die angegebenen Empfehlungen beruhen auf Erfahrungen bei Erwachsenen. Da Cefotaxim durch Hämodialyse weitgehend entfernt wird, sollte bei Dialysepatienten eine zusätzliche Dosis nach der Dialyse verabreicht Ältere Patienten Bei älteren Patienten mit normaler Nierenfunktion ist keine Dosisanpassung erforderlich. Verabreichungsmethoden Für die Zubereitung der gebrauchsfertigen Lösung siehe Abschnitt 6.6. Bei der intramuskulären Verabreichung empfiehlt es sich, einseitig nicht mehr als 4 ml zu injizieren. Beträgt die Tagesdosis mehr als 2 g Cefotaxim oder wird Cefotaxim Hikma häufiger als zweimal täglich injiziert, wird die intravenöse Anwendung empfohlen. Dauer der Anwendung Die Behandlungsdauer richtet sich nach dem Verlauf der Krankheit. Allgemein wird empfohlen, Cefotaxim nach einer Besserung/dem Rückgang der Symptome noch 3 bis 4 Tage weiter zu verabreichen. 4.3 Gegenanzeigen Bekannte Überempfindlichkeit gegen Cefotaxim oder andere Cephalosporine. Vorbekannte Sofortreaktionen oder schwere Überempfindlichkeitsreaktion gegenüber einem Penicillin oder einem anderen Betalaktam-Antibiotikum. Mit Lidocain rekonstituierte Cefotaxim-Lösungen sind kontraindiziert für die intravenöse Anwendung. Die intramuskuläre Verabreichung ist kontraindiziert bei Kindern unter einem Jahr (siehe auch Abschnitt 4.4). 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Cefotaxim sollte bei Patienten, die andere Überempfindlichkeitsreaktionen gegen Penicillin oder andere Betalaktam-Antibiotika hatten, mit Vorsicht angewendet sollte ebenfalls mit Vorsicht bei Patienten mit anderen Allergien oder Asthma in der Vorgeschichte angewendet Eine Kreuzallergie mit anderen Betalaktam- Antibiotika (z. B. Penicilline) ist zu berücksichtigen. Anaphylaxie bzw. ein anaphylaktischer Schock sind lebensbedrohlich und erfordern entsprechende Notfallmaßnahmen (siehe Abschnitt 4.8). Elektrolytgehalt der Injektionslösungen: Da Cefotaxim als Natriumsalz vorliegt, ist der Natriumgehalt pro Dosis in klinischen Situationen, die eine Natriumrestriktion erfordern, zu berücksichtigen. Berechnungsgrundlage: Für 1 g Cefotaxim (entsprechend 1,048 g Cefotaxim-Natrium) sind 48 mg Natrium, entsprechend 2,18 mmol Natrium, zu berechnen. Für Patienten mit stark eingeschränkter Nierenfunktion (glomeruläre Filtrationsrate unter 20 ml/min) gelten spezielle Dosierungsrichtlinien (siehe Abschnitt 4.2). Wenn die Behandlung länger als 10 Tage dauert, sind Kontrollen des Blutbilds durchzuführen, und im Falle einer Neutropenie sollte die Behandlung abgebrochen werden (siehe Abschnitt 4.8). Die Leber- und Nierenfunktion sollten bei längerer Anwendung ebenfalls überwacht Insbesondere bei längerer Anwendung ist die Möglichkeit des Überwucherns mit Erregern zu berücksichtigen, die gegen Cefotaxim unempfindlich sind, wie Enterococcus spp und Candida spp. Leichte Durchfälle klingen häufig während oder ansonsten nach Beendigung der Behandlung ab. Bei schweren und anhaltenden Durchfällen ist an eine durch Clostridium difficile hervorgerufene pseudomembranöse Colitis zu denken, die lebensbedrohlich sein kann. In Abhängigkeit von der Erkrankung ist eine Beendigung der Behandlung mit Cefotaxim Hikma zu erwägen und eine angemessene Behandlung einzuleiten (z. B. Gabe von speziellen Antibiotika/Chemotherapeutika, deren Wirksamkeit klinisch erwiesen ist). Antiperistaltika sind kontraindiziert (siehe auch Abschnitt 4.8). Wird über einen zentralen Venenkatheter (ZVK) zu schnell (in weniger als 1 Minute) injiziert, kann es zu schweren Herzrhythmusstörungen kommen (siehe Abschnitt 4.8). Wird nach Zubereitung mit Lidocain intramuskulär verabreicht, sind die Produkteigenschaften des Lidocain-haltigen Arzneimittels zu beachten. 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Cefotaxim/andere Antibiotika Cefotaxim sollte möglichst nicht mit Substanzen kombiniert werden, die eine bakteriostatische Wirkung haben (z. B. Tetrazyklin, Erythromycin, Chloramphenicol oder Sulfonamide), da in vitro eine antagonistische Wirkung beobachtet wurde. Bei der Kombination mit Aminoglykosiden kann es zu einer synergistischen Wirkung kommen. Bei gleichzeitiger Anwendung von Cefotaxim mit Aminoglykosiden wurde ein erhöhtes Risiko für Oto- und Nephrotoxizität berichtet. Eine Dosisanpassung kann erforderlich werden und die Nierenfunktion muss überwacht werden (siehe Abschnitt 4.2). Cefotaxim/Probenecid Die gleichzeitige Gabe von Probenecid führt über eine Hemmung der renalen Clearance zu höheren, länger anhaltenden Konzentrationen von Cefotaxim im Serum. Cefotaxim/potentiell nephrotoxische Arzneimittel und Schleifendiuretika Bei der Kombination mit potentiell nierenschädigenden Arzneimitteln (wie z. B. Aminoglykosid-Antibiotika, Polymyxin B und Colistin) und mit Schleifendiuretika muss die Nierenfunktion überwacht werden, da es zu einer Verstärkung der nephrotoxischen Eigenschaften der aufgeführten Substanzen kommen kann. Einfluss auf labordiagnostische Untersuchungen Unter der Behandlung mit kann in seltenen Fällen der Coombs-Test falsch-positiv ausfallen. Bei Harn- und Blutzuckerbestimmungen kann es je nach der verwendeten Methode zu falsch-positiven oder falsch-negativen Ergebnissen kommen; dies lässt sich durch Anwendung enzymatischer Methoden vermeiden. 4.6 Schwangerschaft und Stillzeit Schwangerschaft Bisher liegen keine klinischen Erfahrungen mit der Anwendung von während der Schwangerschaft vor. Tierstudien zeigten keine Reproduktionstoxizität. Cefotaxim passiert die menschliche Plazenta. Cefotaxim sollte nicht während der Schwangerschaft angewendet werden, es sei denn, es ist zwingend erforderlich. Stillzeit Cefotaxim geht in geringen Mengen in die Muttermilch über. Die Anwendung von Cefotaxim Hikma während der Stillzeit kann bei Säuglingen zu Störungen der physiologischen Darmflora mit Durchfall, zur Besiedelung mit Saccharomyces und möglicherweise auch zu einer Sensibilisierung führen. Die Verabreichung an stillende Frauen sollte mit Vorsicht erfolgen. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und das Bedienen von Maschinen durchgeführt. In Einzelfällen ist bei Anwendung hoher Dosen und vor allem bei gleichzeitigem Bestehen einer Nierenfunktionseinschränkung über Krampfanfälle (tonisch/klonisch), Muskelspasmen (Myoklonien) und Schwindelgefühle berichtet worden. Daher sollte unter diesen Umständen auf die genannten Tätigkeiten verzichtet 4.8 Nebenwirkungen Innerhalb jeder Häufigkeitsgruppe werden die Nebenwirkungen nach abnehmendem Schweregrad angegeben. Die Nebenwirkungen wurden unter den Überschriften der Organklassen eingeordnet und bei der Bewertung werden folgende Häufigkeitsangaben zugrunde gelegt: Sehr häufig: mehr als 1 von 10 Behandelten Häufig: weniger als 1 von 10, 100 Behandelten A n
3 Organ Klassen Häufigkeit Nebenwirkung Infektionen und parasitaere Erkrankungen Erkrankungen des Blutes und des Lymphsystems Häufig Sehr selten Längerer und wiederholter Einsatz von Cefotaxim kann zu Superinfektionen und Besiedelung mit resistenten Bakterien und Pilzen führen (siehe Abschnitt 4.4) hämolytische Anämie, Granulozytopenie, Leukozytopenie, Eosinophilie oder Thrombozytopenie, Agranulozytose und Neutropenie. Wenn die Behandlungsdauer 10 Tage überschreitet, sollten Blutbildkontrollen durchgeführt werden (siehe 4.4) Erkrankungen des Nervensystems Sehr selten Krampfanfälle wurden berichtet, besonders bei Anwendung hoher Dosen und bei Patienten mit Nierenfunktionsstörungen (siehe Abschnitt 4.9) Herzerkrankungen Sehr selten schwere Fälle von Arrhythmien im Zusammenhang mit zu schneller (weniger als 1 Minute) Verabreichung über einen zentralen Venenkatheter (ZVK). Erkrankungen des Gastrointestinal- Selten Appetitlosigkeit, Übelkeit, Erbrechen, Magenschmerzen und Durchfall trakts Sehr selten pseudomembranöse Kolitis (siehe Abschnitt 4.4) Leber- und Gallenerkrankungen Selten Vorübergehend leichter Anstieg des Bilirubin-wertes und/oder der Leberenzyme im Serum (SGOT, SGPT, Gamma GT, alkalische Phosphatase, LDH). Erkrankungen der Haut und des Häufig Allergische Reaktionen (bei Patienten mit einer Neigung zu Allergien) Unterhautzellgewebes Selten schwere akute Überempfindlichkeitsreaktionen Anaphylaxie (siehe Abschnitt 4.4), allergische Hautreaktionen (z. B. Urticaria, Exantheme), Juckreiz und Arzneimittelfieber Sehr selten Erythema multiforme (leichte bis schwere Formen z. B. Stevens-Johnsons Syndrom) und toxisch-epidermale Nekrolyse Erkrankungen der Nieren und Gelegentlich Anstieg der Kreatinin und Harnstoff-Konzentration im Serum Harnwege Selten Akute interstitielle Nephritis Allgemeine Erkrankungen und Häufig Unverträglichkeitsreaktionen wie Hitzegefühl oder Übelkeit nach rascher i.v. Injektion. Beschwerden am Verabreichungsort Gelegentlich Selten Schmerzen und Verhärtung des Gewebes (Indurationen) am Injektionsort nach intramuskulärer Injektion entzündliche Reizungen der Venenwand (bis zur Thrombophlebitis) und Schmerzen am Ort der Injektion, nach intravenöser Applikation. Gelegentlich: weniger als 1 von 100, 1000 Behandelten Selten: weniger als 1 von 1000, Behandelten Sehr selten: weniger als 1 von Behandelten, einschließlich Einzelfälle Nebenwirkungen unter der Behandlung mit Cefotaxim traten bei etwa 5 % der Patienten auf und waren im Allgemeinen leichter und vorübergehender Natur. Siehe Tabelle oben Lidocain, das zur Verdünnung von Cefotaxim Hikma zur intramuskulären Verabreichung verwendet wird, kann schwere Nebenwirkungen auslösen. Die Produkteigenschaften des Lidocain-haltigen Arzneimittels müssen beachtet werden (siehe auch Abschnitt 4.3 und 4.4). 4.9 Überdosierung a) Symptome einer Überdosierung Intoxikationen im strengen Sinn sind beim Menschen nicht bekannt. Bei bestimmten Risikokonstellationen und bei Gabe sehr hoher Dosen kann es zu zentralnervösen Erregungszuständen, Myoklonien und Krämpfen kommen, wie sie auch für andere Betalaktame beschrieben worden sind. Das Risiko des Auftretens dieser unerwünschten Wirkungen ist bei Patienten mit stark eingeschränkter Nierenfunktion, Epilepsie und Meningitis erhöht A n b) Notfallmaßnahmen Zentral ausgelöste Krämpfe können mit Diazepam oder Phenobarbital, nicht jedoch mit Phenytoin behandelt Bei anaphylaktischen Reaktionen bzw. den ersten Anzeichen des anaphylaktischen Schocks sind die üblichen Notfallmaßnahmen einzuleiten. 5. PHARMAKOLOGISCHE EIGEN- SCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Cephalosporine der dritten Generation ATC-Code: J01DD01 Wirkungsweise Cefotaxim stört die bakterielle Zellwandsynthese und wirkt bakterizid. Mechanismen der Resistenz Bakterielle Resistenz gegenüber Cefotaxim kann durch einen oder mehrere der folgenden Resistenzmechanismen ausgelöst werden: Effektive Hydrolyse des Wirkstoffs durch extended-sprectrum-betalaktamasen (ESBL) oder chromosomal codierte (AmpC) Betalaktamasen. Cefotaxim wird nicht durch die weitverbreiteten Betalaktamasen, wie TEM-1, TEM-2 oder SHV-1, hydrolysiert. Impermeabilisierung. Efflux-Pumpen. Mehr als einer dieser Mechanismen können in Krankheitserregern gleichzeitig vorliegen. Breakpoints Entsprechend dem Klinischen und Laboratorischen Standards Institut (Clinical and Laboratory Standards Institute, CLSI) sind die Breakpoints wie folgt: Siehe Tabelle 1 auf Seite 4 oben Die Verbreitung von erworbener Resistenz kann örtlich und mit der Zeit für spezielle Spezies schwanken. Es ist wünschenswert Informationen über regionale Resistenzen zu haben, besonders bei der Behandlung schwerer Infektionen. Als Notwendigkeit wird angesehen, dass Expertenrat eingeholt wird, wenn die regional erworbenen Resistenzen so sind, dass die Wirksamkeit des Wirkstoffes bei mindestens einigen Infektionstypen fraglich ist. Üblicherweise empfindliche Species Staphylococcus aureus* MSSA Staphylococcus epidermidis* MSSE Streptococcus pyogenes* Haemophilus influenzae* Haemophilus parainfluenza* Klebsiella pneumoniae Morganella morganii Moraxella catarrhalis* Neisseria gonorrhoea* Neisseria meningitidis* Proteus mirabilis* Serratia marcescens Yersinia enterocolitica 3
4 Tabelle 1: Empfindlichkeits Breakpoints Bakterielle Breakpoints Organismen CLSI Breakpoints S: 8 mg/l I: mg/l R: 64 mg/l Enterobacteriaceae, Staphylococcus ssp., Pseudomonas aeruginosa S: 2 mg/l Haemophilus influenzae S: 0,5 mg/l Neisseria gonorrhoeae S: 1 mg/l I: 2 mg/l R: 4 mg/l Streptococcus pneumoniae (nonmeningitis) S: 0,5 mg/l I: 1 mg/l R: 2 mg/l Streptococcus pneumoniae (meningitis) S: Empfindlich (susceptible), I: mittelmäßig empfindlich (intermediate susceptible), R: resistent (resistant). Clostridium perfringens Peptostreptococcus spp. Propionibacterium spp. Andere Borrelia burgdorferi im engeren Sinne Borrelia afzelii Borrelia garinii Borrelia valaisiana Species, bei denen erworbene Resistenzen ein Problem bei der Anwendung darstellen können Streptococcus pneumoniae + Citrobacter freundii + Enterobacter aerogenes Enterobacter cloacae Clostridium difficile Bacteroides fragilis Von Natur aus resistente Spezies Staphylococcus aureus MRSA Staphylococcus epidermidis MRSE Enterococcus spp. Acinetobacter spp Pseudomonas aeruginosa Stenotrophomonas maltophilia Bacteroides spp. Clostridium difficile Andere Chlamydia spp. Legionella pneumophila Listeria spp. Mycoplasma spp. + Die nationalen Resistenz-Raten variieren in bestimmten Regionen Europas. * Wirksamkeit wurde in klinischen Studien nachgewiesen. 5.2 Pharmakokinetische Eigenschaften Cefotaxim wird parenteral angewendet. Nach intravenöser Injektion von 1 g Cefotaxim wurden Serumkonzentrationen nach 5 Min. von etwa mg/l und nach 15 Min. von 46 mg/l nachgewiesen. Nach i.v. Injektion von 2 g Cefotaxim wurden Serumkonzentrationen von mg/l nach 8 Min. gemessen. Nach intramuskulärer Gabe werden maximale Serumkonzentrationen (etwa 20 mg/l nach 1 g) innerhalb von 30 Min. erreicht. Verteilung Cefotaxim ist gut gewebegängig, passiert die Plazentaschranke und erreicht hohe Konzentrationen in fetalen Geweben (bis 6 mg/kg). Es tritt nur zu einem geringen Prozentsatz in die Muttermilch über (Konzentrationen in der Muttermilch: 0,4 mg/l nach 2 g). Bei entzündeten Meningen penetrieren Cefotaxim und Desacetyl-Cefotaxim in den Liquorraum und erreichen dort therapeutisch wirksame Konzentrationen (z. B. bei Infektionen, die durch gramnegative Bakterien und Pneumokokken verursacht sind). Das scheinbare Verteilungsvolumen liegt bei l. Die Serumproteinbindung beträgt etwa %. Metabolismus Cefotaxim wird beim Menschen in beträchtlichem Umfang metabolisiert. Etwa % einer parenteralen Dosis werden als O-Desacetyl-Cefotaxim ausgeschieden. Der Metabolit ist antibakteriell aktiv. Neben Desacetyl-Cefotaxim finden sich noch zwei inaktive Lactone. Aus Desacetyl- Cefotaxim entsteht ein Lacton als kurzlebiges Intermediärprodukt, das weder im Urin noch im Plasma nachgewiesen werden kann, weil es einer raschen Umwandlung in Stereoisomere des ringoffenen (Betalaktamring) Lactons unterliegt. Diese werden ebenfalls im Urin ausgeschieden. Ausscheidung Die Ausscheidung von Cefotaxim und Desacetyl-Cefotaxim erfolgt überwiegend renal. Ein kleiner Prozentsatz (ca. 2 %) wird mit der Galle ausgeschieden. Im 6-Stunden- Sammelurin werden % einer Dosis in unveränderter Form und ca. 20 % als Desacetyl-Cefotaxim wiedergefunden. Nach i.v. Gabe von radioaktiv markiertem Cefotaxim wurden etwas mehr als 80 % im Urin wiedergefunden, davon entfielen % auf unveränderte Muttersubstanz und der Rest auf 3 Metabolite. Die totale Clearance des Cefotaxims beträgt ml/min und die renale Clearance ml/min. Die Serumhalbwertzeit für Cefotaxim und seinen aktiven Metaboliten liegt bei Minuten beziehungsweise 125 Minuten. Bei geriatrischen Patienten ( 80 Jahre) betrug die Halbwertzeit Minuten beziehungsweise 5 Stunden für den aktiven Metaboliten. Bei schweren Nierenfunktionsstörungen (Kreatinin-Clearance 3 10 ml/min) kann die Halbwertzeit des Cefotaxims auf 2,5 10 Stunden verlängert sein. Cefotaxim akkumulierte unter diesen Bedingungen nur in geringem Umfang, im Gegensatz zu den aktiven und inaktiven Metaboliten. Sowohl Cefotaxim als auch Desacetyl-Cefotaxim werden durch Hämodialyse in größerem Umfang aus dem Blut entfernt. 5.3 Präklinische Daten zur Sicherheit Die Toxizität von Cefotaxim ist bei einmaliger Gabe sehr gering. Der Mikronucleustest ergab für Cefotaxim keine Hinweise auf mutagenes Potential. Studien an Ratte und Maus gaben keine Hinweise auf fruchtschädigende Eigenschaften von Cefotaxim. Die Fertilität war nicht beeinträchtigt. In perinatalen und postnatalen Studien an Ratten hatten die Nachkommen bei Gabe von hohen Dosen an die Muttertiere ein signifikant niedrigeres Geburtsgewicht und blieben in den ersten 21 Tagen der Stillzeit kleiner als die Kontrolltiere. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile Keine 6.2 Inkompatibilität Die folgenden Substanzen/Lösungen sind mit nicht kompatibel: Natriumhydrogencarbonatlösung, Infusionslösungen mit einem ph-wert größer als 7, Aminoglykoside. Kompatibilität mit anderen Antibiotika/ Chemotherapeutika Cefotaxim/Aminoglykoside Auf Grund einer physikalischen und chemischen Inkompatibilität mit allen Aminoglykosiden sollte Cefotaxim nicht in einer Injektion oder Infusionslösung mit Aminoglykosiden gleichzeitig verabreicht Die beiden Antibiotika sollten mit getrennten Bestecken an verschiedenen Stellen injiziert 6.3 Dauer der Haltbarkeit Pulver zur Rekonstitution: 2 Jahre (ungeöffnetes Behältnis) Haltbarkeit der rekonstituierten Lösung: Lagerung bei 2 8 C: Nicht länger als 24 Stunden, Lagerung bei 25 C: Nicht mehr als 12 Stunden. Aus mikrobiologischer Sicht sollte die Lösung unmittelbar nach ihrer Herstellung verwendet Wenn die Lösung nicht sofort eingesetzt wird, ist der Anwender für die Dauer und die Bedingungen der Aufbewah A n
5 rung verantwortlich. Sofern die Herstellung nicht unter kontrollierten und validierten aseptischen Bedingungen erfolgt, ist die Lösung nicht länger als 24 Stunden bei 2 bis 8 C aufzubewahren. Eine schwach gelbliche Färbung der Lösung hat keine Auswirkung auf die Wirksamkeit und Unbedenklichkeit des Antibiotikums. 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Nicht über 25 C lagern. Durchstechflasche fest verschlossen halten. Durchstechflasche im Umkarton aufbewahren. Bezüglich Lagerungsbedingungen des rekonstituierten Arzneimittels, siehe Abschnitt Art und Inhalt des Behältnisses 1,0 g Pulver zur Herstellung einer Injektionslösung: 10 ml Durchstechflaschen aus farblosem Pressglas Typ III, mit Gummistopfen und versiegelt mit einer Aluminium-Kappe in Packungen zu 1, 5, 10, 25, 50, 100, 250 und 1000 Stück. 2,0 g Pulver zur Herstellung einer Infusionslösung: 50 ml Durchstechflaschen aus farblosem Pressglas Typ I, mit Gummistopfen und versiegelt mit einer Aluminium-Kappe in Packungen zu 1, 5, 10, 25, 50, 100, 250 und 1000 Stück. Einige Packungen sind nur für den Einsatz in Kliniken bestimmt. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Handhabung und Entsorgung Intravenöse Injektion Für die intravenöse Injektion wird Cefotaxim Hikma 1,0 g Pulver zur Herstellung einer Injektionslösung, enthalten in einer 10-ml- Durchstechflasche, in mindestens 4 ml und 2,0 g Pulver zur Herstellung einer Infusionslösung, enthalten in einer 50-ml-Durchstechflasche, in mindestens 10 ml Wasser für Injektionszwecke gelöst und anschließend direkt während 3 bis 5 Minuten in die Vene oder nach Abklemmen des Infusionsschlauchs in das distale Schlauchende injiziert. Infusion Für die Kurzinfusion wird 2,0 g Pulver zur Herstellung einer Infusionslösung, enthalten in einer 50-ml-Durchstechflasche, in 40 bis 50 ml Wasser für Injektionszwecke oder einer kompatiblen Infusionslösung (siehe weiter unten) gelöst und anschließend während ca. 20 Minuten intravenös infundiert. Für die Dauertropfinfusion wird Cefotaxim Hikma 2,0 g Pulver zur Herstellung einer Infusionslösung, enthalten in einer 50-ml- Durchstechflasche, in 50 ml einer Natriumchloridlösung 9 mg/ml (0,9 %) gelöst. Die erhaltene Lösung wird auf 100 ml verdünnt und anschließend während 50 bis 60 Minuten intravenös infundiert. Zur Zubereitung kann auch eine andere kompatible Lösung verwendet A n Intramuskuläre Injektion Für die intramuskuläre Injektion wird Cefotaxim Hikma 1,0 g Pulver zur Herstellung einer Injektionslösung, enthalten in einer 10-ml- Durchstechflasche, in 4 ml Wasser für Injektionszwecke gelöst. Anschließend sollte die Injektion tief in den Gesäßmuskel erfolgen. Schmerzen bei der intramuskulären Injektion lassen sich durch Lösen von Cefotaxim Hikma 1,0 g Pulver zur Herstellung einer Injektionslösung in 4 ml 1%iger Lidocainlösung vermeiden. ist kompatibel mit den folgenden Infusionslösungen: Wasser für Injektionszwecke, Natriumchloridlösung 9 mg/ml (0,9 %), Glucoselösung 50 mg/ml (5 %), Glucoselösung 100 mg/ml (10 %), Natriumlactatlösung, Metronidazollösung 500 mg/100 ml, Vollelektrolytlösung und 2 / 3 -Elektrolytlösung (bezüglich des Natriumgehaltes siehe Abschnitt 4.4) Cefatoxim ist auch mit Lidocain kompatibel, es dürfen jedoch nur frisch zubereitete Lösungen ausschließlich für die intramuskuläre Injektion verwendet werden (siehe Abschnitt 4.3, 4.4 und 4.8). Die fertig zubereitete Lösung muss klar sein. Wenn Partikel sichtbar sind, darf die Lösung nicht verwendet Die fertig zubereitete Lösung ist nur zur Anwendung bei einem Patienten bestimmt. Ungebrauchte Lösung muss entsorgt 7. INHABER DER ZULASSUNG Hikma Farmacêutica (Portugal), S.A. Estrada do Rio da Mó n 8, 8A e 8B Fervença Terrugem SNT Portugal Tel.: Fax: ZULASSUNGSNUMMER(n) 1,0 g Pulver zur Herstellung einer Injektionslösung: ,0 g Pulver zur Herstellung einer Infusionslösung: DATUM DER VERLÄNGERUNG DER ZULASSUNG STAND DER INFORMATION 11. VERKAUFSABGRENZUNG Verschreibungspflichtig Mitvertrieb: GmbH Am Woog Nieder-Olm Tel.: +49(0) Fax: +49(0) Zentrale Anforderung an: Rote Liste Service GmbH FachInfo-Service Postfach Berlin 5
Cefotaxim-ratiopharm
 1. BEZEICHNUNG DER ARZNEIMITTEL (Pulver zur Herstellung einer Injektionslösung) (Pulver zur Herstellung einer Injektions- bzw. Infusionslösung) (Pulver zur Herstellung einer Injektions- bzw. Infusionslösung)
1. BEZEICHNUNG DER ARZNEIMITTEL (Pulver zur Herstellung einer Injektionslösung) (Pulver zur Herstellung einer Injektions- bzw. Infusionslösung) (Pulver zur Herstellung einer Injektions- bzw. Infusionslösung)
Fresenius Kabi. Cefotaxim Fresenius 2 g. Fachinformation. Tagesdosis Cefotaxim. Dosierungsintervall. Cefotaxim. 1. Bezeichnung des Arzneimittels
 1. Bezeichnung des Arzneimittels, Pulver zur Herstellung einer Injektionslösung 2. Qualitative und quantitative Zusammensetzung 1 Durchstechflasche enthält 2,096 g Cefotaxim-Natrium, entsprechend 2 g Cefotaxim.
1. Bezeichnung des Arzneimittels, Pulver zur Herstellung einer Injektionslösung 2. Qualitative und quantitative Zusammensetzung 1 Durchstechflasche enthält 2,096 g Cefotaxim-Natrium, entsprechend 2 g Cefotaxim.
Fachinformation. Die sonstigen Bestandteile sind im Abschnitt 6.1 vollständig aufgelistet.
 Fachinformation 1. Bezeichnung des Arzneimittels Epogam Weichkapseln 500 mg Nachtkerzensamenöl 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 Weichkapsel Epogam enthält 500 mg Nachtkerzensamenöl.
Fachinformation 1. Bezeichnung des Arzneimittels Epogam Weichkapseln 500 mg Nachtkerzensamenöl 2. Qualitative und quantitative Zusammensetzung Wirkstoff: 1 Weichkapsel Epogam enthält 500 mg Nachtkerzensamenöl.
Hedera Effervescent Tablets MODULE Product Information SPC, Labelling and Package Leaflet 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 50 mg Brausetabletten
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 50 mg Brausetabletten
werden Folgende Angaben können als Dosierungsrichtlinie dienen: Art der Infektion Einzeldosis Cefotaxim Infektionen, bei denen ein empfindlicher
 Claforan 0,5 g-trockenstechampullen 2. Qualitative und quantitative Zusammensetzung 1 Durchstechflasche enthält 0,524 g Cefotaxim-Natrium, entsprechend 0,5 g Cefotaxim. Na +- Konzentration: 2,09 mmol/g.
Claforan 0,5 g-trockenstechampullen 2. Qualitative und quantitative Zusammensetzung 1 Durchstechflasche enthält 0,524 g Cefotaxim-Natrium, entsprechend 0,5 g Cefotaxim. Na +- Konzentration: 2,09 mmol/g.
FACHINFORMATION ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. 1. BEZEICHNUNG DES ARZNEIMITTELS Tonsipret Tabletten
 1/5 FACHINFORMATION ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tonsipret Tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG In 1 Tablette sind enthalten: Capsicum
1/5 FACHINFORMATION ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Tonsipret Tabletten 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG In 1 Tablette sind enthalten: Capsicum
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Penstapho 1 g, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung.
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Penstapho 1 g, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung. Natriumoxazillin Monohydrat Lesen Sie die gesamte Packungsbeilage sorgfältig
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Penstapho 1 g, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung. Natriumoxazillin Monohydrat Lesen Sie die gesamte Packungsbeilage sorgfältig
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET
 1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 100 mg Brausetabletten
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 100 mg Brausetabletten
Gebrauchsinformation: Information für Anwender. Combactam 1 g - Trockenstechampullen Sulbactam-Natrium
 1 Gebrauchsinformation: Information für Anwender Combactam 1 g - Trockenstechampullen Sulbactam-Natrium Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
1 Gebrauchsinformation: Information für Anwender Combactam 1 g - Trockenstechampullen Sulbactam-Natrium Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Fachinformation 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Echinacin Salbe Madaus 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: 100 g Salbe enthalten: Presssaft aus frischem blühendem Purpursonnenhutkraut
Fachinformation 1. BEZEICHNUNG DES ARZNEIMITTELS Echinacin Salbe Madaus 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Wirkstoff: 100 g Salbe enthalten: Presssaft aus frischem blühendem Purpursonnenhutkraut
Mucosan 15 mg - Ampullen werden als zusätzliches Arzneimittel zur Behandlung des Atemnotsyndroms bei Früh- und Neugeborenen (IRDS) angewendet.
 PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Mucosan 15 mg - Ampullen Wirkstoff: Ambroxolhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor der Arzt mit der
PACKUNGSBEILAGE 1 Gebrauchsinformation: Information für Anwender Mucosan 15 mg - Ampullen Wirkstoff: Ambroxolhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor der Arzt mit der
Fachinformation. Sehr geehrte Damen und Herren,
 Datum: 09.05.2014 Kontakt: Veronika Iro Abteilung: REGA Tel. / Fax: +43 (0) 505 55 36247 E-Mail: pv-implementation@ages.at Unser Zeichen: 16c-140509-00024-A-PHV Ihr Zeichen: PHV-issue: Clindamycin hältige
Datum: 09.05.2014 Kontakt: Veronika Iro Abteilung: REGA Tel. / Fax: +43 (0) 505 55 36247 E-Mail: pv-implementation@ages.at Unser Zeichen: 16c-140509-00024-A-PHV Ihr Zeichen: PHV-issue: Clindamycin hältige
FACHINFORMATION. der Tagesdosis auf 200 mg Cefotaxim pro Kilogramm Körpergewicht erforderlich
 FACHINFORMATION Claforan Juni 2017 204107 1. BEZEICHNUNG DER ARZNEIMITTEL Claforan 1,0 g Pulver mit Lösungsmittel zur Herstellung Claforan 2,0 g Pulver mit Lösungsmittel zur Herstellung 2. QUALITATIVE
FACHINFORMATION Claforan Juni 2017 204107 1. BEZEICHNUNG DER ARZNEIMITTEL Claforan 1,0 g Pulver mit Lösungsmittel zur Herstellung Claforan 2,0 g Pulver mit Lösungsmittel zur Herstellung 2. QUALITATIVE
Gebrauchsinformation: Information für Anwender. Cefuroxim Fresenius 1500 mg - Trockenstechampullen Wirkstoff: Cefuroxim (als Cefuroxim-Natrium)
 Gebrauchsinformation: Information für Anwender Cefuroxim Fresenius 1500 mg - Trockenstechampullen Wirkstoff: Cefuroxim (als Cefuroxim-Natrium) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender Cefuroxim Fresenius 1500 mg - Trockenstechampullen Wirkstoff: Cefuroxim (als Cefuroxim-Natrium) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Patienten. Trobicin 2 g Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Spectinomycin
 Gebrauchsinformation: Information für Patienten Trobicin 2 g Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Spectinomycin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Patienten Trobicin 2 g Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Spectinomycin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Fachinformation. Sonstige Bestandteile mit bekannter Wirkung:Enthält u.a. Macrogolglycerolhydroxystearat und Ethanol.
 Fachinformation 1. Bezeichnung des Arzneimittels Thymian Hustenlösung Flüssigkeit zum Einnehmen 2. Qualitative und quantitative Zusammensetzung 100 ml (entsprechend 97 g) Flüssigkeit enthalten: Wirkstoff:
Fachinformation 1. Bezeichnung des Arzneimittels Thymian Hustenlösung Flüssigkeit zum Einnehmen 2. Qualitative und quantitative Zusammensetzung 100 ml (entsprechend 97 g) Flüssigkeit enthalten: Wirkstoff:
Cefotaxim-Pharmore 0,5 g
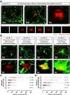 1. Bezeichnung des Arzneimittels, Pulver zur Herstellung einer Injektionslösung 2. Qualitative und quantitative Zusammensetzung 1 Durchstechflasche Cefotaxim-Pharmore 0,5 g enthält 0,524 g Cefotaxim-Natrium,
1. Bezeichnung des Arzneimittels, Pulver zur Herstellung einer Injektionslösung 2. Qualitative und quantitative Zusammensetzung 1 Durchstechflasche Cefotaxim-Pharmore 0,5 g enthält 0,524 g Cefotaxim-Natrium,
Fachinformation. (Zusammenfassung der Merkmale des Arzneimittels / SmPC)
 (Zusammenfassung der Merkmale des Arzneimittels / SmPC) 1. Bezeichnung des Arzneimittels Myacyne-Salbe 5 mg/g Salbe Wirkstoff: Neomycinsulfat 2. Qualitative und quantitative Zusammensetzung Wirkstoff:
(Zusammenfassung der Merkmale des Arzneimittels / SmPC) 1. Bezeichnung des Arzneimittels Myacyne-Salbe 5 mg/g Salbe Wirkstoff: Neomycinsulfat 2. Qualitative und quantitative Zusammensetzung Wirkstoff:
Fachinformation. Sonstige Bestandteile Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Fachinformation 1. Bezeichnung des Arzneimittels Luivac 3 mg Tabletten 2. Qualitative und quantitative Zusammensetzung Wirkstoff 1 Tablette enthält 3 mg Lysat aus mindestens je 1 x 10 9 Keimen von Staphylococcus
Fachinformation 1. Bezeichnung des Arzneimittels Luivac 3 mg Tabletten 2. Qualitative und quantitative Zusammensetzung Wirkstoff 1 Tablette enthält 3 mg Lysat aus mindestens je 1 x 10 9 Keimen von Staphylococcus
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Claforan 2,0 g Pulver (bzw. Pulver und Lösungsmittel) zur Herstellung einer Injektions-/Infusionslösung Wirkstoff: Cefotaxim-Natrium Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender Claforan 2,0 g Pulver (bzw. Pulver und Lösungsmittel) zur Herstellung einer Injektions-/Infusionslösung Wirkstoff: Cefotaxim-Natrium Lesen Sie die gesamte
Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem Antigenhalt)
 Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. 1 Durchstechflasche enthält Sulbactam-Natrium entsprechend 1 g Sulbactam (ca. 4,4 mmol Natrium).
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Combactam 1 g - Trockenstechampullen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche enthält Sulbactam-Natrium
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Combactam 1 g - Trockenstechampullen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche enthält Sulbactam-Natrium
Fachinformation. 2. Qualitative und quantitative Zusammensetzung
 Benproperinphosphat überzogene Tabletten 33 mg Stoff Darreichungsform Menge Anlage Fachinformation 1. Bezeichnung des Arzneimittels Tussafug, überzogene Tabletten 2. Qualitative und quantitative Zusammensetzung
Benproperinphosphat überzogene Tabletten 33 mg Stoff Darreichungsform Menge Anlage Fachinformation 1. Bezeichnung des Arzneimittels Tussafug, überzogene Tabletten 2. Qualitative und quantitative Zusammensetzung
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. Addaven Konzentrat zur Herstellung einer Infusionslösung
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Addaven Konzentrat zur Herstellung einer Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Addaven enthält:
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Addaven Konzentrat zur Herstellung einer Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Addaven enthält:
Fachinformation. einer chronisch obstruktiven Lungenerkrankung
 Stand: September 2016 1. Bezeichnung der Arzneimittel Ceftriaxon HEXAL 0,5 g Pulver zur Herstellung einer Injektionslösung Ceftriaxon HEXAL 1 g Pulver zur Herstellung einer Injektionslösung Ceftriaxon
Stand: September 2016 1. Bezeichnung der Arzneimittel Ceftriaxon HEXAL 0,5 g Pulver zur Herstellung einer Injektionslösung Ceftriaxon HEXAL 1 g Pulver zur Herstellung einer Injektionslösung Ceftriaxon
Natriumhydrogencarbonat-Lösung 4,2 %/8.4 % AlleMan Pharma. Fachinformation FACHINFORMATION
 Natriumhydrogencarbonat-Lösung 4,2 %/8.4 % AlleMan Pharma Fachinformation FACHINFORMATION 1. Bezeichnung der Arzneimittel Wirkstoff: Natriumhydrogencarbonat 2. Qualitative und quantitative Zusammensetzung
Natriumhydrogencarbonat-Lösung 4,2 %/8.4 % AlleMan Pharma Fachinformation FACHINFORMATION 1. Bezeichnung der Arzneimittel Wirkstoff: Natriumhydrogencarbonat 2. Qualitative und quantitative Zusammensetzung
8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen
 8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Amoxicillin Amoxypen j Grampositive (nicht S. aureus) und gramnegative Keime (H. influenzae ca. 10 % Resistenz) * Erwachsene, Kinder 412 Jahre
8 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Amoxicillin Amoxypen j Grampositive (nicht S. aureus) und gramnegative Keime (H. influenzae ca. 10 % Resistenz) * Erwachsene, Kinder 412 Jahre
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. NAME DES TIERARZNEIMITTELS Metacam 20 mg/ml Injektionslösung für Rinder und Schweine 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Metacam 20 mg/ml
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. NAME DES TIERARZNEIMITTELS Metacam 20 mg/ml Injektionslösung für Rinder und Schweine 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Metacam 20 mg/ml
PACKUNGSBEILAGE : INFORMATION FÜR DEN ANWENDER. Ampicillin-Natrium
 PACKUNGSBEILAGE : INFORMATION FÜR DEN ANWENDER PENTREXYL 250 mg Pulver zur Herstellung einer Injektionslösung PENTREXYL 1 g Pulver zur Herstellung einer Injektionslösung PENTREXYL 2 g Pulver zur Herstellung
PACKUNGSBEILAGE : INFORMATION FÜR DEN ANWENDER PENTREXYL 250 mg Pulver zur Herstellung einer Injektionslösung PENTREXYL 1 g Pulver zur Herstellung einer Injektionslösung PENTREXYL 2 g Pulver zur Herstellung
Fachinformation. 4.2 Dosierung und Art der Anwendung
 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche enthält 500 mg Ceftriaxon als Ceftriaxon-Natrium
1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche enthält 500 mg Ceftriaxon als Ceftriaxon-Natrium
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Heumann s Blasen- und Nierentee Solubitrat 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Messlöffel (= 1,2 g) Teeaufgusspulver
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Heumann s Blasen- und Nierentee Solubitrat 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Messlöffel (= 1,2 g) Teeaufgusspulver
Fachinformation. 4.2 Dosierung und Art der Anwendung
 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche enthält 1 g Ceftriaxon als Ceftriaxon-Natrium.
1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche enthält 1 g Ceftriaxon als Ceftriaxon-Natrium.
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Ancesol 10 mg/ml Injektionslösung für Rinder 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml enthält:
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Ancesol 10 mg/ml Injektionslösung für Rinder 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml enthält:
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 [Version 7.3.2, 10/2011] ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Theranekron D6 Injektionslösung für Tiere 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
[Version 7.3.2, 10/2011] ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Theranekron D6 Injektionslösung für Tiere 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. Was ist Medivitan iv und wofür wird es angewendet?
 Medivitan iv Vitamin B6, Vitamin B12 und Folsäure, Steigerung körperlicher und geistiger Vitalität, Vitamin-B-Mangel, Abgeschlagenheit, Erschöpfung, Schlafstörungen, Konzentrationsschwäche Antriebslosigkeit,
Medivitan iv Vitamin B6, Vitamin B12 und Folsäure, Steigerung körperlicher und geistiger Vitalität, Vitamin-B-Mangel, Abgeschlagenheit, Erschöpfung, Schlafstörungen, Konzentrationsschwäche Antriebslosigkeit,
Zusammenfassung der Merkmale des Arzneimittels
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Carvomin Verdauungstropfen 2. Qualitative und quantitative Zusammensetzung 10 g (entsprechen 10,8 ml) enthalten: 10 g Flüssigextrakt
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Carvomin Verdauungstropfen 2. Qualitative und quantitative Zusammensetzung 10 g (entsprechen 10,8 ml) enthalten: 10 g Flüssigextrakt
Gebrauchsinformation: Information für Anwender. Cefobid 2 g Trockenstechampullen Wirkstoff: Cefoperazon-Natrium
 Gebrauchsinformation: Information für Anwender Cefobid 2 g Trockenstechampullen Wirkstoff: Cefoperazon-Natrium Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
Gebrauchsinformation: Information für Anwender Cefobid 2 g Trockenstechampullen Wirkstoff: Cefoperazon-Natrium Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses
GEBRAUCHSINFORMATION FÜR. Novomate 277,8 mg/ml Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension für. für Rinder
 GEBRAUCHSINFORMATION FÜR Novomate 277,8 mg/ml Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension für Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES
GEBRAUCHSINFORMATION FÜR Novomate 277,8 mg/ml Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension für Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES
FACHINFORMATION. 4.2 Dosierung und Art der Anwendung
 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche mit 0,596 g Pulver enthält 0,596 g Ceftriaxon-Dinatrium
1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Durchstechflasche mit 0,596 g Pulver enthält 0,596 g Ceftriaxon-Dinatrium
Fachinformation von Cordes BPO 3%, -5%, -10%
 1. Bezeichnung des Arzneimittels Cordes BPO 3% / -5% / -10% Gel Wirkstoff: Benzoylperoxid 2. Qualitative und quantitative Zusammensetzung Cordes BPO 3% 1 g Gel enthält: Wirkstoff: Benzoylperoxid 0,03 g
1. Bezeichnung des Arzneimittels Cordes BPO 3% / -5% / -10% Gel Wirkstoff: Benzoylperoxid 2. Qualitative und quantitative Zusammensetzung Cordes BPO 3% 1 g Gel enthält: Wirkstoff: Benzoylperoxid 0,03 g
apothekenpflichtig Trockenextrakt aus Efeublättern (4-8:1), Auszugsmittel: Ethanol 30 % (m/m) Brausetabletten 50 mg Fachinformation
 1. Bezeichnung des Arzneimittels Bronchogard Hustenlöser, Brausetabletten Fachinformation 2. Qualitative und quantitative Zusammensetzung Wirkstoff: Efeublätter-Trockenextrakt Eine Brausetablette enthält:
1. Bezeichnung des Arzneimittels Bronchogard Hustenlöser, Brausetabletten Fachinformation 2. Qualitative und quantitative Zusammensetzung Wirkstoff: Efeublätter-Trockenextrakt Eine Brausetablette enthält:
Gebrauchsinformation: Information für Anwender. Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung. Wirkstoff: Cefuroxim
 PACKUNGSBEILAGE Gebrauchsinformation: Information für Anwender Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung Wirkstoff: Cefuroxim Lesen Sie die gesamte Packungsbeilage sorgfältig
PACKUNGSBEILAGE Gebrauchsinformation: Information für Anwender Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung Wirkstoff: Cefuroxim Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Medivitan iv Ampullen 5mg, 1mg, 1,05mg Injektionslösung Wirkstoffe: Pyridoxinhydrochlorid / Cyanocobalamin / Folsäure Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Medivitan iv Ampullen 5mg, 1mg, 1,05mg Injektionslösung Wirkstoffe: Pyridoxinhydrochlorid / Cyanocobalamin / Folsäure Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Medivitan iv Fertigspritze 5mg, 1mg, 1,05mg Injektionslösung Wirkstoffe: Pyridoxinhydrochlorid / Cyanocobalamin / Folsäure Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für Anwender Medivitan iv Fertigspritze 5mg, 1mg, 1,05mg Injektionslösung Wirkstoffe: Pyridoxinhydrochlorid / Cyanocobalamin / Folsäure Lesen Sie die gesamte Packungsbeilage
Proposed Summary of Product Characteristic in Germany Clean version
 Page 1 Proposed Summary of Product Characteristic in Germany Clean version Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Tantum Verde mit Orange-Honiggeschmack 3 mg Lutschtabletten
Page 1 Proposed Summary of Product Characteristic in Germany Clean version Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Tantum Verde mit Orange-Honiggeschmack 3 mg Lutschtabletten
Gebrauchsinformation: Information für Anwender. Vancomycin-MIP 1000 mg Pulver zur Herstellung einer Infusionslösung Vancomycin Hydrochlorid
 Gebrauchsinformation: Information für Anwender Vancomycin-MIP 1000 mg Pulver zur Herstellung einer Infusionslösung Vancomycin Hydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender Vancomycin-MIP 1000 mg Pulver zur Herstellung einer Infusionslösung Vancomycin Hydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
1. Was ist Cefuroxim Fresenius Kabi und wofür wird es angewendet?
 Gebrauchsinformationen: Information für Anwender Cefuroxim Fresenius Kabi 750 mg Pulver zur Herstellung einer Injektionslösung / Infusionslösung Cefuroxim Lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformationen: Information für Anwender Cefuroxim Fresenius Kabi 750 mg Pulver zur Herstellung einer Injektionslösung / Infusionslösung Cefuroxim Lesen Sie die gesamte Packungsbeilage sorgfältig
Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 Modul 1.3.1 Pentofuryl 200mg Hartkapseln Seite 1 Fachinformation 1. Bezeichnung des Arzneimittels Pentofuryl 200mg Hartkapseln Wirkstoff: Nifuroxazid 2. Qualitative und quantitative Zusammensetzung 1 Hartkapsel
Modul 1.3.1 Pentofuryl 200mg Hartkapseln Seite 1 Fachinformation 1. Bezeichnung des Arzneimittels Pentofuryl 200mg Hartkapseln Wirkstoff: Nifuroxazid 2. Qualitative und quantitative Zusammensetzung 1 Hartkapsel
Zusammenfassung der Merkmale des Arzneimittels
 1. Bezeichnung des Arzneimittels Eucabal -Hustensaft Zusammenfassung der Merkmale des Arzneimittels 2. Qualitative und quantitative Zusammensetzung 100 ml enthalten: 19,2 g Flüssigextrakt aus Thymian (Thymi
1. Bezeichnung des Arzneimittels Eucabal -Hustensaft Zusammenfassung der Merkmale des Arzneimittels 2. Qualitative und quantitative Zusammensetzung 100 ml enthalten: 19,2 g Flüssigextrakt aus Thymian (Thymi
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Claforan 1,0 g Pulver (bzw. Pulver und Lösungsmittel) zur Herstellung einer Injektions-/Infusionslösung Wirkstoff: Cefotaxim-Natrium Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender Claforan 1,0 g Pulver (bzw. Pulver und Lösungsmittel) zur Herstellung einer Injektions-/Infusionslösung Wirkstoff: Cefotaxim-Natrium Lesen Sie die gesamte
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 2 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Page 1 of 6 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 BEZEICHNUNG DES ARZNEIMITTELS Poliovaccine SSI Injektionslösung in einer Fertigspritze 2 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Je Dosis
Page 1 of 6 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 BEZEICHNUNG DES ARZNEIMITTELS Poliovaccine SSI Injektionslösung in einer Fertigspritze 2 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Je Dosis
Mycostatin - orale Suspension
 Dermapharm GmbH Gebrauchsinformation: Information für den Anwender Mycostatin - orale Suspension Wirkstoff: Nystatin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Dermapharm GmbH Gebrauchsinformation: Information für den Anwender Mycostatin - orale Suspension Wirkstoff: Nystatin Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender. Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung
 PACKUNGSBEILAGE Gebrauchsinformation: Information für Anwender Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung Wirkstoff: Cefuroxim-Natrium Lesen Sie die gesamte Packungsbeilage
PACKUNGSBEILAGE Gebrauchsinformation: Information für Anwender Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung Wirkstoff: Cefuroxim-Natrium Lesen Sie die gesamte Packungsbeilage
GEBRAUCHSINFORMATION FÜR. Baytril - Das Original mg/ml Injektionslösung
 GEBRAUCHSINFORMATION FÜR Baytril - Das Original - 100 mg/ml Injektionslösung 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTER- SCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
GEBRAUCHSINFORMATION FÜR Baytril - Das Original - 100 mg/ml Injektionslösung 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTER- SCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
Gebrauchsinformation. Excenel FLOW 50mg/ml Injektionssuspension für Schweine und Rinder
 Gebrauchsinformation Excenel FLOW 50mg/ml Injektionssuspension für Schweine und Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
Gebrauchsinformation Excenel FLOW 50mg/ml Injektionssuspension für Schweine und Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
Antibiotika in der Praxis mit Hygieneratschlägen
 Antibiotika in der Praxis mit Hygieneratschlägen Bearbeitet von Uwe Frank, Franz Daschner 9., vollst. überarb. Aufl. 2010. Taschenbuch. XII, 201 S. Paperback ISBN 978 3 642 10459 6 Weitere Fachgebiete
Antibiotika in der Praxis mit Hygieneratschlägen Bearbeitet von Uwe Frank, Franz Daschner 9., vollst. überarb. Aufl. 2010. Taschenbuch. XII, 201 S. Paperback ISBN 978 3 642 10459 6 Weitere Fachgebiete
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Natriumhydrogencarbonat-Lösung 8,4 % DELTAMEDICA Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1000 ml
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Natriumhydrogencarbonat-Lösung 8,4 % DELTAMEDICA Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1000 ml
9 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Kosten
 9 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Kosten 9 Amikacin Amikacin j Grampositive (Staphylokokken, nicht: Pneumokokken, Streptokokken, Enterokokken), gramnegative Keime, insbesondere
9 Antibiotika, Antimykotika: Spektrum Dosierung Nebenwirkungen Kosten 9 Amikacin Amikacin j Grampositive (Staphylokokken, nicht: Pneumokokken, Streptokokken, Enterokokken), gramnegative Keime, insbesondere
Creme Bactroban Creme ist eine weiße Creme von homogenem Aussehen.
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bactroban 2 % - Creme 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jedes Gramm Creme enthält 21,5 mg Mupirocin-Calcium
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bactroban 2 % - Creme 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jedes Gramm Creme enthält 21,5 mg Mupirocin-Calcium
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Otanol 1 mg Ohrentropfen, Lösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine 0,5 ml Einzeldosis enthält: Ciprofloxacin,
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Otanol 1 mg Ohrentropfen, Lösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine 0,5 ml Einzeldosis enthält: Ciprofloxacin,
VANCOMYCIN ENTEROCAPS 250 mg; Hartkapseln Wirkstoff: Vancomycinhydrochlorid
 Gebrauchsinformation: Information für den Anwender VANCOMYCIN ENTEROCAPS 250 mg; Hartkapseln Wirkstoff: Vancomycinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
Gebrauchsinformation: Information für den Anwender VANCOMYCIN ENTEROCAPS 250 mg; Hartkapseln Wirkstoff: Vancomycinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der
VITAMIN C-ROTEXMEDICA
 Gebrauchsinformation: Information für den Anwender 100 mg/ml, Injektionslösung Wirkstoff: Ascorbinsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
Gebrauchsinformation: Information für den Anwender 100 mg/ml, Injektionslösung Wirkstoff: Ascorbinsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER. Neurobion 100 mg 100 mg 1 mg / 3 ml Injektionslösung Vitamine B 1 + B 6 + B 12
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Neurobion 100 mg 100 mg 1 mg / 3 ml Injektionslösung Vitamine B 1 + B 6 + B 12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch bevor Sie mit der Anwendung
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Neurobion 100 mg 100 mg 1 mg / 3 ml Injektionslösung Vitamine B 1 + B 6 + B 12 Lesen Sie die gesamte Packungsbeilage sorgfältig durch bevor Sie mit der Anwendung
Cefuroxim-ratiopharm p.i.
 1. BEZEICHNUNG DER ARZNEIMITTEL Pulver zur Herstellung einer Injektionslösung Pulver zur Herstellung einer Injektions- oder Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Durchstechflasche
1. BEZEICHNUNG DER ARZNEIMITTEL Pulver zur Herstellung einer Injektionslösung Pulver zur Herstellung einer Injektions- oder Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Durchstechflasche
Wortlaut der für die Packungsbeilage vorgesehenen Angaben
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender Cefuroxim 1500 mg Generics Pulver zur Herstellung einer Injektionslösung Wirkstoff: Cefuroxim-Natrium
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation: Information für den Anwender Cefuroxim 1500 mg Generics Pulver zur Herstellung einer Injektionslösung Wirkstoff: Cefuroxim-Natrium
SYNULOX TABL 250 mg GI. [Version 7.3.1, 11/2010] B. PACKUNGSBEILAGE. Seite
![SYNULOX TABL 250 mg GI. [Version 7.3.1, 11/2010] B. PACKUNGSBEILAGE. Seite SYNULOX TABL 250 mg GI. [Version 7.3.1, 11/2010] B. PACKUNGSBEILAGE. Seite](/thumbs/72/67018840.jpg) [Version 7.3.1, 11/2010] B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Synulox forte 200 mg/ 50 mg Tabletten für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
[Version 7.3.1, 11/2010] B. PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION Synulox forte 200 mg/ 50 mg Tabletten für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
PACKUNGSBEILAGE Carprogesic 50mg/ml Injektionslösung für Hunde und Katzen
 B. PACKUNGSBEILAGE PACKUNGSBEILAGE Carprogesic 50mg/ml Injektionslösung für Hunde und Katzen 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
B. PACKUNGSBEILAGE PACKUNGSBEILAGE Carprogesic 50mg/ml Injektionslösung für Hunde und Katzen 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
Cefuroxim-ratiopharm p.i
 1. BEZEICHNUNG DER ARZNEIMITTEL Cefuroxim-ratiopharm 250 mg p.i. Pulver zur Herstellung einer Injektionslösung Cefuroxim-ratiopharm 750 mg p.i. Cefuroxim-ratiopharm 1500 mg p.i. Pulver zur Herstellung
1. BEZEICHNUNG DER ARZNEIMITTEL Cefuroxim-ratiopharm 250 mg p.i. Pulver zur Herstellung einer Injektionslösung Cefuroxim-ratiopharm 750 mg p.i. Cefuroxim-ratiopharm 1500 mg p.i. Pulver zur Herstellung
250 mg Kapsel: Braune 21,4 ± 0,40 mm Hartkapsel, mit einer weißen bis fast weißen flüssigen Mischung als feste Masse.
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Vancomycin Dr. Eberth 250 mg Hartkapseln 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede 250 mg Hartkapsel enthält 250
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Vancomycin Dr. Eberth 250 mg Hartkapseln 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede 250 mg Hartkapsel enthält 250
FACHINFORMATION. der Tagesdosis auf 200 mg Cefotaxim pro Kilogramm Körpergewicht erforderlich
 Claforan 1. BEZEICHNUNG DER ARZNEIMITTEL Claforan 0,5 g einer Injektionslösung Claforan 1,0 g Claforan 2,0 g Wirkstoff: Cefotaxim-Natrium Folgende Tabelle kann als Dosierungsrichtlinie gelten: Art der
Claforan 1. BEZEICHNUNG DER ARZNEIMITTEL Claforan 0,5 g einer Injektionslösung Claforan 1,0 g Claforan 2,0 g Wirkstoff: Cefotaxim-Natrium Folgende Tabelle kann als Dosierungsrichtlinie gelten: Art der
Sonstige Bestandteile: Eine vollständige Auflistung der sonstigen Bestandteile finden Sie unter Abschnitt 6.1.
 1. BEZEICHNUNG DES TIERARZNEIMITTELS Shotaflor 300 mg/ml Injektionslösung für Schweine 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Injektionslösung enthält: Wirkstoff: Florfenicol 300 mg Sonstige
1. BEZEICHNUNG DES TIERARZNEIMITTELS Shotaflor 300 mg/ml Injektionslösung für Schweine 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml Injektionslösung enthält: Wirkstoff: Florfenicol 300 mg Sonstige
Wortlaut der für die Packungsbeilage vorgesehenen Angaben. Kesium 500 mg / 125 mg Kautabletten für Hunde
 Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation Kesium 500 mg / 125 mg Kautabletten für Hunde 1. Name und Anschrift des Zulassungsinhabers und, wenn unterschiedlich, des
Wortlaut der für die Packungsbeilage vorgesehenen Angaben Gebrauchsinformation Kesium 500 mg / 125 mg Kautabletten für Hunde 1. Name und Anschrift des Zulassungsinhabers und, wenn unterschiedlich, des
Zur Anwendung bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen
 Gebrauchsinformation: Information für den Anwender Captin Zäpfchen 500 mg Zur Anwendung bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen Wirkstoff: Paracetamol Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender Captin Zäpfchen 500 mg Zur Anwendung bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen Wirkstoff: Paracetamol Lesen Sie die gesamte Packungsbeilage
Lösung zur Anwendung auf der Haut. Stoff Darreichungsform Menge. Fachinformation
 Clindamycin-2- dihydrogenphosphat Lösung zur Anwendung auf der Haut 11,9 mg (entspricht 10mg Clindamycin) Stoff Darreichungsform Menge Anlage Fachinformation 1. Bezeichnung des Arzneimittels Basocin 1%
Clindamycin-2- dihydrogenphosphat Lösung zur Anwendung auf der Haut 11,9 mg (entspricht 10mg Clindamycin) Stoff Darreichungsform Menge Anlage Fachinformation 1. Bezeichnung des Arzneimittels Basocin 1%
Paracetamol 1000 mg Heumann Zäpfchen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Paracetamol 1000 mg Heumann Zäpfchen Zur Anwendung bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen Wirkstoff: Paracetamol Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Paracetamol 1000 mg Heumann Zäpfchen Zur Anwendung bei Kindern und Jugendlichen ab 12 Jahren und Erwachsenen Wirkstoff: Paracetamol Lesen Sie die gesamte
Jede Lutschtablette enthält 3 mg Benzydaminhydrochlorid (entsprechend 2,68 mg Benzydamin).
 1. BEZEICHNUNG DES ARZNEIMITTELS Tantum Verde mit Minzgeschmack 3 mg Lutschtabletten Benzydaminhydrochlorid 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Lutschtablette enthält 3 mg Benzydaminhydrochlorid
1. BEZEICHNUNG DES ARZNEIMITTELS Tantum Verde mit Minzgeschmack 3 mg Lutschtabletten Benzydaminhydrochlorid 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Lutschtablette enthält 3 mg Benzydaminhydrochlorid
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. Nux vomica-homaccord -Tropfen
 1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
1/5 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN Nux vomica-homaccord -Tropfen Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses Arzneimittels beginnen, denn
1. WAS SIND BRONCHO-VAXOM TROPFEN UND WOFÜR WERDEN SIE ANGEWENDET?
 Gebrauchsinformation: Information für den Anwender Broncho-Vaxom Tropfen 3,5 mg Tropfen zum Einnehmen, Lösung Zur Anwendung bei Kindern ab 1 Jahr Wirkstoff: Bakterienextrakt Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender Broncho-Vaxom Tropfen 3,5 mg Tropfen zum Einnehmen, Lösung Zur Anwendung bei Kindern ab 1 Jahr Wirkstoff: Bakterienextrakt Lesen Sie die gesamte Packungsbeilage
Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahre
 Gebrauchsinformation: Information für den Anwender Aspecton Eukaps 200 mg Weichkapseln Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahre Wirkstoff: Eucalyptusöl Lesen Sie die gesamte Packungsbeilage
Gebrauchsinformation: Information für den Anwender Aspecton Eukaps 200 mg Weichkapseln Zur Anwendung bei Erwachsenen und Jugendlichen ab 12 Jahre Wirkstoff: Eucalyptusöl Lesen Sie die gesamte Packungsbeilage
Aciclovir A Pharma ist ein Arzneimittel zur Behandlung von Virusinfektionen
 Gebrauchsinformation: Information für den Anwender Aciclovir 200-1 A Pharma Wirkstoff: Aciclovir 200 mg pro Tablette Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte Packungsbeilage sorgfältig
Gebrauchsinformation: Information für den Anwender Aciclovir 200-1 A Pharma Wirkstoff: Aciclovir 200 mg pro Tablette Liebe Patientin, lieber Patient! Bitte lesen Sie die gesamte Packungsbeilage sorgfältig
[Version 7.3.2, 10/2011] B. PACKUNGSBEILAGE. Seite 1 von 5
![[Version 7.3.2, 10/2011] B. PACKUNGSBEILAGE. Seite 1 von 5 [Version 7.3.2, 10/2011] B. PACKUNGSBEILAGE. Seite 1 von 5](/thumbs/72/67018826.jpg) [Version 7.3.2, 10/2011] B. PACKUNGSBEILAGE Seite 1 von 5 GEBRAUCHSINFORMATION FÜR Synulox 40 mg/10 mg /ml Pulver zur Herstellung einer Suspension zum Eingeben für Hunde und Katzen 1. NAME UND ANSCHRIFT
[Version 7.3.2, 10/2011] B. PACKUNGSBEILAGE Seite 1 von 5 GEBRAUCHSINFORMATION FÜR Synulox 40 mg/10 mg /ml Pulver zur Herstellung einer Suspension zum Eingeben für Hunde und Katzen 1. NAME UND ANSCHRIFT
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Cefepim Sandoz 2 g Pulver zur Herstellung einer Injektions-/Infusionslösung Wirkstoff: Cefepim Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Cefepim Sandoz 2 g Pulver zur Herstellung einer Injektions-/Infusionslösung Wirkstoff: Cefepim Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für Sie.
 Gebrauchsinformation: Information für den Anwender Bromhexin Krewel Meuselbach Tabletten 12 mg Wirkstoff: Bromhexinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält
Gebrauchsinformation: Information für den Anwender Bromhexin Krewel Meuselbach Tabletten 12 mg Wirkstoff: Bromhexinhydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält
Cefpodoxim - 1 A Pharma
 Stand: Februar 205. Bezeichnung der Arzneimittel Cefpodoxim - A Pharma 00 mg 2. Qualitative und quantitative Zusammensetzung Cefpodoxim - A Pharma 00 mg Filmtablette enthält 00 mg Cefpodoxim, als Cefpodoximproxetil.
Stand: Februar 205. Bezeichnung der Arzneimittel Cefpodoxim - A Pharma 00 mg 2. Qualitative und quantitative Zusammensetzung Cefpodoxim - A Pharma 00 mg Filmtablette enthält 00 mg Cefpodoxim, als Cefpodoximproxetil.
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Curocef 1500 mg Pulver zur Herstellung einer Injektions- oder Infusionslösung 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Gebrauchsinformation: Information für Anwender. Zur Anwendung bei Säuglingen und Kleinkindern
 Gebrauchsinformation: Information für Anwender Peditrace, Infusionslösungskonzentrat Zur Anwendung bei Säuglingen und Kleinkindern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Gebrauchsinformation: Information für Anwender Peditrace, Infusionslösungskonzentrat Zur Anwendung bei Säuglingen und Kleinkindern Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit
Natriumglycerophosphat-Ampulle Fresenius, 306,1 mg/ml, Konzentrat zur Herstellung einer Infusionslösung
 1. BEZEICHNUNG DES ARZNEIMITTELS, 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml enthält: Wasserhaltiges Natriumglycerophosphat (Ph.Eur.) mit ca. 5 H 2O 306,1 mg Na + Phosphat 2-2 mmol/ml 1 mmol/ml
1. BEZEICHNUNG DES ARZNEIMITTELS, 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 ml enthält: Wasserhaltiges Natriumglycerophosphat (Ph.Eur.) mit ca. 5 H 2O 306,1 mg Na + Phosphat 2-2 mmol/ml 1 mmol/ml
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN. EXACYL 500 mg/5 ml Injektionslösung
 GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN EXACYL 500 mg/5 ml Injektionslösung Tranexamsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
GEBRAUCHSINFORMATION: INFORMATION FÜR PATIENTEN EXACYL 500 mg/5 ml Injektionslösung Tranexamsäure Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung dieses Arzneimittels
MediPreis Produktsteckbrief
 MediPreis Produktsteckbrief DOCPELIN NACHTSTERNE DOCPELIN Nachtsterne Filmtabletten Pelikan-Apotheke PZN: 04386054 Menge: 20 St Art: Filmtabletten Link: https://www.medipreis.de/04386054 Anwendungsgebiete
MediPreis Produktsteckbrief DOCPELIN NACHTSTERNE DOCPELIN Nachtsterne Filmtabletten Pelikan-Apotheke PZN: 04386054 Menge: 20 St Art: Filmtabletten Link: https://www.medipreis.de/04386054 Anwendungsgebiete
Gebrauchsinformation
 Gebrauchsinformation Enroxal Max 100 mg/ml Injektionslösung für Rinder und Schweine 1. Name und Anschrift des Zulassungsinhabers und, wenn unterschiedlich, des Herstellers, der für die Chargenfreigabe
Gebrauchsinformation Enroxal Max 100 mg/ml Injektionslösung für Rinder und Schweine 1. Name und Anschrift des Zulassungsinhabers und, wenn unterschiedlich, des Herstellers, der für die Chargenfreigabe
Unübertroffene Compliance durch 3x1 Dosierung
 Unübertroffene Compliance durch 3x1 Dosierung HNO- und Atemwegsinfekte erfordern eine wirksame Therapie mit hoher Sicherheit und bestmöglicher Compliance 3 x 1 ZITHROMAX empfiehlt sich als Mittel der Wahl,
Unübertroffene Compliance durch 3x1 Dosierung HNO- und Atemwegsinfekte erfordern eine wirksame Therapie mit hoher Sicherheit und bestmöglicher Compliance 3 x 1 ZITHROMAX empfiehlt sich als Mittel der Wahl,
Natriumchlorid-Lösung 5,85 % / 10 % / 20 % AlleMan Pharma Fachinformation FACHINFORMATION
 Natriumchlorid-Lösung 5,85 % / 10 % / 20 % AlleMan Pharma Fachinformation FACHINFORMATION 1. Bezeichnung des Arzneimittels 2. Qualitative und quantitative Zusammensetzung Wirkstoffe: Natriumchlorid Sonstige
Natriumchlorid-Lösung 5,85 % / 10 % / 20 % AlleMan Pharma Fachinformation FACHINFORMATION 1. Bezeichnung des Arzneimittels 2. Qualitative und quantitative Zusammensetzung Wirkstoffe: Natriumchlorid Sonstige
FACHINFORMATION. 1 Hartkapsel enthält: 6 mg lysierte immunaktive Fraktionen aus ausgewählten Escherichia-coli-Stämmen.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
Cefuroxim-ratiopharm 125 mg/5 ml TS
 1. BEZEICHNUNG DES ARZNEIMITTELS Granulat zur Herstellung einer Suspension zum Einnehmen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 5 ml (= 1 Messlöffel) der zubereiteten Suspension enthalten 150,36
1. BEZEICHNUNG DES ARZNEIMITTELS Granulat zur Herstellung einer Suspension zum Einnehmen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 5 ml (= 1 Messlöffel) der zubereiteten Suspension enthalten 150,36
ANHANG ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Metacam 1,5 mg/ml Suspension zum Eingeben für Hunde 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Metacam 1,5 mg/ml Suspension zum Eingeben für Hunde 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Fachinformation. Die offiziellen Richtlinien für den angemessenen. Wirkstoffen sind zu berücksichtigen.
 1. BEZEICHNUNG DER ARZNEIMIT- TEL Pulver zur Herstellung einer Injektionslösung Pulver zur Herstellung einer Injektionslösung Pulver zur Herstellung einer Infusionslösung 2. QUALITATIVE UND QUANTITATIVE
1. BEZEICHNUNG DER ARZNEIMIT- TEL Pulver zur Herstellung einer Injektionslösung Pulver zur Herstellung einer Injektionslösung Pulver zur Herstellung einer Infusionslösung 2. QUALITATIVE UND QUANTITATIVE
Cefixim-ratiopharm 100 mg/5 ml Granulat zur Herstellung einer Suspension zum Einnehmen
 1. BEZEICHNUNG DES ARZNEIMITTELS zur Herstellung einer Suspension 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 5 ml der gebrauchsfertigen Suspension enthalten 111,9 mg Cefixim 3 H 2 O (entsprechend
1. BEZEICHNUNG DES ARZNEIMITTELS zur Herstellung einer Suspension 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 5 ml der gebrauchsfertigen Suspension enthalten 111,9 mg Cefixim 3 H 2 O (entsprechend
Cefuroxim 250 mg - 1 A Pharma Cefuroxim 500 mg - 1 A Pharma
 Stand: März 2013 1. BEZEICHNUNG DER ARZNEIMITTEL Wirkstoff: Cefuroxim 250 mg/ - 500 mg pro überzogene Tablette 2. QUALITATIVE UND QUANTITATIVE ZU- SAMMENSETZUNG 1 überzogene Tablette enthält 300,72 mg
Stand: März 2013 1. BEZEICHNUNG DER ARZNEIMITTEL Wirkstoff: Cefuroxim 250 mg/ - 500 mg pro überzogene Tablette 2. QUALITATIVE UND QUANTITATIVE ZU- SAMMENSETZUNG 1 überzogene Tablette enthält 300,72 mg
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS AFLUBIN- Grippetropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 ml enthalten: 1 ml Gentiana lutea D1, 10 ml Aconitum
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS AFLUBIN- Grippetropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 ml enthalten: 1 ml Gentiana lutea D1, 10 ml Aconitum
