Wege der Forschung nach einer Therapie der Duchenne-Muskeldystrophie. Teil 1 Exon Skipping
|
|
|
- Claudia Fürst
- vor 7 Jahren
- Abrufe
Transkript
1 Dr. Günter Scheuerbrandt Forschungsbericht, März 2013 Wege der Forschung nach einer Therapie der Duchenne-Muskeldystrophie. Teil 1 Exon Skipping Im Jahr 2000 fand in der amerikanischen Gesundheitsbehörde National Institutes of Health in Bethesda nahe Washington in den USA eine Tagung zur Erforschung von Therapiemethoden für Duchenne Muskeldystrophie statt. Dort wurde mir bewusst, dass es für Familien mit an Duchenne erkrankten Jungen, ihren Ärzten und anderen pflegenden Personen wichtig wäre zu wissen, welche Informationen Wissenschaftler und Klinikärzte während dieser Tagung über den aktuellen Stand ihrer Forschungsprojekte miteinander austauschten. Ich habe daraufhin meinen ersten Bericht geschrieben. Es sollten viele weitere Berichte folgen. Ich schrieb sie alle nicht in einer schwer verständlichen Fachsprache, ich erklärte vielmehr in einfachen Worten, was in den Laboratorien für Ihre Jungen geleistet wird. Die Erklärungen sollten auch für alle verständlich sein, die nicht moderne Biochemie oder Genetik studiert haben. Auf meinen Internetseiten können Sie die letzten dieser Berichte auf Englisch, Deutsch und Spanisch lesen. Zudem finden Sie dort einige Interviews, die seit 2008 veröffentlicht wurden. Ich beginne den ersten Teil meines Berichtes mit der Erklärung, wie Dystrophin in den Muskelzellen hergestellt wird und wie das Fehlen dieses wichtigen Proteins die Krankheit Duchenne-Muskeldystrophie verursacht. Da das Exon-Skipping momentan die am weitesten vorangekommene Technik für eine wirkungsvolle Therapie ist, wird es in diesem Teil des Berichtes ausführlich beschrieben. Für dieses Verfahren wurden schon viele klinische Studien an Duchenne-Patienten durchgeführt, andere Studien laufen noch oder sind geplant. Im zweiten Teil dieses Berichtes, der später im Jahr 2013 zu lesen sein wird, werde ich die wichtigsten Forschungsansätze außerhalb der Skipping-Methode beschreiben. Dazu gehören Gentransfer, das Verwenden von Stammzellen, die Utrophin-Hochregulierung, die Hemmung von Myostatin, die Verwendung von Steroiden und die diagnostischen Verfahren, um die Mutationen des Dystrophin-Gens unserer jungen Duchenne-Patienten zu finden. Beide Teile des Berichtes enthalten hauptsächlich Informationen über therapeutische Forschung. Ich weiß, dass mir viele von Ihnen nach dem Lesen des Berichtes s senden werden. Sie werden mich zu den Forschungsansätzen fragen, besonders aber zu dem Thema, welche Regionen mit genetischer Information Exons übersprungen, geskippt werden müssten, damit eine Behandlung Ihres kranken Kindes oder von Ihnen selbst möglich wird, wenn Sie ein erwachsener Patient sind. Am Ende dieses Berichtes werde ich in einem separaten Kapitel erklären, wie ich mit diesen Anfragen umgehen werde und wie ich die wenigen persönlichen Daten verwalten werde, die Sie mir schicken, damit wir in Kontakt bleiben können. In meinen Zusammenfassungen erwähne ich nur die Namen der Laborleiter, auch wenn diese Kollegen und Studenten haben, die als Team an den Projekten arbeiten, von denen hier berichtet wird. Es ist jedoch unmöglich, alle Namen aufzuführen. Ich habe die Namen der Wissenschaftler ohne ihre akademischen Titel aufgeführt. Die meisten von ihnen sind Professoren und alle haben einen Doktortitel in Medizin oder in Naturwissenschaften. Eine Liste der wichtigsten Veröffentlichungen finden Sie am Ende dieses Berichtes. Mit einer in Klammern gesetzten Nummer, z.b. (12) weise ich in meinen Zusammenfassungen an der Stelle im Text auf diese Artikel hin, zu der diese Ihnen mehr Einzelheiten zu dem betreffenden Thema geben können. Diese Veröffentlichungen sind für Sie als Laien sicher nicht einfach zu verstehen. Wenn Sie jedoch die eine oder andere Veröffentlichung gerne per erhalten möchten, lassen Sie es mich wissen. Bitte stören Sie sich nicht daran, wenn ich das so häufig verwendete Exon-Skipping nicht ändere und das dazugehörige Verb wie ein deutsches schreibe: skippen, skippte, geskippt. Das ist einfacher als immer überspringen schreiben zu müssen. Ich danke Frau Pat Furlong, Leiterin der amerikanischen Elterngesellschaft Muskeldystrophie Parent Project Muscular Dystrophy, PPMD, und Frau Professor Kate Busby, Koordinatorin von TREAT-NMD, dem europäischen Netzwerk für neuromuskuläre Erkrankungen für die Erlaubnis, ihre Logos verwenden zu dürfen. Dies zeigt, dass sie meine Arbeit, Ihnen die Forschungen nach einer Therapie Ihrer Kinder zu erklären, unterstützen und befürworten. Diesen Bericht habe ich zuerst auf Englisch geschrieben und im Januar 2013 veröffentlicht. Diese deutsche Übersetzung davon wurde von meinem Sohn Ralph Scheuerbrandt im Februar 2013 angefertigt. 1
2 Wie stellen Gene Proteine her? Gene sind Funktionseinheiten des genetischen Materials Desoxyribonukleinsäure, DNA. Seine Struktur sieht aus wie eine Wendeltreppe, die sogenannte Doppelhelix. Sie wurde von James Watson und Francis Crick 1953 beenthält zwei der vier schrieben. Jede Stufe dieser Treppe verschiedenen kleinen Moleküle, die Basen Adenin, Guawerden mit A, G, C und T nin, Cytosin und Thymin. Sie abgekürzt, wir nennen sie die genetischen Buchstaben. Auf den Stufen der Treppe sind nur zwei Basenkombinationen möglich, die Basenpaare A-T und G-C, die genau zwischen die beiden Stränge der Doppelhelix passen. Wenn zum Beispiel an einem Strang der DNA die Basenfolge, die Sequenz, GGCTTAATCGT ist, muss die Basenfolge am anderen Strang komplementär dazu sein. Die Base A steht immer gegenüber der Base T und G gegenüber von C. -GGCTTAATCGT- -CCGAATTAGCA- Die Folge dieser Basen, dieser genetischen Buchstaben, ist die genetische Information,, die notwendig ist für die Entwicklung und die Erhaltung von lebenden Organismen. Sie wird von einer Generation an die nächste weitergegeben. Die meisten Gene enthalten Anweisungen für die biologische Synthese von Proteinen. Im Zellkern werden die genetischen Anweisungen von aktiven Genen kopiert, in eine andere genetische Substanz umgeschrieben,, die unfertige oder Prä-Boten-Ribonukleinsäure premrna, die auch Transkript ge- nannt wird. Die meisten Gene haben aktiv codierende Bereiche, die Exons, die die Information n für die Produkenthalten. Zwischen den Exons liegen die oft sehr tion der Proteine viel längeren Introns, die wichtige Informationen für die Steuerung der Aktivität der Gene enthalten. Die Ribonukleinsäuren, RNAs, verwenden die Base U, Uracil, anstatt der ähnlichen Base T der DNA. Da die Struktur der RNA wichtig ist für das Exon-Skipping, wird sie auf Seite 6 im Absatz über die beiden Arten von Antisense- Oligos erklärt. Nach dem Kopiervorgang werden noch innerhalb des Zellkerns die Introns aus der pre-mrna entfernt und die Exons zusammengespleißt zur Boten-Ribonukleinsäure mrna. Englisch messenger RNA. Diese enthält dann nur Exons mit der genetischen Information für die Biosynthese eines Proteins. Auch in deutschen wissenschaftlichen Texten werden, wie auch hier, die englischen Abkürzungen DNA, RNA, pre-rna und mrna verwendet. Die mrna verlässt den Kern und wandert zu den Riden Protein aufbauenden Strukturen, die sich im Zellplasma außerhalb des Zellkerns befinden. Spleißstellen sind kurze Basensequenzen an den Grenzen von Exons bosomen, und Introns, die wichtig sind für die korrekte Entfernung der Introns aus der pre-mrna. Das Spleißen selbst geschieht in Spleißosomen,, einem Komplex aus vielen Proteinen und kleinen RNAs. Der genetische Code. Um die Sprache der Gene in die der Proteine übersetzen zu können, ist die genetische Ingenetische Worte gefasst. Jedes Wort besteht aus drei aufeinanderfolgenden Basen, den formation der mrna in Codons. Diese bedeuten mit drei Ausnahmen eine der 20 verschiedenen Aminosäuren, den Bauelementen des Proteins, nach dem genetischen Code. Es gibt 64 verschie- dene Code-Wörter, die aus je drei Buchstaben bestehen. Hier sind einige Beispiele: GUU = Valin, ACC = Serin, AUG = Methionin, ACG = Threonin, CAC = Histidin, CCA = Prolin, UUU = Phenylalanin, CGA = Alanin, GCG = Alanin. Die meisten Aminosäuren haben mehr als ein RNA-Code- Wort. Es gibt keine Abstände zwischen den Codewörtern. So bedeutet beispielsweise die kurze Basen- Sequenz AUG-AGC-GCA-CCA- am Anfang eines Genes, dass das Protein, das vom Gen hergestellt wird, mit den Aminosäuren Methionin, Serin, Alanin und Prolin beginnt. Es gibt also einen Leseraster, ein aus drei Buchstaben bestehendes Wort nach dem anderen ohne Abstand zwischen ihnen. Dieses Raster wird von dem ersten Code-Wort festgelegt, das immer AUG ist. Die Bindestriche in diesem Beispiel existieren nicht wirklich, sie verdeutlichen nur das Leseraster. Wenn im Beispiel oben der rote Buchstabe G zufällig entfernt wird durch eine Mutation, ändert sich die Sequenz in AUG-ACG-CAC-CA... Das Leseraster wird verschoben und die Code-Wörter ändern nach der Mutati- on ihre Bedeutung. Sie stehen dann für andere Aminosäuren, in diesem Fall für Methionin, Threonin, Histidin. Diesen folgen dann weitere falsche Aminosäuren. Solche Leseraster-Verschiebungen sind für das Verständnis des Exon-Skippings sehr wichtig. In den Ribosomen werden die genetischen Code-Wörter der mrna gelesen und in die Sprache der Proteine übersetzt. Diese setzen sich aus vielen tausenden Aminosäuren zusammen. Die drei Ausnahmen, die zuvor erwähnt wurden, sind die Worte UAA, UAG und UGA. Diese sind Stopp-Codons, Stoppzeichen, an denen der Zusammenbau des Proteins in den Ribosomen beendet wird. Dystrophin-Gen und -Protein. Duchenne Muskeldystrifft nur Jungen. Die Häufigkeit beträgt trophie etwa 2
3 1:3500 aller neugeborenen Jungen. Frauen haben, wenn sie Überträgerinnen dieser geschlechtsgebundenen Krankheit sind, eine Mutation, einen Fehler, im Dystrophin-Gen auf einem ihrer beiden X- Chromosomen. Sie übertragen diesen Fehler im Durchschnitt auf jeden zweiten ihrer Söhne, die dann nur dieses eine X-Chromosom mit der Mutation haben. Da sie kein intaktes Dystrophin-Gen auf einem zweiten Chromosom haben wie die Frauen, verursacht diese Mutation die immer noch unheilbare Erbkrankheit Duchenne-Muskeldystrophie. Manchmal taucht eine derartige Mutation ganz neu in einer Familie auf. Das Dystrophin-Gen ist das zweitgrößte unserer Gene. Das Gen für das Muskelprotein Titin, das wichtig ist für die Elastizität der Muskelzellen, ist ungefähr 100mal größer als das Dystrophin-Gen. Das nächste Bild zeigt den Ort des Gens auf dem kurzen Arm des X-Chromosoms. Seine DNA besteht aus genetischen Buchstaben, deren aktive Sequenzen in 79 Exons zusammengefasst sind. Es sind auch 7 Promoter zu sehen. Das sind Sequenzen, die für den Beginn der Produktion des normalen Proteins sowie seiner 6 Varianten notwendig sind. Nach dem Spleißen enthält die mrna nur noch genetische Buchstaben, das sind 0,5% der Buchstaben des gesamten Gens. In den Ribosomen wird das Dystrophin-Protein nach der genetischen Information in der mrna aus Aminosäuren zusammengesetzt. Diese Bausteine werden von einer anderen Art von RNA, der Transfer-RNA oder trna an den Ort der Biosynthese im Innern der Ribosomen gebracht. Moleküle in den Zellmembranen wurden durch leuchtende, fluoreszierende Antikörper sichtbar gemacht. Größe des Dystrophin-Gens und seines Proteins. Die Doppelhelix-Struktur des Dystrophin-Gens ist 0,75 mm lang. Zusammen mit den etwa anderen menschlichen Genen passt es in einen Zellkern, der einen Durchmesser von etwa 0,01 mm hat. Das ist möglich, weil das genetische Material darin extrem dicht gepackt ist. Ein Molekül des normalen Dystrophin-Proteins ist viel kürzer als sein Gen, es ist 125 nm, Nanometer, lang. Das sind 0, mm dieser Moleküle würden, wenn sie in einer geraden Linie aneinandergereiht wären, gerade einmal 1 mm lang sein. In einem Gramm Muskel gibt es 114 Milliarden Dystrophin-Moleküle. Die Rolle des Dystrophins. Dystrophin wird für die mechanische Stabilität der Muskelzellen benötigt. Es befindet sich auf der Innenseite der Muskelzellmembranen. Sein C-terminales Ende ist mit einer Gruppe anderer Proteine in der Membran verbunden, dem Dystrophin-Glykoprotein- Komplex. Das andere Ende, das N-terminale, hat Verbindung zu den zusammenziehbaren, kontraktilen, Strukturen innerhalb der Muskelzellen. Die zentrale Struktur des Dystrophins besteht aus ineinander verdrehten Aminosäure- Ketten, die mehrfach auf sich selbst zurückgeklappt sind. Wenn das Zusammenziehen, die Kontraktion, der Muskelzelle das Dystrophin-Protein zwingt, seine Länge zu ändern, funktioniert seine gefaltete Struktur wie eine Feder oder wie ein Stoßdämpfer. Das Dystrophin übermittelt also die mechanische Energie, die im Actin-Myosin-Kontraktionsgefüge entsteht, an die Muskelzellmembranen und die Strukturen außerhalb der Zellen, dem Bindegewebe und den Sehnen. Dies geschieht in einer ausgeglichenen Art und Weise, die alle beteiligten Strukturen nicht überstrapaziert. Die nicht aktiven Sequenzen zwischen den Exons, die 99,5% des gesamten Gens ausmachen, sind die Introns. Es ist jetzt bekannt, dass einige dieser Sequenzen wichtig sind für die Regulierung der genetischen Aktivitäten. Sie könnten auch noch andere, bisher unbekannte Funktionen haben, die zu den manchmal unterschiedlichen Symptomen von Duchenne-Patienten führen, obwohl diese die gleichen Mutationen in den Exons haben. Das Dystrophin-Protein ist ein langgestrecktes Molekül mit 24 sich wiederholenden Aminosäure-Sequenzen, die von 4 Gelenkregionen getrennt sind. Seine beiden Endregionen werden N- und C-Terminals genannt. Es gibt auch eine Region mit vielen Cysteinen, das sind Aminosäuren die Schwefel enthalten. Im Bild wird auch ein Schnitt durch gesundes Muskelgewebe gezeigt. Die Dystrophin- Der Dystrophin-Glykoprotein-Komplex. Dystrophin hat mehrere Aufgaben: Es reguliert die komplizierte Struktur des Dystrophin-Glykoprotein-Komplexes und die Position vieler anderer Proteine. Es reguliert aber auch biologische Prozesse wie z.b. die Steuerung des Muskelwachstums und den richtigen Kalziumgehalt in den Zellen. Viele Einzelheiten dieser verschlungenen gegenseitigen Abhängigkeiten zwischen den zahlreichen Komponenten in einer lebenden Zelle sind noch nicht bekannt. 3
4 Duchenne-Jungen haben entweder gar kein oder nur sehr wenig Dystrophin in ihren Muskelzellen. Wenn die Schutz- und Regulationseffekte von Dystrophin fehlen, verursacht das Zusammenziehen der Muskeln Risse und Löcher in den Muskelmembranen. Dadurch kann relativ viel Kalzium in die Fasern fließen. Überschüssiges Kalzium aktiviert Enzyme wie zum Beispiel Kalpain oder die Proteasen. Diese Enzyme spalten Muskelproteine auf und verursachen Zelltod-Programme, Apoptosen. Dann kommt es zu einer Reihe von Reaktionen wie Entzündungen und einer Aktivierung von Fibroblasten. Diese führen zur Fibrosen oder Narbengewebe, das die Regeneration der Muskeln verlangsamt und typische Symptome bei älteren Duchenne-Patienten hervorruft. Jungen mit der langsamer verlaufenden Becker-Muskeldystrophie haben weniger Dystrophin-Protein in ihren Muskelzellmembranen, das oft auch in verkürzter Form vorliegt. Es kann seine Funktion zwar noch erfüllen, funktioniert meist jedoch weniger wirksam als das normale Dystrophin. Es leiden jedoch nicht nur die Skelettmuskeln, wenn Dystrophin fehlt, sondern auch die glatten Muskeln und die Herzmuskeln. Schäden an den Herzmuskeln führen zu Kardiomyopathien, Herzmuskelerkrankungen. Die Schwächung der glatten Muskulatur hat viele Folgen: Blutgefäße können schlechter entspannen, wenn sich der Blutdurchfluss erhöht. Dies wiederum führt zu Atemschwierigkeiten und anderen Problemen. Der Magen- Darmtrakt wird in Mitleidenschaft gezogen, wenn die Bewegungen der Därme eingeschränkt werden. Ein einziges beschädigtes Gen kann also große Teile des Körpers in Mitleidenschaft ziehen. Auf Seite 12 habe ich ein Kapitel unter der Überschrift Muskelreparatur, eine allgemeine Einführung eingefügt. Sie wurde von Annemieke Aartsma-Rus geschrieben mit vielen Einzelheiten über die Entwicklung und den Verlauf der Duchenne-Muskeldystrophie. Hier wird auch empfohlen, das Exon-Skipping, das ich als nächstes beschreiben werde, sobald wie möglich nach der Geburt zu beginnen, wenn die meisten Muskeln der Duchenne-Jungen noch vorhanden sind. Exon Skipping Die Aufgabe der Forschung. Ein gesunder 5jähriger Junge, der 30 kg wiegt, hat ungefähr 12 kg Muskeln. Diese enthalten 1,5 Billiarden (1,5 x ) Dystrophin-Moleküle. Ein 5jähriger Duchenne-Junge hat schon 30% seiner Muskeln verloren und hat demnach nur noch 8 kg Muskelmasse. Diese verbleibenden Muskeln haben nur noch Spuren oder gar kein Dystrophin mehr. Die Information des geschädigten Gens kann nicht korrekt gelesen werden für die Biosynthese des Proteins. Die geringe Zahl der Muskelzellen, die Spuren von Dystrophin enthalten, weniger als 3%, werden revertierte Fasern genannt. Ihr Dystrophin ist durch spontanes Exon-Skipping entstanden. Es ist nicht bekannt, wie viel Dystrophin notwendig ist, um das Fortschreiten der Krankheit zu verhindern, es ist jedoch besser als nichts (1). Das neue Dystrophin, das durch Exon-Skipping entsteht, muss nicht genauso lang sein wie das normale Dystrophin, es kann kürzer sein, aber es muss richtig arbeiten können. Exon-Skipping, eine Gentherapie für Duchenne. Während einer Diskussion Mitte der 1990-Jahre erklärte mir Gertjan van Ommen von der Universität Leiden in den Niederlanden, wie eine Gentherapie diese Aufgabe lange Zeit ohne ernste Nebenwirkungen erfüllen könnte. Diese Therapie wird jetzt Exon-Skipping genannt. Sie wurde in den letzten 15 Jahren von vielen Forschungsgruppen, vor allem in den Niederlanden, in Frankreich, Japan, Australien, dem Vereinigten Königreich und den Vereinigten Staaten von Amerika weiter entwickelt und zwar so intensiv, dass dieses Verfahren nicht nur an Tieren in Labors, sondern auch in klinischen Studien an Duchenne-Patienten getestet wird. Exon-Skipping bedeutet das Springen von einem Exon zum nächsten. Exons sind die aktiven Abschnitte der Basen-Sequenzen eines Gens. Im Dystrophin-Gen von Duchenne-Jungen ist es zu Mutationen gekommen, so dass ein oder mehrere Exons fehlen, das Gen hat dann Deletionen. Es gibt auch Verdopplungen, Duplikationen, oder Fehler in der Buchstabenfolge eines Wortes, Punkt-Mutationen. Solche Mutationen haben das Leseraster bei den kranken Jungen um einen oder zwei Buchstaben verschoben, so daß ein normales Raster, in-frame, zu einem nicht normalen Raster wird, out-of-frame. Kurz nach der Mutation entsteht dann ein vorzeitiges Stopp-Codon. Der Leseprozess der genetischen Information für die Biosynthese des Proteins ist unterbrochen an solch einem Stoppzeichen. Es kann kein Dystrophin mehr produziert werden. Diese Fehler können korrigiert werden, d.h. die Protein-Produktion kann wieder gestartet werden, wenn ein oder mehrere der noch vorhandenen Nachbar-Exons in der pre-mrna so blockiert werden, dass der Mechanismus, der die Exons verbindet, spleißt, sie überspringt, sie skippt, und sie nicht mehr in die mrna aufnimmt (2). Für diese Blockade sind Antisense-Oligonukleotide, notwendig, abgekürzt Antisense Oligos, oder in diesem Bericht oft nur Oligos genannt. Sie sind kurze Stücke von genetischem RNA-Material, die eine besondere Sequenz von nur genetischen Buchstaben haben. Sie können sich innerhalb der zu skippenden Exons durch die Watson- Crick-Basenpaarung an komplementäre, genau passende Sequenzen anlagern und so deren Spleißen mit den anderen Exons verhindern. Wo geschieht das Exon-Skipping? Wie zuvor beschrieben, werden die 2,2 Millionen genetischen Buchstaben des Dystrophin-Gens im Muskelzellkern kopiert und in die pre-mrna umgeschrieben. Die meistens sehr langen Intron-Sequenzen werden dann herausgeschnitten und nur die 79 Exon-Sequenzen diese sind nur insgesamt Buchstaben lang werden zu der sehr viel kürzeren mrna gespleißt, zusammengesetzt. Das Exon-Skipping passiert während dieses Spleißens. Die verkürzte Boten- Ribonukleinsäure, mrna, ohne die durch Mutation entfernten und die geskippten, übersprungenen, Exons ver- 4
5 lässt den Kern und wandert zu den Ribosomen im Zellplasma. Dort wird die genetische Information der mrna gelesen und in die Sprache der Proteine übersetzt, in die Aminosäure-Frequenz des Dystrophins, das dort produziert wird. Duchenne- wird in Becker-Dystrophie umgewandelt. Wegen der fehlenden Exons der durch die Mutation entfernten und der zusätzlich geskippten werden auch die Aminosäuren, die durch die fehlenden Exons bestimmt werden, in dem neu hergestellten Dystrophin fehlen. Das neue Dystrophin hat also eine Aminosäuren-Kette, die weniger als die normale Zahl, 3.685, an Aminosäuren enthält. Oft jedoch ist es noch fähig, die Muskelzellmembranen bis zu einem gewissen Ausmaß vor den mechanischen Belastungen einer Muskelkontraktion zu schützen. Die Symptome der Krankheit werden dadurch weniger ausgeprägt, der Abbau der Muskeln erfolgt langsamer und die Lebenserwartung der Patienten steigt deutlich. Sie erreicht in manchen Fällen sogar die normale Lebenserwartung. Die Duchenne-Dystrophie wäre dann in eine Becker- Muskeldystrophie, die mildere Variante der Krankheit, umgewandelt worden. Eine Therapie, jedoch noch keine Heilung. Das Ziel des Exon-Skippings ist es also, die Krankheit in eine mildere Variante umzuwandeln und dadurch das Fortschreiten der Krankheit zu verlangsamen. Exon-Skipping ist also nur eine Therapie, keine Heilung. Mit dieser Gentechnologie wird das geschädigte Gen selbst nicht verändert, es wird weder ersetzt noch repariert, es wird lediglich der Mechanismus seines Informationsflusses korrigiert. Molekulare Einzelheiten des Skippens von Exon 51. Bei den klinischen Versuchen mit Patienten wird zunächst Exon 51 geskippt. Hier erkläre ich die molekularen Einzelheiten dieses Skippings bei einem Patienten mit der Deletion von Exon 50. Das Ziel dieses Skippens ist es, das Leseraster in der mrna wiederherzustellen, das durch die Deletion von Exon 50 im Gen verschoben worden war. Zunächst zeige die Basensequenzen vom Anfang und Ende der Exons 50 und 51 der normalen mrna des Gens und auch vom Ende von Exon 49 und dem Anfang von Exon 52. Im Exon 50 sind 29 Codons nicht aufgeführt und auch nicht 52 Codons im Exon 51. Unter jedem Codon steht der abgekürzte Name der Aminosäure im Dystrophin-Protein, die von dem Codon determiniert wird. Die Aminosäuren werden in den Ribosomen aneinandergereiht. Sie sind nicht, wie hier gezeigt, mit den Codons verbunden. Die Codons folgen aufeinander ohne Zwischenräume, die Bindestriche zeigen nur das Leseraster an und die senkrechten Striche die Grenzen der Exons. Die drei Basen des versteckten Stoppsignals UGA sind rot markiert. Exon 50 hört nach der ersten Base des letzten Codons auf, das dann zu UCU mit den ersten beiden Basen von Exon 51 komplettiert wird (blau markiert). Ende Exon 49 Start Exon 50 Ende Exon 50 Start Exon CAG-CCA-GUG-AAG AGG-AAG-UUA-GAA---AUU-GGA-GCC-U CU-CCU-ACU-CAG-ACUgln pro val lys arg lys leu glu ile gly ala ser pro thr gln thr verstecktes Stoppcodon ---GUU-ACU-CUG-GUG-ACA-CAA---AAA-CUA-GAA-AUG-CCA-UCU-UCC-UUG-AUG-UUG-GAG--- val thr leu val thr gln lys leu glu met pro ser ser leu met leu glu Ende Exon 51 Start Exon AUG-AUC-AUC-AAG-CAG-AAG GCA-ACA-AUG-CAG-GAU-UUG--- met ile ile lys gln lys ala thr met gln asp leu Wenn Exon 50 im Gen und also auch in der mrna deletiert ist, folgt auf Exon 49 direkt das Exon 51. Dies verschiebt das Leseraster im Exon 51 um eine Base nach rechts mit der Konsequenz, dass in den Ribosomen acht falsche Aminosäuren in die wachsende Dystrophinkette eingebaut werden, bis schließlich das zuvor versteckte, aber jetzt aktivierte, vorzeitige Stoppsignal UGA erreicht wird. Die verschobenen Basensequenzen und die falschen Aminosäuren sind rot markiert. Die Biosynthese des Proteins Dystrophin wird vorzeitig abgebrochen, es bleibt unfertig und wird zerstört. Dadurch entwickelt sich Duchenne- Muskeldystrophie. Ende Exon 49 Start Exon CAG-CCA-GUG-AAG CUC-CUA-CUC-AGA-CUG-UUAgln pro val lys leu leu leu arg leu leu aktives Stoppcodon Antisense-Oligoribonukleotid UC-UUU-ACG-GUA-GAA-GGA-ACU -CUC-UGG-UGA-CAC AAG---AAC-UAG-AAA-UGC-CAU-CUU-CCU-UGA-UGU-UGG-- leu trp STOPP! Ende Exon 51 Start Exon AU-GAU-CAU-CAA-GCA-GAA-G GC-AAC-AAU-GCA-GGA-UUU--- 5
6 Das von den holländischen Forschern verwendete exonskippende Antisense-Oligoribonukleotid PRO051, hier blau markiert, bindet sich durch Watson-Crick-Paarung an 20 Basen im Exon 51. Es blockiert dort die ESE-Sequenz, die zum Spleißen notwendig ist, und verursacht das Skippen von Exon 51 in der mrna des mutierten Gens, die in diesem Beispiel die Sequenz des Exons 50 nicht enthält. Wenn zusätzlich zum deletierten Exon 50 das Exon 51 durch Skippen entfernt wurde, dann folgt auf Exon 49 direkt Exon 52. Das Leseraster ist nicht mehr gestört, weil Exon 49 mit einem vollständigen Codon aufhört und Exon 52 mit einem vollständigen Codon von drei Basen anfängt. Ende Exon 49 Start Exon CAG-CCA-GUG-AAG GCA-ACA-AUG-CAG-GAU-UUG--- gln pro val lys ala thr met gln asp leu Jetzt gibt es kein vorzeitiges Stoppsignal mehr im Exon 52 oder später, aber 77 Aminosäuren fehlen von den des normalen Proteins, diejenigen, deren Information in den Sequenzen der Exons 50 und 51 enthalten war. Sie fehlen im mittleren Teil des verkürzten Dystrophins, dessen Funktion aber wahrscheinlich wenig beeinträchtigt ist, so daß die schweren Symptome der Duchenne- in die weniger schweren der Becker-Muskeldystrophie abgeschwächt werden. Antisense Oligoribonukleotide, die potentiellen Exon-Skipping-Medikamente. Verschiedene Typen von Antisense-Oligos. Für die Tierversuche und die ersten klinischen Exon-Skipping Studien, die von den Firmen Prosensa und Sarepta ausgeführt wurden, wurden zwei Arten von Antisense-Oligos verwendet. Sie haben die Basis-Struktur von Ribonukleinsäuren, RNAs, die neben der DNA die zweitwichtigste natürliche Nukleinsäure ist. Die RNA besteht aus einer langen Kette von sich abwechselnden Einheiten der zuckerartigen Substanz Ribose und einer Phosphorsäure. Jede Ribose-Einheit trägt eine der 4 genetischen Buchstaben: Adenin (A), Guanin (G), Cytosin (C) und, in diesem Fall, Uracil (U), welches ähnlich dem Buchstaben T (Thymin) der DNA ist. Die Reihenfolge dieser Buchstaben ist wichtig für die Funktion von vielen langen und kurzen RNAs, da sie sich selbst an die komplementären Sequenzen von DNAs und anderen RNAs durch die Watson-Crick-Basenpaarung anlagern können. G steht dann gegenüber von C und A gegenüber von U (oder T in der DNA). Dies funktioniert wie ein effizienter Reißverschluss mit 4 verschiedenen Zähnen. Die potentiellen Medikamente zum Exon-Skipping, die Antisense-Oligos, sind kurze RNA-Stücke mit nur ca genetischen Buchstaben. Diese kurzen Sequenzen genügen, um sicherzustellen, dass sie sich nur an diejenigen RNA- oder DNA-Sequenzen anlagern, die blockiert werden sollen. Das passiert, obwohl unsere gesamte DNA in all unseren 46 Chromosomen in jeder Zelle Sequenzen von mehr als 3 Milliarden Buchstaben aufweist, von denen ungefähr 1%, also nur 30 Millionen zu unseren Genen gehören und daher in RNA kopiert wird, wenn es nötig ist. Dies ist sehr wichtig, weil ein Antisense-Oligo gegen Duchenne nur die genetische Information des Dystrophin- Gens auf dem X-Chromosom von kranken Jungen beeinflussen darf und keine anderen Gene. Jegliche Art von falschen Verbindungen zu anderen Genstrukturen könnte schwere Nebenwirkungen zur Folge haben, wenn ein zukünftiges Exon-Skipping-Medikament einem Duchenne- Jungen gegeben wird während der hoffentlich vielen Jahre seines verlängerten Lebens. Die Antisense Oligos müssen nach der Injektion so lange wie möglich im Blutkreislauf überleben. Sie müssen Zeit haben, von den Blutgefäßen in die Zellen aller Muskeln zu gelangen. Dort müssen sie die vielen Kerne in jeder Zelle eindringen und ihre Aufgabe erfüllen: Ein oder mehrere Exons der mutierten pre-mrna während des Spleißens blockieren, um so eine verkürzte, mrna zu erzeugen. Wenn die ankommenden Oligos die normale RNA-Struktur hätten, würden sie von Enzymen als fremde Nukleinsäuren erkannt und zerstört werden. Aus diesem Grund müssen die Oligos chemisch geschützt werden, so dass diese Enzyme sie nur sehr langsam oder gar nicht zerstören. Die niederländischen Wissenschaftler verwenden 2 O- Methyl-Phosphorothioate, in diesem Bericht auch 2 O- Methyle genannt. Sie haben eine Methylgruppe, die aus einem Kohlenstoff- mit drei Wasserstoff-Atomen besteht, an dem Sauerstoffatom des zweiten Kohlenstoffatoms der Ribose-Einheiten, sowie ein Schwefelatom anstatt eines der Sauerstoffatome an den Phosphatbrücken. Die Morpholinos, die von der Firma Sarepta verwendet werden, haben eines der Phosphat-Sauerstoffatome durch eine Dimethylamid-Gruppe ersetzt. Dies ist ein Stickstoff-Atom mit zwei Methylgruppen. Und alle Ribose-Einheiten sind durch Morpholinoringe ersetzt. Dies sind sechsgliedrige Ringe, die aus 4 Kohlstoffatomen, 1 Sauerstoffatom und 1 Stickstoffatom bestehen. Ich zeige Ihnen auf der nächsten Seite die chemische Struktur dieser zwei Arten von geschützten Antisense- Oligos mit nur zwei ihrer genetischen Buchstaben, die als Base gekennzeichnet sind. Die Kohlenstoffatome werden nicht gezeigt, sie sitzen an den Ecken und den Enden der Linien dieser vereinfacht dargestellten Strukturen. Jedes Kohlenstoffatom hat ein oder mehrere Wasserstoffatome, die auch nicht gezeigt werden. Eine dritte Art von Antisense-Oligos wird Vivo-Morpholino genannt. Es wird in einem Absatz über das Multiexon-Skipping auf Seite 21 beschrieben. Um das Exon 51 in den zahlreichen klinischen Studien mit Patienten zu skippen, wird das 2 O-Methyl Antisense- Oligo verwendet. Diese Studien werden von den Firmen Prosensa und GlaxoSmithKline, GSK, durchgeführt. Dieses Oligo PRO051, das jetzt Drisapersen genannt wird, hat 20 genetische Buchstaben mit folgender Sequenz: 6
7 UCUUUACGGUAGAAGGAACU Das Morpholino-Antisense-Oligo, das von der Firma Sarepta, die früher AVI hieß, in den Studien eingesetzt wurde, hieß zunächst AVI-4658 und heißt jetzt Eteplirsen. Es hat 30 Buchstaben, die 20 Buchstaben des niederländischen Oligos sind darin enthalten und hier unterstrichen: GAUCUUUACGGUAGAAGGAACUACAACCUC 2 O-Methyl-Antisense-Oligo Morpholino-Antisense-Oligo Die Moleküle dieser Antisense-Oligos mit ihren 20 oder 30 genetischen Buchstaben haben recht komplizierte chemische Strukturen. Drisapersen besteht aus 699 Atomen und Eteplirsen aus mehr als Dies zeigt, dass diese möglichen Medikamente für unsere Duchenne-Jungen sich von kleineren Arzneimittel-Molekülen stark unterscheiden. Sie können mit jeder gewünschten Sequenz ihrer Buchstaben von automatischen Maschinen in denjenigen Labors hergestellt werden, die vorklinische Versuche an Gewebekulturen und Tieren durchführen. Wenn bei diesen Versuchen ein vielversprechendes Oligo gefunden wurde, werden klinische Studien an Duchenne-Jungen geplant und durchgeführt. Die Oligos dafür müssen als klinische Reagenzien unter strengen Regeln und Vorschriften von spezialisierten Firmen hergestellt werden. Verschiedene Eigenschaften der Antisense-Oligos. Die Moleküle der Antisense-Oligos sind nicht so groß wie Proteine und Nukleinsäuren. Deswegen werden sie vom Körper durch die Nieren schnell ausgeschieden. Die 2 O-Methyle sind elektrisch geladen und verbinden sich mit verschiedenen Proteinen im Blut. Sie werden daher nicht so schnell mit dem Urin ausgeschieden wie die Morpholinos, die elektrisch neutral sind. Wie bei Versuchen mit Mäusen gezeigt wurde, beträgt die Halbwertzeit im Serum, d.h. die Zeit, bis die Hälfte der Oligos aus dem Serum entfernt wird, bei 2 O-Methylen ca. 4-5 Wochen und bei Morpholinos nur etwa 2-3 Stunden. Daher haben die 2 O-Methyle viel mehr Zeit als die Morpholinos, um in die Muskelzellen aufgenommen zu werden, wo sie dann ihre therapeutische Wirkung entfalten können. Die Situation beim Menschen ist wahrscheinlich ähnlich, da bei diesen zwei verschiedenen Typen von Antisense Oligos und das werde ich später erklären bei ersten klinischen Studien an Patienten zur Erzielung von ähnlichen Ergebnissen viel höhere Dosen und längere Behandlungszeiten für Morpholinos nötig waren als bei den 2 O-Methylen. Da eine Exon-Skipping-Behandlung wahrscheinlich während des ganzen Lebens der Jungen notwendig sein wird, sind Injektionen unter die Haut praktischer als intravenöse Injektionen in den Blutkreislauf. Solche subkutane Injektionen können zu Hause von Laien oder dem Patienten selbst durchgeführt werden. Injektionen in die Vene setzen häufige Besuche in einer Arztpraxis voraus. Aus diesem Grunde werden die in Wasser löslichen 2 O-Methyle während der klinischen Studien bereits subkutan angewendet. Morpholinos können in hohen Dosen jedoch nicht in Wasser aufgelöst werden und erfordern daher Injektionen oder Infusionen in ein Blutgefäß. Wie zuvor erklärt, haben die Muskelzellen von Duchenne-Jungen kein oder nur sehr wenig Dystrophin unter den Zellmembranen. Die vielen verschiedenen Proteine, die mit Dystrophin in Verbindung stehen, fehlen ebenso. Die Membranen haben also keinen Stoßdämpfer mehr, der normale Membranen vor der mechanischen Belastung muskulärer Kontraktionen schützt. Mit der Zeit lösen sich diese Membranen auf oder bekommen Risse und Löcher. Durch sie gelangen Teile des Zellinhalts in den Blutkreislauf wie zum Beispiel das Enzym Creatinkinase, CK. Die Konzentration dieses Enzyms steigt dramatisch an und gibt einen ersten Hinweis darauf, dass ein Junge Muskeldystrophie haben kann. Andererseits können Substanzen von außen die beschädigten Zellmembranen einfacher und schneller passieren als gesunde Muskelzellmembranen. Für Techniken wie das Exon-Skipping, die darauf angewiesen sind, dass ihre aktiven Substanzen so schnell und so wirksam wie möglich in die Muskelzellen gelangen, ist diese defekten Zellmembranen also ein Vorteil. Es wurde sogar schon gesagt, dass die Duchenne-Muskeldystrophie die Zellmembranen öffnet, um die Arzneimittel einzulassen, weil sie gerne geheilt werden möchte. Wie wird die therapeutische Wirkung eines möglichen Duchenne Arzneimittels gemessen? In den klinischen Studien mit dem Exon-Skipping muss bewiesen werden, dass die Antisense-Oligos tatsächlich den Abbau der dystrophen Muskeln bei Duchenne-Jungen über viele Jahre hinweg verlangsamen. Eine Möglichkeit dies zu tun ist der Sechs-Minuten-Gehtest, 6MWT englische Abkürzung. Dies ist eine sogenannte outcome measure, eine Ergebnis-Messung, die von der US-amerikanischen Gesundheitsbehörde FDA und der Europäischen Arzneimittelbehörde EMA akzeptiert wird, um die Wirkung einer Behandlung auf die Muskelfunktion zu messen. Duchenne- Jungen, die noch unabhängig gehen können, sollen 6 Minuten lang so schnell sie können gehen, nicht laufen, z.b. hin und zurück im Flur eines Krankenhauses. Die durchschnittliche Entfernung, die an verschiedenen Tagen vor der ersten Injektion zurückgelegt wurde, ist der durchschnittliche 6MWT-Ausgangswert. Ein 10 Jahre alter Junge kann in 6 Minuten etwa 300 bis 400 Meter gehen. Während der Studie z.b. alle 6 Wochen wird dieser 7
8 Test wiederholt. Normalerweise nimmt die zurückgelegte Strecke ab, weil der Muskelabbau voranschreitet. Die Abnahme in Metern zu verschiedenen Zeiten wird in einem Diagramm festgehalten, das damit das Schlechterwerden der Muskelfunktionen und das Fortschreiten der Krankheit dokumentiert. Um die kombinierten Ergebnisse größerer Patientengruppen zu zeigen, wird der durchschnittliche 6MWT-Ausgangswert für alle Patienten dieser Gruppe auf null gesetzt. Dort starten die Kurven, die durch verschiedene Dosen und die Ergebnisse der Placebo-Gruppe zustande kommen. Die Punkte in den Kurven stehen für die durchschnittlichen Veränderungen aller Jungen einer Gruppe in Metern zu verschiedenen Zeiten. Diese Veränderungen sind wegen der geringeren Gehstrecken in 6 Minuten, meist negativ. Der Zweck dieser graphischen Darstellung ist es zu zeigen, ob die Behandlung in der klinischen Studie den gewünschten Effekt hat oder nicht. Um dies jedoch zuverlässig und objektiv und ohne menschliche Einflüsse zu bewerkstelligen, muss die Studie doppelblind durchgeführt werden. Ein Drittel, manchmal auch die Hälfte der Patienten in einer Studie erhalten nicht das aktive Arzneimittel, sondern ein Placebo. Das ist Material wie z.b. Milchzucker, das wie das Arzneimittel aussieht, aber keine medizinische Wirkung hat. Die Entscheidung, ob ein Patient das Arzneimittel oder das Placebo erhält wird per Zufall gefällt, denn er wird zufällig einer der Teilnehmergruppen in der Studie zugeteilt. Weder die Eltern noch die Patienten noch das Klinik- oder Laborpersonal wissen, zu welcher Gruppe der Patient gehört bevor die Studie abgeschlossen und analysiert wird. Solch eine graphische Darstellung, die auch Daten einer Placebo-Gruppe enthält, gibt es noch nicht für die klinischen Studien, mit denen das Exon-Skipping geprüft wird. Wir werden noch auf das Ende der langen Phase III-Studie zum Skippen des Exons 51 und die Auswertung aller Daten warten müssen. Vor Ende 2013 werden wir sie wohl nicht sehen. Eine solche Darstellung mit Placebo-Daten existiert jedoch für die Phase- IIb-Studie mit Ataluren, das auch als PTC124 bekannt war. Diese Studie wurde im März 2010 unterbrochen, da das vorher bestimmte primäre Messergebnis nicht erreicht wurde. Die Ergebnisse des 6-Minuten-Gehtests bei 174 Patienten über 48 Wochen hinweg wurden im April 2010 (3) veröffentlicht. Es gab 2 Patientengruppen mit verschiedenen Dosen und eine Placebo- Gruppe. Ich zeige Ihnen hier die Ergebnisse als Beispiel, wie die Daten einer klinischen Studie präsentiert werden. Die Linie in der Mitte wurde mit den Jungen in der Placebo-Gruppe erhalten. Die obere Linie zeigt die Ergebnisse der Jungen, die die niedrigere Dosis erhielten, 40 mg Ataluren/kg/Woche. Die untere Linie zeigt die Ergebnisse der Jungen, die die höhere Dosis erhielten, 80 mg Ataluren/kg/ Woche. Sie können sehen, dass die Linien der Placebound der Hochdosis-Gruppe sehr ähnlich sind. Die Linie der Niedrigdosis-Gruppe zeigt jedoch, dass die Distanz, die in 6 Minuten zurückgelegt wurde, nicht so schnell abnahm wie bei den anderen beiden Gruppen. Es sieht also so aus, als ob die niedrige Dosis die Krankheit in einem Jahr wirksam verlangsamt hat im Vergleich zu den Jungen, die keine Behandlung erfuhren. Eine hohe Dosis hat den Verlauf der Krankheit nicht beeinflusst. Ich werde im zweiten Teil meines Berichtes auf dieses unerwartete und noch nicht zu erklärende Ergebnis und seine Folgen zurückkommen. Sobald die Ergebnisse der Phase III der Exon-51-Studie analysiert und in ähnlicher Weise veröffentlicht sind, werde ich sie in die aktualisierte Fassung dieses Berichtes aufnehmen, wenn ich diese Forschungsberichte weiterhin schreiben kann. Die Mutationen des Dystrophin-Gens. Nach der Veröffentlichung von Annemieke Aartsma-Rus und ihren Kollegen im Jahr 2006 (4) machen die Deletionen, das Fehlen eines oder mehrerer Exons bis zu 72% aller Mutationen aus. Verdoppelungen eines oder mehrerer Exons werden in 7% aller Patienten gefunden, 20% der Patienten haben Punktmutationen. Das sind kleine Deletionen oder Einschübe oder Änderungen von einem oder einiger weniger genetischer Buchstaben. Das verbleibende 1% setzt sich aus mehreren seltenen Mutationen zusammen wie z.b. 8
9 diejenigen die Spleißstellen stören oder große Teile der Genstruktur neu ordnen. Die Leseraster-Regel. Die Autoren kommen zu dem Schluss, dass für 91% aller Patienten diese Regel gilt. Das bedeutet, dass out-of-frame-mutationen Duchenne verursachen, hier bleibt das Raster nicht erhalten, und inframe-mutationen Becker Muskeldystrophie. Sie sagen weiterhin, dass bei den meisten Patienten, deren Mutationen Ausnahmen zu dieser Leseraster-Regel sind, die Struktur ihrer mrna dieser Regel jedoch folgt. In den meisten Fällen wird die mrna-sequenz aber nicht bestimmt, wenn eine Genanalyse durchgeführt wird. Bevor eine Exon-Skipping-Behandlung begonnen wird, ist es anzuraten, in einem Gewebe-Kultur-Versuch zu bestätigen, dass diese Behandlung zu einer in-frame-mrna führen würde. Anwendbarkeit des Exon-Skippings. Obwohl Duchenne Patienten mehr oder weniger ähnliche klinische Symptome haben, gibt es viele verschiedene Ursachen für ihre Krankheit. Das liegt daran, dass Mutationen auf dem sehr langen Dystrophin-Gen an vielen verschiedenen Stellen auftreten können. Exon-Skipping ist daher mutations-spezifisch. Es wird eine personalisierte Therapie sein. Jeder Patient benötigt eine ganz bestimmtes Antisense-Oligo, aber jedes Antisense-Oligo kann oft für eine Gruppe von Patienten mit verschiedenen Mutationen verwendet werden, bei denen ein oder mehrere ganz bestimmte Exons geskippt werden müssen. Annemieke Aartsma-Rus und ihre Kollegen haben die Anwendbarkeit des Skippens für Duchenne-Patienten mit Deletionen, Punktmutationen und Verdoppelungen aufgelistet (5), die in den Leiden Duchenne Muscular Dystrophy Seiten verzeichnet sind. Ihre Liste enthält 130 Patientengruppen, die das Skippen eines oder zweier ganz bestimmter Exons benötigen in Prozent aller Duchenne-Patienten mit allen möglichen verschiedenen Mutationen. Die Autoren fanden heraus, dass 83% aller Duchenne-Patienten Mutationen haben, die durch das Exon-Skipping möglicherweise repariert werden können. Die verbleibenden 17% haben Mutationen, die zu schwierig für eine Reparatur mit der Exon-Skipping- Methode sind. Diese Patienten würden aber von pharmakologischen und anderen Therapien profitieren, die nicht mutationsspezifisch sind und daher allen Patienten zugutekommen würden. Im zweiten Teil dieses Berichtes werde ich die Ergebnisse der wichtigsten dieser Forschungsprojekte zusammenfassen. Die ersten 11 der 130 Patientengruppen sind in der folgenden kurzen Liste aufgeführt. Unter ihnen sind auch diejenigen, für die in den nächsten Jahren Skipping-Medikamente von den Firmen GSK/Prosensa und Sarepta entwickelt werden. Wie Sie sehen können, benötigen 13% aller Patienten das Skippen ihres Exons 51. Das 51-Antisense-Oligo ist damit ein mögliches Skipping-Medikament für die größte Gruppe aller Duchenne-Patienten. Daher wurde für die ersten abgeschlossenen und noch laufenden klinischen Studien des Exon-Skippings dieses Exon ausgesucht, da es der größten Patientengruppe möglichst bald helfen würde. Rang zu skippendes Exon % aller Patienten Rot: Prioritätsliste von Prosensa/GSK, 41.1% Blau: Prioritätsliste von Sarepta, 32.8% Wird das Exon-Skipping eine Therapie für meinen Sohn sein? Viele Duchenne-Familien aus der ganzen Welt stellen mir diese Frage. Ich erkläre Ihnen daher hier, wie Sie selbst das mögliche Skipping-Medikament für Ihren Sohn finden können. Da das Exon-Skipping jedoch eine mutations-spezifisches Verfahren ist, besteht der erste Schritt darin, die genaue Mutation im Dystrophin-Gen Ihres kranken Jungen zu kennen. Die Mutation kann am besten mit der MLPA- Methode (multiplex ligation-dependent probe amplification) in einem modernen genetischen Labor bestimmt werden, die alle 79 Exons bei Duchenne-Jungen, ihren Müttern und anderen weiblichen Verwandten analysiert. Diese und andere diagnostische Verfahren werden im zweiten Teil dieses Berichtes ausführlich beschrieben. Wenn die genaue Mutation bekannt ist hauptsächlich Deletionen, Verdoppelungen oder Punktmutationen können Sie selbst die Sequenz der genetischen Buchstaben der kombinierten 79 Exons der Dystrophin-mRNA anschauen, die die Anweisungen für die Zusammensetzung der Aminosäuren des normalen Dystrophin- Proteins enthält. Sie können sich die 15 Seiten mit diesen elftausend Buchstaben dieser Sequenz von den Leiden Muscular Dystrophy Pages im Internet herunterladen: Aus dieser Sequenz können Sie bestimmen, ob die Mutation Ihres Sohnes das Leseraster verschiebt oder beibehält. So lässt sich feststellen, ob diese genetische Information auf eine Duchenneoder Becker-Muskeldystrophie bei Ihrem Kind hinweist. Wenn Sie die Sequenzen an den Grenzregionen der Exons betrachten, können Sie auch bestimmen, welches Exon oder welche Exons geskippt werden müssen, um das Leseraster aus einer out-of-frame -Situation zurück in eine in-frame -Situation zu bringen. Es gibt noch einen einfacheren Weg, das Exon oder die Exons zu finden, die geskippt werden müssen, wenn Sie die Mutation des Dystrophin-Gens kennen. Die Anordnung der 79 Exons in der mrna können Sie in dem Bild auf der nächsten Seite sehen, das ich von Annemieke Aartsma-Rus erhalten habe: Um bei einer Deletion herauszufinden welches Exon geskippt werden muss, streichen Sie das fehlende oder die fehlenden Exons und entscheiden, ob das Exon vor oder nach der Deletion oder eventuell beide geskippt werden 9
10 müssen, so dass das Ende des vorangehenden Exons mit dem Anfang des folgenden Exons zusammenpaßt, wenn das deletierte Exon und das oder die geskippten Exons fehlen. Wenn z.b. die Deletion aus den 8 Exons besteht, kann man sehen, dass die beiden Exons 44 und 53, die vor und nach der Deletion kommen, nicht zusammenpassen. Wenn jedoch Exon 53 übersprungen wird, würde das Ende von Exon 44 zum Anfang von Exon 54 passen. Sie werden auch sehen, dass die Deletion der Exons repariert werden könnte, indem man die beiden benachbarten Exons 43 und 51 skippt, so dass die Exons 42 und 52 zusammenpassen. Sie werden auch erkennen, dass die Deletion von Exon 44 nicht zusammenpassende Exon-Enden verursacht, also das Leseraster verschiebt und so zu Duchenne führt. Eine Deletion der Exons hingegen produziert passende Exon-Enden, die das Leseraster nicht verschieben, was zu einer Becker-Dystrophie führen könnte. Diese Vorgehensweise funktioniert auch für Verdoppelungen und Punktmutationen. Dieses Bild zeigt die relative Größe der Exons, die Linie am linken unteren Rand zeigt die Länge von 100 Nukleotiden, genetischen Buchstaben. Hellblaue Exons sind in-frame -Exons. Wenn sie fehlen oder geskippt werden müssen, wenn sie eine Punktmutation enthalten, würden sie das Leseraster nicht verschieben. Dunkelblaue Exons sind out-of-frame -Exons. Ihre Deletion kann repariert werden, wenn sie und ein benachbartes Exon geskippt werden, so dass die Enden der verbleibenden Exons wieder zueinanderpassen. Die dritte und einfachste Möglichkeit besteht darin, auf die Exon-Skipping-Listen der Doktorarbeit von Annemieke Aartsma-Rus zu schauen. Hier können Sie direkt ablesen, welches Exon oder welche Exons geskippt werden müssen, wenn Sie die Einzelheiten der Mutation Ihres Sohnes kennen. Diese Listen können Sie im Internet wie folgt finden: Deletionen. Verdoppelungen: Punktmutationen: Als Beispiel habe ich hier 10 Einträge aus der Liste der Deletionen aufgeführt: Deletierte Exons zu skippende Exon(s) oder oder Wenn Sie die genaue Mutation Ihres Duchenne-Jungen in seinem Dystrophin-Gen kennen und wenn Sie das Exon oder die Exons gefunden haben, die in seiner mrna geskippt werden müssen, dann haben Sie meine Erklärungen hier verstanden. Sie sollten wissen, dass dies keine Garantie dafür ist, dass seine schweren Duchenne-Symptome in die milderen Symptome der Becker-Dystrophie umgewandelt werden, wenn er seine personalisierte Exon-Skipping- Arznei bekommt, die auf diesem Weg bestimmt wurde. Alles was gesagt werden kann, ist, dass das spezielle Skippen, das Sie korrekt identifiziert haben, das Leseraster der genetischen Information der mrna von einer out-offrame -Situation zurück in eine in-frame -Situation verschiebt. Es besagt nicht, dass diese in-frame -Situation in jedem Fall eine Becker-Dystrophin produzieren wird, da die Leseraster-Regel Ausnahmen hat. Die Gründe für diese Ausnahmen sind nicht für alle Fälle bekannt. Die Grenzen der Deletionen im Dystrophin- Gen stimmen in den meisten Fällen beispielsweise nicht mit den Grenzen der Exons überein, sondern liegen etwas innerhalb der oft sehr langen Introns zwischen den Exons. Diese Grenzen werden normalerweise nicht durch die üblichen genetischen Testmethoden gefunden und können unterschiedlich sein bei Patienten, die die gleichen Deletionen haben. Da die Introns Sequenzen haben, die wichtig für die Regulierung der Gene sind, kann ihr Vorhandenoder Nicht-Vorhandensein verschiedene Krankheitssymptome hervorrufen. Andererseits hat das Dystrophin-Protein eine Struktur mit Regionen, die unterschiedlich wichtig sind. Einige Deletionen können zusammen mit den geskippten Exons in einigen Fällen eine veränderte Proteinstruktur zur Folge 10
11 haben, die es nicht erlaubt, dass das verkürzte Dystrophin mehr oder weniger normal funktioniert. Obwohl also die Exon-Skipping-Therapie in vielen Fällen ein Protein produziert, das die Duchenne-Symptome verringern könnte, kann es Überraschungen geben, die während der klinischen Studien und den eigentlichen Behandlungen zutage treten werden. Mutationen, die nicht mit dem Exon-Skipping repariert werden können. Wie ich zuvor erwähnte, haben 17% aller Duchenne-Jungen Mutationen, die nicht mit Exon-Skipping behandelt werden können. Dies ist zum Beispiel der Fall, wenn das erste oder letzte Exon fehlt oder wenn die Mutationen in der Region der Exons auftreten, die für das wichtige Cystein-reiche Ende des Proteins notwendig ist. Ebenfalls nicht behandelbar sind lange Deletionen oder wenn sie die Actin-bindenden Teile des Proteins betreffen. Nicht reparabel sind auch große Umstrukturierungen wie das Verdrehen der Reihenfolge oder das Platzieren von Sequenzen an andere Stellen des Gens, was die genetische Information unkontrollierbar durcheinanderbringt. Wenn die genetischen Testergebnisse Ihres Sohnes Ihnen nicht erlaubt, nach meiner Anleitung hier das zu skippende Exon, oder die Exons, zu finden, oder wenn Sie andere Fragen haben, was für ihren Sohn getan werden könnte, bitte schreiben Sie eine persönliche an mich: und ich werde sobald wie möglich antworten. Wie werden Exon-Skipping-Medikamente entwickelt? Nachdem Sie meine Erklärungen gelesen haben, wissen Sie, welche Art von Exon-Skipping möglicherweise eine Therapie für Ihren Sohn sein könnte. Jetzt erkläre ich Ihnen, wie diese möglichen Medikamente entwickelt werden. Das geschieht in drei Teilen: Im ersten wird beschrieben, welche klinischen Studien gemacht werden müssen. Dann beschreibe ich, welche Skippings zuerst entwickelt werden und schließlich beschreibe ich, welche klinischen Studien schon abgeschlossen sind, welche gerade laufen und welche für die nähere Zukunft geplant sind. Welche Art von klinischen Studien müssen durchgeführt werden? Die US-amerikanische Gesundheitsbehörde FDA in Atlanta, die Europäische Arzneimittelbehörde EMA in London und andere Regulierungsbehörden verlangen, dass die normale Entwicklung eines klassischen Medikamentes mit den folgenden Phasen durchlaufen werden muss: Vorklinische Phase. Laborstudien und Tierversuche, um die Sicherheit, die biologische Aktivität und die beste Verabreichungsmethode des neuen Arzneimittels zu prüfen. Klinische Phase I. Studien an gesunden Freiwilligen, um die Sicherheit bei Menschen zu prüfen. Klinische Phase II. Studien an Patienten, um optimale Dosierungen, die Sicherheit und die Wirksamkeit zu prüfen. Klinische Phase III. Studie an Patienten, um die Sicherheit und Wirksamkeit des Arzneimittels zu bestätigen, wenn es über einen längeren Zeitraum eingenommen wird. Die Kosten aller drei klinischer Forschungsstudien können sich auf bis zu 500 Millionen US-Dollar für ein Arzneimittel belaufen. Es kann bis zu 15 Jahre von der ersten Idee für ein neues Medikament bis zu seiner Marktzulassung dauern. Diese Vorschriften wurden entstanden zu einer Zeit, als patientenspezifische Forschungsansätze wie das Exon- Skipping noch nicht existierten. Um ein personalisiertes genetisches Duchenne-Medikament durch diese Phasen zu bekommen, müssen verschiedene Herausforderungen gemeistert und überwunden werden. Die Studien mit Antisense-Oligos an gesunden Freiwilligen in Phase I könnte zum Beispiel das Leseraster in einer normalen Dystrophin mrna verschieben und so, wenn sie wirksam genug sind, zu Duchenne-Dystrophie bei diesen gesunden Freiwilligen führen. Dies wäre eine sehr ernstzunehmende Nebenwirkung, die nichts mit normalen widrigen Umständen zu tun hat. Eine andere große Sorge besteht in unerwünschten Wirkungen, sogenannten off-target -Effekten. Es könnten Exons in den genetischen Informationen anderer Gene als dem Dystrophin-Gen geskippt werden und somit schwerwiegende und möglicherweise unbekannte Krankheiten verursachen. Ein weiteres Problem, das nicht in der normalen Arzneimittelentwicklung auftritt, könnte spezifisch für die Duchenne- Dystrophie sein: Da Dystrophin fehlt, haben die Zellmembranen der Duchenne-Muskeln Risse und Löcher, durch die die Exon-Skipping Arzneien in das Zellplasma der Zellen gelangen und auch in die Kerne, wo sie für ihre therapeutischen Wirkungen gebraucht werden. Es könnte also nur bei Duchenne-Patienten zu negativen Auswirkungen kommen, die bei Personen ohne diese Krankheit nicht auftreten. Daher können klinische Studien der Phase I mit gesunden Freiwilligen mit möglichen Exon-Skipping Arzneimitteln nicht durchgeführt werden. Teilnahme an klinischen Studien. Klinische Studien an Patienten sind unverzichtbare Bestandteile in der Entwicklung einer Exon-Skipping-Therapie. Es ist verständlich, dass Familien versuchen, dass ihre kranken Kinder für diese Studien akzeptiert werden. Sie hoffen, dass ihr Kind dann eine Chance hat, früher eine Therapie zu bekommen anstatt noch mehrere Jahre auf die endgültige Zulassung dieser personalisierten Medikamente warten zu müssen. Klinische Studien sind jedoch nur Experimente an Menschen, die auch schiefgehen können. Familien sollten also den Informationen der Klinikärzte, die diese Studien durchführen, genau beachten, bevor sie ihre Einwilligung nach Aufklärung geben. Eine Teilnahme hat auch Nachteile, die von Kate Bushby von TREAT-NMD in einem Interview erklärt wurden, das ich mit ihr im März 2009 aufgezeichnet habe: Ich glaube nicht, dass es praktisch für die Kinder ist, von weit her zu kommen, um an klinischen Studien teilzunehmen, da sie jede Woche für Injektionen in den klini- 11
12 schen Zentren sein müssen und eine Menge Blutproben genommen werden. Es ist also besser, wenn sie in der Nähe dieser Zentren wohnen. Auch wenn sie in der Nähe wohnen, müssen die Familien ihr gesamtes Leben umstellen. Sie sollten sich im Klaren sein, dass die Studien nur Studien sind. In den späteren Wirksamkeitsstudien könnte ihr Kind in der Placebo-Gruppe sein. Das kann ihm während der Studie nicht helfen und es kann unvorhergesehene Nebenwirkungen geben. Studien bedeuten wirklich harte Arbeit. Ich würde sogar sagen, dass die Kinder in den Studien fast einen Nachteil haben. Sie müssen diese ganzen Unannehmlichkeiten über sich ergehen lassen, um etwas zu bekommen, von dem später jeder profitieren wird vorausgesetzt, dass es funktioniert. Wir sind den Familien und Jungen wirklich sehr dankbar, die all die Zeit und Anstrengung investieren, um an diesen Studien teilzunehmen, die hoffentlich die Sache für jeden ein Stück voranbringt. Es gibt jedoch einen wichtigen, potenziellen Vorteil für die Studien-Teilnehmer: Wenn die Studien der Phase II oder Phase III zeigen, dass sie bis zu einem gewissen Grad wirksam sind, dann kann der Studie eine offene Verlängerungs-Phase über mehrere Jahre folgen, in der alle Jungen auch die, die während der Studie Placebos erhalten haben die wirksamste Dosis, die in der Studie verwendet wurde, erhalten und zwar bis die Arznei in ihrem Land zugelassen wird. Muskelreparatur, eine allgemeine Einführung. Der Text dieses Abschnittes wurde von Annemieke Aartsma- Rus nach einer Tagung über Muskelstammzellen geschrieben, die im Juli 2012 in New Orleans in den USA stattfand. Muskeldystrophien wie zum Beispiel die Duchenne- Muskeldystrophie zeichnen sich durch eine kontinuierliche Schädigung von Muskelgewebe aus, die schließlich zum Verlust von Muskelgewebe und Muskelfunktion führt. Wie die meisten Gewebe sind Muskeln fähig sich zu regenerieren, wenn sie beschädigt wurden. Im Gegensatz zu den meisten anderen Gewebsarten, bestehen Muskeln jedoch nicht aus Einzelzellen, sondern aus Fasern, die aus Einzelzellen zusammengeschmolzen wurden. Danach können sich die Muskelfasern mehr teilen oder regenerieren. Auf den Muskelfasern liegen spezialisierte Einzelzellen, sogenannte Satellitenzellen, die sich teilen können, um Muskelzellen zu reparieren. Sobald Muskelfasern beschädigt sind, werden Proteine als Schadenssignale ausgesendet, die die Satellitenzellen aktivieren. Diese fangen sich dann an zu teilen, wandern zu den beschädigten Stellen und reparieren sie, indem sie mit den Muskelfasern zusammenschmelzen oder wenn die Beschädigung sehr groß ist sie schmelzen untereinander zusammen um eine neue Faser zu bilden. Um sicherzustellen, dass der Muskel nach der nächsten Beschädigung auch repariert werden kann, wird eine dieser Zellen eine inaktive Satellitenzelle, die sich wieder auf der neuen oder reparierten Muskelfaser ansiedelt. Jeder erleidet gelegentlich Schäden an seinen Muskeln. Das Regenerationssystem stellt sicher, dass die Beschädigung repariert wird und die Muskeln dicker und stärker wachsen, damit einer zukünftigen Beschädigung vorgebeugt wird. Das Problem bei Duchenne-Muskeldystrophie besteht darin, dass die Muskelfasern sehr viel empfindlicher gegenüber Beschädigungen sind, da ihnen wichtige Proteine fehlen, die die Muskelfasern während der Kontraktion stabilisieren. Diese Proteine sind z.b. Dystrophin und die mit ihm verbundenen anderen Proteine. Muskelfasern von Duchenne-Patienten werden leichter und öfter beschädigt als bei gesunden Personen. Dies verursacht chronischen Stress im Reparatursystem und führt zu Entzündungen. Normalerweise spielen Entzündungszellen bei Muskelbeschädigungen eine wichtige Rolle. Sie lösen nämlich das beschädigte Gewebe auf, um neuen Muskelfasern Platz zu machen. Sie sind also eine Art Abfallbeseitigungssystem. Aufgrund der chronischen Natur der Krankheit, liegt eine ständige Entzündung vor, die schließlich zur Fibrose führt. Dabei wird statt neuem Muskelgewebe ein Bindegewebe geformt, da die Entzündungszellen Signalpeptide aussondern, die dazu führen, dass Satellitenzellen Fibroblasten werden anstatt muskelaufbauende Zellen. Fibroblasten produzieren Signalpeptide, kurze Aminosäureketten, die die Fibrose verstärken bzw. aufrechterhalten. Es kommt zu einem Teufelskreis, indem mehr und mehr Fibrose produziert wird und Muskelreparaturen immer weniger stattfinden. Da Muskelgewebe weiterhin beschädigt wird, werden schließlich die meisten Muskelfasern durch Fibrose-Gewebe ersetzt, die Muskelfunktion geht verloren. Nach dieser Erklärung versteht man, wie wichtig das ist, was die Exon-Skipping-Therapie mit sich bringen wird: das Wiedererlangen des stabilisierenden Proteins Dystrophin und der mit ihm im Dystrophin-Komplex verbundenen Proteine in den überlebenden Muskelfasern. Dies verlangsamt oder stoppt den Fibroseprozess. Das bereits bestehende Bindegewebe bleibt allerdings erhalten. Exon-Skipping sollte daher so früh wie möglich im Leben eines Duchenne Jungen gestartet werden, möglichst bevor der Fibrose-Prozesse einsetzt und die meisten Muskelfasern noch vorhanden sind. Klinische Studien zum Exon-Skipping Die Entwicklung von personalisierten, genetischen Exon- Skipping-Medikamenten muss durch Firmen erfolgen, die über genügende finanzielle Mittel verfügen, um technische und ethische Probleme zu überwinden, die mit dieser neuen Art von Arzneimitteln einhergehen, die aber nicht ein Gen des Menschen verändern, sondern nur seine genetische Information reparieren. Ich nenne hier drei Firmen, die das Exon-Skipping zu dem am weitest entwickelten Verfahren zur Therapie von Duchenne-Muskeldystrophie gebracht haben. Mit weltweit etwa Patienten, gehört Duchenne-Muskeldystrophie zusammen mit Mukoviszidose zu den häufigsten Erbkrankheiten des Kindesalters. 12
13 Ich beschreibe Ihnen diese Firmen hier nicht mit meinen eigenen Worten, sondern gebe Ihnen ihre Namen und Adressen, so dass Sie sich auf ihren Internet-Seiten über ihre Duchenne-Forschungsarbeiten informieren können: Prosensa Therapeutics BV in Leiden, Niederlande, GlaxoSmithKline PLC (GSK) mit Zentrale in London, Geben Sie Duchenne in das Suchfeld oben rechts ein und klicken Sie auf go. Sarepta Therapeutics (ehemals AVI Biopharma) in Cambridge, MA, USA, Die vier ersten klinischen Studien über das Skippen von Exon 51 bei Duchenne-Jungen. Es erforderte viele Jahre von vorklinischen Arbeiten an Antisense-Oligos mit Muskelkulturen im Labor, mit dystrophen mdx-mäusen, die ein vorzeitiges Stopp-Codon in ihrem Exon 23 haben, und mit Mäusen, die das menschliche Dystrophin-Gen haben, bevor die vier klinischen Studien zum Exon- 51-Skippen mit Duchenne-Jungen in den Jahren 2006 bis 2009 durchgeführt werden konnten. Zwei von ihnen waren lokale Studien, bei denen nur unwichtige einzelne Muskeln behandelt wurden. Von ihnen konnten die teilnehmenden Jungen daher keine Änderung ihrer Symptome erwarten. Die beiden anderen Studien waren systemische Studien, bei denen die Exon- 51- Antisense-Oligos in die Blutbahn gespritzt wurden, um alle Muskeln zu erreichen. Diese vier Studien sollten vor allem die Frage beantworten, ob diese Antisense-Behandlung sicher ist, ob es Beweise für neu gebildetes Dystrophin gibt und ob eine Verbesserung der Muskelfunktion zu erwarten ist. Wenn das neue Medikament Wirkung zeigt, muss es später den Jungen schließlich jahrelang während ihres hoffentlich verlängerten Lebens gegeben werden. Sie sollte daher keine ernsten Nebenwirkungen haben und sie sollte vor allen Dingen nur die genetischen Informationen des Dystrophin- Gens reparieren und nicht die anderen mehr als menschlichen Gene und ihre Informationen beeinflussen. Lokale offene-phase-ii-studie in den Niederlanden zum Skippen von Exon 51. Die erste an Menschen vorgenommene Studie mit der Exon-Skipping-Technik wurde von Judith van Deutekom, Jan Verschuuren und anderen Mitarbeitern der Firma Prosensa Therapeutics und des medizinischen Universitätszentrums in Leiden zwischen Januar 2006 und März 2007 vorgenommen. Sie war lediglich darauf ausgelegt, einen Grundsatzbeweis zu erbringen. Es war eine lokale Studie an einer kleinen Stelle des Tibialis-anterior-Muskels, des vorderen Schienbeinmuskels, der mit PRO051, dem 2 O-Methyl-Antisense-Oligo gegen Exon 51 behandelt wurde. Die vier nicht mehr gehfähigen Jungen in dieser offenen Studie ohne Placebos waren zwischen 10 und 13 Jahren alt. Sie hatten Deletionen der Exons, 50, 52, und Jeder Junge erhielt eine einmalige Dosis von 0,8 mg PRO051, die direkt in den Schienbeinmuskel gespritzt wurde. Nach 4 Wochen wurde in einer Biopsie Muskelgewebe von der Injektionsstelle entnommen und auf die geskippte mrna und neues Dystrophin-Protein hin untersucht. Bis zu 94% der Muskelfasern in den Biopsie-Proben zeigten neues Dystrophin an seiner normalen Position unter den Muskelzellmembranen. Verglichen mit gesundem Muskelgewebe lag das Dystrophin in Konzentrationen von 33%, 35%, 17% und 25% vor. Die mrnas wurden isoliert und zeigten Sequenzen, bei denen die genetischen Buchstaben der deletierten und des geskippten Exons fehlten. Dies bewies, dass das Exon-Skipping tatsächlich das gewünschte Exon nicht nur in Mäusen, sondern auch im menschlichen Muskel überspringt, skippt. Diese erste Anwendung des Exon-Skipping Verfahrens an Duchenne-Jungen wurde am 27. Dezember 2007 in der Zeitschrift New England Journal of Medicine veröffentlicht (6). Systemische Studien der Phase IIa in Schweden und Belgien zum Skippen von Exons 51 bei Duchenne- Jungen. Im nächsten Schritt dieser Entwicklung mussten die Wissenschaftler zeigen, dass das Antisense-Oligo PRO051 auch systemisch durch eine Injektion in den Blutkreislauf angewendet werden kann, so dass es alle Muskelzellen erreichen und therapieren kann. Zwischen Juli 2008 und Januar 2009 führte Prosensa seine erste systemische Studie mit 12 Duchenne-Jungen durch, die 5-13 Jahre alt waren. Dabei wurde das Antisense Oligo PRO051 unter die Haut, subkutan, gespritzt. Die Injektionen wurden von den Teams um Nathalie M. Goemans an der kinderneurologischen Abteilung der Universität in Löwen in Belgien und um Mar Tulinius im Königin-Silvia-Kinderkrankenhaus in Göteborg in Schweden vorgenommen. In dieser offenen Dosis-Eskalationsstudie haben vier Gruppen mit jeweils drei Jungen das 51-Antisense-Oligo einmal pro Woche über 5 Wochen hinweg erhalten. Die Dosen betrugen 0,5, 2, 4 und 6 mg/kg. In der ersten Gruppe wurde Muskelgewebe in Biopsien vor und nach der Behandlung entnommen. In der höher dosierten Gruppe wurden die Muskel-Proben zwei und sieben Wochen nach der Behandlung entnommen. Damit wollte man erfahren, ob das neu geformte Dystrophin stabil ist. Die Struktur der mrna und des neuen Dystrophin- Proteins aus allen Biopsie-Proben wurden wie bei der lokalen Studie untersucht und zeigten, dass das Exon-Skipping-Antisense-Oligo die vorgesehenen Exons geskippt hatte und dass das neue Dystrophin wie erwartet ein leicht geringeres Molekulargewicht hatte als normales Dystrophin. Zwei Wochen nach Ende der Studie, enthielten % der Muskelfasern immer noch neues Dystrophin, wobei die höchsten Prozentsätze bei denjenigen Jungen gefunden wurden, die die höchste Dosis bekommen hatten. Wegen der kurzen Behandlungszeit, war, wie erwartet, keine Verbesserung der Muskelfunktionen zu verzeichnen. Diese Studie zeigte jedoch, dass zum ersten Mal die subkutane Anwendung von PRO051 zu einem Skippen 13
14 Exons 51 führte und die Produktion von neuem Dystrophin begonnen hatte. Das Ausmaß der Produktion hing mit der Dosierung zusammen, die höchste Dosis brachte die größte Menge an Dystrophin. Diese erste systemische Studie mit der Exon-Skipping- Technik bei Duchenne sollte die wichtigste Frage beantworten: Ist diese genetische Behandlung sicher? Die Gesamtkörper-Therapie wurde gut vertragen, es gab keine negative Immunreaktion auf das neue Protein und es wurden keine anderen bedeutsamen klinischen Probleme bei den 12 Duchenne-Patienten der Studie festgestellt. Alle Einzelheiten dieser Studie wurden in der Zeitschrift New England Journal of Medicine im März 2011 veröffentlicht (7). Dieser Studie folgte und folgt immer noch eine offene Verlängerungsstudie, die auf Seite 16 beschrieben wird. Zusammenarbeit Prosensa GSK. Das positive Resultat dieser zwei klinischen Studien der Phase II hat die Firmen Prosensa und GlaxoSmithKline, GSK, noch vor Bekanntgabe aller Einzelheiten davon überzeugt, dass eine weltweite exklusive Zusammenarbeit für die Entwicklung und Vermarktung ihrer Exon-Skipping-Technik unter Verwendung der 2 O-Methyl-Antisense-Oligoribonuleotide sinnvoll ist. In dieser Übereinkunft erhält GSK die Exklusiv- Lizenz für die Entwicklung und Vermarktung von Prosensas Antisense-Oligo für das Skippen des Exons 51 auf dem Dystrophin-Gen. Beide Firmen werden weiter zusammenarbeiten, um dieses Oligo fortzuentwickeln. Als erster gemeinsamer Schritt wurde 2010 mit der entscheidenden, internationalen klinischen Studie der Phase III begonnen, an der mindestens 180 Duchenne-Jungen teilnehmen sollten, die ein Skippen des Exons 51 benötigen. GSK wird alle Kosten dieser großen Studie übernehmen. Außerdem erhält GSK die Option, drei weitere Antisense-Oligos zu lizensieren und zwar für das Skippen des Exons 44, und entweder der Exons 45 und 53 oder 52 und 55. Das Skippen von Exon 44 wird schon in einer Phase- II- Studie getestet. Ergebnisse werden hier im Laufe des Jahres 2013 erwartet. Klinische Studien zum Skippen der Exons 45 und 53 werden im Jahr 2013 beginnen. GSKs Optionsrechte können bei einem erfolgreichen Abschluss der Exon-44-Studie in Anspruch genommen werden. Erste klinische Studien mit Morpholino-Antisense Oligos für das Skippen von Exon 51. Bevor ich die Studien, die von Prosensa und GSK durchgeführt werden, weiter beschreibe, fasse ich zwei Exon- Skipping-Studien und eine Erweiterungsstudie zusammen, die ähnlich waren wie die von Prosensa vorgenommenen Studien, die jedoch eine andere Art von Antisense-Oligos, die Morpholinos, verwendeten. Diese wurden von der Firma AVI BioPharma in Bothell nahe Seattle in den USA entwickelt. Die Firma heißt heute Sarepta Therapeutics und hat ihre Zentrale in Cambridge in der Nähe von Boston im US-Bundesstaat Massachusetts. Diese beiden Studien wurden im Vereinigten Königreich und nicht in den USA durchgeführt, da eine Starterlaubnis von der Europäischen Arzneimittelbehörde EMA einfacher und schneller zu bekommen war, als von der US-amerikanischen Gesundheitsbehörde FDA. Erste lokale klinische Studie mit einem Morpholino-51 Antisense Oligo im Vereinigten Königreich. Diese Exon-Skipping-Studie der Phase IIa wurde im Vereinigten Königreich zwischen Herbst 2007 und Ende 2008 unter Leitung von Kate Bushby von TREAT-NMD in Newcastle und Francesco Muntoni vom Imperial College in London durchgeführt. Während der vorklinischen Versuche zeigte Dominic Wells in London, dass sich das von Steve Wilton in Perth in Australien entwickelte Morpholino-Antisense-Oligo AVI-4658 als genügend stabil für eine langfristige klinische Behandlung eignet. Die Studie war lokal und diente dazu, die Sicherheit und die biochemische Wirksamkeit dieses Morpholino- Exon-51-Oligos zu untersuchen. Es wurde mit einer einzigen Injektion in den kleinen, unwichtigen Muskel, extensor digitorum brevis, EDB-Muskel, an der Außenseite des Fußes gespritzt. Sieben 11-16jährige Duchenne-Jungen, die das Skippen des Exons 51 benötigen, nahmen an der Studie teil. Einige von ihnen konnten nicht mehr laufen. Jeder der 7 Patienten hatte weniger als 5% revertierter Fasern in seinen Muskeln. Das wurde im Muskelgewebe nach einer Biopsie vor der Behandlung festgestellt. Geringe Mengen dieser Dystrophin-haltigen Muskelfasern gibt es bei vielen Duchenne-Jungen. Sie entstehen durch spontanes Exon-Skipping. Diese Studie war eine einfachblinde Studie. Die Forscher, die die Muskelproben untersuchten, wussten nicht, ob das Gewebe vom behandelten Muskel des Jungen stammte oder vom Vergleichsmuskel seines anderen Fußes. Zwei Jungen erhielten 0,09 mg des Morpholinos, die anderen fünf Jungen erhielten die 10fache Dosis, 0,90 mg. Drei bis vier Wochen nach den Injektionen wurden fast die gesamten behandelten EDB-Muskeln bei Biopsien entnommen. Die höhere Dosis führte zu einer neuen Dystrophin- Produktion in allen behandelten Muskeln. Die Menge des Dystrophins schwankte zwischen 22 und 32% verglichen mit der Intensität in Muskeln bei gesunden Menschen. Sie war 11-21% größer als die Menge des revertierten Dystrophins im Kontrollmuskel des anderen Fußes. Zusätzliche Tests ergaben, dass das neue Dystrophin tatsächlich ein reduziertes Molekulargewicht hatte, wie es vom verkürzten Becker-Dystrophin erwartet wird. In den Patienten, die die sehr geringe Dosis des Oligos erhalten hatten, wurde mrna ohne die geskippten Exons gefunden. Es konnte jedoch keine Zunahme des Dystrophin-Proteins nachgewiesen werden, da der Protein-Test nicht empfindlich genug war, um sehr kleine Unterschiede in der Proteinmenge feststellen zu können. Diese in-vivo-studie zeigte, dass das Antisense-Oligo AVI-4658 das gewünschte Skippen des Exons 51 verursachte und auch die Produktion des neuen Dystrophins. Dieses war an seinen normalen Platz an der Unterseite der Muskelzellmembran gewandert und hatte sich dort korrekt 14
15 mit den Proteinen des Dystrophin-Glykoprotein-Komplexes verbunden. Wie bei allen lokalen Behandlungen war kein therapeutischer Nutzen für die teilnehmenden Jungen erwartet worden. Beide Lokalstudien, die niederländische und die englische Studie, sollten vor allem das Prinzip beweisen, dass das Skippen von Exons beim Menschen funktioniert. Beide Studien haben gezeigt, dass das tatsächlich der Fall ist. Es gab einige technische Unterschiede zwischen den beiden Studien. Die Ergebnisse können daher nicht in allen Einzelheiten direkt verglichen werden. Die Einzelheiten dieser lokalen Studie wurden 2009 in der Fachzeitschrift The Lancet Neurology (8) veröffentlicht. Erste systemische klinische Studie mit einem Morpholino-51-Antisense-Oligo im Vereinigten Königreich. In dieser offenen Studie der Phase II wurden 19 Jungen behandelt, die 6-13 Jahre alt waren, noch laufen konnten und ein Skippen des Exons 51 benötigten. Die Studie wurde im Laufe des Jahres 2009 in London und Newcastle upon Tyne, ebenfalls unter Leitung von Kate Bushby und Francesco Muntoni durchgeführt. Die Jungen erhielten 12 Wochen lang Dosen von 0,5 bis 20 mg/kg des AVI Antisense-Oligos. Dieses wurde durch wöchentliche intravenöse Injektionen in den Blutkreislauf gespritzt, damit alle Muskeln erreicht werden konnten. Ziel der Studie war es, die Sicherheit der Methode und die Verträglichkeit zu testen, nicht die Veränderungen der Muskelfunktionen und der Muskelstärke. Es wurde Muskelgewebe mit zwei Biopsien aus dem Bizeps jedes Jungen vor und nach der Behandlung entnommen. Hiermit sollte die niedrige Menge an Dystrophin in den revertierten Fasern vor dem Start der Studie und die Zunahme nach der Behandlung bestimmt werden. Bei den 7 Patienten, die höhere Dosen zwischen 2 und 20 mg/kg/woche erhalten hatten, wurde, verglichen mit der normalen Menge in gesunden Menschen, zwischen 9 und 16% neues Dystrophin gefunden und zwar oberhalb der Menge des revertierten Dystrophins im Kontrollmuskel. Diese Ergebnisse wurden durch Analyse der geskippten mrna und des verkürzten Proteins erhalten. Drei der vier Patienten, die die höchste Dosis von 20 mg/kg erhielten, wiesen nach der Behandlung in 21%, 15% und 55% ihrer Fasern Dystrophin auf. Nach der Behandlung traten auch einige mit Dystrophin assoziierten Proteine wieder an gewohnter Stelle in den Muskelzellmembranen auf, die bei Duchenne-Patienten mit dem Dystrophin verloren gehen. Während der gesamten Studie, gab es keine Nebenwirkungen, die mit dem Medikament in Verbindung gebracht werden konnten. Eine Verbesserung der Muskelfunktion war nicht erwartet worden, da die Studie zu kurz war, um eine Veränderung der Muskelleistung herbeizuführen, die zuverlässig gedeutet werden kann. Die Autoren kamen zu dem Schluss, dass die Sicherheit der Behandlung und der Beweis, dass die systemisch angewandte Oligo AVI-4658 tatsächlich das Exon 51 geskippt hat, dass also AVI 4658 wahrscheinlich den Verlauf der Duchenne Muskeldystrophie beeinflussen kann (9). Verlängerungsstudie mit Sareptas Morpholino-51 Antisense-Oligo. NCT Diese Studie, die US-201 genannt wird, ist der doppelblinde Teil der von Sarepta durchgeführten Verlängerung der vorangegangenen systemischen Studie. Es wurden jedoch zwei höhere Dosen von Eteplirsen, 30 und 50 mg/kg/woche und ein Placebo über 24 Wochen injiziert. Mithilfe von mehreren Muskelproben, die durch Biopsien nach Ende dieses doppelblinden Teils der Studie entnommen wurden, sollte herausgefunden werden, ob neues Dystrophin in den Muskeln entstanden war. Meine Zusammenfassung über die Durchführung und die Ergebnisse dieser Studie basieren auf einer Reihe von Veröffentlichungen von Sarepta. Die letzte Veröffentlichung erschien am 7. Dezember 2012 (10). Die Studie begann im Februar 2012 und wurde unter Leitung von Jerry Mendell und seinen Kollegen am Nationwide Children s Hospital in Columbus im US-Bundesstaat Ohio durchgeführt. Während der ersten 24 Wochen haben 12 Duchenne- Jungen in 3 Gruppen wöchentliche intravenöse Injektionen erhalten. 4 Jungen bekamen eine Dosis von 30 mg/kg, 4 weitere eine Dosis von 50 mg/kg, die restlichen 4 Jungen bekamen Placebos. Vor der ersten Injektion, nach 12 Wochen mit der 50 mg/kg-dosis und nach 24 Wochen mit der 30 mg/kg-dosis wurden Proben nach Biopsien entnommen, um den Dystrophin-Gehalt zu bestimmen. Nach 48 Wochen wurde von allen Jungen eine dritte Biopsie vorgenommen. Um festzustellen, ob diese Behandlungen die klinischen Symptome verbessert haben, wurden verschiedene Muskelfunktionstests durchgeführt. Am Ende des doppelblinden Teils der Studie zeigte jedoch der wichtigste Test, der 6-Minuten-Geh-Test, bei der Gruppe mit den 30 und 50 mg/kg-dosierungen keine bedeutsamen Veränderungen nach 12 bzw. 24 Wochen. Nach 24 Wochen wurde daher die Studie ohne Zeitbegrenzung als offene Verlängerung unter dem Namen 4658-US-202 fortgeführt, um zu sehen, ob unter diesen Umständen die Verbesserung der Muskelfunktion hauptsächlich durch den 6-Minuten-Geh-Test gemessen werden kann. Zwei der Placebo-Patienten wurden den 4 Jungen der Gruppe zugeordnet, die die 50 mg/kg-dosis erhielt. Die anderen beiden Jungen wurden in die 30 mg/kg-gruppe integriert. In der Zwischenzeit verloren zwei Jungen der 30 mg/kg-gruppe die Gehfähigkeit, so dass sie den 6-Minuten-Geh-Test nicht mehr ausführen konnten. Es gibt jetzt also 3 Gruppen: 4 Jungen, die die 50 mg/kg-dosis jede Woche von Beginn an erhielten, 4 Jungen, die die 30 mg/kg-dosis jede Woche von Beginn an erhielten von denen aber nur zwei noch am 6-Minuten-Geh-Test teilnehmen konnten und 4 Placebo-delayed -Jungen, die 24 Wochen lang Placebos erhielten und dann mit 30 bzw. 50 mg/kg pro Woche behandelt wurden. Sie sind die Jungen, die eine durch Placebos verzögerte Behandlung erhalten haben. Ich werde für sie hier die englische kurze Bezeichnung placebo-delayed verwenden. Da es über 62 Wochen hinweg keine merklichen Unterschiede in den Ergebnissen des 6-Minuten-Geh-Tests zwischen den 30 und 50 mg/kg-dosierungen mit Eteplirsen 15
16 gab, sollen hier nur die Ergebnisse von zwei Patientengruppen diskutiert werden: Gruppe I mit 6 Jungen, die von Beginn der Studie über 62 Wochen behandelt wurden, und Gruppe II mit den 4 Placebo-delayed -Jungen, die zunächst 24 Wochen Placebos erhalten hatten und dann 38 Wochen lang die 30 oder 50 mg/kg-dosis Eteplirsen. Nach 62 Behandlungswochen liefen die 6 behandelten Jungen der Gruppe I 16 Meter weniger im 6-Minuten-Geh- Test als zu Beginn der Studie. Die 4 Placebo-delayed - Jungen liefen 78 Meter weniger. Die behandelten Jungen hatten gegenüber den Placebo -Jungen also den bedeutenden Vorteil, dass sie 62 Meter weiter laufen konnten. Diese Ergebnisse wurden unter den Jungen gemittelt und auf volle Meter gerundet. Die Tatsache, dass die behandelten Jungen in 62 Wochen (1 Jahr und 2,5 Monate) nur 16 Metern an Laufleistung einbüßten, bedeutet, dass sie weniger als 5% der 400 Meter Laufleistung verloren hatten, die sie zu Beginn der Studie in 6 Minuten erbringen konnten. Die 4 Placebodelayed -Jungen verloren während der 38wöchigen Behandlung weniger als 10 m Laufleistung. Dies bedeutet, dass durch die Exon-Skipping Behandlung die Duchenne- Muskeldystrophie, wie erwartet, deutlich gebremst wurde und der Becker-Dystrophie ähnlicher wurde. Annemieke sagte dazu: Diese Ergebnisse müssen mit Vorsicht betrachtet werden, da die Gruppen sehr klein sind und es bekannt ist, dass es bei den einzelnen Jungen erhebliche Unterschiede im Fortschreiten der Krankheit gibt. Dies wird noch dadurch unterstrichen, dass zwei der behandelten Patienten während der Studie ihre Gehfähigkeit verloren. Die positiven Ergebnisse der Dystrophin-Bestimmung im Muskelgewebe nach Biopsien, sind ein weiterer Hinweis, dass diese Art von Exon-Skipping funktioniert. Nach 24 Wochen Behandlung führte das Morpholino-51 Antisense-Oligo Eteplirsen bei einer Dosis von 30 mg/kg pro Woche zu einem deutlichen Anstieg der Zahl der Fasern mit neuem Dystrophin zwischen 16 und 29%. Bei einer kürzeren Behandlung von 12 Wochen wurde selbst bei der höheren Dosis von 50 mg/kg pro Woche keine nennenswerte Zunahme von neuem Dystrophin gefunden. Dies zeigt, dass eine längere Behandlung als 6 Monate notwendig ist, bevor durch das Eteplirsen eine nennenswerte Zunahme von neuem Dystrophin bewirkt wird. Bei den Jungen, die über 48 Wochen behandelt wurden, stieg bei beiden Dosierungen der Prozentsatz der Muskelfasern, die neues Dystrophin erhielten, von weniger als 5% auf 47% der normalen Menge. Bei den Placebo-delayed - Jungen, die erst nach den ersten 24 Wochen wirklich behandelt wurden, enthielt nur 38% der Fasern neues Dystrophin. Eteplirsen erwies sich über den gesamten Zeitraum der Studie von 62 Wochen in beiden Dosierungen als sicher. Sarepta hat angekündigt, dass es diese Ergebnisse mit der US-amerikanischen Gesundheitsbehörde FDA besprechen will und im Jahr 2014 eine entscheidende, doppelblinde Studie der Phase III beginnen möchte. Klinische Studien zum Skippen des Exons 51, die von GlaxoSmithKline (GSK) und Prosensa durchgeführt werden Zum Zeitpunkt des Niederschreibens dieses Berichtes, waren die ersten vier klinischen Studien zum Skippen des Exons 51 beendet und ihre Ergebnisse veröffentlicht. Eine recht große Anzahl von zusätzlichen Studien zum Skippen des Exons 51 ist derzeit am Laufen. Sie werden von GSK mit dem 51 Antisense-Oligo PRO051 von Prosensa ausgeführt. Dieses Oligo heißt jetzt Drisapersen und GSK Jede dieser Studien hat eine GSK-Identifikationsnummer, die mit DMD beginnt sowie eine NCT- Nummer unter der sie im Internet von den US-amerikanischen National Institutes of Health, NIH, dokumentiert sind und häufig aktualisiert werden. Um aktuelle Informationen über eine besondere Studie zu finden, gehen Sie bitte auf geben die NCT-Nummer im Kästchen search for study ein und klicken dann auf search. Danach müssen Sie auf den Titel der Studie klicken. In den jetzt folgenden Absätzen gebe ich Ihnen kurze Zusammenfassungen der wichtigsten dieser Duchenne- Studien und erwähne ihre NCT-Nummern und ihre GSK- Namen, wenn sie von GSK durchgeführt werden. Prosensa offene Verlängerungsstudie PRO Nachdem Prosensa zwei offene 51-Studien durchgeführt hatte eine lokale und eine systemische, siehe Seite 13 erhalten jetzt alle 12 Jungen, die an der systemischen Studie teilgenommen hatten, die höchste Dosis an Drisapersen, 6 mg/kg pro Woche, subkutan gespritzt in der offenen Verlängerungsstudie, die schon mehr als 3 Jahre läuft. Bisher sind noch keine ernstzunehmenden Sicherheitsprobleme aufgetreten. Bei der Tagung des Parent Projet Muscular Dystrophy, die im Juni 2012 in Fort Lauderdale im US-Bundesstaat Florida stattfand, wurden die vorläufigen Ergebnisse des 6-Minuten-Geh-Tests nach 96 Wochen, = 22 Monate, vorgestellt. In dieser Zeit hatten 7 Jungen ihre Gehfähigkeit erhalten oder verbessert. Von den 10 Jungen, die zu Beginn der Studie den 6-Minuten-Geh-Test ausführen, konnten zwei nicht mehr allein gehen. Sie befanden sich bereits am Ende der Laufphase, als sie begannen, an der Studie teilzunehmen. Dies bedeutet, dass die Jungen mit einer besseren Laufleistung zu Beginn der Studie von der Behandlung im stärkeren Maße profitiert haben. Dies ist ein Indiz für die langfristige positive Wirkung des Exon-Skippings. Die Ergebnisse müssen jedoch vorsichtig interpretiert werden, da alle Jungen behandelt wurden und es keine Placebo-Kontrollen gab. Ein Vergleich mit dem normalen Verlauf der Krankheit ist daher nicht möglich. Eine graphische Darstellung ähnlich wie für die Ataluren-Studie auf Seite 8 ist noch nicht verfügbar. Phase III der Exon-51 GSK-Studie GSK DMD NCT Diese wichtige und entscheidende Studie ist eine Doppelblind-Studie der Phase III. Sie soll definitiv beweisen, dass das Skippen des Exons 51 die Geschwindigkeit der Duchenne-Muskeldegeneration verlangsamt, 16
17 die mit dem 6-Minuten-Geh-Test gemessen wird. Dadurch könnte das 51-Antisense-Oligo des Typs 2 O-Methyl, Drisapersen, durch die Regulierungsbehörden FDA in den USA und EMA in Europa zum Vertrieb zugelassen werden. Diese große Studie wird in 45 klinischen Zentren in 21 Staaten durchgeführt: in Argentinien, Belgien, Brasilien, Chile, Dänemark, Deutschland, Frankreich, Italien, Japan, Kanada, in den Niederlanden, in Norwegen, Polen, Russland, Serbien, Spanien, Südkorea, Taiwan, in der Tschechischen Republik und in der Türkei. Die Vereinigten Staaten fehlen in dieser Liste, da die FDA andere Anforderungen stellte. Daher wird hier eine ähnliche Studie mit zwei verschiedenen Dosen durchgeführt. Sie wird in der rechten Spalte dieser Seite beschrieben. Die Injektionen dieser Phase-III-Studie begannen im Dezember Die letzten Jungen wurden im dritten Quartal 2012 aufgenommen. Die Studie wird also Ende 2013 abgeschlossen sein, wenn die letzten Jungen ein Jahr lang behandelt wurden. Ihre Ergebnisse werden voraussichtlich 2014 zur Verfügung stehen. Sie werden dann auf dem ersten dafür geeigneten medizinischen Kongress vorgestellt und in einer wichtigen wissenschaftlichen Fachzeitschrift veröffentlicht. Für diese wichtige Studie wurden 186 Duchenne-Jungen aufgenommen, die mindestens 5 Jahre alt waren und vor Teilnahme an der Studie mindestens 6 Monate lang Steroide erhalten hatten. Die Jungen erhalten entweder 6 mg/kg des potenziellen Medikaments oder eine nicht aktive Substanz als Placebo 48 Wochen lang jede Woche unter die Haut gespritzt. Es mußten mindestens 180 Jungen an der Studie teilnehmen, um sicherzugehen, dass die Ergebnisse statistisch signifikant sind, d.h. zuverlässig zumindest einen Unterschied von 30 Metern zwischen den behandelten und den Placebo-Jungen zeigen können, falls das 51-Antisense- Oligo wirksam ist. Die wichtigste Methode, eine Verbesserung der Muskelfunktion festzustellen, wird, wie in den meisten anderen Exon-Skipping-Studien auch, der 6-Minuten-Geh-Test sein. Es werden jedoch auch andere Tests durchgeführt, die beispielsweise die Muskelstärke und die Atemleistung messen. Am Ende der Behandlung wird Muskelgewebe durch Biopsien entnommen, um auf neu entstandenes verkürztes Dystrophin zu testen. Während der gesamten Studie werden klinische Analysen in wiederholten Blutproben durchgeführt, um nachzuweisen, dass die Behandlung weiterhin sicher ist. Mit Fragebögen sollen die Eltern Veränderungen in der Lebensqualität dokumentieren. Das Vorhandensein des neuen, verkürzten Dystrophins in den Muskeln der behandelten Patienten reicht nicht aus, um zu beweisen, dass dieses Exon-Skipping tatsächlich funktioniert. Das neue Dystrophin könnte entstanden, jedoch nicht an seinem normalen Platz gewandert sein. Dann könnte es die Muskeln nicht stabiler machen und ihre Funktion verbessern. Der 6-Minuten-Geh-Test ist die beste Methode, um Änderungen der Muskelfunktion zu beweisen. Wenn das Medikament eine positive Wirkung hat, dann können die behandelten Jungen mehr Meter in 6 Minuten gehen als die Placebo-Patienten. Positive Ergebnisse Des 6-Minuten-Geh-Tests werden von der FDA und der EMA als der zuverlässigste Beweis akzeptiert, dass ein neues Medikament bei Muskelkrankheiten wirksam ist. Offene GSK Verlängerungsstudie DMD , NCT Ähnlich wie die von Prosensa durchgeführte, systemische Studie der Phase II, siehe Seite 13, ist diese Studie eine Fortführung der Behandlung derjenigen Patienten, die die 48 Wochen der Injektionen der Phase III-Studie GSK und der Studie GSK mit periodischer Dosierung, siehe unten auf dieser Seite, abgeschlossen hatten. Alle teilnehmenden Patienten erhalten eine Dosis von 6 mg/kg pro Woche, auch diejenigen, die während der ersten Studie Placebos erhalten hatten. Die Behandlung mit Steroiden muss ebenfalls ohne Unterbrechung aufrechterhalten werden. Diese Studie begann im September 2011 und wird im Dezember 2014 abgeschlossen werden. Die Jungen werden in den gleichen klinischen Zentren behandelt, in denen sie auch während der doppelblinden Studien behandelt wurden. Wahrscheinlich werden bis zu 200 Jungen teilnehmen. Die Ergebnisse werden Anfang 2015 zur Verfügung stehen und in einer wichtigen medizinischen Fachzeitschrift veröffentlicht. GSK Phase II-Studie mit zwei Dosen in den USA, DMD , NCT Diese Studie ist ähnlich wie die internationale Studie der Phase III. Es werden jedoch zwei Dosen angewendet, 3 und 6 mg/kg pro Woche. Sie wird nur in den USA durchgeführt und zwar in Sacramento, Stanford (beide Kalifornien), Gulf Breeze (Florida), Iowa City (Iowa), Kansas City (Kansas), Baltimore (Maryland), Minneapolis (Minnesota), St. Louis (Missouri), New York, Durham (North Carolina), Cincinnati, Columbus (beide Ohio), Portland (Oregon) und Dallas (Texas). Es werden 54 Duchenne-Jungen, die mindestens 5 Jahre alt sind und noch allein gehen können, an der Studie teilnehmen. Jeder von ihnen erhält jede Woche einmal das potenzielle Medikament oder ein Placebo. Die Studie dauert 24 Wochen lang. Danach schließt sich eine Beobachtungsperiode von 24 Wochen an, die auch GSK DMD Verlängerungsstudie heißt. Die Injektionen wurden im Oktober 2011 begonnen, der letzte Junge wird seine ein Jahr dauernde Behandlung Ende 2013 abschließen. Die Methoden, um die Ergebnisse der Studien zu messen, sind der 6-Minuten-Geh-Test, das Bestimmen von Dystrophin in Muskelgewebe nach einer Biopsie und viele andere Tests, die die Sicherheit feststellen. Es werden auch Methoden zur Anwendung kommen, die die Pharmakokinetik untersuchen. Hier wird gemessen, wie schnell ein Medikament in die Muskeln gelangt und wie schnell es abgebaut und aus dem Körper ausgeschieden wird. Außerdem wird die neue und teure Magnetresonanzuntersuchung, MRI, angewendet werden, die den Zustand der Gliedmaßen, des Herzens und des Zwerchfellmuskels überprüft, um zu prüfen, welche Wirkung das 51-Antisense-Oligo hier hat. Skippen von Exon 51 mit periodischer Behandlung, GSK Studie DMD , NCT Das Ziel dieser Studie der Phase II war es herauszufinden, ob eine pe- 17
18 riodische Behandlung mit dem Antisense-Oligo von GSK zu einer besseren langfristigen Sicherheit mit gleicher therapeutischer Wirkung führt als eine Behandlung mit wöchentlichen Injektionen. Diese Studie wurde von September 2010 bis Ende 2012 in 13 klinischen Zentren in 9 Ländern durchgeführt: in Australien, Belgien, Deutschland, Frankreich, Israel, den Niederlanden, Spanien, in der Türkei und im Vereinigten Königreich. Es nahmen 53 Duchenne-Jungen teil, die mindestens 5 Jahre alt waren und noch selbst gehen konnten. Sie mussten vorher mindestens 6 Monate lang Steroide erhalten haben und diese Behandlung auch während der Studie fortsetzen. Etwa ein Drittel der Jungen erhielt 6 mg/kg des Anti-51-Oligos 48 Wochen lang jede Woche unter die Haut gespritzt. Ein weiteres Drittel wurde in fünf 10- Wochen-Zyklen behandelt. In den Wochen 1, 3 und 5 erhielten die Jungen zweimal Injektionen von 6 mg/kg, in den Wochen 2, 4 und 6 nur einmal, in den Wochen 7-10 fand keine Behandlung statt. Das letzte Drittel der Patienten erhielt Placebos unter den gleichen Bedingungen. Diese Studie war also eine Doppelblind-Studie. Das primäre Ergebnis dieser Studie war die Wirksamkeit nach einer Behandlungszeit von 24 Wochen. Als Ergebnis wurde gemessen die Veränderung der Muskelfunktion mit dem oft wiederholten 6-Minuten-Geh- Test. Außerdem wurde die Pharmakokinetik bestimmt, das Verhalten des Oligos im Körper, sowie die Sicherheit durch mehrere Blut- und Urinanalysen. Vor und nach der Studie wurde in Muskelgewebe nach Biopsien die Menge an neuem und verkürztem Dystrophin bestimmt, das durch das Skipping entstanden war. Die Ergebnisse werden veröffentlicht, sobald sie vollständig analysiert und ausgewertet sind. Skipping des Exons 51 bei Rollstuhlpatienten, GSK Studie DMD , NCT Das Ziel dieser systemischen Studie war es, die Sicherheit und Verträglichkeit des Skippens von Exon 51 bei 19 Patienten zu untersuchen, die nicht mehr gehen konnten. Die Patienten waren älter als 9 Jahre und mussten schon mindestens 1 Jahr, jedoch nicht länger als 4 Jahre, einen Rollstuhl benutzen. Da die anderen Studien mit Jungen, die noch gehen konnten, bisher zu keinen Sicherheitsproblemen führten, sollte diese Studie sicherstellen, dass bei Rollstuhlpatienten keine bisher unbekannten Sicherheitsprobleme auftreten. Weil diese Jungen weniger aktiv sind als die noch gehenden und sie deutlich weniger Muskeln haben, könnte sich das neue Medikament in den Muskeln anders verhalten und auch sein Ausscheiden aus dem Körper anders sein. Dies könnte zur Folge haben, dass sie eine andere Dosis bekommen müssten. Die Ergebnisse dieser Studie werden wichtige Informationen zu weiteren Studien an älteren Duchenne-Jungen und jungen Männern liefern. Die 19 Teilnehmer dieser Studie wurden in zwei Gruppen von je 8 Jungen eingeteilt und in eine von 3 Jungen. Bei den zwei ersten Gruppen erhielten jeweils 6 Jungen einmalig subkutane Injektionen von 3 oder 6 mg/kg des GSK Anti-51-Oligos Zwei Jungen in jeder dieser Gruppen erhielten die gleiche Dosis einer nicht aktiven Substanz als Placebo. Diese Studie war also eine Doppelblind-Studie. In der dritten Gruppe erhielten 2 Jungen 9 mg/kg und 1 Junge ein Placebo. Eine und 4 Wochen nach den Injektionen wurden ausgedehnte klinische Tests durchgeführt. Es gab keine ernsten Nebenwirkungen. Die Studie wurde in Columbus im US-Bundesstaat Ohio und in Paris durchgeführt. Sie fand von Juli 2010 bis Februar 2012 statt. Die Ergebnisse werden veröffentlicht, sobald sie vollständig analysiert sind. Die Exon-51-Studien müssen beweisen, dass das Exon- Skipping wirkt. Die Studien über das Skippen des Exons 51 sind die wichtigsten, um Antisense-Oligos gegen Duchenne Muskeldystrophie in Europa und den Vereinigten Staaten für den Vertrieb zugelassen zu bekommen. Wenn die Ergebnisse aller Exon-51-Studien die beiden wichtigsten Zulassungsbehörden FDA und EMA überzeugen können, dass das Skippen des Exons 51 wirksam und über viele Jahre hinweg eine sichere Therapie für Patienten ist, könnte das erste genetische Medikament zur Behandlung einer schweren Erbkrankheit innerhalb der nächsten Jahre für den Verkauf zugelassen werden. Das Skippen von Exon 51würde jedoch nur 13% aller Duchenne-Patienten helfen. Um eine Skipping-Therapie für die restlichen 70% der Patienten anbieten zu können, die Exon-Skipping brauchen, die aber weniger häufige oder seltene Mutationen haben, müssten mehr als 100 verschiedene Antisense-Oligos entwickelt werden. Um das Exon-51-Medikament bis zur Zulassung zu entwickeln, werden schließlich mehr als 10 Jahre vergangen sein. Es werden zudem viele Millionen Euro und Dollar in vorklinische Arbeiten und in die 3 Phasen der klinischen Studien investiert worden sein. Diese Zeitspanne und diese Kosten müssen deutlich reduziert werden, um die vielen anderen Skipping-Medikamente für die Mehrheit der Duchenne- Patienten zu entwickeln. Es laufen Diskussionen und Verhandlungen zwischen TREAT-NMD, PPMD sowie anderen Patienten-Organisationen und den Behörden FDA und EMA, um sie davon zu überzeugen, dass eine schnellere Entwicklung der vielen anderen Oligos unbedingt nötig ist, wenn sich das 51- Oligo und das 44-Oligo als zweites nach ausgiebiger Überprüfung als sicher und wirksam erwiesen haben, die zusammen schon 19,2% aller Patienten helfen würden. Klinische Studien zum Skippen anderer Exons als 51. Klinische Phase-II-Studie zum Skippen von Exon 44. NCT Prosensa führt diese offene Studie mit seinem Antisense-Oligo PRO044-CLIN-01 in vier klinischen Zentren durch: in Löwen in Belgien, in Leiden in den Niederlanden, in Göteborg in Schweden und in Ferrara in Italien. Die Studie wurde im Dezember 2009 begonnen und wird in der zweiten Hälfte des Jahres 2013 abgeschlossen werden. Die 18 teilnehmenden Duchenne-Jungen sind zwischen 5 und 16 Jahre alt. Es gibt 3 Jungen in jeder Dosierungsgruppe. Sie erhalten pro Woche subkutane Injektionen mit ansteigender Dosierung, 0,5-1, und 12 mg/kg. Ei- 18
19 nige der Jungen werden mit intravenösen Injektionen von 1,5, 5 und 12 mg/kg 5 Wochen lang nachdosiert. Dreizehn Wochen nach der Behandlung wird Muskelgewebe in Biopsien entnommen, um zu bestimmen, wie viel neues Dystrophin in den Muskelzellen entstanden ist. Außerdem werden andere Tests durchgeführt, um die Sicherheit, mögliche Nebenwirkungen und die Pharmakokinetik zu überprüfen. Wenn die Resultate dieser Studie der Phase II zeigen, dass das Skippen von Exon 44 genauso wirksam und sicher ist wie das Skippen von Exon 51, verlangen FDA und EMA vielleicht nicht eine zeitaufwendige und teure Studie der Phase III für dieses Exon 44, bevor sie beide Skipping- Medikamente zulassen. Skipping von anderen Exons. In verschiedenen Pressemitteilungen hat Prosensa angekündigt, dass vorklinische Arbeiten für das Skippen der vier Exons 45, 52, 53 und 55, die neben den Exons 51 und 44 ebenfalls auf der Prioritätenliste, siehe Seite 9, stehen, bald abgeschlossen sein werden. Die ersten klinischen Studien zum Skippen der Exons 45 und 53 werden 2013 beginnen, die Studien für die Exons 52 und 55 werden bald folgen. Sarepta plant ähnliche Studien zum Skippen der Exons 45, 50 und 53. Neugeborenenscreening und klinische Studie mit sehr jungen Duchenne-Patienten. GSK plant, im Jahr 2013 eine klinische Studie über das Skipping des Exons 51 bei Jungen zu beginnen, die jünger als 5 Jahre alt sind Da Exon-Skipping nur Muskelfasern behandeln kann, die noch vorhanden sind und von dem Dystrophie-Prozess noch nicht zu sehr geschädigt wurden, können verschwundene Muskelfasern nicht ersetzt werden. Aus diesem Grund könnte Exon-Skipping wirksamer bei Jungen sein, die noch keine Symptome haben und die noch genügend Muskeln haben bevor die Krankheit mit etwa drei Jahren sichtbar wird. Die beste Lösung wäre es, die Skipping-Behandlung im ersten Jahr nach der Geburt zu beginnen. Um diese Jungen zu finden, wäre ein Screening männlicher Neugeborener mit einem Suchtest auf sehr hohe Aktivitäten des Enzyms Creatinkinase, CK, nötig. Dabei wird ein trockener Blutfleck der Neugeborenen auf Filterpapier untersucht. Sehr hohe CK-Aktivitäten von mehr als U/L im Blut eines neugeborenen Jungen deuten auf Duchenne-Dystrophie oder eine andere muskuläre Erkrankung wie z.b. eine der Gliedergürteldystrophien hin. In einem Pilot-Screeningprogramm an Neugeborenen, das von der Gruppe um Jerry Mendell in Columbus im US-Bundesstaat Ohio durchgeführt wurde, war es sogar möglich, die Sequenz des Dystrophin-Gens in der DNA zu bestimmen, die man von den Leukozyten, den weißen Blutzellen in den trockenen Blutflecken der Jungen mit hohen CK-Aktivitäten, erhalten hatte (11). Man könnte damit nicht nur die Duchenne-Jungen gleich nach ihrer Geburt finden, sondern man wüsste auch kurz danach ihre Gen-Mutation und könnte innerhalb sehr kurzer Zeit eine Diagnose stellen. Eine wirksame Exon- Skipping-Therapie könnte dann sofort eingeleitet und ein Degenerieren der Muskeln gleich verhindert werden. Diese Duchenne-Jungen würden dann keine Duchenne-Muskeldystrophie haben! In naher Zukunft werden in vielen Staaten solche Duchenne Screening-Programme wahrscheinlich zusätzlich zu den schon bestehenden Neugeborenen-Untersuchungen derjenigen Krankheiten durchgeführt werden, die behandelt werden können. Der internationale Workshop des European Neuromuscular Center ENMC über Duchenne- Screening, der vom Dezember 2012 in Naarden nahe Amsterdam stattfand, wird die Akzeptanz für diese Art von frühen Untersuchungen erhöhen, sobald Drisapersen, das von Prosensa und GSK entwickelte Medikament zum Skippen von Exons 51, sich definitiv als sicher und wirksam erwiesen hat. Viele Leser meiner Berichte wissen sicherlich, dass ich 1974 ein privates Labor in meinem Haus in Breitnau, einem Dorf im Schwarzwald 30 km östlich von Freiburg, gegründet hatte und seitdem auf dem Gebiet der Muskeldystrophien arbeite. Von März 1977 bis November 2011 führte ich mit meinen Mitarbeitern in diesem Testlaboratorium Breitnau ein freiwilliges Früherkennungsprogramm auf Duchenne-Muskeldystrophie für ganz Deutschland durch. Zusammen mit Kollegen habe ich dieses Programm und den neuen Bioluminiszenz-Test zur Bestimmung der Creatinkinase in trockenen Blutflecken im Jahr 1986 beschrieben (12). Wir haben Jungen getestet, unter denen wir 155 mit Duchenne- (1:3.600) und 35 Jungen mit Becker- Muskeldystrophie (1:15.300) innerhalb ihrer ersten Lebenswochen fanden. Exon-Skipping mit Gentransfer. Die Wissenschaftler Luis García, Aurélie Goyenvalle, Dame Kay Davies und ihre Kollegen an den Universitäten in Versailles und Oxford arbeiten an einer Kombination des Exon-Skippings mit einer Gentherapie. Ziel ist es, die Muskelzellen dazu zu bringen, die Antisense-Oligos selbst zu erzeugen. Sie hoffen, dass nur eine Injektion von Viren notwendig sein wird, die die genetische Sequenz zur kontinuierlichen Produktion von Antisense-Oligos in die Muskelzellen transportieren. Ständige, sich wiederholende Injektionen von freien Antisense-Oligos während des möglicherweise verlängerten Lebens der Patienten wären dann nicht mehr nötig. Im Jahr 2004 haben die Wissenschaftler bereits den gentherapeutischen Teil dieses Verfahrens entwickelt, in dem sie die RNA-Antisense-Sequenzen an U7-snRNAs angefügt haben. Diese sind kleine RNAs, die Teil der Spleißosomen sind, der biochemische Maschinerie, die die 79 Exons im Kern zur aktiven mrna zusammensetzen, die dann die Information für das Protein Dystrophin enthält. Die veränderten U7-snRNAs wurden mit Vektoren, mit harmlosen adeno-assoziierten Viren, AAV, in die Muskelzellen transportiert, wo sie in die Zellkerne wandern, um dort das Exon-Skipping während des Spleiß- Prozesses zu veranlassen. Diese beladenen Viren wurden zunächst lokal in einzelne Muskeln von mdx-mäusen gespritzt, danach dann systemisch in den Blutkreislauf. In den Muskelzellen hat das Skipping des Exons 23 das Leseraster wieder hergestellt. Das neue, etwas kürzere Dystrophin trat in bis zu 80% der Fasern der behandelten Muskeln auf. Es wanderte 19
20 dann zu seiner normalen Position unterhalb der Zellmembranen und war dort mehr als ein Jahr stabil. Es gab keine Immunreaktionen. Die dystrophischen Prozesse in den mdx-muskeln, d.h. ihre beschleunigte Degeneration und Regeneration, kamen komplett zum Erliegen. Die mdx-mäuse, die systemisch behandelt wurden, entwickelten keine Muskelschäden, die normalerweise an nicht behandelten mdx-mäusen auftreten (13). Vor fünf Jahren wurde dieses U7-Gentransferverfahren angewendet, um Golden-Retriever-Hunde klinisch zu behandeln, die wirklich krank waren wie Duchenne-Patienten. Diese Hunde haben eine Mutation an der Spleißstelle des Exons 7, die durch ein Skipping der Exons 6 und 8 behoben werden kann. Die Verwendung der für Hunde adaptierten U7-snRNAs, die Antisense-Sequenzen gegen die Exons 6 und 8 enthielten, führte dazu, dass verkürztes Dystrophin in beinahe normalen Konzentrationen in vielen Muskeln gebildet wurde. Hierzu wurden Injektionen in die Muskeln vorgenommen und eine regionale, systemische Injektion in ein Bein, dessen Blutkreislauf mit einer Blutdruckmanschette blockiert war. Jetzt, fünf Jahre nach diesen Experimenten sind die langfristigen Ergebnisse dieser Behandlung von Adeline Vulin, Aurélie Goyenvalle, Luis García und ihren Mitarbeitern veröffentlicht worden (14). Nach dieser Zeit war das verkürzte Dystrophin in den 6 behandelten Hunden noch vorhanden, die Zahl der Fasern mit dem neuen Dystrophin hatte sich jedoch langsam verringert. Dies geschah nicht wegen einer Immunreaktion, sondern wahrscheinlich, weil es, wie bei der menschlichen Becker-Muskeldystrophie, zu einem langsam fortschreitenden dystrophischen Prozess kam. Der Hauptgrund ist jedoch wahrscheinlich darauf zurückzuführen, dass bei dem geretteten, verkürzten Dystrophin nicht nur das Exon 7 und die beiden geskippten Exons 6 und 8 fehlten, sondern aus unerklärlichen Gründen auch das Exon 9, das jedoch das Leseraster nicht verschiebt. In dem Protein fehlten also 158 Aminosäuren, die von den fehlenden Exons 6-9 definiert sind. Diese sind Teil der Struktur an einem Ende des Proteins, die es mit dem Actin-Netzwerk des Zellgerüsts der Muskelzellen verbindet. Da diese Verbindung dann nicht mehr perfekt ist, könnte dies zu der langsamen Degeneration der Muskeln beitragen. Die Autoren schlagen vor, dass dieses genetische Exon- Skipping als Beginn einer Langzeit-Therapie dienen könnte, die dann nach ein paar Jahren von normalen Exon- Skipping- Injektionen abgelöst werden könnte. Nachdem mit diesem Verfahren 2004 das Skippen des Exons 23 in mdx-mäusen möglich war, die aber nur wenig krank sind, wurde die gleiche Methode bei sogenannten doppel-ko-mäusen angewandt. Diese hatten weder Dystrophin noch Utrophin in ihren Muskeln und waren daher so krank wie die Duchenne-Jungen (15). Nach einer einzigen intravenösen Injektion des AAV-Virus, das die Antisense-Sequenzen an der U7-snRNA gegen das Exon 23 der Mäuse mitbrachte, wurden fast normale Konzentrationen von Dystrophin in allen Muskeln gefunden, auch in den Herzmuskeln. Dies führte zu einer deutlichen Verbesserung ihrer Muskelfunktionen, einer Normalisierung der Muskelstrukturen und zu einer bemerkenswerten Verlängerung ihrer Lebenszeit von ca. 10 Wochen auf mehr als 1 Jahr. Die Wissenschaftler haben jetzt spezifische U7snRNAs entwickelt, um Exons in menschlichen Dystrophin-Genen zu skippen, damit diese Strategie auch bei DMD-Patienten angewandt werden kann (16). Sie haben auch gezeigt, dass mehrere verschiedene U7snRNAs durch dieses AAV- Virus transportiert werden kann, die dann das gleichzeitige Skippen mehrerer Exons ermöglicht. Diese Arbeiten bedeuten einen wichtigen Schritt zur klinischen Anwendung an Patienten, die von Génethon zusammen mit dem Institut de Myologie und Forscherteams in Nantes für das Jahr 2015 geplant sind. Multiexon-Skipping. Annemiekes Liste mit 130 Skipping-Medikamenten (5) enthält 77 zum Skippen eines einzelnen Exons und 53, die zwei Exons skippen würden. Das bedeutet, dass 64% aller Patienten vom Skippen einzelner Exons profitieren würden, 19% bräuchten das Skippen von zwei Exons. Wie ich auf Seite 9 erwähnte, gibt es sieben Skippings auf den Prioritätenlisten von Prosensa/GSK und Sarepta, die zusammen 45,1% aller Patienten helfen würden. Es handelt sich um die Exons 44, 45, 50, 51, 52, 53 und 55. Nur einige wenige Arbeiten befassten sich bisher mit dem Skippen von zwei Exons, zwei benachbarten oder zwei getrennten. Es gibt noch keine klinischen Studien für Doppelskipping, da die drei aktiven Firmen auf diesem Gebiet mit großem finanziellem Engagement sich vorerst auf die Entwicklung des Skippings der einzelnen Exons auf ihren Prioritätslisten konzentrieren. Wenn diese sich als sicher und wirksam erweisen und ohne Verzögerung zugelassen werden, können wir hoffen, dass die Skipping-Medikamente für die weniger häufigen oder seltenen und komplizierten Mutationen nicht die gleiche Zahl von Studien wie bisher durchlaufen müssen. Für ihre Entwicklung wäre dann wesentlich weniger Geld und Zeit nötig. Erster Versuch zum Skippen der Exons 45 bis 55 mit 2 O-Methylen. Es gibt jedoch eine Ausnahme zu dem eben beschriebenen Szenario. Es geht um das Skippen von mehr als zwei Exons mit einem Gemisch, einem Cocktail, von mehreren Antisense-Oligos. Im Jahr 2007 haben Christophe Beroud und seine Mitarbeiter an der Universität von Montpellier in Südfrankreich ihre Prognose veröffentlicht (17), dass das gleichzeitige Skippen der 11 Exons 45 bis 55 zu einem verkürzten Dystrophin führen würde, das eine Becker-Dystrophie mit sehr milden oder gar keinen Symptomen in bis zu 63% aller Duchenne-Patienten zur Folge hätte. Tatsächlich wurde bei einigen Becker-Patienten eine natürliche Deletion der Exons 45 bis 55 beschrieben. Diese Patienten hatten fast keine Beeinträchtigungen. Im Jahr 2008 haben Annemieke Aartsma-Rus und ihre Kollegen versucht, in Zellkulturen diese 11 Exons von der Dystrophin mrna einer gesunden Person und von 20
Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten.
 Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten. Wie bezeichnet man den Strang der DNA- Doppelhelix, der die
Was ist der Promotor? Antwort: Eine spezielle Nucleotidsequenz auf der DNA, an der die RNA-Polymerase bindet um die Transkription zu starten. Wie bezeichnet man den Strang der DNA- Doppelhelix, der die
ERBKRANKHEITEN (mit den Beispielen Albinismus, Chorea Huntington, Bluterkrankheit u. Mitochondriopathie)
 ERBKRANKHEITEN (mit den Beispielen Albinismus, Chorea Huntington, Bluterkrankheit u. Mitochondriopathie) Als Erbkrankheit werden Erkrankungen und Besonderheiten bezeichnet, die entweder durch ein Gen (monogen)
ERBKRANKHEITEN (mit den Beispielen Albinismus, Chorea Huntington, Bluterkrankheit u. Mitochondriopathie) Als Erbkrankheit werden Erkrankungen und Besonderheiten bezeichnet, die entweder durch ein Gen (monogen)
3.5 Moderne Genetik - Vorgänge
 3.5 Moderne Genetik - Vorgänge Der genetische Code Jedes Gen besteht aus sogenannten Basentriplets. Das ist eine Sequenz von drei aufeinanderfolgenden Nukleinbasen, die für eine bestimmte Aminosäure stehen.
3.5 Moderne Genetik - Vorgänge Der genetische Code Jedes Gen besteht aus sogenannten Basentriplets. Das ist eine Sequenz von drei aufeinanderfolgenden Nukleinbasen, die für eine bestimmte Aminosäure stehen.
Autosomal-dominanter Erbgang
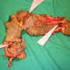 12 Autosomal-dominanter Erbgang Bearbeitetes Informationsblatt herausgegeben vom Guy s and St. Thomas Hospital, London und dem London IDEAS Genetic Knowledge Park, entsprechend deren Qualitätsstandards.
12 Autosomal-dominanter Erbgang Bearbeitetes Informationsblatt herausgegeben vom Guy s and St. Thomas Hospital, London und dem London IDEAS Genetic Knowledge Park, entsprechend deren Qualitätsstandards.
Interview mit Dr. Annemieke Aartsma-Rus.
 Exon-Skipping zur Therapie der Duchenne-Muskeldystrophie. Interview mit Dr. Annemieke Aartsma-Rus. Universität Leiden, Medizinisches Zentrum, Niederlande. Am 1. April 2011 beim 20. Kongreß des Wissenschaftlichen
Exon-Skipping zur Therapie der Duchenne-Muskeldystrophie. Interview mit Dr. Annemieke Aartsma-Rus. Universität Leiden, Medizinisches Zentrum, Niederlande. Am 1. April 2011 beim 20. Kongreß des Wissenschaftlichen
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Die gentechnische Produktion von Insulin - Selbstlerneinheit zur kontextorientierten Wiederholung der molekularen Genetik Das komplette
Was machen unsere Gene. Ein paar Gedanken für Nichtmediziner
 Was machen unsere Gene. Ein paar Gedanken für Nichtmediziner Zum Verständnis der Arbeitsweise der Gene sei zunächst eine Frage gestellt: Wie entsteht in einem Vogelei, das ausgebrütet wird, der Schnabel
Was machen unsere Gene. Ein paar Gedanken für Nichtmediziner Zum Verständnis der Arbeitsweise der Gene sei zunächst eine Frage gestellt: Wie entsteht in einem Vogelei, das ausgebrütet wird, der Schnabel
Teil 1: Exon-Skipping.
 Wege der Forschung nach einer Therapie der Duchenne-Muskeldystrophie. Teil 1: Exon-Skipping. Veröffentlicht am 15. Juli 2009. Dieser Bericht über Exon-Skipping, die am weitesten vorangeschrittene genetische
Wege der Forschung nach einer Therapie der Duchenne-Muskeldystrophie. Teil 1: Exon-Skipping. Veröffentlicht am 15. Juli 2009. Dieser Bericht über Exon-Skipping, die am weitesten vorangeschrittene genetische
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit
 In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
In den Proteinen der Lebewesen treten in der Regel 20 verschiedene Aminosäuren auf. Deren Reihenfolge muss in der Nucleotidsequenz der mrna und damit in der Nucleotidsequenz der DNA verschlüsselt (codiert)
Pharmazeutische Biologie WS2011/2012. Das neue Paradigma: Personalisierte Medizin
 2. Vorlesung Pharmazeutische Biologie WS2011/2012 Das neue Paradigma: Personalisierte Medizin Prof. Theo Dingermann Institut für Pharmazeutische Biologie Biozentrum Max-von Laue-Str. 9 60438 Frankfurt
2. Vorlesung Pharmazeutische Biologie WS2011/2012 Das neue Paradigma: Personalisierte Medizin Prof. Theo Dingermann Institut für Pharmazeutische Biologie Biozentrum Max-von Laue-Str. 9 60438 Frankfurt
Leben mit einem Lambert-Eaton Myasthenischen Syndrom
 Leben mit einem Lambert-Eaton Myasthenischen Syndrom Bei Ihnen ist ein Lambert-Eaton Myasthenisches Syndrom, kurz LEMS, diagnostiziert worden. Dieses Merkblatt soll Sie und Ihre Angehörigen darüber informieren,
Leben mit einem Lambert-Eaton Myasthenischen Syndrom Bei Ihnen ist ein Lambert-Eaton Myasthenisches Syndrom, kurz LEMS, diagnostiziert worden. Dieses Merkblatt soll Sie und Ihre Angehörigen darüber informieren,
Prosensas Fortsetzung der Entwicklung des Exon-51 Skippings mit Drisapersen nach der enttäuschenden klinischen Phase-III Prüfung.
 Ein neuer Forschungsbericht von April 2015 Dr. rer. nat. Günter Scheuerbrandt Prosensas Fortsetzung der Entwicklung des Exon-51 Skippings mit Drisapersen nach der enttäuschenden klinischen Phase-III Prüfung.
Ein neuer Forschungsbericht von April 2015 Dr. rer. nat. Günter Scheuerbrandt Prosensas Fortsetzung der Entwicklung des Exon-51 Skippings mit Drisapersen nach der enttäuschenden klinischen Phase-III Prüfung.
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016
 Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 2 (06.06. 10.06.) DNA-Schäden, Mutationen und Reparatur 1.
Biologie I/B: Klassische und molekulare Genetik, molekulare Grundlagen der Entwicklung Theoretische Übungen SS 2016 Fragen für die Übungsstunde 2 (06.06. 10.06.) DNA-Schäden, Mutationen und Reparatur 1.
Grundlegendes zur Genetik
 Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Die genetische 'Grauzone' der Huntington Krankheit: Was bedeutet
Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Die genetische 'Grauzone' der Huntington Krankheit: Was bedeutet
16. Biomoleküle : Nucleinsäuren
 Inhalt Index 16. Biomoleküle : Nucleinsäuren Die gesamte Erbinformation ist in den Desoxyribonucleinsäuren (DNA) enthalten. Die Übersetzung dieser Information in die Synthese der Proteine wird von den
Inhalt Index 16. Biomoleküle : Nucleinsäuren Die gesamte Erbinformation ist in den Desoxyribonucleinsäuren (DNA) enthalten. Die Übersetzung dieser Information in die Synthese der Proteine wird von den
SCHLAGANFALL RATGEBER
 SCHLAGANFALL RATGEBER 0 Impressum Zarenga GmbH, Bonn 2015 Zarenga GmbH, Pfaffenweg 15, 53227 Bonn Alle Rechte sind vorbehalten. Dieses Buch, einschließlich seiner einzelnen Teile ist urheberrechtlich geschützt.
SCHLAGANFALL RATGEBER 0 Impressum Zarenga GmbH, Bonn 2015 Zarenga GmbH, Pfaffenweg 15, 53227 Bonn Alle Rechte sind vorbehalten. Dieses Buch, einschließlich seiner einzelnen Teile ist urheberrechtlich geschützt.
USHER SYMPOSIUM IN MAINZ
 (Mariya Moosajee) Okay. Meine Damen und Herren, ich möchte mich auch ganz herzlich dafür bedanken, dass ich heute hier an dieser Konferenz teilnehmen darf. Die letzten paar Tage waren sehr, sehr inspirierend
(Mariya Moosajee) Okay. Meine Damen und Herren, ich möchte mich auch ganz herzlich dafür bedanken, dass ich heute hier an dieser Konferenz teilnehmen darf. Die letzten paar Tage waren sehr, sehr inspirierend
Wie funktioniert Muskelaufbau? Eine Reise in die Welt des Muskels.
 Wie funktioniert Muskelaufbau? Eine Reise in die Welt des Muskels. Wie funktioniert Muskelaufbau? Wie funktioniert Muskelaufbau also wirklich. Immer wieder hört man Märchen wie zum Beispiel, dass Muskeln
Wie funktioniert Muskelaufbau? Eine Reise in die Welt des Muskels. Wie funktioniert Muskelaufbau? Wie funktioniert Muskelaufbau also wirklich. Immer wieder hört man Märchen wie zum Beispiel, dass Muskeln
Chromosomale Translokationen
 12 Unique - The Rare Chromosome Disorder Support Group in the UK Service-Telefon: + 44 (0) 1883 330766 Email:info@rarechromo.org Web:www.rarechromo.org Chromosomale Translokationen Orphanet Frei zugängliche
12 Unique - The Rare Chromosome Disorder Support Group in the UK Service-Telefon: + 44 (0) 1883 330766 Email:info@rarechromo.org Web:www.rarechromo.org Chromosomale Translokationen Orphanet Frei zugängliche
Erstellen eines Referates in Word
 Seite 1 von 9 Erstellen eines Referates in Word Von Antje Borchers Oftmals bekommt man ein Thema zugeteilt über das man ein Referat halten soll. Aber, wie macht man das eigentlich? 1.) Informationen sammeln
Seite 1 von 9 Erstellen eines Referates in Word Von Antje Borchers Oftmals bekommt man ein Thema zugeteilt über das man ein Referat halten soll. Aber, wie macht man das eigentlich? 1.) Informationen sammeln
Der molekulare Bauplan des Lebens; biologische Nano- und Mikrobausteine von Lebewesen. RNA und DNA als sich selbst replizierende Informationsspeicher
 Der molekulare Bauplan des Lebens; biologische Nano- und Mikrobausteine von Lebewesen RNA und DNA als sich selbst replizierende Informationsspeicher Quelle: Biochemie, J.M. Berg, J.L. Tymoczko, L. Stryer,
Der molekulare Bauplan des Lebens; biologische Nano- und Mikrobausteine von Lebewesen RNA und DNA als sich selbst replizierende Informationsspeicher Quelle: Biochemie, J.M. Berg, J.L. Tymoczko, L. Stryer,
CRISPR/Cas9. Breakthrough to genome editing. Science 18. Dezember 2015
 CRISPR/Cas9 Breakthrough to genome editing Durchbruch beim Bearbeiten von Genen Das wichtigste wissenschaftliche Ergebnis im Jahr 2015 Science 18. Dezember 2015 Ich werde zuerst über Duchenne-Muskeldystrophie
CRISPR/Cas9 Breakthrough to genome editing Durchbruch beim Bearbeiten von Genen Das wichtigste wissenschaftliche Ergebnis im Jahr 2015 Science 18. Dezember 2015 Ich werde zuerst über Duchenne-Muskeldystrophie
GESUNDHEIT ANDERS BETRACHTET
 GESUNDHEIT ANDERS BETRACHTET GESUND WERDEN AUF ANDERE WEISE 2 Durchblutung Gewebereparatur Entzündung Schmerz Gesund zu sein ist für die meisten Menschen etwas ganz Selbstverständliches. Doch manchmal
GESUNDHEIT ANDERS BETRACHTET GESUND WERDEN AUF ANDERE WEISE 2 Durchblutung Gewebereparatur Entzündung Schmerz Gesund zu sein ist für die meisten Menschen etwas ganz Selbstverständliches. Doch manchmal
Eukaryotische messenger-rna
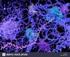 Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende u.u. nicht-codierende Bereiche (Introns) Spleißen von prä-mrna Viele Protein-codierende Gene in Eukaryoten sind durch nicht-codierende
Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende u.u. nicht-codierende Bereiche (Introns) Spleißen von prä-mrna Viele Protein-codierende Gene in Eukaryoten sind durch nicht-codierende
Wir sollen erarbeiten, wie man mit Hilfe der Mondentfernung die Entfernung zur Sonne bestimmen kann.
 Expertengruppenarbeit Sonnenentfernung Das ist unsere Aufgabe: Wir sollen erarbeiten, wie man mit Hilfe der Mondentfernung die Entfernung zur Sonne bestimmen kann. Konkret ist Folgendes zu tun: Lesen Sie
Expertengruppenarbeit Sonnenentfernung Das ist unsere Aufgabe: Wir sollen erarbeiten, wie man mit Hilfe der Mondentfernung die Entfernung zur Sonne bestimmen kann. Konkret ist Folgendes zu tun: Lesen Sie
Material zur der Prüfung im Fach Biologie
 Material zur der Prüfung im Fach Biologie 1) Empfohlene Literatur Duden: Basiswissen Schule, Biologie-Abitur, Duden-Verlag Linder: Biologie, Schroedel-Verlag Natura: Biologie für Gymnasien, 3b NRW, Klett-Verlag
Material zur der Prüfung im Fach Biologie 1) Empfohlene Literatur Duden: Basiswissen Schule, Biologie-Abitur, Duden-Verlag Linder: Biologie, Schroedel-Verlag Natura: Biologie für Gymnasien, 3b NRW, Klett-Verlag
Übungsklausur Auswertung/Statistik. Dr. Yvonne Lorat
 Übungsklausur Auswertung/Statistik Dr. Yvonne Lorat Achten Sie bei Multiple-Choice-Fragen auf die Fragestellung: Welche Aussage trifft nicht zu? Hier ist nur eine Aussage falsch! Alle anderen sind richtig.
Übungsklausur Auswertung/Statistik Dr. Yvonne Lorat Achten Sie bei Multiple-Choice-Fragen auf die Fragestellung: Welche Aussage trifft nicht zu? Hier ist nur eine Aussage falsch! Alle anderen sind richtig.
Translation benötigt trnas und Ribosomen. Genetischer Code. Initiation Elongation Termination
 8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
Translation benötigt trnas und Ribosomen. Genetischer Code. Initiation Elongation Termination
 8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
8. Translation Konzepte: Translation benötigt trnas und Ribosomen Genetischer Code Initiation Elongation Termination 1. Welche Typen von RNAs gibt es und welches sind ihre Funktionen? mouse huma n bacter
Antwort: 2.Uracil. Antwort: 2. durch Wasserstoffverbindungen. Adenin, Cystein und Guanin kommen alle in der RNA und DNA vor.
 Antwort: 2.Uracil Adenin, Cystein und Guanin kommen alle in der RNA und DNA vor. Thymin kommt nur in der DNA vor; Uracil nimmt seinen Platz in den RNA- Molekülen ein. Antwort: 2. durch Wasserstoffverbindungen
Antwort: 2.Uracil Adenin, Cystein und Guanin kommen alle in der RNA und DNA vor. Thymin kommt nur in der DNA vor; Uracil nimmt seinen Platz in den RNA- Molekülen ein. Antwort: 2. durch Wasserstoffverbindungen
Leichter atmen mit. Pulmonx-Ventilen
 Leichter atmen mit Pulmonx-Ventilen Was ist ein Emphysem? Ein Emphysem ist eine schwere, chronische Krankheit, die zu Kurzatmigkeit führt und die Lebensqualität einschränkt. Weltweit leben mehr als 30
Leichter atmen mit Pulmonx-Ventilen Was ist ein Emphysem? Ein Emphysem ist eine schwere, chronische Krankheit, die zu Kurzatmigkeit führt und die Lebensqualität einschränkt. Weltweit leben mehr als 30
Exon Skipping, eine Therapie für Duchenne Muskeldystrophie.
 Exon Skipping, eine Therapie für Duchenne Muskeldystrophie. Interview mit Dr. Gerard Platenburg, Präsident der Firma Prosensa B.V. Leiden, Holland. Dieses Interview habe ich, Dr. Günter Scheuerbrandt,
Exon Skipping, eine Therapie für Duchenne Muskeldystrophie. Interview mit Dr. Gerard Platenburg, Präsident der Firma Prosensa B.V. Leiden, Holland. Dieses Interview habe ich, Dr. Günter Scheuerbrandt,
Känguru der Mathematik 2014 Gruppe Benjamin (5. und 6. Schulstufe) Österreich - 20.3.2014
 Känguru der Mathematik 2014 Gruppe Benjamin (5. und 6. Schulstufe) Österreich - 20.3.2014-3 Punkte Beispiele - 1. Arno legt mit 8 Karten das Wort KANGAROO. Einige Karten liegen aber verdreht. Durch zweimaliges
Känguru der Mathematik 2014 Gruppe Benjamin (5. und 6. Schulstufe) Österreich - 20.3.2014-3 Punkte Beispiele - 1. Arno legt mit 8 Karten das Wort KANGAROO. Einige Karten liegen aber verdreht. Durch zweimaliges
Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte)
 Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Datum: 06.12.2010 Name: Matrikel-Nr.: Vorname: Studiengang: Bioinformatik Biochemie (für Bioinformatiker) WS 2010/2011, 1. Klausur (50 Punkte) Modulnr.: FMI-BI0027 iermit bestätige ich meine Prüfungstauglichkeit.
Fettmoleküle und das Gehirn
 Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Spezielle "Gehirn Fett Injektion hilft Huntington Mäusen Direktes
Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Spezielle "Gehirn Fett Injektion hilft Huntington Mäusen Direktes
Wirkstoff: Natriumchondroitinsulfat
 Gebrauchsinformation: Information für Anwender CONDROSULF 800 mg - Tabletten Wirkstoff: Natriumchondroitinsulfat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Gebrauchsinformation: Information für Anwender CONDROSULF 800 mg - Tabletten Wirkstoff: Natriumchondroitinsulfat Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Einnahme dieses
Leichter atmen mit. Pulmonx-Ventilen
 Leichter atmen mit Pulmonx-Ventilen Was ist ein Emphysem? Ein Emphysem ist eine schwere, chronische Krankheit, die zu Kurzatmigkeit führt und die Lebensqualität einschränkt. Weltweit leben mehr als 30
Leichter atmen mit Pulmonx-Ventilen Was ist ein Emphysem? Ein Emphysem ist eine schwere, chronische Krankheit, die zu Kurzatmigkeit führt und die Lebensqualität einschränkt. Weltweit leben mehr als 30
Extra: Schilddrüsenprobleme. Alle wichtigen Heilmethoden Das können Sie selbst tun. Gesunde Rezepte für die Schilddrüse. natürlich behandeln
 DR. ANDREA FLEMMER Schilddrüsenprobleme natürlich behandeln Alle wichtigen Heilmethoden Das können Sie selbst tun Extra: Gesunde Rezepte für die Schilddrüse Krankheiten und Probleme Schilddrüsenerkrankungen
DR. ANDREA FLEMMER Schilddrüsenprobleme natürlich behandeln Alle wichtigen Heilmethoden Das können Sie selbst tun Extra: Gesunde Rezepte für die Schilddrüse Krankheiten und Probleme Schilddrüsenerkrankungen
9.) Wie heißen die kurzen RNA-Moleküle, mit deren Hilfe die Polymerase die Replikation der DNA starten kann? a) Starter b) Primer c) Beginner
 Lernkontrolle M o d u l 1 A w i e... A n k r e u z e n! 1.) Wie viele Chromosomen besitzt eine menschliche Körperzelle? a) 23 b) 46 c) 44 2.) In welchem Zellorganell befindet sich die DNA? a) Zellkern
Lernkontrolle M o d u l 1 A w i e... A n k r e u z e n! 1.) Wie viele Chromosomen besitzt eine menschliche Körperzelle? a) 23 b) 46 c) 44 2.) In welchem Zellorganell befindet sich die DNA? a) Zellkern
Modul Biologische Grundlagen Kapitel I.2 Grundbegriffe der Genetik
 Frage Was sind Fachbegriffe zum Thema Grundbegriffe der Genetik? Antwort - Gene - Genotyp - Phänotyp - Genom - Dexoxyribonucleinsäure - Träger genetischer Information - Nukleotide - Basen - Peptid - Start-Codon
Frage Was sind Fachbegriffe zum Thema Grundbegriffe der Genetik? Antwort - Gene - Genotyp - Phänotyp - Genom - Dexoxyribonucleinsäure - Träger genetischer Information - Nukleotide - Basen - Peptid - Start-Codon
Posttranskriptionale RNA-Prozessierung
 Posttranskriptionale RNA-Prozessierung Spaltung + Modifikation G Q Spleissen + Editing U UUU Prozessierung einer prä-trna Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende
Posttranskriptionale RNA-Prozessierung Spaltung + Modifikation G Q Spleissen + Editing U UUU Prozessierung einer prä-trna Eukaryotische messenger-rna Cap-Nukleotid am 5 -Ende Polyadenylierung am 3 -Ende
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Betahistine Sandoz 8 mg Tabletten Betahistine Sandoz 16 mg Tabletten. Betahistindihydrochlorid
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Betahistine Sandoz 8 mg Tabletten Betahistine Sandoz 16 mg Tabletten Betahistindihydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Betahistine Sandoz 8 mg Tabletten Betahistine Sandoz 16 mg Tabletten Betahistindihydrochlorid Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
IV. Übungsaufgaben für die Jahrgangstufe 9 & 10
 IV. Übungsaufgaben für die Jahrgangstufe 9 & 10 Von der Erbanlage zum Erbmerkmal: 34) Welche Aufgaben haben Chromosomen? 35) Zeichne und benenne die Teile eines Chromosoms, wie sie im Lichtmikroskop während
IV. Übungsaufgaben für die Jahrgangstufe 9 & 10 Von der Erbanlage zum Erbmerkmal: 34) Welche Aufgaben haben Chromosomen? 35) Zeichne und benenne die Teile eines Chromosoms, wie sie im Lichtmikroskop während
Jahrestagung, 13. bis 16. Juli 2006 in Cincinnati/Ohio, USA Duchenne-Muskeldystrophie: Die Wege zur Therapie werden kürzer.
 Jahrestagung, 13. bis 16. Juli 2006 in Cincinnati/Ohio, USA Duchenne-Muskeldystrophie: Die Wege zur Therapie werden kürzer. Face it! Live it! Change it! Dies war das Motto der Jahrestagung des Parent Project
Jahrestagung, 13. bis 16. Juli 2006 in Cincinnati/Ohio, USA Duchenne-Muskeldystrophie: Die Wege zur Therapie werden kürzer. Face it! Live it! Change it! Dies war das Motto der Jahrestagung des Parent Project
Soll ich am Mammographie-Screening-Programm teilnehmen?
 Soll ich am Mammographie-Screening-Programm teilnehmen? Eine Entscheidungshilfe für Frauen im Alter von 50. Warum soll ich mich entscheiden, ob ich am Mammographie-Screening- Programm teilnehme? In Deutschland
Soll ich am Mammographie-Screening-Programm teilnehmen? Eine Entscheidungshilfe für Frauen im Alter von 50. Warum soll ich mich entscheiden, ob ich am Mammographie-Screening- Programm teilnehme? In Deutschland
5. Endoplasmatisches Reticulum und Golgi-Apparat
 5. Endoplasmatisches Reticulum und Golgi-Apparat Institut für medizinische Physik und Biophysik Ramona Wesselmann Endoplasmatisches Reticulum Umfangreiches Membransystem endoplasmatisch im Cytoplasma reticulum
5. Endoplasmatisches Reticulum und Golgi-Apparat Institut für medizinische Physik und Biophysik Ramona Wesselmann Endoplasmatisches Reticulum Umfangreiches Membransystem endoplasmatisch im Cytoplasma reticulum
Algorithmus Sortieren von Zahlen (aufsteigend)
 Hausaufgabe https://de.wikipedia.org/wiki/dualsystem http://de.wikipedia.org/ieee_754 (Darstellung von Gleitkommazahlen) http://de.wikipedia.org/wiki/wurzel_(mat hematik)#berechnung - lesen, verstehen
Hausaufgabe https://de.wikipedia.org/wiki/dualsystem http://de.wikipedia.org/ieee_754 (Darstellung von Gleitkommazahlen) http://de.wikipedia.org/wiki/wurzel_(mat hematik)#berechnung - lesen, verstehen
Terminplanungstool Foodle
 VERSION: 1.0 STATUS: fertiggestellt VERTRAULICHKEIT: öffentlich STAND: 14.04.2015 INHALTSVERZEICHNIS 1 ALLGEMEINE INFORMATIONEN... 3 2 TERMINPLAN ERSTELLEN... 4 2.1 Terminplan beschreiben... 5 2.2 Termine
VERSION: 1.0 STATUS: fertiggestellt VERTRAULICHKEIT: öffentlich STAND: 14.04.2015 INHALTSVERZEICHNIS 1 ALLGEMEINE INFORMATIONEN... 3 2 TERMINPLAN ERSTELLEN... 4 2.1 Terminplan beschreiben... 5 2.2 Termine
Zudem wird er mithilfe der grundlegenden Flechttechniken keine speziellen Anleitungen mehr benötigen, um mit mehr oder weniger Strängen zu flechten.
 Einfache Flechtanleitungen und Flechttechniken Grundsätzlich ist es nicht schwer, zu flechten. Dies liegt daran, dass die Flechtmuster jeweils auf einem einfachen Schema basieren und dieses Schema auf
Einfache Flechtanleitungen und Flechttechniken Grundsätzlich ist es nicht schwer, zu flechten. Dies liegt daran, dass die Flechtmuster jeweils auf einem einfachen Schema basieren und dieses Schema auf
Handbuch ECDL 2003 Professional Modul 3: Kommunikation Aufgaben annehmen und zuweisen
 Handbuch ECDL 2003 Professional Modul 3: Kommunikation Aufgaben annehmen und zuweisen Dateiname: ecdl_p3_03_02_documentation.doc Speicherdatum: 08.12.2004 ECDL 2003 Professional Modul 3 Kommunikation
Handbuch ECDL 2003 Professional Modul 3: Kommunikation Aufgaben annehmen und zuweisen Dateiname: ecdl_p3_03_02_documentation.doc Speicherdatum: 08.12.2004 ECDL 2003 Professional Modul 3 Kommunikation
Molekularbiologie 6c Proteinbiosynthese. Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird
 Molekularbiologie 6c Proteinbiosynthese Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird 1 Übersicht: Vom Gen zum Protein 1. 2. 3. 2 Das Dogma
Molekularbiologie 6c Proteinbiosynthese Bei der Proteinbiosynthese geht es darum, wie die Information der DNA konkret in ein Protein umgesetzt wird 1 Übersicht: Vom Gen zum Protein 1. 2. 3. 2 Das Dogma
Mathematische Funktionen
 Mathematische Funktionen Viele Schüler können sich unter diesem Phänomen überhaupt nichts vorstellen, und da zusätzlich mit Buchstaben gerechnet wird, erzeugt es eher sogar Horror. Das ist jedoch gar nicht
Mathematische Funktionen Viele Schüler können sich unter diesem Phänomen überhaupt nichts vorstellen, und da zusätzlich mit Buchstaben gerechnet wird, erzeugt es eher sogar Horror. Das ist jedoch gar nicht
Der Ratgeber mit Informationen und Tipps rund ums Thema.
 Der Ratgeber mit Informationen und Tipps rund ums Thema. 2 Liebe Leserin, lieber Leser Verstopfung Verstopfung ist längst eine ernstzunehmende Volkskrankheit geworden und für die überwiegende Mehrzahl
Der Ratgeber mit Informationen und Tipps rund ums Thema. 2 Liebe Leserin, lieber Leser Verstopfung Verstopfung ist längst eine ernstzunehmende Volkskrankheit geworden und für die überwiegende Mehrzahl
Es ist die Zeit gekommen, zu verstehen, wie es zur Proteinbiosynthese kommt?! Wobei jeweils eine AS von 3 Basen codiert wird..
 Proteinbiosynthese Es ist die Zeit gekommen, zu verstehen, wie es zur Proteinbiosynthese kommt?! Alle Proteine, sind über die DNA codiert Wobei jeweils eine AS von 3 Basen codiert wird.. GENETISCHER CODE
Proteinbiosynthese Es ist die Zeit gekommen, zu verstehen, wie es zur Proteinbiosynthese kommt?! Alle Proteine, sind über die DNA codiert Wobei jeweils eine AS von 3 Basen codiert wird.. GENETISCHER CODE
Zustimmungserklärung für Jugendliche im Alter von 10 bis 18 Jahren
 Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Zustimmungserklärung für Jugendliche im Alter von 10 bis 18 Jahren Wir bitten Dich an einer wissenschaftlichen Studie mit
Medizinischen Klinik und Poliklinik III Direktor: Prof. Dr. med. Stefan Bornstein Zustimmungserklärung für Jugendliche im Alter von 10 bis 18 Jahren Wir bitten Dich an einer wissenschaftlichen Studie mit
6.2 Elektromagnetische Wellen
 6.2 Elektromagnetische Wellen Im vorigen Kapitel wurde die Erzeugung von elektromagnetischen Schwingungen und deren Eigenschaften untersucht. Mit diesem Wissen ist es nun möglich die Entstehung von elektromagnetischen
6.2 Elektromagnetische Wellen Im vorigen Kapitel wurde die Erzeugung von elektromagnetischen Schwingungen und deren Eigenschaften untersucht. Mit diesem Wissen ist es nun möglich die Entstehung von elektromagnetischen
Vorlesung Molekulare Humangenetik
 Vorlesung Molekulare Humangenetik WS 2013/2014 Dr. Shamsadin DNA-RNA-Protein Allgemeines Prüfungen o. Klausuren als indiv. Ergänzung 3LP benotet o. unbenotet Seminar Block 2LP Vorlesung Donnerstags 14-16
Vorlesung Molekulare Humangenetik WS 2013/2014 Dr. Shamsadin DNA-RNA-Protein Allgemeines Prüfungen o. Klausuren als indiv. Ergänzung 3LP benotet o. unbenotet Seminar Block 2LP Vorlesung Donnerstags 14-16
Meinungen der Bürgerinnen und Bürger in Hamburg zur Bewerbung um die Austragung der Olympischen Spiele 2024
 Meinungen der Bürgerinnen und Bürger in Hamburg zur Bewerbung um die Austragung der Olympischen Spiele 2024 November 2015 q5600.02/32437 Le forsa Politik- und Sozialforschung GmbH Büro Berlin Schreiberhauer
Meinungen der Bürgerinnen und Bürger in Hamburg zur Bewerbung um die Austragung der Olympischen Spiele 2024 November 2015 q5600.02/32437 Le forsa Politik- und Sozialforschung GmbH Büro Berlin Schreiberhauer
Hören mit High-Tech. HNO-Klinik der Medizinischen Hochschule Hannover Hörzentrum Hannover. Direktor: Prof. Dr. Th. Lenarz
 Hören mit High-Tech HNO-Klinik der Medizinischen Hochschule Hannover Hörzentrum Hannover Direktor: Prof. Dr. Th. Lenarz Mitarbeiter im Ideenpark: Prof. Dr. med. A. Lesinski-Schiedat, Dr. A. Büchner, S.
Hören mit High-Tech HNO-Klinik der Medizinischen Hochschule Hannover Hörzentrum Hannover Direktor: Prof. Dr. Th. Lenarz Mitarbeiter im Ideenpark: Prof. Dr. med. A. Lesinski-Schiedat, Dr. A. Büchner, S.
Ergotherapeutische Befunderhebung
 Ergotherapeutische Befunderhebung.1 ICF als Grundlage der ergotherapeutischen Befunderhebung 24.2 Wie kann eine ergothera-peutische Befunderhebung bei demenzkranken Menschen aussehen? 25. Bogen zur ergotherapeutischen
Ergotherapeutische Befunderhebung.1 ICF als Grundlage der ergotherapeutischen Befunderhebung 24.2 Wie kann eine ergothera-peutische Befunderhebung bei demenzkranken Menschen aussehen? 25. Bogen zur ergotherapeutischen
5. Was ist der Zweck der Studie der Phase II-Palovarotene?
 PALOVAROTENE 1. Was ist Palovarotene? ANTWORT: Palovarotene ist ein Retinoic Säure-Gamma (RARγ)-Rezeptoragonist und ist eine Klasse von Verbindungen genannt systemische Retinoide. Diese Verbindungen haben
PALOVAROTENE 1. Was ist Palovarotene? ANTWORT: Palovarotene ist ein Retinoic Säure-Gamma (RARγ)-Rezeptoragonist und ist eine Klasse von Verbindungen genannt systemische Retinoide. Diese Verbindungen haben
Gebrauchsinformation: Informationen für den Anwender. Lora-ADGC. Wirkstoff: Loratadin 10 mg, Tabletten
 Gebrauchsinformation: Informationen für den Anwender Lora-ADGC Wirkstoff: Loratadin 10 mg, Tabletten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für
Gebrauchsinformation: Informationen für den Anwender Lora-ADGC Wirkstoff: Loratadin 10 mg, Tabletten Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige Informationen für
PREISE UND PREISLISTEN UNTER ORGAMAX BEARBEITEN
 PREISE UND PREISLISTEN UNTER ORGAMAX BEARBEITEN Inhalt 1 Einführung... 1 2 Kundenspezifische Preise für bestimmte Artikel hinterlegen... 1 3 Anlegen einer Preisliste... 5 4 Bearbeitung von Preislisten:
PREISE UND PREISLISTEN UNTER ORGAMAX BEARBEITEN Inhalt 1 Einführung... 1 2 Kundenspezifische Preise für bestimmte Artikel hinterlegen... 1 3 Anlegen einer Preisliste... 5 4 Bearbeitung von Preislisten:
Übungsaufgabe zum Thema Angebot und Nachfrage. Anzahl der nachgefragten Menge (pro Jahr in 10g Dosen)
 Übungsaufgabe zum Thema Angebot und Nachfrage Die Nachfolgende Tabelle zeigt den Preis an Schnupftabak sowie das Angebot und die Nachfrage: Preise für 10 g in Euro Anzahl der nachgefragten Menge (pro Jahr
Übungsaufgabe zum Thema Angebot und Nachfrage Die Nachfolgende Tabelle zeigt den Preis an Schnupftabak sowie das Angebot und die Nachfrage: Preise für 10 g in Euro Anzahl der nachgefragten Menge (pro Jahr
Ertragseinbußen durch Herbizidabdrift von Mais auf Spargel verhindern
 Ertragseinbußen durch Herbizidabdrift von Mais auf Spargel verhindern In den letzten Jahren werden gehäuft Schäden an Spargel sichtbar, die durch Abdrift spezieller Maisherbizide verursacht werden. Dabei
Ertragseinbußen durch Herbizidabdrift von Mais auf Spargel verhindern In den letzten Jahren werden gehäuft Schäden an Spargel sichtbar, die durch Abdrift spezieller Maisherbizide verursacht werden. Dabei
BHV Dummyprüfung. Stufe 2
 BHV Dummyprüfung Stufe 2 Dummyprüfung BHV Stufe 2 Dummyprüfung des BHV Stufe 2 Gelände: Alle Übungen der Stufe 2 werden im Gelände geprüft. Es soll ein aufgelockerter Bewuchs in einer Höhe vorherrschen,
BHV Dummyprüfung Stufe 2 Dummyprüfung BHV Stufe 2 Dummyprüfung des BHV Stufe 2 Gelände: Alle Übungen der Stufe 2 werden im Gelände geprüft. Es soll ein aufgelockerter Bewuchs in einer Höhe vorherrschen,
a. Was tut das Tier, welches beobachtbare und messbare Verhalten führt es aus?
 1. Beobachten Sie das Zielverhalten und definieren Sie es operational. a. Was tut das Tier, welches beobachtbare und messbare Verhalten führt es aus? 2. Identifizieren Sie die entfernten und die unmittelbaren
1. Beobachten Sie das Zielverhalten und definieren Sie es operational. a. Was tut das Tier, welches beobachtbare und messbare Verhalten führt es aus? 2. Identifizieren Sie die entfernten und die unmittelbaren
Großer Fragebogen Hund
 Großer Fragebogen Hund Konstitutionsbehandlung Um Ihren Hund im Sinne der klassischen Tierhomöopathie zu behandeln zu können, müssen Sie mir nun einige Fragen zu Ihrem Hund beantworten. Bitte nehmen sie
Großer Fragebogen Hund Konstitutionsbehandlung Um Ihren Hund im Sinne der klassischen Tierhomöopathie zu behandeln zu können, müssen Sie mir nun einige Fragen zu Ihrem Hund beantworten. Bitte nehmen sie
Klare ANTWORTEN auf wichtige Fragen
 Klare ANTWORTEN auf wichtige Fragen Der HARMONY PRÄNATAL-TEST ist ein neuartiger, DNA-basierter Bluttest zur Erkennung von Trisomie 21 (Down-Syndrom). Der Harmony- Test ist zuverlässiger als herkömmliche
Klare ANTWORTEN auf wichtige Fragen Der HARMONY PRÄNATAL-TEST ist ein neuartiger, DNA-basierter Bluttest zur Erkennung von Trisomie 21 (Down-Syndrom). Der Harmony- Test ist zuverlässiger als herkömmliche
Einleitung. Replikation
 (C) 2014 - SchulLV 1 von 9 Einleitung Der Action-Film von gestern Abend war wieder ziemlich spannend. Mal wieder hat es der Superheld geschafft, alle Zeichen richtig zu deuten, diverse Geheimcodes zu knacken
(C) 2014 - SchulLV 1 von 9 Einleitung Der Action-Film von gestern Abend war wieder ziemlich spannend. Mal wieder hat es der Superheld geschafft, alle Zeichen richtig zu deuten, diverse Geheimcodes zu knacken
Wissenschaftliche Arbeiten und große Dokumente. Kompaktkurs mit Word 2013. Dr. Susanne Weber 1. Ausgabe, Dezember 2013 K-WW2013-BW
 Wissenschaftliche Arbeiten und große Dokumente Dr. Susanne Weber. Ausgabe, Dezember 03 Kompaktkurs mit Word 03 K-WW03-BW 9 9 Dokument kontrollieren Voraussetzungen Text eingeben und bearbeiten Ziele Rechtschreibung
Wissenschaftliche Arbeiten und große Dokumente Dr. Susanne Weber. Ausgabe, Dezember 03 Kompaktkurs mit Word 03 K-WW03-BW 9 9 Dokument kontrollieren Voraussetzungen Text eingeben und bearbeiten Ziele Rechtschreibung
STARTHILFE. für die Basalinsulintherapie
 STARTHILFE für die Basalinsulintherapie INSULIN HILFT IHNEN WEITER LIEBE PATIENTIN, LIEBER PATIENT, wenn Sie diese kleine Broschüre in der Hand halten, hat Ihr Arzt Ihnen zur Behandlung Ihres Diabetes
STARTHILFE für die Basalinsulintherapie INSULIN HILFT IHNEN WEITER LIEBE PATIENTIN, LIEBER PATIENT, wenn Sie diese kleine Broschüre in der Hand halten, hat Ihr Arzt Ihnen zur Behandlung Ihres Diabetes
KeptSecret User Guide
 User Guide Mit können Sie Ihre Bilder und Notizen verschlüsselt und damit privat speichern. verwendet die im iphone und ipod Touch eingebaute 256-Bit starke Verschlüsselung nach dem Advances Encryption
User Guide Mit können Sie Ihre Bilder und Notizen verschlüsselt und damit privat speichern. verwendet die im iphone und ipod Touch eingebaute 256-Bit starke Verschlüsselung nach dem Advances Encryption
Aufgabe 2: (Aminosäuren)
 Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Aufgabe 2: (Aminosäuren) Aufgabenstellung Die 20 Aminosäuren (voller Name, 1- und 3-Buchstaben-Code) sollen identifiziert und mit RasMol grafisch dargestellt werden. Dann sollen die AS sinnvoll nach ihren
Patienten-Ratgeber für die Behandlung der feuchten altersbedingten Makuladegeneration mit EYLEA. (Afl ibercept Injektionslösung)
 Patienten-Ratgeber für die Behandlung der feuchten altersbedingten Makuladegeneration mit EYLEA (Afl ibercept Injektionslösung) P Lesen Sie sich bitte vor Beginn Ihrer Behandlung mit EYLEA das gesamte
Patienten-Ratgeber für die Behandlung der feuchten altersbedingten Makuladegeneration mit EYLEA (Afl ibercept Injektionslösung) P Lesen Sie sich bitte vor Beginn Ihrer Behandlung mit EYLEA das gesamte
Reizleitung in Nervenzellen. Nervenzelle unter einem Rasterelektronenmikroskop
 Reizleitung in Nervenzellen Nervenzelle unter einem Rasterelektronenmikroskop Gliederung: 1. Aufbau von Nervenzellen 2. Das Ruhepotential 3. Das Aktionspotential 4. Das Membranpotential 5. Reizweiterleitung
Reizleitung in Nervenzellen Nervenzelle unter einem Rasterelektronenmikroskop Gliederung: 1. Aufbau von Nervenzellen 2. Das Ruhepotential 3. Das Aktionspotential 4. Das Membranpotential 5. Reizweiterleitung
T 5 FF 16 Arbeitsblatt 4
 T 5 FF 16 Arbeitsblatt 4 Zell bestandteile als Teile eines Staates Ordne die folgenden Begriffe aus der Staatskunde den Beschreibungen zu : produktive Fläche Transportsystem Grenze Brachland / Speicher
T 5 FF 16 Arbeitsblatt 4 Zell bestandteile als Teile eines Staates Ordne die folgenden Begriffe aus der Staatskunde den Beschreibungen zu : produktive Fläche Transportsystem Grenze Brachland / Speicher
Känguru der Mathematik 2004 Gruppe Écolier (3. und 4. Schulstufe) 18.3.2004
 Känguru der Mathematik 2004 Gruppe Écolier (3. und 4. Schulstufe) 18.3.2004-3 Punkte Beispiele - 1 1) 21+ 22 + 23 =? A) 56 B) 64 C) 65 D) 66 E) 76 Antwort: D 2) Am Tag der Geburt seiner Schwester war Andreas
Känguru der Mathematik 2004 Gruppe Écolier (3. und 4. Schulstufe) 18.3.2004-3 Punkte Beispiele - 1 1) 21+ 22 + 23 =? A) 56 B) 64 C) 65 D) 66 E) 76 Antwort: D 2) Am Tag der Geburt seiner Schwester war Andreas
Die Verbindungen zwischen Parkinson und der Huntington Krankheit
 Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Erfolgreiche Studie zu Gentherapie bei Parkinson macht Hoffnung
Neuigkeiten aus der Huntington-Forschung. In einfacher Sprache. Von Wissenschaftlern geschrieben Für die Huntington-Gemeinschaft weltweit. Erfolgreiche Studie zu Gentherapie bei Parkinson macht Hoffnung
1 Gibt es eine zweite Erde?
 6 / 7 1 Gibt es eine zweite Erde? Joachim Wambsganß 8 1 Gibt es eine zweite Erde? Unsere Erde ist ein Planet, der um die Sonne kreist. So wie Merkur, Venus, Mars, Jupiter, Saturn, Uranus und Neptun. Der
6 / 7 1 Gibt es eine zweite Erde? Joachim Wambsganß 8 1 Gibt es eine zweite Erde? Unsere Erde ist ein Planet, der um die Sonne kreist. So wie Merkur, Venus, Mars, Jupiter, Saturn, Uranus und Neptun. Der
1. Stammbaum einer Familie, in der Mukoviszidose aufgetreten ist.
 Die Prüfungsarbeit besteht aus drei zu bearbeitenden Teilen Aufgabe I Aufgabe II A oder II B Aufgabe III A oder III B I Aufgabe I: Humangenetik / klassische Genetik / Molekulargenetik Mukoviszidose Mukoviszidose,
Die Prüfungsarbeit besteht aus drei zu bearbeitenden Teilen Aufgabe I Aufgabe II A oder II B Aufgabe III A oder III B I Aufgabe I: Humangenetik / klassische Genetik / Molekulargenetik Mukoviszidose Mukoviszidose,
Patienteninformation Ich bin schwanger. Warum wird allen Schwangeren ein HIV-Test angeboten?
 Patienteninformation Ich bin schwanger. Warum wird allen Schwangeren ein HIV-Test angeboten? Was passiert bei einem HIV-Test? Für einen HIV-Test wird eine Blutprobe entnommen und in einem Labor untersucht.
Patienteninformation Ich bin schwanger. Warum wird allen Schwangeren ein HIV-Test angeboten? Was passiert bei einem HIV-Test? Für einen HIV-Test wird eine Blutprobe entnommen und in einem Labor untersucht.
Chemie für Biologen. Vorlesung im. WS 2004/05 V2, Mi 10-12, S04 T01 A02. Paul Rademacher Institut für Organische Chemie der Universität Duisburg-Essen
 Chemie für Biologen Vorlesung im WS 004/05 V, Mi 0-, S04 T0 A0 Paul Rademacher Institut für rganische Chemie der Universität Duisburg-Essen (Teil 3: 9.0.005) MILESS: Chemie für Biologen 36 D-Aldosen C
Chemie für Biologen Vorlesung im WS 004/05 V, Mi 0-, S04 T0 A0 Paul Rademacher Institut für rganische Chemie der Universität Duisburg-Essen (Teil 3: 9.0.005) MILESS: Chemie für Biologen 36 D-Aldosen C
DIRA. Deficiency of IL-1 Receptor Antagonist (DIRA)
 Center Deficiency of IL-1 Receptor Antagonist () Was ist? ist eine seltene genetische Erkrankung. Betroffene Kinder leiden an schwerwiegenden Hautund Knochenentzündungen. Andere Organe wie z.b. die Lungen
Center Deficiency of IL-1 Receptor Antagonist () Was ist? ist eine seltene genetische Erkrankung. Betroffene Kinder leiden an schwerwiegenden Hautund Knochenentzündungen. Andere Organe wie z.b. die Lungen
Weitere Tipps & Tricks und vieles mehr rund ums Thema Pferd unter: www.hadel.net/reitertreff/reitertreff.html
 Das Knotenhalfter Ein Halfter zum - selber Ein Halfter basteln zum selber basteln Eine Anleitung von Martina Grabski email: martina@hadel.net, Internet: www.hadel.net Weitere Tipps & Tricks und vieles
Das Knotenhalfter Ein Halfter zum - selber Ein Halfter basteln zum selber basteln Eine Anleitung von Martina Grabski email: martina@hadel.net, Internet: www.hadel.net Weitere Tipps & Tricks und vieles
MORBUS FABRY Morbus Fabry ist eine seltene und schwere, aber behandelbare Krankheit
 MORBUS FABRY Morbus Fabry ist eine seltene und schwere, aber behandelbare Krankheit Diese Broschüre möchte Sie über die Entstehung, Vererbung und Behandlung der Fabry-Erkrankung informieren. Hier finden
MORBUS FABRY Morbus Fabry ist eine seltene und schwere, aber behandelbare Krankheit Diese Broschüre möchte Sie über die Entstehung, Vererbung und Behandlung der Fabry-Erkrankung informieren. Hier finden
Wie viele Pfunde möchten Sie in 4 Wochen abnehmen?
 Wie viele Pfunde möchten Sie in 4 Wochen abnehmen? Warum reine Diäten nicht funktionieren und dick machen! Und zwei Methoden, wie Sie den Erfolg und die Nachhaltigkeit jeder Diät deutlich steigern können!
Wie viele Pfunde möchten Sie in 4 Wochen abnehmen? Warum reine Diäten nicht funktionieren und dick machen! Und zwei Methoden, wie Sie den Erfolg und die Nachhaltigkeit jeder Diät deutlich steigern können!
Zentrales Dogma der Biologie
 Zentrales Dogma der Biologie Transkription: von der DNA zur RNA Biochemie 01/1 Transkription Biochemie 01/2 Transkription DNA: RNA: Biochemie 01/3 Transkription DNA: RNA: Biochemie 01/4 Transkription RNA:
Zentrales Dogma der Biologie Transkription: von der DNA zur RNA Biochemie 01/1 Transkription Biochemie 01/2 Transkription DNA: RNA: Biochemie 01/3 Transkription DNA: RNA: Biochemie 01/4 Transkription RNA:
Ich möchte Sie daher bitten, diesen Fragebogen vor der Untersuchung bei mir auszufüllen.
 Schwindelfragebogen Sehr geehrte Patientin, sehr geehrter Patient, Schwindel tritt bei einer Vielzahl von Erkrankungen auf. Eine genaue Schilderung der Beschwerden ist wichtig, da die Ursache von Schwindel
Schwindelfragebogen Sehr geehrte Patientin, sehr geehrter Patient, Schwindel tritt bei einer Vielzahl von Erkrankungen auf. Eine genaue Schilderung der Beschwerden ist wichtig, da die Ursache von Schwindel
Chromosom enthält DNA besteht aus Nucleotiden bestehen aus Phosphat und Basen sind Adenin, Guanin, Cytosin, Thymin
 2 Molekulargenetik Natura Genetik 2 Molekulargenetik Lösungen zu den Aufgaben Seiten 20 21 2.1 DNA ist das genetische Material 1 Stelle in einem Begriffsnetz den Zusammenhang zwischen folgenden Begriffen
2 Molekulargenetik Natura Genetik 2 Molekulargenetik Lösungen zu den Aufgaben Seiten 20 21 2.1 DNA ist das genetische Material 1 Stelle in einem Begriffsnetz den Zusammenhang zwischen folgenden Begriffen
Mathematik und Naturwissenschaften, Biologie, Biochemie. Biochemie II - Tutorium
 Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
Mathematik und Naturwissenschaften, Biologie, Biochemie Biochemie II - Tutorium Dresden, 20.10.2016 Alexander Götze 3.Semester Molekulare Biotechnologie a.goetze2207@googlemail.com Mi. 2DS DRU. 68 H Michel
C SB. Genomics Herausforderungen und Chancen. Genomics. Genomic data. Prinzipien dominieren über Detail-Fluten. in 10 Minuten!
 Genomics Herausforderungen und Chancen Prinzipien dominieren über Detail-Fluten Genomics in 10 Minuten! biol. Prin cip les Genomic data Dr.Thomas WERNER Scientific & Business Consulting +49 89 81889252
Genomics Herausforderungen und Chancen Prinzipien dominieren über Detail-Fluten Genomics in 10 Minuten! biol. Prin cip les Genomic data Dr.Thomas WERNER Scientific & Business Consulting +49 89 81889252
Schönheit erleben. Falten glätten und Konturgebung mit Sculptra : Liquid Lifting
 Schönheit erleben Falten glätten und Konturgebung mit Sculptra : Liquid Lifting Ihr Gesicht Es ist das Erste, das an Ihnen auffällt... das Ich, das Sie der Welt zeigen. Wenn aber Ihre äußere Erscheinung
Schönheit erleben Falten glätten und Konturgebung mit Sculptra : Liquid Lifting Ihr Gesicht Es ist das Erste, das an Ihnen auffällt... das Ich, das Sie der Welt zeigen. Wenn aber Ihre äußere Erscheinung
(x) intakte Gene in kranke Zellen eingeschleust. Gentherapien verliefen bisher in allen Fällen ohne Nebenwirkungen.
 LEVEL 1 1 Unser Erbgut enthält nur einen bestimmten Anteil an funktionierenden Genen. Wie hoch ist der prozentuale Anteil der Gene, welche in Proteine umgeschrieben werden? 20% (x) 2% 5% Chromosom 22:
LEVEL 1 1 Unser Erbgut enthält nur einen bestimmten Anteil an funktionierenden Genen. Wie hoch ist der prozentuale Anteil der Gene, welche in Proteine umgeschrieben werden? 20% (x) 2% 5% Chromosom 22:
Im Vorlesungsskript (5) auf Seite 7 haben wir folgendes Bild:
 Übungsblatt 4 Aufgabe 1 Sie möchten ein IEEE 802.11-Netzwerk (WLAN) mit einem IEEE 802.3-Netzwerk (Ethernet) verbinden. 1a) Auf welcher Schicht würden Sie ein Zwischensystem zur Übersetzung ansiedeln?
Übungsblatt 4 Aufgabe 1 Sie möchten ein IEEE 802.11-Netzwerk (WLAN) mit einem IEEE 802.3-Netzwerk (Ethernet) verbinden. 1a) Auf welcher Schicht würden Sie ein Zwischensystem zur Übersetzung ansiedeln?
Fragen und Antworten für Plasmaspender. Plasma spenden
 Fragen und Antworten für Plasmaspender Plasma spenden Was ist Blut? Blut ist eine Flüssigkeit, die durch den menschlichen Körper fließt. Blut transportiert Sauerstoff, Kohlendioxid, Nährstoffe und Abfallprodukte
Fragen und Antworten für Plasmaspender Plasma spenden Was ist Blut? Blut ist eine Flüssigkeit, die durch den menschlichen Körper fließt. Blut transportiert Sauerstoff, Kohlendioxid, Nährstoffe und Abfallprodukte
Warum war die Studie notwendig?
 Eine Studie, in der untersucht wurde, ob BI 409306 die geistigen Fähigkeiten von Menschen mit milder Alzheimer-Krankheit und Problemen bei der geistigen Funktionsfähigkeit verbessert Nachfolgender Text
Eine Studie, in der untersucht wurde, ob BI 409306 die geistigen Fähigkeiten von Menschen mit milder Alzheimer-Krankheit und Problemen bei der geistigen Funktionsfähigkeit verbessert Nachfolgender Text
Übergang in den Ruhestand und Renteneinkommen
 DZA Deutsches Zentrum für Altersfragen 1 Übergang in den Ruhestand und Renteneinkommen Der Deutsche Alterssurvey (DEAS): Älterwerden und der Einfluss von Kontexten 1996 2002 2008 2011 Einführung Im letzten
DZA Deutsches Zentrum für Altersfragen 1 Übergang in den Ruhestand und Renteneinkommen Der Deutsche Alterssurvey (DEAS): Älterwerden und der Einfluss von Kontexten 1996 2002 2008 2011 Einführung Im letzten
