Feldbuch für die Untersuchungen. Fliessgewässer: Bioindikation und chemisch-physikalische Untersuchungen. Walter Hauenstein, GLOBE Schweiz
|
|
|
- Liese Beutel
- vor 6 Jahren
- Abrufe
Transkript
1 Feldbuch für die Untersuchungen Fliessgewässer: Bioindikation und chemisch-physikalische Untersuchungen Walter Hauenstein, GLOBE Schweiz
2 Inhaltsverzeichnis Feldbuch Datenblatt A Landschaftsökologische Beurteilung 1 Charakterisierung Untersuchungsstelle/Koordinaten 2 Hydrologie: Temperatur / Transparenz/ Leitfähigkeit 3 Hydrologie: ph-wert 4 Hydrologie: Alkalinität 6 Hydrologie: Nitrat 7 Hydrologie: Sauerstoff 9 Bioindikation: Proben sammeln 11 Bioindikation: Erkennungshilfen 12 Bioindikation Datenblatt B Biologische Beurteilung 15 Zusammenstellung Resultate/Liste Makroinvertebraten 16 Bioindikation C Bestimmung Gewässergüte 17
3 - 1 - A) Datenblatt Landschaftsökologische Beurteilung Bewertung (es sind auch halbe Punkte möglich, z.b. 1.5 oder 2.5) 1 Bachverlauf Linienführung 2 Bachbreite abwechselnd eng, breit 3 Wassertiefen stark wechselnd (an Prall- Gleith, ev. Inselbildung) 4 Wasserdurchfluss 1 Punkt 2 Punkte 3 Punkte Pte Natürl. Korrekturen sichtbar, gestreckt, kanalisiert mäandrierend, bogig geschwungen schlängelnd stark abwechselnd, schnell /langsam fliessende Stellen, stehendes Wasser 5 Bachsohle sehr vielgestaltig, natürlich (Steine, Kies, Sand, Falllaub,...) 6 Uferneigung und - gliederung 7 Uferbeschaffen heit Ufersicherheit vielfältig, abwechselnd flach und steil unregelm. reich gegliedert natürlich, häufig unterspült 8 Uferbewuchs natürlich und vielfältig, Bäume, Sträucher, Gräser, Kräuter, Hochstauden,... 9 Durchwanderbarkeit für Fische 10 Nutzungseinflüsse im natürlichen Bach gewährleistet (ausgenommen bei natürlichen Wasserfällen) keine erkennbar leicht abwechselnd, etwas schmaler, breiter werdend mindestens im Uferbereich variierend unterschiedliche Durchflussgeschwindigk eiten, ohne stehendes Wasser abwechselnd, teilweise natürlich, künstliche Eingriffe erkennbar abwechselnd künstliche und natürliche Abschnitte Künstl. Ufersicherung erkennbar (z.b. Blockwurf) abw. mit natürlichen Stellen künstlich angelegt und mehr oder weniger einheitlich (Wiese, Gebüsch, Baumreihe,...) Niedere Gefällstufen (Schwellen < 20 cm) mit Steinen/ anderen natürlichen Materialien behindern nur wenig geringe Auswirkungen erkennbar (z.b. durch Wasserentnahme, Kanalisationseinleitung kanalisierte Einheitsbreite völlig einheitlich einheitliche Durchflussgeschwindi gkeit künstlich, einheitlich (z.b. nur Kies, nur Sand, Betonplatten,..) völlig einheitlich, gleichförmig verfugte Steinblöcke, Betonmauer fehlend, bewirtschaftete Flächen bis zum Gewässerrand hohe Schwellen (> 0.70 m) und künstliche Abstürze verhindern den Aufstieg starke Auswirkungen (z.b. Trockenlegung Wasserkraftnutzung, Gülleeinfluss Gesamtbeurteilung des Untersuchten Abschnitts: Summe aller Punkte:
4 - 2 - Charakterisierung der Untersuchungsstelle Koordinaten LK 1: (aus Karte) Bestimmung Bestimmung mit GPS app: gis:ch /gis:ch plus WGS84 CH-Koord. LV 03 Bestimmung 1 Bestimmung 2 Bestimmung 3 Bestimmung 4 Bestimmung Fliessgeschwindigkeit: Wert 1: Wert 2: Wert 3: Abstand Ufer Abstand Ufer Abstand Ufer Bestimmung der Flussbreite mit Trigonometrie Flussbreite Winkel alpha = Abstand Ufer = Basis = Flussbreite= Basis x tan (alpha) Abstand Ufer => Flussbreite =
5 Hydrologie: Temperatur Messungen im fliessenden Wasser Messung Temperatur Messgerät MITTEL Hydrologie Transparenz Messung mit Rohr: Wasser auffüllen bis schwarz/weiss Markierung nicht mehr sichtbar. (wenn bei vollem Rohr noch erkennbar ist Wert > 120 cm.) Messung 1 Messung 2 Messung 3 Messung 4 Mittel: Hydrologie Leitfähigkeit (im Kursraum bei 25 Grad) Mit geeichtem Messgerät. Sensor in Wasserprobe halten, leicht schwenken, ablesen wenn Messwert stabil (kann einige Minuten dauern!) Messung Leitfähigkeit in µs/cm Messgerät Mittel:
6 - 4 - ph-wert Hach Material 1 Color Komparator mit Farbscheibe 2 Proberöhrchen mit Stopfen Bromthymol Blue Indicator Solution Prinzip Eine spezielle chemische Reaktion ergibt eine Färbung, welche abhängig ist vom ph- Wert ( Säuregehalt ) des Wassers. Durchführung der Messung 1. Beide Proberöhrchen mehrmals mit dem zu testenden Wasser spülen und bis zum unteren Markierungsstrich 5 ml füllen. 2. Eines der Röhrchen bleibt unbehandelt und kommt in Position A in den Komparator 3. Zum zweiten Röhrchen 8 Tropfen des Bromthymols Blau Indicator Lösung zugeben. Kurz schütteln. 4. Proberöhrchen mit dem behandelten Wasser in Position B des Komparators einsetzen. 5. Den Komparator in Augenhöhe gegen das Licht halten und die Farbe der Lösung durch drehen der Scheibe zuordnen. ph-wert ablesen! Sofort nach Gebrauch Proberöhrchen mit Wasser spülen.
7 - 5 - Unsere Messwerte: Messwert 1 Messwert 2 Messwert 3 Messwert 4 Mittelwert Beurteilung: Kriterien zur Beurteilung des ph-wertes Reines Wasser, H2O ist zu einem sehr geringen Teil in seine Ionen (= geladene Teilchen) H+ und OH- aufgespalten. Ein Liter Wasser enthält 1/107 Wasserstoff-Ionen (H+). Da auch die gleiche Menge an Hydroxyl-Ionen (OH-) vorhanden ist, reagiert reines Wasser neutral. Zur Vereinfachung gibt man an Stelle der Zahl 1/107 den ph- Wert mit der Zahl des Exponenten von 10 im Nenner an (ph = 7). Wasser mit einem ph-wert von 7 ist neutral, unter 7 sauer und über 7 alkalisch oder basisch. Natürliche Gewässer haben im Allgemeinen einen ph-wert um den Neutralpunkt herum. Abweichungen sind meist auf die Beschaffenheit des Bodens (Kalk -- >alkalisch, Moorboden --> sauer wegen der Humussäuren) oder Industrieabwässer zurückzuführen. Die im Wasser lebenden Organismen gedeihen am besten bei einem ph-wert zwischen etwa 6.8 und 7.8. Innerhalb von Tag- und Nachtrhythmus und im Rhythmus der Jahreszeiten kommt es zu Schwankungen im ph Bereich. In den Sommermonaten kann tagsüber durch, den CO2-Verbrauch der Pflanzen (Photosynthese) der ph-wert von 7 auf 9 steigen und nachts durch CO2-Ausscheidung bei der Atmung wieder auf 7 absinken. Eine einmalige Messung des ph-wertes eines Gewässers ist deshalb wenig aufschlussreich. Der ph Wert beeinflusst stark den Anteil der gelösten Kohlensäure.
8 - 6 - Alkalinität Visocolor HE Diese Bestimmungen werden mit dem Visocolor Titrierset AL7 durchgeführt. An der Titrierpipette wird nach Erreichen des Titrationsendpunktes die Konzentration auf einer Skala abgelesen. Vorbereitung: Tropfspitze auf Titrierspritze aufsetzen. Die Titrierpipette wird lose auf den Behälter gesetzt und der Kolben nach unten gedrückt. Dann zieht man den Kolben in die obere Ausgangsposition, die Unterkante der schwarzen Kolbendichtung steht auf 0. Nach Zugabe des Indikators wird das Reagens tropfenweise aus der Pipette der Probe zugegeben bis zum Farbumschlag und dann der Verbrauch abgelesen. Alkalinität/ Carbonathärte (=Säurebindungsvermögen SBV) - Messgefäss mit Probewasser spülen und mit 5 ml (bis zur Ringmarkierung) Probewasser füllen. - 1 Tropfen Indikatorlösung m zugeben und durch Schwenken lösen. --> Probe färbt sich blau. - Mit Titrierpipette sorgfältig Tropf um Tropf zugeben und schwenken, bis zum Farbumschlag von blau über grauviolett nach rot titrieren. (Falls Spritzenfüllung nicht ausreicht, füllt man die Spritze und titriert weiter bis zum Farbumschlag. Zum abgelesenen Wert wird dann 7.2 mmol/l addiert.) - Skala ablesen: SBV in mmol/l Umrechnungen: SBV in mmol/l * 2.8 ergibt Karbonathärte in dkh o. SBV in mmol/l * 50 ergibt mg/l CaCO3. Messwerte: mmol/l mg/l CaCO Mittel
9 - 7 - Nitrat Hach (low range) Material 1 Color Komparator mit Farbscheibe 2 Proberöhrchen mit Stopfen NitraVer 6 Reagens (Pulver in Minialubeutel, mit Nitrate LR beschriftet) NitriVer 3 Reagens (Pulver in Minialubeutel, mit Nitrit LR beschriftet) Prinzip Eine spezielle chemische Reaktion ergibt eine Rotfärbung, welche dem Nitratgehalt des Wassers proportional ist. Durchführung der Messung 1.1. Erwarteter Wert <1 mg/l Nitrat-N: Beide Proberöhrchen mehrmals mit dem zu testenden Wasser spülen und bis zum unteren Markierungsstrich 5 ml füllen. 1.2 Erwarteter Wert > 1 mg/l Nitrat-N: Beide Proberöhrchen mehrmals mit dem zu testenden Wasser spülen und mit der Pipette je 1 ml Probewasser in die Röhrchen geben. Mit dest. Wasser bis zur unteren Marke auffüllen (4 ml dest. Wasser) 2. Eines der Röhrchen bleibt unbehandelt und kommt in Position A in den Komparator 3. Zum zweiten Röhrchen das Pulver aus dem Minibeutel NitraVer 6 (Nitrate LR) Reagens zugeben. 3 Minuten schütteln. Falls am Grunde feine schwarze Cadmium Partikel ausfallen, Lösung sorgfältig in ein neues RG umgiessen. 4. Zu dieser Lösung nun das Pulver aus dem Minibeutel NitriVer 3 (Nitrite LR) Reagens zugeben und 30 Sekunden schütteln. Proberöhrchen mit dem behandelten Wasser in Position B des Komparators einsetzen. 5. Nach 10 Minuten Komparator in Augenhöhe gegen das Licht halten und die Farbe der Lösung durch drehen der Scheibe zuordnen. Nitrat-N Gehalt ablesen! Bei kleinen Mengen Nitrat ein weisses Blatt Papier 5-10 cm hinter den Komparator halten, um die Ablesung zu erleichtern. Für Messung nach 1.2 abgelesener Wert mit 5 multiplizieren! Angabe in mg/liter Nitrat- N. (für Nitrat NO3- mit 4.4 multiplizieren) Sofort nach Gebrauch Proberöhrchen mit dest. Wasser spülen.
10 Unsere Messwerte: (alle als Nitrat-N) Messwert 1 Messwert 2 Messwert 3 Messwert 4 Mittelwert Beurteilung: Kriterien zur Beurteilung des Nitratgehaltes In geringen Mengen sind Nitrate fast in jedem Wasser vorhanden. Man findet im allgemeinen 5-10 mg/l (entsprechend rund 1-2 mg/l Nitrate-N). In gesundheitlicher Hinsicht ist ein Nitrat-Gehalt über 50 mg/1 nicht unproblematisch. Das Nitrat selbst ist zwar nicht giftig, doch können daraus im ungünstigen Falle im Verdauungstrakt giftige N-Verbindungen entstehen. (Blausucht bei Kleinkindern) Wichtig ist seine Bedeutung als Verschmutzungsindikator mit sehr hoher Aussagekraft über die Belastung mit organischen oder anorganischen, stickstoffhaltigen Abfallstoffen und die Intensität ihres Abbaus. Nitrat entsteht in der Regel als Endprodukt beim Abbau stickstoffhaltiger organischer Verbindungen wie Eiweisse durch spezialisierte Bakterien. Nitratsalze sind aber auch wichtiger Bestandteil der meisten Kunstdünger. Da diese im Boden nur leicht gebunden sind, kommt es nach Niederschlägen oft zur Auswaschung. Dadurch wird die Landwirtschaft zum Hauptverursacher der Nitratbelastung der Gewässer. Qualitätsziel für Fliessgewässer ist 25 mg/l.
11 - 9 - Sauerstoff Visocolor HE Bestimmung durch Titrieren Prinzip: Eine Reagenzlösung mit bekannter Konzentration wird tropfenweise zur Probelösung zugegeben, bis der zu bestimmende Stoff komplett reagiert hat. Das Ende der Reaktion wird durch einen Farbumschlag sichtbar gemacht. Diese Bestimmungen werden mit der Visocolor Titrierpipette durchgeführt, auf der nach Erreichen des Titrationsendpunktes die Konzentration auf einer Skala abgelesen werden kann. Vorbereitung Zuerst wird die Titrierpipette lose auf den Behälter gesetzt und der Kolben nach unten gedrückt. Dann zieht man den Kolben nach oben bis Marke 0. Durchführung Am Entnahmeort: Spezielle Glasflasche mit dem Probewasser spülen und bis zum Überlaufen sorgfältig und blasenfrei mit dem Wasser füllen. - 4 Tropfen Sauerstoff Reagens 1 zugeben - 4 Tropfen Sauerstoff Reagens 2 zugeben, Flasche luftblasenfrei verschliessen und gut schütteln. 2 Minute stehen lassen. - Flasche öffnen, 12 Tropfen Sauerstoff-Reagens 3 zugeben, Flasche wieder schliessen und wieder gut schütteln, bis sich Niederschlag löst. - Mit dieser Lösung Messgefäss kurz spülen und bis 5 ml Ringmarke füllen. - l Tropfen Reagens 4 zugeben. - Titrierpipette Sauerstoff vorbereiten und langsam durch Zutropfen bis zum Farbumschlag schwarzviolett zu farblos titrieren. Dabei das Messgefäss ständig schwenken... - den Sauerstoffgehalt in mg/l ablesen. Resultate Messung 1 Messung 2 Mittel Gruppe 1 Gruppe 2 Gruppe 3 Gruppe 4 Mittel...mg/l
12 Sauerstoffsättigung Für 500 m über Meer gelten folgende Maximalwerte (in mg pro Liter): 0 o C o C Für die Sättigung in % wird der gefundene Wert durch den bei der gemessenen Temperatur maximal möglichen Wert geteilt und mit 100 multipliziert. Woher stammt der Sauerstoff? Es kommen zwei Quellen in Frage: Erstens gelangt Sauerstoff aus der Luft in das Wasser, v.a. bei Wellengang, Wasserfällen oder allgemein bei Turbulenz in der Oberfläche. Zweitens produzieren Algen und Wasserpflanzen in den oberen Schichten des Gewässers durch Photosynthese Sauerstoff. (Was kurzfristig sogar zu einem Sauerstoff-Überschuss führen kann) Wer (ver)braucht den Sauerstoff? Der im Wasser gelöste Sauerstoff wird von allen Lebewesen im Wasser durch die Atmung verbraucht. Ins Gewicht fällt v.a. der Sauerstoffverbrauch der Reduzenten (Mikroorganismen) beim "veratmen" (oxidieren, mineralisieren) von organischen Verunreinigungen des Wassers bei der biologischen Selbstreinigung. Also ist der Sauerstoffverbrauch ein Mass für organische Verunreinigungen (vgl. BSB5 Bestimmung) Bei starker Belastung durch die Abwässer oder z.b. nach Algenblüten (abgestorbene Algen) kann der Sauerstoffgehalt v.a. in tiefen Schichten auf null absinken, es bildet sich Faulschlamm, der See kippt um. Der maximal mögliche Sauerstoffgehalt des Wassers ist temperaturabhängig. Fischgewässer brauchen mindestens 5 mg Sauerstoff pro Liter. Für die Wassergüteklasse I (=unbelastet) muss der Sauerstoffgehalt mindestens 8 mg/l für Klasse II (=mässig belastet) mindestens 6 mg/l und für Klasse III (=stark belastet) mindestens 4 mg/l sein. Qualitätsziel für Fliessgewässer: Nicht unter 6 mg/l
13 Bioindikation: Proben sammeln Vgl. laminierte Kurzanleitung Total werden 10 Proben gesammelt. 1 Probe umfasst: - 5 grosse Stein sammeln und Tiere ablesen, oder - 5 Mal an verschiedenen Stellen kicken mit Kicknetz (Thur: Hüftstiefel, mit Fuss am Grund vor dem Netz kicken (Kies, Steine aufwühlen), oder - 5 Mal mit Mehlsieb durch Sand fahren und aufwühlen, oder - 5 Mal mit Mehlsieb 1 Meter durch Pflanzen, Falllaub fahren. 1. Die Steine, Proben aus dem Netz werden zuerst in eine grosse Schale gegeben: 2. Tiere ablesen, heraussuchen und in Tellerschalen überführen (= Probeschalen) 3. Aussortieren Aus den Probeschalen die unterscheidbaren Arten/Formen (= Zählformen) in die kleinen quadratische Schälchen aussortieren (1 Form pro Schälchen) => Bestimmungsschalen 4. Bestimmen Zählformen mit Erkennungshilfen 1-3 bestimmen (Lupen!) Name der Zählform auf Post-it Zettel notieren und an Bestimmungsschale anheften. Für die weitere Untersuchung/Bestimmung im Kursraum des Besucherzentrums in Dosen überführen, Post-it an Dose anbringen. (1 Zählform/Dose, mehrere Tiere) 5. Auswerten: Mit Datenblättern B und C die Gewässergüte bestimmen. (S. 15 und 17 weiter hinten
14 Erkennungshilfen Auswahl einiger wirbelloser Kleintiere in Bach und Fluss Abbildungen aus W. Engelhardt: Was lebt in Tümpel, Bach und Weiher?
15 Erkennungshilfen forts. (2)
16 Erkennungshilfen forts. (3)
17 B Datenblatt Biologische Beurteilung der Gewässergüte
18 Zusammenstellung Resultate (für Eingabe Web-GIS) Koordinaten Untersuchungsstelle: WGS84: Höhe: CH-Koordinaten LV03: Landschaftsökologie: Gemittelte Bewertung (Pte): Hydrologie (alle Werte gemittelt) Temperatur: o C Transparenz: cm ph-wert: Leitfähigkeit: µs/cm Alkalinität: mg CaCO3/l Nitrat (als Nitrat-N/l): mg/l Sauerstoff: mg/l Bioindikation: Gemittelte Bewertung: Liste der gefundenen Makroinvertebraten Zählform (i.d.r.gattung/familie) System. Gruppe Häufigkeit
19 C Biologische Beurteilung Gewässergüte (Bioindikation) Bestimmung der Gewässergüte durch insgesamt 10 Proben. GLOBE Schweiz, Version 3, 2018 Bei Fragen direkt an: info@globe-swiss.ch
Ablauf Rietbachwanderung
 Ablauf Rietbachwanderung - Einführung in Thematik: Vier bis fünf Bilder von verschiedenen Bächen (die gleichen Bilder wie bei der Auswertung nach den zwei Bachtagen) zeigen und Qualität der Bäche besprechen
Ablauf Rietbachwanderung - Einführung in Thematik: Vier bis fünf Bilder von verschiedenen Bächen (die gleichen Bilder wie bei der Auswertung nach den zwei Bachtagen) zeigen und Qualität der Bäche besprechen
Interpretation der chemischen und physikalischen Untersuchungen
 Interpretation der chemischen und physikalischen Untersuchungen in Fliessgewässern Für die Interpretation der chemischen (ph, Nitrat, Sauerstoff, Alkalinität), physikalischen (Temperatur, Transparenz,
Interpretation der chemischen und physikalischen Untersuchungen in Fliessgewässern Für die Interpretation der chemischen (ph, Nitrat, Sauerstoff, Alkalinität), physikalischen (Temperatur, Transparenz,
Gewässeruntersuchung im Bienhorntal
 Gewässeruntersuchung im Bienhorntal Am Morgen des 4.7., eines Donnerstags, brachen wir gemeinsam zur zweiten Stunde auf. Unser Ziel war das Bienhorntal in Pfaffendorf. Als wir dort angekommen waren, verteilten
Gewässeruntersuchung im Bienhorntal Am Morgen des 4.7., eines Donnerstags, brachen wir gemeinsam zur zweiten Stunde auf. Unser Ziel war das Bienhorntal in Pfaffendorf. Als wir dort angekommen waren, verteilten
3. Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14
 3. Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14 Teil des Moduls MN-C-AlC S. Sahler, M. Wolberg 20.01.14 Titrimetrie (Volumetrie) Prinzip: Messung des Volumenverbrauchs einer Reagenslösung
3. Seminar zum Quantitativen Anorganischen Praktikum WS 2013/14 Teil des Moduls MN-C-AlC S. Sahler, M. Wolberg 20.01.14 Titrimetrie (Volumetrie) Prinzip: Messung des Volumenverbrauchs einer Reagenslösung
I feel goo o d! Wissenschaftliche Grundlagen für klares Wasser. in tropischen Süßwasseraquarien
 I feel goo o d! Wissenschaftliche Grundlagen für klares Wasser in tropischen Süßwasseraquarien Philips hat diesen Wasserreiniger für tropische Aquarien in enger Zusammenarbeit mit Aquarien- und Wasserexperten
I feel goo o d! Wissenschaftliche Grundlagen für klares Wasser in tropischen Süßwasseraquarien Philips hat diesen Wasserreiniger für tropische Aquarien in enger Zusammenarbeit mit Aquarien- und Wasserexperten
Titration von Speise-Essig
 Titration von Speise-Essig Wir werden in diesem Versuch die Titration [frz.titer = Feingehalt] Konzentration der Essigsäure in Analytisches Verfahren, bei dem die Reagenzlösung tropfenweise zugesetzt wird,
Titration von Speise-Essig Wir werden in diesem Versuch die Titration [frz.titer = Feingehalt] Konzentration der Essigsäure in Analytisches Verfahren, bei dem die Reagenzlösung tropfenweise zugesetzt wird,
Bestimmung des ph-wertes des Bodens
 Bestimmung des ph-wertes des Bodens Durch den ph-wert erhältst du eine Angabe zum Säuregehalt. Er wird im Bereich zwischen 1 (sehr sauer!!!) und 14 (sehr basisch!) angegeben. Bei einem ph-wert von 7 spricht
Bestimmung des ph-wertes des Bodens Durch den ph-wert erhältst du eine Angabe zum Säuregehalt. Er wird im Bereich zwischen 1 (sehr sauer!!!) und 14 (sehr basisch!) angegeben. Bei einem ph-wert von 7 spricht
[ PROTOKOLL: TAGESPERIODIK DES MEERFELDER MAARES VOM ]
![[ PROTOKOLL: TAGESPERIODIK DES MEERFELDER MAARES VOM ] [ PROTOKOLL: TAGESPERIODIK DES MEERFELDER MAARES VOM ]](/thumbs/54/33253451.jpg) 2012 Hannah Klingener, Natalja Böhm Otto-Hahn-Gymnasium und Katharina Schwander [ PROTOKOLL: TAGESPERIODIK DES MEERFELDER MAARES VOM 16.08.2012] Biologie, LK MSS 13, Herr Kohlhepp S e i t e 1 Inhaltsverzeichnis
2012 Hannah Klingener, Natalja Böhm Otto-Hahn-Gymnasium und Katharina Schwander [ PROTOKOLL: TAGESPERIODIK DES MEERFELDER MAARES VOM 16.08.2012] Biologie, LK MSS 13, Herr Kohlhepp S e i t e 1 Inhaltsverzeichnis
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2012
 Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2012 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme Chem.
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch 2012 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme Chem.
Elektrochemie und Sauerstoffmessung mit LDO. Der gelöste Sauerstoff
 Elektrochemie und Sauerstoffmessung mit LDO Der gelöste Sauerstoff 2 Was ist gelöster Sauerstoff? Gelöster Sauerstoff beschreibt die Konzentration von freiem (nicht chemisch gebundenem) molekularem Sauerstoff
Elektrochemie und Sauerstoffmessung mit LDO Der gelöste Sauerstoff 2 Was ist gelöster Sauerstoff? Gelöster Sauerstoff beschreibt die Konzentration von freiem (nicht chemisch gebundenem) molekularem Sauerstoff
Laborbericht. Wasserhärte Leitfähigkeit. Anna Senn Bianca Theus
 Laborbericht Wasserhärte Leitfähigkeit Anna Senn Bianca Theus 14.09. 2004 03.11. 2004 Inhaltsverzeichnis 1. Ziel... 1 2. Theorie... 1 2.1 Leitfähigkeit... 1 2.2 Wasserhärte... 2 2.3 Entstehung von Wasserhärte...
Laborbericht Wasserhärte Leitfähigkeit Anna Senn Bianca Theus 14.09. 2004 03.11. 2004 Inhaltsverzeichnis 1. Ziel... 1 2. Theorie... 1 2.1 Leitfähigkeit... 1 2.2 Wasserhärte... 2 2.3 Entstehung von Wasserhärte...
Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O.
 Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O. 2 Er wollte herausfinden woher die Pflanze die Stoffe bezieht wenn sie beim Wachstum
Damit er sicher sein konnte, dass die neuen Stoffe nicht aus dem Giesswasser kommen. Regenwasser enthalt reines H 2 O. 2 Er wollte herausfinden woher die Pflanze die Stoffe bezieht wenn sie beim Wachstum
7HWUDWHVW$QDO\6HW *HEUDXFKVDQOHLWXQJ :DUXP$TXDULXPZDVVHUWHVWHQ"
 *HEUDXFKVDQOHLWXQJ 7HWUDWHVW$QDO\6HW :DUXP$TXDULXPZDVVHUWHVWHQ" Wasser wird von seiner Umwelt geprägt. Reines Regenwasser nimmt schon in der Atmosphäre Umweltschadstoffe auf. Beim Versickern in den Boden
*HEUDXFKVDQOHLWXQJ 7HWUDWHVW$QDO\6HW :DUXP$TXDULXPZDVVHUWHVWHQ" Wasser wird von seiner Umwelt geprägt. Reines Regenwasser nimmt schon in der Atmosphäre Umweltschadstoffe auf. Beim Versickern in den Boden
3.11 Zerlegung von Wasser durch Reduktionsmittel. Aufgabe. Aus welchen Elementen besteht Wasser?
 Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755500) 3. Zerlegung von Wasser durch Reduktionsmittel Experiment von: Seb Gedruckt: 24.03.204 :42:33
Naturwissenschaften - Chemie - Anorganische Chemie - 3 Wasser, Wasserbestandteile und Wasserreinigung (P755500) 3. Zerlegung von Wasser durch Reduktionsmittel Experiment von: Seb Gedruckt: 24.03.204 :42:33
Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011
 Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme
Analyse der Chemischen/Biologischen Wasseruntersuchungen der mittleren Aisch 2011 Meßstellen: Pegel-Birkenfeld Flß/km60,7 ; oberhalb Wehr Pahres Flß/km49,1 ; Trafo vor Dachsbach Flß/km43,1 Anlagen: Diagramme
Gewässeruntersuchung. Allgemein. Untersuchung der Gegebenheiten. Allgemein: Untersuchung eines Gewässers. Jens Breitbart
 Gewässeruntersuchung Allgemein Die Gewässergüte wird mit Hilfe von der Verschmutzungen in Klassen eingeteilt. Diese Klassen haben den Namen Saprobienklasse. Das Wort ist aus den griechischen Wörtern sapros
Gewässeruntersuchung Allgemein Die Gewässergüte wird mit Hilfe von der Verschmutzungen in Klassen eingeteilt. Diese Klassen haben den Namen Saprobienklasse. Das Wort ist aus den griechischen Wörtern sapros
Empfehlungen für die Beschaffung von Chemikalien zur Ermittlung der chemischen Gewässergüte
 Empfehlungen für die Beschaffung von Chemikalien zur Ermittlung der chemischen Gewässergüte Am Anfang der Tabelle sind die für die Ermittlung der chemischen Gewässergüte nach G.R.E.E.N. und BACH relevanten
Empfehlungen für die Beschaffung von Chemikalien zur Ermittlung der chemischen Gewässergüte Am Anfang der Tabelle sind die für die Ermittlung der chemischen Gewässergüte nach G.R.E.E.N. und BACH relevanten
Europäischer Chemielehrerkongress Leoben Österreich im April 2007
 Einfache und erprobte Experimente für den Anfangsunterricht im Fach Chemie 1. Stoffumwandlung Stoffe reagieren Aggregatzustandsänderung Zusammensetzung der Luft Gesetz von der Erhaltung der Masse Reaktion
Einfache und erprobte Experimente für den Anfangsunterricht im Fach Chemie 1. Stoffumwandlung Stoffe reagieren Aggregatzustandsänderung Zusammensetzung der Luft Gesetz von der Erhaltung der Masse Reaktion
Band 2, Thema 3 Perpetual Preservation System Karbonathärte, Kraft des Wasserstoffs und Kohlendioxid Das KH, ph und CO2 Verhältnis.
 Band 2, Thema 3 Nachdem wir uns in den vorherigen Artikeln dem Nitrat, Phosphat, Calcium, Magnesium und der Gesamthärte zugewendet haben, wollen wir nun die Karbonathärte (KH), Kohlendioxid (CO2) und die
Band 2, Thema 3 Nachdem wir uns in den vorherigen Artikeln dem Nitrat, Phosphat, Calcium, Magnesium und der Gesamthärte zugewendet haben, wollen wir nun die Karbonathärte (KH), Kohlendioxid (CO2) und die
Sie kann auf biologischen oder auf chemischen Untersuchungen des Gewässers beruhen:
 Wasser und Abwasser Wiederholung: Gewässereutrophierung und Gewässergüteklassen Gewässergütebestimmung Sie kann auf biologischen oder auf chemischen Untersuchungen des Gewässers beruhen: Die Gewässergüte:
Wasser und Abwasser Wiederholung: Gewässereutrophierung und Gewässergüteklassen Gewässergütebestimmung Sie kann auf biologischen oder auf chemischen Untersuchungen des Gewässers beruhen: Die Gewässergüte:
Pflanz en und ihre ph-vorlieben
 Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Pflanz en und ihre ph-vorlieben Extrablatt 1 zu Arbeitsblatt 1, Aufgabe 2 Beispiele für Wildpflanzen als Zeigerpflanzen Stark sauer (ph unter 4,5) Sauer (ph 4,5 bis 5,2) Basisch/alkalisch Borstengras Schafschwingel
Kapitel 13: Laugen und Neutralisation
 Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
Kapitel 13: Laugen und Neutralisation Alkalimetalle sind Natrium, Kalium, Lithium (und Rubidium, Caesium und Francium). - Welche besonderen Eigenschaften haben die Elemente Natrium, Kalium und Lithium?
CHEMIE KAPITEL 4 SÄURE-BASE. Timm Wilke. Georg-August-Universität Göttingen. Wintersemester 2013 / 2014
 CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
CHEMIE KAPITEL 4 SÄURE-BASE Timm Wilke Georg-August-Universität Göttingen Wintersemester 2013 / 2014 Folie 2 Aufgaben In einen Liter Wasser werden 2 g NH - 2 (starke Base) eingeleitet welchen ph-wert hat
Umwelt. Umwelt. Kein Leben ohne Wasser 1/18. Kein Leben ohne Wasser 2/18
 Kein Leben ohne Wasser 1/18 Stell dir vor, du sitzt auf dem Mond und siehst mit dem Fernrohr auf die Erde. Was siehst du? Eine nahezu blaue Scheibe. Das kommt daher, dass weit mehr als die Hälfte der Oberfläche
Kein Leben ohne Wasser 1/18 Stell dir vor, du sitzt auf dem Mond und siehst mit dem Fernrohr auf die Erde. Was siehst du? Eine nahezu blaue Scheibe. Das kommt daher, dass weit mehr als die Hälfte der Oberfläche
allgemeine Aussagen zum Wasser Aufgaben des Wassers Aggregatzustände Aufbau des Wassermoleküls
 Gliederung allgemeine Aussagen zum Wasser Aufgaben des Wassers Aggregatzustände Aufbau des Wassermoleküls physikalische Eigenschaften Lichtdurchlässigkeit Wassertemperatur, Wärmespeichervermögen Dichte,
Gliederung allgemeine Aussagen zum Wasser Aufgaben des Wassers Aggregatzustände Aufbau des Wassermoleküls physikalische Eigenschaften Lichtdurchlässigkeit Wassertemperatur, Wärmespeichervermögen Dichte,
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Säure-Base-Reaktion. Versuch 5.1 5.2. Neutralisation, Gehaltsbestimmungen und Titrationskurven
 Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse
 Trennen von Farben Was Du brauchst: schwarzfarbige Filzstifte Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse Wie Du vorgehst: Schneide einen Kreis aus dem Kaffeefilter. Steche mit
Trennen von Farben Was Du brauchst: schwarzfarbige Filzstifte Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse Wie Du vorgehst: Schneide einen Kreis aus dem Kaffeefilter. Steche mit
Praktikum: Grundlagen der Hydrochemie
 TU Dresden Institut für Wasserchemie Chemische Entsäuerung mittels Calciumcarbonat und halbgebranntem Dolomit Praktikum: Grundlagen der Hydrochemie V 1 1. Thema: Kalk-Kohlensäure-Gleichgewicht Chemische
TU Dresden Institut für Wasserchemie Chemische Entsäuerung mittels Calciumcarbonat und halbgebranntem Dolomit Praktikum: Grundlagen der Hydrochemie V 1 1. Thema: Kalk-Kohlensäure-Gleichgewicht Chemische
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Rein oder nicht rein?
 Station 1: Rein oder nicht rein? Versuche: 1 Bestimmen Sie experimentell die Löslichkeit von Kochsalz. [Hinweis: Unter der Löslichkeit versteht man die Masse eines Stoffes in Gramm, die sich gerade noch
Station 1: Rein oder nicht rein? Versuche: 1 Bestimmen Sie experimentell die Löslichkeit von Kochsalz. [Hinweis: Unter der Löslichkeit versteht man die Masse eines Stoffes in Gramm, die sich gerade noch
Lünersee. Letzte Untersuchung Probenahme: Uhrzeit: 09:30 10:00. schwach windig. Lufttemperatur: 10 C Sichttiefe: maximale Tiefe:
 Lünersee Abbildung: Übersichtsplan, Lage der Probenstelle, Naturaufnahme Letzte Untersuchung Probenahme: 28.10.2009 Uhrzeit: 09:30 10:00 Witterung: Wind: heiter Lufttemperatur: 10 C Sichttiefe: maximale
Lünersee Abbildung: Übersichtsplan, Lage der Probenstelle, Naturaufnahme Letzte Untersuchung Probenahme: 28.10.2009 Uhrzeit: 09:30 10:00 Witterung: Wind: heiter Lufttemperatur: 10 C Sichttiefe: maximale
Was sagt mein Wasserbefund aus?
 Was sagt mein Wasserbefund aus? Themen Formale Anforderungen Dimensionen Parameter und deren Bedeutung Ergebnisse Volluntersuchungen 2008/2009 Formale Anforderungen Anschrift Auftraggeber Datum Ausfertigung
Was sagt mein Wasserbefund aus? Themen Formale Anforderungen Dimensionen Parameter und deren Bedeutung Ergebnisse Volluntersuchungen 2008/2009 Formale Anforderungen Anschrift Auftraggeber Datum Ausfertigung
Naturbeobachtung und Experiment
 Bestimmung chemischer Bodenparameter 1 Bodenfruchtbarkeit Darunter verstehen wir die Produktionskraft eines Bodens, ausgedrückt in dt (=Dezitonnen = 100 kg) organische Substanz/ha und Jahr. Die Fruchtbarkeit
Bestimmung chemischer Bodenparameter 1 Bodenfruchtbarkeit Darunter verstehen wir die Produktionskraft eines Bodens, ausgedrückt in dt (=Dezitonnen = 100 kg) organische Substanz/ha und Jahr. Die Fruchtbarkeit
Natürliche ökologische Energie- und Stoffkreisläufe
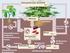 Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
Informationsmaterialien über den ökologischen Landbau für den Unterricht an allgemein bildenden Schulen. Initiiert durch das Bundesministerium für Verbraucherschutz, Ernährung und Landwirtschaft im Rahmen
3.1.2 Oberflächenwasser
 3.1.2 Oberflächenwasser - Die chemische Zusammensetzung hängt vom Untergrund des Einzugsgebietes, von der Zusammensetzung und der Menge des Niederschlages sowie von Zu- und Abfluss ab. - Flusswasser hat
3.1.2 Oberflächenwasser - Die chemische Zusammensetzung hängt vom Untergrund des Einzugsgebietes, von der Zusammensetzung und der Menge des Niederschlages sowie von Zu- und Abfluss ab. - Flusswasser hat
Bodentests selber machen Univ.Lek.DI Hans Unterfrauner. Download. www.landschaftsoekologie.at. Bodentests einfach durchführbar (im Feld und im Haus)
 Bodentests selber machen Univ.Lek.DI Hans Unterfrauner Download www.landschaftsoekologie.at Bodentests selber machen Bodentests einfach durchführbar (im Feld und im Haus) Materialien sind kostengünstig
Bodentests selber machen Univ.Lek.DI Hans Unterfrauner Download www.landschaftsoekologie.at Bodentests selber machen Bodentests einfach durchführbar (im Feld und im Haus) Materialien sind kostengünstig
Technische Universität Chemnitz Chemisches Grundpraktikum
 Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Technische Universität Chemnitz Chemisches Grundpraktikum Protokoll «CfP5 - Massanalytische Bestimmungsverfahren (Volumetrie)» Martin Wolf Betreuerin: Frau Sachse Datum:
Kleines Wasserlexikon
 Kleines Wasserlexikon Lösung von Kohlenstoffdioxid. Kohlenstoffdioxid CO 2 ist leicht wasserlöslich und geht mit manchen Inhaltsstoffen des Wassers auch chemische Reaktionen ein. In einem ersten Schritt
Kleines Wasserlexikon Lösung von Kohlenstoffdioxid. Kohlenstoffdioxid CO 2 ist leicht wasserlöslich und geht mit manchen Inhaltsstoffen des Wassers auch chemische Reaktionen ein. In einem ersten Schritt
Überprüfe alkoholhaltige Getränke mit Hilfe eines AlcoTest- Röhrchens.
 Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77800) 4.3 Alco-Test-Röhrchen Experiment von: Anouch Gedruckt: 25.02.204 3:44:30 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Organische Chemie - 4 Alkohole (P77800) 4.3 Alco-Test-Röhrchen Experiment von: Anouch Gedruckt: 25.02.204 3:44:30 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
S Primärproduktion >> Watt für Fortgeschrittene Naturschule Wattenmeer
 Wie funktioniert Primärproduktion im Meer? Aufgabe 1: Beschäftigen Sie sich mit den Steuerungsfaktoren der marinen Primärproduktion. Es gibt fünf Stationen, die Sie in beliebiger Reihenfolge durchlaufen
Wie funktioniert Primärproduktion im Meer? Aufgabe 1: Beschäftigen Sie sich mit den Steuerungsfaktoren der marinen Primärproduktion. Es gibt fünf Stationen, die Sie in beliebiger Reihenfolge durchlaufen
Anleitung. www.tatortgewaesser.de
 Anleitung www.tatortgewaesser.de Einmalige Probenahme im Zeitraum vom 2.11. bis 15.11.2015 Zeitplan mindestens ein Tag vor der Probenahme: Bereiten Sie sich zu Hause vor. Phase 1-2 Arbeitsaufwand circa
Anleitung www.tatortgewaesser.de Einmalige Probenahme im Zeitraum vom 2.11. bis 15.11.2015 Zeitplan mindestens ein Tag vor der Probenahme: Bereiten Sie sich zu Hause vor. Phase 1-2 Arbeitsaufwand circa
Der biologische Kreislauf im Aquarium
 Der biologische Kreislauf im Aquarium Einleitung Wie versuchen mit unseren Aquarien ein kleines Stück Natur in unseren Lebensbereich zu holen, also sind unsere Aquarien quasi ein kleiner Ausschnitt aus
Der biologische Kreislauf im Aquarium Einleitung Wie versuchen mit unseren Aquarien ein kleines Stück Natur in unseren Lebensbereich zu holen, also sind unsere Aquarien quasi ein kleiner Ausschnitt aus
AnC I Protokoll: 7.1 Synthese und Charakterisierung von Tetraamminkupfer(II)-sulfat! SS Analytische Chemie I.
 Analytische Chemie I Versuchsprotokoll 7.1 Synthese und Charakterisierung der Komplexverbindung Tetraamminkupfer(II)-sulfat 1.! Theoretischer Hintergrund Aus Kupfer(II)-sulfat und Ammoniak wird zunächst
Analytische Chemie I Versuchsprotokoll 7.1 Synthese und Charakterisierung der Komplexverbindung Tetraamminkupfer(II)-sulfat 1.! Theoretischer Hintergrund Aus Kupfer(II)-sulfat und Ammoniak wird zunächst
Hintergründe, Zusammenhänge, Maßnahmen. Dipl.-Biol. Christian Edler, Obere Fischereibehörde, Bez.-Reg. Münster
 Landwirtschaft Einleitungen Fische Hintergründe, Zusammenhänge, Maßnahmen Dipl.-Biol. Christian Edler, Obere Fischereibehörde, Bez.-Reg. Münster Landwirtschaft - Einleitungen - Fischbestände Inhalt A.
Landwirtschaft Einleitungen Fische Hintergründe, Zusammenhänge, Maßnahmen Dipl.-Biol. Christian Edler, Obere Fischereibehörde, Bez.-Reg. Münster Landwirtschaft - Einleitungen - Fischbestände Inhalt A.
3. Säure-Base-Beziehungen
 3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
3.1 Das Ionenprodukt des Wassers In reinen Wasser sind nicht nur Wassermoleküle vorhanden. Ein kleiner Teil liegt als Ionenform H 3 O + und OH - vor. Bei 25 C sind in einem Liter Wasser 10-7 mol H 3 O
Welcher Unterschied besteht zwischen schwefliger Säure und Schwefelsäure?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: PHYWE Gedruckt: 0.0.205 3:05:3 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: PHYWE Gedruckt: 0.0.205 3:05:3 intertess (Version 3.2 B24, Export 2000) Aufgabe Aufgabe
STATION Gewässeruntersuchung
 STATION und Temperatur Material Stationen-Karte digitale ph-elektrode Flasche mit Leitungswasser Lagerungsflüssigkeit Präsenzmaterial Auswertung STATION der Geis Der gibt Auskunft darüber, ob das Gewässer
STATION und Temperatur Material Stationen-Karte digitale ph-elektrode Flasche mit Leitungswasser Lagerungsflüssigkeit Präsenzmaterial Auswertung STATION der Geis Der gibt Auskunft darüber, ob das Gewässer
Dauerüberwachung der Fliessgewässer in den Urkantonen
 Ein gemeinsames Projekt der Kantone Uri, Schwyz, Obwalden, Nidwalden und Luzern Dauerüberwachung der Fliessgewässer in den Urkantonen Datenanhang Kanton Schwyz 000 bis 003 Inhaltsverzeichnis ÜBERSICHT
Ein gemeinsames Projekt der Kantone Uri, Schwyz, Obwalden, Nidwalden und Luzern Dauerüberwachung der Fliessgewässer in den Urkantonen Datenanhang Kanton Schwyz 000 bis 003 Inhaltsverzeichnis ÜBERSICHT
G1 pk S -Wert Bestimmung der Essigsäure
 G1 pk S -Wert Bestimmung der Essigsäure Bürette Rührer, Rührfisch ph-meter mit Einstabmesskette Stativ Becherglas Essigsäure H: 226, 314 P: 210, 260, 280.1+3, 303+361+353, 304+340, 305+351+338, 310 Phenolphthalein
G1 pk S -Wert Bestimmung der Essigsäure Bürette Rührer, Rührfisch ph-meter mit Einstabmesskette Stativ Becherglas Essigsäure H: 226, 314 P: 210, 260, 280.1+3, 303+361+353, 304+340, 305+351+338, 310 Phenolphthalein
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH)
 Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Titrationskurve einer starken Säure (HCl) mit einer starken Base (NaOH) Material 250 mlbecherglas 100 ml Messzylinder 50 mlbürette, Magnetrührer, Magnetfisch, Stativmaterial phmeter Chemikalien Natronlauge
Bezirksregierung Detmold. Der Zustand der Gewässer in Ostwestfalen-Lippe.
 Bezirksregierung Detmold Der Zustand der Gewässer in Ostwestfalen-Lippe www.weser.nrw.de Stand Mai 2014 Der Zustand der Gewässer in Ostwestfalen-Lippe Das Land NRW hat mit bundesweit abgestimmten Methoden
Bezirksregierung Detmold Der Zustand der Gewässer in Ostwestfalen-Lippe www.weser.nrw.de Stand Mai 2014 Der Zustand der Gewässer in Ostwestfalen-Lippe Das Land NRW hat mit bundesweit abgestimmten Methoden
Dichteanomalie von Wasser
 Prinzip Die Veränderung der Dichte von Wasser bei Änderung der Temperatur lässt sich mit einfachen Mitteln messen. Dazu wird die Volumenänderung in Abhängigkeit von der Temperatur gemessen. Die Daten werden
Prinzip Die Veränderung der Dichte von Wasser bei Änderung der Temperatur lässt sich mit einfachen Mitteln messen. Dazu wird die Volumenänderung in Abhängigkeit von der Temperatur gemessen. Die Daten werden
Grundwassermodell. 4.2 Wasserkreislauf. Einführung: Wir alle kennen den Wasserkreislauf:
 4.2 Wasserkreislauf Einführung: Wir alle kennen den Wasserkreislauf: Regen fällt zu Boden... und landet irgendwann irgendwie wieder in einer Wolke, die einen schon nach ein paar Stunden, die anderen erst
4.2 Wasserkreislauf Einführung: Wir alle kennen den Wasserkreislauf: Regen fällt zu Boden... und landet irgendwann irgendwie wieder in einer Wolke, die einen schon nach ein paar Stunden, die anderen erst
Aktueller Zustand der deutschen Gewässer
 Stand: Oktober 2016 Factsheet Aktueller Zustand der deutschen Gewässer Alle Gewässer in Deutschland müssen bis spätestens zum Jahr 2027 einen guten Zustand erreichen. Um dieses Ziel der EU- Wasserrahmenrichtlinie
Stand: Oktober 2016 Factsheet Aktueller Zustand der deutschen Gewässer Alle Gewässer in Deutschland müssen bis spätestens zum Jahr 2027 einen guten Zustand erreichen. Um dieses Ziel der EU- Wasserrahmenrichtlinie
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008
 Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Versuch 3: Säure-Base Titrationen Chemieteil, Herbstsemester 2008 Verfasser: Zihlmann Claudio Teammitglied: Knüsel Philippe Datum: 29.10.08 Assistent: David Weibel E-Mail: zclaudio@student.ethz.ch 1. Abstract
Regenwasseranalyse. Sommersemester Studienprojekt. Verfasst durch: Markus Siemssen. Lara Kreft. Betreuender Professor: Prof. Dr.
 Regenwasseranalyse Sommersemester 2014 Studienprojekt Verfasst durch: Markus Siemssen Lara Kreft Betreuender Professor: Prof. Dr. Elsholz Hochschule für Angewandte Wissenschaften Hamburg Campus Bergedorf
Regenwasseranalyse Sommersemester 2014 Studienprojekt Verfasst durch: Markus Siemssen Lara Kreft Betreuender Professor: Prof. Dr. Elsholz Hochschule für Angewandte Wissenschaften Hamburg Campus Bergedorf
Beispiele zu Neutralisationsreaktionen
 Beispiele zu Neutralisationsreaktionen Einleitung: Im Zuge des folgenden Blocks wird die Titration als Beispiel einer gängigen quantitativen Bestimmungsmethode in der Chemie genauer besprochen und für
Beispiele zu Neutralisationsreaktionen Einleitung: Im Zuge des folgenden Blocks wird die Titration als Beispiel einer gängigen quantitativen Bestimmungsmethode in der Chemie genauer besprochen und für
Bestimmung des Essigsäuregehalts von Speiseessig mittels Titration
 Grundlagenfach Chemie 4. Kl. 1/5 Bestimmung des Essigsäuregehalts von Speiseessig mittels Titration Einführung Säure-Base-Reaktion Eine Säure ist ein Teilchen, welches ein Wasserstoffion (H + ) abgeben
Grundlagenfach Chemie 4. Kl. 1/5 Bestimmung des Essigsäuregehalts von Speiseessig mittels Titration Einführung Säure-Base-Reaktion Eine Säure ist ein Teilchen, welches ein Wasserstoffion (H + ) abgeben
AnC I Protokoll: 6.1 Extraktionsphotometrische Bestimmung von Cobalt mit HDEHP! SS Analytische Chemie I. Versuchsprotokoll
 Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
Analytische Chemie I Versuchsprotokoll 6.1 Extraktionsphotometrische Bestimmung von Mikromengen an Cobalt mit Phosphorsäure-bis- (2-ethylhexylester) (HDEHP) 1.! Theoretischer Hintergrund Zur Analyse wird
SÄUR E. BASE oder LAU GE SAUE R BASI SCH
 SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
SÄUR E BASE oder LAU GE SAUE R BASI SCH INDIKATOR (Ital. indicare, heißt zeigen oder anzeigen) Das Forscherlabor Wir treiben es bunt im Forscherlabor Rechtenthal in Tramin! Datum: Name:. Klasse: Lehrpersonen:
Bestimmung des Stickstoffgehalts von Erde
 Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
Bestimmung des Stickstoffgehalts von Erde Schülerversuch, ca. 25 Minuten Experiment Teil 1 Material und Chemikalien: Ofentrockene Erde Kaliumchloridlösung (c = 2 mol/l) Flasche (250 ml) Trichter Filterpapier
Auen Bewertung Gewässerdynamik. Kantonsschule Wettingen Variowoche Eine Bewertung von. Chantal Hischier, Abteilung G2G
 Auen Bewertung Gewässerdynamik Eine Bewertung von Chantal Hischier Abteilung G2G Kantonsschule Wettingen Variowoche 2014 Leitende Lehrpersonen Michael Studer Sibylle Stämpfli Inhaltsverzeichnis 1. Grund
Auen Bewertung Gewässerdynamik Eine Bewertung von Chantal Hischier Abteilung G2G Kantonsschule Wettingen Variowoche 2014 Leitende Lehrpersonen Michael Studer Sibylle Stämpfli Inhaltsverzeichnis 1. Grund
Wie wirkt sich die Zugabe von Salz auf den Schmelz- und Siedepunkt von Wasser aus?
 Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Naturwissenschaften - Chemie - Allgemeine Chemie - 7 Chemische Bindung (P752400) 7.4 Schmelzpunktserniedrigung und Siedepunktserhöhung Experiment von: Phywe Gedruckt:.0.203 3:5:43 intertess (Version 3.06
Posten 2: Experiment Wasserkraft Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Die Sch lösen in Gruppen den vorliegenden Posten unter Einbezug der vorhandenen Unterlagen und Materialien. Ziel Material Sozialform Die Sch sind in der Lage, die beschriebene
Lehrerinformation 1/5 Arbeitsauftrag Die Sch lösen in Gruppen den vorliegenden Posten unter Einbezug der vorhandenen Unterlagen und Materialien. Ziel Material Sozialform Die Sch sind in der Lage, die beschriebene
Praktikum Quantitative Analysen
 Praktikum Quantitative Analysen Wintersemester 2009/10 Arbeitsmethoden der Quantitativen Analyse A: klassische Methoden vorwiegend chemische Arbeitsmethoden Bestimmung der Bestandteile durch eine chemische
Praktikum Quantitative Analysen Wintersemester 2009/10 Arbeitsmethoden der Quantitativen Analyse A: klassische Methoden vorwiegend chemische Arbeitsmethoden Bestimmung der Bestandteile durch eine chemische
Antwort 31 Die Fließgeschwindigkeit des Abwassers wird vermindert. Frage 31 Wodurch erreicht man im Sandfang, dass sich der Sand absetzt?
 Frage 31 Wodurch erreicht man im Sandfang, dass sich der Sand absetzt? Antwort 31 Die Fließgeschwindigkeit des Abwassers wird vermindert. Frage 32 Welche Stoffe sind im Abwasser, die dort nicht hinein
Frage 31 Wodurch erreicht man im Sandfang, dass sich der Sand absetzt? Antwort 31 Die Fließgeschwindigkeit des Abwassers wird vermindert. Frage 32 Welche Stoffe sind im Abwasser, die dort nicht hinein
Ergänzende Informationen zum Praktikum
 Philipps-Universität Marburg Medipraktikum Ergänzende Informationen zum Praktikum Assistent: Markus Dörr E-mail: markusdoerr@hotmail.de Wintersemester 10/11 Inhaltsverzeichnis Inhaltsverzeichnis 1 Allgemeine
Philipps-Universität Marburg Medipraktikum Ergänzende Informationen zum Praktikum Assistent: Markus Dörr E-mail: markusdoerr@hotmail.de Wintersemester 10/11 Inhaltsverzeichnis Inhaltsverzeichnis 1 Allgemeine
Orisbach. Wasserqualität und Äusserer Aspekt 2009/2010. und Umweltschutzdirektion Kanton Basel-Landschaft. Amt für Umweltschutz und Energie
 4410 Liestal, Rheinstrasse 29 Telefon 061 552 55 05 Telefax 061 552 69 84 Bau- und Umweltschutzdirektion Kanton Basel-Landschaft Amt für Umweltschutz und Energie Orisbach Wasserqualität und Äusserer Aspekt
4410 Liestal, Rheinstrasse 29 Telefon 061 552 55 05 Telefax 061 552 69 84 Bau- und Umweltschutzdirektion Kanton Basel-Landschaft Amt für Umweltschutz und Energie Orisbach Wasserqualität und Äusserer Aspekt
Die Europäische Wasserrahmenrichtlinie
 Die Europäische Wasserrahmenrichtlinie Monitoring Grundwasser und Seen Die Europäische Wasserrahmenrichtlinie Die EU-Wasserrahmenrichtlinie Monitoring Seen Die Europäische Folie: 2 Wasserrahmenrichtlinie
Die Europäische Wasserrahmenrichtlinie Monitoring Grundwasser und Seen Die Europäische Wasserrahmenrichtlinie Die EU-Wasserrahmenrichtlinie Monitoring Seen Die Europäische Folie: 2 Wasserrahmenrichtlinie
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch zwischen Flß. km 60,7 und Flß. km 43,1 im Jahr 2014
 Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch zwischen Flß. km 60,7 und Flß. km 43,1 im Jahr 2014 Meßstellen: Brücke Birkenfeld Flß.km 60,7 und Trafo oberhalb Dachsbach Anlagen: Diagramme
Analyse der Chemischen Wasseruntersuchungen der mittleren Aisch zwischen Flß. km 60,7 und Flß. km 43,1 im Jahr 2014 Meßstellen: Brücke Birkenfeld Flß.km 60,7 und Trafo oberhalb Dachsbach Anlagen: Diagramme
1. Sicheres Experimentieren
 1. Sicheres Experimentieren Versuchsanleitung vor der Stunde sorgfältig lesen, allfällige Fragen und Unklarheiten notieren. Genau nach Anweisung arbeiten und nur die vorgeschriebenen Arbeiten durchführen.
1. Sicheres Experimentieren Versuchsanleitung vor der Stunde sorgfältig lesen, allfällige Fragen und Unklarheiten notieren. Genau nach Anweisung arbeiten und nur die vorgeschriebenen Arbeiten durchführen.
Übungsblatt zu Säuren und Basen
 1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
1 Übungsblatt zu Säuren und Basen 1. In einer wässrigen Lösung misst die Konzentration der Oxoniumionen (H 3 O + ) 10 5 M. a) Wie gross ist der ph Wert? b) Ist die Konzentration der OH Ionen grösser oder
Baden in der Aare. Qualitätsklasse C Qualitätsklasse D. Qualitätsklasse B. Spielen am Wasser (Foto: creato)
 Erholung und Freizeit Baden in der Aare Das kantonale Labor des Gesundheitsamtes überprüft während der Badesaison an ausgewählten Stellen die hygienische Qualität des Aarewassers und des Wassers des Burgäschisees.
Erholung und Freizeit Baden in der Aare Das kantonale Labor des Gesundheitsamtes überprüft während der Badesaison an ausgewählten Stellen die hygienische Qualität des Aarewassers und des Wassers des Burgäschisees.
Stelle Stoffgemische aus Flüssigkeiten her und untersuche ihre Eigenschaften.
 Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
Naturwissenschaften - Chemie - Allgemeine Chemie - 2 Stoffgemische (P750700) 2.2 Flüssigkeitsgemische Experiment von: Phywe Gedruckt:.0.203 2:50:52 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufbau
Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease.
 A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
A 36 Michaelis-Menten-Kinetik: Hydrolyse von Harnstoff Aufgabe: Untersuchung der Kinetik der Zersetzung von Harnstoff durch Urease. Grundlagen: a) Michaelis-Menten-Kinetik Im Bereich der Biochemie spielen
Stofftransport. Kapitel 1: Aufgabe des Blutes 2.1 Der Stofftransport/Zellatmung / Seiten Bezug
 Stufe 3 2.1 / Das Blut Lehrerinformation 1/5 Bezug Kapitel 1: Aufgabe des Blutes 2.1 Der /Zellatmung / Seiten 12 13 Arbeitsauftrag Die Schüler beantworten die Fragen auf den Arbeitsblättern. Material Arbeitsblätter
Stufe 3 2.1 / Das Blut Lehrerinformation 1/5 Bezug Kapitel 1: Aufgabe des Blutes 2.1 Der /Zellatmung / Seiten 12 13 Arbeitsauftrag Die Schüler beantworten die Fragen auf den Arbeitsblättern. Material Arbeitsblätter
Biologie Referat für Felix
 Biologie Referat für Felix Sehr geehrter Herr Professor, liebe Mitschüler. Wir möchten euch mit unserem heutigen Referat das Wasser ein bißchen näher vorstellen. Wir haben unser Referat in 3 Abschnitte
Biologie Referat für Felix Sehr geehrter Herr Professor, liebe Mitschüler. Wir möchten euch mit unserem heutigen Referat das Wasser ein bißchen näher vorstellen. Wir haben unser Referat in 3 Abschnitte
Nitrifikation Nitritoxidation. Von Patrycja Kosnik und Nico Tennigkeit
 Nitrifikation Nitritoxidation Von Patrycja Kosnik und Nico Tennigkeit Als Nitrifikation bezeichnet man die Oxidation von Ammoniak über Nitrit zu Nitrat Die Oxidation ist in zwei Schritte unterteilt, wobei
Nitrifikation Nitritoxidation Von Patrycja Kosnik und Nico Tennigkeit Als Nitrifikation bezeichnet man die Oxidation von Ammoniak über Nitrit zu Nitrat Die Oxidation ist in zwei Schritte unterteilt, wobei
WIE GUT IST DAS WASSER VON MAIN, NIDDA UND URSELBACH?
 WIE GUT IST DAS WASSER VON MAIN, NIDDA UND URSELBACH? GK 13 Chemie & Dirk Schüpke Wenn man diese Frage beantworten will, dann muss man früh aufstehen und um 7 Uhr in Kelsterbach die erste Wasserprobe nehmen.
WIE GUT IST DAS WASSER VON MAIN, NIDDA UND URSELBACH? GK 13 Chemie & Dirk Schüpke Wenn man diese Frage beantworten will, dann muss man früh aufstehen und um 7 Uhr in Kelsterbach die erste Wasserprobe nehmen.
Säure-Base-Titrationen
 Säure-Base-Titrationen Dieses Skript gehört: Säure Base - Titrationen Seite 2 Hinweis: Mit den Säuren und Basen ist vorsichtig umzugehen, um Verätzungen zu vermeiden! Versuch 1: Herstellen einer Natronlauge
Säure-Base-Titrationen Dieses Skript gehört: Säure Base - Titrationen Seite 2 Hinweis: Mit den Säuren und Basen ist vorsichtig umzugehen, um Verätzungen zu vermeiden! Versuch 1: Herstellen einer Natronlauge
Gasthermometer. durchgeführt am von Matthias Dräger, Alexander Narweleit und Fabian Pirzer
 Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Gasthermometer 1 PHYSIKALISCHE GRUNDLAGEN durchgeführt am 21.06.2010 von Matthias Dräger, Alexander Narweleit und Fabian Pirzer 1 Physikalische Grundlagen 1.1 Zustandgleichung des idealen Gases Ein ideales
Titrationen. Experimentiermappe zum Thema. Lernwerkstatt Schülerlabor Chemie
 Lernwerkstatt Schülerlabor Chemie Experimentiermappe zum Thema Titrationen Friedrich-Schiller-Universität Jena Arbeitsgruppe Chemiedidaktik August-Bebel-Straße 6-8 07743 Jena Fonds der Chemischen Industrie
Lernwerkstatt Schülerlabor Chemie Experimentiermappe zum Thema Titrationen Friedrich-Schiller-Universität Jena Arbeitsgruppe Chemiedidaktik August-Bebel-Straße 6-8 07743 Jena Fonds der Chemischen Industrie
III. Tiefe Teichzone. Es gibt allerdings Unterscheidungen zwischen den Stillgewässern: See, Teich, Tümpel und Weiher.
 III. Tiefe Teichzone Bei einem Teich handelt es sich um ein künstlich angelegtes Stillgewässer, in welchem viele verschiedene Pflanzen- und Tierarten leben. Die meisten Gärten beherbergen Teiche, da sie
III. Tiefe Teichzone Bei einem Teich handelt es sich um ein künstlich angelegtes Stillgewässer, in welchem viele verschiedene Pflanzen- und Tierarten leben. Die meisten Gärten beherbergen Teiche, da sie
Anhang Zustand Solothurner Gewässer_Inhalt_def.indd :15
 Anhang Beurteilungskriterien für Oberflächengewässer und Grundwasser Beurteilungskriterien für Oberflächengewässer Biochemischer Sauerstoffbedarf (BSB 5 2 bis 4 mg/l O 2 Gelöster organischer Kohlenstoff
Anhang Beurteilungskriterien für Oberflächengewässer und Grundwasser Beurteilungskriterien für Oberflächengewässer Biochemischer Sauerstoffbedarf (BSB 5 2 bis 4 mg/l O 2 Gelöster organischer Kohlenstoff
Titration. Weiterbildung für fachfremd unterrichtende Lehrkräfte
 Titration Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Zerlegung der Verbindung Wasser Herstellung von Natronlauge Öltröpfchen versuch
Titration Weiterbildung für fachfremd unterrichtende Lehrkräfte Chromatografi e von Blattfarbstoffen Destillation von Rotwein Zerlegung der Verbindung Wasser Herstellung von Natronlauge Öltröpfchen versuch
Grundwasser: chemische Vorgänge bei der Infiltration. Redoxprozesse im Grundwasser Transport reaktiver Spezies
 Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Grundwasser: chemische Vorgänge bei der Infiltration Redoxprozesse im Grundwasser Transport reaktiver Spezies Belastungsquellen für Grundwasser Problematische Stoffe im Grundwasser für Trinkwassernutzung
Bestimmung des Salzgehaltes in Böden
 Bestimmung des Salzgehaltes in Böden Seminar: Methoden der chemischen, physikalischen und biologischen Bodenanalytik Julia C. Dziallas Landnutzung und Wasserbewirtschaftung 1 Gliederung 1. Grundlagen 2.
Bestimmung des Salzgehaltes in Böden Seminar: Methoden der chemischen, physikalischen und biologischen Bodenanalytik Julia C. Dziallas Landnutzung und Wasserbewirtschaftung 1 Gliederung 1. Grundlagen 2.
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Wie bestimmt ein Chemiker Säuren und Laugen?
 Wie bestimmt ein Chemiker Säuren und Laugen? Mit den Zahlen von 0 14 wird der ph Wert angegeben. 1 ist eine sehr starke Säure, 14 ist eine sehr starke Lauge. Aus: onlineenzyklopaedie.de Das Forscherlabor
Wie bestimmt ein Chemiker Säuren und Laugen? Mit den Zahlen von 0 14 wird der ph Wert angegeben. 1 ist eine sehr starke Säure, 14 ist eine sehr starke Lauge. Aus: onlineenzyklopaedie.de Das Forscherlabor
1 Aus dem Englischen übersetzt: Saps Photosynthese Kit
 Untersuchung der Photosynthese mit Algenbällen 1 Herstellung der Algenbälle: (Passend zur schriftlichen Beschreibung finden Sie die Arbeitsschritte auch in Bildern in der Datei (Herstellung von Algenbällen/Bilder)
Untersuchung der Photosynthese mit Algenbällen 1 Herstellung der Algenbälle: (Passend zur schriftlichen Beschreibung finden Sie die Arbeitsschritte auch in Bildern in der Datei (Herstellung von Algenbällen/Bilder)
Analytische Schnellverfahren im Vorfeld der instrumentellen Laboranalytik
 Analytische Schnellverfahren im Vorfeld der instrumentellen Laboranalytik Screening: - Begriff wird verwendet, wenn Test unter statistischen Gesichtspunkten durchgeführt werden (z.b. großflächige Untersuchungen,
Analytische Schnellverfahren im Vorfeld der instrumentellen Laboranalytik Screening: - Begriff wird verwendet, wenn Test unter statistischen Gesichtspunkten durchgeführt werden (z.b. großflächige Untersuchungen,
Welcher Unterschied besteht zwischen schwefliger Säure und Schwefelsäure?
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: Phywe Gedruckt: 5.0.203 :47:54 intertess (Version 3.06 B200, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - Säuren (P75800).2 Oxidation von schwefliger Säure Experiment von: Phywe Gedruckt: 5.0.203 :47:54 intertess (Version 3.06 B200, Export 2000) Aufgabe
Anleitung. Zum Herunterladen auf
 Anleitung Zum Herunterladen auf www.tatortgewaesser.de Einmalige Probenahme im Zeitraum vom 2.11. bis 15.11.2015 1 Zeitplan Mindestens ein Tag vor der Probenahme: Bereiten Sie sich zu Hause vor. Phase
Anleitung Zum Herunterladen auf www.tatortgewaesser.de Einmalige Probenahme im Zeitraum vom 2.11. bis 15.11.2015 1 Zeitplan Mindestens ein Tag vor der Probenahme: Bereiten Sie sich zu Hause vor. Phase
Saurer Regen, was ist das?
 Saurer Regen, was ist das? 1. SO x (x=2,3) => SO 2 und SO 3 SO 2 + H 2 O H 2 SO 3 (schwefelige Säure) SO 3 + H 2 O H 2 SO 4 (Schwefelsäure) 2. NO x (x=1,2) 2 NO + H 2 O + ½O 2 2 H NO 2 (salpetrige Säure)
Saurer Regen, was ist das? 1. SO x (x=2,3) => SO 2 und SO 3 SO 2 + H 2 O H 2 SO 3 (schwefelige Säure) SO 3 + H 2 O H 2 SO 4 (Schwefelsäure) 2. NO x (x=1,2) 2 NO + H 2 O + ½O 2 2 H NO 2 (salpetrige Säure)
Der Einfluss des Wassers auf die Qualität der Kühlschmierstoff-Emulsion
 Der Einfluss des Wassers auf die Qualität der KühlschmierstoffEmulsion Markus Kühni, Leiter Kundendienst Blaser Swisslube AG Winterseistrasse 3415 HasleRüegsau Tel: 034 460 01 01 email: contact@blaser.com
Der Einfluss des Wassers auf die Qualität der KühlschmierstoffEmulsion Markus Kühni, Leiter Kundendienst Blaser Swisslube AG Winterseistrasse 3415 HasleRüegsau Tel: 034 460 01 01 email: contact@blaser.com
Chemie zur Weihnacht. Farbreihe
 Farbreihe Reagenzien: 2 ml Phenolphthalein in 200 ml Wasser verdünnte Natronlauge in Tropfflasche Kaliumpermanganat 2,5 g Eisen(II)-sulfat in 50 ml Wasser 2,5 g Kaliumthiocyanat in 50 ml Wasser 2,5 g Kaliumhexacyanoferrat(II)
Farbreihe Reagenzien: 2 ml Phenolphthalein in 200 ml Wasser verdünnte Natronlauge in Tropfflasche Kaliumpermanganat 2,5 g Eisen(II)-sulfat in 50 ml Wasser 2,5 g Kaliumthiocyanat in 50 ml Wasser 2,5 g Kaliumhexacyanoferrat(II)
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Leckner See. Letzte Untersuchung. schwach windig Lufttemperatur: maximale Tiefe: Nutzung/Aktivität: Anmerkung:
 Leckner See Abbildung: Übersichtsplan, Lage der Probenstelle, Naturaufnahme Letzte Untersuchung Probenahme: 04.09.2006 Uhrzeit: 11:20 12:30 Witterung: heiter Wind: schwach windig Lufttemperatur: 22 C Sichttiefe:
Leckner See Abbildung: Übersichtsplan, Lage der Probenstelle, Naturaufnahme Letzte Untersuchung Probenahme: 04.09.2006 Uhrzeit: 11:20 12:30 Witterung: heiter Wind: schwach windig Lufttemperatur: 22 C Sichttiefe:
Ökologische Bestimmung der Güte von Fliessgewässern mit Bioindikatoren
 Ökologische Bestimmung der Güte von Fliessgewässern mit Bioindikatoren Lektüre / Hintergrund Paul Lassleben: "Gewässerdiagnose für jedermann." Kosmos 1983, Heft 6, S. 40-46. Abrufbar von: http://lernen.ksh.edu/bd/leitformen_fliessgewaesser_dburkhard/web-content/seite05_druckmat.html.
Ökologische Bestimmung der Güte von Fliessgewässern mit Bioindikatoren Lektüre / Hintergrund Paul Lassleben: "Gewässerdiagnose für jedermann." Kosmos 1983, Heft 6, S. 40-46. Abrufbar von: http://lernen.ksh.edu/bd/leitformen_fliessgewaesser_dburkhard/web-content/seite05_druckmat.html.
