Chemie. Hayley Birch. schlüssel ideen
|
|
|
- Walter Kramer
- vor 7 Jahren
- Abrufe
Transkript
1 Chemie Hayley Birch schlüssel ideen
2 Hayley Birch 50 Schlüsselideen Chemie Aus dem Englischen übersetzt von Angela Simeon
3 Inhalt Einleitung 3 01 Atome 4 02 Elemente 8 03 Isotope Verbindungen Wie alles zusammenhält Wechsel von Zustandsformen Energie Chemische Reaktionen Gleichgewichte Thermodynamik Säuren Katalysatoren Redox Gärung Cracken Chemische Synthese Das Haber-Bosch-Verfahren Chiralität Grüne Chemie Trennung Spektren Kristallographie Elektrolyse Fertigung im Mikromaßstab Selbstorganisation Lab-on-a-chip Computergestützte Chemie Kohlenstoff Wasser Der Ursprung des Lebens Astrochemie Proteine Enzymaktivität Zucker DNA Biosynthese Photosynthese Chemische Boten Kraftstoffe Kunststoffe CFKWs Verbundwerkstoffe Solarzellen Arzneistoffe Nanotechnologie Graphen D-Druck Künstliche Muskeln Synthetische Biologie Brennstoffe der Zukunft 200 Periodensystem der Elemente 204 Index 206
4 Einleitung 3 Einleitung Chemie wird oft als der Underdog unter den Naturwissenschaften betrachtet. Erst kürzlich sprach ich mit einer Chemikerin, die sagte, sie habe genug davon, dass ihr Fach als ein Haufen von Leuten, die mit übelriechenden Dingen im Labor herumfummeln gelte. Irgendwie scheint Chemie nicht so bedeutend wie Biologie und nicht so interessant wie Physik zu sein. Als Autorin eines Buches über Chemie ist es deshalb meine Aufgabe, Ihnen einen Blick hinter dieses Bild zu ermöglichen und Sie für den Underdog einzunehmen. Denn Chemie ist viele wissen das nicht die beste Naturwissenschaft. Chemie steckt im Kern von fast allem. Aus ihren Bausteinen Atome, Moleküle, Verbindungen und Mischungen besteht jedes Staubkorn und jede Faser auf diesem Planeten. Ihre Reaktionen sind dafür verantwortlich, dass es Leben gibt, und schaffen alles, wovon Leben abhängt. Ihre Produkte kennzeichnen den Fortschritt unserer Existenz als Menschen, von Bier bis zu Feinstrumpfhosen. Der Grund, warum Chemie ein Imageproblem hat, beruht meiner Meinung nach darauf, dass wir uns nicht auf die relevanten und interessanten Themen konzentrieren, sondern uns damit verzetteln, eine Garnitur Regeln zu lernen: Wie Chemie funktioniert, Formeln von molekularen Strukturen, Rezepte für Reaktionen und so weiter. Auch wenn Chemiker anführen mögen, dass diese Regeln und Rezepte wichtig sind, so werden doch die meisten zustimmen, dass sie nicht besonders spannend sind. Deshalb werden wir uns in diesem Buch nicht allzu viel mit Regeln befassen. Wenn Sie möchten, können Sie Regeln und Rezepte anderswo nachschlagen. Ich habe versucht, mich auf das zu konzentrieren, was relevant und interessant ist an der Chemie. Und nebenbei habe ich versucht, den Geist meines Chemielehrers Mr. Smailes einfließen zu lassen, der mir zeigte, wie ich Seife oder Nylon herstellen kann, und der wirklich großartige Krawatten trug.
5 4 Atome 01 Atome Atome sind die Bausteine der Chemie und unseres Universums. Sie bilden die Elemente, die Planeten, die Sterne und uns. Atome zu verstehen wie sie aufgebaut sind und wie sie aufeinander einwirken kann fast alles erklären, was bei chemischen Reaktionen im Labor und in der Natur passiert. Bill Bryson, der Autor von Ein kurze Geschichte von fast allem, schrieb, dass jeder einzelne von uns bis zu einer Milliarde Atome in sich tragen könnte, die einmal zu William Shakespeare gehörten. Hoppla, könnten Sie jetzt denken, das sind eine Menge tote Shakespeare-Atome. Nun, das stimmt und auch wieder nicht. Einerseits ist eine Milliarde ( ) etwa die Anzahl an Sekunden, die jeder von uns bis zu seinem 33. Geburtstag gelebt hat. Andererseits ist eine Milliarde etwa die Anzahl an Salzkörnchen, die in eine gewöhnliche Badewanne passen, und weniger als ein Milliardstel eines Milliardstels der Atome in Ihrem ganzen Körper. Dies deutet an, wie klein ein Atom ist: Es gibt mehr als eine Milliarde mal eine Milliarde mal eine Milliarde Atome nur in uns und es bedeutet, dass wir nicht genug toten Shakespeare in uns haben, um auch nur eine Gehirnzelle daraus zu bauen. Das Leben ist ein Pfirsich Atome sind so winzig, dass es bis vor Kurzem unmöglich war, sie zu sehen. Das hat sich mit der Entwicklung superhochauflösender Mikroskope insofern geändert als australische Wissenschaftler 2013 eine Aufnahme von dem Schatten machen konnten, den ein einzelnes Atom warf. Aber Chemiker mussten Atome nicht immer sehen, um zu verstehen, dass sich mit Atomen grundsätzlich das Meiste von dem erklären lässt, was im Reagenzglas und auch im Leben vor sich geht. Viele chemische Vorgänge beruhen auf den Aktivitäten von noch kleineren, subatomaren Teilchen, den Elektronen, die die äußeren Bereiche der Atome ausmachen. Wenn wir ein Atom wie einen Pfirsich in der Hand halten könnten, wäre der Stein des Pfirsichs das, was Nukleus (Atomkern) genannt wird. Er enthält die H. Birch, 50 Schlüsselideen Chemie, DOI / _1, Springer-Verlag Berlin Heidelberg 2016 Zeitleiste ca. 400 v. Chr. der griechische Philosoph Demokrit verwendet den Begriff Atom für kleinste, nicht weiter teilbare Bausteine 1803 John Dalton schlägt eine Atomtheorie vor 1904 Joseph John Thomsons Plum-Pudding-Modell des Atomaufbaus 1911 Ernest Rutherford beschreibt den Atomkern
6 Atome hielt der englische Chemiker John Dalton eine Vorlesung, in der er eine Theorie der Materie vorschlug. Sie beruhte auf unzerstörbaren Teilchen, welche er Atome nannte. Zusammengefasst sagte er, dass verschiedene Elemente auch ver- Protonen und Neutronen. All das saftige Pfirsichfleisch in Ihrer Hand bestünde aus Atomtheorie und chemische Elektronen. Wenn der Pfirsich tatsächlich Reaktionen ein Atom wäre, bestünde er hauptsächlich aus Fleisch, und der Stein wäre so klein, dass Sie ihn schlucken könnten, ohne es auch nur zu bemerken so viel Raum des Atoms machen die Elektronen aus. Doch schiedene Atome besitzen, die sich zu unter- der feste Kern ist es, der das Atom zusammenhält. Die Protonen darin sind positiv geladene Teilchen, die gerade genug Anziehung auf die negativ geladenen Elektronen Umverteilung dieser Atome gehört. ausüben, um sie davon abzuhalten, bei der ersten Gelegenheit in alle Richtungen davonzufliegen. schiedlichen Verbindungen zusammenfügen können, und dass zu chemischen Reaktionen eine Warum ist ein Sauerstoff-Atom ein Sauerstoff-Atom? Nicht alle Atome sind gleich. Ihnen ist vielleicht schon klar, dass ein Atom nicht allzu viel Ähnlichkeit mit einem Pfirsich hat, doch lassen Sie uns die Analogie noch ein wenig weiter treiben. Atome gibt es in vielen verschiedenen Geschmacksrichtungen. Wenn unser Pfirsich ein Sauerstoff-Atom ist, könnte eine Pflaume vielleicht ein Kohlenstoff-Atom sein. Beides sind kleine Bälle aus Elektronen, die einen Proton-Kern umgeben, aber mit völlig verschiedenen Eigenschaften. Sauerstoff- Atome schweben als Paare herum (O 2 ), während Kohlenstoff-Atome in Massen zusammenkleben und harte Stoffe wie Diamant oder den Graphit in Bleistiftminen bilden. Was sie zu unterschiedlichen Elementen macht ( Kap. 2), ist ihre jeweilige Anzahl von Protonen im Kern. Sauerstoff-Atome haben acht Protonen, zwei mehr als Kohlenstoff-Atome. Wirklich große, schwere Elemente wie Seaborgium und Nobelium haben mehr als hundert Protonen im Inneren ihrer Atome. Wenn so viele positive Ladungen in den verschwindend geringen Platz des Atomkerns gestopft werden, die sich alle gegenseitig abstoßen, gerät das Gebilde leicht aus dem Gleichgewicht. Deshalb sind sehr schwere Elemente instabil Forscher bei IBM fügen einzelne Atome zum Schriftzug IBM 2012 Entdeckung des Higgs-Bosons bestätigt das Standardmodell des Atoms
7 6 Atome Das Atom spalten J. J. Thomson betrachtete in seinem frühen Plum-Pudding-Modell das Atom als eine teigige, positiv geladene Masse, in der negativ geladene Elektronen wie Rosinen im Kuchen gleichmäßig verteilt sind. Diese Modellvorstellung hat sich verändert. Wir wissen inzwischen, dass Protonen und andere subatomare Teilchen, die Neutronen genannt werden, den winzigen, sehr dichten Kern der Atome bilden, und die Elektronen eine Art Wolke um den Kern herum ausmachen. Wir wissen auch, dass Protonen und Neutronen noch kleinere Teilchen enthalten, die wir Quarks nennen. Chemiker gehen normalerweise nicht weiter auf diese kleineren Teilchen ein sie werden von Physikern untersucht, die Atome in Teilchenbeschleunigern in Stücke zerschlagen, um die kleineren Teilchen zu finden. Aber für uns ist es wichtig, nicht zu vergessen, dass sich die Vorstellungen der Wissenschaftler darüber, wie sich die Materie in unserem Universum zusammenfügt, immer noch weiterentwickeln. Der Entdeckung des Higgs-Bosons im Jahr 2012 bestätigte zum Beispiel die Existenz eines Teilchens, das Physiker bereits in Elektron Nukleus Neutron Proton Der unglaublich dichte Kern eines Atoms enthält positiv geladene Protonen und neutrale Neutronen. Sie werden umrundet von negativ geladenen Elektronen. ihre Modelle aufgenommen hatten und das sie benutzten, um Vorhersagen über andere Teilchen zu machen. Doch sie müssen immer noch herausfinden, ob es sich auch um genau das Higgs-Boson handelt, das sie gesucht hatten. Normalerweise wird ein Atom egal welcher Geschmacksrichtung die gleiche Anzahl Elektronen haben, wie es Protonen im Kern besitzt. Wenn ein Elektron verlorengeht oder das Atom ein zusätzliches Elektron einsammelt, dann sind die positiven und negativen Ladungen nicht mehr im Gleichgewicht, und aus dem Atom wird, wie die Chemiker sagen, ein Ion ein geladenes Atom oder Molekül. Ionen sind wichtig, denn ihre Ladungen helfen, alle möglichen Arten von Stoffen zusammenzuhalten, zum Beispiel das Natriumchlorid von Kochsalz oder das Calciumcarbonat der Kalkränder in unseren Bädern. Die Bausteine des Lebens Neben Bestandteilen unserer Küchenschränke und Bäder ist alles, was krabbelt, atmet oder Wurzeln schlägt, aus Atomen auf-
8 Atome 7 gebaut. Atome fügen sich zu verblüffend komplexen Molekülen wie der DNA und den Proteinen zusammen, die unsere Muskeln, Knochen und unser Haar bilden. Sie tun dies, indem sie mit anderen Atomen Bindungen eingehen ( Kap. 5). Interessant daran ist, dass alle Lebensformen auf der Erde, trotz ihrer enormen Vielfalt, Atome einer ganz bestimmten Geschmacksrichtung enthalten: Kohlenstoff. Von Bakterien, die sich um die rauchenden Tiefseeschlote herum an den tiefsten, dunkelsten Plätzen der Ozeane an ihr Die Schönheit eines Lebewesens beruht nicht auf den Atomen, die es enthält, sondern in der Art, wie sich diese Atome zusammenfügen. ʻ Carl Sagan Leben klammern, bis zu den Vögeln, die in die Himmel aufsteigen, gibt es kein Lebewesen auf unserem Planeten, das das Element Kohlenstoff nicht mit den anderen gemeinsam hat. Doch weil wir noch kein Leben außerhalb unseres Planeten entdeckt haben, können wir nicht sagen, ob sich das Leben einfach nur zufällig auf diese Art entwickelte oder ob Leben auch auf der Basis anderer Atomarten gedeihen könnte. Science-Fiction-Fans sind andere biologische Formen wohlbekannt: Wesen auf Siliciumbasis sind zum Beispiel in der TV-Serie Star Trek und den Star-Wars-Filmen aufgetreten. Atom um Atom Fortschritte auf dem Gebiet der Nanotechnologie ( Kap. 45), die uns von effizienteren Solarzellen bis zu medizinischen Wirkstoffen, die Krebszellen erkennen und zerstören können, alles verspricht, haben die Welt der Atome verstärkt ins Scheinwerferlicht gerückt. Die Werkzeuge der Nanotechnologie hantieren im Größenbereich von einem Milliardstel Millimeter. Das ist immer noch größer als ein Atom, doch in dieser Größenordnung lässt sich darüber nachdenken, Atome und Moleküle einzeln zu handhaben. Forscher bei IBM drehten 2013 den kleinsten Kurzfilm der Welt, indem sie im Stop-Motion-Verfahren einen Jungen aufnahmen, der mit einem Ball spielt. Sowohl der Junge als auch der Ball bestehen aus einzeln erkennbaren Kohlenmonoxid-Molekülen auf einer Leinwand aus Kupfer. Damit beginnt die Naturwissenschaft endlich, in Größenordnungen zu arbeiten, die der Sicht der Chemiker auf die Welt entsprechen. Worum es geht Bausteine
9 8 Elemente 02 Elemente Chemiker bemühen sich sehr, neue Elemente, die grundlegenden chemischen Stoffe, zu entdecken. Das Periodensystem der Elemente hilft uns, ihre Entdeckungen zu ordnen. Doch es ist nicht nur ein Verzeichnis. Muster im Periodensystem geben uns Hinweise auf das Wesen jedes Elements und wie es sich verhalten könnte, wenn es auf andere Elemente trifft. Hennig Brand, Alchemist im 17. Jahrhundert, war auf Gold aus. Nach der Hochzeit gab er seinen Beruf als Armeeoffizier auf und nutzte das Geld seiner Frau, um eine Suche nach dem Stein der Weisen zu finanzieren eine mystische Substanz oder ein Mineral, nach dem Alchemisten bereits seit Jahrhunderten suchten. Der Legende nach konnte der Stein gewöhnliche Metalle wie Eisen oder Blei in Gold transmutieren. Als seine erste Frau starb, heiratete Brand nochmals und setze seine Suche auf ähnliche Weise fort. Offensichtlich war er auf die Idee gekommen, der Stein der Weisen ließe sich aus Körpersäften gewinnen. Deshalb erwarb er nicht weniger als 1500 Gallonen menschlichen Urins, aus dem er den Stein extrahieren wollte machte er eine erstaunliche Entdeckung. Es war jedoch nicht der Stein der Weisen, den er gefunden hatte. Durch seine Experimente, zu denen das Kochen und Auftrennen des Urins gehörte, wurde Brand unwissentlich der erste Mensch, der ein Element mit chemischen Methoden entdeckte. Brand hatte eine Substanz isoliert, die Phosphor enthielt und die er kaltes Feuer nannte, da sie im Dunkeln leuchtete. Aber erst in den 1770er-Jahren wurde Phosphor als neues Element erkannt. Zu dieser Zeit wurden ständig neue Elemente entdeckt: Sauerstoff, Stickstoff, Chlor und Mangan wurden von Chemikern innerhalb eines einzigen Jahrzehnts erstmals isoliert. 1869, zwei Jahrhunderte nach Brands Entdeckung, ordnete der russische Chemiker Mendelejew die damals bekannten Elemente zum Periodensystem. Phosphor erhielt darin seinen rechtmäßigen Platz, zwischen Silicium und Schwefel. H. Birch, 50 Schlüsselideen Chemie, DOI / _2, Springer-Verlag Berlin Heidelberg 2016 Zeitleiste 1669 Phosphor als erstes Element über chemische Methoden entdeckt 1869 Dmitri Iwanowitsch Mendelejew veröffentlicht die erste Fassung seines Periodensystems 1913 Henry Mosely definiert Elemente über ihre Ordnungszahl
10 Elemente 9 Was ist ein Element? Lange Zeit wurden Feuer, Luft, Wasser und Erde als die Das Periodensystem entziffern Elemente betrachtet. Ein geheimnisvolles Im Periodensystem werden die Elemente durch fünftes Element, Äther, wurde hinzugefügt, Buchstaben dargestellt. Einige Buchstaben sind offensichtliche Abkürzungen, wie Si für Silicium, das die Sterne repräsentieren sollte, denn diese, so der Philosoph Aristoteles, konnten nicht aus den irdischen Elementen zusammengesetzt sein. Der Begriff Element stammt von dem lateinischen Wort die Anzahl von Nukleonen (also Protonen plus elementum ab und bedeutet erstes Prinzip oder Grundform das ist keine tiefgestellte Zahl (die Ordnungszahl) gibt die Anzahl der Protonen an. schlechte Beschreibung, doch sie klärt uns nicht auf über die Unterscheidung zwischen Elementen und Atomen. Diese Unterscheidung ist einfach: Elemente sind Stoffe, in beliebigen Mengen, Atome sind ihre grundlegenden Einheiten. Ein fester Klumpen von Brands Phosphor der zufällig ein giftiges Element ist und Bestandteil von Nervengas ist eine Ansammlung von Atomen eines bestimmten Elements. Merkwürdigerweise wird nicht jeder Klumpen Phosphor gleich aussehen, denn seine Atome können sich unterschiedlich anordnen, und mit dem Wechsel der inneren Struktur ändert sich auch die äußere Erscheinung. Je nachdem, wie die Atome in Phosphor angeordnet sind, kann der Klumpen weiß, schwarz, rot oder violett aussehen. Diese unterschiedlichen Phosphorsorten verhalten sich auch unterschiedlich, zum Beispiel schmelzen sie bei sehr verschiedenen Temperaturen. Weißer Phosphor etwa schmilzt an einem warmen Tag bereits in der Sonne, während schwarzer Phosphor in einem kräftigen Heizofen auf über 600 C erhitzt werden muss. Dennoch bestehen beide aus genau den gleichen Atomen mit 15 Protonen und 15 Elektronen. während andere, wie H für Wasserstoff, zunächst keinen logischen Sinn zu haben scheinen sie leiten sich oft von altertümlichen Bezeichnungen ab. Die Zahl über den Buchstaben ist die Massenzahl Neutronen) in den Atomkernen des Elements. Die Muster im Periodensystem Für das ungeübte Auge sieht das Periodensystem wie eine ungewöhnliche Variante des Spiels Tetris aus, bei dem je nach der Version, die Sie spielen einige Blöcke nicht bis auf den Boden gefallen sind. Es wirkt, als könnte es eine Runde Aufräumen gebrauchen. Doch in Wirk das erste künstlich erzeugte Element, Technetium, wird nachgewiesen 2000 russische Wissenschaftler stellen das superschwere Element Livermorium her 2010 Synthese des Elements mit der Ordnungszahl 117 ( Ununseptium ) wird bekanntgegeben
11 10 Elemente lichkeit ist es ein wohlsortiertes Durcheinander, und jede/r Chemiker/in wird in der scheinbaren Unordnung schnell das finden, was er oder sie sucht. Das kommt daher, dass Mendelejews schlaues Design versteckte Muster enthält, die die Elemente nach ihren Atomstrukturen und ihrem chemischen Verhalten untereinander verknüpfen. Entlang den Tabellenreihen, von links nach rechts, sind die Atome nach ihrer Ordnungszahl angeordnet, also nach der Anzahl von Protonen in den Atomkernen jedes Elements. Das Geniale von Mendelejews Anordnung liegt darin, zu zeigen, wann die Eigenschaften der Elemente anfangen, sich zu wiederholen, und eine neue Reihe beginnen muss. Es sind deshalb die Spalten, die uns einige spitzfindigere Hinweise liefern. Nehmen wir einmal die Spalte ganz rechts, von Helium zu Radon. Das sind die Edelgase, unter normalen Bedingungen farblose Gase und recht träge, wenn es darum geht, bei einer chemischen Reaktion mitzumachen. Neon ist zum Beispiel so unreaktiv, dass es nicht überredet werden kann, auch nur mit einem anderen Element eine Verbindung Die Welt der chemischen Reaktionen ist wie eine Bühne Die Schauspieler auf ihr sind die Elemente. ʻ Clemens Alexander Winkler, Entdecker des Elements Germanium einzugehen. Der Grund dafür hängt mit seinen Elektronen zusammen. Bei jedem Atom sind die Elektronen in konzentrischen Schichten oder Schalen angeordnet, in denen nur für eine bestimmte Zahl von Elektronen Platz ist. Wenn eine Schale gefüllt ist, müssen die nächsten Elektronen in eine neue, weiter außen liegende Schale ausweichen. Und weil die Anzahl von Elektronen in den Atomen aller Elemente mit der Ordnungszahl ansteigt, hat jedes Element auch eine ganz bestimmte Elektronenanordnung. Das Hauptmerkmal der Edelgase ist, dass ihre äußersten Schalen voll sind. Diese vollen Schalen sind sehr stabil, das heißt, die Elektronen lassen sich nur sehr schwer mobilisieren. Wir können noch viele andere Muster im Periodensystem erkennen. Wenn wir uns in den Reihen von links nach rechts bewegen, braucht es immer mehr Anstrengung (Energie), ein Elektron von einem Atom der einzelnen Elemente wegzunehmen, und dasselbe gilt, wenn wir uns von unten nach oben bewegen. In der Mitte der Tabelle finden wir hauptsächlich Metalle, und diese verhalten sich umso metallischer, je weiter wir uns der linken unteren Ecke nähern. Chemiker nutzen ihr Wissen über diese Muster, um vorherzusagen, wie sich Elemente bei Reaktionen verhalten. Superschwergewichte Eines der wenigen Dinge, die Chemie und Boxen gemeinsam haben, ist, dass es bei beiden Superschwergewichte gibt. Während die Fliegengewichte an der Spitze des Periodensystems schwimmen, allen
12 Elemente 11 Die Jagd nach dem schwersten Superschweren Niemand mag Schwindler, doch sie finden sich in allen Bereichen, die Naturwissenschaften sind keine Ausnahme haben Wissenschaftler des Lawrence Berkeley Labors in Kalifornien einen Artikel veröffentlicht, in dem sie ihre Entdeckung der superschweren Elemente 116 (Livermorium) und 118 (Ununoctium) feierten. Aber irgendetwas stimmte nicht. Nachdem sie den Bericht gelesen hatten, versuchten andere Wissenschaftler, die Experimente zu wiederholen. Doch egal, wie sie es anstellten, sie konnten kein einziges Atom von Element 116 heraufbeschwören. Schließlich stellte sich heraus, dass einer der Entdecker die Daten erfunden hatte, und eine US-Regierungsstelle musste einen peinlichen Rückzieher von Aussagen über die Weltklasse-Wissenschaft machen, die sie finanzierte. Der Artikel wurde zurückgezogen, und der Beifall für die Entdeckung von Livermorium ging ein Jahr später an eine russische Arbeitsgruppe. Der Wissenschaftler, der die ursprünglichen Daten gefälscht hatte, wurde entlassen. Das Prestige, das mit der Entdeckung eines neuen Elements verbunden wird, ist so hoch, dass Wissenschaftler unter Umständen ihre ganze Karriere dafür aufs Spiel setzen. voran Wasserstoff und Helium mit nur einem beziehungsweise zwei Protonen, werden die Elemente in den tieferen Reihen durch ihre hohen Atomgewichte nach unten gezogen. Das Periodensystem ist über viele Jahre gewachsen und hat viele neue Entdeckungen und schwerere Elemente aufgenommen. Doch mit Nummer 92, dem radioaktiven Element Uran, ist das letzte natürlich vorkommende Element erreicht. Obwohl durch den radioaktiven Zerfall von Uran Plutonium entsteht, sind die Mengen verschwindend gering. Plutonium wurde in einem Atomreaktor entdeckt, und die anderen Superschwergewichte werden gefunden, indem in Teilchenbeschleunigern Atome aufeinander geschleudert werden. Die Jagd ist noch nicht völlig vorüber, doch sie ist gewiss sehr viel schwieriger geworden als das Erhitzen von Körpersäften. Worum es geht Die einfachsten Stoffe
13 12 Isotope 03 Isotope Isotope sind nicht nur tödliche Stoffe, die beim Bau von Bomben und zur Vergiftung von Menschen eingesetzt werden. Isotope gibt es von vielen chemischen Elementen, die eine leicht unterschiedliche Zusammensetzung an kleinsten, subatomaren Teilchen haben. Sie kommen in der Luft vor, die wir atmen, ebenso wie im Wasser, das wir trinken. Wir können mit ihnen sogar vollkommen ungefährlich Eis sinken lassen. Eis schwimmt außer es geht unter. So, wie alle Atome eines Elements gleich sind außer sie unterscheiden sich. Wenn wir das einfachste Element nehmen, Wasserstoff, so besitzen all seine Atome ein Proton und ein Neutron. Ein Wasserstoff-Atom ist nur dann ein Wasserstoff-Atom, wenn es ein Elektron hat sowie in seinem Kern ein Proton. Doch was geschieht, wenn zu dem Proton ein Neutron kommt? Ist es immer noch ein Wasserstoff-Atom? Neutronen waren das fehlende Glied, das sich Chemikern und Physikern bis in die 1930er-Jahre entzog ( Box: Die fehlenden Neutronen). Diese neutralen Teilchen ändern nichts am Gesamtgleichgewicht der Ladungen in einem Atom, können aber seine Masse stark beeinflussen. Der Masseunterschied zwischen einem und zwei Nukleonen im Kern der Wasserstoff-Atome reicht aus, Eis sinken zu lassen. Schweres Wasser Ein zusätzliches Neutron in ein Wasserstoff-Atom zu packen, heißt für diese Fliegengewichtsatome, dass sie nun die doppelte Anzahl an Nukleonen besitzen. Dieser schwerere Wasserstoff hat einen eigenen Namen, Deuterium (D oder 2 H). Genau wie normale Wasserstoff-Atome verbinden sich Deuterium-Atome mit Sauerstoff-Atomen zu Wasser. Nur sind dies keine normalen Wassermoleküle (H 2 O), sondern Moleküle mit zusätzlichen Neutronen: schweres Wasser oder D 2 O der korrekte Name ist Deuteriumoxid. Nehmen Sie schweres Wasser das leicht online zu kaufen ist und lassen Sie es in einem Eiswürfelbehälter gefrieren: In ein Glas mit normalem H. Birch, 50 Schlüsselideen Chemie, DOI / _3, Springer-Verlag Berlin Heidelberg 2016 Zeitleiste um 1500 Alchemisten versuchen, Stoffe zu transmutieren, um sie in Edelmetalle zu verwandeln 1896 radioaktive Strahlung wird erstmals zur Behandlung von Krebs eingesetzt 1920 Ernest Rutherford vermutet, es gibt ein Kernteilchen ohne Ladung, das Neutron
14 Isotope 13 Die Entdeckung der Neutronen durch den Physiker James Chadwick, der später an der Entwicklung der Atombombe mitarbeitete, löste ein quälendes Problem mit den Massen der Atome. Schon seit Jahren war offensichtlich, dass die Atome aller Elemente schwerer waren, als sie sein sollten. Nach Chadwicks Meinung konnten Atomkerne nicht diese Massen haben, wenn sie nur Protonen enthielten. Es war, als ob die Elemente mit einem Koffer voller Ziegelsteine in Urlaub fahren wollten. Nur, dass keiner diese Ziegelsteine entdecken konnte. Chadwick hatte von Rutherford, bei dem er gearbeitet hatte, die Überzeugung übernommen, dass Atome weitere subatomare Teilchen schmuggeln. Rutherford beschrieb diese neutral doublets oder Neutronen erstmals Doch es dauerte bis 1932, bis Chadwick seine Vermutung experimentell beweisen konnte. Er fand heraus, dass beim Beschießen des Die fehlenden Neutronen silbrigen Metalls Beryllium mit Strahlung aus Polonium elektrisch neutrale subatomare Teilchen ausgestoßen werden: Neutronen. Vakuumpumpe Poloniumquelle Berylliumplatte alpha-teilchen luftleerer Raum Detektor Neutron Die Reaktion, mit der Neutronen (n) aus Beryllium herausgeschleudert werden, lautet: 4 2 He Be 1 0 n C Wasser gegeben, wird dieser Eiswürfel sinken! Geben Sie zum Vergleich noch einen gewöhnlichen Eiswürfel hinzu und staunen Sie über den Unterschied, den ein einziges subatomares Teilchen pro Atom ausmacht! Im Durchschnitt findet sich in etwa einem von 6400 Wasserstoff-Atomen zusätzlich ein Neutron. Es gibt aber auch noch eine dritte Art ein drittes Isotop von Wasserstoff, und diese ist viel seltener und zu Hause weit unsicherer zu handhaben. Tritium (T oder 3 H) ist ein Wasserstoff-Isotop, bei dem jeder Atomkern ein Proton und zwei Neutronen besitzt. Wie auch andere radioaktive Elemente unterliegt es radioaktivem Zerfall. Tritium wird bei dem Mechanismus eingesetzt, mit dem Wasserstoffbomben gezündet werden. Radioaktivität Wenn wir das Wort Isotop lesen, steht häufig der Zusatz radioaktiv davor. Wir könnten deshalb vermuten, dass alle Isotope radioaktiv 1932 James Chadwick entdeckt das Neutron 1960 Willard Libby erhält den Nobelpreis für die Entwicklung der Radiokarbondatierung mit dem Isotop 14 C 2006 der russische Geheimdienst - agent Alexander Litvinenko stirbt an einer Vergiftung durch radioaktives Polonium
15 14 Isotope sind. Sie sind es nicht. Wie wir eben gesehen haben, ist es problemlos möglich, dass ein Wasserstoff-Isotop existiert, das nicht radioaktiv ist mit anderen Worten: ein stabiles Isotop. Ganz genauso kommen in der Natur stabile Isotope von Kohlenstoff, Sauerstoff und anderen Elementen vor. Instabile radioaktive Isotope zerfallen. Das heißt, ihre Atome zerbrechen und geben dabei Material aus ihrem Inneren in Form von Protonen, Neutronen und Elektronen frei ( Box: Arten radioaktiver Strahlung). Das Ergebnis ist, dass sich ihre Massezahlen ändern und sie sich auch in ganz andere Elemente verwandeln können. Für die Alchemisten des 16. und 17. Jahrhunderts, die davon besessen waren, einen Weg zur Umwandlung eines Elements in ein anderes (idealerweise in Gold) zu finden, hätte der radioaktive Zerfall wie Magie ausgesehen. Alle radioaktiven Elemente zerfallen mit unterschiedlichen Raten. Kohlenstoff-14 ( 14 C), eine Form von Kohlenstoff mit acht Neutronen anstelle der üblichen sechs (plus jeweils sechs Protonen), kann gefahrlos und ohne besondere Vorkehrungen gehandhabt werden. Wenn wir ein Gramm Kohlenstoff-14 abmessen und aufs Fensterbrett legen wollten, müssten wir ziemlich lange auf den Zerfall warten: Es würde 5700 Jahren dauern, bis die Hälfte der Atome zerfallen wäre. Diese Zeitangabe, die Zerfallsrate, wird Halbwertszeit genannt. Polonium-214 hat im Gegensatz zu Kohlenstoff-14 eine Halbwertszeit von weniger als einer tausendstel Sekunde. In einer wahnwitzigen Parallelwelt, in der das Abwiegen von einem Gramm radioaktiven Poloniums erlaubt wäre, würden wir es nicht schaffen, es auch nur auf das Fensterbrett zu legen, bevor alles unter Aussendung gefährlicher Strahlung zerfallen wäre. Arten radioaktiver Strahlung Der frühere russische Geheimdienstagent Alexander Litvinenko und möglicherweise auch Palästinenserführer Jassir Arafat wurden mit einem stabileren Isotop von Polonium getötet, das innerhalb von ein paar Tagen und nicht innerhalb von Sekunden zerfällt, wenngleich auch dieses tödlich ist. Im menschlichen Körper durchdringt die Strahlung, die die zerfallenden Polonium-210-Atome aussenden, die Zellen und führt so zu Schmerzen, Übelkeit und dem Versagen des Immunsystems. Bei der Untersu- Alpha-Strahlen bestehen aus zwei Protonen und zwei Neutronen, das entspricht dem Atomkern von Helium. Sie sind schwach und können schon von einem Blatt Papier aufgehalten werden. Beta- Strahlen sind Elektronen, die sich schnell bewegen und die Haut durchdringen können. Gamma- Strahlen sind, wie Licht, elektromagnetische Strahlen und können nur durch eine Bleischicht gestoppt werden. Die Auswirkungen von Gamma- Strahlen sind sehr schädlich. Gamma-Strahlen mit hoher Energie werden bei der Strahlentherapie eingesetzt, um Tumore zu zerstören.
Chemie. Hayley Birch. schlüssel ideen
 Chemie Hayley Birch schlüssel ideen Hayley Birch 50 Schlüsselideen Chemie Aus dem Englischen übersetzt von Angela Simeon Inhalt Einleitung 3 01 Atome 4 02 Elemente 8 03 Isotope 12 04 Verbindungen 16 05
Chemie Hayley Birch schlüssel ideen Hayley Birch 50 Schlüsselideen Chemie Aus dem Englischen übersetzt von Angela Simeon Inhalt Einleitung 3 01 Atome 4 02 Elemente 8 03 Isotope 12 04 Verbindungen 16 05
Atomphysik NWA Klasse 9
 Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
Atomphysik NWA Klasse 9 Atome wurden lange Zeit als die kleinsten Teilchen angesehen, aus denen die Körper bestehen. Sie geben den Körpern ihre chemischen und physikalischen Eigenschaften. Heute wissen
Atomphysik Klasse 9. Aufgabe: Fülle die freien Felder aus!
 1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1. Was gibt die Massenzahl A eines Atoms an? Die Zahl der Neutronen im Kern. Die Zahl der Protonen im Kern. Die Summe aus Kernneutronen und Kernprotonen. Die Zahl der Elektronen. Die Summe von Elektronen
1 Aufbau der Materie. 1.1 Anfänge und Kernhüllenmodell. Bauchemie / Bauphysik II Modul M-T 6
 1 Aufbau der Materie 1.1 Anfänge und Kernhüllenmodell 400 J. v. Chr. suchte Demokrit als erster die kleinsten Teile der Materie. Und weil auch er diese damals nicht sehen konnte, entwickelte er eine Modellvorstellung
1 Aufbau der Materie 1.1 Anfänge und Kernhüllenmodell 400 J. v. Chr. suchte Demokrit als erster die kleinsten Teile der Materie. Und weil auch er diese damals nicht sehen konnte, entwickelte er eine Modellvorstellung
FOS: Radioaktivität und Strahlenschutz. Chemische Elemente und ihre kleinsten Teilchen
 R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
R. Brinkmann http://brinkmann-du.de Seite 5..03 Chemische Elemente FOS: Radioaktivität und Strahlenschutz Chemische Elemente und ihre kleinsten Teilchen Der Planet Erde besteht aus 9 natürlich vorkommenden
Arbeitsfragen zur Vorbereitung auf den Quali
 Arbeitsfragen zur Vorbereitung auf den Quali Atombau 1 Was bedeutet das Wort Atom? 2 Welche Aussage mache Dalton über die Atome? 3 Was ist der größte Teil eines Atoms? 4 Was sind Moleküle? 5 Durch welchen
Arbeitsfragen zur Vorbereitung auf den Quali Atombau 1 Was bedeutet das Wort Atom? 2 Welche Aussage mache Dalton über die Atome? 3 Was ist der größte Teil eines Atoms? 4 Was sind Moleküle? 5 Durch welchen
Das Periodensystem der Elemente Spektakuläres ABC der Chemie
 Das Periodensystem der Elemente Spektakuläres ABC der Chemie Prof. Dr. Roger Alberto, Dr. René Oetterli, Phil Frei email: ariel@chem.uzh.ch 27. März 2019 Zum UNESCO Jahr des 150. Geburtstages des Periodensystems
Das Periodensystem der Elemente Spektakuläres ABC der Chemie Prof. Dr. Roger Alberto, Dr. René Oetterli, Phil Frei email: ariel@chem.uzh.ch 27. März 2019 Zum UNESCO Jahr des 150. Geburtstages des Periodensystems
Radioaktivität, Kernspaltung. medizinische, friedliche und kriegerische Nutzungen der Radioaktivität
 Radioaktivität, Kernspaltung. medizinische, friedliche und kriegerische Nutzungen der Radioaktivität LaCh Seite 1 von 7 1. Grundlagen der Atomtheorie... 3 Aufbau eines Atoms... 3 2. Eigenschaften der radioaktiven
Radioaktivität, Kernspaltung. medizinische, friedliche und kriegerische Nutzungen der Radioaktivität LaCh Seite 1 von 7 1. Grundlagen der Atomtheorie... 3 Aufbau eines Atoms... 3 2. Eigenschaften der radioaktiven
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Strahlung
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Strahlung Das komplette Material finden Sie hier: Download bei School-Scout.de SCHOOL-SCOUT
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 7 bis 9: Strahlung Das komplette Material finden Sie hier: Download bei School-Scout.de SCHOOL-SCOUT
Vorlesung Allgemeine Chemie (CH01)
 Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Vorlesung Allgemeine Chemie (CH01) Für Studierende im B.Sc.-Studiengang Chemie Prof. Dr. Martin Köckerling Arbeitsgruppe Anorganische Festkörperchemie Mathematisch-Naturwissenschaftliche Fakultät, Institut
Thema heute: Aufbau der Materie: Atommodelle 1
 Wiederholung der letzten Vorlesungsstunde: Naturwissenschaften, Unterteilung der Naturwissenschaften in einzelne Wissensgebiete, Modellvorstellungen, der "reine Stoff", thermische Eigenschaften, Siedepunkt,
Wiederholung der letzten Vorlesungsstunde: Naturwissenschaften, Unterteilung der Naturwissenschaften in einzelne Wissensgebiete, Modellvorstellungen, der "reine Stoff", thermische Eigenschaften, Siedepunkt,
Nawi 2AHMI Atommodelle I Glavas, Jakovljevic, Josipovic
 e -1. Teil Das Wort Atom kommt aus dem Griechischen atomos und bedeutet unteilbar ; unteilbarer Urstoff. Ein Atom ist der kleinste Baustein eines chemischen Grundstoffes oder Elements, der ohne Verlust
e -1. Teil Das Wort Atom kommt aus dem Griechischen atomos und bedeutet unteilbar ; unteilbarer Urstoff. Ein Atom ist der kleinste Baustein eines chemischen Grundstoffes oder Elements, der ohne Verlust
1 Einführung in den Strahlenschutz der Feuerwehr
 1 Einführung in den Strahlenschutz der Feuerwehr Als das erste Rote Heft»Strahlenschutz«im Jahr 1960 erschien, war das Thema radioaktive Stoffe Neuland für die Feuerwehren. Heute finden die Feuerwehren
1 Einführung in den Strahlenschutz der Feuerwehr Als das erste Rote Heft»Strahlenschutz«im Jahr 1960 erschien, war das Thema radioaktive Stoffe Neuland für die Feuerwehren. Heute finden die Feuerwehren
DIE SACHE MIT DEN KERNBAUSTEINEN
 Und nun sind wir unterwegs unterwegs mit flotten Gesellen! Jetzt wollen wir uns mit einem Stoff beschäftigen, der sogar in zwei Formen auftritt. Es ist der Kohlenstoff. Um diese Sache zu verstehen musst
Und nun sind wir unterwegs unterwegs mit flotten Gesellen! Jetzt wollen wir uns mit einem Stoff beschäftigen, der sogar in zwei Formen auftritt. Es ist der Kohlenstoff. Um diese Sache zu verstehen musst
Wie sind Atome aufgebaut Welche Informationen enthält das Periodensystem?
 2. DIE KLEINSTEN TEILCHEN ARBEITSBLATT 2.1 DER ATOMAUFBAU FRAGE Wie sind Atome aufgebaut Welche Informationen enthält das Periodensystem? Bausteine der Atome Ladung (+, -, 0) Masse (hoch, sehr gering)
2. DIE KLEINSTEN TEILCHEN ARBEITSBLATT 2.1 DER ATOMAUFBAU FRAGE Wie sind Atome aufgebaut Welche Informationen enthält das Periodensystem? Bausteine der Atome Ladung (+, -, 0) Masse (hoch, sehr gering)
11. Kernphysik. [55] Ianus Münze
![11. Kernphysik. [55] Ianus Münze 11. Kernphysik. [55] Ianus Münze](/thumbs/52/29657300.jpg) 11. Kernphysik Der griechische Gott Ianus ist einer der ältesten römischen Gottheiten. Er gehört zur rein römischen Mythologie, das heißt es gibt in der griechischen Götterwelt keine vergleichbare Gestalt.
11. Kernphysik Der griechische Gott Ianus ist einer der ältesten römischen Gottheiten. Er gehört zur rein römischen Mythologie, das heißt es gibt in der griechischen Götterwelt keine vergleichbare Gestalt.
Radioaktivität. Bildungsstandards Physik - Radioaktivität 1 LEHRPLANZITAT. Das radioaktive Verhalten der Materie:
 Bildungsstandards Physik - Radioaktivität 1 Radioaktivität LEHRPLANZITAT Das radioaktive Verhalten der Materie: Ausgehend von Alltagsvorstellungen der Schülerinnen und Schüler soll ein grundlegendes Verständnis
Bildungsstandards Physik - Radioaktivität 1 Radioaktivität LEHRPLANZITAT Das radioaktive Verhalten der Materie: Ausgehend von Alltagsvorstellungen der Schülerinnen und Schüler soll ein grundlegendes Verständnis
1 Chemische Elemente und chemische Grundgesetze
 1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
1 Chemische Elemente und chemische Grundgesetze Die Chemie ist eine naturwissenschaftliche Disziplin. Sie befasst sich mit der Zusammensetzung, Charakterisierung und Umwandlung von Materie. Unter Materie
Die Anzahl der Protonen und Neutronen entspricht der Atommassenzahl.
 Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Atom Der Begriff Atom leitet sich von atomos her, was unteilbar heisst. Diese Definition ist alt, da man heutzutage fähig ist, Atome zu teilen. Atommassenzahl Die Anzahl der Protonen und Neutronen entspricht
Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten.
![Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten. Hewlett-Packard Company. [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten.](/thumbs/95/126174167.jpg) Hewlett-Packard Company [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten Johanika [Datum] Walter Whites Chemie Quiz Fragen 1. Aus wie vielen Atomen besteht
Hewlett-Packard Company [Dokumenttitel] [Untertitel des Dokuments] Walter Whites explosives Chemie Quiz Fragen & Antworten Johanika [Datum] Walter Whites Chemie Quiz Fragen 1. Aus wie vielen Atomen besteht
Vorstellungen über den Bau der Materie
 Atombau Die Welt des ganz Kleinen Vorstellungen über den Bau der Materie Demokrit denkt sich das Unteilbare, das Atom Dalton entwirft ein Atommodell Rutherford formuliert das Kern-Hüllenmodell Bohr spricht
Atombau Die Welt des ganz Kleinen Vorstellungen über den Bau der Materie Demokrit denkt sich das Unteilbare, das Atom Dalton entwirft ein Atommodell Rutherford formuliert das Kern-Hüllenmodell Bohr spricht
Radioaktivität. den 7 Oktober Dr. Emőke Bódis
 Radioaktivität den 7 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Eigenschaften und Entstehung der radioaktiver Strahlungen: Alpha- Beta- und Gamma- Strahlungen. Aktivität. Zerfallgesetz. Halbwertzeit.
Radioaktivität den 7 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Eigenschaften und Entstehung der radioaktiver Strahlungen: Alpha- Beta- und Gamma- Strahlungen. Aktivität. Zerfallgesetz. Halbwertzeit.
Lernziele zu Radioaktivität 1. Radioaktive Strahlung. Entdeckung der Radioaktivität. Entdeckung der Radioaktivität
 Radioaktive Strahlung Entstehung Nutzen Gefahren du weisst, Lernziele zu Radioaktivität 1 dass Elementarteilchen nur bedingt «elementar» sind. welche unterschiedlichen Arten von radioaktiven Strahlungen
Radioaktive Strahlung Entstehung Nutzen Gefahren du weisst, Lernziele zu Radioaktivität 1 dass Elementarteilchen nur bedingt «elementar» sind. welche unterschiedlichen Arten von radioaktiven Strahlungen
Kernphysik. Physik Klasse 9. Quelle: AkadOR W. Wagner, Didaktik der Chemie, Universität Bayreuth (verändert für Kl.9/Sachsen
 Kernphysik Physik Klasse 9 Quelle: AkadOR W. Wagner, Didaktik der Chemie, Universität Bayreuth (verändert für Kl.9/Sachsen Lehrplan Atomodelle Niels Bohr Rutherford Begriff: Modell Ein Modell zeichnet
Kernphysik Physik Klasse 9 Quelle: AkadOR W. Wagner, Didaktik der Chemie, Universität Bayreuth (verändert für Kl.9/Sachsen Lehrplan Atomodelle Niels Bohr Rutherford Begriff: Modell Ein Modell zeichnet
Die Idee des Atoms geht auf Demokrit von Abdera und Leukipp von Milet zurück. (5. Jhdt. v. Chr.) atomos (griech.) = unteilbar
 2Aufbau der Materie Hofer 1 2 Aufbau der Materie 2.1 Die Bestandteile der Materie Chemische Versuche und hoch auflösende Spezialmikroskope zeigen, dass alle Stoffe aus den chemischen Grundstoffen oder
2Aufbau der Materie Hofer 1 2 Aufbau der Materie 2.1 Die Bestandteile der Materie Chemische Versuche und hoch auflösende Spezialmikroskope zeigen, dass alle Stoffe aus den chemischen Grundstoffen oder
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Ordnung in der Vielfalt - das verstehen und lesen lernen Das komplette aterial finden Sie hier: School-Scout.de 1 von 10 Ordnung in
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Ordnung in der Vielfalt - das verstehen und lesen lernen Das komplette aterial finden Sie hier: School-Scout.de 1 von 10 Ordnung in
10TG. Training II2. 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene.
 Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Training II2 1. Schreibe die Reaktionsgleichungen folgender Reaktionen. Benenne die Produkte. Erkläre die Teilchenebene. (4X4=1 X4=16P) a. Verbrennung von Kohlenstoff C + O2 CO2 Kohlenstoffdioxid b. Thermolyse
Aufbau des Atomkerns a) Gib an, aus wie vielen Protonen und Neutronen die
 Aufbau des Atomkerns a) Gib an, aus wie vielen Protonen und Neutronen die Atomkerne von Cl bestehen. b) Erkläre, was man unter Isotopen versteht. Gib ein Beispiel an. 3, Cl c) Im Periodensystem wird die
Aufbau des Atomkerns a) Gib an, aus wie vielen Protonen und Neutronen die Atomkerne von Cl bestehen. b) Erkläre, was man unter Isotopen versteht. Gib ein Beispiel an. 3, Cl c) Im Periodensystem wird die
5. Die Physik der Atomhülle
 Protokoll vom 03.11.003 Lukas Heberger 5. Die Physik der Atomhülle 5.1 Die frühen Atommodelle 5.1.1. Von Demokrit bis Dalton a) Demokrit (um 460-371 v.chr.) - Es gibt unveränderliche kleinste Teilchen
Protokoll vom 03.11.003 Lukas Heberger 5. Die Physik der Atomhülle 5.1 Die frühen Atommodelle 5.1.1. Von Demokrit bis Dalton a) Demokrit (um 460-371 v.chr.) - Es gibt unveränderliche kleinste Teilchen
Radioaktivität Haller/ Hannover-Kolleg 1
 Radioaktivität 17.09.2007 Haller/ Hannover-Kolleg 1 Radioaktivität 17.09.2007 Haller/ Hannover-Kolleg 2 Radioaktivität 1. Was verstehe ich darunter? 2. Welche Wirkungen hat die Radioaktivität? 3. Muss
Radioaktivität 17.09.2007 Haller/ Hannover-Kolleg 1 Radioaktivität 17.09.2007 Haller/ Hannover-Kolleg 2 Radioaktivität 1. Was verstehe ich darunter? 2. Welche Wirkungen hat die Radioaktivität? 3. Muss
Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem mit Lösungen Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu?
Chemie Zusammenfassung III
 Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Chemie Zusammenfassung III Inhaltsverzeichnis Atombau & Kernphysik... 2 Aufbau der Atome... 2 Atomkern... 2 Atomhülle... 2 Atomgrösse und Kernladung... 3 Reaktivität und Gruppen des Periodensystems...
Bestandteile des Atoms Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Sozialform Die SuS lesen die Informationstexte. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. Anschliessend zeichnen
Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Sozialform Die SuS lesen die Informationstexte. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. Anschliessend zeichnen
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Grundwissen Atome und radioaktiver Zerfall
 Atome, Radioaktivität und radioaktive Abfälle Arbeitsblatt 6 1 Grundwissen Atome und radioaktiver Zerfall Repetition zum Atombau Die Anzahl der... geladenen Protonen bestimmt die chemischen Eigenschaften
Atome, Radioaktivität und radioaktive Abfälle Arbeitsblatt 6 1 Grundwissen Atome und radioaktiver Zerfall Repetition zum Atombau Die Anzahl der... geladenen Protonen bestimmt die chemischen Eigenschaften
Kapitel 03. Aufbau der Materie (Buch ab Seite 17)
 Kapitel 03 Aufbau der Materie (Buch ab Seite 17) ATOME SIND DIE BAUSTEINE DER CHEMIE Film1 Geschichtliches Kern-Hülle-Modell 8min ATOME SIND DIE BAUSTEINE DER CHEMIE Alle Stoffe im Universum (Sonne, Mond,
Kapitel 03 Aufbau der Materie (Buch ab Seite 17) ATOME SIND DIE BAUSTEINE DER CHEMIE Film1 Geschichtliches Kern-Hülle-Modell 8min ATOME SIND DIE BAUSTEINE DER CHEMIE Alle Stoffe im Universum (Sonne, Mond,
Das Periodensystem der Elemente Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Die SuS lesen den Informationstext. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. Die SuS verstehen, dass sich
Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Die SuS lesen den Informationstext. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. Die SuS verstehen, dass sich
2. Verhalten der Elemente bei einer Reaktion: Warum funkt s bei unterschiedlichen
 1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
1. Atombau und Periodensystem 1a) Nach welchem Gesichtspunkt sind die Elemente im Periodensystem von 1- ca. 103 angeordnet? 1b) Nach welchem Gesichtspunkt ist ein Element einer PERIODE zugeordnet? 1c)
Themenheft. Chemie. chemische Gesetze, Atombau und Formeln. Arbeitsblätter für den deutschsprachigen Fachunterricht an Auslandsschulen
 Themenheft Chemie chemische Gesetze, Atombau und Formeln Arbeitsblätter für den deutschsprachigen Fachunterricht an Auslandsschulen Inhaltsverzeichnis: Blatt 1: Die Masse bei chemischen Reaktionen Blatt
Themenheft Chemie chemische Gesetze, Atombau und Formeln Arbeitsblätter für den deutschsprachigen Fachunterricht an Auslandsschulen Inhaltsverzeichnis: Blatt 1: Die Masse bei chemischen Reaktionen Blatt
Atombau. Chemie. Zusammenfassungen. Prüfung Mittwoch, 14. Dezember Elektrische Ladung. Elementarteilchen. Kern und Hülle
 Chemie Atombau Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Elektrische Ladung Elementarteilchen Kern und Hülle Atomsorten, Nuklide, Isotope Energieniveaus und Schalenmodell Steffi Alle saliorel
Chemie Atombau Zusammenfassungen Prüfung Mittwoch, 14. Dezember 2016 Elektrische Ladung Elementarteilchen Kern und Hülle Atomsorten, Nuklide, Isotope Energieniveaus und Schalenmodell Steffi Alle saliorel
3. Übung Allgemeine Chemie AC01
 Allgemeine und Anorganische Chemie Aufgabe 1: 3. Übung Allgemeine Chemie AC01 Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten im Kern immer die
Allgemeine und Anorganische Chemie Aufgabe 1: 3. Übung Allgemeine Chemie AC01 Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten im Kern immer die
Lösungen der Kontrollaufgaben
 Lösungen der Kontrollaufgaben Lösungen zu den Kontrollaufgaben 1.1 1.) 1000 2.) Glas und PVC ziehen einander an. - Begründung: Da offenbar Hartgummi und PVC gleichartig geladen sind (Abstossung), Glas
Lösungen der Kontrollaufgaben Lösungen zu den Kontrollaufgaben 1.1 1.) 1000 2.) Glas und PVC ziehen einander an. - Begründung: Da offenbar Hartgummi und PVC gleichartig geladen sind (Abstossung), Glas
Big Bang zweiter Akt
 Harald Lesch / Jörn Müller Big Bang zweiter Akt Auf den Spuren des Lebens im All C. Bertelsmann Inhalt Einleitung 11 1. Das Handwerkszeug 17 Bei der Beschäftigung mit dem Universum stößt man allenthalben
Harald Lesch / Jörn Müller Big Bang zweiter Akt Auf den Spuren des Lebens im All C. Bertelsmann Inhalt Einleitung 11 1. Das Handwerkszeug 17 Bei der Beschäftigung mit dem Universum stößt man allenthalben
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Gruppe 1. Lies den folgenden Text aus einem Biologiebuch.
 Gruppe Lies den folgenden Text aus einem Biologiebuch.. Notiere das Wachstum der Salmonellen übersichtlich in einer Tabelle. Am Anfang soll eine Salmonelle vorhanden sein. Verwende dabei auch Potenzen..
Gruppe Lies den folgenden Text aus einem Biologiebuch.. Notiere das Wachstum der Salmonellen übersichtlich in einer Tabelle. Am Anfang soll eine Salmonelle vorhanden sein. Verwende dabei auch Potenzen..
Radioaktivität und Strahlenschutz. FOS: Kernumwandlungen und Radioaktivität
 R. Brinkmann http://brinkmann-du.de Seite 25..23 -, Beta- und Gammastrahlen Radioaktivität und Strahlenschutz FOS: Kernumwandlungen und Radioaktivität Bestimmte Nuklide haben die Eigenschaft, sich von
R. Brinkmann http://brinkmann-du.de Seite 25..23 -, Beta- und Gammastrahlen Radioaktivität und Strahlenschutz FOS: Kernumwandlungen und Radioaktivität Bestimmte Nuklide haben die Eigenschaft, sich von
Atombau und Periodensystem
 Atombau und Periodensystem Patrick Bucher 15. August 2011 Inhaltsverzeichnis 1 Die chemischen Grundlagen und Daltons Atomhypothese 1 2 Modelle zum Atombau 2 2.1 Die elektrische Ladung..............................
Atombau und Periodensystem Patrick Bucher 15. August 2011 Inhaltsverzeichnis 1 Die chemischen Grundlagen und Daltons Atomhypothese 1 2 Modelle zum Atombau 2 2.1 Die elektrische Ladung..............................
Natürliche Radioaktivität Lehrerinformation
 Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Sozialform Die SuS lesen den Informationstext. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. In Partnerarbeit
Lehrerinformation 1/7 Arbeitsauftrag Ziel Material Sozialform Die SuS lesen den Informationstext. Als Verständnishilfe verwenden sie gleichzeitig das Arbeitsblatt Leitfragen zum Text. In Partnerarbeit
durch Teilungsversuche durch Spektraluntersuchungen Jedes Atom besitzt einen Atomkern, in dem fast die gesamte Masse vereinigt ist.
 1. Kreuze die richtige Aussage über Atome an: Sie sind sehr kleine, unteilbare Körper aus einem einheitlichen (homogenen) Stoff. Sie sind so klein, dass man ihren Aufbau nicht erforschen kann. Sie sind
1. Kreuze die richtige Aussage über Atome an: Sie sind sehr kleine, unteilbare Körper aus einem einheitlichen (homogenen) Stoff. Sie sind so klein, dass man ihren Aufbau nicht erforschen kann. Sie sind
Messung radioaktiver Strahlung
 α β γ Messung radioaktiver Strahlung Radioaktive Strahlung misst man mit dem Geiger-Müller- Zählrohr, kurz: Geigerzähler. Nulleffekt: Schwache radioaktive Strahlung, der wir ständig ausgesetzt sind. Nulleffekt
α β γ Messung radioaktiver Strahlung Radioaktive Strahlung misst man mit dem Geiger-Müller- Zählrohr, kurz: Geigerzähler. Nulleffekt: Schwache radioaktive Strahlung, der wir ständig ausgesetzt sind. Nulleffekt
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
Der Teilchenzoo wächst Intermezzo Kosmische Strahlung
 Der Teilchenzoo wächst Intermezzo Kosmische Strahlung Entdeckung neuer Teilchen die niemand brauchte... Elementarteilchen (von lat. elementum Grundstoff ) sind die Bausteine der Materie. So besteht die
Der Teilchenzoo wächst Intermezzo Kosmische Strahlung Entdeckung neuer Teilchen die niemand brauchte... Elementarteilchen (von lat. elementum Grundstoff ) sind die Bausteine der Materie. So besteht die
Übungsaufgaben zum Atomaufbau und Periodensystem
 Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten
Allgemeine und Anorganische Chemie Übungsaufgaben zum Atomaufbau und Periodensystem Aufgabe 1: Welche der folgenden Aussagen trifft für alle Atome, einschließlich des Wasserstoffatoms, zu? Sie enthalten
3) Natürliche und künstliche Radioaktivität (1)
 3) Natürliche und künstliche Radioaktivität (1) Kosmische Strahlung - Protonen (93 %) - Alpha-Teilchen (6.3 %) - schwerere Kerne (0. %) - Ohne Zerfallsreihen - 0 radioaktive Nuklide, die primordial auf
3) Natürliche und künstliche Radioaktivität (1) Kosmische Strahlung - Protonen (93 %) - Alpha-Teilchen (6.3 %) - schwerere Kerne (0. %) - Ohne Zerfallsreihen - 0 radioaktive Nuklide, die primordial auf
Atombau. Die Welt des ganz Kleinen
 Atombau Die Welt des ganz Kleinen Modellvorstellungen als Verständnishilfen Stoffebene Teilchenebene Elemente sind Grundstoffe Stoffe können elektrisch geladen sein Elemente reagieren zu Verbindungen in
Atombau Die Welt des ganz Kleinen Modellvorstellungen als Verständnishilfen Stoffebene Teilchenebene Elemente sind Grundstoffe Stoffe können elektrisch geladen sein Elemente reagieren zu Verbindungen in
Wasser à. Nachweis: Wasser ist
 Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Arbeitsblatt zu Kap. 5. Atome Bausteine der Stoffe 5.1 Elemente und Verbindungen Elektrolyse des Reinstoffes Wasser Wasser à Nachweis: Wasser ist Stoffeinteilung 5.2 Von den Elementen zu den Atomen Synthese
Uran. Uran ist ein silberglänzendes, weiches, radioaktives Metall. Es bildet eine Vielzahl verschiedener Legierungen.
 Uran Uran ist ein silberglänzendes, weiches, radioaktives Metall. Es bildet eine Vielzahl verschiedener Legierungen. Bei Raumtemperatur läuft auch massives Uranmetall an der Luft an. Dabei bilden sich
Uran Uran ist ein silberglänzendes, weiches, radioaktives Metall. Es bildet eine Vielzahl verschiedener Legierungen. Bei Raumtemperatur läuft auch massives Uranmetall an der Luft an. Dabei bilden sich
Dieter Suter Physik B3
 Dieter Suter - 421 - Physik B3 9.2 Radioaktivität 9.2.1 Historisches, Grundlagen Die Radioaktivität wurde im Jahre 1896 entdeckt, als Becquerel feststellte, dass Uransalze Strahlen aussenden, welche den
Dieter Suter - 421 - Physik B3 9.2 Radioaktivität 9.2.1 Historisches, Grundlagen Die Radioaktivität wurde im Jahre 1896 entdeckt, als Becquerel feststellte, dass Uransalze Strahlen aussenden, welche den
Widerlegung des Modells von Thomson durch Rutherford
 Atomkerne Eine wichtige Frage stellt sich nach dem Aufbau eines Atoms aus diesen subatomaren Bausteinen. Gibt es eine Systematik des Aufbaus der Atome der verschiedenen chemischen Element im Hinblick auf
Atomkerne Eine wichtige Frage stellt sich nach dem Aufbau eines Atoms aus diesen subatomaren Bausteinen. Gibt es eine Systematik des Aufbaus der Atome der verschiedenen chemischen Element im Hinblick auf
Die Stoffteilchen (II): Ionengruppen und ihre Ionen
 Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Die Stoffteilchen (II): Ionengruppen und ihre Ionen Ionen sind die Bausteine der Ionengruppen, den gedachten Stoffteilchen der Salze. Was haben Ionengruppen mit der Formel von Salzen zu tun? DARUM GEHT
Welcher Wissenschaftler sagte, dass sich die Materie aus unteilbaren Teilchen ("atomos") zusammensetzen würde?
 Posten 1a Welcher Wissenschaftler sagte, dass sich die Materie aus unteilbaren Teilchen ("atomos") zusammensetzen würde? a) Leukipp von Milet (=> Posten 2a) b) Demokrit (=> Posten 3d) c) Rutherford (=>
Posten 1a Welcher Wissenschaftler sagte, dass sich die Materie aus unteilbaren Teilchen ("atomos") zusammensetzen würde? a) Leukipp von Milet (=> Posten 2a) b) Demokrit (=> Posten 3d) c) Rutherford (=>
Radioaktivität und seine Strahlung
 Radioaktivität und seine Strahlung Radioaktivität (radioactivité wurde 1898 von Marie Curie eingeführt) ist ein Phänomen der Kerne von tomen. Darum ist die Radioaktivität heute in die Kernphysik eingeordnet.
Radioaktivität und seine Strahlung Radioaktivität (radioactivité wurde 1898 von Marie Curie eingeführt) ist ein Phänomen der Kerne von tomen. Darum ist die Radioaktivität heute in die Kernphysik eingeordnet.
hält uns auf der Erde.
 Weltbild des Thales von Milet Kreisel-Drehmomente ermöglichen stabiles Fahren auf nur zwei Rädern. Die Gravitationskraft hält uns auf der Erde. Im Universum gibt es Milliarden Galaxien. Optimaler Einsatz
Weltbild des Thales von Milet Kreisel-Drehmomente ermöglichen stabiles Fahren auf nur zwei Rädern. Die Gravitationskraft hält uns auf der Erde. Im Universum gibt es Milliarden Galaxien. Optimaler Einsatz
d 10 m Cusanus-Gymnasium Wittlich Das Bohrsche Atomodell Nils Bohr Atomdurchmesser 10 Kerndurchmesser 14 d 10 m Atom
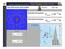 Das Bohrsche Atomodell Nils Bohr 1885-1962 Atomdurchmesser 10 d 10 m Atom Kerndurchmesser 14 http://www.matrixquantenenergie.de d 10 m Kern 14 dkern 10 m 10 datom 10 m Masse und Ladung der Elementarteilchen
Das Bohrsche Atomodell Nils Bohr 1885-1962 Atomdurchmesser 10 d 10 m Atom Kerndurchmesser 14 http://www.matrixquantenenergie.de d 10 m Kern 14 dkern 10 m 10 datom 10 m Masse und Ladung der Elementarteilchen
Natürliche Radioaktivität
 Natürliche Radioaktivität Definition Natürliche Radioaktivität Die Eigenschaft von Atomkernen sich spontan in andere umzuwandeln, wobei Energie in Form von Teilchen oder Strahlung frei wird, nennt man
Natürliche Radioaktivität Definition Natürliche Radioaktivität Die Eigenschaft von Atomkernen sich spontan in andere umzuwandeln, wobei Energie in Form von Teilchen oder Strahlung frei wird, nennt man
Struktur des Atomkerns
 Struktur des Atomkerns den 6 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Struktur des Atomkerns. Die Eigenschaften des Kernkraftes. Bindungsenergie. Massendefekt. Tröpfchenmodell und Schallmodell. Magische
Struktur des Atomkerns den 6 Oktober 2016 Dr. Emőke Bódis Prüfungsfrage Die Struktur des Atomkerns. Die Eigenschaften des Kernkraftes. Bindungsenergie. Massendefekt. Tröpfchenmodell und Schallmodell. Magische
Thema heute: Aufbau der Materie, Atommodelle Teil 2
 Wiederholung der letzten Vorlesungsstunde: Atomistischer Aufbau der Materie, historische Entwicklung des Atombegriffes Atome Thema heute: Aufbau der Materie, Atommodelle Teil 2 Vorlesung Allgemeine Chemie,
Wiederholung der letzten Vorlesungsstunde: Atomistischer Aufbau der Materie, historische Entwicklung des Atombegriffes Atome Thema heute: Aufbau der Materie, Atommodelle Teil 2 Vorlesung Allgemeine Chemie,
Kernreaktionen chemisch beschrieben
 Physics Meets Chemistry Kernreaktionen chemisch beschrieben 1 Kernreaktionen chemisch beschrieben 1. Ausgangslage 2. Ziele 3. Unterrichtsvorschlag mit Übungen Physics Meets Chemistry Kernreaktionen chemisch
Physics Meets Chemistry Kernreaktionen chemisch beschrieben 1 Kernreaktionen chemisch beschrieben 1. Ausgangslage 2. Ziele 3. Unterrichtsvorschlag mit Übungen Physics Meets Chemistry Kernreaktionen chemisch
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Physikalische. Grundlagen. L. Kölling, Fw Minden
 Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
Physikalische Grundlagen L. Kölling, Fw Minden Radioaktivität kann man weder sehen, hören, fühlen, riechen oder schmecken. Daher muss sie der FA (SB) zumindest verstehen, um im Einsatzfall die erforderlichen
2. Der Aufbau der Atome wird mit dem Rutherford schen und dem Bohr schen Atommodellen beschrieben. Ordne die Aussagen zu und verbinde.
 Atommodelle 1. Vervollständige den Lückentext. Atome bestehen aus einer mit negativ geladenen und einem mit positiv geladenen und elektrisch neutralen. Die Masse des Atoms ist im konzentriert. Die Massenzahl
Atommodelle 1. Vervollständige den Lückentext. Atome bestehen aus einer mit negativ geladenen und einem mit positiv geladenen und elektrisch neutralen. Die Masse des Atoms ist im konzentriert. Die Massenzahl
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
1.4. Aufgaben zum Atombau
 1.4. Aufgaben zum Atombau Aufgabe 1: Elementarteilchen a) Nenne die drei klassischen Elementarteilchen und vergleiche ihre Massen und Ladungen. b) Wie kann man Elektronen nachweisen? c) Welche Rolle spielen
1.4. Aufgaben zum Atombau Aufgabe 1: Elementarteilchen a) Nenne die drei klassischen Elementarteilchen und vergleiche ihre Massen und Ladungen. b) Wie kann man Elektronen nachweisen? c) Welche Rolle spielen
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Die Bausteine der Natur
 Die Bausteine der Natur Teilchenwelt - Masterclass 2011 Matthias Schröder, Jan Thomsen Fragen der Teilchenphysik Woraus bestehen wir und unsere Welt? Was sind die fundamentalen Kräfte in unserem Universum?
Die Bausteine der Natur Teilchenwelt - Masterclass 2011 Matthias Schröder, Jan Thomsen Fragen der Teilchenphysik Woraus bestehen wir und unsere Welt? Was sind die fundamentalen Kräfte in unserem Universum?
Anorganische Chemie! der unbelebten Natur keine Kohlenstoffverbindung (Kohlenstoffatome C) Metall Nichtmetallverbindungen Ionenbindung
 3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
3 Chemie / Physik 3.1 Eigenheiten der Chemie und Physik Chemie ist die Lehre von den Stoffen, ihrer Zusammensetzung, dem Aufbau, der Struktur und ihrer Umwandlung Die Chemie untersucht und beschreibt die
Was ist radioaktive Strahlung?
 Was ist radioaktive Strahlung? Wir haben ja gelernt, dass das Licht zu den Radiowellen gehört. Wir haben mit unserem Kurzwellenradio die Radiowellen eingefangen und ihre Modulation in Schallwellen umgewandelt,
Was ist radioaktive Strahlung? Wir haben ja gelernt, dass das Licht zu den Radiowellen gehört. Wir haben mit unserem Kurzwellenradio die Radiowellen eingefangen und ihre Modulation in Schallwellen umgewandelt,
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Technologie/Informatik Kernaufbau und Kernzerfälle. Dipl.-Phys. Michael Conzelmann, StR Staatliche FOS und BOS Bad Neustadt a. d.
 Technologie/Informatik Kernaufbau und Kernzerfälle Dipl.-Phys. Michael Conzelmann, StR Staatliche FOS und BOS Bad Neustadt a. d. Saale Übersicht Kernaufbau Rutherford-Experiment, Nukleonen Schreibweise,
Technologie/Informatik Kernaufbau und Kernzerfälle Dipl.-Phys. Michael Conzelmann, StR Staatliche FOS und BOS Bad Neustadt a. d. Saale Übersicht Kernaufbau Rutherford-Experiment, Nukleonen Schreibweise,
Was wussten die Menschen vor über 230 Jahren vom Weltraum?
 Was wussten die Menschen vor über 230 Jahren vom Weltraum? Die Milchstraße war der ganze Weltraum Den Urknall hat s noch nicht gegeben Olbers und der dunkle Himmel Das Sonnensystem reichte bis zum Uranus
Was wussten die Menschen vor über 230 Jahren vom Weltraum? Die Milchstraße war der ganze Weltraum Den Urknall hat s noch nicht gegeben Olbers und der dunkle Himmel Das Sonnensystem reichte bis zum Uranus
Allgemeine Chemie 1. Skript Allgemeine und Anorganische Chemie
 Allgemeine Chemie 1 Skript Allgemeine und Anorganische Chemie Inhaltsverzeichnis: 1. Atome...3 A Elektronen...3 B Protonen...4 C Neutronen...5 D Aufbau von Atomen...5 E Isotope...6 F Radioaktivität...6
Allgemeine Chemie 1 Skript Allgemeine und Anorganische Chemie Inhaltsverzeichnis: 1. Atome...3 A Elektronen...3 B Protonen...4 C Neutronen...5 D Aufbau von Atomen...5 E Isotope...6 F Radioaktivität...6
Selbstorganisation: Konstruktion der Zukunft? Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Eine Kernüberlegung der Nanotechnologien besteht darin, dass sich die Moleküle in den unterschiedlichen Formen und Strukturen selbst organisieren. Dies
Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Eine Kernüberlegung der Nanotechnologien besteht darin, dass sich die Moleküle in den unterschiedlichen Formen und Strukturen selbst organisieren. Dies
Grundlagen. Maximilian Ernestus Waldorfschule Saarbrücken
 Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
Grundlagen Maximilian Ernestus Waldorfschule Saarbrücken 2008/2009 Inhaltsverzeichnis 1 Chemische Elemente 2 2 Das Teilchenmodell 3 3 Mischungen und Trennverfahren 4 4 Grundgesetze chemischer Reaktionen
41. Kerne. 34. Lektion. Kernzerfälle
 41. Kerne 34. Lektion Kernzerfälle Lernziel: Stabilität von Kernen ist an das Verhältnis von Protonen zu Neutronen geknüpft. Zu viele oder zu wenige Neutronen führen zum spontanen Zerfall. Begriffe Stabilität
41. Kerne 34. Lektion Kernzerfälle Lernziel: Stabilität von Kernen ist an das Verhältnis von Protonen zu Neutronen geknüpft. Zu viele oder zu wenige Neutronen führen zum spontanen Zerfall. Begriffe Stabilität
umwandlungen Atommodelle, Rutherford-Experiment, Atomaufbau, Elektronen, Protonen,
 Wiederholung der letzten Vorlesungsstunde: Atommodelle, Rutherford-Experiment, Atomaufbau, Elektronen, Protonen, Neutronen, Element, Ordnungszahl Thema heute: Aufbau von Atomkernen, Kern- umwandlungen
Wiederholung der letzten Vorlesungsstunde: Atommodelle, Rutherford-Experiment, Atomaufbau, Elektronen, Protonen, Neutronen, Element, Ordnungszahl Thema heute: Aufbau von Atomkernen, Kern- umwandlungen
QUALIFIZIERENDER ABSCHLUSS DER MITTELSCHULE. Mittelschule Marktoberdorf. - Fach PCB -
 QUALIFIZIERENDER ABSCHLUSS DER MITTELSCHULE Mittelschule Marktoberdorf - Fach PCB - Themenschwerpunkte aus dem Lehrplan: Grundlagen der Kommunikation Aufnahme und Verarbeitung von Informationen beim Menschen
QUALIFIZIERENDER ABSCHLUSS DER MITTELSCHULE Mittelschule Marktoberdorf - Fach PCB - Themenschwerpunkte aus dem Lehrplan: Grundlagen der Kommunikation Aufnahme und Verarbeitung von Informationen beim Menschen
LB1 Stoffe. LB1 Stoffe. LB1 Stoffe. Womit beschäftigt sich die Chemie?
 Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Lernkartei Klasse 7 LB1: Stoffe Womit beschäftigt sich die Chemie? LB1 Stoffe mit den Stoffen, ihren Eigenschaften und ihren Veränderungen (Stoffumwandlungen) Was sind Stoffe? LB1 Stoffe Stoffe sind die
Stoffmenge. Isotope Radioaktivität. Aufgabe 1-1: Welche Aussagen zum Atomaufbau treffen zu bzw. sind falsch?
 Zusammenfassung Atome bestehen aus Protonen (p + ), Elektronen (e - ) und Neutronen (n) Elemente sind durch ihre Ordnungszahl und Massezahl definiert Stoffmenge n ist ein Maß für die Teilchenanzahl (Atome,
Zusammenfassung Atome bestehen aus Protonen (p + ), Elektronen (e - ) und Neutronen (n) Elemente sind durch ihre Ordnungszahl und Massezahl definiert Stoffmenge n ist ein Maß für die Teilchenanzahl (Atome,
Anorganische-Chemie. Dr. Stefan Wuttke Butenandstr. 11, Haus E, E
 Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Dr. Stefan Wuttke Butenandstr. 11, Haus E, E 3.039 stefan.wuttke@cup.uni-muenchen.de www.wuttkegroup.de Anorganische-Chemie Grundpraktikum für Biologen 2014/2015 Inhaltliche Schwerpunkte Stöchiometrie
Grundbausteine des Mikrokosmos (4) Die Entdeckung des Atomkerns...
 Grundbausteine des Mikrokosmos (4) Die Entdeckung des Atomkerns... Alles begann mit den Röntgenstrahlen... November 1895, Würzburg Wilhelm Conrad Röntgen untersuchte Kathodenstrahlen, wobei er eine Fluoreszenz
Grundbausteine des Mikrokosmos (4) Die Entdeckung des Atomkerns... Alles begann mit den Röntgenstrahlen... November 1895, Würzburg Wilhelm Conrad Röntgen untersuchte Kathodenstrahlen, wobei er eine Fluoreszenz
Basiswissen Chemie. Vorkurs des MINTroduce-Projekts
 Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Basiswissen Chemie Vorkurs des MINTroduce-Projekts Christoph Wölper christoph.woelper@uni-due.de Sprechzeiten (Raum: S07 S00 C24 oder S07 S00 D27) Organisatorisches Kurs-Skript http://www.uni-due.de/ adb297b
Bundesrealgymnasium Imst. Chemie Klasse 4. Aufbauprinzipien der Materie Periodensystem de Elemente
 Bundesrealgymnasium Imst Chemie 2010-11 Periodensystem de Elemente Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff
Bundesrealgymnasium Imst Chemie 2010-11 Periodensystem de Elemente Dieses Skriptum dient der Unterstützung des Unterrichtes - es kann den Unterricht aber nicht ersetzen, da im Unterricht der Lehrstoff
Keine Welt ohne explodierende Sterne. Bruno Leibundgut Europäische Südsternwarte (ESO)
 Keine Welt ohne explodierende Sterne Bruno Leibundgut Europäische Südsternwarte (ESO) Alter der Alpen Entstanden vor etwa 30 bis 35 Millionen Jahren Dinosaurier haben die Alpen nie gekannt! (vor 65 Millionen
Keine Welt ohne explodierende Sterne Bruno Leibundgut Europäische Südsternwarte (ESO) Alter der Alpen Entstanden vor etwa 30 bis 35 Millionen Jahren Dinosaurier haben die Alpen nie gekannt! (vor 65 Millionen
Vorkurs Chemie 17. Oktober 2016 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie. Prof. Dr. Helmut Sitzmann
 Vorkurs Chemie 17. Oktober 2016 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie Prof. Dr. Helmut Sitzmann Vorkurs Chemie 19. Oktober 2015 Fünf Tage Fünf Themen Atombau und Periodensystem Chemische
Vorkurs Chemie 17. Oktober 2016 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie Prof. Dr. Helmut Sitzmann Vorkurs Chemie 19. Oktober 2015 Fünf Tage Fünf Themen Atombau und Periodensystem Chemische
EDUKTE PRODUKTE. Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Reagiert zu
 L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
L2 1 Chemische Reaktion, Energetik Bei einer chemischen Reaktion wandeln sich Stoffe in neue Stoffe mit anderen Eigenschaften um. Symbolische Schreibweise: Ausgangsstoff e EDUKTE Reagiert zu Endstoffe
ATÖMCHEN ... ICH NICHT! STRAHLEN. α Alpha-Strahlen β Beta-Strahlen γ Gamma-Strahlen
 Ihr habt jetzt eine Menge von Strahlung gehört. Was aber sind denn nun diese Strahlen, von denen ich euch erzähle. Sie haben uralte Namen, denn sie werden nach den ersten drei Buchstaben des griechischen
Ihr habt jetzt eine Menge von Strahlung gehört. Was aber sind denn nun diese Strahlen, von denen ich euch erzähle. Sie haben uralte Namen, denn sie werden nach den ersten drei Buchstaben des griechischen
Chemie für Biologen SS 2007. Georg Jansen AG Theoretische Organische Chemie Universität Duisburg Essen. (Teil 1: Einleitung/Atome)
 ChemiefürBiologen SS2007 GeorgJansen AGTheoretischeOrganischeChemie UniversitätDuisburg Essen (Teil1:Einleitung/Atome) Lehrbücher B.Keppler,A.Ding H.P.Latscha,U.Kazmaier,H.A.Klein ChemiefürBiologen 2.Aufl.,Springer
ChemiefürBiologen SS2007 GeorgJansen AGTheoretischeOrganischeChemie UniversitätDuisburg Essen (Teil1:Einleitung/Atome) Lehrbücher B.Keppler,A.Ding H.P.Latscha,U.Kazmaier,H.A.Klein ChemiefürBiologen 2.Aufl.,Springer
