ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
|
|
|
- Calvin Hofmann
- vor 6 Jahren
- Abrufe
Transkript
1 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1
2 1. BEZEICHNUNG DES ARZNEIMITTELS M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension. Masern-Mumps-Röteln-Lebendimpfstoff. 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Dosis (0,5 ml) des rekonstituierten Impfstoffs enthält: Masern-Virus, Stamm Enders Edmonston (lebend, attenuiert) 1 mind. 1 x 10 3 GKID 50 * Mumps-Virus, Stamm Jeryl-Lynn (Level B) (lebend, attenuiert) 1 mind. 12,5 x 10 3 GKID 50 * Röteln-Virus, Stamm Wistar RA 27/3 (lebend, attenuiert) 2 mind. 1 x 10 3 GKID 50 * * Gewebekulturinfektiöse Dosis 50 %. 1 Gezüchtet in Hühnerembryo-Zellen. 2 Gezüchtet in humanen, diploiden Lungenfibroblasten (WI-38). Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension. Vor der Rekonstitution liegt das Pulver als hellgelber, kompakter kristalliner Kuchen vor; das Lösungsmittel ist eine klare, farblose Flüssigkeit. 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete M-M-RVAXPRO ist indiziert zur gleichzeitigen aktiven Immunisierung gegen Masern, Mumps und Röteln ab einem Alter von 12 Monaten (siehe Abschnitt 4.2). Zur Anwendung bei Masern-Ausbrüchen oder zur postexpositionellen Prophylaxe bei nicht schwangeren Jugendlichen und Erwachsenen, zur Impfung bisher ungeimpfter Kinder, die älter als 12 Monate sind und Kontakt zu empfänglichen schwangeren Frauen haben und bei Personen, die wahrscheinlich empfänglich für Mumps- oder Röteln-Viren sind, siehe Abschnitt Dosierung, Art und Dauer der Anwendung Dosierung M-M-RVAXPRO sollte gemäß den offiziellen Impfempfehlungen angewendet werden. Personen ab 12 Monaten Personen ab 12 Monaten sollten eine Dosis zu einem ausgewählten Zeitpunkt erhalten. Eine zweite Dosis kann gemäß den offiziellen Impfempfehlungen frühestens 4 Wochen nach der ersten Dosis verabreicht werden. Mit der zweiten Dosis sollen Personen geschützt werden, die aus welchem Grund auch immer nach der ersten Dosis keinen Immunschutz entwickelt haben. Kinder zwischen 6 und 12 Monaten 2
3 Über die Wirksamkeit und die Verträglichkeit von M-M-RVAXPRO bei Kindern unter 12 Monaten liegen derzeit keine Daten vor (siehe Abschnitt 5.1). Bei Kindern zwischen 6 und 12 Monaten, die während eines Masern-Ausbruchs einen Impfstoff mit einer Masern-Komponente erhielten oder in diesem Alter gemäß den offiziellen Impfempfehlungen geimpft wurden, kann der Impferfolg wegen zirkulierender maternaler Antikörper ausbleiben. Diese Kinder sollten im Alter von 12 bis 15 Monaten erneut geimpft werden und, gemäß den offiziellen Impfempfehlungen, eine weitere Dosis eines Impfstoffs mit einer Masern-Komponente erhalten. Art der Anwendung Der Impfstoff wird subkutan injiziert. Subkutane Injektionen können in den anterolateralen Oberschenkel oder im Bereich des M. deltoideus am Oberarm erfolgen. Anleitung zur Zubereitung des Impfstoffs siehe Abschnitt 6.6. NICHT INTRAVASAL VERABREICHEN. 4.3 Gegenanzeigen Überempfindlichkeit auf frühere Masern-, Mumps- oder Röteln-Impfungen oder gegen einen sonstigen Bestandteil des Impfstoffs einschließlich Neomycin (siehe Abschnitte 2, 4.4 und 6.1). Schwangerschaft (siehe auch Abschnitte 4.4 und 4.6). Bei Erkrankungen mit Fieber > 38,5 C sollte die Impfung verschoben werden. Aktive, unbehandelte Tuberkulose (siehe Abschnitt 4.4). Pathologische Blutbildveränderungen, Leukämie, Lymphome oder andere Malignome mit Auswirkung auf das hämatopoetische oder lymphatische System. Immunsuppressive Behandlung (einschließlich hoher Dosen von Kortikosteroiden). M-M-RVAXPRO ist nicht kontraindiziert bei Personen mit topischer oder niedrig dosierter parenteraler Kortikosteroidtherapie (z. B. zur Asthmaprophylaxe oder als Substitutionstherapie). Humorale oder zelluläre Immundefizienz (angeboren oder erworben), einschließlich Hypo- und Dysgammaglobulinämie, AIDS, symptomatische HIV-Infektion bzw. ein altersspezifischer CD4+-T- Lymphozyten-Anteil von < 25 % (siehe Abschnitt 4.4). Bei stark immungeschwächten Patienten, die versehentlich einen Impfstoff mit einer Masern-Komponente erhielten, wurden Masern- Einschlusskörperchen-Enzephalitis, Pneumonitis und Todesfälle als direkte Folge einer durch das Impfvirus ausgelösten disseminierten Masern-Infektion berichtet. Kongenitale oder erbliche Immundefizienz in der Familienanamnese, es sei denn, der Impfling hat ein nachgewiesenermaßen intaktes Immunsystem. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Für den Fall einer seltenen anaphylaktischen Reaktion nach Verabreichung des Impfstoffs sollten stets geeignete medizinische Behandlungs- und Überwachungsmöglichkeiten unmittelbar zur Verfügung stehen. Die Masern- und die Mumpskomponente des Lebendimpfstoffs werden in Hühnerembryo-Zellen gezüchtet. Bei Personen mit bekannten anaphylaktischen, anaphylaktoiden oder anderen 3
4 Überempfindlichkeitsreaktionen vom Soforttyp (wie Nesselsucht, Schwellungen im Mund- und Rachenraum, Atembeschwerden, Blutdruckabfall oder Schock) nach Verzehr von Hühnereiern besteht daher möglicherweise ein erhöhtes Risiko für Überempfindlichkeitsreaktionen vom Soforttyp. Bei diesen Personen sollte eine sorgfältige Nutzen-Risiko-Abwägung erfolgen. M-M-RVAXPRO sollte bei Personen mit Krampfanfällen oder zerebralen Schädigungen in der Eigenoder Familienanamnese mit Vorsicht angewendet werden. Der Arzt sollte aufmerksam auf eine mögliche Temperaturerhöhung nach Verabreichung des Impfstoffs achten (siehe Abschnitt 4.8). Der Impfstoff enthält 1,9 mg Saccharose als sonstigen Bestandteil. Diese Menge ist nicht ausreichend, um Nebenwirkungen bei Patienten mit seltenen erblichen Erkrankungen wie Fruktose-Intoleranz, Glukose-Galaktose-Malabsorption oder Saccharase-Isomaltase-Insuffizienz hervorzurufen. Der Impfstoff enthält in Spuren rekombinantes Humanalbumin (rha) aus dem Produktionsprozess. In einer Studie mit Kindern, die eine zweite Dosis M-M-RVAXPRO erhielten, wurde keine Sensibilisierung gegen rha beobachtet. Ein theoretisches Risiko einer Überempfindlichkeitsreaktion gegen rha in seltenen Fällen kann nicht ausgeschlossen werden. Daher sollte jedes rha-haltige Produkt nur mit Vorsicht bei Personen angewendet werden, die bereits einmal Anzeichen einer Überempfindlichkeit gegen rha gezeigt haben. Schwangerschaft Schwangere dürfen nicht mit M-M-RVAXPRO geimpft werden. Des Weiteren muss nach der Impfung eine Schwangerschaft 3 Monate lang verhindert werden (siehe Abschnitte 4.3 und 4.6). Thrombozytopenie Eine bestehende Thrombozytopenie kann sich durch die Impfung möglicherweise verschlechtern. Personen, die nach der ersten Dosis von M-M-RVAXPRO (oder nach Gabe der monovalenten Impfstoff-Komponenten) eine Thrombozytopenie entwickelten, können bei erneuter Gabe wieder eine Thrombozytopenie entwickeln. Durch Bestimmung des serologischen Status kann überprüft werden, ob weitere Dosen des Impfstoffs benötigt werden. Vor der Verabreichung des Impfstoffs an diese Personen sollte eine sorgfältige Nutzen-Risiko-Abwägung erfolgen (siehe Abschnitt 4.8). Sonstiges Personen mit nachgewiesener HIV-Infektion ohne Immunsuppression können geimpft werden. Diese Personen sollten sorgfältig hinsichtlich des Auftretens von Masern, Mumps und Röteln beobachtet werden, da der Impfschutz bei Ihnen möglicherweise weniger effektiv ist als bei nicht HIV-infizierten Personen (siehe Abschnitt 4.3). Bei Kindern, die gegen Tuberkulose behandelt werden, führte die Impfung mit Masern- Lebendimpfstoff nicht zu einer Exazerbation der Tuberkulose. Es gibt jedoch keine Studien über die Auswirkungen von Masern-Impfstoffen auf Kinder mit unbehandelter Tuberkulose (siehe Abschnitt 4.3). Wie bei anderen Impfstoffen auch sind nach Impfung mit M-M-RVAXPRO möglicherweise nicht alle Personen geschützt. Übertragung 7 bis 28 Tage nach Verabreichung des Impfstoffs kommt es bei der Mehrzahl empfänglicher Geimpfter zur Ausscheidung von geringen Mengen des attenuierten Röteln-Impfvirus aus dem Nasenoder Rachenraum. Es gibt keinen gesicherten Nachweis, dass auf diesem Weg ausgeschiedene Viren auf empfängliche Personen, die Kontakt mit geimpften Personen haben, übertragen werden. Daher wird eine Übertragung durch engen persönlichen Kontakt zwar als theoretische Möglichkeit, jedoch nicht als signifikantes Risiko betrachtet. Die Übertragung des Röteln-Impfvirus auf Säuglinge über die Muttermilch ist jedoch dokumentiert, allerdings ohne jegliche Anzeichen einer Erkrankung (siehe Abschnitt 4.6). 4
5 Es gibt keine Berichte über eine Übertragung des Enders' Edmonston Masern-Virus-Stamms oder des Jeryl-Lynn TM Mumps-Virus-Stamms von Geimpften auf empfängliche Personen. 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Immunglobulin (Ig) darf nicht gleichzeitig mit M-M-RVAXPRO verabreicht werden. Die gleichzeitige Gabe von Immunglobulinen und M-M-RVAXPRO kann die zu erwartende Immunantwort beeinträchtigen. Die Impfung sollte frühestens 3 Monate nach Blut- oder Plasmatransfusionen oder der Gabe von Human-Immunglobulinen erfolgen. Die Gabe von Blutprodukten mit Masern-, Mumps- oder Röteln-Virus-Antikörpern, einschließlich Immunglobulin-Präparaten, sollte frühestens einen Monat nach Impfung mit M-M-RVAXPRO erfolgen, es sei denn, die Gabe dieser Präparate ist unumgänglich. Nach Impfung mit Masern-Mumps-Röteln-Lebendimpfstoffen kann die Empfindlichkeit von Tuberkulin-Hauttestungen vorübergehend vermindert sein. Wenn ein Tuberkulintest geplant ist, sollte der Test entweder vor, gleichzeitig mit oder mindestens 4 bis 6 Wochen nach der Impfung mit M-M-RVAXPRO durchgeführt werden. Gleichzeitige Gabe mit anderen Impfstoffen Publizierte klinische Daten belegen, dass die bisherige Formulierung von Masern-, Mumps- und Röteln-Impfstoff von Merck & Co., Inc. gleichzeitig mit anderen pädiatrischen Impfstoffen, einschließlich DTaP (oder DTwP), IPV (oder OPV), Hib (Haemophilus influenzae Typ b), Hib-HBV (Haemophilus influenzae Typ b, kombiniert mit Hepatitis B) und VAR (Varizellen) verabreicht werden kann. Es wurden bisher keine speziellen Studien zur gleichzeitigen Gabe von M-M-RVAXPRO mit anderen Impfstoffen durchgeführt. Es wurde jedoch gezeigt, dass das Nebenwirkungs- und Immunogenitäts- Profil von M-M-RVAXPRO mit dem bisherigen Masern-, Mumps- und Röteln- Kombinationsimpfstoff von Merck & Co., Inc. vergleichbar ist. Deshalb kann die Erfahrung mit diesem Impfstoff zu Grunde gelegt werden. M-M-RVAXPRO kann daher an unterschiedlichen Körperstellen gleichzeitig oder im Abstand von einem Monat mit anderen Virus-Lebendimpfstoffen verabreicht werden. 4.6 Schwangerschaft und Stillzeit Es wurden keine Studien über die Anwendung von M-M-RVAXPRO bei Schwangeren durchgeführt. Es ist daher nicht bekannt, ob M-M-RVAXPRO schädliche Auswirkungen auf den Fetus haben kann oder die Fortpflanzungsfähigkeit beeinträchtigen kann. Daher dürfen Schwangere nicht mit M-M- RVAXPRO geimpft werden. Des Weiteren muss nach der Impfung eine Schwangerschaft 3 Monate lang verhindert werden (siehe Abschnitte 4.3 und 4.4). Bei der Beratung von Frauen, die versehentlich während der Schwangerschaft geimpft wurden oder die in den ersten 3 Monaten nach der Impfung schwanger wurden, sollte der Arzt folgendes beachten: (1) In einem Zeitraum von 10 Jahren wurden mehr als 700 schwangere Frauen beobachtet, denen bis zu drei Monate vor oder nach Konzeption ein Röteln-Impfstoff verabreicht worden war (189 dieser Frauen erhielten den Röteln-Impfstamm Wistar RA 27/3). Bei keinem der Neugeborenen wurden die für eine Röteln-Embryopathie typischen Schädigungen festgestellt. (2) Die Infektion mit Mumps- Wildvirus im ersten Trimenon kann zu einer erhöhten Rate von Spontanaborten führen. Obwohl Infektionen von Plazenta und Fetus mit Mumps-Impfvirus nachgewiesen wurden, gibt es keinen Nachweis kongenitaler Fehlbildungen beim Menschen durch diese Infektion. (3) Es gibt Belege dafür, dass eine Infektion mit Masern-Wildvirus in der Schwangerschaft zu einem erhöhten Risiko einer fetalen Schädigung führt. Nach Masern-Wildinfektion in der Schwangerschaft wurde eine erhöhte Rate von Spontanaborten, Totgeburten, angeborenen Missbildungen und Frühgeburten beobachtet. Es gibt keine geeigneten Studien darüber, wie sich ein Kontakt mit attenuierten Masern-Impfvirus- 5
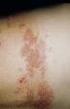
6 Stämmen während der Schwangerschaft auswirkt. Vorsichtshalber sollte jedoch davon ausgegangen werden, dass auch der Impfvirus-Stamm zu fetalen Schädigungen führen könnte. Hinweis: Offizielle Impfempfehlungen können hinsichtlich der Dauer der Kontrazeption nach Impfung in verschiedenen Ländern unterschiedlich sein. Wochenbett Es hat sich vielfach als vorteilhaft erwiesen, für Röteln empfängliche Frauen unmittelbar nach der Entbindung zu impfen. Studien haben gezeigt, dass stillende Mütter, die postpartal mit einem attenuierten Röteln- Lebendimpfstoff geimpft wurden, das Virus mit der Muttermilch ausscheiden und so auf ihre Säuglinge übertragen können. Keiner der Säuglinge, bei denen eine Röteln-Infektion serologisch nachgewiesen wurde, zeigte Symptome einer Röteln-Erkrankung. Es ist nicht bekannt, ob Masernoder Mumps-Impfviren mit der Muttermilch ausgeschieden werden. Daher sollte sorgfältig abgewogen werden, ob M-M-RVAXPRO an stillende Mütter verabreicht wird. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. 4.8 Nebenwirkungen In einer klinischen Studie wurden 641 Kinder (siehe Abschnitt 5.1) mit M-M-RVAXPRO geimpft. Das allgemeine Nebenwirkungsprofil war vergleichbar mit dem Nebenwirkungsprofil von früheren Formulierungen des Masern-, Mumps- und Röteln-Impfstoffs von Merck & Co., Inc. Alle bei 634 Kindern beobachteten Nebenwirkungen wurden ausgewertet. Bei diesen Kindern wurden folgende Impfstoff-bezogenen Nebenwirkungen nach Gabe von M-M-RVAXPRO beobachtet (nicht berücksichtigt sind Einzelfälle mit einer Häufigkeit von < 0,2 %): [Sehr häufig ( 1/10); häufig ( 1/100 bis < 1/10); gelegentlich ( 1/1.000 bis < 1/100)] Infektionen und parasitäre Erkrankungen Gelegentlich: Nasopharyngitis, Infektionen der oberen Atemwege oder virale Infekte. Erkrankungen der Atemwege, des Brustraums und des Mediastinums Gelegentlich: Rhinorrhoe. Erkrankungen des Gastrointestinaltrakts Gelegentlich: Durchfall oder Erbrechen. Erkrankungen der Haut und des Unterhautzellgewebes Häufig: morbilliformes Exanthem oder anderes Exanthem. Gelegentlich: Urtikaria. Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Sehr häufig: Fieber (38,5 C oder höher), Erythem an der Injektionsstelle, Schmerz an der Injektionsstelle, Schwellung an der Injektionsstelle. Häufig: Hämatom an der Injektionsstelle. Gelegentlich: Exanthem an der Injektionsstelle. Im Vergleich zur ersten Dosis treten nach Verabreichung einer zweiten Dosis M-M-RVAXPRO klinische Symptome, einschließlich solcher, die auf allergische Reaktionen hinweisen, weder häufiger noch stärker ausgeprägt auf. 6
7 Mögliche Nebenwirkungen Weitere Nebenwirkungen wurden in klinischen Studien und nach Zulassung von früheren Formulierungen der monovalenten Masern-, Mumps- und Röteln-Impfstoffe und des MMR-Kombinationsimpfstoffs von Merck & Co., Inc. berichtet. Diese Nebenwirkungen sind ohne Berücksichtigung einer möglichen Kausalität oder der Häufigkeit ihres Auftretens im Folgenden aufgeführt. Mögliche Nebenwirkungen, über die in vorhergehenden Abschnitten bereits berichtet wurde (und die sich auf klinische Studien mit M-M-RVAXPRO beziehen), sind nicht mehr aufgeführt. Infektionen und parasitäre Erkrankungen Aseptische Meningitis (siehe unten), atypische Masern, Orchitis, Otitis media, Parotitis, Rhinitis, subakute sklerosierende Panenzephalitis (siehe unten). Über Fälle aseptischer Meningitis wurde nach Masern-Mumps-Röteln-Impfung berichtet. Ein Kausalzusammenhang zwischen anderen Stämmen des Mumps-Impfstoffs und aseptischer Meningitis konnte gezeigt werden, es gibt jedoch keinen Hinweis auf einen Zusammenhang zwischen dem im Impfstoff enthaltenen Jeryl-Lynn -Mumps-Impfstamm und aseptischer Meningitis. Erkrankungen des Blutes und des Lymphsystems Regionale Lymphadenopathie, Thrombozytopenie. Erkrankungen des Immunsystems Anaphylaktoide Reaktionen, Anaphylaxie und verwandte Symptome wie angioneurotisches Ödem, Gesichtsödem und periphere Ödeme. Psychiatrische Erkrankungen Reizbarkeit. Erkrankungen des Nervensystems Afebrile Krämpfe oder Anfälle, Ataxie, Benommenheit, Enzephalitis (siehe unten), Enzephalopathie (siehe unten), Fieberkrämpfe (bei Kindern), Guillain-Barré-Syndrom, Kopfschmerzen, Masern- Einschlusskörperchen-Enzephalitis (MIBE) (siehe Abschnitt 4.3), Augenmuskellähmungen, Optikusneuritis, Parästhesien, Polyneuritis, Polyneuropathie, Retrobulbärneuritis, Synkopen. Pro 3 Millionen verabreichter Dosen von Impfstoffen mit einer Masernkomponente, hergestellt von Merck & Co., Inc., wurde ein Fall von Enzephalitis und Enzephalopathie, ausgenommen subakute sklerosierende Panenzephalitis (SSPE), berichtet. Postmarketing-Beobachtungen mit den weltweit über einen Zeitraum von fast 25 Jahren (1978 bis 2003) mehr als 400 Millionen verkauften Dosen weisen darauf hin, dass schwerwiegende Nebenwirkungen wie Enzephalitis und Enzephalopathie auch weiterhin nur selten beobachtet werden. In keinem Fall konnte schlüssig nachgewiesen werden, dass die Nebenwirkungen tatsächlich durch die Impfung verursacht wurden; die Daten lassen jedoch vermuten, dass einige der Fälle möglicherweise durch Masern-Impfstoffe hervorgerufen worden sein könnten. Es gibt keinen Beleg dafür, dass Masern-Impfstoffe SSPE verursachen können. Es gab Berichte über SSPE bei Kindern, die sich laut Anamnese nicht mit dem Masern-Wildvirus infiziert, jedoch einen Masern-Impfstoff erhalten hatten. Einige dieser Fälle könnten auf eine unerkannte Masern-Infektion während des ersten Lebensjahres oder auch auf die Masern-Impfung zurückzuführen sein. Eine retrospektive Fall-Kontrollstudie, die von den US-amerikanischen Centers for Disease Control and Prevention durchgeführt wurde, deutet darauf hin, dass eine Masern-Impfung insgesamt gegen SSPE schützt, da die Impfung eine Masern-Erkrankung und das damit einhergehende Risiko einer SSPE verhindert. Augenerkrankungen Konjunktivitis, Retinitis. 7
8 Erkrankungen des Ohrs und des Labyrinths Retrokochläre Taubheit. Erkrankungen der Atemwege, des Brustraums und des Mediastinums Bronchospasmus, Husten, Pneumonitis (siehe Abschnitt 4.3), Halsschmerzen. Erkrankungen des Gastrointestinaltrakts Übelkeit. Erkrankungen der Haut und des Unterhautzellgewebes Panniculitis, Purpura, Verhärtung der Haut, Stevens-Johnson-Syndrom. Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Arthritis und/oder Arthralgien (in der Regel vorübergehend und selten chronisch [siehe unten]), Myalgien. Arthralgie und/oder Arthritis (in der Regel vorübergehend und selten chronisch) sowie Polyneuritis sind charakteristisch für eine Infektion mit Röteln-Wildvirus; Häufigkeit und Schweregrad variieren in Abhängigkeit von Alter und Geschlecht und sind am ausgeprägtesten bei erwachsenen Frauen, am wenigsten ausgeprägt bei Kindern vor der Pubertät. Bei Kindern sind Gelenkbeschwerden nach einer Impfung in der Regel weniger häufig (0 3 %) und von kurzer Dauer. Bei Frauen ist die Inzidenz von Arthritis und Arthralgien in der Regel höher als bei Kindern (12 20 %); die Symptome sind tendenziell ausgeprägter und länger anhaltend und können über mehrere Monate persistieren, in seltenen Fällen sogar über Jahre. Die Häufigkeit bei weiblichen Jugendlichen scheint zwischen der bei Kindern und erwachsenen Frauen beobachteten Häufigkeit zu liegen. Diese Nebenwirkungen werden in der Regel auch von Frauen zwischen 35 und 45 Jahren gut toleriert und beeinträchtigen den normalen Tagesablauf kaum. Chronische Arthritis wurde mit Röteln-Wildvirus-Infektionen in Verbindung gebracht und auf persistierende Viren und/oder virale Antigene zurückgeführt, die aus Körpergewebe isoliert wurden. Bei geimpften Personen kam es nur selten zu chronischen Gelenkbeschwerden. Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Brennen und/oder Stechen von kurzer Dauer an der Injektionsstelle, Fieber (38,5 C oder höher), Unwohlsein, Papillitis, periphere Ödeme, Schwellung, Schmerzhaftigkeit, Bläschen an der Injektionsstelle, Quaddeln und Entzündungen an der Injektionsstelle. 4.9 Überdosierung Fälle von Überdosierung wurden selten berichtet und hatten keine schweren Nebenwirkungen zur Folge. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Viraler Impfstoff, ATC-Code: J07BD52. Bewertung der Immunogenität und klinischen Wirksamkeit Eine vergleichende klinische Studie mit Personen, die entweder mit M-M-RVAXPRO oder der früheren Formulierung des Masern-, Mumps- und Röteln-Impfstoffs von Merck & Co., Inc. (hergestellt mit humanem Serumalbumin), geimpft worden waren, zeigte eine vergleichbare Immunogenität und ein vergleichbares Nebenwirkungsprofil der beiden Produkte. Klinische Studien an 284 (dreifach) seronegativen Kindern im Alter von 11 Monaten bis 7 Jahren belegen, dass die frühere Formulierung des Masern-, Mumps- und Röteln-Impfstoffs von Merck & 8
9 Co., Inc. hoch immunogen und generell gut verträglich ist. In diesen Studien konnten nach Gabe einer Einzeldosis bei 95 % der empfänglichen Probanden Hämagglutinations-hemmende (HI) Antikörper gegen Masern, bei 96 % neutralisierende Antikörper gegen Mumps und bei 99 % HI-Antikörper gegen Röteln nachgewiesen werden. Die Wirksamkeit der Komponenten der früheren Formulierung des Masern-, Mumps- und Röteln- Impfstoffs von Merck & Co., Inc. wurde durch eine Reihe von kontrollierten Doppel-Blind- Feldstudien belegt; in diesen Studien wurde eine hohe Schutzwirkung der einzelnen Impfstoffkomponenten nachgewiesen. Diese Studien belegen außerdem, dass eine postvakzinale Serokonversion gegen Masern, Mumps und Röteln mit dem Schutz vor diesen Krankheiten korreliert. Postexpositionelle Impfung Die Impfung nach Masern-Wildvirus-Exposition kann einen gewissen Schutz bieten, wenn der Impfstoff innerhalb von 72 Stunden nach Exposition verabreicht wird. Wenn der Impfstoff einige Tage vor einer Exposition verabreicht wird, kann jedoch ein guter Schutz aufgebaut werden. Es gibt keine Daten darüber, ob eine postexpositionelle Impfung nach Mumps- oder Röteln-Wildvirus- Exposition Schutz bietet. Wirksamkeit Weltweit wurden mehr als 400 Millionen Dosen der früheren Formulierung des Masern-, Mumps- und Röteln-Impfstoffs von Merck & Co., Inc. vertrieben (1978 bis 2003). Die weit verbreitete Anwendung eines 2-Dosen-Impfschemas in den Vereinigten Staaten und in Ländern wie Finnland und Schweden führte zu einem Rückgang der Häufigkeit aller drei Erkrankungen um mehr als 99 %. Nicht schwangere Jugendliche und Erwachsene Die Impfung empfänglicher nicht schwangerer Jugendlicher und Erwachsener im gebärfähigen Alter mit Röteln-Lebendimpfstoff ist angezeigt, wenn bestimmte Vorsichtsmaßnahmen beachtet werden (siehe Abschnitte 4.4 und 4.6). Die Impfung von empfänglichen Frauen nach der Pubertät schützt gegen eine Infektion mit Röteln während der Schwangerschaft und damit vor einer Infektion des Ungeborenen mit nachfolgender Röteln-Embryopathie. Ungeimpfte Kinder über 12 Monate mit Kontakt zu empfänglichen Schwangeren sollten mit Röteln- Lebendimpfstoff geimpft werden (wie beispielsweise M-M-RVAXPRO oder monovalenter Röteln- Impfstoff), um das Expositionsrisiko für die Schwangere zu reduzieren. Möglicherweise für Mumps und Röteln empfängliche Personen M-M-RVAXPRO ist vorzugsweise auch bei Personen mit Masern-Immunität, jedoch unklarem Immunstatus gegen Mumps und Röteln, anzuwenden. Personen ohne Masern-Immunität können unabhängig von ihrem Immunstatus mit M-M-RVAXPRO gegen Mumps oder Röteln geimpft werden, wenn kein monovalenter Masern-Impfstoff zur Verfügung steht. 5.2 Pharmakokinetische Eigenschaften Daten zu pharmakokinetischen Eigenschaften sind für Impfstoffe nicht erforderlich. 5.3 Präklinische Daten zur Sicherheit Herkömmliche präklinische Studien wurden nicht durchgeführt, da keine präklinischen Effekte zu erwarten sind, die über die in anderen Abschnitten dieser Zusammenfassung der Merkmale des Arzneimittels beschriebenen Daten hinausgehen und die im Hinblick auf die klinische Sicherheit relevant sind. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile 9
10 Pulver Sorbitol Natriumphosphat Kaliumphosphat Saccharose Hydrolisierte Gelatine Medium 199 mit Hanks Salzen Minimum Essential Medium, Eagle (MEM) Natriumglutamat Neomycin Phenolrot Natriumhydrogencarbonat Salzsäure (zur ph-einstellung) Natriumhydroxid (zur ph-einstellung) Lösungsmittel Wasser für Injektionszwecke 6.2 Inkompatibilitäten Da keine Kompatibilitätsstudien durchgeführt wurden, darf dieser Impfstoff nicht mit anderen Arzneimitteln gemischt werden. 6.3 Dauer der Haltbarkeit 2 Jahre. Nach Rekonstitution sollte der Impfstoff umgehend angewendet werden; entsprechende Daten belegen jedoch die Stabilität des rekonstituierten Impfstoffs bis zu 8 Stunden, wenn er im Kühlschrank bei 2 C 8 C gelagert wird. 6.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung Kühl lagern und transportieren (2 C 8 C). Nicht einfrieren. Vor Licht schützen. Lagerungsbedingungen des rekonstituierten Impfstoffs siehe Abschnitt Art und Inhalt des Behältnisses Pulver in einem Fläschchen (Glasart 1) mit Stopfen (Butyl-Gummi) und Lösungsmittel in einem Fläschchen (Glasart 1) mit Stopfen (Chlorobutyl-Gummi) in Packungsgrößen zu 1x1 und 10x1 Dosis. Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht. 6.6 Besondere Vorsichtsmaßnahmen für die Beseitigung Zur Rekonstitution des Impfstoffs muss das beigepackte Lösungsmittel verwendet werden. Das Lösungsmittel ist eine klare, farblose Flüssigkeit. Vor dem Mischen mit dem Lösungsmittel liegt das Pulver als hellgelber, kompakter kristalliner Kuchen vor. Nach der Rekonstitution ist der Impfstoff eine klare, gelbe Flüssigkeit. Es ist unerlässlich, für jeden Impfling jeweils eine separate sterile Spritze und Kanüle zu verwenden, um die Übertragung von Krankheitserregern von einem Impfling auf den anderen zu verhindern. Anleitung zur Rekonstitution 10
11 Zur Rekonstitution des Pulvers wird die gesamte Lösungsmittelmenge in einer Spritze aufgezogen. Der gesamte Inhalt der Spritze wird in das Fläschchen mit dem Pulver injiziert. Das Fläschchen wird vorsichtig geschwenkt, um den Inhalt gründlich zu mischen. Die gesamte Menge des rekonstituierten Impfstoffs wird wieder in die Spritze aufgezogen und vollständig verimpft. Der rekonstituierte Impfstoff darf nicht verwendet werden, wenn er Partikel enthält oder das Aussehen des Lösungsmittels, des Pulvers oder des rekonstituierten Impfstoffs von dem oben beschriebenen abweicht. Nicht verwendeter Impfstoff oder Abfallmaterial ist gemäß den nationalen Anforderungen zu entsorgen. 7. INHABER DER ZULASSUNG Sanofi Pasteur MSD SNC 8, rue Jonas Salk F Lyon Frankreich 8. ZULASSUNGSNUMMER(N) 9. DATUM DER ERTEILUNG DER ZULASSUNG/VERLÄNGERUNG DER ZULASSUNG 10. STAND DER INFORMATION 11
12 1. BEZEICHNUNG DES ARZNEIMITTELS M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze. Masern-Mumps-Röteln-Lebendimpfstoff. 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Eine Dosis (0,5 ml) des rekonstituierten Impfstoffs enthält: Masern-Virus, Stamm Enders Edmonston (lebend, attenuiert) 1 mind. 1 x 10 3 GKID 50 * Mumps-Virus, Stamm Jeryl-Lynn (Level B) (lebend, attenuiert) 1 mind. 12,5 x 10 3 GKID 50 * Röteln-Virus, Stamm Wistar RA 27/3 (lebend, attenuiert) 2 mind. 1 x 10 3 GKID 50 * * Gewebekulturinfektiöse Dosis 50 %. 1 Gezüchtet in Hühnerembryozellen. 2 Gezüchtet in humanen, diploiden Lungenfibroblasten (WI-38). Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt DARREICHUNGSFORM Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze. Vor der Rekonstitution liegt das Pulver als hellgelber, kompakter kristalliner Kuchen vor; das Lösungsmittel ist eine klare, farblose Flüssigkeit. 4. KLINISCHE ANGABEN 4.1 Anwendungsgebiete M-M-RVAXPRO ist indiziert zur gleichzeitigen aktiven Immunisierung gegen Masern, Mumps und Röteln ab einem Alter von 12 Monaten (siehe Abschnitt 4.2). Zur Anwendung bei Masern-Ausbrüchen oder zur postexpositionellen Prophylaxe bei nicht schwangeren Jugendlichen und Erwachsenen, zur Impfung bisher ungeimpfter Kinder, die älter als 12 Monate sind und Kontakt zu empfänglichen schwangeren Frauen haben und bei Personen,, die wahrscheinlich empfänglich für Mumps- oder Röteln-Viren sind, siehe Abschnitt Dosierung, Art und Dauer der Anwendung Dosierung M-M-RVAXPRO sollte gemäß den offiziellen Impfempfehlungen angewendet werden. Personen ab 12 Monaten Personen ab 12 Monaten sollten eine Dosis zu einem ausgewählten Zeitpunkt erhalten. Eine zweite Dosis kann gemäß den offiziellen Impfempfehlungen frühestens 4 Wochen nach der ersten Dosis verabreicht werden. Mit der zweiten Dosis sollen Personen geschützt werden, die aus welchem Grund auch immer nach der ersten Dosis keinen Impfschutz entwickelt haben. Kinder zwischen 6 und 12 Monaten 12
13 Über die Wirksamkeit und die Verträglichkeit von M-M-RVAXPRO bei Kindern unter 12 Monaten liegen derzeit keine Daten vor (siehe Abschnitt 5.1). Bei Kindern zwischen 6 und 12 Monaten, die während eines Masern-Ausbruchs einen Impfstoff mit einer Masern-Komponente erhielten oder in diesem Alter gemäß den offiziellen Impfempfehlungen geimpft wurden, kann der Impferfolg wegen zirkulierender maternaler Antikörper ausbleiben. Diese Kinder sollten im Alter von 12 bis 15 Monaten erneut geimpft werden und, gemäß den offiziellen Impfempfehlungen, eine weitere Dosis eines Impfstoffs mit einer Masern-Komponente erhalten. Art der Anwendung Der Impfstoff wird subkutan injiziert. Subkutane Injektionen können in den anterolateralen Oberschenkel oder im Bereich des M. deltoideus am Oberarm erfolgen. Anleitung zur Zubereitung des Impfstoffs siehe Abschnitt 6.6. NICHT INTRAVASAL VERABREICHEN. 4.3 Gegenanzeigen Überempfindlichkeit auf frühere Masern-, Mumps- oder Röteln-Impfungen oder gegen einen sonstigen Bestandteil des Impfstoffs einschließlich Neomycin (siehe Abschnitte 2, 4.4 und 6.1). Schwangerschaft (siehe auch Abschnitte 4.4 und 4.6). Bei Erkrankungen mit Fieber > 38,5 C sollte die Impfung verschoben werden. Aktive, unbehandelte Tuberkulose (siehe Abschnitt 4.4). Pathologische Blutbildveränderungen, Leukämie, Lymphome oder andere Malignome mit Auswirkung auf das hämatopoetische oder lymphatische System. Immunsuppressive Behandlung (einschließlich hoher Dosen von Kortikosteroiden). M-M-RVAXPRO ist nicht kontraindiziert bei Personen mit topischer oder niedrig dosierter parenteraler Kortikosteroidtherapie (z. B. zur Asthmaprophylaxe oder als Substitutionstherapie). Humorale oder zelluläre Immundefizienz (angeboren oder erworben), einschließlich Hypo- und Dysgammaglobulinämie, AIDS, symptomatische HIV-Infektion bzw. ein altersspezifischer CD4+-T- Lymphozyten-Anteil von < 25 % (siehe Abschnitt 4.4). Bei stark immungeschwächten Patienten, die versehentlich einen Impfstoff mit einer Masern-Komponente erhielten, wurden Masern- Einschlusskörperchen-Enzephalitis, Pneumonitis und Todesfälle als direkte Folge einer durch das Impfvirus ausgelösten disseminierten Masern-Infektion berichtet. Kongenitale oder erbliche Immundefizienz in der Familienanamnese, es sei denn, der Impfling hat ein nachgewiesenermaßen intaktes Immunsystem. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen für die Anwendung Für den Fall einer seltenen anaphylaktischen Reaktion nach Verabreichung des Impfstoffs sollten stets geeignete medizinische Behandlungs- und Überwachungsmöglichkeiten unmittelbar zur Verfügung stehen. Die Masern- und die Mumpskomponente des Lebendimpfstoffs werden in Hühnerembryo-Zellen gezüchtet. Bei Personen mit bekannten anaphylaktischen, anaphylaktoiden oder anderen 13
14 Überempfindlichkeitsreaktionen vom Soforttyp (wie Nesselsucht, Schwellungen im Mund- und Rachenraum, Atembeschwerden, Blutdruckabfall oder Schock) nach Verzehr von Hühnereiern besteht daher möglicherweise ein erhöhtes Risiko für Überempfindlichkeitsreaktionen vom Soforttyp. Bei diesen Personen sollte eine sorgfältige Nutzen-Risiko-Abwägung erfolgen. M-M-RVAXPRO sollte bei Personen mit Krampfanfällen oder zerebralen Schädigungen in der Eigenoder Familienanamnese mit Vorsicht angewendet werden. Der Arzt sollte aufmerksam auf eine mögliche Temperaturerhöhung nach Verabreichung des Impfstoffs achten (siehe Abschnitt 4.8). Der Impfstoff enthält 1,9 mg Saccharose als sonstigen Bestandteil. Diese Menge ist nicht ausreichend, um Nebenwirkungen bei Patienten mit seltenen erblichen Erkrankungen wie Fruktose-Intoleranz, Glukose-Galactose-Malabsorption oder Saccharase-Isomaltase-Insuffizienz hervorzurufen. Der Impfstoff enthält in Spuren rekombinantes Humanalbumin (rha) aus dem Produktionsprozess. In einer Studie mit Kindern, die eine zweite Dosis M-M-RVAXPRO erhielten, wurde keine Sensibilisierung gegen rha beobachtet. Ein theoretisches Risiko einer Überempfindlichkeitsreaktion gegen rha in seltenen Fällen kann nicht ausgeschlossen werden. Daher sollte jedes rha-haltige Produkt nur mit Vorsicht bei Personen angewendet werden, die bereits einmal Anzeichen einer Überempfindlichkeit gegen rha gezeigt haben. Schwangerschaft Schwangere dürfen nicht mit M-M-RVAXPRO geimpft werden. Des Weiteren muss nach der Impfung eine Schwangerschaft 3 Monate lang verhindert werden (siehe Abschnitte 4.3 und 4.6). Thrombozytopenie Eine bestehende Thrombozytopenie kann sich durch die Impfung möglicherweise verschlechtern. Personen, die nach der ersten Dosis von M-M-RVAXPRO (oder nach Gabe der monovalenten Impfstoff-Komponenten) eine Thrombozytopenie entwickelten, können bei erneuter Gabe wieder eine Thrombozytopenie entwickeln. Durch Bestimmung des serologischen Status kann überprüft werden, ob weitere Dosen des Impfstoffs benötigt werden. Vor der Verabreichung des Impfstoffs an diese Personen sollte eine sorgfältige Nutzen-Risiko-Abwägung erfolgen (siehe Abschnitt 4.8). Sonstiges Personen mit nachgewiesener HIV-Infektion ohne Immunsuppression können geimpft werden. Diese Personen sollten sorgfältig hinsichtlich des Auftretens von Masern, Mumps und Röteln beobachtet werden, da der Impfschutz bei Ihnen möglicherweise weniger effektiv ist als bei nicht HIV-infizierten Personen (siehe Abschnitt 4.3). Bei Kindern, die gegen Tuberkulose behandelt werden, führte die Impfung mit Masern- Lebendimpfstoff nicht zu einer Exazerbation der Tuberkulose. Es gibt jedoch keine Studien über die Auswirkungen von Masern-Impfstoffen auf Kinder mit unbehandelter Tuberkulose (siehe Abschnitt 4.3). Wie bei anderen Impfstoffen auch sind nach Impfung mit M-M-RVAXPRO möglicherweise nicht alle Personen geschützt. Übertragung 7 bis 28 Tage nach Verabreichung des Impfstoffs kommt es bei der Mehrzahl empfänglicher Geimpfter zur Ausscheidung von geringen Mengen des attenuierten Röteln-Impfvirus aus dem Nasenoder Rachenraum. Es gibt keinen gesicherten Nachweis, dass auf diesem Weg ausgeschiedene Viren auf empfängliche Personen, die Kontakt mit geimpften Personen haben, übertragen werden. Daher wird eine Übertragung durch engen persönlichen Kontakt zwar als theoretische Möglichkeit, jedoch nicht als signifikantes Risiko betrachtet. Die Übertragung des Röteln-Impfvirus auf Säuglinge über die Muttermilch ist jedoch dokumentiert, allerdings ohne jegliche Anzeichen einer Erkrankung (siehe Abschnitt 4.6). 14
15 Es gibt keine Berichte über eine Übertragung des Enders' Edmonston Masern-Virus-Stamms oder des Jeryl-Lynn TM Mumps-Virus-Stamms von Geimpften auf empfängliche Personen. 4.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen Immunglobulin (Ig) darf nicht gleichzeitig mit M-M-RVAXPRO verabreicht werden. Die gleichzeitige Gabe von Immunglobulinen und M-M-RVAXPRO kann die zu erwartende Immunantwort beeinträchtigen. Die Impfung sollte frühestens 3 Monate nach Blut- oder Plasmatransfusionen oder der Gabe von Human-Immunglobulinen erfolgen. Die Gabe von Blutprodukten mit Masern-, Mumps- oder Röteln-Virus-Antikörpern, einschließlich Immunglobulin-Präparaten, sollte frühestens einen Monat nach Impfung mit M-M-RVAXPRO erfolgen, es sei denn, die Gabe dieser Präparate ist unumgänglich. Nach Impfung mit Masern-Mumps-Röteln-Lebendimpfstoffen kann die Empfindlichkeit von Tuberkulin-Hauttestungen vorübergehend vermindert sein. Wenn ein Tuberkulintest geplant ist, sollte der Test entweder vor, gleichzeitig mit oder mindestens 4 bis 6 Wochen nach der Impfung mit M-M-RVAXPRO durchgeführt werden. Gleichzeitige Gabe mit anderen Impfstoffen Publizierte klinische Daten belegen, dass die bisherige Formulierung von Masern-, Mumps- und Röteln-Impfstoff von Merck & Co., Inc. gleichzeitig mit anderen pädiatrischen Impfstoffen, einschließlich DTaP (oder DTwP), IPV (oder OPV), Hib (Haemophilus influenzae Typ b), Hib-HBV (Haemophilus influenzae Typ b, kombiniert mit Hepatitis B) und VAR (Varizellen) verabreicht werden kann. Es wurden bisher keine speziellen Studien zur gleichzeitigen Gabe von M-M-RVAXPRO mit anderen Impfstoffen durchgeführt. Es wurde jedoch gezeigt, dass das Nebenwirkungs- und Immunogenitäts- Profil von M-M-RVAXPRO mit dem bisherigen Masern-, Mumps- und Röteln- Kombinationsimpfstoff von Merck & Co., Inc. vergleichbar ist. Deshalb kann die Erfahrung mit diesem Impfstoff zu Grunde gelegt werden. M-M-RVAXPRO kann daher an unterschiedlichen Körperstellen gleichzeitig oder im Abstand von einem Monat mit anderen Virus-Lebendimpfstoffen verabreicht werden. 4.6 Schwangerschaft und Stillzeit Es wurden keine Studien über die Anwendung von M-M-RVAXPRO bei Schwangeren durchgeführt. Es ist daher nicht bekannt, ob M-M-RVAXPRO schädliche Auswirkungen auf den Fetus haben kann oder die Fortpflanzungsfähigkeit beeinträchtigen kann. Daher dürfen Schwangere nicht mit M-M- RVAXPRO geimpft werden. Des Weiteren muss nach der Impfung eine Schwangerschaft 3 Monate lang verhindert werden (siehe Abschnitte 4.3 und 4.4). Bei der Beratung von Frauen, die versehentlich während der Schwangerschaft geimpft wurden oder die in den ersten 3 Monaten nach der Impfung schwanger wurden, sollte der Arzt folgendes beachten: (1) In einem Zeitraum von 10 Jahren wurden mehr als 700 schwangere Frauen beobachtet, denen bis zu drei Monate vor oder nach Konzeption ein Röteln-Impfstoff verabreicht worden war (189 dieser Frauen erhielten den Röteln-Impfstamm Wistar RA 27/3). Bei keinem der Neugeborenen wurden die für eine Röteln-Embryopathie typischen Schädigungen festgestellt. (2) Die Infektion mit Mumps- Wildvirus im ersten Trimenon kann zu einer erhöhten Rate von Spontanaborten führen. Obwohl Infektionen von Plazenta und Fetus mit Mumps-Impfvirus nachgewiesen wurden, gibt es keinen Nachweis kongenitaler Fehlbildungen beim Menschen durch diese Infektion. (3) Es gibt Belege dafür, dass eine Infektion mit Masern-Wildvirus in der Schwangerschaft zu einem erhöhten Risiko einer fetalen Schädigung führt. Nach Masern-Wildinfektion in der Schwangerschaft wurde eine erhöhte Rate von Spontanaborten, Totgeburten, angeborenen Missbildungen und Frühgeburten beobachtet. Es gibt keine geeigneten Studien darüber, wie sich ein Kontakt mit attenuierten Masern-Impfvirus- 15
16 Stämmen während der Schwangerschaft auswirkt. Vorsichtshalber sollte jedoch davon ausgegangen werden, dass auch der Impfvirus-Stamm zu fetalen Schädigungen führen könnte. Hinweis: Offizielle Impfempfehlungen können hinsichtlich der Dauer der Kontrazeption nach Impfung in verschiedenen Ländern unterschiedlich sein. Wochenbett Es hat sich vielfach als vorteilhaft erwiesen, für Röteln empfängliche Frauen unmittelbar nach der Entbindung zu impfen. Studien haben gezeigt, dass stillende Mütter, die postpartal mit einem attenuierten Röteln- Lebendimpfstoff geimpft wurden, das Virus mit der Muttermilch ausscheiden und so auf ihre Säuglinge übertragen können. Keiner der Säuglinge, bei denen eine Röteln-Infektion serologisch nachgewiesen wurde, zeigte Symptome einer Röteln-Erkrankung. Es ist nicht bekannt, ob Masernoder Mumps-Impfviren mit der Muttermilch ausgeschieden werden. Daher sollte sorgfältig abgewogen werden, ob M-M-RVAXPRO an stillende Mütter verabreicht wird. 4.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen Es wurden keine Studien zu den Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen durchgeführt. 4.8 Nebenwirkungen In einer klinischen Studie wurden 641 Kinder (siehe Abschnitt 5.1) mit M-M-RVAXPRO geimpft. Das allgemeine Nebenwirkungsprofil war vergleichbar mit dem Nebenwirkungsprofil von früheren Formulierungen des Masern-, Mumps- und Röteln-Impfstoffs von Merck & Co., Inc. Alle bei 634 Kindern beobachteten Nebenwirkungen wurden ausgewertet. Bei diesen Kindern wurden folgende Impfstoff-bezogenen Nebenwirkungen nach Gabe von M-M-RVAXPRO beobachtet (nicht berücksichtigt sind Einzelfälle mit einer Häufigkeit von < 0,2 %): [Sehr häufig ( 1/10); häufig ( 1/100 bis < 1/10); gelegentlich ( 1/1.000 bis < 1/100)] Infektionen und parasitäre Erkrankungen Gelegentlich: Nasopharyngitis, Infektionen der oberen Atemwege oder virale Infekte. Erkrankungen der Atemwege, des Brustraums und des Mediastinums Gelegentlich: Rhinorrhoe. Erkrankungen des Gastrointestinaltrakts Gelegentlich: Durchfall oder Erbrechen. Erkrankungen der Haut und des Unterhautzellgewebes Häufig: morbilliformes Exanthem oder anderes Exanthem. Gelegentlich: Urtikaria. Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Sehr häufig: Fieber (38,5 C oder höher), Erythem an der Injektionsstelle, Schmerz an der Injektionsstelle, Schwellung an der Injektionsstelle. Häufig: Hämatom an der Injektionsstelle. Gelegentlich: Exanthem an der Injektionsstelle. Im Vergleich zur ersten Dosis treten nach Verabreichung einer zweiten Dosis M-M-RVAXPRO klinische Symptome, einschließlich solcher, die auf allergische Reaktionen hinweisen, weder häufiger noch stärker ausgeprägt auf. 16
17 Mögliche Nebenwirkungen Weitere Nebenwirkungen wurden in klinischen Studien und nach Zulassung von früheren Formulierungen der monovalenten Masern-, Mumps- und Röteln-Impfstoffe und des MMR-Kombinationsimpfstoffs von Merck & Co., Inc. berichtet. Diese Nebenwirkungen sind ohne Berücksichtigung einer möglichen Kausalität oder der Häufigkeit ihres Auftretens im Folgenden aufgeführt. Mögliche Nebenwirkungen, über die in vorhergehenden Abschnitten bereits berichtet wurde (und die sich auf klinische Studien mit M-M-RVAXPRO beziehen), sind nicht mehr aufgeführt. Infektionen und parasitäre Erkrankungen Aseptische Meningitis (siehe unten), atypische Masern, Orchitis, Otitis media, Parotitis, Rhinitis, subakute sklerosierende Panenzephalitis (siehe unten). Über Fälle aseptischer Meningitis wurde nach Masern-Mumps-Röteln-Impfung berichtet. Ein Kausalzusammenhang zwischen anderen Stämmen des Mumps-Impfstoffs und aseptischer Meningitis konnte gezeigt werden, es gibt jedoch keinen Hinweis auf einen Zusammenhang zwischen dem im Impfstoff enthaltenen Jeryl-Lynn -Mumps-Impfstamm und aseptischer Meningitis. Erkrankungen des Blutes und des Lymphsystems Regionale Lymphadenopathie, Thrombozytopenie. Erkrankungen des Immunsystems Anaphylaktoide Reaktionen, Anaphylaxie und verwandte Symptome wie angioneurotisches Ödem, Gesichtsödem und periphere Ödeme. Psychiatrische Erkrankungen Reizbarkeit. Erkrankungen des Nervensystems Afebrile Krämpfe oder Anfälle, Ataxie, Benommenheit, Enzephalitis (siehe unten), Enzephalopathie (siehe unten), Fieberkrämpfe (bei Kindern), Guillain-Barré-Syndrom, Kopfschmerzen, Masern- Einschlusskörperchen-Enzephalitis (MIBE) (siehe Abschnitt 4.3), Augenmuskellähmungen, Optikusneuritis, Parästhesien, Polyneuritis, Polyneuropathie, Retrobulbärneuritis, Synkopen. Pro 3 Millionen verabreichter Dosen von Impfstoffen mit einer Masernkomponente, hergestellt von Merck & Co., Inc., wurde ein Fall von Enzephalitis und Enzephalopathie, ausgenommen subakute sklerosierende Panenzephalitis (SSPE), berichtet. Postmarketing-Beobachtungen mit den weltweit über einem Zeitraum von fast 25 Jahren (1978 bis 2003) mehr als 400 Millionen verkauften Dosen weisen darauf hin, dass schwerwiegende Nebenwirkungen wie Enzephalitis und Enzephalopathie auch weiterhin nur selten beobachtet werden. In keinem Fall konnte schlüssig nachgewiesen werden, dass die Nebenwirkungen tatsächlich durch die Impfung verursacht wurden; die Daten lassen jedoch vermuten, dass einige der Fälle möglicherweise durch Masern-Impfstoffe hervorgerufen worden sein könnten. Es gibt keinen Beleg dafür, dass Masern-Impfstoffe SSPE verursachen können. Es gab Berichte über SSPE bei Kindern, die sich laut Anamnese nicht mit dem Masern-Wildvirus infiziert, jedoch einen Masern-Impfstoff erhalten hatten. Einige dieser Fälle könnten auf eine unerkannte Masern-Infektion während des ersten Lebensjahres oder auch auf die Masern-Impfung zurückzuführen sein. Eine retrospektive Fall-Kontrollstudie, die von den US-amerikanischen Centers for Disease Control and Prevention durchgeführt wurde, deutet darauf hin, dass eine Masern-Impfung insgesamt gegen SSPE schützt, da die Impfung eine Masern-Erkrankung und das damit einhergehende Risiko einer SSPE verhindert. Augenerkrankungen Konjunktivitis, Retinitis. 17
18 Erkrankungen des Ohrs und des Labyrinths Retrokochläre Taubheit. Erkrankungen der Atemwege, des Brustraums und des Mediastinums Bronchospasmus, Husten, Pneumonitis (siehe Abschnitt 4.3), Halsschmerzen. Erkrankungen des Gastrointestinaltrakts Übelkeit. Erkrankungen der Haut und des Unterhautzellgewebes Panniculitis, Purpura, Verhärtung der Haut, Stevens-Johnson-Syndrom. Skelettmuskulatur-, Bindegewebs- und Knochenerkrankungen Arthritis und/oder Arthralgien (in der Regel vorübergehend und selten chronisch [siehe unten]), Myalgien. Arthralgie und/oder Arthritis (in der Regel vorübergehend und selten chronisch) sowie Polyneuritis sind charakteristisch für eine Infektion mit Röteln-Wildvirus; Häufigkeit und Schweregrad variieren in Abhängigkeit von Alter und Geschlecht und sind am ausgeprägtesten bei erwachsenen Frauen, am wenigsten ausgeprägt bei Kindern vor der Pubertät. Bei Kindern sind Gelenkbeschwerden nach einer Impfung in der Regel weniger häufig (0 3 %) und von kurzer Dauer. Bei Frauen ist die Inzidenz von Arthritis und Arthralgien in der Regel höher als bei Kindern (12 20 %); die Symptome sind tendenziell ausgeprägter und länger anhaltend und können über mehrere Monate persistieren, in seltenen Fällen sogar über Jahre. Die Häufigkeit bei weiblichen Jugendlichen scheint zwischen der bei Kindern und erwachsenen Frauen beobachteten Häufigkeit zu liegen. Diese Nebenwirkungen werden in der Regel auch von Frauen zwischen 35 und 45 Jahren gut toleriert und beinträchtigen den normalen Tagesablauf kaum. Chronische Arthritis wurde mit Röteln-Wildvirus-Infektionen in Verbindung gebracht und auf persistierende Viren und/oder virale Antigene zurückgeführt, die aus Körpergewebe isoliert wurden. Bei geimpften Personen kam es nur selten zu chronischen Gelenkbeschwerden. Allgemeine Erkrankungen und Beschwerden am Verabreichungsort Brennen und/oder Stechen von kurzer Dauer an der Injektionsstelle, Fieber (38,5 C oder höher), Unwohlsein, Papillitis, periphere Ödeme, Schwellung, Schmerzhaftigkeit, Bläschen an der Injektionsstelle, Quaddeln und Entzündungen an der Injektionsstelle. 4.9 Überdosierung Fälle von Überdosierung wurden selten berichtet und hatten keine schweren Nebenwirkungen zur Folge. 5. PHARMAKOLOGISCHE EIGENSCHAFTEN 5.1 Pharmakodynamische Eigenschaften Pharmakotherapeutische Gruppe: Viraler Impfstoff, ATC-Code: J07BD52. Bewertung der Immunogenität und klinischen Wirksamkeit Eine vergleichende klinische Studie mit Personen, die entweder mit M-M-RVAXPRO oder der früheren Formulierung des Masern-, Mumps- und Röteln-Impfstoffs von Merck & Co., Inc. (hergestellt mit humanem Serumalbumin), geimpft worden waren, zeigte eine vergleichbare Immunogenität und ein vergleichbares Nebenwirkungsprofil der beiden Produkte. Klinische Studien an 284 (dreifach) seronegativen Kindern im Alter von 11 Monaten bis 7 Jahren belegen, dass die frühere Formulierung des Masern-, Mumps- und Röteln-Impfstoffs von Merck & 18
19 Co., Inc. hoch immunogen und generell gut verträglich ist. In diesen Studien konnten nach Gabe einer Einzeldosis bei 95 % der empfänglichen Probanden Hämagglutinations-hemmenden (HI) Antikörper gegen Masern, bei 96 % neutralisierende Antikörper gegen Mumps und bei 99 % zu Röteln-HI- Antikörper gegen Röteln nachgewiesen werden. Die Wirksamkeit der Komponenten der früheren Formulierung des Masern-, Mumps- und Röteln- Impfstoffs von Merck & Co., Inc. wurde durch eine Reihe von kontrollierten Doppel-Blind- Feldstudien belegt; in diesen Studien wurde eine hohe Schutzwirkung der einzelnen Impfstoffkomponenten nachgewiesen. Diese Studien belegen außerdem, dass eine postvakzinale Serokonversion gegen Masern, Mumps und Röteln mit dem Schutz vor diesen Krankheiten korreliert. Postexpositionelle Impfung Die Impfung nach Masern-Wildvirus-Exposition kann einen gewissen Schutz bieten, wenn der Impfstoff innerhalb von 72 Stunden nach Exposition verabreicht wird. Wenn der Impfstoff einige Tage vor einer Exposition verabreicht wird, kann jedoch ein guter Schutz aufgebaut werden. Es gibt keine Daten darüber, ob eine postexpositionelle Impfung nach Mumps- oder Röteln-Wildvirus- Exposition Schutz bietet. Wirksamkeit Weltweit wurden mehr als 400 Millionen Dosen der früheren Formulierung des Masern-, Mumps- und Röteln-Impfstoffs von Merck & Co., Inc. vertrieben (1978 bis 2003). Die weit verbreitete Anwendung eines 2-Dosen-Impfschemas in den Vereinigten Staaten und in Ländern wie Finnland und Schweden führte zu einem Rückgang der Häufigkeit aller drei Erkrankungen um mehr als 99 %. Nicht schwangere Jugendliche und Erwachsene Die Impfung empfänglicher nicht schwangerer Jugendlicher und Erwachsener im gebärfähigen Alter mit Röteln-Lebendimpfstoff ist angezeigt, wenn bestimmte Vorsichtsmaßnahmen beachtet werden (siehe Abschnitte 4.4 und 4.6). Die Impfung von empfänglichen Frauen nach der Pubertät schützt gegen eine Infektion mit Röteln während der Schwangerschaft und damit vor einer Infektion des Ungeborenen mit nachfolgender Röteln-Embryopathie. Ungeimpfte Kinder über 12 Monate mit Kontakt zu empfänglichen Schwangeren sollten mit Röteln- Lebendimpfstoff geimpft werden (wie beispielsweise M-M-RVAXPRO oder monovalenter Röteln- Impfstoff), um das Expositionsrisiko für die Schwangere zu reduzieren. Möglicherweise für Mumps und Röteln empfängliche Personen M-M-RVAXPRO ist vorzugsweise auch bei Personen mit Masern-Immunität, jedoch unklarem Immunstatus gegen Mumps und Röteln, anzuwenden. Personen ohne Masern-Immunität können unabhängig von ihrem Immunstatus mit M-M-RVAXPRO gegen Mumps oder Röteln geimpft werden, wenn kein monovalenter Masern-Impfstoff zur Verfügung steht. 5.2 Pharmakokinetische Eigenschaften Daten zu pharmakokinetischen Eigenschaften sind für Impfstoffe nicht erforderlich. 5.3 Präklinische Daten zur Sicherheit Herkömmliche präklinische Studien wurden nicht durchgeführt, da keine präklinischen Effekte zu erwarten sind, die über die in anderen Abschnitten dieser Zusammenfassung der Merkmale des Arzneimittels beschriebenen Daten hinausgehen und die im Hinblick auf die klinische Sicherheit relevant sind. 6. PHARMAZEUTISCHE ANGABEN 6.1 Liste der sonstigen Bestandteile 19
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS)
 1. BEZEICHNUNG DES ARZNEIMITTELS 010432-27389 Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE
1. BEZEICHNUNG DES ARZNEIMITTELS 010432-27389 Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Lebendimpfstoff
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Lebendimpfstoff
Vi-Polysaccharid von Salmonella typhi (Ty2 Stamm)
 Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Zusammenfassung der Merkmale des Arzneimittels 1. Bezeichnung des Arzneimittels Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff 2. Qualitative und quantitative Zusammensetzung
Mumpsviren, Stamm RIT , abgeleitet vom Stamm Jeryl Lynn (lebend, attenuiert) mindestens 10 3,7 ZKID 50
 1. BEZEICHNUNG DES ARZNEIMITTELS MMR-PRIORIX - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis
1. BEZEICHNUNG DES ARZNEIMITTELS MMR-PRIORIX - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis
M-M-RVAXPRO-Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension
 M-M-RVAXPRO-Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff 2. Qualitative und quantitative Zusammensetzung Eine Dosis (0,5
M-M-RVAXPRO-Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff 2. Qualitative und quantitative Zusammensetzung Eine Dosis (0,5
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER M-M-RvaxPro Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER M-M-RvaxPro Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die
Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem Antigenhalt)
 Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
Zusammenfassung der Merkmale des Arzneimittels 1 Bezeichnung des Arzneimittels Td-IMMUN, Injektionssuspension, Einzeldosis-Fertigspritze. Diphtherie- und Tetanus-Impfstoff (adsorbiert, mit reduziertem
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender ProQuad Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff Lesen Sie
Gebrauchsinformation: Information für Anwender ProQuad Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff Lesen Sie
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert)
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Hepatyrix, Injektionssuspension Hepatitis-A- (inaktiviert) und Typhus-Polysaccharid-Impfstoff (adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A, C, Y und W 135 -Impfstoff 2.
Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt
 1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Td-RIX Injektionssuspension Diphtherie-Tetanus-Kombinationsimpfstoff (adsorbiert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels)
 1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einem Mehrdosenbehältnis Polysaccharid-Impfstoff
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
FACHINFORMATION IPV Mérieux 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 FACHINFORMATION IPV Mérieux 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
FACHINFORMATION IPV Mérieux 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Fachinformation. Internationale Einheiten, untere Vertrauensgrenze (p=0,95) der nach der Methode der Ph.Eur. ermittelten Wirksamkeit
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) 2. Qualitative und quantitative
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) 2. Qualitative und quantitative
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET
 1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 100 mg Brausetabletten
1.3.1 SPC, LABELLING AND PACKAGE LEAFLET Beschriftungsentwurf der Fachinformation Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Bronchoverde Hustenlöser 100 mg Brausetabletten
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Meningokokken-Impfstoff A + C Mérieux
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningokokken-Impfstoff A + C Mérieux Lyophilisat (Trockensubstanz) und Lösungsmittel zur Herstellung einer Injektionssuspension Lesen Sie die gesamte
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Meningokokken-Impfstoff A + C Mérieux Lyophilisat (Trockensubstanz) und Lösungsmittel zur Herstellung einer Injektionssuspension Lesen Sie die gesamte
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
Fachinformation. 32 D-Antigen²-Einheiten³. Antigenmenge im Endprodukt (Final Bulk Product), gemäß WHO (TRS 673, 1982) 3
 1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. Qualitative und quantitative Zusammensetzung 1 Impfdosis (0,5 ml) enthält: Wirkstoffe:
1. Bezeichnung des Arzneimittels Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. Qualitative und quantitative Zusammensetzung 1 Impfdosis (0,5 ml) enthält: Wirkstoffe:
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert)
 1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (1,0 ml) enthält: Hepatitis A Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 1440 Injektionssuspension Hepatitis A Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (1,0 ml) enthält: Hepatitis A Virus
Fachinformation IPV Mérieux Stand: Juli 2010
 Fachinformation IPV Mérieux Stand: Juli 2010 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE
Fachinformation IPV Mérieux Stand: Juli 2010 1. BEZEICHNUNG DES ARZNEIMITTELS IPV Mérieux Injektionssuspension in einer Fertigspritze Inaktivierter Poliomyelitis-Impfstoff 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE
Priorix Pulver in einer Durchstechflasche und Lösungsmittel in einer Fertigspritze zur Herstellung einer Injektionslösung
 1 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Priorix Pulver in einer Durchstechflasche und Lösungsmittel in einer Fertigspritze zur Herstellung einer
1 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Priorix Pulver in einer Durchstechflasche und Lösungsmittel in einer Fertigspritze zur Herstellung einer
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. RIKA-VACC Duo Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Kaninchen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. RIKA-VACC Duo Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Kaninchen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS ProQuad Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS ProQuad Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff
GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension
 GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION Eurican Lmulti Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS ProQuad Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension ProQuad Pulver und Lösungsmittel zur
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS ProQuad Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension ProQuad Pulver und Lösungsmittel zur
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften)
 F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS Influvac - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff aus inaktivierten Oberflächenantigenen)
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS Influvac - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff aus inaktivierten Oberflächenantigenen)
Influenzavirus-Oberflächenantigene (Hämagglutinin und Neuraminidase), der folgenden Stämme*:
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS BEGRIPAL Injektionssuspension in Fertigspritze Influenza-Impfstoff (Oberflächenantigen, inaktiviert) (Saison 2013/2014) 2.
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS BEGRIPAL Injektionssuspension in Fertigspritze Influenza-Impfstoff (Oberflächenantigen, inaktiviert) (Saison 2013/2014) 2.
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1 1. BEZEICHNUNG DES ARZNEIMITTELS HBVAXPRO 5 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Sanofi Pasteur MSD GmbH 1. BEZEICHNUNG DES ARZNEIMITTELS
 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis(inaktiviert)-Adsorbat-Impfstoff (reduzierter Antigengehalt) 2. QUALITATIVE UND QUANTITATIVE
1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis(inaktiviert)-Adsorbat-Impfstoff (reduzierter Antigengehalt) 2. QUALITATIVE UND QUANTITATIVE
2 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Page 1 of 8 FACHINFORMATION 1 BEZEICHNUNG DES ARZNEIMITTELS Tuberkulin PPD RT23 SSI 2 T.E./0,1 ml, Injektionslösung. Tuberkulin PPD RT23 SSI 10 T.E./0,1 ml, Injektionslösung. 2 QUALITATIVE UND QUANTITATIVE
Page 1 of 8 FACHINFORMATION 1 BEZEICHNUNG DES ARZNEIMITTELS Tuberkulin PPD RT23 SSI 2 T.E./0,1 ml, Injektionslösung. Tuberkulin PPD RT23 SSI 10 T.E./0,1 ml, Injektionslösung. 2 QUALITATIVE UND QUANTITATIVE
Fachinformation (Zusammenfassung der Merkmale des Arzneimittels)
 1 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Xanaflu Saison 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Impfstoff aus Oberflächenantigen
1 Fachinformation (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Xanaflu Saison 2016/2017 Injektionssuspension in einer Fertigspritze Influenza-Impfstoff aus Oberflächenantigen
1. BEZEICHNUNG DES ARZNEIMITTELS 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 3. DARREICHUNGSFORM 4. KLINISCHE ANGABEN
 1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 720 Kinder Injektionssuspension Hepatitis-A-Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5ml) enthält: Hepatitis-A-Virus
1. BEZEICHNUNG DES ARZNEIMITTELS Havrix 720 Kinder Injektionssuspension Hepatitis-A-Impfstoff (inaktiviert, adsorbiert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Dosis (0,5ml) enthält: Hepatitis-A-Virus
FACHINFORMATION REVAXiS
 FACHINFORMATION REVAXiS 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt)
FACHINFORMATION REVAXiS 1. BEZEICHNUNG DES ARZNEIMITTELS REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt)
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, denn sie enthält wichtige
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS)
 FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS) 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP Injektionssuspension in einer Fertigspritze Influenza Impfstoff (Spaltimpfstoff, inaktiviert).
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS) 1. BEZEICHNUNG DES ARZNEIMITTELS VAXIGRIP Injektionssuspension in einer Fertigspritze Influenza Impfstoff (Spaltimpfstoff, inaktiviert).
Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
 Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
1. NAME UND ANSCHRIFT DES PHARMAZEUTISCHEN UNTERNEHMERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS
 GEBRAUCHSINFORMATION Eurican SHPL Staupe-Adenovirose-Parvovirose-Lebendimpfstoff und Leptospirose-lmpfstoff, inaktiviert; Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde
GEBRAUCHSINFORMATION Eurican SHPL Staupe-Adenovirose-Parvovirose-Lebendimpfstoff und Leptospirose-lmpfstoff, inaktiviert; Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Hunde
GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
 GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION Purevax RCP Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
FACHINFORMATION. 4.4 Besondere Warnhinweise und Vorsichtsmaßnahmen
 FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
FACHINFORMATION Mencevax ACWY März 2014 493134PD502J 1. BEZEICHNUNG DES ARZNEIMITTELS Mencevax ACWY Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Polysaccharid-Gruppe-A,
ZUSAMMENFASSUNG DER MERKMALE DES MITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES MITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Vacoviron FS, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Rinder 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES MITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Vacoviron FS, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension, für Rinder 2. QUALITATIVE UND QUANTITATIVE
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG. Influenzavirus Oberflächenantigene (Hämagglutinin und Neuroaminidase) der folgenden Stämme*:
 1. BEZEICHNUNG DES ARZNEIMITTELS Sandovac Injektionssuspension in einer Fertigspritze Influenzaimpfstoff (Oberflächenantigene, inaktiviert) (2014/2015) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Influenzavirus
1. BEZEICHNUNG DES ARZNEIMITTELS Sandovac Injektionssuspension in einer Fertigspritze Influenzaimpfstoff (Oberflächenantigene, inaktiviert) (2014/2015) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Influenzavirus
FACHINFORMATION (ZUSAMMENFASSUNG DER MERKMALE DER ARZNEIMITTEL)
 1. BEZEICHNUNG DER ARZNEIMITTEL Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff
1. BEZEICHNUNG DER ARZNEIMITTEL Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff
GEBRAUCHSINFORMATION. Bronchi-Shield Lyophilisat und Lösungsmittel zur Herstellung einer Suspension zur intranasalen Applikation für Hunde
 GEBRAUCHSINFORMATION Bronchi-Shield Lyophilisat und Lösungsmittel zur Herstellung einer Suspension zur intranasalen Applikation für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH,
GEBRAUCHSINFORMATION Bronchi-Shield Lyophilisat und Lösungsmittel zur Herstellung einer Suspension zur intranasalen Applikation für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH,
1 Impfdosis (0,5 ml) enthält: inaktivierte Influenza-Virus Spaltantigene* der folgenden Stämme:
 Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
Zusammenfassung der Merkmale des Arzneimittels 1. BEZEICHNUNG DES ARZNEIMITTELS Fluarix Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE
GEBRAUCHSINFORMATION Purevax RCPCh Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
 GEBRAUCHSINFORMATION Purevax RCPCh Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION Purevax RCPCh Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION Eurican SHPPi2LT Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Hunde
 GEBRAUCHSINFORMATION Eurican SHPPi2LT Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
GEBRAUCHSINFORMATION Eurican SHPPi2LT Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Hunde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
GEBRAUCHSINFORMATION. VERSIFEL CVR, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Katzen
 GEBRAUCHSINFORMATION VERSIFEL CVR, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Katzen 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
GEBRAUCHSINFORMATION VERSIFEL CVR, Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Katzen 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS,
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften)
 F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS FluVaccinol Subunit Impfstoff - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff
F A C H I N F O R M A T I O N (Zusammenfassung der Produkteigenschaften) 1. BEZEICHNUNG DES ARZNEIMITTELS FluVaccinol Subunit Impfstoff - Injektionssuspension in einer Fertigspritze (Influenza-Impfstoff
GEBRAUCHSINFORMATION Bovalto Respi 3 Injektionssuspension für Rinder
 GEBRAUCHSINFORMATION Bovalto Respi 3 Injektionssuspension für Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
GEBRAUCHSINFORMATION Bovalto Respi 3 Injektionssuspension für Rinder 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt
 1. BEZEICHNUNG DES ARZNEIMITTELS Td-pur Injektionssuspension in Fertigspritze Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS Td-pur Injektionssuspension in Fertigspritze Tetanus und Diphtherie-Adsorbat-Impfstoff (inaktiviert) mit reduziertem Antigengehalt 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Gallivac IB88, gefriergetrocknet, zur Verabreichung als Spray nach Auflösung, für Hühner
 1. BEZEICHNUNG DES TIERARZNEIMITTELS Gallivac IB88, gefriergetrocknet, zur Verabreichung als Spray nach Auflösung, für Hühner 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Impfdosis enthält: Arzneilich
1. BEZEICHNUNG DES TIERARZNEIMITTELS Gallivac IB88, gefriergetrocknet, zur Verabreichung als Spray nach Auflösung, für Hühner 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG Jede Impfdosis enthält: Arzneilich
Gebrauchsinformation: Information für Anwender. Inaktivierter Poliomyelitis-Impfstoff
 Gebrauchsinformation: Information für Anwender IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Gebrauchsinformation: Information für Anwender IMOVAX POLIO Injektionssuspension Inaktivierter Poliomyelitis-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit der Anwendung
Sonstige Bestandteile: Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP 2013/2014 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml)
1. BEZEICHNUNG DES ARZNEIMITTELS MUTAGRIP 2013/2014 Injektionssuspension in einer Fertigspritze Influenza-Spaltimpfstoff (inaktiviert) 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Impfdosis (0,5 ml)
Gebrauchsinformation: Information für Anwender. Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff
 Gebrauchsinformation: Information für Anwender Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Für Kinder ab 2 Jahren und Erwachsene Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender Typhim Vi 25 Mikrogramm Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Für Kinder ab 2 Jahren und Erwachsene Lesen Sie die gesamte
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels)
 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Epaxal - Suspension zur Injektion in einer Fertigspritze Hepatitis A-Impfstoff (inaktiviert, virosomal)
FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Epaxal - Suspension zur Injektion in einer Fertigspritze Hepatitis A-Impfstoff (inaktiviert, virosomal)
 FACHINFORMATION Bezeichnung des Arzneimittels KEYTRUDA 50 mg Pulver für ein Konzentrat zur Herstellung einer Infusionslösung Qualitative und Quantitative Zusammensetzung Eine Durchstechflasche mit Pulver
FACHINFORMATION Bezeichnung des Arzneimittels KEYTRUDA 50 mg Pulver für ein Konzentrat zur Herstellung einer Infusionslösung Qualitative und Quantitative Zusammensetzung Eine Durchstechflasche mit Pulver
GEBRAUCHSINFORMATION FÜR. Eurican LR Injektionssuspension
 PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION FÜR Eurican LR Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
PACKUNGSBEILAGE 1 GEBRAUCHSINFORMATION FÜR Eurican LR Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH
FACHINFORMATION. 1 Hartkapsel enthält: 6 mg lysierte immunaktive Fraktionen aus ausgewählten Escherichia-coli-Stämmen.
 FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
FACHINFORMATION 1. BEZEICHNUNG DES ARZNEIMITTELS Uro-Vaxom 6 mg Hartkapseln Wirkstoff: E. coli-fraktionen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 1 Hartkapsel enthält: 6 mg lysierte immunaktive
Gebrauchsinformation
 Gebrauchsinformation Virbagen canis SHAPPi/LT Kombinationsimpfstoff gegen Staupe, Hepatitis, Parvovirose, Parainfluenza, Leptospirose und Tollwut: Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssupension
Gebrauchsinformation Virbagen canis SHAPPi/LT Kombinationsimpfstoff gegen Staupe, Hepatitis, Parvovirose, Parainfluenza, Leptospirose und Tollwut: Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssupension
Priorix Pulver und Lösungsmittel zur Herstellung einer Injektionslösung
 1 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Priorix Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff
1 FACHINFORMATION (Zusammenfassung der Merkmale des Arzneimittels) 1. BEZEICHNUNG DES ARZNEIMITTELS Priorix Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Masern-Mumps-Röteln-Lebendimpfstoff
GEBRAUCHSINFORMATION Vacoviron FS Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
 GEBRAUCHSINFORMATION Vacoviron FS Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
GEBRAUCHSINFORMATION Vacoviron FS Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR
Sonstige Bestandteile: Die vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
 1. BEZEICHNUNG DES ARZNEIMITTELS Masern-Impfstoff Mérieux Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
1. BEZEICHNUNG DES ARZNEIMITTELS Masern-Impfstoff Mérieux Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Priorix-Tetra Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze
 1. BEZEICHNUNG DES ARZNEIMITTELS Priorix-Tetra Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE
1. BEZEICHNUNG DES ARZNEIMITTELS Priorix-Tetra Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Masern-Mumps-Röteln-Varizellen-Lebendimpfstoff 2. QUALITATIVE UND QUANTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 2. QUALTITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Primucell FIP ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Primucell FIP, Lyophilisat und Lösungsmittel zur Herstellung einer intranasalen Suspension für Katzen
Primucell FIP ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Primucell FIP, Lyophilisat und Lösungsmittel zur Herstellung einer intranasalen Suspension für Katzen
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Primucell FIP, Lyophilisat und Lösungsmittel zur Herstellung einer intranasalen Suspension für Katzen 2. QUALTITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Primucell FIP, Lyophilisat und Lösungsmittel zur Herstellung einer intranasalen Suspension für Katzen 2. QUALTITATIVE
GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde
 GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION ProteqFlu Injektionssuspension für Pferde 1. NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST Zulassungsinhaber:
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. Fovepta 200 I.E. Injektionslösung in einer Fertigspritze Hepatitis-B-Immunglobulin vom Menschen
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Fovepta 200 I.E. Injektionslösung in einer Fertigspritze Hepatitis-B-Immunglobulin vom Menschen Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Fovepta 200 I.E. Injektionslösung in einer Fertigspritze Hepatitis-B-Immunglobulin vom Menschen Lesen Sie die gesamte Packungsbeilage sorgfältig durch,
ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS
 [Version 7.3.2, 10/2011] ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Theranekron D6 Injektionslösung für Tiere 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
[Version 7.3.2, 10/2011] ANHANG I ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1 1. BEZEICHNUNG DES TIERARZNEIMITTELS Theranekron D6 Injektionslösung für Tiere 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS. Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension für Rinder
 Rispoval Pasteurella ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Rispoval Pasteurella Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
Rispoval Pasteurella ZUSAMMENFASSUNG DER MERKMALE DES TIERARZNEIMITTELS 1. BEZEICHNUNG DES TIERARZNEIMITTELS Rispoval Pasteurella Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
Gebrauchsinformation: Information für Anwender. HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
Gebrauchsinformation: Information für Anwender HBVAXPRO 5 Mikrogramm, Injektionssuspension in einer Fertigspritze Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS: FLUAD, Injektionssuspension in einer Fertigspritze Influenza-Impfstoff, Oberflächenantigene, inaktiviert, mit MF59C.1 als
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS: FLUAD, Injektionssuspension in einer Fertigspritze Influenza-Impfstoff, Oberflächenantigene, inaktiviert, mit MF59C.1 als
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER. TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung. Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die Packungsbeilage sorgfältig durch, bevor Sie oder Ihr Kind
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER TYPHIM Vi, 25 Microgramm/ dosis, Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die Packungsbeilage sorgfältig durch, bevor Sie oder Ihr Kind
1. NAME UND ANSCHRIFT DES PHARMAZEUTISCHEN UNTERNEHMERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS
 GEBRAUCHSINFORMATION Eurican SHPLT Staupe-Adenovirose-Parvovirose-Lebendimpfstoff und Leptospirose-Tollwutlmpfstoff, inaktiviert; Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
GEBRAUCHSINFORMATION Eurican SHPLT Staupe-Adenovirose-Parvovirose-Lebendimpfstoff und Leptospirose-Tollwutlmpfstoff, inaktiviert; Lyophilisat und Lösungsmittel zur Herstellung einer Injektionssuspension
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für Kinder
Gebrauchsinformation: Information für Anwender REVAXiS Injektionssuspension in einer Fertigspritze Tetanus-Diphtherie-Poliomyelitis (inaktiviert)-adsorbat-impfstoff (reduzierter Antigengehalt) Für Kinder
1. Was ist TdaP-IMMUN und wofür wird es angewendet?
 Page 1 of 6 Gebrauchsinformation: Information für Anwender TdaP-IMMUN Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis- (azelluläre Komponente) Impfstoff (adsorbiert, reduzierter
Page 1 of 6 Gebrauchsinformation: Information für Anwender TdaP-IMMUN Injektionssuspension in einer Fertigspritze Diphtherie-, Tetanus- und Pertussis- (azelluläre Komponente) Impfstoff (adsorbiert, reduzierter
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Td-Impfstoff Mérieux Injektionssuspension Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Für Kinder ab 5 Jahren und Erwachsene Lesen Sie
Gebrauchsinformation: Information für Anwender Td-Impfstoff Mérieux Injektionssuspension Diphtherie-Tetanus-Adsorbat-Impfstoff (reduzierter Antigengehalt) Für Kinder ab 5 Jahren und Erwachsene Lesen Sie
Gebrauchsinformation: Information für Anwender. Typhim Vi Injektionslösung in einer Fertigspritze. Typhus-Polysaccharid-Impfstoff
 Gebrauchsinformation: Information für Anwender Typhim Vi Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr
Gebrauchsinformation: Information für Anwender Typhim Vi Injektionslösung in einer Fertigspritze Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie bzw. Ihr
Gebrauchsinformation: Information für Anwender. HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns)
 Gebrauchsinformation: Information für Anwender HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem Impfstoff
Gebrauchsinformation: Information für Anwender HBVAXPRO 40 Mikrogramm, Injektionssuspension Hepatitis B-Impfstoff (rdns) Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem Impfstoff
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS AFLUBIN- Grippetropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 ml enthalten: 1 ml Gentiana lutea D1, 10 ml Aconitum
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS AFLUBIN- Grippetropfen 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG 100 ml enthalten: 1 ml Gentiana lutea D1, 10 ml Aconitum
Tetravac. 1. Bezeichnung des Arzneimittels. 2. Qualitative und quantitative Zusammensetzung. 3. Darreichungsform
 1. Bezeichnung des Arzneimittels, Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis (inaktiviert)-adsorbat-impfstoff 2. Qualitative und quantitative Zusammensetzung
1. Bezeichnung des Arzneimittels, Injektionssuspension in einer Fertigspritze Diphtherie-Tetanus-Pertussis (azellulär)-poliomyelitis (inaktiviert)-adsorbat-impfstoff 2. Qualitative und quantitative Zusammensetzung
Fachinformation 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
 Seite 1 von 7 PIERRE FABRE PHARMA Fachinformation RIBOMUNYL uno Tabletten, Granulat 1. BEZEICHNUNG DER ARZNEIMITTEL Ribomunyl uno Tabletten Ribomunyl uno Granulat 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Seite 1 von 7 PIERRE FABRE PHARMA Fachinformation RIBOMUNYL uno Tabletten, Granulat 1. BEZEICHNUNG DER ARZNEIMITTEL Ribomunyl uno Tabletten Ribomunyl uno Granulat 2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Boehringer Ingelheim Vetmedica GmbH
 PACKUNGSBEILAGE FÜR Insol Dermatophyton, Injektionssuspension für Pferde, Hunde und Katzen 1. NAME/FIRMA UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
PACKUNGSBEILAGE FÜR Insol Dermatophyton, Injektionssuspension für Pferde, Hunde und Katzen 1. NAME/FIRMA UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH, DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE
Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff
 GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
GEBRAUCHSINFORMATION: INFORMATION FÜR DEN ANWENDER Typherix 25 Mikrogramm/0,5 ml Injektionslösung Typhus-Polysaccharid-Impfstoff Lesen Sie die gesamte Packungsbeilage sorgfältig durch, bevor Sie mit diesem
Gebrauchsinformation: Information für Patienten und Anwender
 Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
Gebrauchsinformation: Information für Patienten und Anwender Nimenrix - Pulver und Lösungsmittel zur Herstellung einer Injektionslösung in einer Fertigspritze Meningokokken-Gruppen A, C, W-135 und Y-Konjugatimpfstoff
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER STAMARIL Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Gelbfieber-Lebendimpfstoff Für Säuglinge ab 6 Monaten,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER STAMARIL Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Gelbfieber-Lebendimpfstoff Für Säuglinge ab 6 Monaten,
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER
 GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Act-HIB 10 Mikrogramm/0,5 ml, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Konjugatimpfstoff gegen Haemophilus influenzae Typ b Lesen Sie
GEBRAUCHSINFORMATION: INFORMATION FÜR ANWENDER Act-HIB 10 Mikrogramm/0,5 ml, Pulver und Lösungsmittel zur Herstellung einer Injektionslösung Konjugatimpfstoff gegen Haemophilus influenzae Typ b Lesen Sie
Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert)
 ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. QUALITATIVE
ZUSAMMENFASSUNG DER MERKMALE DES ARZNEIMITTELS 1. BEZEICHNUNG DES ARZNEIMITTELS Twinrix Kinder, Injektionssuspension Hepatitis-A (inaktiviert)- und Hepatitis-B (rdna) (HAB)-Impfstoff (adsorbiert) 2. QUALITATIVE
Gebrauchsinformation für
 Gebrauchsinformation für Virbagen canis SHAPPi/LT Kombinationsimpfstoff gegen Staupe, Hepatitis, Parvovirose, Parainfluenza, Leptospirose und Tollwut: Lyophilisat und Lösungsmittel zur Herstellung einer
Gebrauchsinformation für Virbagen canis SHAPPi/LT Kombinationsimpfstoff gegen Staupe, Hepatitis, Parvovirose, Parainfluenza, Leptospirose und Tollwut: Lyophilisat und Lösungsmittel zur Herstellung einer
EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG
 EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG M-M-RvaxPro Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Lebendimpfstoff BITTE BEANTWORTEN SIE DIE NACHSTEHENDEN FRAGEN:
EINVERSTÄNDISERKLÄRUNG ZUR SCHUTZIMPFUNG M-M-RvaxPro Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension Masern-Mumps-Röteln-Lebendimpfstoff BITTE BEANTWORTEN SIE DIE NACHSTEHENDEN FRAGEN:
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender M-M-RVAXPRO Pulver und Lösungsmittel zur Herstellung einer Injektionssuspension in einer Fertigspritze Masern-Mumps-Röteln-Lebendimpfstoff Lesen Sie die gesamte
Gebrauchsinformation: Information für Anwender
 Gebrauchsinformation: Information für Anwender Tetanus-Impfstoff Mérieux, mind. 40 I.E. Injektionssuspension in einer Fertigspritze Injektionssuspension Tetanus-Adsorbat-Impfstoff Für Säuglinge, Kinder
Gebrauchsinformation: Information für Anwender Tetanus-Impfstoff Mérieux, mind. 40 I.E. Injektionssuspension in einer Fertigspritze Injektionssuspension Tetanus-Adsorbat-Impfstoff Für Säuglinge, Kinder
