1. Steckbrief. 2. Wasser - Molekül. 3. Wasser ein Dipol. Wasser Wasser info
|
|
|
- Axel Lorentz
- vor 5 Jahren
- Abrufe
Transkript
1 1. Steckbrief Wasser (H 2O) ist eine chemische Verbindung aus den Elementen Sauerstoff (O) und Wasserstoff (H). Wasser ist als Flüssigkeit durchsichtig, weitgehend farb-, geruch- und geschmacklos. Wasser ist die einzige chemische Verbindung auf der Erde, die in der Natur als Flüssigkeit, als Festkörper und als Gas vorkommt. Die Bezeichnung Wasser wird dabei für den flüssigen Aggregatzustand verwendet. Im festen Zustand spricht man von Eis, im gasförmigen Zustand von Wasserdampf. Wasser ist Grundlage des Lebens auf der Erde. 2. Wasser - Molekül Ein Wassermolekül besteht aus einem Sauerstoffatom und zwei Wasserstoffatomen. Die zwei Wasserstoffatome sind am Sauerstoffatom gebunden und schließen einen Winkel von ungefähr 104,5 ein. Beim Wassermolekül handelt es sich um eine Elektronenpaarbindung. 3. Wasser ein Dipol Das Maß für die Kraft, die Elektronen der Elektronenpaarbindung an sich zu ziehen, bezeichnet man als Elektronegativität (EN = Maß dafür, wie stark ein Atom gemeinsame Bindungselektronen anzieht). Unterschiedliche Atome weisen einen unterschiedlichen Elektronegativitätswert auf. Das Element mit der höchsten Elektronegativität ist Fluor (EN =4). Sauerstoff hat eine Elektronegativität von 3,5 und Wasserstoff von 2,1. Das wiederum hat Auswirkungen, wenn sich Atome zu einem Molekül zusammenfinden, wie das bei Wasser der Fall ist. Im Wassermolekül hat Sauerstoff also eine größere Elektronegativität als Wasserstoff und zieht damit die Elektronen der beiden Elektronenpaarbindungen an sich auf seine Seite. Somit ergibt sich für das Sauerstoffatom eine negative Teilladung (bezeichnet mit dem altgriechischen Buchstaben delta ; δ-). Die Wasserstoffatome hingegen erhalten eine positive Teilladung (δ+). Aus der gewinkelten Struktur und den unterschiedlichen Elektronegativitätswerten von Sauerstoff und Wasserstoff ergibt sich ein negativer Ladungsschwerpunkt auf der Seite des Sauerstoffs und ein positiver Ladungsschwerpunkt auf der anderen Seite des Wassermoleküls beim Wasserstoff. 1
2 Die Polarität des Wassers kann man durch einen einfachen Versuch nachweisen: man hält einen statisch aufgeladenen Gegenstand neben einen dünnen Wasserstrahl. Dabei kann man beobachten, dass die positive Teilladung der Wasserteilchen vom negativ geladenen Gegenstand angezogen wird. 4. Wassercluster durch Wasserstoffbrückenbindung Cluster Da die Wassermoleküle Dipole sind, also an verschiedenen Enden unterschiedlich geladen. Das eine Ende ist positiv geladen, das andere negativ, ordnen sich die einzelnen Wassermoleküle zu größeren Haufen oder Klumpen englisch Cluster zusammen. Wasserstoffbrückenbindung Aufgrund dieser Ladungsverteilung in dem Wassermolekül können die einzelnen Moleküle untereinander wechselwirken. Wie bei einem Magneten stoßen sich gleiche Ladungszustände ab und unterschiedliche ziehen sich an. Das führt dazu, dass sich zwischen den einzelnen Wassermolekülen starke zwischenmolekulare Bindungen, sogenannte Wasserstoffbrücken ausbilden können. Wie in der Abbildung zu erkennen ist, bilden sich die Wasserstoffbrückenbindungen immer zwischen den Sauerstoffatomen und den Wasserstoffatomen zweier verschiedener Wassermoleküle aus. Dabei bildet das Sauerstoffatom bis zu zwei Wasserstoffbrücken aus und jedes Wasserstoffatom ist in der Lage eine Wasserstoffbrücke zu einem Sauerstoff auszubilden. Moleküle, die in der Lage sind Wasserstoffbrücken auszubilden, nennt man permanente Dipole. 2
3 5. Aggregatzustände oder Phasen1 Das Wort Aggregatzustand bezeichnet den physikalischen Zustand eines Stoffes. Es gibt drei klassische Aggregatzustände: Fest, flüssig und gasförmig. Welcher Aggregatzustand vorliegt, hängt von den Eigenheiten des Stoffes, der Temperatur und dem Umgebungsdruck ab. Prinzipiell kann man sagen, dass Stoffe im Aggregatzustand "fest" die größte Dichte besitzen, welche etwa 5-10 Prozent höher als die der jeweiligen Flüssigkeit ist. Wirkt keine äußere Kraft auf den Stoff ein, behält er seine Form bei. Im flüssigen Zustand hingegen, passt sich der Stoff in seiner Form der Umgebung an und fließt immer zum tiefsten Punkt. Dies gilt auch in der Natur: Flüsse fließen stets den Berg runter. Nach fest und flüssig fehlt nun noch der Aggregatzustand "gasförmig". Erhitzt man eine Flüssigkeit sehr stark, wird sie irgendwann verdampfen, sprich sie "geht in die Luft über". Als Gas weisen die Stoffe die niedrigste Dichte auf. Diese ist bis zu tausendmal kleiner als die der Feststoffe. Aus diesem Grund kann man gasförmige Stoffe auch sehr stark komprimieren. In diesem Aggregatzustand besitzt der Stoff keine feste Oberfläche. Deshalb sind farblose Gase unsichtbar. 6. Aggregatzustände und Phasenänderungen Wasser Auf der Erde kommt Wasser in seinen verschiedenen Aggregatzuständen vor: als Festkörper (Eis), als Flüssigkeit (Wasser) und als Gas (Wasserdampf). Die Sonne verdunstet das Wasser zu Wasserdampf, als Regen kommt es wieder auf die Erde zurück. Bei niedrigen Temperaturen im Winter gefriert das Wasser zu Eis. Unter den chemischen Normalbedingungen ist Wasser flüssig, unter 0 C (Gefrierpunkt) gefriert das Wasser und geht in den festen Zustand (Eis) über. Wenn die Temperatur auf über 100 C (Verdampfungspunkt) erwärmt wird, geht das Wasser in den gasförmigen Zustand über (verdampft). Die Verdampfungsgeschwindigkeit hängt dabei von der Temperatur ab. Je höher diese ist, desto schneller verdampft das Wasser
4 7. Dichteanomalie des Wassers Die bekannteste der ungewöhnlichen Eigenschaften des Wassers ist vermutlich die so genannte Dichteanomalie: Sie beschreibt das Phänomen, dass Wasser bei 3,89 C die höchste Dichte (1g/cm³ bei Normdruck) besitzt. Im festen Aggregatzustand (Eis) wird normalerweise eine hohe Ordnung, meist in Form eines Kristallgitters, erreicht. Im flüssigen Zustand herrscht ein instabiler Zustand und die Moleküle brauchen durch ihre höhere Geschwindigkeit mehr Platz. Darum erhöht sich das Volumen und die Dichte wird geringer. Im gasförmigen Zustand ist die maximale Unordnung erreicht und die Atome brauchen maximalen Raum für die Bewegung. Diese Anomalie des Wassers entsteht durch den Bindungswinkel zwischen den einzelnen Atomen des Wassermoleküls. Wasser ist ein Dipol und darum ordnen sich die Wasserstoffatome mit den Sauerstoffatomen über Wasserstoffbrückenbindungen an. Dadurch ist die Struktur im festen Zustand größer als bei beweglichen Molekülen. Dies ist ein fortschreitender Vorgang, d.h. dass schon im flüssigen Zustand so genannte Cluster aus Wassermolekülen vorhanden sind. Bei 3,98 C ist der Zustand erreicht, bei dem die einzelnen Cluster das geringste Volumen einnehmen und damit die größte Dichte haben. Wenn die Temperatur weiter sinkt, wird durch die weiteren Kristallstrukturen mehr Volumen benötigt. Wenn die Temperatur steigt, benötigen die Moleküle wieder mehr Bewegungsfreiraum, und das Volumen steigt auch. Zufrieren von Wasserflächen Die Wasseranomalie ist wichtig für das Leben in Gewässern kalter Klimazonen, denn sie hat zur Folge, dass Seen und Flüsse bei Temperaturen unter Null von oben zufrieren. Die entstehende Eisschicht ist ein schlechterer Wärmeleiter als flüssiges Wasser und wirkt isolierend, so dass das Wasser darunter weniger schnell abkühlt. Außerdem sorgt die Wasseranomalie für eine bessere Durchmischung tieferliegender Wasserschichten mit gelösten Gasen und Nährstoffen. Die Wassertemperatur unter dem Eis steigt mit zunehmender Tiefe des Wassers. Am Grund des Sees sind es immer 4 Grad Celsius, wodurch das Wasser mit der höchsten Dichte, also das schwerste Wasser sich immer ganz unten befindet, was wiederum das Überleben der Wasserorganismen im Winter erleichtert. 4
5 Eisberge Obwohl Eisberge im Meer treiben, bestehen sie nicht aus gefrorenem Meerwasser, sondern aus Süßwasser. Denn sie stammen von den riesigen Gletschern der Polargebiete. An deren Rändern brechen regelmäßig und leider zunehmend große Stücke von ihnen ab die Eisberge. Man spricht auch davon, dass der Gletscher kalbt. Da Eis leichter ist als Wasser, treibt es im Meer umher, ohne unterzugehen. Da die Polarmeere sind zwischen 4 und 0 Grad Celsius kalt sind, tauen die Eisberge nur sehr langsam ab und werden.jahrzehnte alt. 5
6 8. Wasser als Lösungsmittel Der Dipolcharakter des Wassermoleküls ist der Grund der guten Lösungseigenschaften des Wassers. Für viele Substanzen ist Wasser ein ausgezeichnetes Lösungsmittel. Vor allem für ionische Verbindungen wie Salze bietet sich Wasser als Lösemittel an. Salze: bilden sich durch Ionenbindung. Im festen Salz ordnen sich die positiven und negativen Ionen abwechselnd an, sodass sich ein dreidimensionales Gitter ergibt das Ionengitter. Kochsalz (= Natriumchlorid) besteht aus positiv geladenen Natrium-Ionen und einem negativ geladenen Chlorid-Ion. Diese ziehen sich gegenseitig an.(ionenbindung: Metall+Nichtmetall) Lösungsvorgang Beim Lösevorgang werden die kleinsten Teilchen (Ionen oder Moleküle) aus dem Gitterverband des Feststoffs gelöst. Das Lösen einer Verbindung erfordert Energie, welche dem Wasser in Form von Wärme entzogen wird. Beim Lösen eines Feststoffs in Wasser finden somit zwei Vorgänge gleichzeitig statt: der endotherme Gitterabbau und die exotherme Hydratation. Erfordert der Gitterabbau mehr Energie als bei der Hydratation der Teilchen frei wird, so kühlt sich das Wasser ab. Im anderen Fall wird sich das Wasser erwärmen. Lösungsvorgang von Salz im Wasser: In Wasser lösen sich vor allem Salze gut, die durch elektrostatische Wechselwirkungen der Ionen zusammengehalten werden. Die aus einem Ionenverband gelösten Teilchen treten mit den entgegengesetzt geladenen Enden der Wasserdipole in Wechselwirkung. Die gelösten Ionen werden mit mehreren Wassermolekülen umlagert, wobei Energie frei wird. Man bezeichnet den Vorgang auch als Hydratation und die freigesetzte Energie als Hydratationsenergie. 6
7 Die Ionen lösen sich aus ihrer Gitterstruktur und sind im Wasser frei beweglich. Die Wassermoleküle umlagern das positive Natrium-Ion so, dass das schwach negativ geladene Sauerstoffatom zum positiven Natrium-Ion zeigt. Das negative Chlorid-Ion hingegen wird von den Wassersmolekülen so umlagert, dass die schwach positiv geladenen Wasserstoffatome zu ihm zeigen. Die Anlagerung der Wassermoleküle an gelöste Ionen nennt man Hydratation. Die nun von den Wassermolekülen umschlossenen Ionen lösen sich im Wasser auf. Wasserlösliche Stoffe werden als hydrophil, wasserunlösliche (wie Fette/Öle) als hydrophob bezeichnet. Die Lösungseigenschaften des Wassers sind stoffspezifisch. Es gibt Substanzen die sich bei Raumtemperatur gut, mäßig oder kaum lösen lassen. Eine wässrige Lösung in der kein weiterer Feststoff gelöst werden kann wird als gesättigt bezeichnet. Ein Überschuss eines Feststoffs wird sich als Bodensatz abscheiden. In den meisten Fällen nimmt die Löslichkeit einer Substanz mit steigender Temperatur zu. Die Löslichkeit wird in Gramm pro 100g Lösemittel angegeben. 9. Kohäsion Adhäsion Kapillarwirkung und Oberflächenspannung2 Allgemeines zu Kräften in Flüssigkeitstropfen: im Inneren der Flüssigkeit bleiben die Moleküle aufgrund der Kohäsionskräfte nahe beisammen Kräfte in alle Richtungen heben sich auf: Kräftegleichgewicht an der Oberfläche der Flüssigkeit bleibt eine resultierende Kraft! Moleküle an der Oberfläche spüren Kraft, die nach innen gerichtet ist: Oberfläche krümmt sich, nähert sich Halbkugelform an Adhäsion / Adhäsionskraft um Moleküle an die Oberfläche zu befördern, muss Arbeit gegen diese gegen diese Kraft geleistet werden geleistet werden e näher an Oberfläche, desto größer die Arbeit Arbeit erhöht die Oberflächenenergie Kohäsionskräfte van der Waals-Wechselwirkungen, Dispersionskräfte (London sche Kräfte), Wasserstoffbrückenbindungen, bei Elektrolytlösungen: ionische Kräfte (Coulomb-Kräfte) Kohäsion: Zwischen den Teilchen einer Flüssigkeit wirken Anziehungskräfte. Im Inneren wird ein Teilchen von seinen Nachbarn nach allen Seiten gezogen. Diese Kräfte heben sich deshalb gegenseitig auf. Ein Teilchen, das sich an der Oberfläche befindet, hat über sich keine Nachbarn, die nach oben ziehen können. Es wird deshalb in die Flüssigkeit hineingezogen. Wir nennen diese Erscheinung Kohäsion. Sie ist auch für die Tropfenbildung 2 7
8 verantwortlich. Jedes Teilchen an der Oberfläche erfährt Anziehungskräfte von den unmittelbar benachbarten Oberflächenmolekülen. Dies bewirkt die Oberflächenspannung. Adhäsion: Körper, die aus dem Wasser gezogen werden sind nass, an ihnen haftet Wasser. Das Wasser wird von dem Körper angezogen. Diese Erscheinung heißt Adhäsion. Werden zwei feuchte Glasplatten aneinander gedrückt, lassen sie sich nur sehr schwer auf Grund der Adhäsion auseinanderziehen. Praktische Beispiele dafür sind: -Wetex, Schwamm(tuch, Löschpapier, Würfelzucker, Leitungsbahnen der Pflanzen, feine Blutgefäße (Kapillare) Wird Wasser auf eine Glasplatte gesprüht, bleibt das Wasser aufgrund der Adhäsion an der Glasscheibe haften. Die Kohäsion bewirkt die Tropfenbildung werden die Tropfen zu groß, übersteigt die Gewichtskraft die Adhäsionskraft und die Tropfen fließen runter. Lotoseffekt Oberfläche rauh Tropfen kullert über die raue Fläche und nimmt den Schmutz mit Lotuseffekt eigenes script 8
9 Wasserfilm zwischen 2 Glasplatten Kohäsion zwischen den Wassermolekülen Adhäsion zwischen den Wassermolekülen und der Glasplatte Kapillarwirkung: In engen Röhren steht das Wasser höher als in weiten. Am Rand der Röhren wird das Wasser durch Adhäsion hochgezogen. Die Oberflächenspannung ist ein Effekt, der dazu führt, dass sich die Oberfläche einer Flüssigkeit wie eine elastische Folie verhält und einen möglichst glatten Zustand minimaler Ausdehnung anstrebt. Die Kohäsion der Wasserteilchen an der Oberfläche ist nur nach innen gerichtet. Wassertropfen nehmen daher eine kugelige Gestalt an. Bei der Kohäsion handelt es sich um Bindungskräfte zwischen Molekülen. Im Inneren einer Phase, in diesem Fall Wasser, wirken die Bindungskräfte gleichmäßig nach allen Seiten. Die resultierende Kraft ist gleich Null. Wie im Bild dargestellt, fehlen an der Grenzfläche zu einer anderen Phase, in diesem Fall Luft, die benachbarten Moleküle. Dies führt dazu, Oberflächenspannung spezial eigenes script 9
10 dass die Bindungskräfte der Moleküle an der Grenzfläche verstärkt auf ihre direkten Nachbarn wirken. Daraus resultiert eine Kraft (F), die in das Innere des Mediums gerichtet ist. 10. Spezifische.Wärmekapazität des Wassers Sie ist weitere Besonderheit des Wassers. Um die Temperatur eines Körpers zu erhöhen, muss seine innere Energie vergrößert werden. Verschiedene Stoffe lassen sich unterschiedlich leicht erwärmen. Um verschiedene Stoffe bezüglich ihrer "Erwärmbarkeit" vergleichen zu können, untersucht man 1 kg eines Stoffes und bestimmt die Energiemenge die benötigt wird um diesen Stoff um 1 C zu erwärmen Die Tabelle zeigt, dass Wasser einen vergleichsweise sehr hohen Wert hat. Diese Eigenschaft ist entscheidend für das Klima der Erde. Klimaregulator Die Wärmekapazität von Wasser ist für das Klima auf unserer Erde von höchster Bedeutung. Das Wasser der Ozeane kann riesige Energiemengen (die von der Sonne eingestrahlt werden) speichern, ohne dass sich seine Temperatur stark ändert. Dadurch schwankt die Temperatur der Luft in geringen Grenzen. Durch den Golfstrom fließen große Wassermassen, die im Golf von Mexiko erwärmt worden sind, nach Europa und sorgen durch die damit zu uns transportierten Energiemengen bei uns für ein gemäßigtes Klima. In Form von Wasserdampf hat H 2O ebenfalls einen entscheidenden Einfluss auf den Wärmehaushalt der Erde: Wasserdampf allein trägt zu etwa zwei Dritteln zum natürlichen Treibhauseffekt bei. Er verstärkt die Klimawirkung anderer Stoffe. Steigt zum Beispiel die Temperatur infolge eines höheren Kohlendioxidgehalts, so steigt auch der Gehalt an Wasserdampf, da eine wärmere Atmosphäre dauerhaft mehr Wasserdampf speichern kann. Wasser kühlt nur langsam ab, weil sich immer mehr Wasserstoffbrücken bilden. Umgekehrt geht auch das Erwärmen langsam. 10
11 Diese Eigenschaft unterstützt einen Temperaturausgleich mit der Umgebung. Hierdurch herrscht an den Küsten ein ausgeglichenes Klima. 11
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kinetische Energie der Moleküle / Aggregatzustand Bau und Struktur der Moleküle Intermolekulare Anziehungskräfte Kräfte zwischen Molekülen Van-der-Waals-Kräfte
Vom Atom zum Molekül
 Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Vom Atom zum Molekül Ionenverbindungen Na + Cl NaCl lebensgefährlich giftig lebensgefährlich giftig lebensessentiell Metall + Nichtmetall Salz Beispiel Natriumchlorid Elektronenkonfiguration: 11Na: 1s(2)
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Biologie Arbeitsblätter mit Lösungen - Biochemie Das komplette Material finden Sie hier: Download bei School-Scout.de B201 LÖSUNG:
Materialien für den sprachsensiblen Unterricht Textrekonstruktion: Die Eigenschaften des Wassers
 Materialien für den sprachsensiblen Unterricht Textrekonstruktion: Die Eigenschaften des Wassers Unterrichtsfach Themenbereich/e Chemie Wasser als ohstoff und Lösungsmittel Schulstufe (Klasse) 8. (4.)
Materialien für den sprachsensiblen Unterricht Textrekonstruktion: Die Eigenschaften des Wassers Unterrichtsfach Themenbereich/e Chemie Wasser als ohstoff und Lösungsmittel Schulstufe (Klasse) 8. (4.)
Kinetische Energie der Moleküle / Aggregatzustand
 2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
2.3 Intermolekulare Anziehungskräfte und Molekülkristalle Kräfte zwischen Molekülen - Van-der-Waals-Kräfte Orientierungskräfte bzw. Dipol-Dipol-Kräfte Induktionskräfte bzw. induzierte Dipole Dispersionskräfte
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Meine eigene Physik-Fibel - Grundbegriffe der Physik Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Meine eigene
Die 3 Stoffklassen der Elemente
 Die Art der Bindung hängt davon ab, wie stark die Atome ihre Valenzelektronen anziehen. Elektronegativität (Abb. 17, S. 114) Qualitative Angabe, wie stark die Atomrümpfe die Elektronen in der Valenzschale
Die Art der Bindung hängt davon ab, wie stark die Atome ihre Valenzelektronen anziehen. Elektronegativität (Abb. 17, S. 114) Qualitative Angabe, wie stark die Atomrümpfe die Elektronen in der Valenzschale
1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE VORÜBERLEGUNGEN
 1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE Chemie beschäftigt sich mit Materie. Die Aggregatzustände (s, l und g) sind Formen der Materie. Materie besteht aus
1. STOFFE UND STOFFEIGENSCHAFTEN ARBEITSBLATT 1.1 MATERIE UND IHRE KLEINSTEN BAUSTEINE Chemie beschäftigt sich mit Materie. Die Aggregatzustände (s, l und g) sind Formen der Materie. Materie besteht aus
Gruppenarbeit : Zwischenmolekulare Kräfte
 Expertengruppe A Zwischenmolekulare Kräfte Allgemeines Zwischenmolekulare Kräfte dürfen nicht mit der Kovalenzbindung verwechselt werden. Bei der Kovalenzbindung geht es um Kräfte innerhalb der Moleküle
Expertengruppe A Zwischenmolekulare Kräfte Allgemeines Zwischenmolekulare Kräfte dürfen nicht mit der Kovalenzbindung verwechselt werden. Bei der Kovalenzbindung geht es um Kräfte innerhalb der Moleküle
10. Jahrgangsstufe Organische Chemie Skript Einführungsklasse
 4. Die Eigenschaften von Alkanen 4.1 Der Aggregatszustand bzw. die Siedetemperatur Der Aggregatszustand von Alkanen bei Raumtemperatur ist von der Siedetemperatur abhängig und steht in Zusammenhang mit
4. Die Eigenschaften von Alkanen 4.1 Der Aggregatszustand bzw. die Siedetemperatur Der Aggregatszustand von Alkanen bei Raumtemperatur ist von der Siedetemperatur abhängig und steht in Zusammenhang mit
Grundlagen der Chemie Lösungen Prof. Annie Powell
 Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Lösungen Prof. Annie Powell KIT Universität des Landes Baden-Württemberg und nationales Forschungszentrum in der Helmholtz-Gemeinschaft www.kit.edu Inhalte Konzentrationsmaße Wasser als Lösungsmittel Solvatation,
Polare Bindungen. Die Elektronen eines bindenden. Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich
 Moleküle Polare Bindungen Die Elektronen eines bindenden (gemeinsamen) Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich zwischen den beiden Atomkernen der Bindungspartner
Moleküle Polare Bindungen Die Elektronen eines bindenden (gemeinsamen) Elektronenpaares sind in Wirklichkeit eher zwei Elektronen, die sich mehrheitlich zwischen den beiden Atomkernen der Bindungspartner
Wasser ein besonderer Stoff
 IfU Wasser ein besonderer Stoff Wolfgang Kinzelbach Institut für Umweltingenieurwissenschaft ETH Zürich Email: kinzelbach@ifu.baug.ethz.ch Das Wassermolekül Zusammensetzung H 2 O Molekül insgesamt neutral,
IfU Wasser ein besonderer Stoff Wolfgang Kinzelbach Institut für Umweltingenieurwissenschaft ETH Zürich Email: kinzelbach@ifu.baug.ethz.ch Das Wassermolekül Zusammensetzung H 2 O Molekül insgesamt neutral,
Aufgabe: Erkläre folgende Tatsache mit Hilfe des Teilchenmodells! An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen.
 An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen. Bei einem Flüssigkeitsthermometer kann die Temperatur an der Höhe des Flüssigkeitsstandes im Röhrchen abgelesen werden. 1827
An heißen Tagen bilden sich auf einer gekühlten Getränkeflasche Wassertropfen. Bei einem Flüssigkeitsthermometer kann die Temperatur an der Höhe des Flüssigkeitsstandes im Röhrchen abgelesen werden. 1827
Erscheinungsformen und Eigenschaften des Wassers
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 5 & 6 Erscheinungsformen und Eigenschaften des Wassers Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 5 & 6 Erscheinungsformen und Eigenschaften des Wassers Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll für die Klassenstufen
VORANSICHT I/C. Die Anomalie des Wassers. Der Beitrag im Überblick. 14. Die Anomalie des Wassers 1 von 18. Günther Lohmer, Leverkusen
 14. Die Anomalie des Wassers 1 von 18 Die Anomalie des Wassers Günther Lohmer, Leverkusen Wie können Fische im Winter überleben, obwohl der See zugefroren ist? 1 Warum platzen Wasserflaschen im Gefrierschrank?
14. Die Anomalie des Wassers 1 von 18 Die Anomalie des Wassers Günther Lohmer, Leverkusen Wie können Fische im Winter überleben, obwohl der See zugefroren ist? 1 Warum platzen Wasserflaschen im Gefrierschrank?
1.9. Zwischenmolekulare Kräfte
 1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
1.9. Zwischenmolekulare Kräfte 1.9.1. Schmelzen und Verdampfen von Stoffen fester Zustand geordnetes Kristallgitter Teilchen schwingen um Ruhelage flüssiger Zustand Teilchen sind im Tropfen frei beweglich
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid
 Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
Experimentelle Ermittlung der molaren Lösungswärme von Kaliumchlorid Versuchsaufbau : Um den Versuch durchzuführen, benötigen wir 180 g Wasser, welches in ein Becherglas gefüllt wird. Die Temperatur ermitteln
PHYSIKTEST 3C Dezember 2015 GRUPPE A
 PHYSIKTEST 3C Dezember 2015 GRUPPE A Korrekturvorlage Aufgabe 1. (3 Punkte) Kreuze die richtigen 2 Aussagen an! Die Einheit von Energie ist Kelvin. Die Einheit von Wärmekapazität ist Joule pro Kilogramm
PHYSIKTEST 3C Dezember 2015 GRUPPE A Korrekturvorlage Aufgabe 1. (3 Punkte) Kreuze die richtigen 2 Aussagen an! Die Einheit von Energie ist Kelvin. Die Einheit von Wärmekapazität ist Joule pro Kilogramm
Posten 1a. Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? Antworten: a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k)
 Posten 1a Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k) d) (=> Posten 13f) Posten 1d Welcher der beiden Stoffe hat den tieferen Siedepunkt?
Posten 1a Wie sieht das Kugelwolkenmodell aus von einem Sauerstoffatom? a) (=> Posten 9o) b) (=> Posten 16l) c) (=> Posten 8k) d) (=> Posten 13f) Posten 1d Welcher der beiden Stoffe hat den tieferen Siedepunkt?
Grundlagen der statistischen Physik und Thermodynamik
 Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundlagen der statistischen Physik und Thermodynamik "Feuer und Eis" von Guy Respaud 6/14/2013 S.Alexandrova FDIBA 1 Grundlagen der statistischen Physik und Thermodynamik Die statistische Physik und die
Grundwissen Chemie 9. Jahrgangsstufe G8
 Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Grundwissen Chemie 9. Jahrgangsstufe G8 Ionennachweise Man nutzt die Schwerlöslichkeit vieler Salze (z. B. AgCl) zum Nachweis und zur quantitativen Bestimmung der Ionen. Nachweis molekular gebauter Stoffe
Unterrichtskonzept zum Themenbereich Wasser (NT 5.1.2)
 Staatsinstitut für Schulqualität und Bildungsforschung Unterrichtskonzept zum Themenbereich Wasser (NT 5.1.2) Lehrplanbezug Beim Themenbereich Wasser sollen die Schülerinnen und Schüler die drei Aggregatzustände
Staatsinstitut für Schulqualität und Bildungsforschung Unterrichtskonzept zum Themenbereich Wasser (NT 5.1.2) Lehrplanbezug Beim Themenbereich Wasser sollen die Schülerinnen und Schüler die drei Aggregatzustände
Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate
 Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate Zeitbedarf für die Versuchsdurchführung: ca. 10 Min. Geräte: Magnetrührer mit Magnetrührstäbchen Thermometer (min. 0,5 C Genauigkeit)
Lösungsenthalpie / Lösungswärme unterschiedlicher Zinksulfat-Hydrate Zeitbedarf für die Versuchsdurchführung: ca. 10 Min. Geräte: Magnetrührer mit Magnetrührstäbchen Thermometer (min. 0,5 C Genauigkeit)
WasserKreuzworträtsel
 Das Element Wasser Das Element Wasser ARBEITSBLATT WasserKreuzworträtsel Teste dein WasserWissen! Um dir etwas zu helfen, haben wir dir ein paar Buchstaben bereits richtig eingesetzt. Tipp: Bei der WasserWerkstatt
Das Element Wasser Das Element Wasser ARBEITSBLATT WasserKreuzworträtsel Teste dein WasserWissen! Um dir etwas zu helfen, haben wir dir ein paar Buchstaben bereits richtig eingesetzt. Tipp: Bei der WasserWerkstatt
Bei einer chemischen Reaktion tauschen die Atome ihre Bindungspartner
 3. DIE CHEMISCHE REAKTION ARBEITSBLATT 3.1 DIE MASSE BEI CHEMISCHEN REAKTIONEN Bei einer chemischen Reaktion tauschen die Atome ihre Bindungspartner Wie ändert sich die Masse bei einer chemischen Reaktion?
3. DIE CHEMISCHE REAKTION ARBEITSBLATT 3.1 DIE MASSE BEI CHEMISCHEN REAKTIONEN Bei einer chemischen Reaktion tauschen die Atome ihre Bindungspartner Wie ändert sich die Masse bei einer chemischen Reaktion?
Klassenarbeit - Wasser
 Klassenarbeit - Wasser 4. Klasse / Sachkunde Grundlagen; Aggregatzustände; Verdunstung; Niederschlag; Kondensation; Wasserkreislauf Aufgabe 1 Kreuze an! Richtig oder falsch? Richtig Falsch Beim Erhitzen
Klassenarbeit - Wasser 4. Klasse / Sachkunde Grundlagen; Aggregatzustände; Verdunstung; Niederschlag; Kondensation; Wasserkreislauf Aufgabe 1 Kreuze an! Richtig oder falsch? Richtig Falsch Beim Erhitzen
Flüssigkeitsthermometer Bimetallthermometer Gasthermometer Celsius Fahrenheit
 Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
Wärme Ob etwas warm oder kalt ist können wir fühlen. Wenn etwas wärmer ist, so hat es eine höhere Temperatur. Temperaturen können wir im Bereich von etwa 15 Grad Celsius bis etwa 45 Grad Celsius recht
bestimmte mehratomige Anionen mit Sauerstoff werden mit dem lateinischen Namen benannt und enden auf at.
 DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
DIE BINDUNGSARTEN UND DAS PERIODENSYSTEM 1) IONISCHE VERBINDUNGEN SALZE Wenn die Atome Ionen bilden, haben sie meist die gleiche Elektronenzahl, wie das nächstgelegene neutrale Edelgas. Na bildet dann
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie
 Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Vorkurs Allgemeine Chemie für Ingenieure und Biologen 20. Oktober 2015 Dr. Helmut Sitzmann, Apl.-Professor für Anorganische Chemie DIE CHEMISCHE BINDUNG Ionische Bindung, Beispiel Natriumchlorid Trifft
Wie stelle ich Kärtchen her, auf denen hinten die Lösung aufgedruckt ist?
 Wie stelle ich Kärtchen her, auf denen hinten die Lösung aufgedruckt ist? 1. Fragen- und Lösungsblätter ausdrucken! 3. Von beiden Blättern den Rand abschneiden! 2. Jeweiliges Lösungsblatt zum richtigen
Wie stelle ich Kärtchen her, auf denen hinten die Lösung aufgedruckt ist? 1. Fragen- und Lösungsblätter ausdrucken! 3. Von beiden Blättern den Rand abschneiden! 2. Jeweiliges Lösungsblatt zum richtigen
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt für die Klassen 5 bis 6: Temperatur und Wärme
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 5 bis 6: Temperatur und Wärme Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Lernwerkstatt
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt für die Klassen 5 bis 6: Temperatur und Wärme Das komplette Material finden Sie hier: School-Scout.de SCHOOL-SCOUT Lernwerkstatt
Bau der Metalle Eigenschaften plastisch verformbar elektrisch leitfähig hohe Siede- und Schmelztemperaturen
 Metallbindungen Bau der Metalle bestehen aus positiv geladene Atomrümpfe (= Atomkern und alle Elektrone auβer den Vallenzelektronen) + frei beweglichen Auβenelektronen Atomrümpfe sind sehr fest angeordnet
Metallbindungen Bau der Metalle bestehen aus positiv geladene Atomrümpfe (= Atomkern und alle Elektrone auβer den Vallenzelektronen) + frei beweglichen Auβenelektronen Atomrümpfe sind sehr fest angeordnet
Lernmaterial Lernfeld 1 Grundlagen Physik und Chemie. Chemische Grundlagen, Bindungsarten. Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms
 Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Chemische Grundlagen, Bindungsarten Zu Erinnerung : Schematischer Aufbau eines Wasserstoffatoms Hier ist ein Lithiumatom schematisch dargestellt. Elektronen umkreisen den Kern in diskreten Bahnen IQ Technikum
Das sind vielleicht Zustände!
 1 Das sind vielleicht Zustände! Wasser ist der einzige Stoff auf unserem Planeten, der in drei verschiedenen Formen, sogenannten Aggregatszuständen, vorkommt: fest, flüssig und gasförmig. Das heißt, Wasser
1 Das sind vielleicht Zustände! Wasser ist der einzige Stoff auf unserem Planeten, der in drei verschiedenen Formen, sogenannten Aggregatszuständen, vorkommt: fest, flüssig und gasförmig. Das heißt, Wasser
Stationenbetrieb DBW. 8. Januar 2011
 Stationenbetrieb DBW 8. Januar 2011 1 Station I AUFGABE. Welche Einheit gehört zu welcher Größe? Schreibe den richtigen Buchstaben hinter jeder Einheit: A B C D E F G H Volumen Länge Zeit Beschleunigung
Stationenbetrieb DBW 8. Januar 2011 1 Station I AUFGABE. Welche Einheit gehört zu welcher Größe? Schreibe den richtigen Buchstaben hinter jeder Einheit: A B C D E F G H Volumen Länge Zeit Beschleunigung
Kreislauf 15/24 Winde verblasen die Wolken auch auf andere Teile der Erde. Wenn es an der Erdoberfläche windstill ist, weht in der Höhe trotzdem Wind.
 Kreislauf 13/24 Manche Quellen sind sehr klein: Es rinnt nur ein schmales Rinnsal daraus hervor. Aus manchen Quellen aber sprudelt ein richtiger Bach. Immer wieder fließen kleinere Bäche in den Bach, er
Kreislauf 13/24 Manche Quellen sind sehr klein: Es rinnt nur ein schmales Rinnsal daraus hervor. Aus manchen Quellen aber sprudelt ein richtiger Bach. Immer wieder fließen kleinere Bäche in den Bach, er
Auf der rechten Seite sind Beispiele für kovalente Bindungen.
 Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Bei einem Gemisch aus Natrium und Chlorid wird einen Ionenverbindung entstehen und sich ein Ionengitter ausbilden. Wenn Natrium nicht vorhanden ist, hat Chlorid aber natürlich noch immer das Bedürfnis,
Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1. Bsp.: Grundwissen 9.Klasse NTG 2 Grundwissen 9.Klasse NTG 2
 Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1 Die Stoffmenge n = 1mol ist die Stoffportion, die 6,022 10 23 Teilchen enthält. Die Stoffmenge n n(he) = 1 mol n(h 2 ) = 1 mol enthält 6,022 10 23
Grundwissen 9.Klasse NTG 1 Grundwissen 9.Klasse NTG 1 Die Stoffmenge n = 1mol ist die Stoffportion, die 6,022 10 23 Teilchen enthält. Die Stoffmenge n n(he) = 1 mol n(h 2 ) = 1 mol enthält 6,022 10 23
I. Chemische Bindung und Zwischenmolekulare Kräfte
 I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
I. Chemische Bindung und Zwischenmolekulare Kräfte MINT-UNTERRICHTSEINHEIT A. Ausgangslage Die klare Unterscheidung der chemischen Bindung- und der Zwischenmolekularen Kräfte und die korrekte Zuordnung
Planungsblatt Physik für die 3B
 Planungsblatt Physik für die 3B Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Montag 22.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Planungsblatt Physik für die 3B Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Montag 22.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m
 GRATIS-Übungsdokument Gymnasium Klasse 8 Physik Thema: Mechanik, Wärmelehre, Elektrizitätslehre CATLUX de Energie Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m Energie ist gespeicherte
GRATIS-Übungsdokument Gymnasium Klasse 8 Physik Thema: Mechanik, Wärmelehre, Elektrizitätslehre CATLUX de Energie Arbeit = Kraft Weg ; W = F s ; 1 Joule = 1 Newton Meter ; 1 J = 1 N m Energie ist gespeicherte
(VIII) Wärmlehre. Wärmelehre Karim Kouz WS 2014/ Semester Biophysik
 Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Quelle: http://www.pro-physik.de/details/news/1666619/neues_bauprinzip_fuer_ultrapraezise_nuklearuhr.html (VIII) Wärmlehre Karim Kouz WS 2014/2015 1. Semester Biophysik Wärmelehre Ein zentraler Begriff
Lösungen, Stoffmengen und Konzentrationen
 12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
12 Lösungen, Stoffmengen und Konzentrationen Lösungen sind homogene Mischungen reiner Stoffe, aber umgekehrt sind nicht alle homogenen Mischungen echte Lösungen. Echte Lösungen weisen nur zum Teil die
Wärmelehre/Thermodynamik. Wintersemester 2007
 Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 ladimir Dyakonov #13 am 30.01.2007 Folien im PDF Format unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Einführung in die Physik I Wärmelehre/Thermodynamik Wintersemester 2007 ladimir Dyakonov #13 am 30.01.2007 Folien im PDF Format unter: htt://www.hysik.uni-wuerzburg.de/ep6/teaching.html Raum E143, Tel.
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung.
 Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Thermodynamik 1. Typen der thermodynamischen Systeme. Intensive und extensive Zustandsgröße. Phasenübergänge. Ausdehnung bei Erwärmung. Nullter und Erster Hauptsatz der Thermodynamik. Thermodynamische
Geografie, D. Langhamer. Klimarisiken. Beschreibung des Klimas eines bestimmten Ortes. Räumliche Voraussetzungen erklären Klimaverlauf.
 Klimarisiken Klimaelemente Klimafaktoren Beschreibung des Klimas eines bestimmten Ortes Räumliche Voraussetzungen erklären Klimaverlauf Definitionen Wetter Witterung Klima 1 Abb. 1 Temperaturprofil der
Klimarisiken Klimaelemente Klimafaktoren Beschreibung des Klimas eines bestimmten Ortes Räumliche Voraussetzungen erklären Klimaverlauf Definitionen Wetter Witterung Klima 1 Abb. 1 Temperaturprofil der
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern?
 An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Temperatur Der nullte Hauptsatz der Thermodynamik: Thermoskop und Thermometer Kelvin, Celsius- und der Fahrenheit-Skala Wärmeausdehnung
An welche Stichwörter von der letzten Vorlesung können Sie sich noch erinnern? Temperatur Der nullte Hauptsatz der Thermodynamik: Thermoskop und Thermometer Kelvin, Celsius- und der Fahrenheit-Skala Wärmeausdehnung
Die drei Aggregatzustände - Erklärung
 2.1.3 - Die drei Aggregatzustände - Erklärung VERSUCH 1 - DIE WASSERPISTOLE Versuchsdurchführung: Die Wasserpistole (Bild 4) wird zum einerseits mit Wasser und andererseits mit Luft gefüllt. Anschließend
2.1.3 - Die drei Aggregatzustände - Erklärung VERSUCH 1 - DIE WASSERPISTOLE Versuchsdurchführung: Die Wasserpistole (Bild 4) wird zum einerseits mit Wasser und andererseits mit Luft gefüllt. Anschließend
Planungsblatt Physik für die 3B
 Planungsblatt Physik für die 3B Woche 24 (von 12.02 bis 16.02) Hausaufgaben 1 Bis Montag 19.02: Lerne die Notizen von Woche 24! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Planungsblatt Physik für die 3B Woche 24 (von 12.02 bis 16.02) Hausaufgaben 1 Bis Montag 19.02: Lerne die Notizen von Woche 24! Kernbegriffe dieser Woche: Energie, Leistung, Wärme, Wärmeleitung, Konvektion,
Grundwissen Chemie 9. Jahrgangsstufe
 Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Grundwissen Chemie 9. Jahrgangsstufe 1. Stoffe und Reaktionen Gemisch: Stoff, der aus mindestens zwei Reinstoffen besteht. Homogen: einzelne Bestandteile nicht erkennbar Gasgemisch z.b. Legierung Reinstoff
Alkane. Name: Summenformel: vereinfachte Formel: Zustand: Methan CH 4 CH 4 g (gaseous) Ethan C 2 H 6 CH 3 CH 3 g. Propan C 3 H 8 CH 3 CH 2 CH 3 g
 Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Alkane Name: Summenformel: vereinfachte Formel: Zustand: Methan C 4 C 4 g (gaseous) Ethan C 2 6 C 3 C 3 g Propan C 3 8 C 3 C 2 C 3 g Butan C 4 10 C 3 C 2 C 2 C 3 g Pentan C 5 12 C 3 C 2 C 2 C 2 C 3 l (liquid)
Lösungen, Salze, Ionen und Elektrolyte
 Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Lösungen, Salze, Ionen und Elektrolyte Lösungen Eine Lösung ist in der Chemie ein homogenes Gemisch, das aus zwei oder mehr chemisch reinen Stoffen besteht. Sie enthält einen oder mehrere gelöste Stoffe
Basiskenntnistest - Chemie
 Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Basiskenntnistest - Chemie 1.) Welche Aussage trifft auf Alkohole zu? a. ) Die funktionelle Gruppe der Alkohole ist die Hydroxygruppe. b. ) Alle Alkohole sind ungiftig. c. ) Mehrwertige Alkohole werden
Aggregatzustände (Niveau 1)
 Aggregatzustände (Niveau 1) 1. Wasser kann verschiedene Zustandsformen haben, die sogenannten Aggregatzustände. Im Frühjahr kannst du die verschiedenen Aggregatzustände beobachten. Ergänze im Text die
Aggregatzustände (Niveau 1) 1. Wasser kann verschiedene Zustandsformen haben, die sogenannten Aggregatzustände. Im Frühjahr kannst du die verschiedenen Aggregatzustände beobachten. Ergänze im Text die
1. Vervollständigen Sie folgende Tabelle:
 Die Zwischenmolekularen Kräfte LÖSUG Seite 1 von 8 ÜBUGE 1. Vervollständigen Sie folgende Tabelle: e e Ar Kr Xe Elektronenzahl 2 10 18 36 54 Stärke der Van der Waals Kräfte nimmt in Pfeilrichtung zu Siede-
Die Zwischenmolekularen Kräfte LÖSUG Seite 1 von 8 ÜBUGE 1. Vervollständigen Sie folgende Tabelle: e e Ar Kr Xe Elektronenzahl 2 10 18 36 54 Stärke der Van der Waals Kräfte nimmt in Pfeilrichtung zu Siede-
NH 3. CCl 4 CO 2. Lösungen zur Lernzielkontrolle Sekunda. Hilfsmittel: PSE, Taschenrechner
 Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Lösungen zur Lernzielkontrolle Sekunda Hilfsmittel: PSE, Taschenrechner 1 Stoffklassen / Bindungslehre / Zwischenmolekulare Kräfte (1) 1.1 Elektrische Leitfähigkeit verschiedener Stoffe (3) leitfähig,
Physik für Mediziner im 1. Fachsemester
 Physik für Mediziner im 1. Fachsemester #7 28/10/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Mechanik Teil 3 - Versuche M1 Dichte und Hydrodynamik: Bestimmung der Dichte eines zylindrischen
Physik für Mediziner im 1. Fachsemester #7 28/10/2008 Vladimir Dyakonov dyakonov@physik.uni-wuerzburg.de Mechanik Teil 3 - Versuche M1 Dichte und Hydrodynamik: Bestimmung der Dichte eines zylindrischen
Schätzfragen Wasser. Wasser allgemein Trinkwasser Wasserkreislauf - Flüsse Wasser, Tiere, Pflanzen
 Wasser Wasser allgemein Trinkwasser Wasserkreislauf - Flüsse Wasser, Tiere, Pflanzen 1 Wasser allgemein Die Erde heißt blauer Planet weil sie...??? a) bis zur Hälfte mit Wasser bedeckt ist b) zu drei Viertel
Wasser Wasser allgemein Trinkwasser Wasserkreislauf - Flüsse Wasser, Tiere, Pflanzen 1 Wasser allgemein Die Erde heißt blauer Planet weil sie...??? a) bis zur Hälfte mit Wasser bedeckt ist b) zu drei Viertel
Lest euch folgende Seite durch und schaut das Video an:
 Station 1 Lest euch folgende Seite durch und schaut das Video an: http://bit.ly/9c-station1 Zur Beantwortung folgende Grafik heranziehen: http://bit.ly/9c-station1b Aufgaben: 1. Weshalb sollte die Flasche
Station 1 Lest euch folgende Seite durch und schaut das Video an: http://bit.ly/9c-station1 Zur Beantwortung folgende Grafik heranziehen: http://bit.ly/9c-station1b Aufgaben: 1. Weshalb sollte die Flasche
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg
 TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Gießen von Metallen (Änderung von Volumen und
TU Bergakademie Freiberg Institut für Werkstofftechnik Schülerlabor science meets school Werkstoffe und Technologien in Freiberg GRUNDLAGEN Modul: Versuch: Gießen von Metallen (Änderung von Volumen und
Nachweis molekularer Stoffe. Nachweis von Kationen. Nachweis von Halogenid-Ionen. Nachweis von Sulfat- bzw. Carbonat-Ionen 1 GW 9 NTG 2 GW 9 NTG
 1 1 Glimmspanprobe: Sauerstoff-Nachweis Verbrennung in reinem Sauerstoff ist heftiger als in Luft à glimmender Holzspan glüht auf bzw. entzündet sich wieder Nachweis molekularer Stoffe Knallgasprobe: Wasserstoff-Nachweis
1 1 Glimmspanprobe: Sauerstoff-Nachweis Verbrennung in reinem Sauerstoff ist heftiger als in Luft à glimmender Holzspan glüht auf bzw. entzündet sich wieder Nachweis molekularer Stoffe Knallgasprobe: Wasserstoff-Nachweis
02. Was kann man über die Teilchen eines schmelzenden Stoffes aussagen?
 01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
01. Nenne je beide Übergänge zwischen a) dem festen und dem flüssigen b) dem flüssigen und dem gasförmigen c) dem festen und dem gasförmigen Aggregatzustand. 02. Was kann man über die Teilchen eines schmelzenden
1 Chemie des Wassers. 1.1 Eigenschaften des Wassers. Bindung und Struktur H + O + H H O H
 1 Chemie des Wassers 1.1 Eigenschaften des Wassers Bindung und Struktur Molekül mit der Summenformel H 2 O - kovalente Bindung (Atombindung) zwischen O- und H-Atomen - Modell der kovalenten Bindung Oktettregel
1 Chemie des Wassers 1.1 Eigenschaften des Wassers Bindung und Struktur Molekül mit der Summenformel H 2 O - kovalente Bindung (Atombindung) zwischen O- und H-Atomen - Modell der kovalenten Bindung Oktettregel
1. Wärmelehre 1.1. Temperatur. Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités)
 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für die Temperatur Prinzip
Basiskenntnistest - Physik
 Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
Basiskenntnistest - Physik 1.) Welche der folgenden Einheiten ist keine Basiseinheit des Internationalen Einheitensystems? a. ) Kilogramm b. ) Sekunde c. ) Kelvin d. ) Volt e. ) Candela 2.) Die Schallgeschwindigkeit
TH emeneft. Klima und Klimawandel. Kohlendioxid das besondere Gas. Aufgaben:
 Kohlendioxid das besondere Gas Das Klima auf der Erde wird durch viele verschiedene Dinge bestimmt. Eine wichtige Rolle spielt dabei die Luft. Sie besteht aus einem Gemisch von unsichtbaren Gasen. Dazu
Kohlendioxid das besondere Gas Das Klima auf der Erde wird durch viele verschiedene Dinge bestimmt. Eine wichtige Rolle spielt dabei die Luft. Sie besteht aus einem Gemisch von unsichtbaren Gasen. Dazu
Kovalenzbindungen und zwischenmolekulare Kräfte
 Chemie Kovalenzbindungen und zwischenmolekulare Kräfte Zusammenfassungen Prüfung Donnerstag, 11. Mai 2017 _ Kovalenzbindungen 1 _ Elektronenpaar-Abstossungsmodell 2 _ Polare und apolare Bindungen 3 _ Dipolmoleküle
Chemie Kovalenzbindungen und zwischenmolekulare Kräfte Zusammenfassungen Prüfung Donnerstag, 11. Mai 2017 _ Kovalenzbindungen 1 _ Elektronenpaar-Abstossungsmodell 2 _ Polare und apolare Bindungen 3 _ Dipolmoleküle
Alles was uns umgibt!
 Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Was ist Chemie? Womit befasst sich die Chemie? Die Chemie ist eine Naturwissenschaft, die sich mit der Materie (den Stoffen), ihren Eigenschaften und deren Umwandlung befasst Was ist Chemie? Was ist Materie?
Grundwissen Chemie 8. Klasse NTG
 Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Grundwissen Chemie 8. Klasse NTG Reinstoff hat gleich bleibende Eigenschaften (Stoffebene) besteht aus einer Sorte gleichartiger Teilchen z.b.: dest. Wasser, Kupfer, Gold, Salz 8.1 C NTG Element sind nicht
Materie ist die Gesamtheit aller Stoffe: Energie bei chemischen Reaktionen:
 A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt eine Masse m (Einheit: kg) Dichte = Masse / Volumen
A.1.1 1 Stoffbegriff / Materie / Energie Materie ist die Gesamtheit aller Stoffe: Jeder Stoff füllt einen Raum V (Einheit: m³) aus Jeder Stoff besitzt eine Masse m (Einheit: kg) Dichte = Masse / Volumen
8. Vorlesung EP. EPI WS 2007/08 Dünnweber/Faessler
 8. Vorlesung EP I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik (Fortsetzung: Auftrieb) c) Oberflächenspannung und Kapillarität Versuche:
8. Vorlesung EP I. Mechanik 5. Mechanische Eigenschaften von Stoffen a) Deformation von Festkörpern b) Hydrostatik, Aerostatik (Fortsetzung: Auftrieb) c) Oberflächenspannung und Kapillarität Versuche:
Wiederholungsthema: Ionenbindung und Salze. Zusammenfassung: Ionen und Ionenbildung
 Wiederholungsthema: Ionenbindung und Salze Zusammenfassung: Ionen und Ionenbildung Wie sich Atome auch immer verbinden mögen, so versuchen sie doch stets dabei die Edelgaskonfiguration (Abb.3) zu erhalten,
Wiederholungsthema: Ionenbindung und Salze Zusammenfassung: Ionen und Ionenbildung Wie sich Atome auch immer verbinden mögen, so versuchen sie doch stets dabei die Edelgaskonfiguration (Abb.3) zu erhalten,
1 Chemie des Wassers. 1.1 Eigenschaften des Wassers. Bindung und Struktur H + O + H H O H
 1 Chemie des Wassers 1.1 Eigenschaften des Wassers Bindung und Struktur - Molekül mit der Summenformel H 2 O - kovalente Bindung (Atombindung) zwischen O- und H-Atomen - Modell der kovalenten Bindung Oktettregel
1 Chemie des Wassers 1.1 Eigenschaften des Wassers Bindung und Struktur - Molekül mit der Summenformel H 2 O - kovalente Bindung (Atombindung) zwischen O- und H-Atomen - Modell der kovalenten Bindung Oktettregel
Bohrsches Atommodell
 Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Atome und ihre Bindungen Atomaufbau Im Atomkern befinden sich die Protonen (positiv geladen) und die Neutronen (neutral). P und N sind ungefähr gleich schwer und machen 99% der Atommasse aus. Um den Kern
Element. Verbindung. Reinstoff. homogenes Gemisch
 Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
Element Reinstoff, der chemisch nicht mehr zersetzt werden kann dessen Teilchen (Atome oder Moleküle) aus einer einzigen Atomart (gleiche Ordnungszahl) besteht Verbindung = Reinstoff, der sich in Elemente
1. Aufgaben der Klimaanlage
 Praxiswissen Pkw-Klimaanlagen 1 1. Aufgaben der Klimaanlage In erster Linie kommt der Klimaanlage die Aufgabe zu, die Temperatur im Fahrzeug - innenraum bei entsprechend hohen Außentemperaturen auf ein
Praxiswissen Pkw-Klimaanlagen 1 1. Aufgaben der Klimaanlage In erster Linie kommt der Klimaanlage die Aufgabe zu, die Temperatur im Fahrzeug - innenraum bei entsprechend hohen Außentemperaturen auf ein
DIE FILES DÜRFEN NUR FÜR DEN EIGENEN GEBRAUCH BENUTZT WERDEN. DAS COPYRIGHT LIEGT BEIM JEWEILIGEN AUTOR.
 Weitere Files findest du auf www.semestra.ch/files DIE FILES DÜRFEN NUR FÜR DEN EIGENEN GEBRAUCH BENUTZT WERDEN. DAS COPYRIGHT LIEGT BEIM JEWEILIGEN AUTOR. Physiklabor 2 Michel Kaltenrieder 9. Februar
Weitere Files findest du auf www.semestra.ch/files DIE FILES DÜRFEN NUR FÜR DEN EIGENEN GEBRAUCH BENUTZT WERDEN. DAS COPYRIGHT LIEGT BEIM JEWEILIGEN AUTOR. Physiklabor 2 Michel Kaltenrieder 9. Februar
Aufgaben zu intermolekularen Kräften
 Aufgaben zu intermolekularen Kräften 1L ummerierung und Inhalte der gedruckten Version mit der Download-Version abgleichen! Evtl. gibt es Unterschiede. äufig enthält die Download-Version noch Bonusaufgaben.
Aufgaben zu intermolekularen Kräften 1L ummerierung und Inhalte der gedruckten Version mit der Download-Version abgleichen! Evtl. gibt es Unterschiede. äufig enthält die Download-Version noch Bonusaufgaben.
2. Chemische Bindungen 2.1
 2. Chemische Bindungen 2.1 Chemische Bindungen Deutung von Mischungsversuchen Benzin und Wasser mischen sich nicht. Benzin ist somit eine hydrophobe Flüssigkeit. Auch die Siedepunkte der beiden Substanzen
2. Chemische Bindungen 2.1 Chemische Bindungen Deutung von Mischungsversuchen Benzin und Wasser mischen sich nicht. Benzin ist somit eine hydrophobe Flüssigkeit. Auch die Siedepunkte der beiden Substanzen
Chemieepoche Klasse 11. Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen
 Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Eisengewinnung (Schülervortrag) Fortsetzung Chemische Bindungen Warum sind im Wassermolekül zwei Wasserstoffatome mit
Chemieepoche Klasse 11 Aufbau der Stoffe und die Grundgesetze chemischer Reaktionen Eisengewinnung (Schülervortrag) Fortsetzung Chemische Bindungen Warum sind im Wassermolekül zwei Wasserstoffatome mit
2. Die Klimazonen Fülle die Tabelle aus. Name der Klimazone Wie ist dort der Sommer? Wie ist dort der Winter?
 1. Die Jahreszeiten Das Wetter Sieh dir das Bild an. Du kannst darauf sehen, wie die Erde zur Sonne stehen muss, damit bei uns in Europa Frühling, Sommer, Herbst oder Winter ist. Schreibe die jeweilige
1. Die Jahreszeiten Das Wetter Sieh dir das Bild an. Du kannst darauf sehen, wie die Erde zur Sonne stehen muss, damit bei uns in Europa Frühling, Sommer, Herbst oder Winter ist. Schreibe die jeweilige
Schule mit Erfolg. Heimat-und Sachunterricht Wasser Probe Nr. 03 Blatt 1
 Heimat-und Sachunterricht Wasser Probe Nr. 03 Blatt 1 1. Wie trocknet das nasse Badetuch am schnellsten? Trage die Zahlen von 1 bis 4 in der richtigen Reihenfolge ein! (1= trocknet am schnellsten, 4= trocknet
Heimat-und Sachunterricht Wasser Probe Nr. 03 Blatt 1 1. Wie trocknet das nasse Badetuch am schnellsten? Trage die Zahlen von 1 bis 4 in der richtigen Reihenfolge ein! (1= trocknet am schnellsten, 4= trocknet
Exkurs: Wasser Das Elixier des Lebens
 Exkurs: Wasser Das Elixier des Lebens Wasser Anatomie eines Moleküls VSEPR-Modell sp3-hybridorbital Sigma-Bindung Elektronenkonfiguration Sauerstoff Das vollbesetzte 2s-Orbital sowie die drei p-orbitale
Exkurs: Wasser Das Elixier des Lebens Wasser Anatomie eines Moleküls VSEPR-Modell sp3-hybridorbital Sigma-Bindung Elektronenkonfiguration Sauerstoff Das vollbesetzte 2s-Orbital sowie die drei p-orbitale
Experiment Nr. 1: Wasser hat eine Haut. 1. Lege das Seidenpapier vorsichtig auf die Wasseroberfläche.
 Experiment Nr. 1: Wasser hat eine Haut Siehe Pädagogische Unterlagen, Seite 6, 1: Was ist Wasser? Wasser hat eine erhöhte Oberflächenspannung ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines
Experiment Nr. 1: Wasser hat eine Haut Siehe Pädagogische Unterlagen, Seite 6, 1: Was ist Wasser? Wasser hat eine erhöhte Oberflächenspannung ein Glas, mit Wasser gefüllt Nadel Büroklammer ein kleines
n = V Lsg m n l mol Grundwissen 9. Klasse Chemie (NTG) Analytische Chemie Stoffmenge n Molare Masse M Molares Volumen V M Stoffmengenkonzentration c
 Grundwissen 9. Klasse Chemie (NTG) 1. Analytische Chemie und Stöchiometrie Analytische Chemie Untersuchung von Reinstoffen und Stoffgemischen mit dem Ziel diese eindeutig zu identifizieren (= qualitativer
Grundwissen 9. Klasse Chemie (NTG) 1. Analytische Chemie und Stöchiometrie Analytische Chemie Untersuchung von Reinstoffen und Stoffgemischen mit dem Ziel diese eindeutig zu identifizieren (= qualitativer
Physikalisches Anfaengerpraktikum. Dissoziationsgrad und Gefrierpunkterniedrigung
 Physikalisches Anfaengerpraktikum Dissoziationsgrad und Gefrierpunkterniedrigung Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe ) Montag, 1. Februar 00 1. Versuchsaufbau Um den Dissoziationsgrad
Physikalisches Anfaengerpraktikum Dissoziationsgrad und Gefrierpunkterniedrigung Ausarbeitung von Marcel Engelhardt & David Weisgerber (Gruppe ) Montag, 1. Februar 00 1. Versuchsaufbau Um den Dissoziationsgrad
Bindungsarten. Edelgaskonfiguration. Elektronegativität
 Bindungsarten Einführende Erklärung des Kugelwolkenmodells und der Elektronenpaarschreibweise siehe Seiten 6 10 des Kapitels Historische Entwicklung des Atommodells. Elemente können bei chemischen Reaktionen
Bindungsarten Einführende Erklärung des Kugelwolkenmodells und der Elektronenpaarschreibweise siehe Seiten 6 10 des Kapitels Historische Entwicklung des Atommodells. Elemente können bei chemischen Reaktionen
Besetzung der Orbitale
 Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Frage Beim Wiederholen des Stoffes bin ich auf die Rechnung zur Energie gestoßen. Warum und zu welchem Zweck haben wir das gemacht? Was kann man daran jetzt erkennen? Was beschreibt die Formel zu E(n),
Jetzt wird s undurchsichtig: Der "Louche"-Effekt
 age fotostock / LOOK-foto Jetzt wird s undurchsichtig: Der "Louche"-Effekt Bild 1: Urlaub auf den Kykladen in Griechenland Bild 2: Ouzo (frz.: louche undurchsichtig, verdächtig, anrüchig) Bild 3: Ouzo
age fotostock / LOOK-foto Jetzt wird s undurchsichtig: Der "Louche"-Effekt Bild 1: Urlaub auf den Kykladen in Griechenland Bild 2: Ouzo (frz.: louche undurchsichtig, verdächtig, anrüchig) Bild 3: Ouzo
Ionenbindung Lehrerinformation
 Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Sozialform Zeit Die SuS erarbeiten sich chemische Informationen zu Kochsalz. Sie kennen die Bestandteile und wissen, wie Salz chemisch aufgebaut ist.
Lehrerinformation 1/5 Arbeitsauftrag Ziel Material Sozialform Zeit Die SuS erarbeiten sich chemische Informationen zu Kochsalz. Sie kennen die Bestandteile und wissen, wie Salz chemisch aufgebaut ist.
Skript zur Vorlesung
 Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
Skript zur Vorlesung 1. Wärmelehre 1.1. Temperatur Physikalische Grundeinheiten : Die Internationalen Basiseinheiten SI (frz. Système international d unités) 1. Wärmelehre 1.1. Temperatur Ein Maß für
BIONIK Der Lotuseffekt
 BIONIK Der Lotuseffekt Das Begleitmaterial zur Online- Version Moritz Krause Version: 01.08.14 Einleitung: Dieses Material soll dich durch das Modul Der Lotuseffekt begleiten. Die Homepage bietet viele
BIONIK Der Lotuseffekt Das Begleitmaterial zur Online- Version Moritz Krause Version: 01.08.14 Einleitung: Dieses Material soll dich durch das Modul Der Lotuseffekt begleiten. Die Homepage bietet viele
Staunen, was die Natur aus Wasser zaubert : Raureif, Eisblumen, Eiszapfen, Wolken, Nebel, Tau
 Wasser Nicht alle haben alles erlebt! Die Schule hat sich auf den Weg gemacht, aber das Ziel noch lange nicht erreicht. Die Anhänge bieten einen Überblick über die Arbeit einer ganzen Schule während eines
Wasser Nicht alle haben alles erlebt! Die Schule hat sich auf den Weg gemacht, aber das Ziel noch lange nicht erreicht. Die Anhänge bieten einen Überblick über die Arbeit einer ganzen Schule während eines
6. UNTERRICHTSTUNDE: WASSERKREISLAUF/ VERDUNSTEN (VERDAMPFEN)
 THEMA: THEMA DER WASSERKREISLAUF 2. 6. UNTERRICHTSTUNDE 59 6. UNTERRICHTSTUNDE: WASSERKREISLAUF/ VERDUNSTEN (VERDAMPFEN) Ziel: Die Schüler sollen verstehen, wie ein Wasserkreislauf entsteht. Sprache der
THEMA: THEMA DER WASSERKREISLAUF 2. 6. UNTERRICHTSTUNDE 59 6. UNTERRICHTSTUNDE: WASSERKREISLAUF/ VERDUNSTEN (VERDAMPFEN) Ziel: Die Schüler sollen verstehen, wie ein Wasserkreislauf entsteht. Sprache der
Stoffgemisch. Reinstoff. Homogenes Gemisch. Heterogenes Gemisch. ( 8. Klasse NTG 1 / 48 ) ( 8. Klasse NTG 2 / 48 ) ( 8. Klasse NTG 3 / 48 )
 Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Stoffgemisch ( 8. Klasse NTG 1 / 48 ) besteht aus zwei oder mehr verschiedenen Reinstoffen Gemisch unterschiedlicher kleinster Teilchen Trennung durch physikalische Methoden möglich Reinstoff ( 8. Klasse
Die Zelle. Membranen: Struktur und Funktion
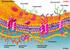 Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Die Zelle Membranen: Struktur und Funktion 8.4 Die Fluidität von Membranen. 8.6 Die Feinstruktur der Plasmamembran einer Tierzelle (Querschnitt). (Zum Aufbau der extrazellulären Matrix siehe auch Abbildung
Planungsblatt Physik für die 3F
 Planungsblatt Physik für die 3F Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Freitag 26.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Gerät, kinetische Energie,
Planungsblatt Physik für die 3F Woche 20 (von 15.01 bis 19.01) Hausaufgaben 1 Bis Freitag 26.01: Lerne die Notizen von Woche 20! Kernbegriffe dieser Woche: Energie, Leistung, Gerät, kinetische Energie,
