Schriftliche Prüfung S Analytische Chemie I Winter 2018
|
|
|
- Gisela Wolf
- vor 5 Jahren
- Abrufe
Transkript
1 Schriftliche Prüfung S Analytische Chemie I Winter 2018 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut ein. Es sind alle Hilfsmittel mit Ausnahme von Computern und Telekommunikation erlaubt. Unleserliche Texte, unklare Formulierungen oder unsaubere Skizzen können nicht bewertet werden. Bitte bemühen Sie sich um eine saubere Darstellung. Beginnen Sie jede Aufgabe auf einem neuen Blatt und schreiben Sie jedes abzugebende Blatt einzeln mit Ihrem Namen und Vornamen an. Notizen auf den Spektren werden nicht bewertet. Dieses Deckblatt ist ausgefüllt abzugeben. Die Aufgabenstellung ist ebenfalls einzureichen. Wir bitten Sie um Fairness und wünschen Ihnen viel Erfolg!
2 Prüfungsaufgabe 1: Spektrenaufgabe Vorwärtslösung (26 Punkte) Im separaten Handout finden Sie die IR, Massen, 13 C NMR und 1 H NMR Spektren der Verbindung C09. Bearbeiten Sie die folgenden Fragen. Ziel: Ermittlung der Konstitution von C09. Zum IR Spektrum: (4 Punkte) (I) Ordnen Sie die Banden bei 3500 cm -1 und 1710 cm -1 den entsprechenden Schwingungen zu. (2 Punkte) 3500 cm cm -1 (II) Welche Einflussgrößen legen die Frequenz einer Schwingung fest? Erläutern Sie qualitativ wie die Wellenzahl mit den Größen korreliert. (2 Punkte) Zum Massenspektrum: (4 Punkte) (I) Welches Fragment Ion könnte zu dem Signal bei m/z= 18 führen? Geben Sie die Summenformel an. (2 Punkte.) (II) a) Berechnen Sie die Massendifferenz zwischen Basispeak und Molekülionenpeak. (1 Punkt) b) Durch den Verlust welches Neutralteilchens könnte die Massendifferenz erklärt werden? Geben Sie eine Summenformel. (1 Punkt) Klausur Winter 2018 Seite 2 von 7
3 Zum 1 H-NMR Spektrum: (4 Punkte) (I) Wie äußert sich der Dacheffekt im NMR Spektrum (erklären Sie Anhand einer schematischen Zeichnung) und wie kann er bei der Interpretation von Nutzen sein? (1 Punkt) (II) Benennen Sie die Multipletts der Signale bei 1.80 und 3.62 ppm. (2 Punkte) 3.62 ppm 1.80 ppm (III) Identifizieren Sie den Kopplungspartner des Signals bei 3.62 ppm und geben Sie die chemische Verschiebung an. (1 Punkt) Zum 13 C-NMR Spektrum: (2 Punkte) (I) Wie können Sie das DEPT Spektrum nutzen, um die Zahl der quaternären Kohlenstoffatome zu bestimmen? Wie viele solcher Kohlenstoffe sind in C09 vorhanden? Geben Sie die jeweiligen chemischen Verschiebungen mit an. (2 Punkte) Zum Gesamten: (12 Punkte) (I) Bestimmen Sie die Summenformel von C09. (2 Punkte) Klausur Winter 2018 Seite 3 von 7
4 (II) a) Welches Fragment Ion könnte zu dem Signal bei m/z = 91 geführt haben? Geben Sie eine Strukturformel inklusive Ladung. (1 Punkt) b) Zeichnen Sie das Substitutionsmuster des Strukturelements, welches zu den Signalen bei 7.05 ppm bis 7.25 ppm im 1 H-NMR Spektrum geführt hat. Verwenden Sie R um Substituenten zu markieren. (1 Punkt) (III) Geben Sie eine mögliche Summenformel für das Fragment Ion bei m/z= 43. (1 Punkt) Nutzen Sie das 1 H-NMR Spektrum, um einen Strukturvorschlag für die entsprechende Teilstruktur zu erarbeiten. (1 Punkt) (IV) Das Signal bei 12.2 ppm im 1 H-NMR Spektrum ist nicht sichtbar, wenn D 2O als Lösungsmittel verwendet wird. Nennen und erklären Sie die Ursache dafür. (1 Punkt) (V) Geben Sie einen Strukturvorschlag für C09. (5 Punkte) Klausur Winter 2018 Seite 4 von 7
5 Prüfungsaufgabe 2: Elementanalytik (14 Punkte) 1. Multiple Choice Es ist jeweils zu beurteilen, ob die Aussage richtig oder falsch ist. Kreuzen Sie zutreffendes an: Jeweils alles richtig beantwortet: 1 Punkt; 3 Antworten richtig beantwortet: 0,5 Punkte; sonst 0 Punkte. a) Welche Aufgabe oder Fragestellung lässt sich mit Methoden der Elementanalytik beantworten? Aus welchem Motorbauteil stammen die Abriebpartikel im alten Motoröl? Wieviel Zink kann ohne erhöhtes gesundheitliches Risiko pro Tag aufgenommen werden? Wieviel Calcium befindet sich in einem Cappuccino? Wie gross ist der Anteil an Carbonsäuren in Butter? b) Messung und Ergebnisse Mehrfaches Messen (N > 3) macht Ergebnisse richtiger. Mehrfaches Messen (N > 3) macht Ergebnisse präziser. Die in ein ICP eingekoppelte Leistung beeinflusst den Ionisierungsgrad von Analyten. c) Merkmale von elementanalytischen Instrumenten Eine geringere Verdünnung der Probe vor der Messung erhöht die Empfindlichkeit des Messinstruments. Mit simultanen ICP-OES-Spektrometern lässt sich Aluminium gleichzeitig in mehreren Proben bestimmen. Effizientere Probenzufuhrsysteme verringern die Nachweisgrenze. Effizientere Probenzufuhrsysteme verringern die Matrixbelastung. Ein-Elementmethoden sind selektiver als Multi-Elementmethoden. d) Eine Lieferung Steinkohle (50 t) soll vor der Weiterverarbeitung auf verschiedene Spurenelemente untersucht werden (z.b. B, Zn, Mo). Sie erhalten 100 Proben zu jeweils 1 kg für die Analyse. Welche Aussagen können Sie daraus für die Analyse ableiten? Zur Ermittlung der mittleren Analytgehalte wird eine Mischprobe aus den Einzelproben erstellt. Die Probenahmeart war repräsentativ. Die auszuwählende Analysenmethode muss in der Lage sein viele Proben schnell zu messen. Die für die Kalibrierung zu verwendenden Standards sollten an die Matrix Steinkohle angepasst sein. Klausur Winter 2018 Seite 5 von 7
6 2. Analysenstrategie Schwermetalle in Bier Es gibt schon seit mehr als einem Jahrhundert immer wieder Berichte über einen erhöhten Schwermetallgehalt in Bier. Zurzeit gibt es dafür keine gesetzlichen Grenzwerte. Ein Bierbrauer, der nach einer weiteren Meldung in den Medien um seinen Absatz besorgt ist, möchte in seinem Betrieb ein Monitoring einrichten. Sie sollen das Unternehmen dabei unterstützen. Der Fachliteratur entnehmen Sie einige typische Angaben für die Metallgehalte von Bier. Rechnen Sie in ppb um. (1 P) Kupfer 6-50 µg L -1 ppb Blei µmol ml -1 ppb Zunächst soll die Produktion eines Monats (500 hl bzw Flaschen) auf die oben genannten Elemente untersucht werden. Bearbeiten Sie folgende Aufgaben: a. Wie viele Proben und wieviel Material pro Probe entnehmen Sie? (1 P) b. Die Analyse soll möglichst ohne weitere Vorbereitung der Probe erfolgen. Wählen Sie eine geeignete Methode. Nennen Sie auch einen konkreten Nachteil der gewählten Methode oder ein mögliches Problem bei dieser Analyse mit dieser Methode. (1.5 P) ICP-OES Flammen-AAS ETV-AAS c. In welchem Massenanteilsbereich erstellen Sie Lösungen für die Kalibrierung von Eisen? (1 P) d. Es stehen Ihnen drei Testgeräte unterschiedlicher Hersteller für die Messungen zur Verfügung. Sie verwenden zunächst externe wässrige Standardlösungen zur Kalibrierung und erhalten folgendes Diagramm. (1 P) Klausur Winter 2018 Seite 6 von 7
7 Im Folgenden ist jeweils eine Antwort richtig, kreuzen Sie diese an. Welches Gerät misst richtig? Typ 1 Typ 2 Typ 3 Das lässt sich damit nicht beantworten. Welches Gerät misst am empfindlichsten? Typ 1 Typ 2 Typ 3 Das lässt sich damit nicht beantworten. Welches Gerät hat den grössten linearen Messbereich? Typ 1 Typ 2 Typ 3 Das lässt sich damit nicht beantworten. Welches Gerät misst präzise? Typ 1 Typ 2 Typ 3 Das lässt sich damit nicht beantworten. e. Angenommen, Sie stellen fest, dass die externe Kalibrierung mit wässrigen Standardlösungen bei der Analyse von Bier zu falschen Ergebnissen führt. Spektrale Interferenzen haben Sie ausgeschlossen. Was ist eine naheliegende Ursache? Wie können Sie diesem Problem ohne Probenverdünnung konkret begegnen? (1 P) f. Neben dem Bier sollen auch Rohstoffe untersucht werden. Sie erhalten eine Probe von 100 g Hopfen. Nennen Sie alle Probenvorbereitungsschritte bis zur Analysenlösung? Machen Sie möglichst konkrete Angaben zu Massen oder Volumen. Berechnen Sie den Verdünnungsfaktor. (2.5 P) g. Angenommen Sie erhalten bei allen Zutaten für Arsen konstant Werte unterhalb der Nachweisgrenze, jedoch für das Bier Werte konstant deutlich oberhalb der Nachweisgrenze. Geben Sie zwei prinzipiell unterschiedliche Ursachen dafür an. (1 P) Klausur Winter 2018 Seite 7 von 7
Schriftliche Prüfung J Analytische Chemie I&II Winter 2018
 Schriftliche Prüfung 529-0058-00J Analytische Chemie I&II Winter 2018 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung 529-0058-00J Analytische Chemie I&II Winter 2018 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung S Analytische Chemie I Sommer 2017
 Schriftliche Prüfung 529-0051- 00S Analytische Chemie I Sommer 2017 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut
Schriftliche Prüfung 529-0051- 00S Analytische Chemie I Sommer 2017 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut
Schriftliche Prüfung S Analytische Chemie I Sommer 2015
 Schriftliche Prüfung 529-0051- 00S Analytische Chemie I Sommer 2015 Vorname: Name: Legi-Nr.: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut
Schriftliche Prüfung 529-0051- 00S Analytische Chemie I Sommer 2015 Vorname: Name: Legi-Nr.: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut
Schriftliche Prüfung Analytische Chemie I Sommer 2014
 Schriftliche Prüfung Analytische Chemie I Sommer 2014 Vorname: Name: Legi-Nr.: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut ein. Es sind
Schriftliche Prüfung Analytische Chemie I Sommer 2014 Vorname: Name: Legi-Nr.: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen Sie sich Ihre Zeit gut ein. Es sind
Schriftliche Prüfungen Smesterkurs Analytische Chemie I Instrumentalanalyse organischer Vebindungen Sommer 2011
 Schriftliche Prüfungen Smesterkurs Analytische Chemie I Instrumentalanalyse organischer Vebindungen Sommer 2011 Vorname: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120
Schriftliche Prüfungen Smesterkurs Analytische Chemie I Instrumentalanalyse organischer Vebindungen Sommer 2011 Vorname: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120
Schriftliche Prüfung Analytische Chemie I&II Winter 2012/2013
 Schriftliche Prüfung Analytische Chemie I&II Winter 2012/2013 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit gut ein.
Schriftliche Prüfung Analytische Chemie I&II Winter 2012/2013 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit gut ein.
Schriftliche Prüfungen Jahreskurs Analytische Chemie I&II Winter 2011/2012 BSc D-CHAB/BIOL
 Schriftliche Prüfungen Jahreskurs Analytische Chemie I&II Winter 2011/2012 BSc D-CHAB/BIOL Vorname: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich
Schriftliche Prüfungen Jahreskurs Analytische Chemie I&II Winter 2011/2012 BSc D-CHAB/BIOL Vorname: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich
Schriftliche Prüfung Analytische Chemie I / Instrumentalanalyse organischer Verbindungen
 Schriftliche Prüfung Analytische Chemie I / Instrumentalanalyse organischer Verbindungen Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen
Schriftliche Prüfung Analytische Chemie I / Instrumentalanalyse organischer Verbindungen Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 60 Min. Teilen
Schriftliche Prüfungen Jahreskurs Analytische Chemie I&II Sommer 2011 BSc D-CHAB/BIOL
 Schriftliche Prüfungen Jahreskurs Analytische Chemie I&II Sommer 2011 BSc D-CHAB/BIOL Vorname: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre
Schriftliche Prüfungen Jahreskurs Analytische Chemie I&II Sommer 2011 BSc D-CHAB/BIOL Vorname: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre
Schriftliche Prüfung J Analytische Chemie I&II Winter 2017
 Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Winter 2017 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Winter 2017 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung J Analytische Chemie I&II Sommer 2015
 Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Sommer 2015 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Sommer 2015 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung J Analytische Chemie I&II Winter 2015
 Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Winter 2015 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Winter 2015 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung BSc Herbst 2007
 Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2004
 Prüfungen Analytische Chemie Dienstag, 1. September 4 Schriftliche Prüfung. Vordiplom / BSc erbst 4 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 1. September 4 Schriftliche Prüfung. Vordiplom / BSc erbst 4 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Frühling 2006
 Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Schriftliche Prüfung BSc Frühling 2008
 Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Herbst 2013
 Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung J Analytische Chemie I&II Sommer 2016
 Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Sommer 2016 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung 529-0058- 00J Analytische Chemie I&II Sommer 2016 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit
Schriftliche Prüfung BSc Herbst 2014
 Prüfungen Analytische Chemie Montag, 25. August 2014 Schriftliche Prüfung BSc Herbst 2014 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Prüfungen Analytische Chemie Montag, 25. August 2014 Schriftliche Prüfung BSc Herbst 2014 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Schriftliche Prüfung BSc Herbst 2010
 Prüfungen Analytische Chemie Dienstag, 24. August 2010 Schriftliche Prüfung BSc Herbst 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Dienstag, 24. August 2010 Schriftliche Prüfung BSc Herbst 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Frühling 2014
 Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 1. Februar 2014 Schriftliche Prüfung BSc Frühling 2014 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Frühling 2006 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die
Prüfungen Analytische Chemie Mittwoch, 8. März 2006 Schriftliche Prüfung BSc Frühling 2006 D CAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die
!! Schriftliche!Prüfung!!!529%0058%00J!Analytische!Chemie!I&II! Winter!2016!
 SchriftlichePrüfung 529%0058%00JAnalytischeChemieI&II Winter2016 Vorname: Legi-Nr.: Name: EssindalleAufgabenzulösen.JedeAufgabewirdseparatbenotet. Zeit:120Min.TeilenSiesichIhreZeitgutein. EssindalleHilfsmittelmitAusnahmevonComputernundTelekommunikation
SchriftlichePrüfung 529%0058%00JAnalytischeChemieI&II Winter2016 Vorname: Legi-Nr.: Name: EssindalleAufgabenzulösen.JedeAufgabewirdseparatbenotet. Zeit:120Min.TeilenSiesichIhreZeitgutein. EssindalleHilfsmittelmitAusnahmevonComputernundTelekommunikation
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006
 Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Mittwoch, 27. September 2006 Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2006 D CHAB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Prüfungen Analytische Chemie Samstag, 9. Februar 2008 Schriftliche Prüfung BSc Frühling 2008 D CHAB/BIL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Schriftliche Prüfung BSc Herbst 2011
 Prüfungen Analytische Chemie Montag, 29. August 2011 Schriftliche Prüfung BSc Herbst 2011 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Prüfungen Analytische Chemie Montag, 29. August 2011 Schriftliche Prüfung BSc Herbst 2011 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt 36.
Schriftliche Prüfung 2. Vordiplom Frühling 2004
 Prüfungen Analytische Chemie Montag, 10. März 2004 Schriftliche Prüfung 2. Vordiplom Frühling 2004 D CAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Montag, 10. März 2004 Schriftliche Prüfung 2. Vordiplom Frühling 2004 D CAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung Analytische Chemie I&II Sommer 2014
 Schriftliche Prüfung Analytische Chemie I&II Sommer 2014 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit gut ein. Es
Schriftliche Prüfung Analytische Chemie I&II Sommer 2014 Vorname: Legi-Nr.: Name: Es sind alle Aufgaben zu lösen. Jede Aufgabe wird separat benotet. Zeit: 120 Min. Teilen Sie sich Ihre Zeit gut ein. Es
Schriftliche Prüfung 2. Vordiplom Frühling 2003
 Prüfungen Analytische Chemie Montag, 10. März 2003 Schriftliche Prüfung 2. Vordiplom Frühling 2003 D ABI/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Montag, 10. März 2003 Schriftliche Prüfung 2. Vordiplom Frühling 2003 D ABI/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Frühling 2010
 Prüfungen Analytische Chemie Donnerstag, 11. Februar 2010 Schriftliche Prüfung BSc Frühling 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Donnerstag, 11. Februar 2010 Schriftliche Prüfung BSc Frühling 2010 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIOL. Musterlösung
 Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Musterlösung Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl
Prüfungen Analytische Chemie Dienstag, 13. August 2013 Schriftliche Prüfung BSc Herbst 2013 D CHAB/BIL Musterlösung Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl
Schriftliche Prüfung BSc Sommer 2016
 Prüfungen Analytische Chemie Donnerstag, 11. August 2016 Schriftliche Prüfung BSc Sommer 2016 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Donnerstag, 11. August 2016 Schriftliche Prüfung BSc Sommer 2016 D CHAB/BIOL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL. Musterlösung. für den Teil Spektroskopie
 Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Prüfungen Analytische Chemie Montag, 3. September 2007 Schriftliche Prüfung BSc Herbst 2007 D CHAB/BIOL Musterlösung für den Teil Spektroskopie Vorname:... Name:... Jede Aufgabe wird separat bewertet.
Schriftliche Prüfung 2. Vordiplom Herbst 2003
 Prüfungen Analytische hemie Mittwoch, 1. ktober 2003 Schriftliche Prüfung 2. Vordiplom erbst 2003 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische hemie Mittwoch, 1. ktober 2003 Schriftliche Prüfung 2. Vordiplom erbst 2003 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
P105. Konstitution. Massenspektrum 100 % m/z
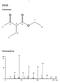 1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
1 P105 Konstitution 7 1 2 6 8 4 5 Massenspektrum 100 % 4 116 50 7 101 29 55 88 15 61 10 14 158 0 0 50 100 150 m/z 2 Direkte Fragmentierungen: 4 115 11 45 129 29 85 7 Damit lassen sich die prominenten Signale
Schriftliche Prüfung 2. Vordiplom / BSc Herbst 2004 D CHAB/BIOL. Musterlösung
 Prüfungen Analytische Chemie Dienstag, 21. September 4 Schriftliche Prüfung 2. Vordiplom / BSc erbst 4 D CAB/BIL Musterlösung Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Dienstag, 21. September 4 Schriftliche Prüfung 2. Vordiplom / BSc erbst 4 D CAB/BIL Musterlösung Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Schriftliche Prüfung BSc Winter 2016/17
 Prüfungen Analytische hemie Donnerstag, 26. Januar 2017 Schriftliche Prüfung BSc Winter 2016/17 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische hemie Donnerstag, 26. Januar 2017 Schriftliche Prüfung BSc Winter 2016/17 D AB/BIL Vorname:... ame:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
LAF-Wiederholungsklausur. Wintersemester 2011/12
 LAF-Wiederholungsklausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
LAF-Wiederholungsklausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
NMR-Spektroskopie. Magnet. Steuerung. Probenrohr Spinner. Shimspulen. B -Spulen. Gradient 2. Vorverstärker
 NMR-Spektroskopie Magnet Steuerung He He CPU Frequenz Pulsform Pulsleistung Zeitkontrolle Temperierung Gradienten Shim/Lock/Gas Vorverstärker N N Probenrohr Spinner Shimspulen B -Spulen Gradient 2 H K
NMR-Spektroskopie Magnet Steuerung He He CPU Frequenz Pulsform Pulsleistung Zeitkontrolle Temperierung Gradienten Shim/Lock/Gas Vorverstärker N N Probenrohr Spinner Shimspulen B -Spulen Gradient 2 H K
Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie
 Analytisches Physikalisches Praktikum SS 07 AAS Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie Assistent: Markus Wälle, waelle@inorg.chem.ethz.ch
Analytisches Physikalisches Praktikum SS 07 AAS Konzentrationsbestimmung von Zink, Natrium und Calcium in verschiedenen Mineralwassern mittels Atom-Absorptions-Spektroskopie Assistent: Markus Wälle, waelle@inorg.chem.ethz.ch
Schriftliche Prüfung BSc Frühling 2012
 Prüfungen Analytische Chemie Samstag, 4. Februar 2012 Schriftliche Prüfung BSc Frühling 2012 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
Prüfungen Analytische Chemie Samstag, 4. Februar 2012 Schriftliche Prüfung BSc Frühling 2012 D CHAB/BIL Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare Punktzahl beträgt
LAF-Wiederholungsklausur. Sommersemester 2011
 LAF-Wiederholungsklausur Sommersemester 2011 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 x x Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile
LAF-Wiederholungsklausur Sommersemester 2011 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 x x Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile
Klausur OC1 (BA-Studiengang) 2. Wiederholung :00 16:00 Uhr N2. Name: Punkte: Matrikel Nr. Note:
 Klausur OC1 (BA-Studiengang) 2. Wiederholung 12.04.2012 13:00 16:00 Uhr N2 PIN: Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Klausur OC1 (BA-Studiengang) 2. Wiederholung 12.04.2012 13:00 16:00 Uhr N2 PIN: Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Bereiten Sie bitte die folgenden Fragen für die Vorlesung am 03.12.2015 schriftlich vor:
 Fragenkatalog 11 Bereiten Sie bitte die folgenden Fragen für die Vorlesung am 03.12.2015 schriftlich vor: 1. Geben Sie zwei Möglichkeiten an, mit denen Sie Untergrundkompensation in der AAS betreiben können
Fragenkatalog 11 Bereiten Sie bitte die folgenden Fragen für die Vorlesung am 03.12.2015 schriftlich vor: 1. Geben Sie zwei Möglichkeiten an, mit denen Sie Untergrundkompensation in der AAS betreiben können
Übungsaufgaben - Analytik
 Übungsaufgaben - Analytik Übung 1 Von einer Substanz soll der molare Extinktionskoeffizient bestimmt werden. Der Laborant hat mässig exakt verdünnt. Er hat jeweils die auf der x-achse angegbene Zahl an
Übungsaufgaben - Analytik Übung 1 Von einer Substanz soll der molare Extinktionskoeffizient bestimmt werden. Der Laborant hat mässig exakt verdünnt. Er hat jeweils die auf der x-achse angegbene Zahl an
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
1. Klausur OC1 (BSc-Studiengang) PIN: 18.02.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
Stoffverteilungsplan Schnittpunkt Band
 Stoffverteilungsplan Schnittpunkt Band 6 978-3-12-742151-4 Schule: Lehrer: - formulieren naheliegende Fragen zu vertrauten Situationen Kompetenzbereich Argumentieren - stellen mathematische Vermutungen
Stoffverteilungsplan Schnittpunkt Band 6 978-3-12-742151-4 Schule: Lehrer: - formulieren naheliegende Fragen zu vertrauten Situationen Kompetenzbereich Argumentieren - stellen mathematische Vermutungen
Standardadditionsverfahren (Eichzusatzverfahren)
 Standardadditionsverfahren (Eichzusatzverfahren) C3CL 1. Eine Farbstofflösung besitzt bei einer Messung in einem Fotometer (Schichtdicke und Wellenlänge unbekannt) die Absorbanz von A= 0,393. Berechnen
Standardadditionsverfahren (Eichzusatzverfahren) C3CL 1. Eine Farbstofflösung besitzt bei einer Messung in einem Fotometer (Schichtdicke und Wellenlänge unbekannt) die Absorbanz von A= 0,393. Berechnen
Kombinierte Übungen zur Spektroskopie Beispiele für die Bearbeitung
 Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Im folgenden soll gezeigt werden, daß es großen Spaß macht, spektroskopische Probleme zu lösen. Es gibt kein automatisches Lösungsschema, sondern höchstens Strategien, wie beim "Puzzle Lösen"; häufig hilft
Standortbestimmung / Äquivalenzprüfung. Chemie. Mittwoch, 13. April 2016, Uhr
 Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Seite 1 von 7 Standortbestimmung / Äquivalenzprüfung Chemie Mittwoch, 13. April 2016, 16.45-18.15 Uhr Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte
Übungsaufgaben zur NMR-Spektrometrie
 Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
Übungsaufgaben NMR 33 Übungsaufgaben zur NMR-Spektrometrie Aufgabe 1 a) Wieviele unterschiedliche Orientierungen des Kernmomentes relativ zu einem externen Magnetfeld sind beim 14 N-Kern (I = 1, γ = 1.932
3. Klausur OC1 (BSc-Studiengang) PIN: LÖSUNGEN :00 14:00 Uhr N6
 3. Klausur OC1 (BSc-Studiengang) PIN: LÖSUNGEN 17.03.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
3. Klausur OC1 (BSc-Studiengang) PIN: LÖSUNGEN 17.03.2016 11:00 14:00 Uhr N6 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 2. Klausur OC1 (BA-Studiengang) PIN: 12.03.2014 13:00 16:00 Uhr N2 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
2. Klausur OC1 (BA-Studiengang) PIN: 12.03.2014 13:00 16:00 Uhr N2 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
LAF-Klausur. Wintersemester 2011/12
 LAF-Klausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden
LAF-Klausur Wintersemester 2011/12 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2017/18 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Klausur OC1 (BA-Studiengang) PIN: :00 16:00 Uhr N10. Name: Punkte: Matrikel Nr. Note:
 Klausur OC1 (BA-Studiengang) PIN: 10.02.2011 13:00 16:00 Uhr N10 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0 49-48=3.3
Klausur OC1 (BA-Studiengang) PIN: 10.02.2011 13:00 16:00 Uhr N10 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0 49-48=3.3
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17
 Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Finale (O-ho!) Dr. Christian Merten, Ruhr-Uni Bochum, WiSe 2016/17 www.ruhr-uni-bochum.de/chirality Rückblick: IR Schwingung von Atomen kann im klassischen Bild als harmonische Schwingung (harmonischer
Z 12 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN
 ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
ANALYTIK 1) BESTIMMUNG DER SUMMENFORMEL: a. AUS DEN MASSENPROZENTEN Ziel: Ermittlung einer Summenformel einer Substanz aus C, und O wenn die Massenprozent der Elemente und die Molmasse M r der Substanz
LAF-Klausur. Sommersemester 2012
 LAF-Klausur Sommersemester 2012 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden
LAF-Klausur Sommersemester 2012 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden
Prüfung zur Vorlesung Mathematik I/II
 Dr. A. Caspar ETH Zürich, August 08 D-BIOL, D-CHAB, D-HEST Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle 3 4 5 Total Vollständigkeit
Dr. A. Caspar ETH Zürich, August 08 D-BIOL, D-CHAB, D-HEST Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle 3 4 5 Total Vollständigkeit
UNIVERSITÄT DUISBURG-ESSEN
 Termin: Musterklausur SS 2011 Prüfungsfach: Makroökonomik I Prüfer: Prof. Dr. Belke Name, Vorname Studiengang MUSTERKLAUSUR MAKROÖKONOMIK I Hinweise zur Bearbeitung der Klausur Seite 1 Bearbeitungszeit:
Termin: Musterklausur SS 2011 Prüfungsfach: Makroökonomik I Prüfer: Prof. Dr. Belke Name, Vorname Studiengang MUSTERKLAUSUR MAKROÖKONOMIK I Hinweise zur Bearbeitung der Klausur Seite 1 Bearbeitungszeit:
!!! Du darfst eine Teilaufgabe von Nr. 2 und zwei der Teilaufgaben von Nr 4 streichen!!!
 1 Klassenarbeit Chemie 1/5 A TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz! In der Tabelle links stehende Elemente haben eher die maximale Wertigkeit! In der Tabelle rechts stehende Elemente
1 Klassenarbeit Chemie 1/5 A TIPP alle Rechenaufgaben mit Einheit, Ergebnis und Antwortsatz! In der Tabelle links stehende Elemente haben eher die maximale Wertigkeit! In der Tabelle rechts stehende Elemente
FernUniversität in Hagen September 2018 Fakultät für Wirtschaftswissenschaft
 FernUniversität in Hagen September 2018 Fakultät für Wirtschaftswissenschaft Bitte beachten Sie, dass auf den Notenbescheiden des Prüfungsamtes nicht die in der Klausur erreichte Punktzahl, sondern die
FernUniversität in Hagen September 2018 Fakultät für Wirtschaftswissenschaft Bitte beachten Sie, dass auf den Notenbescheiden des Prüfungsamtes nicht die in der Klausur erreichte Punktzahl, sondern die
Fachprüfung AI / TI / MI Mathematik 1 Prof. Dr. Wolfgang Konen, Dr. A. Schmitter FH Köln, Institut für Informatik
 Fachprüfung AI / TI / MI Mathematik 1 Name: Vorname: Matr.-Nr.: Unterschrift: Klausurdauer: 60 min. Hilfsmittel: Formelsammlung Mathematik Rezepte Mathe 1+2 nicht-grafikfähiger Taschenrechner Hinweise:
Fachprüfung AI / TI / MI Mathematik 1 Name: Vorname: Matr.-Nr.: Unterschrift: Klausurdauer: 60 min. Hilfsmittel: Formelsammlung Mathematik Rezepte Mathe 1+2 nicht-grafikfähiger Taschenrechner Hinweise:
NMR-Spektroskopie Teil 2
 BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
BC 3.4 : Analytische Chemie I NMR Teil 2 NMR-Spektroskopie Teil 2 Stefanie Wolfram Stefanie.Wolfram.1@uni-jena.de Raum 228, TO Vom Spektrum zur Struktur 50000 40000 Peaks u. Integrale 30000 Chemische Verschiebung
M U S T E R L Ö S U N G
 Prof. Dr.. eiser Prof. Dr. A. Geyer achholklausur zur 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2002 am Freitag, dem 2. August 2002 ame:...vorname:...
Prof. Dr.. eiser Prof. Dr. A. Geyer achholklausur zur 3. Klausur zum Praktikum rganische Chemie I für Studierende der Chemie und der Biochemie im SS 2002 am Freitag, dem 2. August 2002 ame:...vorname:...
Spektroskopie-Seminar SS NMR-Spektroskopie. H-NMR-Spektroskopie. nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie
 1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
1 H-NMR-Spektroskopie nuclear magnetic resonance spectroscopy- Kernmagnetresonanzspektroskopie 5.1 1 H-NMR-Spektroskopie NMR-Spektrum liefert folgende Informationen: Chemische Verschiebung d (in ppm):
Klausur zur Vorlesung Grundlagen der Wirtschaftspolitik Wiederholungstermin Wintersemester 2013/2014
 Prof. Dr. Andreas Freytag Klausur zur Vorlesung Grundlagen der Wirtschaftspolitik Wiederholungstermin Wintersemester 2013/2014... Vorname:... Matrikel-Nr.:... Studiengang:... (B.Sc. WiWi, NF WiWi, LA JM)
Prof. Dr. Andreas Freytag Klausur zur Vorlesung Grundlagen der Wirtschaftspolitik Wiederholungstermin Wintersemester 2013/2014... Vorname:... Matrikel-Nr.:... Studiengang:... (B.Sc. WiWi, NF WiWi, LA JM)
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2014/15vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2014/15vom 19.09.2014 A1 A2 A3 A4 A5 Note 10 10 10 10 10 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2014/15vom 19.09.2014 A1 A2 A3 A4 A5 Note 10 10 10 10 10 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Studiengang Bsc Biowissenschaften. Modulabschluss Prüfung. Organische Chemie
 Studiengang Bsc Biowissenschaften Modulabschluss Prüfung rganische Chemie 04.10.2016 Name: Vorname: Matrikelnummer: Geboren am: in: Dauer der Klausur: 90 Minuten Wiederholer/in dieser Klausur: Ja Nein
Studiengang Bsc Biowissenschaften Modulabschluss Prüfung rganische Chemie 04.10.2016 Name: Vorname: Matrikelnummer: Geboren am: in: Dauer der Klausur: 90 Minuten Wiederholer/in dieser Klausur: Ja Nein
Atomabsorptionsspektrometrie (AAS)
 Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Atomabsorptionsspektrometrie (AAS) Zusammenfassung Mit Hilfe eines Atomabsorptionsspektrometers wurden die Konzentrationen von Arsen und Lithium in drei verschieden Mineralwässern bestimmt. Resultate Konzentrationen
Prüfung zur Vorlesung Mathematik I/II
 Prof. Dr. E. W. Farkas ETH Zürich, Februar 014 BIOL-B HST PHARM Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle MC Total MC Total
Prof. Dr. E. W. Farkas ETH Zürich, Februar 014 BIOL-B HST PHARM Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle MC Total MC Total
LAF-Wiederholungsklausur. Sommersemester 2012
 LAF-Wiederholungsklausur Sommersemester 2012 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
LAF-Wiederholungsklausur Sommersemester 2012 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
LAF-Klausur. Sommersemester 2011
 LAF-Klausur Sommersemester 2011 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 x x Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden nicht
LAF-Klausur Sommersemester 2011 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 x x Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene Teile werden nicht
Übungsaufgaben NMR-Spektroskopie (1)
 Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Übungsaufgaben NMR-Spektroskopie (1) 1. Kerne haben drei wichtige Eigenschaften: Masse m, Ladung Q und Eigendrehimpuls p. Kernsorte Spin natürliche Häufigkeit Gyromagnet. Verhältnis γ [Tsec] 1 1 H 1/2
Klausur im Lehrgebiet. Signale und Systeme. - Prof. Dr.-Ing. Thomas Sikora - Name:... Bachelor ET Master TI Vorname:... Diplom KW Magister...
 Signale und Systeme - Prof. Dr.-Ing. Thomas Sikora - Name:............................ Bachelor ET Master TI Vorname:......................... Diplom KW Magister.............. Matr.Nr:..........................
Signale und Systeme - Prof. Dr.-Ing. Thomas Sikora - Name:............................ Bachelor ET Master TI Vorname:......................... Diplom KW Magister.............. Matr.Nr:..........................
FernUniversität in Hagen September 2016 Fakultät für Wirtschaftswissenschaft
 FernUniversität in Hagen September 2016 Fakultät für Wirtschaftswissenschaft Bitte beachten Sie, dass auf den Notenbescheiden des Prüfungsamtes nicht die in der Klausur erreichte Punktzahl, sondern die
FernUniversität in Hagen September 2016 Fakultät für Wirtschaftswissenschaft Bitte beachten Sie, dass auf den Notenbescheiden des Prüfungsamtes nicht die in der Klausur erreichte Punktzahl, sondern die
Elektrischer Schwingkreis
 Fakultät für Technik Bereich Informationstechnik Elektrischer Schwingkreis Name 1: Name 2: Name 3: Gruppe: Datum: 2 1 Allgemeines Im Versuch Mechanischer Schwingkreis haben Sie einen mechanischen Schwingkreis
Fakultät für Technik Bereich Informationstechnik Elektrischer Schwingkreis Name 1: Name 2: Name 3: Gruppe: Datum: 2 1 Allgemeines Im Versuch Mechanischer Schwingkreis haben Sie einen mechanischen Schwingkreis
Schriftliche Prüfung 2. Vordiplom / BSc Frühling 2005 D CHAB/BIOL. Musterlösung
 Prüfungen Analytische Chemie Dienstag, 1. März 2005 Schriftliche Prüfung 2. Vordiplom / BSc Frühling 2005 D CHAB/BIL Musterlösung Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
Prüfungen Analytische Chemie Dienstag, 1. März 2005 Schriftliche Prüfung 2. Vordiplom / BSc Frühling 2005 D CHAB/BIL Musterlösung Vorname:... Name:... Jede Aufgabe wird separat bewertet. Die maximal erreichbare
FernUniversität in Hagen März 2017 Fakultät für Wirtschaftswissenschaft
 FernUniversität in Hagen März 2017 Fakultät für Wirtschaftswissenschaft Bitte beachten Sie, dass auf den Notenbescheiden des Prüfungsamtes nicht die in der Klausur erreichte Punktzahl, sondern die erreichte
FernUniversität in Hagen März 2017 Fakultät für Wirtschaftswissenschaft Bitte beachten Sie, dass auf den Notenbescheiden des Prüfungsamtes nicht die in der Klausur erreichte Punktzahl, sondern die erreichte
Prüfung zur Vorlesung Mathematik I/II
 Dr. A. Caspar ETH Zürich, August BIOL-B GES+T PHARM Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle MC Total MC Total 3 4 5 6 -
Dr. A. Caspar ETH Zürich, August BIOL-B GES+T PHARM Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle MC Total MC Total 3 4 5 6 -
LAF-Wiederholungsklausur. Wintersemester 2012/13
 LAF-Wiederholungsklausur Wintersemester 2012/13 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
LAF-Wiederholungsklausur Wintersemester 2012/13 Name/Vorname:... Matrikelnummer:... Geburtsdatum:... A1 A2 A3 A4 A5 A6 A7 A8 A9 A10 A11 X X X X Schreiben Sie bitte gut leserlich! Mit Bleistift geschriebene
Klausur Mikroökonomik
 Klausur Mikroökonomik Klausurtermin: 13.10.2017 Dieses Deckblatt bitte vollständig und deutlich lesbar ausfüllen! Vom Prüfer Vom Prüfer Name: auszufüllen: auszufüllen: Aufg.1: / 25 Vorname: Punkte: Aufg.2:
Klausur Mikroökonomik Klausurtermin: 13.10.2017 Dieses Deckblatt bitte vollständig und deutlich lesbar ausfüllen! Vom Prüfer Vom Prüfer Name: auszufüllen: auszufüllen: Aufg.1: / 25 Vorname: Punkte: Aufg.2:
Schreiben Sie Ihre ö AUSSCHLIEßLICH!!! auf. die leeren Seiten 5 8!
 1. Ermitteln Sie die Konstitution der Verbindung aus MQ, Protonen und protonenbreitbandentkoppeltem Kohlenstoffspektrum. a. Ermitteln Sie alle chemischen Verschiebungen ( 1 und 13 ) und Kopplungskonstanten
1. Ermitteln Sie die Konstitution der Verbindung aus MQ, Protonen und protonenbreitbandentkoppeltem Kohlenstoffspektrum. a. Ermitteln Sie alle chemischen Verschiebungen ( 1 und 13 ) und Kopplungskonstanten
Übungen zur Spektroskopie 2
 Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
Übungen zur Spektroskopie 2 C. Dubler und Dr. D. S. Stephenson Department Chemie, Universität München Sie finden diese Übungen und alte Klausuren (mit Lösung) auf unserer Homepage: http://cicum200.cup.unimuenchen.de/intranet/depch/analytik/nmr_f/index.php
2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom
 2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom 02.02.2011 A1 A2 A3 F1 F2 R1 R2 E1 Σ Note 8 7 10 4 5 3 6 7 NAME/VORNAME:... Matrikelnummer:... Schreiben Sie bitte gut leserlich: Name und
2. Teilklausur zum Chemischen Grundpraktikum im WS 2010/11 vom 02.02.2011 A1 A2 A3 F1 F2 R1 R2 E1 Σ Note 8 7 10 4 5 3 6 7 NAME/VORNAME:... Matrikelnummer:... Schreiben Sie bitte gut leserlich: Name und
1. Standortbestimmung, Januar Chemie. Eine gedruckte und/oder eine persönlich erstellte und vom Dozenten visierte Formelsammlung,
 1. Standortbestimmung, Januar 2015 Chemie Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte und vom Dozenten visierte Formelsammlung, Ein netzunabhängiger,
1. Standortbestimmung, Januar 2015 Chemie Dauer der Prüfung: 90 Minuten Erlaubte Hilfsmittel: Eine gedruckte und/oder eine persönlich erstellte und vom Dozenten visierte Formelsammlung, Ein netzunabhängiger,
LMPG 3, Spek-ÜB-20 LÖSUNG Seite 1 von 6
 LMPG 3, Spek-ÜB-20 LÖSUG Seite 1 von 6 Aufgabe 1: a) Woran lässt sich aus dem MS-Spektrum auf die Zahl der -Atome schliessen? Molekülionenpeak ist ungerade, also ist auch die Zahl der -Atome ungerade.
LMPG 3, Spek-ÜB-20 LÖSUG Seite 1 von 6 Aufgabe 1: a) Woran lässt sich aus dem MS-Spektrum auf die Zahl der -Atome schliessen? Molekülionenpeak ist ungerade, also ist auch die Zahl der -Atome ungerade.
Modulabschlussprüfung Chemie für LA-Biologen (o. HF Chemie)
 Modulabschlussprüfung Chemie für LA-Biologen (o. HF Chemie) Nachklausur 18.03.2016 Zeit: 120 min Seite 1 Seite 2 Seite 3 Seite 4 Seite 5 Seite 6 Seite 7 / 18 / 18 / 10 / 10 / 19 / 15 / 10 Gesamt: Note:
Modulabschlussprüfung Chemie für LA-Biologen (o. HF Chemie) Nachklausur 18.03.2016 Zeit: 120 min Seite 1 Seite 2 Seite 3 Seite 4 Seite 5 Seite 6 Seite 7 / 18 / 18 / 10 / 10 / 19 / 15 / 10 Gesamt: Note:
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie)
 Übungen 24.01.2012 Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Aufgabe 1.1 Zeichnen Sie die Strukturformeln der folgenden Verbindungen (jeweils 1 Punkt pro Teilaufgabe).
Übungen 24.01.2012 Teil 1 Aufgaben zum Stoff der Vorlesung C1a (Grundvorlesung rganische Chemie) Aufgabe 1.1 Zeichnen Sie die Strukturformeln der folgenden Verbindungen (jeweils 1 Punkt pro Teilaufgabe).
Prüfung zur Vorlesung Mathematik I/II
 Prof. W. Farkas ETH Zürich, Februar 2018 D-BIOL, D-CHAB, D-HEST Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle 1 2 3 4 5 6 Total
Prof. W. Farkas ETH Zürich, Februar 2018 D-BIOL, D-CHAB, D-HEST Prüfung zur Vorlesung Mathematik I/II Bitte ausfüllen! Name: Vorname: Legi-Nr.: Nicht ausfüllen! Aufgabe Punkte Kontrolle 1 2 3 4 5 6 Total
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie
 1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
1. Klausur Allgemeine und Anorganische Chemie B.Sc. Chemie Name: Vorname: Matrikel Nr.: 15.12.2010 Die Durchführung und Auswertung der 12 Aufgaben im zweiten Teil dieser Klausur mit je vier Aussagen (a-d)
Abiturprüfung Physik, Grundkurs
 Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
Seite 1 von 6 Abiturprüfung 2010 Physik, Grundkurs Aufgabenstellung: Aufgabe: Energieniveaus im Quecksilberatom Das Bohr sche Atommodell war für die Entwicklung der Vorstellung über Atome von großer Bedeutung.
F E R N U N I V E R S I T Ä T I N H A G E N
 F E R N U N I V E R S I T Ä T I N H A G E N Matrikelnummer FAKULTÄT FÜR WIRTSCHAFTSWISSENSCHAFT Name: Vorname: MODULKLAUSUR: TERMIN: 03.09.2018 PRÜFER: Aufgabe 1 2 3 maximale Punktzahl 20 40 40 100 erreichte
F E R N U N I V E R S I T Ä T I N H A G E N Matrikelnummer FAKULTÄT FÜR WIRTSCHAFTSWISSENSCHAFT Name: Vorname: MODULKLAUSUR: TERMIN: 03.09.2018 PRÜFER: Aufgabe 1 2 3 maximale Punktzahl 20 40 40 100 erreichte
Klausur zur Vorlesung VWL II Makroökonomie (SoSe 15)
 Klausur zur Vorlesung VWL II Makroökonomie (SoSe 15) (Prof. Dr. Jochen Michaelis) Persönliche Angaben Vorname: Nachname: Matrikel-Nr.: Studiengang: Punkteverteilung Aufgabe 1 2 3 Punkte /20 /20 /20 Gesamtpunktzahl
Klausur zur Vorlesung VWL II Makroökonomie (SoSe 15) (Prof. Dr. Jochen Michaelis) Persönliche Angaben Vorname: Nachname: Matrikel-Nr.: Studiengang: Punkteverteilung Aufgabe 1 2 3 Punkte /20 /20 /20 Gesamtpunktzahl
Teil 1 Aufgaben zum Stoff der Vorlesung OC1a (Grundvorlesung Organische Chemie) Maximale Punktezahl: 20 Notwendige Mindestpunkte: 8
 2. Klausur OC1 (BA-Studiengang) PIN: 11.03.2015 11:00 14:00 Uhr N5 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
2. Klausur OC1 (BA-Studiengang) PIN: 11.03.2015 11:00 14:00 Uhr N5 Name: Punkte: Matrikel Nr. Note: Notenskala: 80-78=1.0 77-75=1.3 74-71=1.5 70-67=1.7 66-63=2.0 62-59=2.3 58-56=2.5 55-53=2.7 52-50=3.0
Klausur im Lehrgebiet. Signale und Systeme. - Prof. Dr.-Ing. Thomas Sikora -
 Signale und Systeme - Prof. Dr.-Ing. Thomas Sikora - Name:............................ Bachelor ET Master TI Vorname:......................... Diplom KW Magister... Matr.Nr:.......................... Erasmus
Signale und Systeme - Prof. Dr.-Ing. Thomas Sikora - Name:............................ Bachelor ET Master TI Vorname:......................... Diplom KW Magister... Matr.Nr:.......................... Erasmus
SoSe 2015 Klausur zur LV 36654: Einführung in 28. Juli 2015 die Methoden empirischer Forschung. Name: Studiengang: B.A. M.A.
 Name: Studiengang: B.A. M.A. Vorname: Studienfächer: Matrikelnummer: Fachsemester: Allgemeine Hinweise: 1. Überprüfen Sie bitte, ob Sie alle Seiten der Klausurangabe vollständig erhalten haben (Gesamtzahl:
Name: Studiengang: B.A. M.A. Vorname: Studienfächer: Matrikelnummer: Fachsemester: Allgemeine Hinweise: 1. Überprüfen Sie bitte, ob Sie alle Seiten der Klausurangabe vollständig erhalten haben (Gesamtzahl:
Mögliche Punktzahl: 100 Gesamtpunkte aus Teil 1 und 2: Erreichte Punktzahl: Prozentsatz aus Teil 1 und 2:
 Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch. Thienel Bachelorprüfung Prüfungsfach: Geologie, Werkstoffe und Bauchemie am: 28.03.2014
Fakultät für Bauingenieurwesen und Umweltwissenschaften Institut für Werkstoffe des Bauwesens Univ.-Prof. Dr.-Ing. K.-Ch. Thienel Bachelorprüfung Prüfungsfach: Geologie, Werkstoffe und Bauchemie am: 28.03.2014
