Essigherstellung. Fach Klasse Überthema Feinthema Zeit. Bei dem Versuch wird aus Weißwein durch Oxidation an der Luft Essig hergestellt.
|
|
|
- Eva Bachmeier
- vor 7 Jahren
- Abrufe
Transkript
1 V2 Essigherstellung Fach Klasse Überthema Feinthema Zeit Chemie E2 Alkanole xidationsprodukte der Alkanole 5 Tage Zusammenfassung Bei dem Versuch wird aus Weißwein durch xidation an der Luft Essig hergestellt. Einordnung in den Unterricht 1 Der Versuch ist nach dem hessischen Lehrplan G8 der Einführungsphase E2 zuzuordnen. Dort lässt er sich zum verbindlichen Unterrichtsinhalt Alkanole zum Thema c) xidationsprodukte der Alkanole anbringen. 2 Da der Versuch thematisch einen Übergang zwischen Alkanolen und Carbonsäuren schafft, sollte er am Ende der Alkanole stehen. Die SuS wären zu diesem Zeitpunkt mit der Hydroxy-Gruppe vertraut. Auch der Begriff der Redoxreaktion ist ihnen aus der anorganischen Chemie bereits bekannt. Die Übertragung auf organische Verbindungen kann mithilfe des Versuchs geschaffen werden. Auch wird die Carboxy-Gruppe vorgestellt und der Zusammenhang zu den Alkanolen und Carbonylen geschaffen. Dadurch, dass bei dem Versuch ein Alltagsprodukt hergestellt wird, dass mit Sicherheit alle schon einmal gekostet haben, wird das Interesse geweckt und ein Realitätsbezug hergestellt. 1 Vgl. Hirt, A.: Lehrplan Chemie (2010). 2 Vgl. Hirt, A.: Lehrplan Chemie (2010).
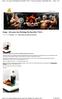
2 Der Versuch Die Durchführung 3 Abbildung 1: Links: Versuchsaufbau zur Herstellung von Essig. Rechts: Der Rotkohlindikator. Drei Gläser und ein Einmachglas werden mit kochendem Wasser ausgespült. Ein günstiger Weißwein wird geöffnet und auf die Gefäße aufgeteilt. Nun werden zu einem der mit Wein gefüllten Gläser 5 Teelöffel Wasser gegeben. Bei einem anderen Glas werden Stücke eines Korkens auf der Weinoberfläche platziert. Nun werden die Gläser beschriftet und der Deckel auf das Einmachglas geschraubt. Die Gefäße werden an einen rt gestellt, an dem sie nicht stören, und einige Tage stehen gelassen. Jeden Tag wird durch Riechen an den Gefäßen überprüft, ob schon Essig entstanden ist. Sobald der charakteristische Geruch wahrnehmbar ist, wird der ph-wert mithilfe des Rotkohlindikators getestet. Dafür wird ein Glas Rotkohl geöffnet und der darin enthaltene Rotkohlsaft in ein Glas gegossen, sodass dieses bis zur Hälfte gefüllt ist. Anschließend wird mit Leitungswasser im Verhältnis 2 (Rotkohlsaft):1 (Leitungswasser) verdünnt und umgerührt. Danach werden 5 Schnappdeckelgläschen bis zur Hälfte mit dem verdünnten Rotkohlsaft gefüllt und dann mit jeweils einer der 4 hergestellten Essig-Proben bis oben hin aufgefüllt. In das fünfte Schnappdeckelgläschen wird zum Vergleich mit Essigessenz aufgefüllt. Nehmen die vier Proben die gleiche Färbung an, wie die mit Essigessenz, besitzen sie ebenfalls einen sauren ph-wert. Die Probe im Marmeladenglas wird weitere drei Wochen stehen gelassen und dann erneut mit dem Rotkohlindikator getestet. 3 Vgl. Friedrich-Schiller-Universität Jena: Lernzirkel Carbonsäuren, für Klasse 9 Thüringen, Regelschule und Gymnasium. URL: S. 2. Letzter Zugriff am:
3 Die Beobachtung Am dritten Tag ist eine weißliche trübe Schicht auf den Proben entstanden. Diese ist bei der Probe mit Wasser am stärksten ausgeprägt. Abbildung 2: Ergebnis der Herstellung von Essig nach vier Tagen. Wird an den Proben gerochen, so ist der Essiggeruch am vierten Tag deutlich wahrnehmbar. Auch der Rotkohlindikator zeigt durch seine Verfärbung ins Rote an, dass Essigsäure entstanden ist. Bei allen Proben ist anscheinend Essig entstanden, wobei die Probe, die nur Wein enthielt, am wenigsten verschmutzt und am wenigsten getrübt ist. Auch die Probe im Einmachglas weist Säure auf, allerdings ist kein wirklicher Geruch nach Essig festzustellen und der Geschmack ähnelt eher dem von Wein. Abbildung 3: Ergebnis des Rotkohlindikatortests.
4 Abbildung 4: Vergleichsprobe von Essigessenz mit Rotkohlindikator. Wird die Essigprobe im Marmeladenglas noch weitere drei Wochen stehen gelassen, so ändert sich die Farbe stark und es ist der Geruch von Essig wahrnehmbar. Wird der Indikatortest wiederholt zeigt sich, dass sich die Probe im Marmeladenglas rot färbt und im Vergleich zu Essig einen ähnlichen Rotton annimmt, die Weinprobe hingegen eher dem Farbton der neutralen Rotkohllösung entspricht. Abbildung 5: Links: Die Essigprobe im Marmeladenglas nach weiteren drei Wochen im Vergleich zum ursprünglichen Weißwein. Rechts: Erneute Prüfung mit dem Rotkohlindikator: von links nach rechts: Rotkohlindikator als Vergleichsprobe, Weißwein mit Rotkohlsaft, Essig aus dem Marmeladenglas mit Rotkohlsaft und Essigessenz mit Rotkohlsaft als Vergleichsprobe. Entsorgung Alle flüssigen Abfälle können in den Abfluss und alle festen in den Hausmüll entsorgt werden.
5 Fachlicher Hintergrund Bei dem Versuch entsteht durch Luftoxidation aus Weißwein Essig. Dies konnte bei allen Proben durch den Indikatortest bestätigt werden. Selbst im Marmeladenglas findet die xidation von Alkohol zur Carbonsäure statt, was zeigt, dass ein geringes Volumen an Luft für die Reaktion ausreicht. Insgesamt stellt die Variante im Marmeladenglas zwar die zeitaufwendigste Methode zur Essigherstellung dar, jedoch konnte dabei die am wenigsten verunreinigte Essigprobe erhalten werden. Alltäglich wird Essig zum Kochen oder Anrichten von Salaten verwendet. Was ist Essig eigentlich und wie wird er hergestellt? Als Essig werden stark verdünnte wässrige Lösungen von Ethansäure (Essigsäure) bezeichnet. Es gibt viele verschiedene Essigsorten, die sich in ihrer Herstellung und in ihren Ausgangssubstanzen unterscheiden. Fehler! Kein Text mit angegebener Formatvorlage im Dokument.-1: Übersicht über die verschiedenen Essigsorten und deren Ausgangsprodukte 4,5 Handelsform Weinessig bstessig Branntweinessig Kräuteressig Reisessig Gemüseessig Syntheseessig Ausgangsprodukte Aus Wein hergestellt Aus verschiedenen Früchten hergestellt Aus Agraralkohol, der aus landwirtschaftlichen Produkten wie Getreide und Kartoffeln hergestellt wird. Aus Weinessig mit Zusatz von Kräutern Aus Reis bzw. Reiswein Aus verschiedenen Gemüsesorten wie z.b. Rote Beete Aus synthetischer Essigsäure 4 Vgl. Asselborn, W., Jäckel M., Risch K.: Chemie heute S1 Gesamtband. Braunschweig S Vgl. Fischerauer. ALLES UM DEN ESSIG. In: Fischerauer- Alles um den Essig. URL: Letzter Zugriff:
6 Zur Produktion von Essig haben sich verschiedene Methoden etabliert. Das historisch älteste Verfahren ist das berflächenverfahren oder rleans-verfahren, das schon seit dem Mittelalter zur Bereitung von Essig verwendet wird. Dabei wird alkoholhaltige Flüssigkeit in Holzfässer gefüllt. Aus der Luft lagern sich mit der Zeit Essigsäurebakterien an, sodass sich die sogenannte Essigmutter auf der berfläche bildet. Diese Bakterien wandeln enzymatisch den Alkohol in Essig um. Der entstandene Essig wird abgeschöpft und durch neuen Alkohol ersetzt. 6 Industriell bedeutsamer ist das Schnellessigverfahren oder Spanbildner-Verfahren, das zur Herstellung von gewöhnlichem Speiseessig verwendet wird. Dabei wird als alkoholische Ausgangslösung häufig der aus Kartoffeln erhaltene Kartoffelsprit verwendet. Dieser wird mit etwas Malzextrakt und fertigem Essig vermischt und auf Rotbuchenholzhobelspäne, die sich aufgeschüttet in einem Behälter befinden, gegossen. Auf den Buchenholzhobelspänen lagern sich die Essigsäurebakterien an. Die alkoholische Lösung sickert nun langsam durch die Schichten der Buchenholzspäne, die noch zusätzlich von unten belüftet werden. Dabei wird der im Kartoffelsprit enthaltene Ethanol durch die Bakterien zu Essig umgesetzt und fließt am Boden des Behälters über den sogenannten Schwanenhals, ein gewinkeltes Röhrchen, ab. 7 Abbildung 6: Darstellung des Schnellessigverfahren. 8 6 Vgl. Fischkandl, V.: Wie entsteht Essig. In: Vom Fass Wien. URL: Letzter Zugriff Vgl. Wollrab, A.: rganische Chemie Eine Einführung für Lehramts- und Nebenfachstudenten. 3., ergänzte Auflage. Heidelberg S Wollrab, A.: rganische Chemie Eine Einführung für Lehramts- und Nebenfachstudenten. 3., ergänzte Auflage. Heidelberg S. 560.
7 Das modernste Verfahren zur Gewinnung von Essig ist das Submersverfahren oder Acetator-Verfahren. Hierbei wird direkt in den alkoholischen Rohstoff, der sich in einem großen Tank befindet, Sauerstoff gepumpt und so die Essigsäurebakterien aus der Luft in der Schwebe gehalten. Dieses Verfahren ist sehr effizient, sodass eine Tagesproduktion von mehreren tausend Litern möglich ist. 9 Wird der Essig aus zucker- oder alkoholhaltigen Lösungen als xidations- oder Gärungsprodukt gewonnen, so handelt es sich meist um einen teuren, gut schmeckenden Essig. Wird er durch einfaches Verdünnen von Ethansäure hergestellt, so handelt es sich eher um einen preislich günstigen Essig. 10 Dies ist der Fall bei der im Supermarkt erhältlichen Essigessenz, die einen Ethansäuregehalt von 25 % aufweist und bei vierfacher Verdünnung als Tafelessig verwendet wird. 11 Die Ethansäure und ihr Anhydrid sind in der Industrie als Grundstoffe von großer Bedeutung für die Produktion von Pharmaka, Farbstoffen, Pestiziden und Polymeren. Die großtechnische Produktion erfolgt über drei wichtige Verfahren: die Ethen- xidation über Acetaldehyd, die Luftoxidation von Butan und die Carbonylierung von Methanol. Alle diese Syntheseverfahren folgen komplexen Mechanismen. 12 xidation von Ethen: 2, H 2, PdCl 2 /CuCl 2 -Katalyse 2, Co 3+ -Katalyse H 2 C CH 2 H H Wacker-Verfahren Ethen Ethanol Ethansäure xidation von Butan: 9 Vgl. Fischkandl, V.: Wie entsteht Essig. URL: Letzter Zugriff am: Vgl. Fischerauer, A.: ALLES UM DEN ESSIG. URL: Was+ist+Essig.html. Letzter Zugriff am: Vgl. Wollrab, A.: rganische Chemie. S Vgl. Butenschön, H. (Hrsg. Der Übersetzungsauflage): Vollhardt, K.P.C., Schore, N.P.: rganische Chemie. 4. Auflage. Weinheim S. 978f.
8 , Co Katalyse, kpa, 180 C 2 Butan H Ethansäure Carbonylierung von Methanol: H Methanol C, Rh 3+ -Katalyse, I 2, kpa, 180 C Monsanto-Verfahren H Ethansäure
9 Nach einiger Zeit entsteht aus Weißwein Essig! Stelle eine Vermutung darüber auf, wie es dazu kommt! Carbonsäuren können durch xidation primärer Alkohole zu Aldehyden und anschließender Weiteroxidation dargestellt werden. Auf sehr einfache Weise entsteht Essig durch enzymatische xidation, wenn Wein an Luft stehen gelassen wird. Schon in der Antike wurde Essig als Erfrischungsgetränk, zur Säuerung und zur Konservierung von Lebensmitteln verwendet. Es war bekannt, dass zur Herstellung Luft, Alkohol und Essigsäurebakterien 13 benötigt werden. Die Essigsäurebakterien können nur im sauerstoffreichen Milieu Ethanol zu Ethansäure umsetzen. Die xidation von Ethanol erfolgt mithilfe der in Acetobacter enthaltenen Alkohol-Dehydrogenase (ADH) und Aldehyd-Dehydrogenase (ALDH). Im ersten Schritt erfolgt die xidation von Ethanol zu Ethanal durch Luftsauerstoff: H ADH 2 + 2(g) H 2 H H H Ethanol Ethanal Anschließend wird Ethanal zu Ethansäure weiteroxidiert: ALDH 2 + 2(g) 2 H H Ethanal Ethansäure Ist am Ende kein Ethanol mehr vorhanden, so wird Essigsäure zu C2 oxidiert. 14,15 Was macht Essig sauer? 13 Systematik: Klassifikation: Lebewesen, Domäne: Bakterien, Abteilung: Proteobacteria, Klasse: Alphaproteobacteria, rdnung: Rhodospirillales, Familie: Acetobacteraceae 14 Vgl. Conatex-Didactic Lehrmittel GmbH: rganische Chemie: Einführung der einfachen Carbonsäuren über die Essigsäure. In: Conatex Didactic Versuchsanleitung. URL: Letzter Zugriff am Vgl. Schmid, R.: Taschenbuch der Biotechnologie und Gentechnik. 2. Auflage. Weinheim S
10 Die in der Ethansäure enthaltene Carboxy-Gruppe erklärt deren sauren Charakter. Denn obwohl das saure Wasserstoffatom wie bei den Alkoholen der Hydroxy-gruppe entstammt, weisen Carbonsäuren wesentlich niedrigere pks-werte auf als Alkohole. Dies liegt daran, dass das Carboxy-Kohlenstoffatom positiv polarisiert ist und dadurch einen elektronenziehenden Effekt auf die benachbarten Gruppen ausübt. Das Wasserstoffatom kann somit leichter abgespalten werden. H3C H basisch sauer Carboxylgruppe Überdies wird das dabei entstehende Carboxylat-Ion durch mögliche Resonanzstrukturen stabilisiert. C H 3 H + - H C H H 3 C pk s = 4,75 gleichwertige Resonsanzformeln Im Gegensatz zu den Enolat-Ionen sind die Resonanzformeln der Carboxylat-Ionen gleichwertig. Dies bedeutet, dass die Carboxylate symmetrisch gebaut sind. Die Kohlenstoff-Sauerstoff-Bindungslängen liegen zwischen denen einer Kohlenstoff- Sauerstoff-Einfach- und Kohlenstoff-Sauerstoff-Doppelbindung Vgl. Vollhardt, K.P.C., Schore, N.P.: rganische Chemie. S
Die Indigotinbottle. Zusammenfassung. Einordnung in den Unterricht 1
 V22 Die Indigotinbottle Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 20 Minuten Zusammenfassung Bei dem Versuch wird ein Redoxsystem erzeugt, dass seine Farbe ändert, je nachdem
V22 Die Indigotinbottle Fach Klasse Überthema Feinthema Zeit Chemie Q4 Farbstoffe Redoxindikator 20 Minuten Zusammenfassung Bei dem Versuch wird ein Redoxsystem erzeugt, dass seine Farbe ändert, je nachdem
Herstellung von Kunsthonig
 V8 erstellung von Kunsthonig Fach Klasse Überthema Feinthema Zeit Chemie Q2 Kohlenhydrate Mono- und Disaccharide 90 Minuten Zusammenfassung Bei dem Versuch wird Saccharose durch Säurehydrolyse in seine
V8 erstellung von Kunsthonig Fach Klasse Überthema Feinthema Zeit Chemie Q2 Kohlenhydrate Mono- und Disaccharide 90 Minuten Zusammenfassung Bei dem Versuch wird Saccharose durch Säurehydrolyse in seine
Reinigen mit Zitronensäure
 V4 Reinigen mit Zitronensäure Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Zitronensäure 30 Minuten Zusammenfassung: Beim dem Versuch werden zitronenhaltige Lösungen zum
V4 Reinigen mit Zitronensäure Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Zitronensäure 30 Minuten Zusammenfassung: Beim dem Versuch werden zitronenhaltige Lösungen zum
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
Essig Ist sauer das Richtige für Sportler? Teil 1
 Page 1 of 5 Suchbegriff hier eingeben Essig Ist sauer das Richtige für Sportler? Teil 1 10. Juni 2013 Von Holger Gugg Kategorie: Aktuelles, Blogger: Holger Gugg, Diät, Sportnahrung 2 Liebe BLOG-Leserinnen
Page 1 of 5 Suchbegriff hier eingeben Essig Ist sauer das Richtige für Sportler? Teil 1 10. Juni 2013 Von Holger Gugg Kategorie: Aktuelles, Blogger: Holger Gugg, Diät, Sportnahrung 2 Liebe BLOG-Leserinnen
Das Ei im Essigbad. Zusammenfassung. Einordnung in den Unterricht 1
 V3 Das Ei im Essigbad Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Ethansäure 1 h Zusammenfassung Ein Ei wird in ein Glas mit Essigessenz gegeben, sodass sich dessen Schale
V3 Das Ei im Essigbad Fach Klasse Überthema Feinthema Zeit Chemie Q1 Alkansäuren und ihre Derivate Ethansäure 1 h Zusammenfassung Ein Ei wird in ein Glas mit Essigessenz gegeben, sodass sich dessen Schale
Versuch: Alkoholtest mit Dichromat. Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz:
 Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: Die klassische Atemalkoholprobe
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: Die klassische Atemalkoholprobe
+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose
![+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose + 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose](/thumbs/54/33374656.jpg) Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Licht und Farben. Kurzprotokoll
 Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Honigessig vom Imker. G.Zach
 Honigessig vom Imker G.Zach Warum selber Honig- Essig herstellen? Qualität durch die komplette Kontrolle der Erzeugung Keine Reaktorware, hergestellt in 24h, kein synthetischer ti h Essig Ihr Essig hat
Honigessig vom Imker G.Zach Warum selber Honig- Essig herstellen? Qualität durch die komplette Kontrolle der Erzeugung Keine Reaktorware, hergestellt in 24h, kein synthetischer ti h Essig Ihr Essig hat
Versuch: Reaktivität von primären, sekundären und tertiären Alkylbromiden gegenüber ethanolischer Silbernitratlösung. keine Reaktion.
 Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Philipps-Universität Marburg 15.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 5, Halogenalkane Versuch: Reaktivität von primären, sekundären
Die enzymatische Bräunung
 V23 Die enzymatische Bräunung Fach Klasse Überthema Feinthema Zeit Chemie Q4 Nahrungsmittelzusatzstoffe Antioxidantien 24 h Zusammenfassung Bei dem Versuch wird im Versuchsteil a) die braungefärbte, wässrige
V23 Die enzymatische Bräunung Fach Klasse Überthema Feinthema Zeit Chemie Q4 Nahrungsmittelzusatzstoffe Antioxidantien 24 h Zusammenfassung Bei dem Versuch wird im Versuchsteil a) die braungefärbte, wässrige
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Vergleich der Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole
 Vergleich der Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole Stand: 03.06.2018 Jahrgangsstufen 12 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material Chemie
Vergleich der Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole Stand: 03.06.2018 Jahrgangsstufen 12 Fach/Fächer Übergreifende Bildungsund Erziehungsziele Zeitrahmen Benötigtes Material Chemie
Frühjahr 2012 Organische Chemie S.1. Staatsexamensklausur Frühjahr 2012 Chemie für das Lehramt an Gymnasien. Teil II: Organische Chemie
 Frühjahr 2012 rganische Chemie S.1 Staatsexamensklausur Frühjahr 2012 Chemie für das Lehramt an Gymnasien Teil II: rganische Chemie Aufgabe 1: Polymere (10 P) 1. Polymere a. Zeichnen Sie Ausschnitte aus
Frühjahr 2012 rganische Chemie S.1 Staatsexamensklausur Frühjahr 2012 Chemie für das Lehramt an Gymnasien Teil II: rganische Chemie Aufgabe 1: Polymere (10 P) 1. Polymere a. Zeichnen Sie Ausschnitte aus
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch: Reaktivität
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: xidation der Propanole
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: xidation der Propanole
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose
 Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Sauer macht lustigund gesünder
 Sauer macht lustigund gesünder Essig aus Obst Herstellung, Vermarktung und gesundheitliche Aspekte Mair s Beerengarten Obstbau seit 1990 (Beerenobst, Steinobst, Kernobst) Veredelung zu ca. 100 Produkten
Sauer macht lustigund gesünder Essig aus Obst Herstellung, Vermarktung und gesundheitliche Aspekte Mair s Beerengarten Obstbau seit 1990 (Beerenobst, Steinobst, Kernobst) Veredelung zu ca. 100 Produkten
6. Carbonyl-Verbindungen
 6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
6. Carbonyl-Verbindungen Hierher gehören vor allem die Aldehyde und Ketone. (später: Die Carbonyl-Gruppe weisen auch die Carbonsäuren und ihre Derivate auf). Carbonylgruppe. Innerhalb der Sauerstoff-Kohlenstoff-Doppelbindung
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Oxidation
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Oxidation
Versuch: Fäden spinnen Polymer aus Citronensäure und Glycerin
 Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Nährstoffe und Nahrungsmittel
 1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
1 Weitere Lehrerversuche Schulversuchspraktikum Annika Nüsse Sommersemester 2016 Klassenstufen 5 & 6 Nährstoffe und Nahrungsmittel Kurzprotokoll 1 Weitere Lehrerversuche Auf einen Blick: Der Lehrerversuch
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure
 Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
RAHMENRICHTLINIEN SEKUNDARSCHULE CHEMIE KULTUSMINISTERIUM. Schuljahrgänge 7 10
 RAHMENRICHTLINIEN SEKUNDARSCHULE (Ergänzung der RRL Sekundarschule Schuljahrgänge 7 10 in Umsetzung der Bildungsstandards für das Fach Chemie für den Mittleren Schulabschluss) CHEMIE Schuljahrgänge 7 10
RAHMENRICHTLINIEN SEKUNDARSCHULE (Ergänzung der RRL Sekundarschule Schuljahrgänge 7 10 in Umsetzung der Bildungsstandards für das Fach Chemie für den Mittleren Schulabschluss) CHEMIE Schuljahrgänge 7 10
Reak%onen an der Carbonylgruppe
 Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Reak%onen an der Carbonylgruppe H. Wünsch 2013 1.1 Struktur der Carbonylgruppe Die Carbonylgruppe entsteht bei der OxidaBon primärer und sekundärer Alkohole. Kohlenstoff und Sauerstoff sind doppelt gebunden,
Darstellung von Phenolphthalein und Fluorescein
 Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Philipps-Universität Marburg 04. Juli 2007 Fachbereich 15: Chemie rganisch-chemisches Grundpraktikum für Lehramtskandidaten Praktikumsleiter: Dr. Philipp Reiß SS 2007 Mario Gerwig Versuch: Darstellung
Schwerpunkte übergeordneter Kompetenzerwartungen:
 Inhaltsfeld: Kohlenstoffverbindungen und Gleichgewichtsreaktionen Inhaltliche Schwerpunkte: Organische (und anorganische) Kohlenstoffverbindungen Zeitbedarf: ca. 38 Std. à 45 Minuten Kontext: Vom Alkohol
Inhaltsfeld: Kohlenstoffverbindungen und Gleichgewichtsreaktionen Inhaltliche Schwerpunkte: Organische (und anorganische) Kohlenstoffverbindungen Zeitbedarf: ca. 38 Std. à 45 Minuten Kontext: Vom Alkohol
Arbeitsplan Chemie Carbonsäuren
 Arbeitsplan Chemie Carbonsäuren S.301 A2 Aus Ethanol wird mithilfe von Essigsäurebakterien Essigsäure (Ethansäure). Dieser Vorgang verläuft in zwei Schritten. Zuerst wird das Ethanol Dehydriert, also das
Arbeitsplan Chemie Carbonsäuren S.301 A2 Aus Ethanol wird mithilfe von Essigsäurebakterien Essigsäure (Ethansäure). Dieser Vorgang verläuft in zwei Schritten. Zuerst wird das Ethanol Dehydriert, also das
Schulcurriculum für die Einführungsphase Chemie Jahrgang 11
 Helene-Lange-Schule Hannover Schulcurriculum für die Einführungsphase Chemie Jahrgang 11 ganzjähriger Unterricht: ca. 64 Unterrichtsstd. Hinweis: Folgende grundlegende Kompetenzen aus dem Bereich Kommunikation
Helene-Lange-Schule Hannover Schulcurriculum für die Einführungsphase Chemie Jahrgang 11 ganzjähriger Unterricht: ca. 64 Unterrichtsstd. Hinweis: Folgende grundlegende Kompetenzen aus dem Bereich Kommunikation
113 Estersynthese GEFAHRENSYMBOLE SICHERHEITSRATSCHLÄGE
 113 Estersynthese GUT ZU WISSEN Die Ester sind eine große Stoffgruppe in der organischen Chemie und auch im Alltag finden haben wir häufig mit ihnen zu tun. Bekannteste Vertreter dürften wohl die Polyester
113 Estersynthese GUT ZU WISSEN Die Ester sind eine große Stoffgruppe in der organischen Chemie und auch im Alltag finden haben wir häufig mit ihnen zu tun. Bekannteste Vertreter dürften wohl die Polyester
Übungsaufgaben: Alkohole und Aldehyde/Ketone
 Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
Übungsaufgaben: Alkohole und Aldehyde/Ketone 15.12.06 1. Alkohol und Schwefelsäure Propan-1-ol wird mit bzw. in Gegenwart von verdünnter Schwefelsäure zur Reaktion gebracht. Geben Sie die Reaktionen für
8 Carbonsäuren und Derivate
 8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
8 arbonsäuren und Derivate 8.1 Allgemeine Darstellungsverfahren xidation primärer Alkohole und Aldehyde (s. Kap. 6) 2 2 xidation durch r 3 /, KMn 4 /, N 3 aloform-eaktion (s. Kap. 9) 3 Br 2 xidation von
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
chulportfolio 3. Schulkonzept 3.7 Kern- und Schulcurricula G9 (Klasse 5 11) Chemie Chemie Klasse 11
 Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Bildungsstandards Kerncurriculum Schulcurriculum Empfohlener Stundenumfang Die SuS können Stoffe beschreiben (Alkane, Alkene ); - die Verwendung Stoffe in Alltag und Technik (Methan, Ethen, ); - den Informationsgehalt
Fachcurriculum Chemie Jahrgang 11 / Einführungsphase ab 2018/19
 Fachcurriculum Chemie Jahrgang 11 / Einführungsphase ab 2018/19 Ganzjähriger Unterricht 2-stündig Unterthemen Kohlenwasserstoffe Kraftstoffe und mehr Organische Chemie organische Verbindungen Definition
Fachcurriculum Chemie Jahrgang 11 / Einführungsphase ab 2018/19 Ganzjähriger Unterricht 2-stündig Unterthemen Kohlenwasserstoffe Kraftstoffe und mehr Organische Chemie organische Verbindungen Definition
Schulversuchspraktikum. Constanze Koch. Sommersemester Klassenstufen 5 & 6. Wasser als Lösungsmittel. Kurzprotokoll
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 5 & 6 Wasser als Lösungsmittel Kurzprotokoll Auf einen Blick: In diesem Protokoll werden ein Lehrerversuch und vier Schülerversuche
Chemisches Praktikum für Biologen
 Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Chemisches Praktikum für Biologen Klausur am 13.02.2015 Name: Vorname: Matrikelnummer: Aufgabe Maximale Punktzahl Erreichte Punktzahl 1 3 2 3 3 3 4 3 5 3 6 3 7 3 8 3 Gesamt 24 Bestanden: Die Klausur besteht
Experimente Arbeitsblatt
 Lehrerinformation 1/6 Arbeitsauftrag Die SuS führen nacheinander verschiedene Versuche durch und protokollieren ihre Beobachtungen. Ziel Die SuS verstehen die chemischen Prozesse und die naturwissenschaftlichen
Lehrerinformation 1/6 Arbeitsauftrag Die SuS führen nacheinander verschiedene Versuche durch und protokollieren ihre Beobachtungen. Ziel Die SuS verstehen die chemischen Prozesse und die naturwissenschaftlichen
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09. Name: Sarah Henkel Datum:
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Gruppe 3: Alkene, Alkine Versuch: omierung von
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 28.11.2008 Gruppe 3: Alkene, Alkine Versuch: omierung von
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2015/16 vom
 Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2015/16 vom 18.09.2015 A1 A2 A3 A4 A5 Note 15 5 9 11 10 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Klausur zum Vorkurs des Chemischen Grundpraktikums WS 2015/16 vom 18.09.2015 A1 A2 A3 A4 A5 Note 15 5 9 11 10 NAME:... VORNAME:... Pseudonym für Ergebnisveröffentlichung:... Schreiben Sie bitte gut leserlich:
Gruppe 06: pulsierende Amöben
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: pulsierende Amöben Reaktion: Chemikalien: Eingesetzte Stoffe Gefahrensymbole
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: pulsierende Amöben Reaktion: Chemikalien: Eingesetzte Stoffe Gefahrensymbole
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Schulversuchspraktikum Nadja Felker Sommersemester 2015 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen Kurzprotokoll Auf einen Blick: Das Protokoll enthält für die Klassen 5 und 6 einen Lehrerversuch
Gruppe 6 Pflichtversuch. Abnahme der Wasserlöslichkeit der Alkanole mit zunehmender Molekülgröße
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. eiß Datum: 02.06.09 SS 09 Gruppe 6 Pflichtversuch Abnahme der Wasserlöslichkeit
ALDEHYDE & KETONE. Referat über die Carbonylverbindungen: Aldehyde und Ketone Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium
 ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
ALDEHYDE & KETONE Referat über die Carbonylverbindungen: und Patrick König und Robert Bozsak LK C2 Sigmund-Schuckert-Gymnasium 1 1 GLIEDERUNG 1. Allgemeiner Vergleich der & Struktur Nomenklatur / Beispiele
Hydrierung von Kohlenmonoxid zu Methanol Kataly?sche Umsetzung von Ethen mit Wasser zu Ethanol
 Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Oxida&onsreak&onen Von Alkenen und Alkokolen zu Aldehyden, Ketonen und Carbonsäuren H. Wünsch 2012 1 Vorbemerkung Grundlage der hier betrachteten Reak?onen sind Alkene und Alkohole. Alkohole sind Produkte
Fassung vom 26. Februar Regionalmarke. Pflichtenheft. für den Produktbereich. Essig
 Fassung vom 26. Februar 2009 Regionalmarke Pflichtenheft für den Produktbereich Essig Pflichtenheft Essig vom 26. Februar 2009 Seite 1 I. Anwendungsbereich / Produktdefinition Die Bezeichnung Essig ist
Fassung vom 26. Februar 2009 Regionalmarke Pflichtenheft für den Produktbereich Essig Pflichtenheft Essig vom 26. Februar 2009 Seite 1 I. Anwendungsbereich / Produktdefinition Die Bezeichnung Essig ist
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 5, 17./18.05.11 Wiederholung: Säurestärke organischer Verbindungen 1. a) Wovon hängt die Säurestärke einer organischen
Eigenschaften von Tensidlösungen
 V17 Eigenschaften von Tensidlösungen Fach Klasse Überthema Feinthema Zeit Chemie Q4 Grenzflächenaktive Substanzen Eigenschaften von Tenisden 30 Minuten Zusammenfassung Bei dem Versuch werden die Eigenschaften
V17 Eigenschaften von Tensidlösungen Fach Klasse Überthema Feinthema Zeit Chemie Q4 Grenzflächenaktive Substanzen Eigenschaften von Tenisden 30 Minuten Zusammenfassung Bei dem Versuch werden die Eigenschaften
Fortbildung am Schülerlabor in Rechtenthal für die Grundschule. Ideen zu weiterführenden Versuchen in der Klasse:
 Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Fortbildung am 16.11.2012 Schülerlabor in Rechtenthal für die Grundschule Ideen zu weiterführenden Versuchen in der Klasse: Lernziele: -Die Kinder erkennen chemische, physikalische Veränderungen (auch
Dokumentation Projekt Entwicklung einer Farbskala PLUS-Kurs SU 4+, GGS Vaalserquartier, Aachen
 Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 230 SchülerInnen
Die Arbeitsgruppe Die Gemeinschaftsgrundschule Vaalserquartier ist eine zweizügige Grundschule im westlichsten Stadtteil von Aachen, 400 m von der Grenze zu den Niederlanden gelegen. Sie hat 230 SchülerInnen
Saure, neutrale und alkalische Lösungen
 Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Schulversuchspraktikum Sina Bachsmann Sommersemester 2014 Klassenstufen 5 & 6 Saure, neutrale und alkalische Lösungen 1 Beschreibung des Themas und zugehörige Lernziele 1 Auf einen Blick: Im Folgenden
Alkansäuren. Nomenklatur & Vorkommen in der Natur
 Alkansäuren Nomenklatur & Vorkommen in der Natur Übersicht Allgemeines Nomenklatur Eigenschaften & Merkmale der Alkansäuren Bekannte Alkansäuren und ihre Salze und die Vorkommen in der Natur Allgemeines
Alkansäuren Nomenklatur & Vorkommen in der Natur Übersicht Allgemeines Nomenklatur Eigenschaften & Merkmale der Alkansäuren Bekannte Alkansäuren und ihre Salze und die Vorkommen in der Natur Allgemeines
Schulversuch-Protokoll Jan gr. Austing
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: Bromierung von Butan ) Reaktionsgleichung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 06/07 Leitung: Prof. Hilt/ Dr. Reiß Schulversuch-Protokoll 6.1.007 Jan gr. Austing 1) Versuchsbezeichnung: Bromierung von Butan ) Reaktionsgleichung:
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 3: Alkene, Alkine Versuch: erstellung und
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 12.11.2008 Gruppe 3: Alkene, Alkine Versuch: erstellung und
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Gruppe 05: Alkylchloride gegenüber AgNO 3
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Alkylchloride gegenüber AgNO 3 Reaktion: am Beispiel des sekundären
1 Lehrerversuch Alkalimetalle in Wasser
 1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
1 Lehrerversuch Alkalimetalle in Wasser Diese Versuchsreihe kann zum Einstieg in das Thema Alkalimetalle verwendet werden, da kein Vorwissen benötigt wird. Die Versuche sind nur gering aufwändig und können
Schulversuchspraktikum. Dennis Roggenkämper. Sommersemester Klassenstufen 11 & 12. Kohlenhydrate. Kurzprotokoll
 Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 11 & 12 Kohlenhydrate Kurzprotokoll Auf einen Blick: Das Kurzprotokoll umfasst vier Lehrer- und zwei Schülerexperimente, die
Schulversuchspraktikum Dennis Roggenkämper Sommersemester 2015 Klassenstufen 11 & 12 Kohlenhydrate Kurzprotokoll Auf einen Blick: Das Kurzprotokoll umfasst vier Lehrer- und zwei Schülerexperimente, die
Versuch: Molischprobe mit Gelatine H 2 SO 4. O - 2 H e H 2. Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Molischprobe
Versuch: Hydrolyse von Stärke mit Speichel
 Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Stoffverteilungsplan Lehrplan für den Erwerb des Hauptschul- und des Realschulabschlusses (Regelschule) in Thüringen 2012 PRISMA Chemie Thüringen
 Stoffverteilungsplan Lehrplan für den Erwerb des Hauptschul- und des Realschulabschlusses (Regelschule) in Thüringen 2012 PRISMA Chemie Thüringen Band 9/10 Schule: Klett 978-3-12-068567-8 Lehrer/Lehrerin:
Stoffverteilungsplan Lehrplan für den Erwerb des Hauptschul- und des Realschulabschlusses (Regelschule) in Thüringen 2012 PRISMA Chemie Thüringen Band 9/10 Schule: Klett 978-3-12-068567-8 Lehrer/Lehrerin:
Chemie für Biologen, Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema ) iii) Carbonsäure iv) Dicarbonsäure
 Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Chemie für Biologen, 2017 Übung 12 Carbonylverbindungen / Carbonsäuren und ihre Derivate (Thema 13.1 14.3) Aufgabe 1: a) Es gibt verschiedene Klassen von Carbonylverbindungen. Zeichnen Sie zu folgenden
Versuch: Bromierung von n-hexan. Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Bemerkung
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe. Beschreiben Sie die Alkane allgemein.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
 Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Carbonsäuren schriftliche Ausarbeitungen zu folgenden Themen: a) Eigenschaften von organischen Säuren b) Begriff der homologen Reihe der Carbonsäuren c) Ein Steckbrief von Ameisen-, Essig- und Citronensäure
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Grundkurs Optische Aktivität 1983/I/1 1992/I/1 1994/III/3 1998/I/1
 Grundkurs Optische Aktivität 1983/I/1 1.1 Definieren Sie den Begriff "optische Aktivität"! 2BE 1.2 Erläutern Sie am Beispiel des Bromchloriodmethans, welche Form von Isomerie bei dieser Verbindung auftritt
Grundkurs Optische Aktivität 1983/I/1 1.1 Definieren Sie den Begriff "optische Aktivität"! 2BE 1.2 Erläutern Sie am Beispiel des Bromchloriodmethans, welche Form von Isomerie bei dieser Verbindung auftritt
Gruppe 4 eigener Versuch. Reduktion von Anthrachinon
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 eigener Versuch Reduktion von Anthrachinon
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 eigener Versuch Reduktion von Anthrachinon
Entscheide bei jeder Aussage, ob es eine reine Beobachtung ist oder nicht, und kreuze an!
 Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Kerze Eine brennende Kerze wandelt Energie und Stoffe um. N_9d_44 Über eine brennende Rechaudkerze (Teelicht) wird ein «leeres» Glas gestülpt. Schülerinnen und Schüler notieren Aussagen zum Versuch. Entscheide
Versuch: Fehling- und Biuretprobe mit Gummibärchen
 Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Fehling- und Biuretprobe mit
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Fehling- und Biuretprobe mit
Bayerisches Landesamt für Gesundheit und Lebensmittelsicherheit
 Fehlaroma: Pentadien Pentadien (ein Kohlenwasserstoff) wird aus dem zugelassenen Konservierungsmittel Sorbinsäure gebildet. Der Abbau von Sorbinsäure wird durch Schimmelpilze verursacht. Die Bildung von
Fehlaroma: Pentadien Pentadien (ein Kohlenwasserstoff) wird aus dem zugelassenen Konservierungsmittel Sorbinsäure gebildet. Der Abbau von Sorbinsäure wird durch Schimmelpilze verursacht. Die Bildung von
Grundwissen Chemie Klasse
 Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Grundwissen Chemie 8. 10. Klasse Grundwissen Chemie 8I Chemie Reinstoff und Gemisch Atome und Moleküle Chemische Reaktionen Analyse und Synthese Katalysatoren Luft Sauerstoff und Wasserstoff Redoxreaktionen
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Grundwissen Chemie Jahrgangsstufe 10, naturwissenschaftlicher Zweig. Methan Ethan Propan Butan Pentan Hexan Heptan Octan Nonan Decan
 Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
Grundwissen hemie Jahrgangsstufe 10, homologe Reihe der Alkane Summenformel 4 2 6 3 8 4 10 5 12 6 14 7 16 8 18 9 20 10 22 Allgemeine Summenformel: n 2n+2 Name Methan Ethan Propan Butan Pentan exan eptan
schulinterne Kurzübersicht der Unterrichtsvorhaben 1
 schulinterne Kurzübersicht der Unterrichtsvorhaben 1 Fach: Chemie Jahrgangsstufe(n): Einführungsphase erstes und zweites Halbjahr Inhaltsfeld: Kohlenstoffverbindungen und Gleichgewichtsreaktionen Fachlicher
schulinterne Kurzübersicht der Unterrichtsvorhaben 1 Fach: Chemie Jahrgangsstufe(n): Einführungsphase erstes und zweites Halbjahr Inhaltsfeld: Kohlenstoffverbindungen und Gleichgewichtsreaktionen Fachlicher
Carbonsäuren (Vollhardt, 3. Aufl., S. 893 ff, 4. Aufl., S. 967 ff; Hart, S. 345 ff; Buddrus, S. 501 ff)
 Vorlesung 39 arbonsäuren (Vollhardt, 3 Aufl, S 893 ff, 4 Aufl, S 967 ff; art, S 345 ff; Buddrus, S 501 ff) Die funktionelle Gruppe der arbonsäuren (= Fettsäuren) ist die arboxyl- (bzw arboxy-) Gruppe In
Vorlesung 39 arbonsäuren (Vollhardt, 3 Aufl, S 893 ff, 4 Aufl, S 967 ff; art, S 345 ff; Buddrus, S 501 ff) Die funktionelle Gruppe der arbonsäuren (= Fettsäuren) ist die arboxyl- (bzw arboxy-) Gruppe In
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler
 Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Vorkurs Chemie (NF) Säuren und Basen, Puffer Ulrich Keßler Alltagserfahrung: sauer Zitrone Essig junger Wein Welcher Stoff bewirkt saure Reaktion? http://www.simplyscience.ch/portal Data/1/Resources/Images_bis_10_
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen
 Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Chemie in der Realschule des SBZ mit blinden, sehenden und ehbehinderten Schülern Reinhard Apelt 2004 Universität
Integration von Schülerinnen und Schülern mit einer Sehschädigung an Regelschulen Didaktikpool Chemie in der Realschule des SBZ mit blinden, sehenden und ehbehinderten Schülern Reinhard Apelt 2004 Universität
Einführung in die Biochemie
 Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
Stoffwechselvorgänge, bei denen Kohlenhydrate abgebaut werden um dem rganismus Energie zur Verfügung zu stellen, können auf verschieden Wegen ablaufen: 1. Die Atmung ist der aerobe Abbau, bei dem zur Energiegewinnung
+ 30,5 O 2 (g) 20 CO 2 (g) + 21 H 2 O
 Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Nachweis
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 11.11.2008 Gruppe 1: Einführung der OC Versuch: Nachweis
Duden Schülerhilfen. Textgleichungen Aufgabentexte umsetzen Lösungsverfahren anwenden. Dudenverlag Mannheim Leipzig Wien Zürich.
 Duden Schülerhilfen Tetgleichungen Aufgabentete umsetzen Lösungsverfahren anwenden von Hans Borucki mit Illustrationen von Detlef Surrey 3., aktualisierte Auflage Dudenverlag Mannheim Leipzig Wien Zürich
Duden Schülerhilfen Tetgleichungen Aufgabentete umsetzen Lösungsverfahren anwenden von Hans Borucki mit Illustrationen von Detlef Surrey 3., aktualisierte Auflage Dudenverlag Mannheim Leipzig Wien Zürich
Gruppe 1 Pflichtversuch. Qualitative Analyse: Nachweis von Kohlenstoff als Kohlendioxid
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: Herr Dr. Reiß Datum: 19.05.09 SS 09 Gruppe 1 Pflichtversuch Qualitative Analyse: Nachweis
Martin Raiber Chemie Protokoll Nr Gruppe 2 (Schrankseite) Untersuchung von Glycin
 Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
Martin Raiber Chemie Protokoll Nr.4 5.3.2006 Gruppe 2 (Schrankseite) Untersuchung von Glycin Chemikalien: Glycin ( c=0,1 mol/l ) Essigsäure ( c=0,1 mol/l ) 0,75g Glycin Salzsäure ( 100ml, c=0,1 mol/l )
+ R 2 OH H 2 SO 4 R 1
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Herstellung
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah Henkel Datum: 02.12.2008 Gruppe 7: Aldehyde und Carbonsäuren Versuch: Herstellung
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Grundwissenkarten Hans-Carossa- Gymnasium
 Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Grundwissenkarten Hans-Carossa- Gymnasium 10. Klasse Chemie SG Es sind insgesamt 20 Karten für die 10. Klasse erarbeitet. Karten ausschneiden : Es ist auf der linken Blattseite die Vorderseite mit Frage/Aufgabe,
Beschreiben Sie den Aufbau und die Eigenschaften der Kohlenwasserstoffe.
 den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
den Aufbau und die Eigenschaften der Kohlenwasserstoffe. nur Kohlenstoff- und Wasserstoffatome mit einander verbunden Kohlenstoffatom ist vierbindig Wasserstoffatom ist einbindig Skelett aller KW wird
Unterrichtsmaterialien in digitaler und in gedruckter Form. Auszug aus: Lernwerkstatt: Organische Chemie II. Das komplette Material finden Sie hier:
 Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Unterrichtsmaterialien in digitaler und in gedruckter Form Auszug aus: Lernwerkstatt: Organische Chemie II Das komplette Material finden Sie hier: School-Scout.de Titel: Lernwerkstatt: Organische Chemie
Versuchsprotokoll. Züchtung von Kandiszucker-Kristallen
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Züchtung von Kandiszucker-Kristallen
Versuch: Bromierung von Phenol
 Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 01.12.2007 Organisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: omierung von Phenol Zeitbedarf: Vorbereitung:
Oxidationsversuche an allen C 1 -C 4 -Alkanolen
 Oxidationsversuche an allen C 1 -C 4 -Alkanolen Chemikalien: Geräte: Methanol, Ethanol, 1-Propanol, 2-Propanol, 1-Butanol, 2-Butanol, 2-Methyl-1-propanol, 2-Methyl-2-propanol, Kupfer-Blech, Wasser, Indikatorpapier,
Oxidationsversuche an allen C 1 -C 4 -Alkanolen Chemikalien: Geräte: Methanol, Ethanol, 1-Propanol, 2-Propanol, 1-Butanol, 2-Butanol, 2-Methyl-1-propanol, 2-Methyl-2-propanol, Kupfer-Blech, Wasser, Indikatorpapier,
Curriculum Chemie Klasse 10 Albert-Einstein-Gymnasium Ulm
 Curriculum Chemie Klasse 10 Albert-Einstein-Gymnasium Ulm Klasse 10 Themen Kohlenwasserstoffe Alkane - Vorkommen, Eigenschaften und Molekülstruktur - Isomerie und Nomenklatur Kohlenwasserstoffe - Energieträger
Curriculum Chemie Klasse 10 Albert-Einstein-Gymnasium Ulm Klasse 10 Themen Kohlenwasserstoffe Alkane - Vorkommen, Eigenschaften und Molekülstruktur - Isomerie und Nomenklatur Kohlenwasserstoffe - Energieträger
Lehrerhandreichung Plankton selbst erkunden. (geeignet für die Klassenstufe 4 und 5)
 Lehrerhandreichung Plankton selbst erkunden (geeignet für die Klassenstufe 4 und 5) Materialien für die Planktonprobenahme Planktonnetz (empfohlene Maschenweite 100 oder 105 µm) Spritzwasserflasche mit
Lehrerhandreichung Plankton selbst erkunden (geeignet für die Klassenstufe 4 und 5) Materialien für die Planktonprobenahme Planktonnetz (empfohlene Maschenweite 100 oder 105 µm) Spritzwasserflasche mit
Merkmale Chemischer Reaktionen (qualitativ)
 Schulversuchspraktikum Carolin Schilling Sommersemester 2016 Klassenstufen 7&8 Merkmale Chemischer Reaktionen (qualitativ) Kurzprotokoll Auf einen Blick: Die beiden Schülerexperimente dieses Kurzprotokolls
Schulversuchspraktikum Carolin Schilling Sommersemester 2016 Klassenstufen 7&8 Merkmale Chemischer Reaktionen (qualitativ) Kurzprotokoll Auf einen Blick: Die beiden Schülerexperimente dieses Kurzprotokolls
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
