Versuchsprotokoll. ph-abhängigkeit der Getränkefarben
|
|
|
- Norbert Fuhrmann
- vor 6 Jahren
- Abrufe
Transkript
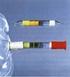
1 AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/ Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll phabhängigkeit der Getränkefarben Gruppe 12, Typ: Assiversuch 1. Reaktionsgleichung ao 3 S + a H + + OH + H + OH ao 3 S + H + a ao 3 S OH a 2. Zeitbedarf Vorbereitung Durchführung achbearbeitung Teil 1 30 min 30 min 5 min 3. Chemikalien ame Summenformel Gefahrensymbol RSätze SSätze Einsatz in der Schule Salzsäure HCl C 34, 37 26, 45 S I (w = 0,37) Salzsäure HCl S I (c = 1 mol/l) Essigsäure (c = 1 mol/l) CH 3 COOH S I 1
2 Wasser H 2 O S I Ammoniak H 3 C, 34, 50 26, 36/37/39, S I (w = 0,25) 45, 61 atronlauge aoh C 34 26, 37/39, 45 S I (c = 1 mol/l) Brillantblau FCF C 37 H 34 2 a 2 O 9 S 3 Xn 33 24/25 S I Iso S I OrangeDrink S I ACEDrink S I ApfelKirsch Drink ApfelZitrone PflaumeDrink S I S I Gefahrensymbole 4. Materialien/Geräte Reagenzglasständer, 42 Reagenzgläser, 12 Bechergläser, 6 Pipetten 5. Versuchsaufbau Abb. 1: Es werden sieben Reagenzgläser mit 3 ml Getränk befüllt. Das linke Reagenzglas verbleibt als Vergleichsprobe, die anderen werden je mit einem der sechs Reagenzien befüllt. 6. Versuchsdurchführung Man gibt je 23 ml von jedem der fünf Getränke in jeweils 7 Reagenzgläser und versetzt je eine Probe mit je 3 Tropfen Salzsäure (W = 36 %), Salzsäure (c = 1 mol/l), Essigsäure (c = 1 mol/l), Wasser, Ammoniak (w = 25 %) und atronlauge (c = 1 mol/l). Das jeweils erste Reagenzglas verbleibt als Vergleichprobe. Man verfährt mit dem Farbstoff Brillantblau wie mit den Getränken. 2
3 7. Beobachtung Bei Zugabe der Reagenzien zeigten sich teilweise Farbänderung, teilweise war jedoch keine Veränderung zu beobachten. Die Ergebnisse sind in Tabelle 1 zusammengefasst: Tabelle 1: Beobachtungen Getränk ohne Salzsäure Salzsäure Essigsäure Wasser Ammoniak atronlauge Zusatz (w = 36 %) (c = 1 mol/l) (c = 1 mol/l) (w = 25 %) (c = 1 mol/l) IsoDrink blass blass gelb blass gelb blass gelb blass blass gelb blass gelb gelb gelb Orange gelb gelb gelb gelb gelb gelb gelb Drink ACEDrink orange orange orange orange orange orange orange Apfel rot rot rot rot rot braun braun Kirsch Apfel Zitrone Pflaume blau grün blau blau blau grün blau Brillantblau blau grün heller blau blau blau dunkelblau dunkelblau Abb. 2: ApfelKirsch Farbänderung in den Reagenzgläser mit Ammoniak und atronlauge Abb. 3: ApfelZitronePflaume Farbänderung in den Reagenzgläser mit konzentrierter Salzsäure und Ammoniak Abb. 4 Brillantblau Deutliche Farbänderung in den Reagenzgläser mit konzentrierter Salzsäure, Ammoniak und atronlauge 8. Entsorgung Die Lösungen werden neutral im Abguss entsorgt, bis auf diejenigen, die mit AmmoniakLösung versetzt wurden. Diese werden in die Schwermetallabfälle gegeben. 9. Fachliche Analyse Vielen Getränken und Lebensmitteln werden Farbstoffe zugesetzt. Dieser Versuch soll zeigen, ob diese Farbstoffe bei wechselndem phwert ihre Farbe wechseln, also als Indikatoren einsetzbar sind. Als Vergleichsprobe wird in der Vorschrift Brillantblau vorgeschlagen. Dieser Versuch zeigt nur eine deutliche Farbänderung bei dem ApfelKirschGetränk und dem ApfelZitronePflaumeGetränk. Brillantblau zeigt eine deutliche Farbänderung im stark sauren Milieu und eine leichte Farbänderung im ammoniakalischem und alkalischem Milieu. Die Struktur des Farbstoffes Brillantblau kann durch zwei mesomere Grenzformeln wieder gegeben werden: 3
4 ao 3 S + a ao 3 S + a [1] Wird Brillantblau mit Säure versetzt, so greift das Stickstoffatom mit dem freien Elektronenpaar das Wasserstoffatom an und bindet dieses. + H + H + ao 3 S + H + a Das Stickstoffatom ist nun vierbindig und positiv geladen. Dadurch erstreckt sich die Mesomerie nicht mehr über das ganze Molekül, sondern reduziert sich auf das chinoide System. Das Absorptionsspektrum verschiebt sich dementsprechend in den kurzwelligen Bereich, wodurch die Farbänderung von blau nach grün zu erklären ist. Im alkalischen Milieu greift das Sauerstoffatom der HydroxidGruppe das zentrale Kohlenstoffatom des Triphenylmethanfarbstoffes Brillantblau an. Dadurch geht die chinoide Struktur verloren und es bildet sich eine benzoide. Auch hier ist die Farbänderung durch eine durch die Strukturänderung hervorgerufene Verschiebung des Absorptionsspektrums in den kürzerwelligen Bereich zu erklären. 4
5 ao 3 S + a OH + OH ao 3 S OH a Dieselbe Reaktion findet mit der AmmoniakLösung statt, denn sobald Ammoniak mit Wasser gemischt wird, welches in großen Mengen in den Getränken vorkommt, bilden sich HydroxidIonen. H 3 + H 2 O H OH Da die Konzentration des Ammoniaks weit höher ist als die der atronlauge, zeigt sich bei dem Apfel ZitronePflaumeGetränk beim Versetzen mit Ammoniak eine Farbänderung, beim Versetzen mit atronlauge jedoch nicht. Im Vergleich dazu zeigt sich jedoch bei dem ApfelKirschGetränk auch eine Farbänderung beim Versetzen mit der atronlauge. Schaut man sich die Inhaltsstoffe der beiden Getränke an, so fällt auf, dass das ApfelZitronePflaumeGetränk den Farbstoff Brillantblau enthält, bei dem ApfelKirschGetränk jedoch angeblich keine Farbstoffe enthalten sind. Es lässt sich also nicht sagen welche Substanz für die Färbung des roten Getränkes beim Versetzen mit Ammoniak und atronlauge verantwortlich ist. Beim ApfelZitronePflaumeGetränk ist es hingegen eindeutig der Triphenylmethanfarbstoff Brillantblau. Vor allem Lebens und Genussmittel, die von Kindern konsumiert werden, werden Farbstoffe zugesetzt. Schon in der Zeit des Altertums färbte man Lebensmittel an. Hierfür benutzte man Pflanzenfarbstoffe. Im Mittelalter wurden schließlich auch Mineralfarben wie Ultramarin (schwefelhaltiges atriumaluminiumsilicat) und Bleipigmente benutzt. Erst Ende des 19. Jahrhunderts 5
6 fand man heraus, dass viele dieser bisher benutzen Farbstoffe toxisch wirken oder Allergien hervorrufen. Deshalb wurde ihr Einsatz verboten traten vermehrt Vergiftungsfälle auf. Aus diesem Grund beschloss man eine gesetzliche Regelung, die genau vorschrieb welche Lebensmittelfarbstoffe verwendet werden durften und welche nicht. Heute muss jedes Produkt, das solche Farbstoffe enthält entsprechend ausgezeichnet werden. Wenn auch die heute erlaubten Farbstoffe nicht toxisch sind, so rufen sie dennoch bei einigen Menschen Allergien hervor. Die meisten werden zwar über den Harn ausgeschieden, einige werden im Darm jedoch gespalten und zu Aminen reduziert, worauf einige Menschen sehr empfindlich reagieren. Deshalb wurden alle erlaubten Lebensmittelfarbstoffe mit Eummern versehen, die angeben, um welchen Farbstoff es sich handelt. Man unterscheidet synthetische und natürliche Farbstoffe. Chlorophylle, Anthocyane und die Carotine gehören z.b. zu den natürlichen Farbstoffen. Die meisten synthetischen Farbstoffe sind Azofarbstoffe, die durch Anfügen von Sulfonsäuregruppen wasserlöslich gemacht werden. Lebensmitteln werden natürlich nicht nur Farbstoffe, sondern auch andere Zusatzstoffe, z.b. für die Konservierung, zugesetzt. Auch diese Substanzen sind in den Eummern aufgeführt. Für die Bewertung ihrer Toxizität gibt es den ADIWert (acceptable daily intake). Er beschreibt die Menge, die der Mensch täglich zu sich nehmen kann, ohne sich oder seine achkommen zu gefährden. In diesem Versuch wurde gezeigt, dass der Lebensmittelfarbstoff Brillantblau (ein Triphenylmethanfarbstoff) auch als Indikatorfarbstoff verwandt werden kann. Dies beruht darauf, dass sich in den mesomeren Grenzformeln ein negativer Ladungsschwerpunkt an dem Stickstoffatom ergibt, welches am weitesten von den Elektronen liefernden Substituenten entfernt ist. Dieses Stickstoffatom kann gut protoniert werden. Dadurch verändert sich das Chromophor und entsprechend auch die Farbe. Die Farbigkeit von Stoffen beruht immer auf den gleichen physikalischchemischen Gesetzmäßigkeiten. Sie entsteht, wenn ein Lichtquant einer bestimmten Energie aus dem sichtbaren Teil des Spektrums von einem Molekül absorbiert ( aufgenommen ) wird. Wenn die Absorption dann stattfindet, wenn das so genannte polychromatische Licht, also Licht, das das ganze elektromagnetische Wellenspektrum umfasst, auf die Substanz trifft, so erscheint die Substanz in der Komplementärfarbe. Chlorophyll z.b. erscheint grün, weil es das rote Licht absorbiert. Moleküle absorbieren dann Licht, wenn die Energie des Lichtquants genau der Energiedifferenz zwischen dem höchsten besetzten Molekülorbital (HOMO) und einem nicht mit Elektronen besetzten Energiezustand bzw. Orbital entspricht. Durch die Energie hv wird das Elektron dann angeregt, also in den höheren Energiezustand angehoben. Die Energie des sichtbaren Lichts entspricht genau dem Betrag, der notwendig ist, um delokalisierte πelektronen mit konjugierten Doppelbindungen vom HOMO zum LUMO (niedrigstes unbesetztes Molekülorbital) anzuregen. Moleküle mit Doppelbindungen, die nicht konjugiert sind, erscheinen demnach farblos, weil der Abstand zwischen LUMO und HOMO zu groß ist. Je größer die Anzahl der πelektronen in einem Molekül ist, umso weiter verschiebt sich die Lichtabsorption vom blauen in den roten Spektralbereich. 6
7 10. Didaktische Analyse ach dem Lehrplan für G9 kann dieser Versuch der Jahrgangstufe 13 (GK und LK) zugeordnet werden. Dort geht es um Das chemische Gleichgewicht, also auch um SäureBaseIndikatoren. Die Schüler sollten in diesem Alter wissen was eine Säure und was eine Base ist. Ebenso sollten sie die Anwendung von Indikatoren kennen. Mit diesem Versuch kann gezeigt werden, dass in einigen Getränken Farbstoffe vorhanden sind, die als SäureBaseIndikator benutzt werden können. Für den Versuch eignen sich nur stark gefärbte Getränke wie die beiden oben angegebenen oder auch Powerade. Es ist davon abzuraten den Versuch mit mehr als drei verschiedenen Getränken durchzuführen, da die Schüler schnell den Überblick verlieren können. Man könnte zwei Getränke wählen, bei denen die Farbwechsel gut zu beobachten sind und evt. eine Vergleichsprobe hinzu nehmen, die keinen Farbstoffe enthält, und somit keine Veränderung zeigt. Man könnte sich auch überlegen diesen Versuch von den Schülern zu Hause durchführen zu lassen, indem sie die Getränke beispielsweise mit Essigessenz oder Zitronensaft versetzen. Man sollte diese Variante nur vorher ausprobiert haben, damit sichergestellt ist, dass auch etwas zu beobachten ist. Aufgrund der Menge der Getränke hat der oben beschriebene Versuch sehr lange gedauert. Wenn man sich jedoch auf auserwählte Getränke beschränkt und z.b. auch die stark verdünnte Salzsäure und das Wasser als Reagenzien weg lässt, ist dieser Versuch innerhalb kürzester Zeit durchzuführen. Bunte Getränke gibt es mittlerweile in jedem Supermarkt für wenig Geld zu kaufen und die Reagenzien sollten in jeder Schule vorhanden sein. Außerdem ist der Versuch in jeder Variante von den Schülern selber gut durchzuführen. Die Anwendung von Alltagsmaterialien sorgt sicherlich für angemessenes Interesse der Schüler. 11. Literatur Versuchsquelle: [1] Dauer, C., Pfeifer, P, Sauer oder alkalisch?, aturwissenschaften im Unterricht Chemie, 3/2008, Heft 105 Fachquellen: [2] Elemente Chemie II, Organische Chemie, 1. Auflage, KlettVerlag, Stuttgart, 2005 [3] Lehrplan Chemie für die Jahrgansstufen G7 bis G12 des hessischen Kultusministeriums, 2005 ( [4] Fachinformationszentrum Chemie, (letzter Zugriff: , 15:09 Uhr) [5] Mortimer, Charles E., Chemie, 7., korrigierte Auflage, Thieme, Stuttgart, 2001 [6] Unfallkasse Hesse (UKH), Hessisches Kultusministerium, Hessisches GefahrstoffInformations System Schule (HessGISS), Version 11.0, 2006/2007 [7] Vollhardt, K. Peter C., Schore, eil E., Organische Chemie, Vierte Auflage, WileyVCH, Weinheim, 2005 [8] Wikimedia Foundation Inc., (letzter Zugriff: , 15:09 Uhr) 7
Versuchsprotokoll. Gruppe 12, Typ: Pflichtversuch - H + Einsatz in der Schule Sulfanilsäure NH 2 C 6 H 4 SO 3 H Xi 36/38, 43 24, 37 S I
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.01.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Synthese von β-aphtolorange
Versuchsprotokoll. Nitrierung von Phenol. Gruppe 4, Typ: Pflichtversuch O O - N
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 19.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll itrierung von Phenol Gruppe 4,
Arbeitsblatt Wie entstehen Farben?
 Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Arbeitsblatt Wie entstehen Farben? Der für das menschliche Auge sichtbare Wellenlängenbereich liegt bei 380-750 nm. Farbstoffe sind in der Lage bestimmte Wellenlängen des Lichts zu absorbieren und eine
Versuchsprotokoll. Mischbarkeit von Alkoholen
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 20.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Mischbarkeit von Alkoholen Gruppe
Versuchsprotokoll. Aktivität der Speichelamylase
 AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Aktivität der Speichelamylase
AnnaLena Eicke PhilippsUniversität Marburg OrganischChemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Aktivität der Speichelamylase
Versuch: Bromierung von n-hexan. Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Bemerkung
 Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 25.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 2: Alkane Versuch: omierung von n-hexan Zeitbedarf: Vorbereitung:
+ MnO MnO 3. Oxidierbarkeit primärer, sekundärer und tertiärer Alkohole. Chemikalien. Materialien
 DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
DaChS xidierbarkeit primärer, sekundärer und tertiärer Alkohole 1 Versuch Nr. 005 xidierbarkeit primärer, sekundärer und tertiärer Alkohole C 3 Mn - 4 (violett) 3 C Mn 2 (braun) 3 C C 3 Mn - 4 (violett)
Versuchsprotokoll:Stärkespaltung
 Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
Versuchsprotokoll:Stärkespaltung Zeitaufwand: Aufbau: 5 Minuten Durchführung: 20 Minuten Abbau/Entsorgung:: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz Pentahydrat
+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose
![+ 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose + 2 [Ag(NH 3 ) 2 ]+ + 2 OH - 2 Ag + 4 NH 3. Versuch: Tollensprobe mit Glucose und Saccharose](/thumbs/54/33374656.jpg) Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Philipps-Universität Marburg 27.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Tollensprobe mit Glucose
Versuchsprotokoll: Fehling- Spaltung von Saccharose
 Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Spaltung von Saccharose Zeitaufwand: Vorbereitung: 5 Minuten Durchführung: 15 Minuten Abbau/Entsorgung: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll. Weißer Zucker schwarze Kohle
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 11.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Weißer Zucker schwarze Kohle
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 11.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Weißer Zucker schwarze Kohle
Versuch: Darstellung eines Azofarbstoffes (Methylorange)
 PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
PhilippsUniversität Marburg 02.02.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß W 2007/08 Gruppe 12, Farbstoffe, Wirkstoffe Versuch: Darstellung eines
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Mischbarkeit):
2-01. Das Ethen-Molekül. Perspektivische Darstellung des Ethen-Moleküls.
 Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Das Ethen-Molekül 2-01 Perspektivische Darstellung des Ethen-Moleküls. Rot: Sigma-Bindungen σ mit je zwei Bindungselektronen Blau: pz-orbitale mit je einem Elektron Die C-Atome sind sp 2 -hybridisiert,
Farbstoffe Einleitung
 Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Einleitung Farben, die aus Mineralien gewonnen wurden, wie die Mineralfarben Mennige, Zinnober oder Malachit dienten bereits in der Altsteinzeit für Höhlenmalereien. Diese Farben bestehen aus anorganischen
Versuch: Denaturierung von Eiweiß
 Philipps-Universität Marburg 29.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Denaturierung
Philipps-Universität Marburg 29.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 10, Amine, Aminosäuren, Peptide Versuch: Denaturierung
Versuch: Qualitativer Nachweis von Kohlenstoff und Wasserstoff
 Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Philipps-Universität Marburg 20.11.2007 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 1, Einführung in die OC Versuch: Qualitativer Nachweis
Versuch: Hydrolyse von Stärke mit Speichel
 Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Philipps-Universität Marburg 27.01.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 9, Kohlenhydrate Versuch: Hydrolyse von Stärke mit
Sublimation & Resublimation
 Reaktionsgleichung I 2 (s) I2 (g) I 2 (s) Zeitbedarf Vorbereitung: 15 min. Durchführung: 7 Std. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel R-Sätze S-Sätze Gefahrensymbole Schuleinsatz
Reaktionsgleichung I 2 (s) I2 (g) I 2 (s) Zeitbedarf Vorbereitung: 15 min. Durchführung: 7 Std. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel R-Sätze S-Sätze Gefahrensymbole Schuleinsatz
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen
 ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
ph-wert ph-wert eine Kenngröße für saure, neutrale oder basische Lösungen ChemikerInnen verwenden den ph-wert um festzustellen, wie sauer oder basisch eine Lösung ist. Man verwendet eine Skala von 0-14:
Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker
 Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Name: Datum: Versuch: Kohlenhydrate in Lebensmitteln Nachweis von Zucker Geräte Heizplatte, Bechergläser, Reagenzgläser, Reagenzglasständer, Spatel, Faltenfilter, Trichter Materialien Lebensmittel: Glucose,
Versuchsprotokoll: Ampel-Bottle - Experiment
 Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Versuchsprotokoll: Ampel-Bottle - Experiment Zeitaufwand: Aufbau: 5 Minuten Durchführung: 1 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalien Menge R-Sätze S-Sätze Gefahrensymbol Schuleinsatz
Säuren und Basen. Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17.
 Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Säuren und Basen Dr. Torsten Beweries AC I - Allgemeine Chemie LAC-CH01 WS 2016/17 torsten.beweries@catalysis.de http://www.catalysis.de/forschung/koordinationschemische-katalyse/koordinationschemische-wasserspaltung/
Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Elementarnachweis: Kohlenstoff- und Wasserstoffnachweis Reaktion:
Versuchsprotokoll. Nachweis von Kohlenstoff und Wasserstoff in Spagetti
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 12.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Nachweis von Kohlenstoff und Wasserstoff
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 12.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Nachweis von Kohlenstoff und Wasserstoff
+ Na. Gruppe 4 vorgegebener Versuch. Reaktion aromatischer Ketone mit elementarem Natrium. Reaktion: Zeitbedarf: Versuchsdurchführung:
 Philipps- Universität Marburg FB 15 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 vorgegebener Versuch Reaktion aromatischer
Philipps- Universität Marburg FB 15 hemie rganisch-hemisches Grundpraktikum für das Lehramt hristian Lego Leitung: Herr Dr. Reiß Datum: 0.05.09 SS 09 Gruppe 4 vorgegebener Versuch Reaktion aromatischer
Versuchsprotokoll. Alkoholische Gärung von Traubensaft
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 27.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Alkoholische Gärung von Traubensaft
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 27.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Alkoholische Gärung von Traubensaft
Versuch: Nachweis von Salicylsäure
 Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Philipps-Universität Marburg 11.02.2008 Organisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 12, Farb- und Wirkstoffe Versuch: Nachweis von Salicylsäure
Bromierung von Hexan G2 Pflichtversuch Bromierung von Cyclohexan und Cyclohexen G3 Pflichtversuch
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.11.08 Schulversuche Assistentin: Beate Abé omierung von exan G2 Pflichtversuch omierung von
Anna-Lena Eicke Philipps-Universität Marburg Organisch-hemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 13.11.08 Schulversuche Assistentin: Beate Abé omierung von exan G2 Pflichtversuch omierung von
Versuchsprotokoll. Oxidation von Brenztraubensäure. Gruppe 7, Typ: Assiversuch. Cr 2 O 7 SO 4 /H 2
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 27.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll xidation von Brenztraubensäure
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 27.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll xidation von Brenztraubensäure
Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 05: Darstellung von 2-Chlor-2 Methylpropan Reaktion: Chemikalien:
Gruppe 8 eigener Versuch. Hydrolyse der Seife
 Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Philipps- Universität Marburg FB 15 Chemie rganisch-chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 23.06.09 SS 09 Gruppe 8 eigener Versuch ydrolyse der Seife Reaktion:
Versuchsprotokoll. Dünnschichtchromatographie von Aminosäuren
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Dünnschichtchromatographie
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll Dünnschichtchromatographie
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose
 Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll: Fehling- Fructose, Saccharose und Glucose Zeitaufwand: Aufbau: 5 Minuten Durchführung: 10 Minuten Entsorgung/Abbau: 5 Minuten Chemikalien: Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol
Versuchsprotokoll. Atemalkoholtest
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 28.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Atemalkoholtest Gruppe 6, Typ:
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 28.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Atemalkoholtest Gruppe 6, Typ:
Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe.
 2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
2. Azofarbstoffe 2.1 Azofarbstoffe Azofarbstoffe enthalten als Chromophor die beiderseits aromatisch gebundene Azogruppe. aromatische Verbindung -= - aromatische Verbindung Sie stellen mengenmäßig die
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Beate Abé Name: Johannes Hergt Datum: 30.11.2010 Gruppe 6: Alkohole Versuch (Alkoholtest):
Versuchsprotokoll. Reaktion von Natrium mit Ethanol
 Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktion von Natrium mit Ethanol
Anna-Lena Eicke Philipps-Universität Marburg Organisch-Chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 26.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Reaktion von Natrium mit Ethanol
7. Tag: Säuren und Basen
 7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
7. Tag: Säuren und Basen 1 7. Tag: Säuren und Basen 1. Definitionen für Säuren und Basen In früheren Zeiten wußte man nicht genau, was eine Säure und was eine Base ist. Damals wurde eine Säure als ein
Versuchsprotokoll. Herstellung von Polyurethanschaum
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll erstellung von Polyurethanschaum
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 15.1.09 Schulversuche Assistentin: Katrin ohmann Versuchsprotokoll erstellung von Polyurethanschaum
Qualitativer Nachweis von Säuren und Basen
 Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Schulversuchspraktikum Constanze Koch Sommersemester 2015 Klassenstufen 9 & 10 Qualitativer Nachweis von Säuren und Basen Kurzprotokoll Auf einen Blick: In diesem Protokoll wird ein Lehrerversuch, der
Gruppe I : Darstellung und Nachweis von Säuren
 Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Gruppe I : Darstellung und Nachweis von Säuren Behauptung: Säuren lassen sich durch die Reaktion von Nichtmetalloxiden mit Wasser darstellen. 1. Überprüfen Sie experimentell die aufgeführte Behauptung
Wie kann eine Bräunung von zerkleinertem Obst und Gemüse verhindert werden?
 Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788500) 8.4 Enzymatische Bräunung Experiment von: Anouch Gedruckt: 28.02.204 :7:37 intertess (Version 3.2 B24, Export 2000) Aufgabe
Naturwissenschaften - Chemie - Lebensmittelchemie - 8 Zusatzstoffe (P788500) 8.4 Enzymatische Bräunung Experiment von: Anouch Gedruckt: 28.02.204 :7:37 intertess (Version 3.2 B24, Export 2000) Aufgabe
Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse
 Trennen von Farben Was Du brauchst: schwarzfarbige Filzstifte Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse Wie Du vorgehst: Schneide einen Kreis aus dem Kaffeefilter. Steche mit
Trennen von Farben Was Du brauchst: schwarzfarbige Filzstifte Wasser Kaffeefilter ein Streifen Filterpapier als Docht Schere Tasse Wie Du vorgehst: Schneide einen Kreis aus dem Kaffeefilter. Steche mit
Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und Pigmente Übungen mit Lösungen
 Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und Pigmente Übungen mit Lösungen Korrektorat: Dina Baars, Bern Illustrationen: Christoph Frei, Bern 1.
Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und Pigmente Übungen mit Lösungen Korrektorat: Dina Baars, Bern Illustrationen: Christoph Frei, Bern 1.
Versuch: Fäden spinnen Polymer aus Citronensäure und Glycerin
 Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Philipps-Universität Marburg 16.02.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: alph Wieneke Leitung: Dr. Ph. eiß WS 2007/08 Gruppe 13, Polymere Versuch: Fäden spinnen Polymer aus Citronensäure
Protokoll 2. Labor für Physikalische Chemie. Modul IV. Säure-Base-Reaktion. Versuch 5.1 5.2. Neutralisation, Gehaltsbestimmungen und Titrationskurven
 Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Protokoll 2 Labor für Physikalische Chemie Modul IV Säure-Base-Reaktion Versuch 5.1 5.2 Neutralisation, Gehaltsbestimmungen und Titrationskurven Fachbereich MT 1 Wintersemester 2005/2006 Thorsten Huber,
Gruppe 06: Alkoholnachweis mit Dichromat
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: Alkoholnachweis mit Dichromat Reaktion: 2 Cr 2 O 7 2 + 3 CH 3
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 06: Alkoholnachweis mit Dichromat Reaktion: 2 Cr 2 O 7 2 + 3 CH 3
7. Studieneinheit. Siebte Studieneinheit
 86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
86 Siebte Studieneinheit 7. Studieneinheit Lernziele Löslichkeit organisch-chemischer Substanzen unter verschiedenen Bedingungen Charakteristische Reaktionen ausgewählter organisch-chemischer Stoffklassen
Versuchsprotokoll. Untersuchung der Waschwirkung
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Untersuchung der Waschwirkung
Anna-Lena Eicke Philipps-Universität Marburg rganisch-chemisches Praktikum (LA) Leitung: Dr. Reiß WS 08/09 17.12.08 Schulversuche Assistentin: Katrin Hohmann Versuchsprotokoll Untersuchung der Waschwirkung
Schneiden der Alkalimetalle und Autoxidation
 Reaktionsgleichungen 4 Li s + O 2 g 2 Li 2 O s 2 Na s + O 2 g Na 2 O 2 s K s + O 2 g KO 2 s Zeitbedarf Vorbereitung: 1 min. Durchführung: 10 min. Nachbereitung: 1 min. Chemikalienliste Edukte Chemikalien
Reaktionsgleichungen 4 Li s + O 2 g 2 Li 2 O s 2 Na s + O 2 g Na 2 O 2 s K s + O 2 g KO 2 s Zeitbedarf Vorbereitung: 1 min. Durchführung: 10 min. Nachbereitung: 1 min. Chemikalienliste Edukte Chemikalien
Farbigkeit und Theorien
 Farbigkeit und Theorien Farbigkeit von Dinah Shafry Licht ist elektromagnetische Strahlung, bei der jede Farbe eine einzelne Wellenlänge besitzt, die als unterschiedliche Farben vom Menschen wahrgenommen
Farbigkeit und Theorien Farbigkeit von Dinah Shafry Licht ist elektromagnetische Strahlung, bei der jede Farbe eine einzelne Wellenlänge besitzt, die als unterschiedliche Farben vom Menschen wahrgenommen
Die sprühende Vereinigung von Aluminium und Brom
 Reaktionsgleichung 3 2 l + 2 Al s 2 Al 3 solv Zeitbedarf Vorbereitung: 10 min. Durchführung: 5 min. Nachbereitung: 10 min. Chemikalienliste Edukte Chemikalien Summen- Menge R-Sätze S-Sätze formel Schuleinsatz
Reaktionsgleichung 3 2 l + 2 Al s 2 Al 3 solv Zeitbedarf Vorbereitung: 10 min. Durchführung: 5 min. Nachbereitung: 10 min. Chemikalienliste Edukte Chemikalien Summen- Menge R-Sätze S-Sätze formel Schuleinsatz
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 200/ Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 5.2.200 Gruppe 9: Kohlenhydrate Versuch (selbst):
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 200/ Praktikumsleitung: Dr. Reiß Assistent(in): Julia Konen Name: Johannes Hergt Datum: 5.2.200 Gruppe 9: Kohlenhydrate Versuch (selbst):
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure
 Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Versuchsprotokoll: Reaktion von Zucker mit Schwefelsäure Zeitaufwand: Aufbau: Durchführung: Abbau/Entsorgung: 5 Minuten 10 Minuten 5 Minuten Chemikalien: Chemikalie Menge RSätze SSätze Gefahrensymbol Schwefelsäure
Versuchsprotokoll. Synthese und Nachweis eines Aldehyds. Gruppe 7, Typ: Eigenversuch
 Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 28.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese und Nachweis eines Aldehyds
Anna-Lena Eicke Philipps-Universität Marburg rganisch-hemisches Praktikum (LA) Leitung: Dr. eiß WS 08/09 28.11.08 Schulversuche Assistentin: Beate Abé Versuchsprotokoll Synthese und Nachweis eines Aldehyds
Versuch: Seifenherstellung aus Kokosfett
 Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
Philipps-Universität Marburg 18.01.2008 rganisches Grundpraktikum (LA) Katrin Hohmann Assistent: Ralph Wieneke Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 8, Ester, Fette, Seifen, Tenside Versuch: Seifenherstellung
4. Anorganisch-chemische Versuche
 4. Anorganisch-chemische Versuche o 4.4 Redoxreaktionen 4.4.1 Reduktion von Mangan(VII) in schwefelsaurer Lsg. 4.4.2 Oxidation von Mangan(II) in salpetersaurer Lsg. 4.4.3 Oxidation von Chrom(III) in alkalischer
4. Anorganisch-chemische Versuche o 4.4 Redoxreaktionen 4.4.1 Reduktion von Mangan(VII) in schwefelsaurer Lsg. 4.4.2 Oxidation von Mangan(II) in salpetersaurer Lsg. 4.4.3 Oxidation von Chrom(III) in alkalischer
Aspirin und Paracetamol im chemischen Vergleich
 Aspirin und Paracetamol im chemischen Vergleich Achtung Aspirin und Paracetamol sind geschützte Namen und dürfen nicht ohne weiteres verwendet werden. Strukturformeln Aus den Strukturformeln leiten wir
Aspirin und Paracetamol im chemischen Vergleich Achtung Aspirin und Paracetamol sind geschützte Namen und dürfen nicht ohne weiteres verwendet werden. Strukturformeln Aus den Strukturformeln leiten wir
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr. 2,
 Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Übung zum chemischen Praktikum für Studierende mit Chemie als Nebenfach Übung Nr., 6.04.11 1. Sie legen 100 ml einer 0, mol/l Natronlauge vor. Als Titrant verwenden Sie eine 0,8 mol/l Salzsäure. Berechnen
Nachweis der Kochsalzbestandteile
 Reaktionsgleichungen + NaCl (aq ) + AgNO 3 (aq ) AgCl (s) + NO 3 (aq ) + Na (aq ) Na Na h ν Na Zeitbedarf Vorbereitung: 5 min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Reaktionsgleichungen + NaCl (aq ) + AgNO 3 (aq ) AgCl (s) + NO 3 (aq ) + Na (aq ) Na Na h ν Na Zeitbedarf Vorbereitung: 5 min. Durchführung: 5 min. Nachbereitung: 5 min. Chemikalienliste Edukte Chemikalien
Stoffe oder Teilchen, die Protonen abgeben kånnen, werden als SÄuren bezeichnet (Protonendonatoren).
 5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
5 10 15 20 25 30 35 40 45 O C 50 Chemie Technische BerufsmaturitÄt BMS AGS Basel Kapitel 6 SÄuren und Basen Baars, Kap. 12.1; 12.2; 13 Versuch 1 Ein Becherglas mit Thermometer enthält violette FarbstofflÅsung
3-01. Triphenylmethan
 Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Triphenylmethan 3-01 Triphenylmethan ist ein farbloser Feststoff. Die Verbindung kann aus Benzol und Trichlormethan durch FRIEDL-CRAFTS-Alkylierung (elektrophile Substitution) hergestellt werden. Die H-Atome
Zuckernachweis mit Tollens-Reagenz
 Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Zuckernachweis mit Tollens-Reagenz Betriebsanweisung nach 0 Gefahrstoffverordnung Verwendete Chemikalien Bezeichnung R-Sätze S-Sätze Gefährlichkeitsmerkmale Silbernitrat (öllenstein) AgN 3 3-0/3 6--60-61
Thema 12 Lebensmittelfarbstoffe
 Thema 12 Lebensmittelfarbstoffe Anna Bella Rohweder Inhalt: 1. Lebensmittelfarbstoffe S. 2 2. Farbigkeit S. 3 Über die Eigenschaften von Licht S. 3 Anregung von Elektronen S. 4 Absorption von Lichtquanten
Thema 12 Lebensmittelfarbstoffe Anna Bella Rohweder Inhalt: 1. Lebensmittelfarbstoffe S. 2 2. Farbigkeit S. 3 Über die Eigenschaften von Licht S. 3 Anregung von Elektronen S. 4 Absorption von Lichtquanten
Qualitative Nachweise von Säuren und Basen
 Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Schulversuchspraktikum Miriam Jarrar Sommersemester 2012 Klassenstufen 9 & 10 Qualitative Nachweise von Säuren und Basen Auf einen Blick: Dieses Protokoll beinhaltet 3 Lehrerversuche und 2 Schülerversuche
Zusammenfassung vom
 Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Zusammenfassung vom 20.10. 09 Löslichkeitsprodukt = quantitative Aussage über die Löslichkeit einer schwerlöslichen Verbindung bei gegebener Temperatur A m B n m A n+ + n B m- K L = (c A n+ ) m (c B m-
Organisch-chemisches Praktikum für Studierende des Lehramts WS 08/09
 rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: Die klassische Atemalkoholprobe
rganisch-chemisches Praktikum für Studierende des Lehramts WS 08/09 Praktikumsleitung: Dr. Reiß Assistent: Beate Abé Name: Sarah enkel Datum: 27.11.2008 Gruppe 6: Alkohole Versuch: Die klassische Atemalkoholprobe
Kontrollaufgaben zur Optik
 Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Kontrollaufgaben zur Optik 1. Wie schnell bewegt sich Licht im Vakuum? 2. Warum hat die Lichtgeschwindigkeit gemäss moderner Physik eine spezielle Bedeutung? 3. Wie nennt man die elektromagnetische Strahlung,
Licht und Farben. Kurzprotokoll
 Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Schulversuchspraktikum Name: Annika Münch Semester: 2. Mastersemester Klassenstufen 5/6 Licht und Farben Kurzprotokoll Auf einen Blick: Für eine Unterrichtseinheit zum Thema Licht und Farben im naturwissenschaftlichen
Grundkurs Farbstoffe 1983/II 1984/I 1984/IV 1985/IV
 Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Grundkurs Farbstoffe 1983/II 3. Der Farbstoff Chrysoidin wird unter anderem zum Färben von Leder und Papier verwendet. 3.1 Als Ausgangsstoffe für die Darstellung dieses Farbstoffes dienen Anilin, Natriumnitrit
Versuch: Fünf Farben in einer Lösung
 Name: Datum: Versuch: Materialien: 5 x 100 ml Bechergläser (nummeriert von 1-5), Tropfpipetten, Messzylinder (50 ml), Spritzflasche mit destilliertem Wasser Chemikalien: Lösung Nr. 1: Lösung Nr. 2: Lösung
Name: Datum: Versuch: Materialien: 5 x 100 ml Bechergläser (nummeriert von 1-5), Tropfpipetten, Messzylinder (50 ml), Spritzflasche mit destilliertem Wasser Chemikalien: Lösung Nr. 1: Lösung Nr. 2: Lösung
Gruppenarbeit physikalische und chemische Eigenschaften von Alkansäuren
 Gruppenarbeit Gruppe 1: Siedetemperaturen von Alkansäuren Löst die gestellten Aufgaben in eurer Gruppe. Ihr habt dafür 20 Minuten Zeit. Tragt die Ergebnisse in die Folie ein. Wählt eine Gruppensprecherin
Gruppenarbeit Gruppe 1: Siedetemperaturen von Alkansäuren Löst die gestellten Aufgaben in eurer Gruppe. Ihr habt dafür 20 Minuten Zeit. Tragt die Ergebnisse in die Folie ein. Wählt eine Gruppensprecherin
Projekt- Nachweisreaktionen. Dieses Skript gehört: NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz
 Projekt- Nachweisreaktionen NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz Dieses Skript gehört: 1 Nachweise von Anionen 1. Nachweis von Sulfat 3 Reagenzgläser im Reagenzglasständer
Projekt- Nachweisreaktionen NaT-Lab für Schülerinnen und Schüler Johannes Gutenberg-Universität Mainz Dieses Skript gehört: 1 Nachweise von Anionen 1. Nachweis von Sulfat 3 Reagenzgläser im Reagenzglasständer
Zusammenfassung: Säure Base Konzept
 Zusammenfassung: Säure Base Konzept 1. Grundlegende Eigenschaften von Säuren und Laugen Säure und Laugen ätzen sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator.
Zusammenfassung: Säure Base Konzept 1. Grundlegende Eigenschaften von Säuren und Laugen Säure und Laugen ätzen sie werden durch Indikatoren für uns erkenntlich gemacht. Oft verwendet man Universalindikator.
Reaktion zwischen Aluminiumpulver und Iod
 Reaktionsgleichung 2 Al (s) + 3 2 (s) Al 2 6 (s) Zeitbedarf Vorbereitung: 5 min. Durchführung: 15 min. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel Menge R-Sätze S-Sätze Gefahrensymbole
Reaktionsgleichung 2 Al (s) + 3 2 (s) Al 2 6 (s) Zeitbedarf Vorbereitung: 5 min. Durchführung: 15 min. Nachbereitung: 20 min. Chemikalienliste Edukte Chemikalien Summenformel Menge R-Sätze S-Sätze Gefahrensymbole
Versuch: Synthese von Indigo
 Philipps-Universität Marburg 16.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: Synthese von Indigo Zeitbedarf: Vorbereitung:
Philipps-Universität Marburg 16.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: Synthese von Indigo Zeitbedarf: Vorbereitung:
VORANSICHT II/H. Die Farbe Blau in Lebensmitteln. Hintergrundinformationen. Julia Lorke, Katrin Sommer, Bochum. Niveau: Sek.
 18. Die Farbe Blau in Lebensmitteln 1 von 10 Die Farbe Blau in Lebensmitteln Julia Lorke, Katrin Sommer, Bochum Niveau: Sek. II Dauer: 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen:
18. Die Farbe Blau in Lebensmitteln 1 von 10 Die Farbe Blau in Lebensmitteln Julia Lorke, Katrin Sommer, Bochum Niveau: Sek. II Dauer: 4 Unterrichtsstunden Bezug zu den KMK-Bildungsstandards Fachwissen:
Versuche zur Untersuchung von Fruchtfarbstoffen
 Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
Versuche zur Untersuchung von Fruchtfarbstoffen Durchgeführt und protokolliert von: Annika Bauland, Corinna Brockers, Anne Jonas, Isabelle Schmidt 1.Versuch: Dünnschichtchromatographie Für diesen Versuch
Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie
 Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Name Datum Identifizierung des Farbstoffes in blauen M&Ms durch Dünnschichtchromatographie Material: DC-Karten (Kieselgel), Glas mit Deckel(DC-Kammer), Kapillare, Messzylinder Chemikalien: Blaue M&Ms,
Laborführerschein. Dieses Skript gehört:
 Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Laborführerschein Dieses Skript gehört: Laborführerschein Seite 2 Station 1: Laborgeräte, ein Muss für jeden Chemiker Welche Laborgeräte des Titelbildes findest Du in der Liste wieder? Suche an deinem
Vorgehen bei der qualitativen Analyse. Nachweisreaktion. Nachweisreaktionen. molekular gebauter Stoffe
 Vorgehen bei der qualitativen Analyse 1. Vorprobe liefert Hinweise auf die mögliche Zusammensetzung der Probe ; Bsp. Flammenfärbung 2. Blindprobe zeigt aus Aussehen der Nachweisreagenzien; Vergleichsprobe
Vorgehen bei der qualitativen Analyse 1. Vorprobe liefert Hinweise auf die mögliche Zusammensetzung der Probe ; Bsp. Flammenfärbung 2. Blindprobe zeigt aus Aussehen der Nachweisreagenzien; Vergleichsprobe
Zusatzveranstaltung 1: Sauer macht lustig!
 Zusatzveranstaltung 1: Sauer macht lustig! Station 1: Sauer - was ist das? E1 Manche Stoffe reagieren ziemlich sauer! E2 Säuren lassen sich besänftigen! Station 2: Säuren im täglichen Leben E3 Eine Zitronenbatterie???
Zusatzveranstaltung 1: Sauer macht lustig! Station 1: Sauer - was ist das? E1 Manche Stoffe reagieren ziemlich sauer! E2 Säuren lassen sich besänftigen! Station 2: Säuren im täglichen Leben E3 Eine Zitronenbatterie???
Versuch: Alkoholtest mit Dichromat. Chemikalien: Menge: R-Sätze: S-Sätze: Gefahrensymbol: Schuleinsatz:
 Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
Philipps-Universität Marburg 03.01.2008 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 6, Alkohole Versuch: Alkoholtest mit Dichromat Zeitbedarf:
3.5 Hydrolyse von Salzen. Aufgabe. Reagieren wässrige Salzlösungen neutral? Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze
 Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Naturwissenschaften - Chemie - Säuren, Basen, Salze - 3 Salze (P759800) 3.5 Hydrolyse von Salzen Experiment von: Phywe Gedruckt: 5.0.203 2:2:26 intertess (Version 3.06 B200, Export 2000) Aufgabe Aufgabe
Gruppe 9 eigener Versuch. Reaktion von Saccharose und Schwefelsäure
 Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 3.06.09 SS 09 Gruppe 9 eigener Versuch Reaktion von Saccharose
Philipps- Universität Marburg FB 15 Chemie Organisch-Chemisches Grundpraktikum für das Lehramt Christian Lego Leitung: err Dr. Reiß Datum: 3.06.09 SS 09 Gruppe 9 eigener Versuch Reaktion von Saccharose
Experiment: Synthese von Gold-Nanopartikeln (Klasse 9)
 Experiment: Synthese von Gold-Nanopartikeln (Klasse 9) Chemikalien Gold(III)-chlorid-Lösung c = 0,000 44 mol/l Natriumcitrat-Lösung c = 1 % Geräte siedendes Wasserbad, Reagenzgläser, Messpipette 10 ml,
Experiment: Synthese von Gold-Nanopartikeln (Klasse 9) Chemikalien Gold(III)-chlorid-Lösung c = 0,000 44 mol/l Natriumcitrat-Lösung c = 1 % Geräte siedendes Wasserbad, Reagenzgläser, Messpipette 10 ml,
DEFINITIONEN REINES WASSER
 SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
SÄUREN UND BASEN 1) DEFINITIONEN REINES WASSER enthält gleich viel H + Ionen und OH Ionen aus der Reaktion H 2 O H + OH Die GGWKonstante dieser Reaktion ist K W = [H ]*[OH ] = 10 14 In die GGWKonstante
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau
 Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
Versuch 6.14 ph-abhängigkeit eines Indikators am Beispiel Thymolblau Einleitung Lösungen mit verschiedenen ph-werten von stark sauer bis stark basisch werden mit gleich viel Thymolblau-Lösung versetzt.
LMPG 2, ÜB21, Molekülbau & UV/VIS-Absorption LÖSUNG 1 von 11
 LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
LMPG 2, ÜB21, Molekülbau & UV/VISAbsorption LÖSUG 1 von 11 Übung 1: Charakterisierung von Absorptionsbanden Veränderungen der Molekülstruktur können zu Verschiebungen der einzelnen Absorptionsbanden im
Triphenylmethanfarbstoffe
 3. Triphenylmethanfarbstoffe 3.1 Triphenylmethanfarbstoffe Diese Farbstoffklasse leitet sich vom Triphenylcarbeniumion als Chromophor ab. Durch Einführung auxochromer Gruppen in Parastellung kann man die
3. Triphenylmethanfarbstoffe 3.1 Triphenylmethanfarbstoffe Diese Farbstoffklasse leitet sich vom Triphenylcarbeniumion als Chromophor ab. Durch Einführung auxochromer Gruppen in Parastellung kann man die
Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen. Kurzprotokoll. Schulversuchspraktikum.
 Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Schulversuchspraktikum Isabel Großhennig Sommersemester 2015 Klassenstufen 7 & 8 Chemische Gesetzmäßigkeiten I Erhaltung der Masse und konstante Proportionen Kurzprotokoll Auf einen Blick: Dieses Kurzprotokoll
Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und organische farbige Stoffe Übungen mit Lösungen
 Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und organische farbige Stoffe Übungen mit Lösungen Korrektorat: Dina Baars, Bern Illustrationen: Christoph
Günter Baars E-Lern- und Lehrmedium: Quantenchemie und Chemie farbiger Stoffe Modul: Quantenchemie und organische farbige Stoffe Übungen mit Lösungen Korrektorat: Dina Baars, Bern Illustrationen: Christoph
Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle
 Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle Reaktion: Saccharose
Phillipps- Universität Marburg Isabelle Kuhn Organisch Chemisches Grundpraktikum Lehramt WS 2006/07 Praktikumsleiter: Herr Reiß Gruppe 01: Verbesserung Weißer Zucker... Schwarze Kohle Reaktion: Saccharose
Analytische Chemie. B. Sc. Chemieingenieurwesen. 14. März Prof. Dr. T. Jüstel. Name: Matrikelnummer: Geburtsdatum:
 Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Analytische Chemie B. Sc. Chemieingenieurwesen 14. März 2007 Prof. Dr. T. Jüstel Name: Matrikelnummer: Geburtsdatum: Denken Sie an eine korrekte Angabe des Lösungsweges und der Endergebnisse. Versehen
Versuch: Darstellung des Dibenzalacetons
 Philipps-Universität Marburg 02.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: Darstellung des Dibenzalacetons Zeitbedarf:
Philipps-Universität Marburg 02.12.2007 rganisches Grundpraktikum (LA) Katrin ohmann Assistent: Beate Abé Leitung: Dr. Ph. Reiß WS 2007/08 Gruppe 4, Aromaten Versuch: Darstellung des Dibenzalacetons Zeitbedarf:
Isolierung von Pflanzenfarbstoffen und Untersuchung auf ihre Verwendung als Säure- Base-Indikatoren
 Bodensee-Gymnasium Lindau Januar 2009 Isolierung von Pflanzenfarbstoffen und Untersuchung auf ihre Verwendung als Säure- Base-Indikatoren von Marc Bradenbrink und Florian Gerner Betreuungslehrkraft: StR
Bodensee-Gymnasium Lindau Januar 2009 Isolierung von Pflanzenfarbstoffen und Untersuchung auf ihre Verwendung als Säure- Base-Indikatoren von Marc Bradenbrink und Florian Gerner Betreuungslehrkraft: StR
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11
 Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Katrin Hohmann Name: Johannes Hergt Datum: 7.12.2010 Zeitbedarf Gruppe 7: Aldehyde und
Praktikum zur Organischen Chemie für Studierende des Lehramts WS 2010/11 Praktikumsleitung: Dr. Reiß Assistent(in): Katrin Hohmann Name: Johannes Hergt Datum: 7.12.2010 Zeitbedarf Gruppe 7: Aldehyde und
1. Qualitativer Nachweis von Anionen und Sodaauszug
 Anionennachweis 1 1. Qualitativer Nachweis von Anionen und Sodaauszug Die moderne Analytische Chemie unterscheidet zwischen den Bereichen der qualitativen und quantitativen Analyse sowie der Strukturanalyse.
Anionennachweis 1 1. Qualitativer Nachweis von Anionen und Sodaauszug Die moderne Analytische Chemie unterscheidet zwischen den Bereichen der qualitativen und quantitativen Analyse sowie der Strukturanalyse.
